É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Observação e Análise da Espalhamento Raman Aprimorado por Superfície do Piscar de Olhos.
Neste Artigo
Resumo
Este protocolo descreve a análise de superfície-enhanced Raman a piscar espalhamento devido o passeio aleatório de uma única molécula em uma superfície de prata usando as leis do poder.
Resumo
De uma única molécula em uma junção de prata nanoaggregate, piscar superfície-enhanced Raman espalhamento (SERS) é observada. Aqui, um protocolo é apresentado em como preparar o SERS-ativo nanoaggregate de prata, gravar um vídeo de determinados pontos piscando em imagem microscópica e analisar as estatísticas pisca. Nesta análise, uma lei de potência reproduz as distribuições de probabilidade para eventos brilhantes em relação a sua duração. As distribuições de probabilidade para eventos escuros são montadas por uma lei de potência com uma função exponencial. Os parâmetros da lei poder representam o comportamento molecular nos Estados brilhantes e escuros. O modelo de passeio aleatório e a velocidade da molécula através de toda a superfície de prata podem ser estimados. É difícil de estimar, mesmo quando usando as médias, funções de autocorrelação e imagem latente de super-resolução SERS. No futuro, análises de lei de poder devem ser combinadas com imagem espectral, porque as origens de piscar não podem ser confirmadas por este método de análise sozinho.
Introdução
Superfície-enhanced Raman espalhamento (SERS) é altamente sensível Espectroscopia Raman de uma superfície de metal nobre. Desde que o espectro Raman fornece informações detalhadas sobre a estrutura molecular com base nas posições do pico afiado, através dos modos vibracionais dos grupos funcionais nas moléculas, as informações de uma única molécula sobre uma superfície metálica podem ser investigadas usando SERS1,2,3. De um nanoaggregate de prata com um adsorbate no nível do único-molécula, um sinal intermitente é observado1,2,3,4,5,6, 7 , 8 , 9 , 10 , 11 , 12 , 13 , 14 , 15 , 16e o espectro varia1,2,3,4,5,6,7,8, 9,10,11,12,13,14. Piscando pode ser induzida por uma única molécula que aleatoriamente se move dentro e fora de um campo de (EM) eletromagnético melhorado em uma junção de nanoaggregate prata nanômetros de tamanho. Portanto, piscando é considerada uma prova simples para a deteção de único-molécula, comparada com uma técnica usando uma distribuição de Poisson de intensidades SERS e um bi-analito2,3,17. No entanto, os mecanismos detalhados do espectro piscando e flutuante, que pode depender fortemente de comportamento molecular na superfície Ag, são ainda controversos.
Em estudos anteriores, piscar SERS foi analisada usando a função de autocorrelação, que pode calcular o coeficiente de difusão e concentração de moléculas entrando e um reforço EM campo12,13,14 . Além disso, uma pontuação normalizada desvio-padrão, que representa a instabilidade na intensidade total, foram obtida a partir do perfil de tempo do sinal15. No entanto, essas abordagens analíticas podem basear-se sobre o comportamento de algumas moléculas. Em contraste, em uma imagem de super-resolução de piscar SERS, comportamento único-molécula em um campo EM avançado pode ser identificados16. No entanto, essas técnicas podem obter tais parâmetros somente em um campo EM reforçada. O comportamento aleatório de uma única molécula dentro de uma grande variedade (por exemplo, no piscar SERS) pode ser representado como uma lei de potência, ao invés de uma média de4,5,6,7,8 ,9,10,11, semelhante à fluorescência pisca de um único semicondutor quantum dot (QD)18,19. Usando um poder lei análise4,5,6,7,8,9,10,11, comportamento molecular pode ser estimado no estado brilhante (no campo EM reforçada) e no estado escuro10; ou seja, o comportamento da molécula sobre toda a superfície de prata pode ser estimado.
Para esta técnica, a prata coloidais nanoaggregates são usados4,5,6,7,8,9,10,11. Estes nanoaggregates mostrar várias bandas de ressonância (LECC) de plasmon de superfície localizadas que afetam fortemente reforçada de campos eletromagnéticos quando eles estão animados em certos comprimentos de onda. Assim, prata SERS-ativo nanopartículas existem em suspensão coloidal e alguns dados pode ser obtida imediatamente. No caso de nanoestruturas simples, que têm regimes, formas e tamanhos específicos, a dependência de LECC de SERS piscando pode esconder outras dependências7; ou seja, se o bom ou mau nanostructure de LECC é usado, os parâmetros será constantes, e outras dependências, portanto, ficará oculta. Análise de lei do poder tem sido usado para descobrir várias dependências dos SERS piscando de prata coloidal nanoaggregates4,5,6,7,8, 9 , 10 , 11.
Access restricted. Please log in or start a trial to view this content.
Protocolo
1. preparação da amostra
-
Preparação de nanopartículas de prata coloidais 20
- Para fabricar a nanopartículas de prata coloidais, dissolva 0,030 g de nitrato de prata e 0,030 g de citrato trissódico dihidratado em 150 mL de água num balão de fundo redondo de 200 mL.
- Combine o balão com um condensador de refluxo (Dimroth).
- Misture a solução do frasco com uma barra magnética de agitador e mexa. Em seguida, aqueça a solução agita o balão em banho de óleo a 150 ° C por 60 min.
Nota: A solução vai virar cinza amarela, então leitosa. - Arrefecer a suspensão em temperatura ambiente e manter a suspensão no frasco coberto com folha de alumínio em um frigorífico.
Nota: O protocolo pode ser interrompido neste ponto. Use as nanopartículas coloidais, depois armazenar no frigorífico, dentro de um mês.
-
Preparação da amostra para multi-coloridas piscando de emissão 11
- Para preparar uma lâmina de microscópio, lave à mão uma placa de vidro com sabão e enxágue com água.
- Adicionar 0,1% solução aquosa de poli-L-lisina para a placa de vidro e remover a solução com um ventilador.
- Adicionar a suspensão coloidal de prata para a placa de vidro e remover a suspensão com um ventilador.
- Coloque uma área para soltar a placa de vidro com uma caneta de bloqueador líquido.
- Gota de água destilada na placa de vidro e cubra-o com outra placa de vidro para criar um slide de microscópio e evitar que a água evapora.
-
Preparação da amostra para monótonos coloridas piscando SERS 7 , 8 , 9 , 10
- Para preparar uma lâmina de microscópio, lave à mão uma placa de vidro com sabão e enxágue com água.
- Misturar a suspensão coloidal de prata com tintura de thiacyanine ou thiacarbocyanine (µM 25 ou 4, respectivamente) e uma solução aquosa de NaCl (10 mM) em uma relação de volume de 2:1:1.
- Deixar a suspensão da amostra na placa de vidro e remover a suspensão com um ventilador.
- Coloque uma área para soltar a placa de vidro com uma caneta de bloqueador líquido.
- Gota de solução aquosa de NaCl (1 M) na placa de vidro para imobilizar as nanopartículas de prata e cubra-o com outra placa de vidro para criar um prato de corrediça do microscópio e impedir a evaporação da solução.
2. observação de nanopartículas de prata a piscar
-
Iluminação da amostra
- Coloque a placa de vidro de amostra preparada usando protocolo 1.2 ou 1.3 no palco de um microscópio invertido.
- Ilumine a placa de vidro de amostra usando luz branca através de um condensador de campo escuro e foco em vários pontos coloridos (azuis, verdes, amarelos e vermelhos) na placa de vidro, usando uma lente objetiva (60 X).
- Ilumine a placa de vidro de amostra utilizando um feixe atenuado, entregado a um ângulo de 30° em relação à superfície da amostra, de um laser de assemelhace (cw) diodo bombeado de estado sólido (DPSS) através de um filtro de interferência.
- Para usar iluminação laser para observar a nanoaggregates de prata como monótonas manchas coloridas em uma envolvente da mesma cor, mover a área de iluminação do laser para o centro da vista e focalizar os pontos na placa de vidro, ajustando o estágio na direção z.
-
Observação de piscar
- Inserir um filtro de passa-tempo após a lente objetiva e iluminam a placa de vidro de amostra usando um feixe de cw-laser DPSS entregado a um ângulo de 30° em relação à superfície da amostra através de um filtro de interferência.
- Encontrar a piscar pontos conforme mostrado na Figura 1 (ver também Figura S1 no material complementar) movendo o palco na x - e y-direções.
- Gravar vídeo dos pontos piscando com o microscópio invertido, acoplado a uma câmera de refrigeração digital dispositivo de carga acoplada (CCD), que tem uma resolução de tempo de 61-120 ms, por 20 min.
3. análise de piscar SERS
-
Derivação do perfil do tempo de vídeo
- No software que controla a câmera CCD, abra o arquivo de vídeo.
- Para selecionar os pontos piscando e área escura, arraste áreas que cobrem separadamente as regiões com e sem manchas na imagem de vídeo.
- Para derivar perfis de tempo de intensidade de sinal o pontos piscando e áreas escuras no vídeo, selecione Análise Temporal em análisee clique a calcular na janela de Análise Temporal .
- Salve os dados como um arquivo de texto.
-
Análise do perfil do tempo
- Achate uma linha de base do perfil tempo subtraindo-se o perfil de tempo do área escura e/ou montagem com uma função polinomial, como mostrado nas figuras 2A e 2B.
- Avalie uma intensidade média de base que consiste em aproximadamente 2000 pontos, eubasee um desvio-padrão das intensidades de linha de base, σ, como mostrado nas figuras 2 e 2D.
- Distinguir eventos brilhantes de acontecimentos sinistros usando intensidades maiores do que um limiar de eubase + 3σ e registar a duração de cada evento. Na Figura 3, por exemplo, registrar o evento de 0 para 3.5476 s como o evento escuro (com uma duração de t = 3.5476 s) e registrar o evento de 3.5476 para 4.0981 s como o evento brilhante (com uma duração de t = 0.5505 s). Repita o procedimento como mostrado na tabela 1.
- Conte o número de eventos brilhantes e escuros para cada duração, tal como expresso nas primeiras e segunda linhas da tabela 2.
- Soma do número de eventos para cada duração, exceto para eventos mais curtos do que a duração t. Conforme expresso nas segunda e terceiros linhas da tabela 2, por exemplo, somar o número de eventos para cada duração (excepto os eventos para t = 0.0612 s) como 41 + 18 + 9 +...; o resultado é igual a soma de t = 0.1223 s, ou seja, 103.
- Divida os somatórios por cada duração e normalizá-los. Conforme expresso na tabela 2, por exemplo, dividir o somatório para duração t = 0.0612 s pela duração 0.0612 s. O resultado é 3,351.5791. Em seguida, divida o resultado pelo total dos resultados na quarta linha da tabela 2. A distribuição de probabilidade é derivada para ser 0.64494.
- Plotar as distribuições de probabilidade para o brilhante eventos Pem(t) contra sua duração t em um gráfico do logaritmo-logaritmo e caber Log10Pem(t) pelo Log10 (
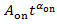 ) para deduzir o poder lei expoente α para um determinado ponto a piscar. Se Pem(t) é montado por
) para deduzir o poder lei expoente α para um determinado ponto a piscar. Se Pem(t) é montado por 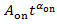 , a linha cabida se desvia as parcelas em valores pequenos de Pem(t), como mostrado pela linha pontilhada na Figura 4A.
, a linha cabida se desvia as parcelas em valores pequenos de Pem(t), como mostrado pela linha pontilhada na Figura 4A. - Plotar as distribuições de probabilidade para eventos escuro Pfora(t) contra sua duração t em um gráfico do logaritmo-logaritmo e apto Log10Pfora(t) por Log10(
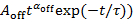 a deduzir a energia lei expoente αfora e o truncamento de tempo τ a piscar mesmo local. Se Pfora(t) é montado por
a deduzir a energia lei expoente αfora e o truncamento de tempo τ a piscar mesmo local. Se Pfora(t) é montado por 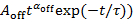 , a cabido curva desvia as parcelas em valores pequenos de Pfora(t).
, a cabido curva desvia as parcelas em valores pequenos de Pfora(t). - Repita 3.2.1 para 3.2.8 para os outros pontos piscando no vídeo.
Access restricted. Please log in or start a trial to view this content.
Resultados
Do nanoaggregates prata com poli-L-lisina, preparado pelo Protocolo 1.2, multicoloridos pontos piscando de SERS e fluorescência avançada superfície são observados, como mostrado na Figura 111. Em contraste, monótonos pontos piscando coloridos de SERS foram observados para a nanoaggregates de prata com as moléculas de corante preparadas pelo Protocolo 1.37,8,
Access restricted. Please log in or start a trial to view this content.
Discussão
Da junção da prata nanoaggregate, SERS é emitido. Assim, precisamos preparar nanoaggregates ao invés de nanopartículas coloidais, que são cobertas com ânions de citrato. Agregados de prata são formados a partir a salgar-para fora o efeito criado pela adição de poli-L-lisina, que tem -NH3+ e é a origem dos SERS, ou cátions at+ de NaCl, conforme mostrado na Figura S2 do material complementar. Além disso, para iluminar os muitos locais na área ampla, o feixe de...
Access restricted. Please log in or start a trial to view this content.
Divulgações
O autor não tem nada para divulgar.
Agradecimentos
O autor agradece a Prof Y. Ozaki (Kwansei Gakuin University) e Dr. T. Itoh (National Institute of Advanced Industrial Science e Technology) para sua discussão proveitosa deste trabalho. Este trabalho foi financiado pelo KAKENHI (subsídio para C de investigação científica) do Ministério da educação, cultura, esportes, ciência e tecnologia (n º 16K. 05671).
Access restricted. Please log in or start a trial to view this content.
Materiais
| Name | Company | Catalog Number | Comments |
| Silver nitrate, 99.8% | Wako | 194-00832 | |
| Trisodium citrate dihydrate, 99. % | Wako | 191-01785 | |
| Poly-L-lysine aqueous solution, 0.1% | Sigma-Aldrich | P8920 | |
| 3,3'-disulfopropylthiacyanine triethylamine | Hayashibara Biochemical Laboratories | NK-2703 | a kind of thiacyanine dyes |
| 3,3'-diethyl-5,5'-dichloro-9-methylthiacarbocyanine iodine salt | Hayashibara Biochemical Laboratories | SMP-9 | a kind of thiacarobocyanine dyes |
| Sodium chloride, 99.5% | Wako | 191-01665 | |
| Dimroth condenser | Iwaki | 61-9722-22 | perchased from AS ONE |
| Magnetic stirrer | Corning | DC-420D | |
| Oil bath | Advantech | OS-220 | |
| Glass plate | Matsunami | S-1112 | Microscope slide |
| Blower | Hozan | Z-288 | Air duster |
| Liquid blocker pen | Daido Sangyo | LIQUID BLOCKER (Super Pap Pen). Ready-to-use hydrophobic barrier pen designed for immunohistochemistry applications | |
| Inverted microscope | Olympus | IX-70 | |
| Objective lens | Olympus | LCPlanFl 60× | NA 0.7 |
| Dark field condenser | Olympus | U-DCD | NA 0.8–0.92 |
| Cooled digital CCD camera | Hamamatsu | ORCA-AG | controlled by software Aqua Cosmos |
| Software for the cooled digital CCD camera | Hamamatsu | AquaCosmos | used for also derivation of the time-profiles from the blinking spots in the video |
| Color CCD camera | ELMO | TNC-C920 | not used for analysis |
| DPSS laser | RGB laser system | NovaPro532-75 | λ = 532 nm; 60 mW (corresponds to a power density of 600 W/cm2) |
| Interference filter | Semrock | LL01-532-12.5 | |
| Long pass filter | Semrock | BLP01-532R-25 | |
| Software for the distinguishment and counting of the bright/dark events | home-maid | programmed by C++ | |
| Software for the fitting by a power law | LightStone | Origin6.1 |
Referências
- Qian, X. M., Nie, S. M. Single-molecule and single-nanoparticle SERS: from fundamental mechanisms to biomedical applications. Chem. Soc. Rev. 37, 912-920 (2008).
- Pieczonka, N. P. W., Aroca, R. F. Single molecule analysis by surfaced-enhanced Raman scattering. Chem. Soc. Rev. 37, 946-954 (2008).
- Kneipp, J., Kneipp, H., Kneipp, K. SERS -a single-molecule and nanoscale tool for bioanalytics. Chem. Soc. Rev. 37, 1052-1060 (2008).
- Kitahama, Y., Ozaki, Y. Analysis of blinking SERS by a power law with an exponential function. Frontiers of Surface-Enhanced Raman Scattering: Single-Nanoparticles and Single Cells. , Wiley. Chichester. Chapter 6 (2014).
- Kitahama, Y. Truncated Power Law Analysis of Blinking SERS. Frontiers of Plasmon Enhanced Spectroscopy Volume 1 (ACS Symposium series Vol. 1245). , American Chemical Society. Washington DC. Chapter 4 (2016).
- Bizzarri, A. R., Cannistraro, S. Lévy Statistics of Vibrational Mode Fluctuations of Single Molecules from Surface-Enhanced Raman Scattering. Phys. Rev. Lett. 94, 068303(2005).
- Kitahama, Y., Tanaka, Y., Itoh, T., Ozaki, Y. Power-law analysis of surface-plasmon-enhanced electromagnetic field dependence of blinking SERS of thiacyanine or thiacarbocyanine adsorbed on single silver nanoaggregates. Phys. Chem. Chem. Phys. 13, 7439-7448 (2011).
- Kitahama, Y., Tanaka, Y., Itoh, T., Ozaki, Y. Analysis of excitation laser intensity dependence of blinking SERRS of thiacarbocyanine adsorbed on single silver nanoaggregates by using a power law with an exponential function. Chem. Commun. 47, 3888-3890 (2011).
- Kitahama, Y., Enogaki, A., Tanaka, Y., Itoh, T., Ozaki, Y. Truncated power law analysis of blinking SERS of thiacyanine molecules adsorbed on single silver nanoaggregates by excitation at various wavelengths. J. Phys. Chem. C. 117, 9397-9403 (2013).
- Kitahama, Y., Araki, D., Yamamoto, Y. S., Itoh, T., Ozaki, Y. Different behaviour of molecules in dark SERS state on colloidal Ag nanoparticles estimated by truncated power law analysis of blinking SERS. Phys. Chem. Chem. Phys. 17, 21204-21210 (2015).
- Kitahama, Y., Nagahiro, T., Tanaka, Y., Itoh, T., Ozaki, Y. Analysis of blinking from multicoloured SERS-active Ag colloidal nanoaggregates with poly-L-lysine via truncated power law. J. Raman. Spectrosc. 48, 570-577 (2017).
- Habuchi, S., et al. Single-Molecule Surface Enhanced Resonance Raman Spectroscopy of the Enhanced Green Fluorescent Protein. J. Am. Chem. Soc. 125, 8446-8447 (2003).
- Weiss, A., Haran, G. Time-Dependent Single-Molecule Raman Scattering as a Probe of Surface Dynamics. J. Phys. Chem. B. 105, 12348-12354 (2001).
- Emory, S. R., Jensen, R. A., Wenda, T., Han, M., Nie, S. Re-examining the origins of spectral blinking in single-molecule and single-nanoparticle SERS. Faraday Discuss. 132, 249-259 (2006).
- Itoh, T., Iga, M., Tamaru, H., Yoshida, K., Biju, V., Ishikawa, M. Quantitative evaluation of blinking in surface enhanced resonance Raman scattering and fluorescence by electromagnetic mechanism. J. Chem. Phys. 136, 024703(2012).
- Willets, K. A. Super-resolution imaging of SERS hot spots. Chem. Soc. Rev. 43, 3854-3864 (2014).
- Dieringer, J. A., Lettan, R. B., Scheidt, K. A., Van Duyne, R. P. A Frequency Domain Existence Proof of Single-Molecule Surface-Enhanced Raman Spectroscopy. J. Am. Chem. Soc. 129, 16249-16256 (2007).
- Cichos, F., von Borczyskowski, C., Orrit, M. Power-law intermittency of single emitters. Curr. Opin. Colloid Interface Sci. 12, 272-284 (2007).
- Tang, J., Marcus, R. A. Mechanisms of fluorescence blinking in semiconductor nanocrystal quantum dots. J. Chem. Phys. 123, 054704(2005).
- Lee, P. C., Meisel, D. Adsorption and surface-enhanced Raman of dyes on silver and gold sols. J. Phys. Chem. 86, 3391-3395 (1982).
- Krichevsky, O., Bonnet, G. Fluorescence correlation spectroscopy: the technique and its applications. Rep. Prog. Phys. 65, 251-297 (2002).
- Hess, S. T., Huang, S., Heikal, A. A., Webb, W. W. Biological and Chemical Applications of Fluorescence Correlation Spectroscopy: A Review. Biochemistry. 41, 697-705 (2002).
Access restricted. Please log in or start a trial to view this content.
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados