Method Article
Estereotaxia guiada por ressonância magnética para infusões no cérebro de porco
Neste Artigo
Resumo
O protocolo aqui apresentado demonstra estereotaxia para o cérebro de suíno usando infusões aprimoradas por convecção, com orientação de visualização por ressonância magnética (RM) em tempo real e visualização de distribuição de infusão em tempo real.
Resumo
O objetivo geral deste procedimento é realizar estereotaxia no cérebro de porco com orientação de visualização de ressonância magnética (RM) em tempo real para fornecer infusões precisas. O sujeito foi posicionado de bruços no furo da RM para acesso ideal ao topo do crânio com o tronco levantado, o pescoço flexionado e a cabeça inclinada para baixo. Dois pinos de ancoragem ancorados no zigoma bilateral mantiveram a cabeça firme usando o suporte de cabeça. Uma bobina flexível de ressonância magnética (RM) foi colocada rostralmente em todo o suporte da cabeça para que o crânio estivesse acessível para o procedimento de intervenção. Uma grade de planejamento colocada no couro cabeludo foi usada para determinar o ponto de entrada apropriado da cânula. A estrutura estereotáxica foi fixada e alinhada iterativamente através de projeção de software até que o erro radial projetado fosse inferior a 0,5 mm. Uma broca manual foi utilizada para criar um furo de rebarba para inserção da cânula. Uma co-infusão reforçada com gadolínio foi usada para visualizar a infusão de uma suspensão celular. Repetidas ressonâncias magnéticas ponderadas em T1 foram registradas em tempo real durante o processo de administração do agente para visualizar o volume de distribuição de gadolínio. A estereotaxia guiada por RM permite uma infusão precisa e controlada no cérebro de suínos, com monitoramento simultâneo da precisão da inserção da cânula e determinação do volume de distribuição do agente.
Introdução
Neste protocolo, descrevemos a aplicação de um sistema estereotáxico de ressonância magnética intervencionista (iMRI) para colocação de cânulas e visualização em tempo real de infusões no cérebro de suínos. O desenvolvimento de sistemas de iMRI permite a colocação precisa do cateter1. A iMRI permite a visualização da distribuição do agente de infusão no cérebro de pacientes sob anestesia geral 1,2 para avaliar a acurácia do procedimento em tempo real.
O sistema estereotáxico guiado por RM é uma plataforma direcionada que permite precisão de direcionamento submilimétrica1. Ele usa um dispositivo de mira montado no crânio em conjunto com um software dedicado que fornece imagens anatômicas do cérebro com trajetórias de inserção de chumbo projetadas e parâmetros de ajuste. A orientação por iMRI para intervenção cirúrgica estereotáxica no cérebro tem se mostrado eficaz em aplicações clínicas, como a estimulação cerebral profunda no tratamento da doença de Parkinson 2,3,4,5, a ablação focal para o tratamento da epilepsia 6,7 e a entrega por convecção aumentada (DCE) de drogas ao sistema nervoso central 8,9.
O método CED é usado para fornecer diretamente agentes terapêuticos ao sistema nervoso central usando convecção de fluidos. Isso é baseado em um pequeno gradiente de pressão hidrostática que permite o fluxo de um infestato da ponta da cânula de infusão para o espaço extracelular circundante10. Métodos estereotáxicos são usados para fornecer altas concentrações de macromoléculas, pequenas moléculas 11,12, transplante de células13,14,15 ou agentes terapêuticos no alvo do tecido cerebral escolhido, contornando a barreira hematoencefálica. Fatores como permeabilidade, coeficientes de difusão, contrapressão, captação e mecanismos de depuração afetam a difusão dos agentes terapêuticos16. Esta técnica utiliza um co-infusato1 à base de gadolínio para CED clínico, para monitorar o agente de infusão em tempo real no alvo parenquimatoso. Parâmetros como o volume de distribuição no tecido e cinética relacionada após a precisão direcionada são monitorados com iMRI.
Estudos de DCE de agentes de infusão através de um sistema de estereotaxia guiado por RM foram estudados em primatas não humanos, resultando em procedimentos precisos, previsíveis e seguros. Demonstrou-se que a precisão da colocação da cânula de infusão atinge o erro de colocação submilimétrica17. O sistema fornece uma distribuição previsível da infusão, com um aumento linear observado no volume de distribuição com o volume de infusão, levando a uma cânula resistente ao refluxo subsequentemente introduzida para infusões de CED18. Este procedimento de infusão de iMRI foi relatado para não incorrer em efeitos indesejáveis em primatas não humanos19.
Aqui, expandimos a aplicação de esterotaxia guiada por RM no cérebro de suínos, para fornecer e monitorar a distribuição de um agente de infusão que consiste em uma suspensão celular de 300 μL. O tamanho do cérebro do porco permite intervenções de imagem e neurocirúrgicas que podem ser aplicadas clinicamente em humanos, o que não é possível em modelos animais menores de doença20. Além disso, o sistema imunológico do porco produz respostas semelhantes às dos seres humanos em termos de respostas a agentes biológicos ou outros agentes terapêuticos21. Portanto, trabalhar com essa espécie animal para procedimentos estereotáxicos de entrega de medicamentos tem implicações clínicas translacionais diretas e pode ser logisticamente mais fácil do que com pesquisas com primatas não humanos.
Utilizou-se um modelo suíno (suínos domésticos, fêmeas, 25 kg, 14 semanas de idade) para estereotaxia guiada por RM. A implementação visual do procedimento estereotáxico em suínos é relatada neste estudo. Descrevemos as adaptações do espaço para acomodar uma cabeça de porco, a visualização do procedimento tanto em vídeo quanto em imagens e a RM concomitante para avaliar a distribuição de infestato no cérebro de porco. A estereotaxia guiada por RM foi realizada em um espaço de RM 3T.
Com este experimento, nosso grupo demonstra o desempenho da estereotaxia guiada por RM no cérebro de porcos e uma linha do tempo básica de imagem para rastrear infusões dentro do cérebro. A técnica geral de estereotaxia clínica realizada em humanos pode ser aplicada ao crânio e ao cérebro de suínos.
O objetivo geral deste procedimento é realizar a estereotaxia guiada por RM no cérebro do porco com orientação de visualização de ressonância magnética em tempo real. Isto é conseguido primeiro posicionando o sujeito propenso no furo da ressonância magnética para um acesso ideal ao topo do crânio. O segundo passo é planejar a inserção cirúrgica com orientação de visualização assistida por ressonância magnética, que envolve a colocação e varredura de uma grade fiducial para determinar o ponto de entrada apropriado para uma trajetória pré-planejada. Isto é conseguido com uma magnetização 3D ponderada em T1 de alta resolução (1 mm isotrópica) preparada para uma varredura de eco de gradiente rápido (MPRAGE) de alta resolução, em uma duração de 7 min e 44 s. Em seguida, fixamos a estrutura estereotáxica na cabeça e ajustamos o alinhamento iterativamente através da projeção de software até que o erro radial projetado seja inferior a 0,5 mm. Digitalizações rápidas de eco turbo spin 2D (duração de 13 s) em orientações oblíquas fornecem orientação de imagem. Em seguida, uma incisão é feita na pele, e uma broca manual é usada para criar um orifício de rebarba para inserção da cânula de infusão nas coordenadas predefinidas. O passo final é monitorar a infusão com repetidas ressonâncias magnéticas ponderadas em T1 (3D MPRAGE; 1 min 45 s) em tempo real com co-infusão de gladolínio. Os resultados mostram que a estereotaxia guiada por RM permite uma infusão precisa e controlada no cérebro de suínos, com base na orientação de RM em tempo real e subsequentes exames de RM 3D MPRAGE ponderados em T1 (resolução isotrópica de 1 mm) usados para visualizar o volume de distribuição.
Protocolo
O estudo foi aprovado pelo Comitê Institucional de Cuidados e Uso de Animais do Houston Methodist Research Institute, número de aprovação da IACUC IS00006378. Todos os métodos experimentais foram realizados de acordo com as diretrizes e regulamentos nacionais e institucionais relevantes.
1. Posicionamento dos animais
- Posicione o sujeito para um acesso ideal ao topo do crânio: coloque-o na mesa de ressonância magnética em preparação para a ressonância magnética.
NOTA: Informação do assunto: suínos domésticos, fêmeas, 25 kg, 14 semanas de idade.- Sedar o indivíduo com cetamina (600 mg por via intramuscular [IM]) e midazolam (5 mg IM). Administrar os analgésicos hidromorfona (4 mg IM), carprofeno (100 mg per os) e fentanil (25 μg tópicos), o antibiótico ceftriaxona (550 mg por via intravenosa [IV]) e NaCl (0,9% IV).
- Intubar o sujeito. Manter a anestesia com isoflurano a 2%-3%.
- Monitore os sinais vitais do sujeito durante todo o procedimento.
- Ventilar mecanicamente a 16-19 respirações/min com um ventilador.
- Coloque o sujeito na mesa de ressonância magnética em preparação para os exames de ressonância magnética.
- Coloque o sujeito em posição prona com a cabeça voltada para o furo da ressonância magnética.
- Coloque uma bobina flexível padrão de quatro canais de ressonância magnética no suporte da cabeça.
- Estabilize a cabeça do sujeito com o suporte da cabeça.
- Levante o tronco com toalhas e almofadas de espuma. O objetivo é que a cabeça caia ligeiramente para baixo, com o pescoço flexionado e o focinho quase tocando a mesa. Isso ajudará a garantir que a estrutura estereotáxica e a cânula de infusão se encaixem no furo do scanner de ressonância magnética. Ancorar os pinos do suporte da cabeça da ressonância magnética no zigoma bilateral para manter a cabeça afixada à mesa da ressonância magnética.
- Verifique se a parte superior do crânio está inclinada em direção à parte de trás do scanner com o pescoço flexionado. Essa posição permite que o cirurgião tenha acesso ao topo do couro cabeludo quando o sujeito entra na ressonância magnética.
- Uma vez definida, a mesa de ressonância magnética é movida para o furo do scanner até que a cabeça do sujeito atinja o final do furo.
2. Planejando a inserção cirúrgica com orientação de visualização assistida por ressonância magnética
- Prepare a área de forma estéril, tomando cuidado para evitar que o material preparado entre nos olhos do sujeito. Coloque toalhas estéreis ao redor da área cirúrgica. Coloque uma cortina estéril com uma abertura em direção ao topo do crânio que o cirurgião possa acessar.
- Coloque a grade de planejamento fiducial no couro cabeludo do sujeito afixando o lado adesivo da grade sobre a cabeça do paciente, centrada em torno do local onde o orifício da rebarba estará.
- Retire a camada superior cheia de líquido da grade enquanto mantém firmemente a camada inferior na posição.
- Execute a varredura de reconhecimento de ressonância magnética com a grade definida no lugar. A varredura geralmente requer a administração de agente de contraste intravenoso por RM para visualizar a vasculatura: use uma concentração de 1 mmol / mL do agente de contraste gadolínio para um volume de infusão de 2,5 mL.
NOTA: A varredura de reconhecimento é uma imagem preliminar tirada antes do estudo de imagem definitivo. O objetivo é que o cirurgião garanta que a imagem seja realizada perto da região de interesse e defina os limites da imagem. A dose recomendada na concentração de 1 mmol/mL, de acordo com o fabricante, para o agente de contraste é de 0,1 mL por quilograma que o animal pesa. - Selecione a localização precisa do cérebro para a inserção da cânula no software de orientação por RM.
- Certifique-se de que o software permite a visualização da trajetória planejada do cirurgião para a colocação da cânula, com base no alvo selecionado. Certifique-se de que o software produz a visualização da trajetória e o ponto de entrada correspondente.
NOTA: Para este estudo, um local no córtex frontal foi selecionado para atingir a substância branca. Este é um local onde muitos gliomas humanos surgem e crescem22. É também um local preferencial para disseminação ao longo dos setores de substância branca23.
NOTA: Considere a decisão do cirurgião por um ponto de entrada, alvo e trajetória desejada para minimizar as transgressões pial e sulcal e evitar os vasos sanguíneos. - Ajuste a trajetória sugerida, incluindo os pontos de entrada e alvo desejados, arrastando manualmente os pontos de entrada e alvo projetados no software para evitar vasos sanguíneos e minimizar transgressões piais e sulcais. A trajetória pode ser alterada e vista em três dimensões.
- Uma vez que a trajetória desejada é identificada com base na preferência do cirurgião, execute o software de orientação por RM para encontrar o ponto de entrada na grade.
- Percorra a trajetória planejada na varredura para encontrar o ponto de entrada no couro cabeludo. O software especifica as coordenadas da grade com base na projeção da trajetória planejada na grade.
3. Protegendo o quadro estereotáxico e ajustando o alinhamento iterativamente através da projeção de software
- Monte a estrutura estereotáxica em torno das coordenadas de ponto de entrada desejadas na grade, primeiro prendendo a base com seis parafusos ancorados no osso e quatro parafusos offset.
- Prenda os seis parafusos ancorados no osso ao crânio sobre a grade, através do couro cabeludo. Os seis parafusos de ancoragem são usados para estabilizar a estrutura estereotáxica e evitar qualquer movimento durante a perfuração.
- Prenda os quatro parafusos deslocados localizados na base da torre através da pele, ancorados no crânio. Eles atuam como uma força contrária para apertar os parafusos ósseos centrais, levantando a base do quadro para os parafusos centrais e estabilizando a base.
- Uma vez que a base do quadro estereotáxico esteja segura, continue com a montagem do quadro.
- Realize a ressonância magnética MPRAGE ponderada em T1 de alta resolução, uma opção no software de ressonância magnética, com o quadro definido para capturar os fiduciais do quadro e confirmar a trajetória.
- Confirme a trajetória de inserção da cânula projetada desejada com o software, visualizando a ressonância magnética e a trajetória planejada.
- Exames de ressonância magnética de eco de spin turbo spin 2D subsequentes são feitos para confirmar o alinhamento do quadro com o objeto, uma vez que o quadro está no lugar. Se houver um desalinhamento entre a posição atual do quadro e a trajetória desejada, o software produz parâmetros de ajuste.
NOTA: O software calcula a diferença radial entre a projeção da posição atual do quadro estereotáxico e o ponto de destino definido. Esse erro é usado para calcular o erro projetado, que por sua vez é usado para calcular os ajustes necessários no quadro para minimizá-lo.
- Exames de ressonância magnética de eco de spin turbo spin 2D subsequentes são feitos para confirmar o alinhamento do quadro com o objeto, uma vez que o quadro está no lugar. Se houver um desalinhamento entre a posição atual do quadro e a trajetória desejada, o software produz parâmetros de ajuste.
- Execute os ajustes pitch-roll e X-Y girando as rodas do polegar, conforme indicado pelos parâmetros de ajuste de saída no software.
- Repita a visualização de ressonância magnética habilitada por software da trajetória e realize ajustes rotacionais e translacionais (usando as rodas do polegar) da cânula de segmentação, conforme necessário.
- Usando o software de orientação por RM, meça a espessura do crânio na trajetória desejada e a distância total ao cérebro.
NOTA: O software calcula a distância do topo do quadro (parafusado ao crânio) até o ponto alvo para estimar o comprimento total.
4. Perfuração e inserção da cânula para perfusão
- Use um esfoliante de iodo antes de realizar a incisão para prevenir a infecção.
- Faça uma incisão de 3 cm no couro cabeludo, usando um bisturi sob a estrutura estereotáxica.
- Configure a estrutura para inserção de broca executando os ajustes antes de criar o orifício de acesso.
- Remova e substitua o tubo guia central por um que se adapte a uma broca de 3,4 mm para perfuração.
- Certifique-se de que um assistente esteja presente para manter o quadro no lugar enquanto o cirurgião treina com uma broca manual para adicionar estabilidade adicional ao quadro.
- Deixe o cirurgião perfurar com uma broca de torção manual para criar um furo de rebarba de 3,4 mm de diâmetro.
- Configure a estrutura para a segunda inserção da broca para alargar o orifício de rebarbas e evitar colisões ósseas que possam alterar a trajetória.
- Configure a broca com a broca de 4,5 mm; substitua o tubo guia central por um que se adapte a esta broca maior.
- Crie um orifício de rebarba de 4,5 mm.
- Realize uma ressonância magnética para garantir que a cânula de direcionamento tenha retornado à trajetória planejada, pois a perfuração através do quadro às vezes pode deslocar a cânula.
- Perfure a dura-máter com um estilete afiado.
- Insira a cânula de perfusão pré-preparada compatível com o quadro. Certifique-se de que a cânula tenha uma contrapressão neutra ou positiva consistente para limitar a introdução de bolhas de ar.
NOTA: O software fornece uma profundidade especificada para o destino planejado. - Meça a profundidade na cânula de infusão compatível com quadro estereotáxico e use o ponto de parada de profundidade associado à cânula. Essa parada de profundidade garante que a cânula atinja o local desejado e não vá além dele. Há também um conjunto de trava e doca com um parafuso adicional para garantir que a cânula permaneça na profundidade desejada.
5. Monitorização da perfusão com ressonâncias magnéticas repetidas
- Realize uma ressonância magnética para avaliar a inserção da cânula no local alvo correto no cérebro.
- Inicie a infusão do agente desejado como uma co-infusão com um agente de contraste à base de gadolínio.
NOTA: Neste experimento, uma concentração de 1 mM de agente de contraste à base de gadolínio foi usada, mas isso pode precisar ser ajustado com base na aplicação. Um total de 300 μL de volume de infusão foi administrado a uma taxa de 10 μL/min, embora isso também possa ser variado. - Realizar uma ressonância magnética em intervalos de tempo regulares para monitorar a infusão e o volume de distribuição do agente inserido em cânula no cérebro, que pode ser inferido devido à co-infusão de gadolínio.
NOTA: Uma área hiperintensa ao redor da ponta da cânula indica a presença do agente de contraste à base de gadolínio. - Quando a perfusão terminar, pare a bomba.
NOTA: A taxa de perfusão utilizada neste estudo foi de 30 μL/min, até que o volume de 300 μL da suspensão celular fosse completamente infundido. - Deixe a cânula permanecer no cérebro por 5 minutos após o término da infusão antes de remover a cânula.
NOTA: A cânula de infusão é tipicamente deixada no lugar por 5 minutos após o término da infusão para reduzir o refluxo21,24. - Remova a cânula manualmente através do quadro.
- Remova o quadro da cabeça desmontando-o em ordem inversa de como ele foi construído.
- Feche a incisão com uma sutura de monocrilo 3-0 ou 4-0.
- Desligue o isoflurano para se preparar para a recuperação.
- Extubar o sujeito e permitir que o sujeito se recupere sob observação da equipe veterinária.
Resultados
A posição do porco no scanner de RM fornece acesso ideal para o cirurgião operar e liberar a armação estereotáxica e a cânula de infusão (Figura 1). O torso do sujeito foi levantado com toalhas e almofadas de espuma. Isso permitiu que a cabeça caísse ligeiramente para baixo no final do furo da RM e, portanto, garantiu que o quadro estereotáxico e o local de inserção da cânula de infusão fossem perfeitamente acessíveis para o cirurgião.
A visualização guiada por RM permite o planejamento preciso e a inserção de uma cânula no cérebro (Figura 2). O software de orientação por RM fornece o ponto de inserção para alcançar a trajetória desejada.
O quadro estereotáxico foi escaneado no software e ajustado para atingir efetivamente o local desejado (Figura 3). Nesta demonstração, um local no córtex frontal foi escolhido. Uma vez que o quadro foi definido, o software foi usado para estimar a espessura do crânio do porco, a distância até o local desejado a partir da base do quadro e os ajustes do parâmetro do quadro para alcançar o local desejado. Nesse caso, para a localização e o ângulo de inserção selecionados, a espessura do crânio que a cânula atravessaria foi de 4,7 mm e de 4,4 mm da superfície interior do crânio até a superfície do cérebro (Figura 3A).
Finalmente, exames de ressonância magnética interoperatória iterativa após a infusão de cânula mostraram como a infusão foi entregue ao tecido cerebral (Figura 4). Esses exames também forneceram uma comparação entre a projeção da cânula (retângulo azul) e a trajetória da cânula projetada (retângulo amarelo), que mostram a eficácia dessa técnica em alcançar o local desejado. Os exames de RM foram realizados em intervalos regulares de 4-6 min e finalizados com exames de 10 e 30 min. A infusão com gadolínio foi tratável nesses exames, o que proporcionou uma visualização em tempo real do volume de distribuição do agente.
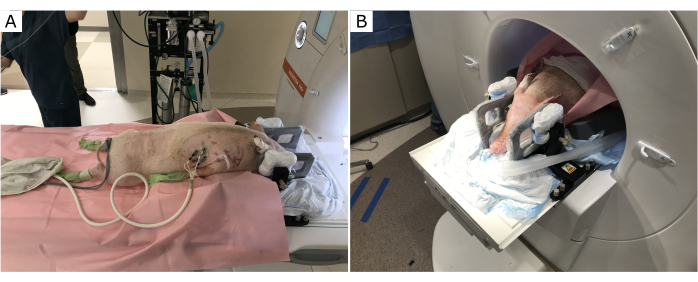
Figura 1: Posição do sujeito na tabela de RM. O tronco é levantado, o pescoço flexionado e a cabeça inclinada para baixo. (A) Antes de entrar no furo MR. (B) Sujeito posicionado através do furo de RM para acesso ideal ao topo do crânio. Por favor, clique aqui para ver uma versão maior desta figura.
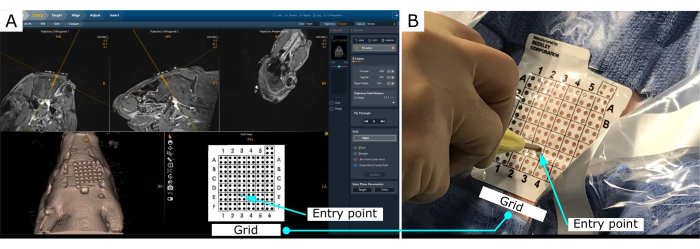
Figura 2: Visualização estereotáxica guiada por RM . (A) Visualização da trajetória planejada. O software produz a localização do ponto de entrada na grade, colocada no couro cabeludo. (B) Localização do ponto de entrada no couro cabeludo. Por favor, clique aqui para ver uma versão maior desta figura.
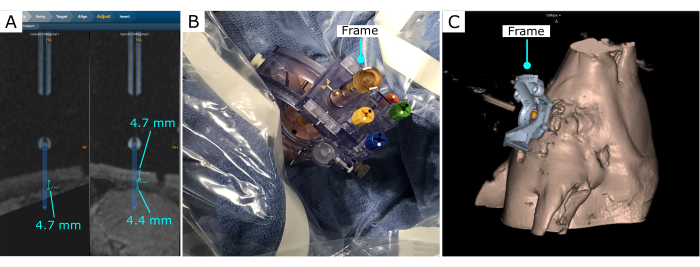
Figura 3: Trajetória de intervenção após o quadro ser fixado no crânio . (A) Medidas de profundidade óssea e distância ao cérebro. (B) Moldura estereotáxica no crânio, com um orifício de rebarba criado com uma broca manual. (C) Projeção de estrutura estereotáxica e reconstrução 3D no software. Por favor, clique aqui para ver uma versão maior desta figura.
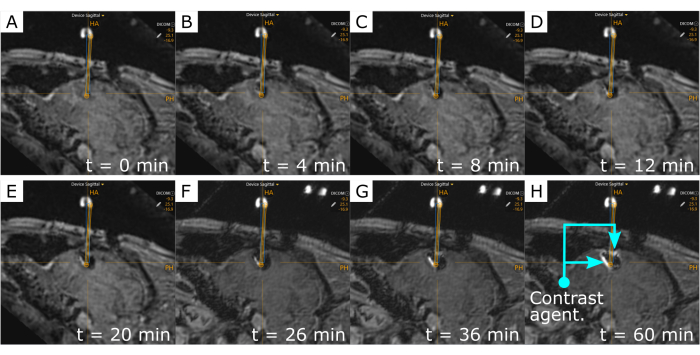
Figura 4: Time-lapse do agente de perfusão com gadolínio. A área hiperintensa ao redor da ponta da cânula indica a presença de gadolínio. Exames repetitivos de RM foram adquiridos ao longo do tempo para rastrear o volume de distribuição do agente durante a infusão: (A) t = 0, (B) t = 4 min, (C) t = 8 min, (D) t = 12 min, (E) t = 20 min, (F) t = 26 min; e após o término da infusão: (G) t = 36 min e (H) t = 60 min. A visualização do agente co-infundido ocorre após 4 minutos. O retângulo azul é a colocação da cânula medida, enquanto o retângulo amarelo mostra a trajetória da cânula projetada. Por favor, clique aqui para ver uma versão maior desta figura.
Discussão
Este protocolo apresenta a realização de estereotaxia guiada por RM para o cérebro de suínos dentro de uma máquina de RM 3T com a possibilidade de precisão de direcionamento submilimétrica, como alcançado em estudos anteriores 1,4,17,18,25. Experimentos prévios com estereotaxia guiada por RM mostraram um erro radial de 0,2 ± 0,1 mm1. Neste relato, o erro final de profundidade em relação à trajetória planejada foi de 1,4 mm devido à avaliação on-line e ajuste da trajetória pelos cirurgiões. O erro de profundidade final foi comparável aos achados de erro radial (abaixo de 2 mm) para implementações clínicas de procedimentos estereotáxicos de iMRI em humanos26.
Aqui, demonstramos a colocação do sujeito na mesa de RM, com o tronco levantado de tal forma que a cabeça possa cair ligeiramente para baixo e apontar para fora em direção ao final do furo da RM. Essa colocação da cabeça é fundamental para proporcionar ao cirurgião espaço para realizar o procedimento. A estrutura estereotáxica permite uma infusão precisa e controlada em modelos de cérebro de porco. Além disso, a ressonância magnética em tempo real permite a determinação precisa do volume de distribuição. Os porcos, como grandes modelos animais para infusões rastreadas em tempo real na ressonância magnética, apresentam a possibilidade do estudo da entrega de drogas ao cérebro, entrega celular e outros agentes de valor translacional.
O porco tem diferenças anatômicas distintas a serem consideradas, em comparação com humanos ou primatas não humanos. À medida que os porcos crescem, o tamanho do corpo no furo de RM torna-se um desafio. A forma da cabeça e do tronco são diferentes dos seres humanos, o que se mostra um desafio para acomodar o acesso ideal ao cérebro para o cirurgião, tanto para o procedimento cirúrgico quanto para a inserção de cânulas no espaço fora do furo da RM. Portanto, é fundamental posicionar o sujeito de forma que o cirurgião tenha acesso à cabeça a partir do final do furo da RM.
A diferença na espessura do crânio entre porcos e humanos é um fator a considerar. Neste protocolo, a visualização por iMRI permitiu estimar com precisão a espessura do crânio para um procedimento eficiente de furo de rebarba. Dado o uso dessas ferramentas neurocirúrgicas minimamente invasivas, a recuperação animal foi sem intercorrências.
A visualização guiada por RM fornece orientação em tempo real para acesso ao cérebro de porco, inserção de cânula e monitoramento do agente de infusão. O processo de perfuração, a deformação tecidual e/ou a ruptura dos tratos da substância branca têm sido relatados como contribuindo para dificuldades na entrega do agente ao cérebro25. Exames de RM iterativos durante o planejamento e a inserção da cânula fornecem a capacidade de pequenos ajustes. Além disso, parâmetros de infusão, como a taxa de infusão ou a precisão da inserção da cânula, podem ser alterados em tempo real ou pausados, conforme ditado pela imagem intraprocedimento. Finalmente, um equilíbrio adequado do co-infusato à base de gadolínio deve ser selecionado, para obter uma avaliação clara do volume de distribuição do agente.
A superconcentração do meio de contraste à base de gadolínio pode ter obscurecido sua distribuição na RM27, mostrando uma mancha preta ao redor da ponta da cânula, circundada por uma área hiperintensa que mostrava os limites externos do volume de infusão. As imagens disponíveis do procedimento são limitadas devido às restrições associadas à filmagem no espaço limitado de ressonância magnética ao redor da área de trabalho do cirurgião. A filmagem intraoperatória foi utilizada para orientar a descrição do protocolo.
Agentes de infusão via estereotaxia guiada por RM em suínos e outros modelos animais de grande porte resultaram em procedimentos precisos, previsíveis e seguros. Demonstrar a estereotaxia de iMRI em porcos fornece a base para a escalabilidade de tratamentos de pesquisa que possuem alto valor translacional para os seres humanos. Modelos suínos têm sido amplamente utilizados para estudar respostas imunológicas devido à sua semelhança com a resposta humana em comparação com outras espécies28. Os agentes terapêuticos entregues ao cérebro podem ser estudados no contexto de infusão precisa de alvo, com o benefício adicional da visualização em tempo real da ressonância magnética do local da infusão, ajustes necessários e avaliação intraoperatória de sua distribuição no tecido.
Divulgações
SG, EAS, CJK têm as seguintes divulgações: Empregado pela ClearPoint Neuro.
Todos os outros autores declaram não haver conflitos de interesse.
Agradecimentos
Os autores declaram que este estudo recebeu financiamento filantrópico da John S. "Steve" Dunn, Jr. & Dagmar Dunn Pickens Gipe Chair in Brain Tumor Research na Houston Methodist. O financiador não esteve envolvido no desenho do estudo, coleta, análise, interpretação dos dados, redação deste artigo ou na decisão de submetê-lo à publicação.
Este trabalho foi financiado em parte pelo número de concessão RP190587 da Iniciativa de Pesquisa e Prevenção do Câncer (CPRIT) e da Fundação Metodista de Houston.
Os autores agradecem a Vi Phan e Lien My Phan, do Centro de Imagem Translacional do Houston Methodist Research Institute, por sua assistência com imagens de RM.
Os autores declaram que este estudo recebeu financiamento filantrópico de Paula e Rusty Walter e Walter Oil & Gas Corp Endowment na Houston Methodist. O financiador não esteve envolvido no desenho do estudo, coleta, análise, interpretação dos dados, redação deste artigo ou na decisão de submetê-lo à publicação.
Materiais
| Name | Company | Catalog Number | Comments |
| 3 Tesla Siemens MAGNETOM Vida | Siemens Healthineers | 70 cm wide-bore 3 Tesla whole body MRI scanner | |
| Four channel flex coil | Siemens Healthineers | Placed ventrally to allow access to the skull | |
| MR Neuro Patient Drape | ClearPoint Neuro, Inc | NGS-PD-05 | MR Neuro Patient Drape, Marker Pen, Track Ball Cover, Cable Cover |
| MR Neuro Procedure Drape Tapered - Long | ClearPoint Neuro, Inc | NGS-PD-02-L | MR Neuro Procedure Drape Tapered, Marker Pen, Track Ball Cover |
| MR Neuro Procedure Drape Tapered w/Extension - Long | ClearPoint Neuro, Inc | NGS-PD-03-L | MR Neuro Procedure Drape Tapered w/Extension, Marker Pen, Track Ball Cover |
| MR Neuro Scanner Bore Drape w/Extension | ClearPoint Neuro, Inc | NGS-PD-04 | MR Neuro Scanner Bore Drape w/Extension |
| Scalp Mount Base | ClearPoint Neuro, Inc | NGS-SM-01 | Scalp Mount Base and centering too |
| Skull Mount Base | ClearPoint Neuro, Inc | NGS-SK-01 | Skull Mount Base |
| SMARTFrame Accessory Kit | ClearPoint Neuro, Inc | NGS -AK-01-11 | Stylet, Lancet, Peel-Away Sheath (2), Ruler, Depth Stop (2) |
| SMARTFrame Guide Tubes | ClearPoint Neuro, Inc | NGS-GT-01 | 15 GA Guide Tube, 18 GA Guide Tube and 16GA Guide Tube |
| SMARTFrame Guide Tubes .052” / 18 ga | ClearPoint Neuro, Inc | NGS-GT-02 | .052” Guide Tubes that fit 18 ga devices (5) |
| SMARTFrame Guide Tubes .060” / 17 ga | ClearPoint Neuro, Inc | NGS-GT-03 | .060” Guide Tubes that fit 17 ga devices (5) |
| SMARTFrame Guide Tubes .064” / CP Stylet | ClearPoint Neuro, Inc | NGS-GT-04 | .064” Guide Tubes that fit ClearPoint Stylets (5) |
| SMARTFrame Guide Tubes .068” / 16 ga | ClearPoint Neuro, Inc | NGS-GT-05 | .068” Guide Tubes that fit 16 ga devices (5) |
| SMARTFrame Guide Tubes .074” / 15 ga | ClearPoint Neuro, Inc | NGS-GT-06 | .074” Guide Tubes that fit 15 ga devices (5) |
| SMARTFrame MR Fiducial | ClearPoint Neuro, Inc | NGS-BM-05 | MR Fiducials (5) |
| SMARTFrame Scalp Mount Rescue Screw – Long | ClearPoint Neuro, Inc | NGS-RS-02 | Short Scalp Mount Rescue Bone Screws (3) |
| SMARTFrame Scalp Mount Rescue Screw – Short | ClearPoint Neuro, Inc | NGS-RS-03 | Long Scalp Mount Rescue Bone Screws (3) |
| SMARTFrame Skull Mount Rescue Screw | ClearPoint Neuro, Inc | NGS-RS-01 | Skull Mount Rescue Bone Screws (3) |
| SMARTFrame Thumb Wheel Extension Set. | ClearPoint Neuro, Inc | NGS -TE-01 | Light Hand Controller |
| SmartFrame XG Device Guide, 2.5 mm | ClearPoint Neuro, Inc | NGS-XG-03 | 2.5-mm Device Guide |
| SmartFrame XG Device Guide, 3.2 mm | ClearPoint Neuro, Inc | NGS-XG-04 | 3.2-mm Device Guide |
| SMARTFrame XG Drill Guide, 4.5 mm | ClearPoint Neuro, Inc | NGS-XG-02 | 4.5-mm Drill Guide |
| SMARTFrame XG Drill Guide, 6.0 mm | ClearPoint Neuro, Inc | NGS-XG-05 | 6.0-mm Drill Guide |
| SMARTFrame XG Exchangeable Device Guides | ClearPoint Neuro, Inc | NGS-XG-01 | Device Guide, 3.4-mm, Device Guide, 14 GA |
| SMARTFrame XG MRI-Guided Trajectory Frame | ClearPoint Neuro, Inc | NGS-SF-02-11 | Stereotactic Frame, Skull Mount Base, Centering Ring, Dock, Standard Device Lock, Large Device Lock, Screwdriver, Roll Lock Screw w/washer |
| SMARTFrame XG MRI-Guided Trajectory Frame, 5 Fr | ClearPoint Neuro, Inc | NGS-SF-02-11-5 | Stereotactic Frame, Centering Ring, Dock, 5 Fr Device Lock, Large Device Lock, Screwdriver, Roll Lock Screw w/washer |
| SMARTFrame XG MRI-Guided Trajectory Frame, 7 Fr | ClearPoint Neuro, Inc | NGS-SF-02-11-7 | Stereotactic Frame, Centering Ring, Dock, 7 Fr Device Lock, Large Device Lock, Screwdriver, Roll Lock Screw w/washer |
| SMARTGrid MR Planning Grid | ClearPoint Neuro, Inc | NGS -SG-01-11 | Marking Grid and Marking Tool |
| SMARTTip MR Drill Kit, 4.5-mm | ClearPoint Neuro, Inc | NGS-DB-45 | 4.5-mm Drill Bit, 3.2-mm Drill Bit, Lancet, Depth Stop, Ruler |
| SMARTTwist MR Hand Drill | ClearPoint Neuro, Inc | NGS-HD-01 | Hand Drill |
| VentiPAC | SurgiVet | V727000 | Mechanical ventilator |
| Wharen Centering Guide | ClearPoint Neuro, Inc | NGS-CG-01 | Wharen Centering Guide |
Referências
- Larson, P. S., et al. An optimized system for interventional magnetic resonance imaging-guided stereotactic surgery: preliminary evaluation of targeting accuracy. Neurosurgery. 70, 95-103 (2012).
- Foltynie, T., et al. MRI-guided STN DBS in Parkinson's disease without microelectrode recording: efficacy and safety. Journal of Neurology, Neurosurgery and Psychiatry. 82 (4), 358-363 (2011).
- Sidiropoulos, C., et al. Intraoperative MRI for deep brain stimulation lead placement in Parkinson's disease: 1 year motor and neuropsychological outcomes. Journal of Neurology. 263 (6), 1226-1231 (2016).
- Ostrem, J. L., et al. Clinical outcomes using ClearPoint interventional MRI for deep brain stimulation lead placement in Parkinson's disease. Journal of Neurosurgery. 124 (4), 908-916 (2016).
- Lee, P. S., et al. Outcomes of interventional-MRI versus microelectrode recording-guided subthalamic deep brain stimulation. Frontiers in Neurology. 9, 241 (2018).
- Patel, N. K., Plaha, P., Gill, S. S. Magnetic resonance imaging-directed method for functional neurosurgery using implantable guide tubes. Operative Neurosurgery. 61 (5), 358-366 (2007).
- Drane, D. L., et al. Better object recognition and naming outcome with MRI-guided stereotactic laser amygdalohippocampotomy for temporal lobe epilepsy. Epilepsia. 56 (1), 101-113 (2015).
- Chittiboina, P., Heiss, J. D., Lonser, R. R. Accuracy of direct magnetic resonance imaging-guided placement of drug infusion cannulae. Journal of Neurosurgery. 122 (5), 1173-1179 (2015).
- Han, S. J., Bankiewicz, K., Butowski, N. A., Larson, P. S., Aghi, M. K. Interventional MRI-guided catheter placement and real time drug delivery to the central nervous system. Expert Review of Neurotherapeutics. 16 (6), 635-639 (2016).
- Bobo, R. H., et al. Convection-enhanced delivery of macromolecules in the brain. Proceedings of the National Academy of Sciences. 91 (6), 2076-2080 (1994).
- Mittermeyer, G., et al. Long-term evaluation of a phase 1 study of AADC gene therapy for Parkinson's disease. Human Gene Therapy. 23 (4), 377-381 (2012).
- Lonser, R. R., Sarntinoranont, M., Morrison, P. F., Oldfield, E. H. Convection-enhanced delivery to the central nervous system. Journal of Neurosurgery. 122 (3), 697-706 (2015).
- Subramanian, T., Deogaonkar, M., Brummer, M., Bakay, R. MRI guidance improves accuracy of stereotaxic targeting for cell transplantation in parkinsonian monkeys. Experimental Neurology. 193 (1), 172-180 (2005).
- Emborg, M. E., et al. Intraoperative intracerebral MRI-guided navigation for accurate targeting in nonhuman primates. Cell Transplantation. 19 (12), 1587-1597 (2010).
- Silvestrini, M. T., et al. Interventional magnetic resonance imaging-guided cell transplantation into the brain with radially branched deployment. Molecular Therapy. 23 (1), 119-129 (2015).
- Faraji, A. H., Rajendran, S., Jaquins-Gerstl, A. S., Hayes, H. J., Richardson, R. M. Convection-enhanced delivery and principles of extracellular transport in the brain. World Neurosurgery. 151, 163-171 (2021).
- Richardson, R. M., et al. T2 imaging in monitoring of intraparenchymal real-time convection-enhanced delivery. Neurosurgery. 69 (1), 154-163 (2011).
- Richardson, R. M., et al. Novel platform for MRI-guided convection-enhanced delivery of therapeutics: preclinical validation in nonhuman primate brain. Stereotactic and Functional Neurosurgery. 89 (3), 141-151 (2011).
- San Sebastian, W., et al. Safety and tolerability of magnetic resonance imaging-guided convection-enhanced delivery of AAV2-hAADC with a novel delivery platform in nonhuman primate striatum. Human Gene Therapy. 23 (2), 210-217 (2012).
- Sauleau, P., Lapouble, E., Val-Laillet, D., Malbert, C. -. H. The pig model in brain imaging and neurosurgery. Animal. 3 (8), 1138-1151 (2009).
- Yin, D., Forsayeth, J., Bankiewicz, K. S. Optimized cannula design and placement for convection-enhanced delivery in rat striatum. Journal of Neuroscience Methods. 187 (1), 46-51 (2010).
- Larjavaara, S., et al. Incidence of gliomas by anatomic location. Neuro-Oncology. 9 (3), 319-325 (2007).
- Pallud, J., Devaux, B., Daumas-Duport, C., Oppenheim, C., Roux, F. X. Glioma dissemination along the corticospinal tract. Journal of Neuro-Oncology. 73 (3), 239-240 (2005).
- White, E., Bienemann, A., Megraw, L., Bunnun, C., Gill, S. Evaluation and optimization of the administration of a selectively replicating herpes simplex viral vector to the brain by convection-enhanced delivery. Cancer Gene Therapy. 18 (5), 358-369 (2011).
- Chen, M. Y., Lonser, R. R., Morrison, P. F., Governale, L. S., Oldfield, E. H. Variables affecting convection-enhanced delivery to the striatum: a systematic examination of rate of infusion, cannula size, infusate concentration, and tissue-cannula sealing time. Journal of Neurosurgery. 90 (2), 315-320 (1999).
- Sterk, B., et al. Initial clinical experience with ClearPoint smartframe array-aided stereotactic procedures. World Neurosurgery. 162, 120-130 (2022).
- Rohrer, M., Bauer, H., Mintorovitch, J., Requardt, M., Weinmann, H. -. J. Comparison of magnetic properties of MRI contrast media solutions at different magnetic field strengths. Investigative Radiology. 40 (11), 715-724 (2005).
- Dawson, H. D. A comparative assessment of the pig, mouse and human genomes. The Minipig in Biomedical Research. 1, 323-342 (2011).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados