Method Article
Cristalização ABCG5/G8 em Ambiente Bitela Lipídica para Cristalografia de Raios-X
Neste Artigo
Resumo
Este protocolo descreve um setup para a cristalização do transportador de esterol ABCG5/G8. ABCG5/G8 é reconstituído em bicelas para cristalização em gota suspensa. O protocolo não requer materiais ou substratos especializados, tornando-o acessível e de fácil adaptação em qualquer laboratório para determinação da estrutura da proteína através da cristalografia de raios X.
Resumo
Os transportadores de ligante de ATP (ABC) constituem proteínas de membrana emblocadas em lipídios. A extração dessas proteínas de membrana da bicamada lipídica para um ambiente aquoso é tipicamente obtida empregando detergentes. Esses detergentes desintegram a bicamada lipídica e solubilizam as proteínas. O habitat intrínseco das proteínas de membrana dentro da bicamada lipídica representa um desafio na manutenção de sua estabilidade e uniformidade em solução para caracterização estrutural. As bicelas, que compreendem uma mistura de fosfolipídios e detergentes de cadeia longa e curta, replicam a estrutura lipídica natural. A utilização de bicelos lipídicos e detergentes serve como um sistema modelo adequado para a obtenção de cristais de difração de alta qualidade, especificamente para determinar a estrutura de alta resolução de proteínas de membrana. Através desses microambientes sintéticos, as proteínas de membrana preservam sua conformação e funcionalidade nativas, facilitando a formação de cristais tridimensionais. Nesta abordagem, o heterodimérico ABCG5/G8 solubilizado em detergente foi reintegrado às células DMPC/CHAPSO, suplementadas com colesterol. Este arranjo foi empregado no procedimento experimental de difusão de vapor para cristalização de proteínas.
Introdução
Os transportadores de ligantes de ATP (ABC) constituem uma superfamília de proteínas de membrana responsáveis por diversos processos de transporte dependentes de ATP através de membranas biológicas 1,2,3,4,5. Essas proteínas transportadoras estão implicadas em doenças cardiovasculares e desempenham um papel significativo na facilitação do efluxo de colesterol para a bile para posterior excreção no fígado. Consequentemente, o metabolismo e o equilíbrio do colesterol têm despertado considerável interesse ao longo dos anos6. Um mecanismo específico envolvido na eliminação de colesterol e outros esteróis do organismo envolve membros da subfamília ABCG humana, notadamente o heterodimérico ABCG5/G8 7,8,9,10. Mutações em qualquer um desses genes interrompem o heterodímero, levando à perda de função e causando sitosterolemia, um distúrbio que afeta o tráfico de esteróis11,12,13. Dada a relevância da doença e seu papel na promoção do efluxo de colesterol, os transportadores de esteróis têm atraído atenção significativa. No entanto, os intrincados detalhes de seu mecanismo molecular e seletividade de substratos permanecem em grande parte não revelados. Assim, a elucidação da estrutura cristalina de ABCG5/G8 é um passo crucial para a compreensão dos mecanismos e funções a jusante no transporte de colesterol.
As proteínas de membrana requerem ancoragem dentro das membranas para dobrar e funcionar corretamente. Consequentemente, a extração de proteínas de membrana de seu ambiente natural frequentemente resulta em instabilidade proteica, enovelamento incorreto e perda de função14,15. Esses desafios ressaltam os principais obstáculos enfrentados na cristalização de proteínas de membrana. Entretanto, a reconstituição de proteínas em bicamadas detergentes sintéticos, como as bicelas, surgiu como solução para essa situação, possibilitando a manutenção de proteínas de membrana em um meio bicamadanativo16. Bicelos são conjuntos de fosfolipídios e detergentes sintéticos suspensos e solubilizados em água. Notadamente, adotam uma estrutura bicamada que mimetiza membranas biológicas16,17,18. As bicelas podem transitar entre as fases líquida e gel com base na temperatura e viscosidade. A cristalização da bicela capitaliza os pequenos discos de bicamada e a baixa viscosidade a temperaturas reduzidas, facilitando a mistura completa de proteínas e soluções de bicela. O tamanho das bicelas depende da relação detergente/lipídio durante o preparo19,20. Os detergentes prevalentes para a formação de bicelas incluem 3-[(3-colelamidopropil)dimetilamônio]-2-hidroxi-1-propanosulfonato (CHAPSO), juntamente com 3-[(3-colelamidopropil)dimetilamônio]-1-propanossulfonato (CHAPS) e 1,2-ditridecanoil-sn-glicerol-3-fosfocolina (DHPC)21. Estes detergentes são usados em conjunto com lipídios como di-miristoil-fosfatidilcolina (DMPC) e 1-palmitoil-2-oleoil-fosfatidilcolina (POPC). Além disso, estudos recentes têm demonstrado a plena funcionalidade das proteínas de membrana dentro das células sob condições fisiológicas. Por exemplo, Lee e colaboradores cristalizaram e relataram com sucesso a estrutura cristalina de ABCG5/ABCG8 com base em uma bicamada lipídica22,23. No processo de cristalização, misturas proteína-bicela podem ser acomodadas usando equipamentos padrão, incluindo robôs de cristalização de alto rendimento24. A viabilidade da utilização de bicelos, no entanto, depende da termoestabilidade das proteínas devido às condições de cristalização em temperaturas mais elevadas. No entanto, quando comparadas a outras técnicas, as condições de cristalização necessárias para proteínas de membrana geralmente permanecem leves, envolvendo baixas concentrações de precipitante, sal e tampão. Isso torna as misturas proteína-bicela e a difusão de vapor ferramentas eficazes e facilmente implementáveis para estudos estruturais de proteínas de membrana.
Este protocolo descreve etapas essenciais na preparação de proteínas e cristalização de bicelas para a determinação da estrutura cristalina de raios X de ABCG5/G8 em alta resolução (Figura 1).
Protocolo
1. Clonagem e expressão proteica
- Clone o gene ABCG5/G8 humano em levedura Pichia pastoris seguindo protocolos prévios25,26. Resumidamente, derive os vetores de expressão pSGP18 e pLIC do pPICZB. Adicione uma tag que codifica um sítio de protease 3C do rinovírus seguido por um peptídeo ligante de calmodulina (CBP) ao término C do cDNA ABCG8 (pSGP18-G8-3C-CBP).
- Adicione uma etiqueta de seis histidinas separada por uma glicina (His 6 GlyHis6) ao término C do cDNA ABCG5 (pLIC-G5-H12). Co-transformar os plasmídeos em Pichia cepa KM71H usando eletroporação.
NOTA: Consulte a Tabela de Materiais para obter detalhes dos plasmídeos, meios e buffers usados. - Cultivar células de levedura transformadas em placas de ágar MD a 28 °C.
- Adicione uma etiqueta de seis histidinas separada por uma glicina (His 6 GlyHis6) ao término C do cDNA ABCG5 (pLIC-G5-H12). Co-transformar os plasmídeos em Pichia cepa KM71H usando eletroporação.
- Após 1-2 dias, selecionar 10-12 colônias e inocular-as em 10 mL de meio base de nitrogênio de levedura de glicerol mínimo (MGY) usando tubos de centrífuga de 50 mL para cultura em pequena escala.
- Faça três pequenos furos na tampa do tubo da centrífuga para melhor aeração. Permitir que as células cresçam a 28 °C com agitação constante a 250 rpm até que a densidade óptica a 600 nm (OD600) atinja 10, geralmente levando 1-2 durante a noite.
NOTA: O crescimento celular geralmente leva entre 12-24 h.
- Faça três pequenos furos na tampa do tubo da centrífuga para melhor aeração. Permitir que as células cresçam a 28 °C com agitação constante a 250 rpm até que a densidade óptica a 600 nm (OD600) atinja 10, geralmente levando 1-2 durante a noite.
- No dia seguinte, tomar 1 L de meio MGY estéril e inocular com a cultura primária em um frasco de 2,4 L. Incubar o balão a 28 °C numa incubadora agitadora a 250 rpm durante 24 horas.
- Para manter o pH entre 5-6, adicionar hidróxido de amônio a 10% (NH4OH) até estabilizar o pH.
- Ajustar o pH e induzir a expressão proteica adicionando 1 ml de metanol puro por 1 L de cultura (0,1 % (v/v) de metanol).
NOTA: Alimentar as células subsequentemente com 5 ml de metanol puro por litro de cultura (0,5 % (v/v) de metanol) a cada 12 h durante uma duração total de 36-48 h. - Colher células centrifugando a 15.000 x g por 30 min a 4 °C.
- Coletar pastilhas de células e ressuspendê-las em tampão de lise (sacarose 0,33 M, Tris-Cl 0,3 M pH 7,5, ácido aminohexanóico 0,1 M, EDTA 1 mM e EGTA 1 mM) até uma concentração de 0,5 g/mL. Conservar a suspensão a -80 °C. Normalmente, pode-se recuperar 30 ± 5 g de massa celular a partir de 1 L de células cultivadas.
NOTA: Armazenar pellets de células diretamente no congelador ou realizar ressuspensão imediata em tampão de lise para preparações de membrana.
2. Preparação da membrana microssomal
- Descongelar as células e adicionar inibidores de protease (2 μg/mL de leupeptina, 2 μg/mL de pepstatina A, 2 mM de PMSF, ver Tabela de Materiais).
- Para lisar ainda mais as células, use um emulsificante ou microfluidificador refrigerado por gelo (consulte Tabela de Materiais) a 25.000-30.000 psi. Repita este processo 3-4 vezes.
- Centrífuga para remover restos celulares: girar a 3.500-4.000 x g por 15 min, seguido por um segundo spin a 15.000 x g por 30 min. Mantenha ambos os giros a 4 °C.
- Para isolar vesículas de membrana microssomal, transferir o sobrenadante para tubos de ultracentrífuga e submetê-lo à ultracentrifugação a 2,00.000 x g por 1,5 h a 4 °C.
- Ressuspender o pellet de membrana em 50 mL de tampão A (50 mM Tris-Cl pH 8,0, 100 mM NaCl e 10% glicerol) usando um homogeneizador dounce. Conservar a suspensão a -80 °C.
3. Preparação-purificação de proteínas de heterodímeros
- Descongelar as membranas microssomais congeladas e ajustar a concentração para 4-6 mg/mL usando tampão de solubilização. O tampão deve conter 50 mM de Tris-HCl, pH 8,0, NaCl 100 mM, glicerol 10%, β-dodecil maltosídeo (β-DDM) a 1%, colato a 0,5% (p/v), hemisuccinato de colesterol a 0,1% (p/v), imidazol 5 mM, β-mercaptoetanol (β-ME) a 5 mM, leupeptina a 2 μg/mL, pepestatina A a 2 μg/mL e PMSF a 2 mM (ver Tabela de Materiais).
NOTA: Pode-se misturar volumes iguais da preparação da membrana e do tampão de solubilização, ou usar 2x tampão de solubilização sem inibidores de protease e agentes redutores. A ebulição curta do tampão ajuda a dissolver o CHS de forma eficiente. Para purificação, utilize apenas o tampão refrigerado a 4 °C.- Agitar a mistura à velocidade média durante 1 h a 4 °C. Siga com agitação adicional à temperatura ambiente (RT) por 20-30 min.
- Centrifugar a mistura a 1,00,000 x g durante 30 min a 4 °C para remover membranas insolúveis. Recolher o sobrenadante solubilizado e adicionar 20 mM de imidazol e 0,1 mM de TCEP.
- Realizar cromatografia em coluna de afinidade26: ligar o sobrenadante solubilizado a esferas de Ni-NTA pré-equilibradas (10-15 mL) (ver Tabela de Materiais) no tampão A (etapa 2.2.1) durante a noite.
NOTA: Evite usar glicerol em buffers de execução a partir deste ponto.- Lavar a coluna duas vezes com 10 volumes de coluna de tampão B (50 mM HEPES, pH 7,5, 100 mM NaCl, 0,1 % (p/v) β-DDM, 0,05 % (p/v) de colato, 0,01 % (p/v) CHS, 0,1 mM TCEP) contendo 25 mM de imidazol.
- Lavar a coluna com 10 volumes de coluna de tampão B contendo imidazol 50 mM.
- Eluir a proteína usando Buffer C (Buffer B com imidazol 200 mM).
- Adicionar 1 mM de TCEP (ver Tabela de Materiais) e 10 mM de MgCl2 às proteínas eluídas.
- Validar as frações eluídas em gel SDS-PAGE para confirmar o tamanho correto da proteína26.
NOTA: Rendimento proteico típico (1ª Ni-NTA): 10-20 mg de proteína por 6 L de cultura. Utilizar DDM a 10x ou 5x de sua concentração micelar crítica (CMC), aproximadamente 0,01%. Este protocolo emprega 0,1% de DDM. - Diluir as frações de pico da eluição de Ni-NTA com um volume igual de Buffer D1 (Buffer B com 1 mM CaCl 2, 1 mM MgCl2), misturar e carregar as frações proteicas em uma coluna CBP (3-5 mL) (ver Tabela de Materiais) que tenha sido pré-equilibrada com o Buffer D1 de lavagem CBP.
- Realizar lavagens sequenciais na coluna CBP para troca de detergentes utilizando Buffer D1 e D2 (Buffer B com 1 mM CaCl 2, 1 mM MgCl2, 0,1% (p/v) decil-maltose neopentilglicol (DMNG), sem β-DDM): primeiramente, lavar com 3 volumes de coluna de D1; segundo, lavar com 3 volumes de coluna de D1:D2 (3:1, v/v); terceiro, lavar com 3 volumes de coluna de D1:D2 (1:1, v/v); quarta etapa, lavar com 3 volumes de coluna de D1:D2 (1:3, v/v), seguido de 6-10 volumes de coluna de D2.
- Eluir a proteína usando o tampão D2 de lavagem com NaCl 300 mM em frações de 1 mL da coluna de CBP (total de 10 mL). Concentrar as frações eluídas em 1-2 mL.
NOTA: O rendimento típico de proteína (1st CBP) é de 5-15 mg de proteína por 6 L de cultura. Os detergentes de maltose neopentilglicol (MNG) melhoram o armazenamento de proteínas purificadas a 4 °C. Tanto DMNG quanto Lauryl MNG (LMNG) foram usados, com DMNG produzindo melhores cristais difratantes de raios-X. Use DMNG a 10-20x de sua concentração micelar crítica (CMC), aproximadamente 0,003%. Esse protocolo utilizou DMNG a 0,1%. Uma fração do eluato de CBP pode ser purificada por cromatografia de gel-filtração (etapa 4.4.) para analisar a atividade ATPase das proteínas ou avaliar a monodispersidade através de microscopia eletrônica de transmissão (MET).
4. Preparação proteica-tratamento de pré-cristalização
- Clivar os glicanos N-ligados e as etiquetas CBP usando endoglicosidase H (Endo H, ~0,2 mg por 10-15 mg de proteína purificada) e protease HRV-3C (~2 mg por 10-15 mg de proteína purificada), respectivamente (ver Tabela de Materiais). Incubar durante a noite a 4 °C.
- Durante a incubação da protease Endo H e 3C, realizar alquilação redutiva sobre as proteínas agrupadas. Comece por incubar com iodoacetamida 20 mM (ver Tabela de Materiais) durante a noite a 4 °C. Siga com uma incubação de 1 h com 2 mM adicionais de iodoacetamida no gelo.
NOTA: Esta etapa estabiliza ainda mais o armazenamento de proteínas por até um mês a 4 °C. - Empregar uma segunda coluna de CBP (1-2 mL) para separar a etiqueta CBP clivada. Use o buffer D2 para esse processo.
NOTA: O rendimento típico de proteína (2ª CBP) é de 5-10 mg de proteína por 6 L de cultura. - Purificar a proteína CBP tag-free usando cromatografia de filtração em gel. O tampão deve conter 10 mM HEPES, pH 7,5, 100 mM NaCl, 0,1% (p/v) DMNG, 0,05% (p/v) colato e 0,01% (p/v) CHS.
NOTA: O rendimento típico de proteínas (filtração em gel) é de 2-8 mg de proteína por 6 L de cultura. Durante esta etapa, a ausência de um pico de DDM (~65 kD) durante a filtração do gel indica o sucesso da troca do detergente para o DMNG. - Modificar as fracções proteicas agrupadas através de metilação redutiva: adicionar 20 mM de dimetilamina borano (DMAB, ver Tabela de Materiais) e 40 mM de formaldeído à proteína. Incubar durante 2 h a 4 °C num agitador oscilatório. Adicione 10 mM DMAB.
- Repetir o passo 4.5, incluindo a adição de 10 mM DMAB, e incubar durante a noite (12-18 h) a 4 °C.
- Interromper a reação adicionando 100 mM Tris-Cl, pH 7,5.
- Carregar a proteína metilada em uma coluna de 2 mL de Ni-NTA pré-equilibrada com Tris-Cl 100 mM, pH 8,0 e NaCl 100 mM.
- Lavar a coluna utilizando 10 volumes de coluna de tampão de lavagem (10 mM HEPES, pH 7,5, 100 mM NaCl, com 0,5 mg/mL DOPC: DOPE (3:1, p/p), 0,1% (p/v) DMNG, 0,05% (p/v) colato, 0,01% (p/v) CHS).
- Eluir a proteína relipidada usando tampão de eluição (10 mM HEPES, pH 7,5, 100 mM NaCl, 200 mM imidazol, 0,5 mg/mL DOPC: DOPE (1:1, p/p), 0,1% (p/v) DMNG, 0,05% (p/v) colato, 0,01% (p/v) CHS).
NOTA: O rendimento típico de proteína (2nd Ni-NTA) é de 1-5 mg de proteína por 6 L de cultura. - Passar os eluados de proteína através de uma coluna de dessalinização PD-10 pré-equilibrada com o tampão utilizado na etapa 4.4.
- Incubar a proteína dessalgada e relipidada durante a noite com colesterol (preparado em isopropanol ou etanol) até uma concentração final de ~20 μM.
- Na manhã seguinte, remova o precipitante por ultracentrifugação a 1,50.000 x g por 10 min a 4 °C. Colete o sobrenadante.
- Concentrar a proteína para uma concentração final de 30-50 mg/mL usando um concentrador centrífugo de corte de 100 kDa.
- Retire o precipitante utilizando uma centrífuga refrigerada de bancada à velocidade máxima durante 30 minutos a 4 °C.
- Manter o sobrenadante sobre gelo a 4 °C e estabelecer condições de cristalização nas bicelas.
NOTA: As proteínas concentradas devem ser usadas para o crescimento de cristais dentro de uma semana. Não congele as proteínas.
5. Cristalização de proteínas em bicelas
- Preparar uma solução-mãe de 10% de bicela com lipídios DMPC e detergente CHAPSO na proporção de 3:1 (p/p) (ver Tabela de Materiais).
NOTA: Use CHAPSO a 5x de sua concentração micelar crítica (CMC), aproximadamente 0,5%. Isso mantém a concentração de detergente ao redor de sua CMC na mistura proteína-bicela (etapa 5.2).- Adicionar detergente dissolvido H2deionizado (CHAPSO) aos lipídios pré-secos (mistura de 5% mol de colesterol e 95% mol de DMPC).
NOTA: Prepare várias composições lipídicas em clorofórmio e seque-as em um tubo de ensaio de vidro usando uma corrente de gás nitrogênio em RT. Elimine solventes residuais colocando-os em uma câmara de vácuo durante a noite, formando uma fina camada lipídica. - Ressuspenda lipídios e detergente usando um sonicador em banho-maria.
- Sonicar a mistura de bicela em água gelada usando energia contínua até que a solução se torne transparente.
OBS: Use protetor auditivo e garanta um suprimento de gelo suficiente para manter a mistura em fase líquida. - Remova os componentes não dissolvidos com um filtro centrífugo de 0,2 μm (ver Tabela de Materiais).
NOTA: Conservar a solução de bicela aliquotada a -80 °C.
- Adicionar detergente dissolvido H2deionizado (CHAPSO) aos lipídios pré-secos (mistura de 5% mol de colesterol e 95% mol de DMPC).
- Crie uma mistura proteína/bicela no gelo combinando suavemente 10% de bicelas (passo 5.1.4) e proteínas (passo 4.7.4) numa proporção de 1:4 (v/v), atingindo uma concentração final de proteína entre 5-10 mg/ml.
- Incubar a mistura de proteína e bicela no gelo por 30 min.
- Configure as condições de cristalização em um formato de difusão de vapor de gota suspensa usando placas de 48 poços.
- Misturar volumes iguais (0,5 ou 1 μL) de mistura proteína/bicela e solução reservatório de cristalização contendo sulfato de amônio 1,6 M-2,0 M, MES 100 mM (pH 6,5), 0%-4% PEG 400 e 1 mM TCEP (ver Tabela de Materiais).
OBS: Criar uma matriz da solução do reservatório antes de cada experimento, ajustando sulfato de amônio (1,6-2,0 M) e PEG 400 (0%-4%). - Incubar para cristalização a 20 °C.
- Verifique as bandejas de cristalização no dia seguinte para garantir a vedação adequada do vidro da tampa.
- Monitore o crescimento de cristais pelo menos uma vez ao dia. Cristais de alta qualidade geralmente aparecem dentro de 1-2 semanas, medindo 50-150 μm x 20-50 μm x 2-5 μm.
NOTA: Os cristais podem demorar mais tempo a formar-se em concentrações de proteína mais baixas. Cristais maduros devem ser colhidos dentro de um mês. - Embeber cristais de proteína em malonato de sódio 0,2 M e congelá-los rapidamente em nitrogênio líquido usando crio-loops de 50 ou 100 μm.
NOTA: Se um difratômetro de raios X estiver disponível, teste alguns cristais com uma exposição de feixe de raios X de 15-30 min para revelar difração de até 5 Å. Difração de alta resolução requer uma fonte de luz síncrotron. Usando malonato de sódio 0,2 M como crioprotetor, um cristal medindo 100 μm x 50 μm x 2 μm pode fornecer cerca de 90 quadros de imagem de difração com raio-X síncrotron.
- Misturar volumes iguais (0,5 ou 1 μL) de mistura proteína/bicela e solução reservatório de cristalização contendo sulfato de amônio 1,6 M-2,0 M, MES 100 mM (pH 6,5), 0%-4% PEG 400 e 1 mM TCEP (ver Tabela de Materiais).
Resultados
Meio-transportadores ABC recombinantes, ABCG5 e ABCG8 humanos, são co-expressos na levedura Pichia pastoris . A fração da membrana da levedura é então fracionada por centrifugação. Conforme descrito neste protocolo, as proteínas heterodiméricas são extraídas por cromatografia em coluna tandem. Posteriormente, proteínas quimicamente pré-tratadas são cristalizadas incubando-as com fosfolipídios/colesterol bicelos. Visões gerais esquemáticas dos processos de purificação e cristalização são fornecidas na Figura 1.
Para avaliar a monodispersidade das proteínas purificadas, amostras contendo 0,01-0,05 mg/mL de proteínas são coradas com acetato de uranila a 1%-2%. Essas amostras são então examinadas com MET negativo (Figura 2A). Para avaliar a estabilidade de proteínas sem a realização de ciclos de congelamento-descongelamento, a cromatografia analítica de filtração em gel é empregada. Essa análise envolve o monitoramento do armazenamento ao longo do tempo das proteínas purificadas por meio do uso de alíquotas pequenas e de igual volume das proteínas (Figura 2B). Pode haver uma ligeira perda de proteínas nas frações de pico após uma semana de incubação a 4 °C, possivelmente devido a agregados proteicos solúveis residuais. No entanto, o rendimento global de proteína permanece suficiente para o crescimento de cristais. O uso de coloração negativa de TEM e cromatografia analítica de filtração em gel é uma prática padrão para avaliar a adequação de proteínas para cristalização, particularmente a partir de diferentes construções projetadas.
Para a avaliação da qualidade proteica em cada etapa do processo de cromatografia em coluna, bem como após o tratamento químico de pré-cristalização, alíquotas de frações correspondentes a duas colunas de Ni-NTA, duas colunas de CBP, uma filtração em gel e alquilação redutiva são carregadas em um gel de SDS-PAGE a 10% (Figura 3). Além disso, o mesmo ambiente reacional utilizado para alquilação pode ser aplicado para marcação de mercúrio com mercúrio etílico (EMTS), embora isso esteja além do escopo do presente estudo.
O crescimento dos cristais é monitorado diariamente usando um estereomicroscópio de mesa equipado com um polarizador. Os cristais maduros e adequados para a coleta de dados geralmente atingem dimensões de 50 μm x 100 μm x 2 μm (Figura 4). Durante o processo de colheita de cristais, cristais menores ou cachos são deliberadamente evitados.
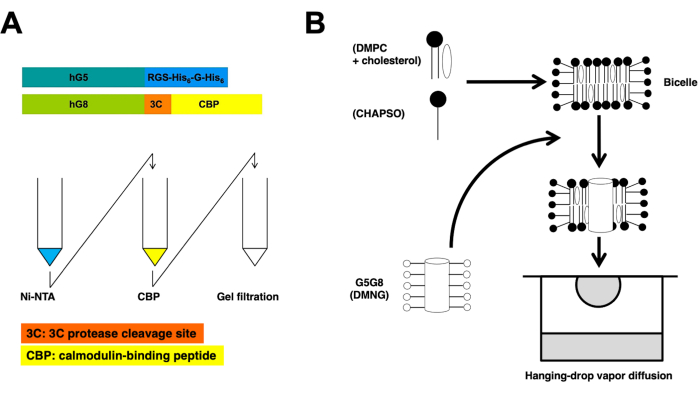
Figura 1: Visões esquemáticas para purificação (A) e cristalização da bicela (B) do heterodimérico ABCG5/G8. Construtos de ABCG5 humano recombinante (hG5) e ABCG8 (hG8) carregam tags RGS-H 6-G-H6 e 3C-CBP, respectivamente (A, topo). Cromatografia em coluna de afinidade em tandem, seguida de cromatografia de filtração em gel para obter purificação heterodimérica (A, fundo). Clique aqui para ver uma versão maior desta figura.
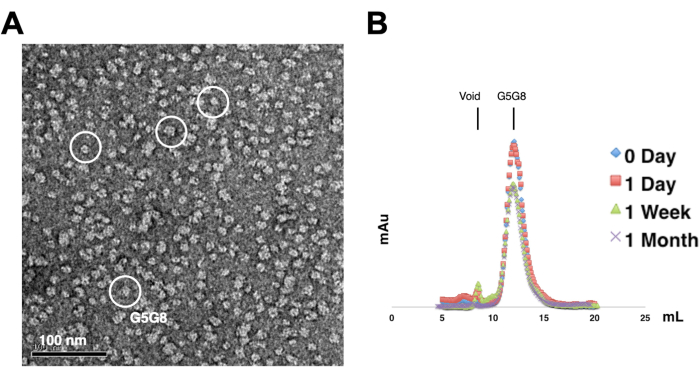
Figura 2: Avaliação da monodispersidade (A) e estabilidade (B) das proteínas purificadas . (A) Micrografia eletrônica de heterodímeros ABCG5/G8 (G5G8) corados negativamente usando MET. Partículas representativas são destacadas em círculos brancos sólidos. Barra de escala = 100 nm. (B) Proteínas alquiladas armazenadas a 4 °C analisadas por cromatografia analítica de filtração em gel ao longo de um mês, com ligeira perda de proteínas após uma semana. Clique aqui para ver uma versão maior desta figura.
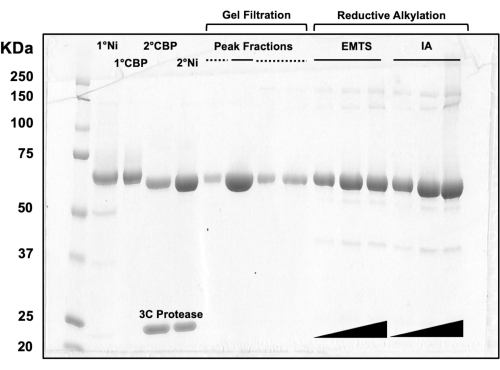
Figura 3: Análise em SDS-PAGE de eluato de proteína por cromatografia em coluna e alquilação redutiva. Vários volumes (1-10 μL) de frações proteicas foram carregados em um gel de Tris/Glicina a 10% e executados por 45 min a uma tensão constante de 200 V. O gel foi corado com azul Coomassie, corado, seco ao ar e escaneado por um scanner de mesa. 1° & 2° Ni: primeira e segunda colunas Ni-NTA; 1° & 2° CBP: primeira e segunda colunas CBP; Linha sólida de Frações de Pico: frações agrupadas para cristalização; Frações de pico linha tracejada: frações de ombro; EMTS: tiosalicinato de mercúrio etílico; IA: iodoacedamida. Clique aqui para ver uma versão maior desta figura.
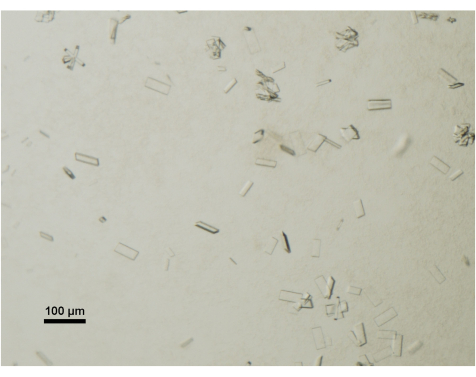
Figura 4: Avaliação da maturação dos cristais de proteínas por microscopia de luz. Cristais maduros de ABCG5/G8 a partir de uma gota de cristalização foram visualizados sob um estereomicroscópio de mesa e equipado com polarizador. Barra de escala = 100 μm. Clique aqui para ver uma versão maior desta figura.
Discussão
Os desafios associados à cristalização de proteínas de membrana têm motivado o desenvolvimento de métodos de cristalização baseados em bicamadas lipídicas, como a abordagem da bicela27 ou da fase cúbica lipídica (LCP)14 . No entanto, alcançar a cristalização bem-sucedida de proteínas de membrana ainda depende da etapa crítica e, às vezes, afunilamento da preparação de proteínas. Notavelmente, os transportadores ABC apresentam um formidável obstáculo no crescimento de cristais adequados para cristalografia de raios X. Este protocolo fornece orientação prática abrangente para simplificar a preparação do transportador de esterol ABCG5/G8 humano e promover o crescimento de cristais através da abordagem de cristalização de bicela.
Uma consideração fundamental na elaboração deste protocolo foi o imperativo de um rendimento proteico substancial nas fases iniciais de purificação proteica, permitindo um certo grau de perda proteica durante o tratamento de pré-cristalização (Figura 3). Estratégias comuns para enfrentar esse desafio envolvem engenharia extensiva de proteínas, utilização de diversos hospedeiros de expressão e exploração de ortólogos ou homólogos, entre outras abordagens. No entanto, com este procedimento aparentemente intrincado, uma série de etapas fundamentais foram identificadas que sustentam o sucesso do protocolo e também fornecem insights sobre possíveis limitações que podem surgir ao estudar outros transportadores ABC ou proteínas de membrana em geral.
Em primeiro lugar, este protocolo emprega centrifugação completa em cada etapa para minimizar a agregação proteica. Além disso, o monitoramento contínuo da termoestabilidade das proteínas purificadas é crucial. A microscopia eletrônica é utilizada para verificar a monodispersão de proteínas, enquanto a filtração analítica em gel rastreia a estabilidade da proteína ao longo do tempo (Figura 2). Técnicas alternativas como dicroísmo circular (CD) ou calorimetria exploratória diferencial (DSC) também poderiam ser incorporadas. Além disso, a incorporação de lipídios em estágios específicos é essencial para maximizar tanto a atividade quanto a cristalogênese do ABCG5/G8 purificado. Por exemplo, colato e CHS são necessários para exibir hidrólise de ATP mensurável; fosfolipídios são indispensáveis para manter a estabilidade das proteínas metiladas; e o colesterol é um componente necessário da solução da bicela, promovendo o crescimento de cristais adequados para difração de raios X de alta resolução (Figura 4).
Em essência, todo o procedimento pode ser realizado dentro de uma semana de esforço. Em contraste com o LCP, a recuperação de cristais de bandejas de cristalização de gotas suspensas é simples. Olhando para o futuro, com um rendimento proteico substancial (aproximadamente 10 mg), este protocolo é facilmente adaptável para o desenvolvimento de investigações cristalográficas envolvendo mutantes ABCG5/G8 ou outras proteínas transportadoras. Isso é particularmente pertinente para os casos que atualmente escapam à visualização por microscopia eletrônica.
Divulgações
Os autores não têm nada a divulgar.
Agradecimentos
Este trabalho é apoiado por uma Bolsa de Descoberta do Conselho de Pesquisa em Ciências Naturais e Engenharia (RGPIN 2018-04070) e uma Bolsa de Projeto de Pesquisa do Canadian Institutes of Health (PJT-180640) para JYL. Este protocolo é baseado nos relatos originais em estruturas cristalinas ABCG5/G8 relatados anteriormente por Farhat et al.22 e Lee et al.23.
Materiais
| Name | Company | Catalog Number | Comments |
| ABCG5 | National Institute of Health collection | NCBI accession number NM_022436 | |
| ABCG8 | National Institute of Health collection | NCBI accession number NM_022437 | |
| ÄKTA FPLC system | Cytiva (formerly GE Healthcare Life Sciences) | ||
| CaCl2 | Wisent | 600-024-CG | Anhydrous |
| CBP | Agilent | 214303 | Calmodulin binding peptide affinity resin |
| Centrifugal concentrators (Vivaspin) | Sartorius | ||
| CHAPSO | Anatrace | C317 | Anagrade |
| Cholesterol | Anatrace | CH200 | |
| CHS | Steraloids | C6823-000 | |
| DMAB | MilliporeSigma | 180238 | 97% |
| DMNG | Anatrace | NG322 | |
| DMPC | Anatrace | D514 | |
| DOPC | Avanti | 850375 | |
| DOPC | Anatrace | D518 | |
| DOPE | Avanti | 850725 | |
| DTT | Fisher | BP172 | |
| Dual Thickness MicroLoops | MiTeGen | ||
| EDTA | BioShop | EDT003 | Disodium salt, dihydrate |
| EGTA | MilliporeSigma | 324626 | |
| Emulsifier (EmulsiFex-C3) | Avestin | ||
| Endo H | New England Biolabs | P0702 | |
| Ethanol | Greenfield | P016EAAN | Ethyl Alcohol Anhydrous |
| Formaldehyde | MilliporeSigma | 252549 | ACS Reagent |
| Glycerol | BioShop | GLY004 | |
| HEPES | BioShop | HEP001 | |
| HRV-3C protease | Homemade | ||
| Imidazole | BioShop | IMD510 | Reagent grade |
| Iodoacetamide | MilliporeSigma | I1149 | BioUltra |
| Isopropanol | Fisher | BP2618212 | |
| Leupeptin | BioShop | LEU001 | |
| MES | MilliporeSigma | 69892 | BioUltra |
| Methanol | Fisher | A412P | |
| MgCl2 | Wisent | 800-070-CG | Hydrated |
| microfluidizer (LM 20) | Microfluidics | ||
| NaCl | BioShop | SOD002 | |
| NH4OH | Fisher | A669-212 | ACS Reagent |
| Ni-NTA superflow | Qiagen | 30430 | Nickel-charged resins |
| PEG 400 | MilliporeSigma | 202398 | |
| Pepstatin | BioShop | PEP605 | |
| PMSF | MilliporeSigma | P7626 | |
| pSGP18 and pLIC | Homemade (derived from pPICZ, Invitrogen) | ||
| SDS | BioShop | SDS003 | |
| Sodium cholate | Fisher | 229101 | |
| Sodium malonate | MilliporeSigma | 63409 | |
| Sucrose | Wisent | 800-081-WG | Ultra pure |
| Superdex 200 30/100 GL | Cytiva (formerly GE Healthcare Life Sciences) | 28990944 | Prepacked gel-filtration column |
| TCEP | |||
| TEM | FEI, Technai | ||
| Tris Base | Fisher | BP152 | |
| β-DDM | Anatrace | D310S | Sol Grade |
| β-mercaptoethanol | MilliporeSigma | ||
| ε-aminocaproic acid | Fisher | AAA1471936 |
Referências
- Hamada, H., Tsuruo, T. Purification of the 170- to 180-kilodalton membrane glycoprotein associated with multidrug resistance. 170- to 180-kilodalton membrane glycoprotein is an ATPase. Journal of Biological Chemistry. 263 (3), 1454-1458 (1988).
- Higgins, F., Hiles, D., Whalley, K., Jamieson, J. Nucleotide binding by membrane components of bacterial periplasmic binding protein-dependent transport systems. The EMBO Journal. 4 (4), 1033-1039 (1985).
- Higgins, F., et al. A family of related ATP-binding subunits coupled to many distinct biological processes in bacteria. Nature. 323 (6087), 448-450 (1986).
- Horio, M., Gottesman, M., Pastan, I. ATP-dependent transport of vinblastine in vesicles from human multidrug-resistant cells. Proceedings of the National Academy of Sciences of the United States of America. 85 (10), 3580-3584 (1988).
- Mimmack, L., et al. Energy coupling to periplasmic binding protein-dependent transport systems: stoichiometry of ATP hydrolysis during transport in vivo. Proceedings of the National Academy of Sciences of the United States of America. 86 (21), 8257-8261 (1989).
- Grundy, M. Absorption and Metabolism of Dietary Cholesterol. Annual Review of Nutrition. 3 (1), 71-96 (1983).
- Berge, E., et al. Accumulation of dietary cholesterol in sitosterolemia caused by mutations in adjacent ABC transporters. Science. 290 (5497), 1771-1775 (2000).
- Repa, J., et al. Regulation of ATP-binding cassette sterol transporters ABCG5 and ABCG8 by the Liver X receptors α and β. Journal of Biological Chemistry. 277 (21), 18793-18800 (2002).
- Yu, L., et al. Stimulation of cholesterol excretion by the Liver X receptor agonist requires ATP-binding cassette transporters G5 and G8. Journal of Biological Chemistry. 278 (18), 15565-15570 (2003).
- Yu, L., et al. Expression of ABCG5 and ABCG8 is required for regulation of biliary cholesterol secretion. Journal of Biological Chemistry. 280 (10), 8742-8747 (2005).
- Lütjohann, D., Björkhem, I., Beil, F., von Bergmann, K. Sterol absorption and sterol balance in phytosterolemia evaluated by deuterium-labeled sterols: effect of sitostanol treatment. Journal of Lipid Research. 36 (8), 1763-1773 (1995).
- Miettinen, A. Phytosterolaemia, xanthomatosis and premature atherosclerotic arterial disease: a case with high plant sterol absorption, impaired sterol elimination and low cholesterol synthesis. European Journal of Clinical Investigation. 10 (1), 27-35 (1980).
- Salen, G., et al. Sitosterolemia. Journal of Lipid Research. 33 (7), 945-955 (1992).
- Caffrey, M. Membrane protein crystallization. Journal of Structural Biology. 142 (1), 108-132 (2003).
- Michel, H. Crystallization of membrane proteins. Trends in Biochemical Sciences. 8 (2), 56-59 (1983).
- Dürr, N., Gildenberg, M., Ramamoorthy, A. The magic of bicelleslights up membrane protein structure. Chemical Reviews. 112 (11), 6054 (2012).
- Dürr, N., Soong, R., Ramamoorthy, A. When detergent meets bilayer: Birth and coming of age of lipid bicelles. Progress in nuclear magnetic resonance spectroscopy. 69 (1), 1-22 (2013).
- Dufourc, J. Bicelles and nanodiscs for biophysical chemistry. Biochimica et Biophysica Acta (BBA) - Biomembranes. 1863 (1), 183478 (2021).
- Beaugrand, M., et al. Lipid concentration and molar ratio boundaries for the use of isotropic bicelles. Langmuir. 30 (21), 6162-6170 (2014).
- Sanders, R., Schwonek, P. Characterization of magnetically orientable bilayers in mixtures of dihexanoylphosphatidylcholine and dimyristoylphosphatidylcholine by solid-state NMR. Biochemistry. 31 (37), 8898-8905 (1992).
- Seddon, M., Curnow, P., Booth, J. Membrane proteins, lipids and detergents: not just a soap opera. Biochimica et Biophysica Acta (BBA) - Biomembranes. 1666 (1-2), 105-117 (2004).
- Farhat, D., et al. Structural analysis of cholesterol binding and sterol selectivity by ABCG5/G8. Journal of Molecular Biology. 434 (20), 167795 (2022).
- Lee, J. Y., et al. Crystal structure of the human sterol transporter ABCG5/ABCG8. Nature. 533 (7604), 561-564 (2016).
- Ujwal, R., Bowie, U. Crystallizing membrane proteins using lipidic bicelles. Methods. 55 (4), 337-341 (2011).
- Johnson, H., Lee, J. Y., Pickert, A., Urbatsch, L. Bile acids stimulate ATP hydrolysis in the purified cholesterol transporter ABCG5/G8. Biochemistry. 49 (16), 3403-3411 (2010).
- Wang, Z., et al. Purification and ATP hydrolysis of the putative cholesterol transporters ABCG5 and ABCG8. Biochemistry. 45 (32), 9929-9939 (2006).
- Faham, S. Crystallization of bacteriorhodopsin from bicelle formulations at room temperature. Protein Science. 14 (3), 836-840 (2005).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados