Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Method Article
Использование плазмонных наноструктур и фотонных кристаллов для работы с улучшенными микро-и наночастиц Манипуляция
В этой статье
Резюме
Плазмонных пинцет и фотонных кристаллов наноструктур показаны для производства полезных улучшений в эффективности и ориентации контроль оптически захвата микро-и нано-частиц.
Аннотация
A method to manipulate the position and orientation of submicron particles nondestructively would be an incredibly useful tool for basic biological research. Perhaps the most widely used physical force to achieve noninvasive manipulation of small particles has been dielectrophoresis(DEP).1 However, DEP on its own lacks the versatility and precision that are desired when manipulating cells since it is traditionally done with stationary electrodes. Optical tweezers, which utilize a three dimensional electromagnetic field gradient to exert forces on small particles, achieve this desired versatility and precision.2 However, a major drawback of this approach is the high radiation intensity required to achieve the necessary force to trap a particle which can damage biological samples.3 A solution that allows trapping and sorting with lower optical intensities are optoelectronic tweezers (OET) but OET's have limitations with fine manipulation of small particles; being DEP-based technology also puts constraint on the property of the solution.4,5
This video article will describe two methods that decrease the intensity of the radiation needed for optical manipulation of living cells and also describe a method for orientation control. The first method is plasmonic tweezers which use a random gold nanoparticle (AuNP) array as a substrate for the sample as shown in Figure 1. The AuNP array converts the incident photons into localized surface plasmons (LSP) which consist of resonant dipole moments that radiate and generate a patterned radiation field with a large gradient in the cell solution. Initial work on surface plasmon enhanced trapping by Righini et al and our own modeling have shown the fields generated by the plasmonic substrate reduce the initial intensity required by enhancing the gradient field that traps the particle.6,7,8 The plasmonic approach allows for fine orientation control of ellipsoidal particles and cells with low optical intensities because of more efficient optical energy conversion into mechanical energy and a dipole-dependent radiation field. These fields are shown in figure 2 and the low trapping intensities are detailed in figures 4 and 5. The main problems with plasmonic tweezers are that the LSP's generate a considerable amount of heat and the trapping is only two dimensional. This heat generates convective flows and thermophoresis which can be powerful enough to expel submicron particles from the trap.9,10 The second approach that we will describe is utilizing periodic dielectric nanostructures to scatter incident light very efficiently into diffraction modes, as shown in figure 6.11 Ideally, one would make this structure out of a dielectric material to avoid the same heating problems experienced with the plasmonic tweezers but in our approach an aluminum-coated diffraction grating is used as a one-dimensional periodic dielectric nanostructure. Although it is not a semiconductor, it did not experience significant heating and effectively trapped small particles with low trapping intensities, as shown in figure 7. Alignment of particles with the grating substrate conceptually validates the proposition that a 2-D photonic crystal could allow precise rotation of non-spherical micron sized particles.10 The efficiencies of these optical traps are increased due to the enhanced fields produced by the nanostructures described in this paper.
протокол
1. Случайные наночастиц Au массива Изготовление 8,10,12,14
- Массивов наночастиц Au формируется сначала создается шаблон, который сделан из плотного слоя адсорбированных случайно латексных шаров с средним диаметром 454 нм. Это достигается за счет испарения первого золота на стекло покровное, чтобы толщиной 20 нм с использованием хрома, как адгезия слоя.
- Монослоя полистирола сфера то самоорганизующихся, подвергая золотым покрытием подложки к смеси 1-этил-3-(3-диметиламинопропил) карбодиимида гидрохлорид (EDC), латексные сферы подвески и де-ионизированной воды.
- Процесс адсорбции разрешено длиться около одного часа, и, не поглощается сферы смыть обильным количеством воды.
- Формируется монослой допускается высохнуть на воздухе.
- Наконец, еще 20 нм золота выпаривают на монослой сферы из латекса для формирования случайного массива наночастиц золота.
- Если SEM доступно, массив AuNP можно увидеть под SEM смотреть, как на рисунке 1 и диаграмма процесса показана на рисунке 8.
2. Биологические Пробоподготовка 9,11
- Подготовка образцов для оптически захвата ядрах клеток мыши в настоящее время показано на рисунке.
- 3T3 ядрах клеток мыши с меткой акридинового оранжевого красителя были получены из группы Тевари на Фреда Хатчинсона онкологический научный центр им.
- 10% бычьего сывороточного альбумина (БСА) в фосфатном буферном растворе (PBS), добавляется в ядрах мыши ячейку в концентрации примерно 1: 10 (BSA: Мышь ядер Cell). BSA помогает предотвратить ядер от прилипания к подложке.
- Смешайте решения с использованием ультразвука.
- 5 мкл наше решение откладывается на массив покровное решетки алюминия. Лучше выполнять этот шаг с алюминиевой решетки на столике микроскопа, так что вам не придется перевозить образца после решения откладывается.
- Два из двух стеков 1 "на 1" покровные используются для поддержки 1 / 5 покровное, через который образец рассматривается.
- Поместите образец под микроскопом для просмотра.
3. Метод Перехват
- Оптический пинцет построены, отправив 35 мВт гелий неонового лазера через Zeiss Axio Imager.D1M оснащен GFP 17 набор фильтров, который изменяется для обеспечения 633 нм лазерного излучения для достижения образца.
- Zeiss LD EC Epiplan - NEOFLUAR 50x цели используется для изображения клеточных ядер, которые примерно 5 микрон в диаметре.
- После того как образец находится под цели, фокус микроскопа на массив наночастиц золота или дифракционной решетки.
- Перевести микроскоп вертикально до достижении фокусировки на ядра, которые вы хотите ловушку.
- Позиция лазерная ловушка месте свыше частиц и частиц должны затем сохранить свои позиции в лазерного пятна даже тогда, когда стадия переведены.
4. Представитель Результаты:
Случайные процедуры наночастиц золота массив должен депозит монослой AuNP о том, что можно посмотреть в SEM, чтобы выглядеть как на рисунке 1. Захват силой, создаваемой этими плазмонных пинцет может быть в 10-20 раз сила, порожденная стандартных оптических пинцетов. Минимальную силу света требуется плазмонных пинцет для достижения удержания частиц приведены для частиц различных размеров на рисунке 4. 9,10 дифракционной решетки достигнута выравнивания и захвата с 20 раз выше, чем эффективность улавливания золота наноточки и может достичь захвата с минимальным до 17 мкВт / мкм 2 (рис. 7). 11
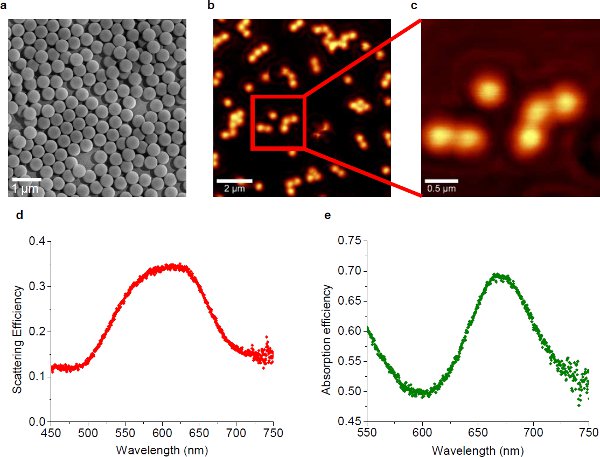
Рис 1 10 () SEM микрофотография самоорганизующихся наночастиц золота. Диаметр отдельных наночастиц золота составляет около 450 нм. (Б) БСОМ образ плазмонных подложки, где наночастицы распределение редких, показывая ближнего поля излучения. Длина волны лазерного возбуждения составляет 633 нм. (С) Высокая зрения увеличения полей, обозначенных красным квадратом в (б). (Г) Рассеяние эффективности спектр плазмонных подложки, показывая пик при 624 нм. (Е) эффективность поглощения спектр плазмонных подложки, показывая пик при 668 нм.
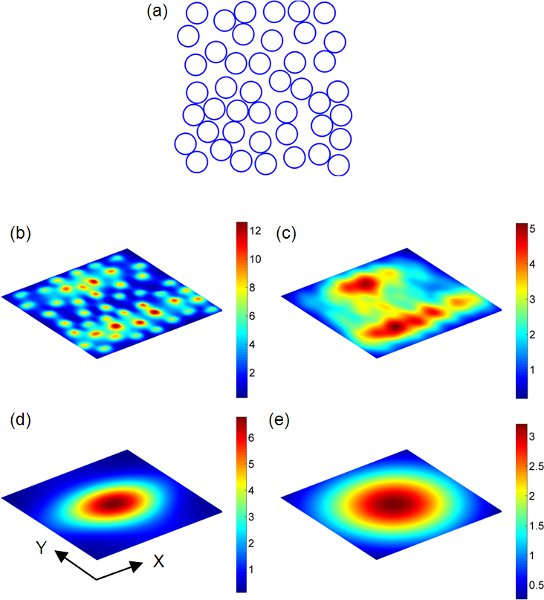
Рисунок 2 13 (а) Au наносферы случайным образом распределены на 2D домена 1 х 1 мкм 2. Каждая синяя точка представляет центр наносфер (= 60 нм). Рассеяния распределения полей по наблюдению самолеты, которые параллельны массив случайных наносферы показаны на (б) - (е). Наносферы массиве равномерно освещенный плоской волны на длине волны 540 нм. Преломления окружающей среды 1.33. Polarization направлении плоской волны направлен вдоль оси Х (горизонтальная в ()). Величина электрического поля инцидент считается 1 в расчет. Расстояние между плоскостью наблюдения и наносферы массив определяется как ч. б) ч =. в) ч = 2а. г) ч = λ. д) ч = 2λ.
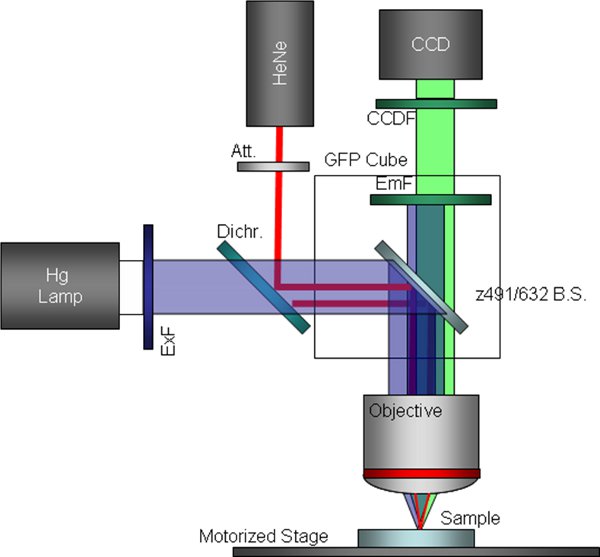
Рис 3 9 Схема настроены флуоресценции конфигурацию микроскопа в том числе обход фильтров возбуждения и заменены дихроичных луч-сплиттер. Это конфигурация, используемая для одновременного захвата и флуоресценции.
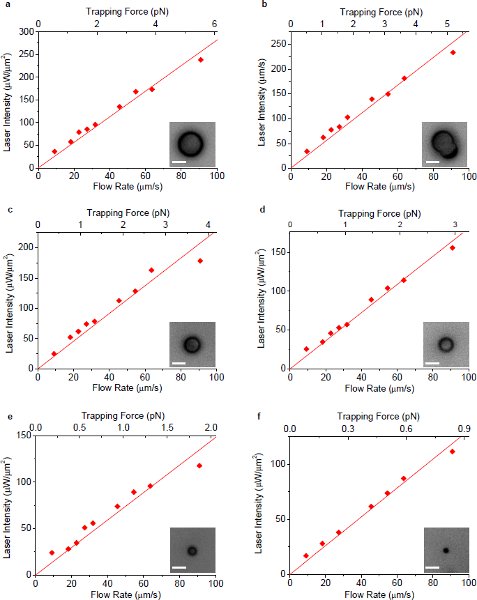
Рис 4 10 интенсивности лазерного минимального поддержания ловушку в зависимости от скорости потока окружающей жидкости использование плазмонных захвата. Все оптические света измеряется в плоскости образца под микроскопом цели. () - (Е) показывают результаты измерений для одной бисера полистирола с диаметром 7,3, 6,3 (несферической), 5,0, 3,9, 2,5 и 1,1 мкм соответственно. Вставках соответствующие микроскопические изображения частиц. Масштабе во всех барах изображения представляют 5 мкм в длину.
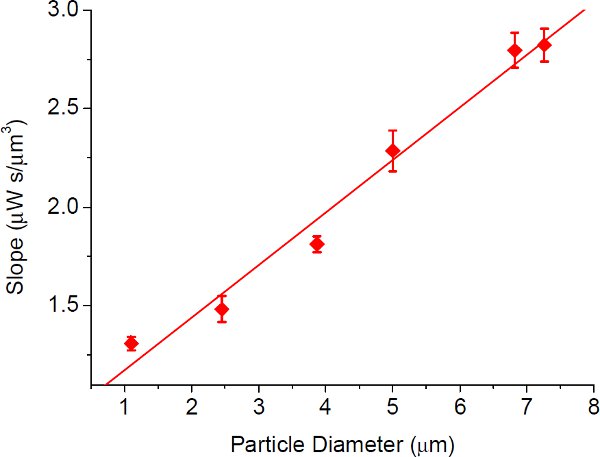
Рис 5 10 склон оборудован линией, проходящей через происхождения на рис. 4 против размер частиц для плазмонных захвата. Погрешности приведены стандартные отклонения линейной подходит. Склона оборудована линия (соотношение между оптическими порог интенсивности и скорости потока) на рис. 4 имеет примерно линейную связь с размером частиц, как показано на этом рисунке, что указывает на преимущество плазмонных захвата особенно для небольших частиц.
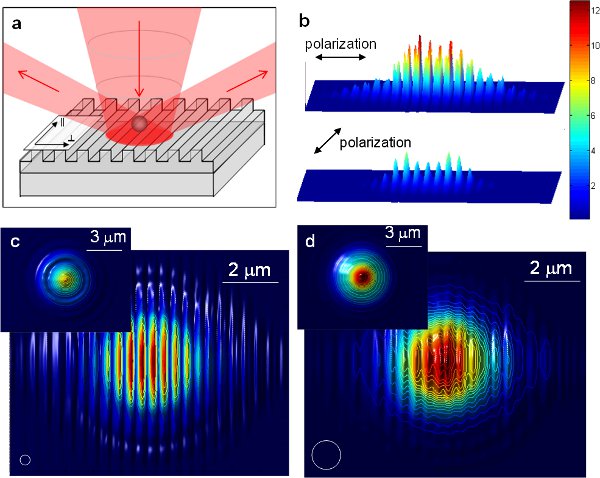
Рисунок 6 11 (а) Схематическое изображение оптического захвата расширение использования 1-D периодических наноструктур. Падающий луч дифрагирует на периодические наноструктуры в дальней зоне. (Б) распределение интенсивности света с двух ортогональных поляризациях наноструктуры в дальней зоне. (Б) распределение интенсивности света с двух ортогональных поляризаций на поверхности алюминиевой решетки с периодом 417 нм, полученные с использованием FDTD моделирования. Распределения нормирована на интенсивность на плоской поверхности алюминия. (С) и (г) Перехват потенциал для частицы непосредственно над поверхностью решетки по сравнению расположение частиц для (с) 350 нм полистирола шарик и (г) 1 мкм полистирола борта. Белые кружки иллюстрируют размеры частиц. На врезках захвата потенциальных над плоской поверхностью алюминия для одинакового размера частицы как сравнение. Значения нормированы для каждого размера частиц. Для всех фигур FDTD моделирования поле зрения 10 х 8 мкм 2.
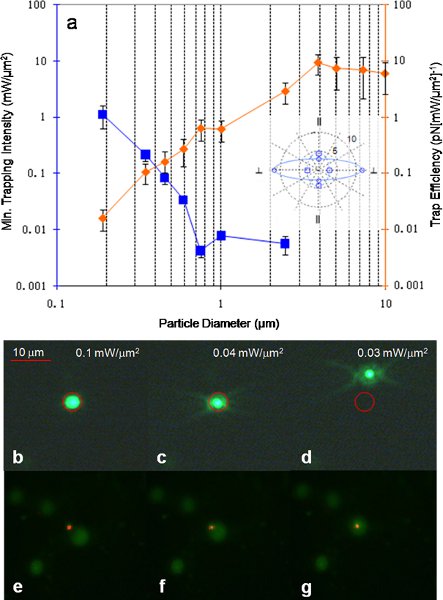
Рисунок 7 11 (а) эффективность ловушки и минимальной интенсивности захвата измеряется для полистирола различных размеров с поляризации пучка перпендикулярно линии решетки. Врезка показывает ловушку асимметрии в эффективности улавливания для перевода 3,87 мкм полистирола бусинка перпендикулярно и параллельно правила решетки. Сплошная линия (большой асимметрии) получается с падающий свет поляризован перпендикулярно к решетке, и пунктирная линия (небольшая асимметрия) получается с инцидентом света, поляризованного параллельно решетки. Устройство находится в (PN [мВт / мкм 2] -1). (Б) - (г) Перехват демонстрации флуоресцентных 590 нм полистирола борта. Красный круг показывает положение лазерного пятна, как лазерный свет был слишком тусклым, чтобы не было видно. Сначала частицы в ловушке пятно в высшую силу, как власть опускается броуновское движение частиц преодолевает силу захвата, что позволяет частиц к бегству. (Е) - (г) Перехват демонстрации флуоресцентных ядра раковых клеток яичников. Минимальной интенсивности, необходимое для начала захвата был 16 мкВт / мкм 2 получены с использованием 20-кратным объективом.
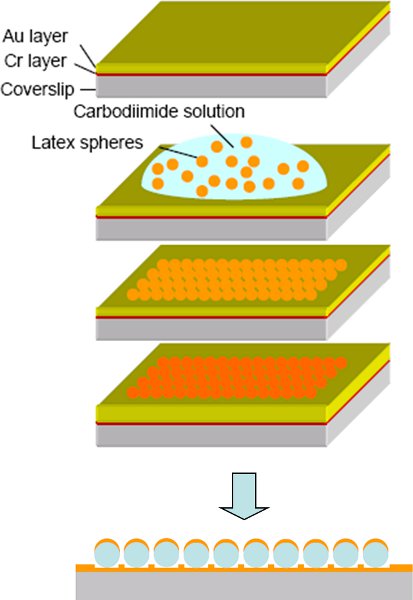
Рис 8 14 Изготовление процедуры крышкой формы наночастиц золота:) Испарение Cr и Au тонким слоем на стекло покровное. б) Воздействие на подвеску полистирола сферы и адсорбции сферах в течение 1 часа. в) удаление без адсорбированных полистирола сферах и сушки поверхности. г) Испарение еще один слой золота поверх шаблона сферах. д) Схема крышкой формы наночастиц Au массив, в котором Au распространяется только на верхней стороне шаблона сферах.
Обсуждение
Значение этих методов захвата является то, что они снижают интенсивности оптического необходимых для устойчивого захвата откуда-то порядка 10 3 мкВт / мкм 2, чтобы где-то порядка 10 мкВт / мкм 2. 10,11 ограничения на эти методы в том, что золотые наночастицы массив опыта отопл?...
Раскрытие информации
Нет конфликта интересов объявлены.
Благодарности
Мы также хотели бы поблагодарить Сяоюй Мяо и Бена Уилсона для разработки большинства методов, описанных в пределах. Эта работа финансировалась Национальным научным фондом (DBI 0454324) и Национального института здоровья (R21 EB005183) и PHS НРСА T32 GM07270 от NIGMS к ECK.
Материалы
| Материал Имя | Тип | Компания | Номер в каталоге | Комментарий |
| Axio Imager микроскоп | D1M | Zeiss | D1M | Zeiss Axio Imager.D1M |
| Объектива микроскопа | 50x/0.55 | Zeiss | Л. Д. ЕС Epiplan - NEOFLUAR 50x/0.55 HD DIC | |
| Микроскоп Zeiss камера | AxioCam MRC | Zeiss | ||
| Гелий неонового лазера | 35 мВт | Исследования Электро-Оптика | ||
| Переменный аттенюатор | Непрерывно Переменная ND | ThorLabs | НДЦ-100С-4М | Для регулировки интенсивности микроскопом |
| Zeiss набора фильтров | Фильтры Set # 17 | Zeiss | 488017-9901-000 | Фильтры Set # 17 |
| Микроскоп Слайды | Толщиной 0,5 мм | VWR | ||
| 3T3 ядрах клеток мыши | Фреда Хатчинсона онкологический научный центр | Магазин так холодно, как возможно | ||
| Акридинового оранжевого красителя | Фреда Хатчинсона онкологический научный центр | |||
| Бычьего сывороточного альбумина | От 1 до 10 паек в PBS | Фреда Хатчинсона онкологический научный центр | ||
| 454 нм сферы полистирола латекса | Polysciences, Inc | |||
| карбодиимида гидрохлорид (EDC) | 1-этил-3-(3-диметиламинопропил) | G-биологических наук | BC25-1 | |
| золото (для осаждения) | ||||
| Отражающие исключено дифракционной решетки | Эдмунд оптики | |||
| Фосфатно-солевым буфером (PBS) | Дульбеко фосфатно-солевом буфере (D-би-эс) (1X) | Invitrogen | 14190-144 | |
Ссылки
- Jones, T. B. . Electromechanics of Particles. , (1995).
- Ashkin, A. Optical trapping and manipulation of neutral particles using lasers. Proc. Natl. Acad. Sci. U.S.A. 94, 4853-4853 (1997).
- Neuman, K. C., Chadd, E. H., Liou, G. F., Bergman, K., Block, S. M. Characterization of photodamage to Escherichia coli in optical traps. Biophys. J. 77, 2856-2856 (1999).
- Chiou, P. C., Ohta, A. T., Wu, M. C. Massively parallel manipulation of single cells and microparticles using optical images. Nature. 436, 370-370 (2005).
- Hsu, H. Y., Ohta, A. T., Chiou, P. Y., Jamshidi, A., Nealea, S. L., Wua, M. C. Phototransistor-based optoelectronic tweezers for dynamic cell manipulation in cell culture media. Lab Chip. 10, 165-172 (2010).
- Righini, M., Ghenuche, P. S., Cherukulappurath, V., Myroshnychenko, F. J., Garcia de Abajo, R. Quidant Nano-optical Trapping of Rayleigh Particles Escherichia coli Bacteria with Resonant Optical Antennas. Nano Letters. 9, 3387-3391 (2009).
- Righini, M., Zelenina, A. S., Girard, C., Quidant, R. Parallel and Selective Trapping in a Patterned Plasmonic Landscape. Nature Physics. 3, 477-480 (2007).
- Miao, X., Lin, L. Y. Large dielectrophoresis force and torque induced by localized surface plasmon resonance of a cap-shaped Au nanoparticle array. Opt. Lett. 32, 295-297 (2007).
- Wilson, B. K. . Manipulation of Nanoparticles and Biological Samples through Enhanced Optical Forces [dissertation]. , (2009).
- Miao, X. Y., Wilson, B. K., Pun, S. H., Lin, L. Y. Optical manipulation of micron/submicron sized particles and biomolecules through plasmonics. Optics Exp. 16, 13517-13525 (2008).
- Wilson, B. K., Mentele, T., Bachar, S., Knouf, E., Bendoraite, A., Tewari, M., Pun, S. H., Lin, L. Y. Nanostructure-enhanced laser tweezers for efficient trapping and alignment of particles. Optics. Exp. 18, 16005-16013 (2010).
- Miao, X., Wilson, B. K., Cao, G., Pun, S. H., Lin, L. Y. Trapping and Rotation of Nanowires Assisted by Surface Plasmons. IEEE Journal of Selected Topics in Quantum Electronics. 15, 1515-1520 (2009).
- Miao, X. Y., Lin, L. Y. Trapping and manipulation of biological particles through a plasmonic platform. IEEE Journal of Selected Topics in Quantum Electronics. 13, 1655-1662 (2007).
- Miao, X. . Plasmonics for Micro/Nano Manipulation and Optofluidics [dissertation]. , (2008).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены