Method Article
Подготовка и инактивации болезнетворных микроорганизмов из продуктов Double Dose Buffy Coat тромбоцитов помощью перехвата системных крови
В этой статье
Резюме
В данной статье описывается процесс, используемый Эребру университет больницы для получения двойной дозы лейкомассы концентратов тромбоцитов готовят из цельного донорства крови и обрабатывали перехвата системных крови для инактивации болезнетворных микроорганизмов. В пробирке Качество конечного тромбоцитов единиц оценивается более 7 дней хранения.
Аннотация
Центры крови сталкиваются со множеством проблем, включая максимизации доходности производства из крови продуктов они получают пожертвования, а также обеспечение максимально возможного уровня безопасности для переливания пациентам, включая защиту от переливания передающихся половым путем. Это должно быть выполнено в финансово ответственным способом, который сводит к минимуму операционные расходы, включая расходные материалы, оборудование, отходы, и расходы на персонал, в частности.
Существует несколько методов для получения концентратов тромбоцитов для переливания. Одним из наиболее распространенных является метод лейкомассы, в которой один терапевтический блок тромбоцитов (≥ 2,0 x10 11 тромбоцитов в единице или в местных правил) получают путем объединения слоев лейкомассы от и до целых шесть донорства крови. Процедура получения "двойную дозу" цельной крови тромбоциты, полученные только недавно была разработана.
Представленные здесь новый метод подготовкидвойной дозы цельной крови, полученных концентратов тромбоцитов из бассейнов из 7 слоев Баффи и последующей обработкой двойных единиц дозы с INTERCEPT системы крови для инактивации болезнетворных микроорганизмов. INTERCEPT был разработан для инактивации вирусов, бактерий, паразитов и загрязняющих доноров белых клеток, которые могут присутствовать в донорской крови. Сопряжение пересечения с методом двойного дозы Баффи пальто, используя INTERCEPT обработки указан с двумя контейнерами для хранения ("DS набор"), позволяет центров крови для лечения каждого из своих двойных единиц доз в одном возбудителя набор обработки инактивации, тем самым максимально безопасность пациента при минимальных затратах. Двойная доза лейкомассы метод требует меньше охристые пальто и сокращает использование расходных материалов до 50% (например, объединение множеств, наборы фильтров, тромбоцитов решение добавка, и стерильных пластин связи) по сравнению с подготовкой и лечения разовую дозу лейкомассы тромбоцитов единиц . Другие экономии включают меньше отходов, меньше оборудования поддерживающейCE, низкие требования к энергопотреблению, сокращение времени персонала, и нижние коллекция стоимости по сравнению с афереза техники.
протокол
1. Всего для сбора крови
- Соберите цельную кровь от доноров, волонтеров в 450 мл верхнего / нижнего коллекции устанавливает в соответствии с местными руководящими принципами сбора крови.
- Цельная кровь хранится в течение как минимум 2 часа на охлаждение пластины до центрифугирования и разделения.
2. Buffy Coat подготовка
- Центрифуга цельной крови при использовании жесткого спина для разделения крови на три слоя: красных кровяных клеток, лейкомассы и плазмы. Центрифуга параметры были использованы 4880 RCF в течение 11 мин при температуре 22 ± 2 ° C.
- Использование автоматизированных сепаратор крови, чтобы выразить плазмы в верхние сумку спутника и красных кровяных телец (эритроцитов) в нижней сумку спутника, оставив Баффи пальто в коллекции контейнер. Целевая средний объем и гематокрита диапазоны для охристые пальто примерно 48 мл и 37%, соответственно.
- Охристо-пальто хранятся в ночь на агитатора тромбоцитов на 22 ± 2 ° C.
3. Buffy Coat пула
- Стерильные Connect 7 охристые пальто и 300 мл SSP + тромбоцитов решения добавки (PAS) в поезде конфигурации с параллельными линиями для уменьшения длины поезда; PAS должны быть в верхней части поезда. Clamp линию между ССА и первый слой кровяного сгустка.
- Откройте стерильную связей между единицами лейкомассы и позволяют охристые пальто, чтобы стекать в последний контейнер.
- Откройте сварного шва и зажима между ПА и первый слой кровяного сгустка. Разрешить треть добавка раствор для полоскания через каждый из контейнеров лейкомассы последовательно. Повторите еще 2 раза каждый раз используя половину оставшегося PAS.
- Средняя Баффи пальто бассейна объем должен быть примерно 600 мл. Если объем целевых и гематокрита отдельных слоев Баффи выполнены, плазма соотношение будет 32 - 47%, как требуется для перехвата возбудителя лечение инактивации позже в процессе.
- Откажитесь от пустых SSP + и Баффипальто контейнеров.
- Для оптимального восстановления тромбоцитов, сохранить бассейн на агитатором за 1 час до центрифугирования.
- Стерильные подключить контейнер для хранения тромбоцитов со встроенным фильтром leukoreduction в бассейн Баффи пальто.
- Выполните «мягкую спина" на бассейн лейкомассы отделить красные кровяные клетки из тромбоцитов в суспензии (462 RCF за 9 мин, 20 сек). Выразите суспензии тромбоцитов с использованием автоматизированной сепаратор крови через leukoreduction фильтр в контейнер для хранения тромбоцитов.
- Описанные выше требования к обработке убедиться, что суспензии тромбоцитов соответствует спецификациям INTERCEPT обработки 300 мл - 420 мл объема, 2.5-7.0 х 10 11 тромбоцитов дозу, и ≤ 4 х 10 6 / мл эритроцитов.
4. INTERCEPT лечение
- Выполните INTERCEPT лечение до конца 1-го дня после сбора (день 0, день сбора).
- Берем INTERCEPT Set обработкас двумя контейнерами для хранения из прозрачного пластика сумке.
- Стерильные подключить тромбоцитов контейнер подвеска НКТ amotosalen контейнер на INTERCEPT набор обработки.
- Этикетка INTERCEPT контейнеры, установленные обработки хранения с соответствующей идентификации продуктов крови после местных требований.
- Повесьте тромбоцитов и разбить сначала нижнюю полую иглу в контейнер amotosalen, позволяя amotosalen решение поступать в освещении контейнер. Пробой верхней полой иглы в контейнере amotosalen позволяет тромбоцитов течь через amotosalen контейнера в контейнер освещения.
- Аккуратно перемешайте тромбоцитов и amotosalen смеси и выразить воздуха от освещения контейнера в контейнер amotosalen.
- Выразите небольшое количество тромбоцитов смесь в трубку, заполняя около 4 см трубы. Это гарантирует тромбоцитов в обеих труб и освещение контейнера пройти возбудителя inactivatiна лечение.
- Уплотнение труб между контейнером для освещения и amotosalen контейнер. Оставьте не более чем примерно на 4 см насосно-компрессорных труб простирается от освещения контейнера. Снять и выбросить пустую тромбоцитов и amotosalen контейнеров и закрыть зажимы на отбор проб мешки.
- Поместите обработки набора в иллюминатор с подсветкой контейнер в большом отсеке слева и организатор в небольших отсека на правой стороне.
- С помощью ручного устройства штрих-кода для входа в дар ID, код продукта и обработки набора номера партии в иллюминатор. Закройте металлическую крышку и при появлении запроса на подсветку графического интерфейса, закройте ящик. Нажмите кнопку "Пуск", чтобы начать освещение.
- После освещение, удалить обработкой множества от осветителя. Подсветка автоматически печатает отчет для лечения обработанных тромбоцитов блока (блоков).
- Берем контейнеров из организаторов и повесить рlatelets и обработки множества, сломать канюлю на выходе из контейнера освещенности и позволяют тромбоцитов поступать в устройство соединения адсорбции (CAD) контейнер.
- Забота, чтобы не погнуть пластины CAD, выразить воздух из контейнера CAD в освещении контейнер с помощью плазмы экстрактор.
- Уплотнение трубы рядом с впускным отверстием контейнера CAD. Удаляют пустой контейнер освещения.
- Поставьте контейнер CAD с прилагаемыми контейнеры для хранения тромбоцитов на агитатора по крайней мере 6 часов, но не более чем на 16 часа. Это приведет к снижению остаточной amotosalen в концентрации ≤ 2 мкм.
- После лечения ИБС, удалить тромбоцитов единиц от агитатора. Повесьте тромбоцитов. Перерыв канюли и позволяют тромбоцитов поступать в контейнерах для хранения.
- Выразите воздух из емкости в емкость CAD. Пусть тромбоцитов остаточного обратного потока концентрата в хранении контейнеровтяжести. Уплотнение трубки над Y-монтаж и удалите пустой контейнер CAD.
- Распространении объем между контейнеры для хранения по мере необходимости. Объем вносятся корректировки путем взвешивания контейнеров для хранения. Уплотнение трубки к каждой емкости для хранения нескольких сантиметрах над входом в контейнер для хранения, это облегчает получение стерильных образцов из конечного продукта, как описано в 5.2.
5. Продукт дискретизации
- Для рутинного тестирования QC, окончательное контейнеры для хранения можно попробовать один раз с использованием выборки сумку на хранение контейнеров. Чтобы сделать это, убедитесь, что тромбоцитов устройство хорошо перемешать, затем откройте зажим для мешочек и отжать несколько раз. Уплотнение труб после сумке была наполнена тромбоцитов. Передача тромбоцитов образца в соответствующей трубе лаборатории и выполняют анализы сразу.
- Для получения образцов в различные моменты времени в течение хранения, например, для проверки исследования, стерильные подключенияновый контейнер отбора проб для труб из контейнера для хранения тромбоцитов. Убедитесь, что тромбоциты хорошо перемешивают до передачи на отбор проб контейнеров.
6. В пробирке функции оценки
- Для этой проверки исследования, в оценке пробирке была проведена после CAD лечения (день 1 или 2-й день, в зависимости от продолжительности CAD) и снова в День 4 (или 5-й день) и День 7. Экстракорпоральное измерений включены объемы, количество тромбоцитов, рН, газов крови (рО 2, рСО 2), глюкозы, лактата, и закрученной.
- Том был определен вес, используя 1,01 г / мл, удельный вес тромбоцитов в аддитивной решение.
- Гемоглобин загрязнения оценивали визуально с помощью сравнения с цветовой шкалой.
- Swirling определяется визуально.
- См. "Таблица оборудования» для методологии других анализов.
7. Представитель Результаты
Процесс производства Double дозы лейкомассы тромбоцитов начинается с производства отдельных слоев охристый, которые отвечают спецификации для целевого объема и гематокрита. Как это не практично для измерения гематокрита отдельных охристые пальто в течение последних процессе проверки, мы начали проведение отдельного усилия, чтобы оптимизировать наши охристые пальто, чтобы мы могли последовательно выполнить запланированный объем и гематокрита. Как показано в таблице 1, наш оптимизированный для пальто Баффи выгодно, чтобы целевые значения для объема и гематокрита на уровне 46 ± 2 мл и 37 ± 3%, соответственно.
После объединения, объем и гематокрита на бассейн Баффи пальто должно быть примерно 600 мл и 20%, соответственно, до мягких центрифугирования спина. Как показано в таблице 2, наши бассейны лейкомассы среднем 615 ± 5 мл; гематокрита среднем 19 ± 1%.
Мягкая спина центрифугирование приводит к двойной концентрированной дозы тромбоцитовentrate, который будет соответствовать входным требованиям к инактивации болезнетворных микроорганизмов использования INTERCEPT системы крови DS обработки множества. Основные входные параметры для INTERCEPT лечения включают объемы, количество тромбоцитов, плазмы отношение, РБК содержания. Кроме того, мы стремимся восстановить ≥ 75% тромбоцитов в концентрат тромбоцитов по сравнению с бассейном Баффи пальто. В соответствии с местными требованиями, белых кровяных клеток (WBC) загрязнение должно быть <1x10 6 / ед. Концентратов тромбоцитов в нашей проверки встретились с ключевыми параметрами для автоматической переадресации обращения, а также задачи по версии WBC загрязнения и восстановления тромбоцитов, как показано в таблице 3.
INTERCEPT процесс инактивации болезнетворных микроорганизмов осуществляется на двойные дозы тромбоцитов концентрат с помощью единого набора обработки перехватить. Обработка набор содержит два встроенных контейнеров для хранения, которые позволяют рассматривать блок должен быть разбит на два отдельных терапевтических доз тромбоцитов при завершении путиOgen инактивации процесса. Европейские руководящие принципы требуют, чтобы 75% единиц испытания содержат ≥ 200х10 9 тромбоцитов на терапевтическое dose1; местным требованиям в Швеции требуют, что 75% единиц испытания содержат> 240x10 9 тромбоцитов на дозу. После INTERCEPT лечения, среднее содержание тромбоцитов составлял 265 ± 22 x10 9 (N = 24). Кроме того, 88% единиц выполнены или перевыполнены 240x10 9 тромбоцитов в терапевтических дозах, это хорошо в обеих европейских принципов и шведского законодательства. См. рисунки 1 и 2 для иллюстрации двойную дозу препарата охристые пальто и INTERCEPT процессов обработки соответственно.
Для этой проверки, мы измерили в пробирке характеристик концентратов тромбоцитов после INTERCEPT лечения (т.е. после раскола в отдельные контейнеры для хранения); параметры измерялись в течение 7 дней хранения. Средние и стандартные отклонения были собраны длятромбоцитов дозу, рН, рО 2, рСО 2, лактата производство и потребление глюкозы.
Рисунок 3 показывает среднее, начиная тромбоцитов дозу двойную дозу тромбоцитов концентрата до INTERCEPT лечения и средних доз тромбоцитов в каждой из расщепленных продуктов после INTERCEPT лечение более 7 дней хранения. Тромбоцитов потерь во время хранения составляет примерно 9%. Это сокращение является не отличаются от ожидаемых потерь во время хранения тромбоциты обычных пластинок 2.
В таблице 4 приведены характеристики в пробирке из INTERCEPT тромбоцитов после обработки и расщепления на отдельные единицы.
По европейским требованиям, рН тромбоцитов должно оставаться выше 6,4 и до конца срока годности. Во время обработки, рН концентратов тромбоцитов снижается незначительно на основе тромбоцитов, концентрации, объема и газопроницаемость тромбоцитов СТОярости контейнер. рисунке 4 показана рН разделения тромбоцитов продукции более 7 дней хранения. Во время хранения, рН является стабильным и хорошо поддерживается в пределах требований к обработке.
Как показано на рисунках 5А и 5В, тромбоцитов потребления O 2 и CO 2 производства указывают на продолжающееся дыхания INTERCEPT тромбоцитов в PL2410 контейнере в течение 7 дней хранения. Цифры 6А и 6Б показать лактата и глюкозы в крови за 7 дней хранения . Тромбоцитов потребление глюкозы и лактата согласуются друг с другом в течение 7 дней хранения. 5 единиц был уровень глюкозы менее 1,11 ммоль / л (нижний предел для анализа глюкозы).
Подготовка лейкомассы и объединения проверка производится концентратов тромбоцитов, которые отвечают критериям для входа INTERCEPT лечения, а именно, объем, количество тромбоцитов, плазмы отношение, и красный BLдревесины клетки загрязнения. Окончательный единиц встретились критериев оценки более 7 дней хранения в том числе тромбоцитов дозу и рН.
| Параметр | Целевой диапазон | Результаты Среднее ± SD |
| Объем (мл) | ~ 48 | 46 ± 2 |
| Гематокрит (%) | ~ 37 | 37 ± 3 |
| Время удержания до объединения | Ночевка на агитатора | Ночевка на агитатора |
Таблица 1. Характеристика отдельных Баффи пальто (n = 19).
| Параметр | Целевой диапазон | Результаты Среднее ± SD |
| Объем (мл) | ~ 600 | 615 ± 5 |
| Хематocrit (%) | ~ 20 | 19 ± 1 |
| Время удержания перед центрифугированием | 1 час на агитатора | 1 час на агитатора |
Таблица 2. Характеристики пальто Баффи бассейны (п = 12).
| Параметр | Цель | Результаты Среднее ± SD |
| Объем (мл) | 370 - 420 | 404 ± 8 |
| Количество тромбоцитов (x10 9 / блок) | 250 - 700 | 577 ± 62 |
| Среднее восстановление тромбоцитов (%) | ≥ 75 | 75 ± 4 |
| Плазменные доли (%) | 32 - 47 | 38 ± 1 |
| РБК (x10 6 / мл) | ≤ 4 | 1,2 ± 0,4 |
| WBC (x10 6 / блок) | ≤ 1 | 0,11 ± 0,1 |
| Время удержания перед INTERCEPT (HR) | ≤ концу 1-й день | ≤ концу 1-й день |
Таблица 3. Характеристики двойной дозы концентратов тромбоцитов (п = 12).
| Среднее ± SD | Мин | Макс | |
| Объем (мл) | 199 ± 16 | 182 | 236 |
| Количество тромбоцитов (x10 9 / блок) | 265 ± 22 | 225 | 292 |
| рН (22 ° C) | 6,9 ± 0,1 | 6,8 | 7,0 |
| рО 2 (кПа) | 21,4 ± 4,8 | 12,8 | 27,3 |
| рСО 2 (кПа) | 4,3 и плusmn, 0,4 | 3,3 | 4,9 |
| Лактата (ммоль / л) | 9,1 ± 1,7 | 6,8 | 12,4 |
| Глюкоза (ммоль / л) | 5,3 ± 0,9 | 3,7 | 6,5 |
Таблица 4. Характеристики INTERCEPT Обработанные Тромбоциты День 1/2 (одной единицы, п = 24).
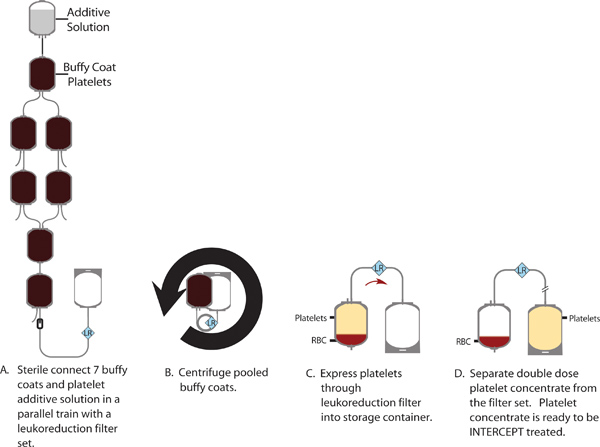
Рисунок 1. Производство концентрата тромбоцитов двойной дозе от бассейна из 7 охристые пальто.
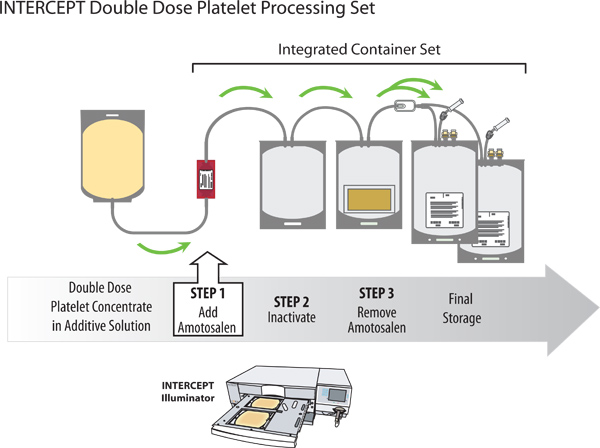
Рисунок 2. Инактивации болезнетворных микроорганизмов с двойной концентрат тромбоцитов дозу с INTERCEPT системы крови.
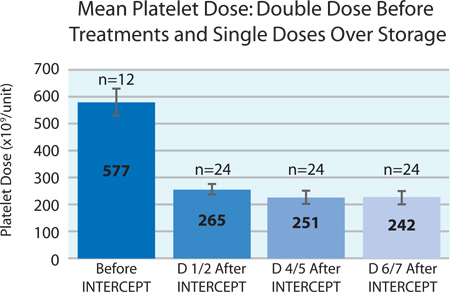
Рисунок 3. Средние дозы тромбоцитов до и в течение7 дней после INTERCEPT лечения (п = 12 до INTERCEPT, п = 24 после перехвата).
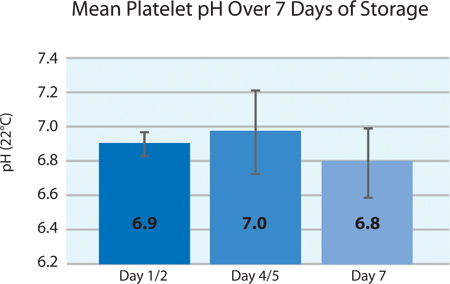
Рисунок 4. Средние тромбоцитов рН ± SD INTERCEPT после лечения (n = 24).
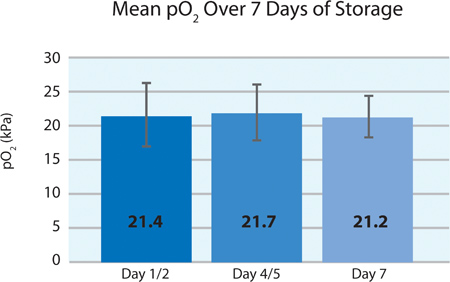
Рисунок 5А. Среднее рО 2 ± SD INTERCEPT после лечения (n = 24).
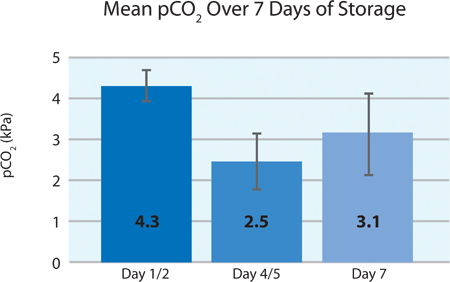
На рисунке 5б. Среднее рО 2 ± SD INTERCEPT после лечения (n = 24).
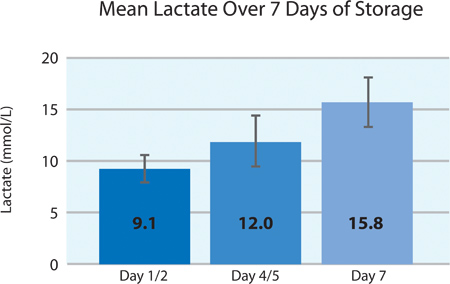
Рисунок 6А. Средний уровень лактата ± SD INTERCEPT после лечения (n = 24).
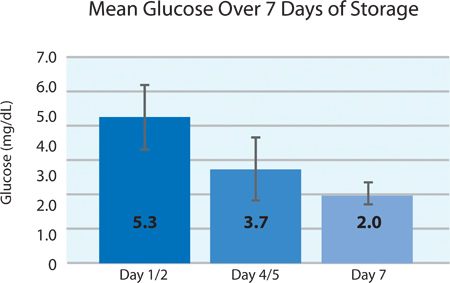
Рисунок 6B. Средние уровни глюкозы иplusmn; SD после лечения INTERCEPT (п = 24).
Обсуждение
Тромбоцитов Баффи пальто требует нескольких этапов обработки, в результате пост-коллекцию расходы, включая персонал времени, расходных материалов, оборудования и отходов, которые должны быть учтены в общей стоимости производства тромбоцитов единиц. Улучшение тромбоцитов выход из каждой Баффи пальто (через оптимизацию объема лейкомассы и гематокрита) позволяет получать двойную дозу лейкомассы тромбоцитов блока из пула семь слоев Баффи. При этом оптимизация проводится, количество охристые пальто, необходимой для получения фиксированного количества тромбоцитов дозы могут быть снижены, тем самым улучшая общее использование охристые пальто и возможности производства дополнительного концентратов тромбоцитов (ПК). Персонал времени, а также расходных материалов и оборудования расходы, такие как объединение множеств, тромбоцитов решение добавка, стерильные пластины связи, наборы фильтров, и центрифугирования процедуры снижается до 50%. В дополнение к оптимизации тромбоцитов и снижение связанных с этим расходов, Тхис объединения метод может генерировать концентрата тромбоцитов (PC), который соответствует входным требованиям для использования с INTERCEPT двойным набором обработки контейнеров хранения, что позволяет нам обеспечить усиленную защиту наших получателей переливания крови, а также.
INTERCEPT системы крови для инактивации болезнетворных микроорганизмов используются amotosalen и ультрафиолетового (УФ) свет ковалентной сшивки ДНК и РНК, препятствуя репликации нуклеиновых кислот и оказание патогенов не может вызвать заболевание. 3 Это эффективно нейтрализующих широкого спектра патогенов, включая вирусы, бактерии , паразитов и загрязняющих доноров белых кровяных клеток. 4-6 INTERCEPT представляет собой альтернативу существующей парадигмы тестирования на появляющиеся патогенные организмы, которые исторически связана с существенной задержкой в то время как новый тест разработан и в конечном итоге требует значительных финансовых инвестиций для реализации, когда тест становится доступной. 7,8 Она также может предоставить альтернативу избыточных безопасности измереннойразрешения, такие как бактериальные обнаружения 9 и гамма-облучения. 10-12 Кроме того, INTERCEPT позволяет рассматривать двойные единицы тромбоцитов дозу, которая приносит пользу нашим эффективности производства и помогает нам придерживаться наших бюджетов.
Перехват и двойная доза лейкомассы метод может быть адаптирован для различных рабочих центров крови. В качестве примера, целых коллекций крови может быть увеличена до 500 мл; коллекции можно также хранить в течение ночи при 22 ° C до разделения. Кроме того, альтернативные лейкомассы объединения метод можно (например, осьминогов метод вместо метода поезда) и / или автоматизированное устройство (например, TACSI) могут быть использованы для второго центрифугирования и разделения суспензии тромбоцитов от остальной эритроцитов .
Если повышенным содержанием тромбоцитов необходимо несколько методов доступны, включая предварительный отбор доноров на основе тромбоцитов, ночной инкубации цельной крови, adjustment центрифугирования настройки, или использование бассейна от 8 пальто Баффи вместо 7.
В связи с ограничением объединение устанавливает в настоящее время и мощность центрифуг ведрах, общий объем бассейна Баффи пальто должно быть примерно 600 мл. В процессе центрифугирования и параметры, описанные в этом протоколе были оптимизированы для получения продукта, который отвечает INTERCEPT параметры для бассейна из 7 слоев Баффи. Центрифугирования параметры должны быть изменены, если число охристые пальто в бассейне будет изменен.
В некоторых странах, минимальная доза тромбоцитов выше, а QC требования более строгие, чем в Швеции. Таким образом, наши результаты не могут быть универсальными. В этих странах, двойной PC дозу до INTERCEPT лечения необходимо содержать большее количество тромбоцитов в целях удовлетворения местных потребностей после INTERCEPT лечения и раскол. Поскольку максимальная тромбоцитов содержания и лечения объем лГ INTERCEPT являются 7x10 11 тромбоциты и 420 мл соответственно, доля единиц, которые превышают INTERCEPT требований к обработке или имеют недостаточные тромбоцитов контент, который будет разделен на два терапевтических дозах, будет варьироваться в зависимости от таких факторов, как местных требований тромбоцитов дозу, QC критериев, лейкомассы результаты оптимизации и стабильность производства.
Если двойная доза превышает PC INTERCEPT требований к обработке, она может быть скорректирована вручную в соответствии с требованиями и затем обрабатывали. В тех немногих случаях, когда 7-лейкомассы бассейн дает недостаточную тромбоцитов для двойной дозы продукта после перехвата, мы решили не выполнять INTERCEPT лечения. Кроме того, другие центры крови может выбрать для лечения ПК с помощью одной дозы INTERCEPT обработки множества (т.е. Большой набор тома) и хранить ПК, как один большой терапевтической дозы, тем самым выполнение инактивации болезнетворных микроорганизмов на всех устройствах. В целях обеспечения мы встречаемся с нашимиQC требования и инактивации патогенов, как многие из наших тромбоцитов единиц, возможно, мы выбираем охристые пальто на основе доноров тромбоцитов, которые при объединяли, приведет к минимальным содержанием тромбоцитов 5.6x10 11 тромбоцитов в бассейне. Это гарантирует достаточное содержание тромбоцитов для получения двух терапевтических дозах после INTERCEPT лечения.
Наша проверка показывает, что 7 цельной крови производных единиц лейкомассы может быть успешно объединяют и обрабатывают INTERCEPT процесс тромбоцитов, что приводит в 2 возбудитель инактивированной тромбоцитов продуктов, которые отвечают критериям приемлемости для производства (шведский требованиям и европейским директивам) и для поддержки пациентов требуется переливание тромбоцитов в соответствии с клинической практики и стандартные методы вливания тромбоцитов в Швеции.
Раскрытие информации
Производство и свободный доступ к этой статье проводится при финансовой поддержке Cerus.
Благодарности
Финансирование для публикации осуществляется Cerus Corp, производитель INTERCEPT системы крови.
Материалы
| Name | Company | Catalog Number | Comments |
| Whole blood donation, primary separation, and platelet production | |||
| Blood collection pack | Fenwal | R6485 | Top/Bottom set |
| Automated component extractor | Fenwal | Optipress-II | |
| Blood mixer and balance system | Baxter | Easymix V3 | |
| Platelet leukocyte filtration set | Fenwal | K4R7042 | |
| Centrifuge | Hettich | Roto Silenta 63 RS | Version 5.5 |
| Platelet additive solution - SSP+ | MacoPharma | SSP2030U | 300 ml |
| Sterile tubing welder | Terumo | T-SCD | |
| INTERCEPT treatment & storage | |||
| INTERCEPT processing set |  Cerus Cerus | INT2503 | Dual Storage (DS) set |
| INTERCEPT Illuminator |  Cerus Cerus | INT100 | |
| PC sample pack | Fenwal | FTX 1122 | |
| Incubator | Helmer | PC2200/PC3200 | |
| Agitator | Helmer | PF48H/PF96H | |
| Evaluation of in vitro Platelet Function | |||
| Blood gas analyzer | Radiometer | ABL 735 | Used for pH, blood gases, and lactate measurement |
| Chemistry system | Ortho Clinical Diagnostic | Vitros 5.1 | Used for glucose measurement |
| Hematology analyzer | Boule Medical AB | Medonic CA620-Cellguard | Used for platelet count measurement |
| Flow cytometer | BD | FACSCanto | Used for white blood cell measurement |
Ссылки
- . . Guide to the preparation, use and quality assurance of blood components. , (2010).
- Van Rhenen, D. J., Vermeij, J., Mayaudon, V., et al. Functional characteristics of S-59 photochemically treated platelet concentrates derived from buffy coats. Vox Sang. 79, 206-214 (2000).
- Wollowitz, S. Targeting DNA and RNA in pathogens: mode of action of amotosalen HCl. Transfus. Med. Rev. 31, 11-16 (2004).
- Irsch, J., Lin, L. Pathogen Inactivation of Platelet and Plasma Blood Components for Transfusion Using the INTERCEPT Blood SystemTM. Transfus. Med. Hemother. 38, (2011).
- Lin, L., Dikeman, R., Molini, B., et al. Photochemical treatment of platelet concentrates with amotosalen and long-wavelength ultraviolet light inactivates a broad spectrum of pathogenic bacteria. Transfusion. 44, 1496-1504 (2004).
- Lin, L., Hanson, C., Alter, H., et al. Inactivation of viruses in platelet concentrates by photochemical treatment with amotosalen and long-wavelength ultraviolet light. Transfusion. 45, 580-590 (2005).
- Allain, J. P., Cianco, C., Blajchman, A., et al. Protecting the blood supply from emerging pathogens: the role of pathogen inactivation. Transfus. Med. Rev. 19, 110-126 (2005).
- Stramer, S., Hollinger, F., Katz, L., et al. Emerging infectious disease agents and their potential threat to transfusion safety. Transfusion. 49, 1S-29S (2009).
- Nussbaumer, W., Allesdorfer, D., Grabmer, C., et al. Prevention of transfusion of platelet components contaminated with low levels of bacteria: a comparison of bacteria culture and pathogen inactivation methods. Transfusion. 47, 1125-1133 (2007).
- Schlenke, P. Protection against Transfusion-Associated Graft-versus-Host Disease in Blood transfusion: Is Gamma-Irradiation the Only Answer? Transfus. Med. Hemother. 31, 24-31 (2004).
- Lin, L., Corash, L., Osselear, J. C. Protection Against TA-GVHD Due to Platelet Transfusion By Using Pathogen Inactivation with the INTERCEPT Blood SystemTM - Gamma Irradiation is Not the Only Answer. Haematologica. 95 (Extra 1), 230-237 (2010).
- Corash, L., Lin, L. Novel processes for inactivation of leukocytes to prevent transfusion-associated graft-verus-host disease. Bone Marrow Transplant. 33, 1-7 (2004).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены