Method Article
Одновременное Цельноклеточная Записи из фоторецепторов и второго порядков Нейроны сетчатки амфибий Подготовка Slice
В этой статье
Резюме
Мы описываем получения тонких срезов сетчатки водных тигра саламандры ( Ambystoma tigrinum) И объяснить, как мы используем эти кусочки для изучения синаптической переработки в сетчатке путем получения двойного цельноклеточная записи напряжения зажим из фоторецепторов и второго порядков горизонтальных и биполярных клеток.
Аннотация
Одной из центральных задач в неврологии сетчатки, чтобы понять схему нейронов сетчатки и как эти соединения ответственны за формирование сигналы передаются в мозг. Фотоны обнаружены в сетчатке глаза палочек и колбочек, фоторецепторов, которые преобразуют эту энергию в электрический сигнал, передаче его в другие нейроны сетчатки, где она обрабатывается и передается в центральный цели в мозг через зрительный нерв. Важно раннее понимание сетчатки схемы и визуальной обработки пришли из гистологического исследования Cajal 1,2, а затем и от электрофизиологических записей пики активности ганглиозных клеток сетчатки - выход клеток сетчатки 3,4.
Детальное понимание визуальной обработки в сетчатке требуется понимание сигнализации на каждом этапе пути от фоторецепторов сетчатки, ганглиозных клеток. Однако во многих типов клеток сетчатки являются бораIED глубоко в ткани и, следовательно, относительно недоступных для электрофизиологические записи. Это ограничение может быть преодолено путем взаимодействия с вертикальной ломтиками, при котором клетки, находящихся внутри каждого из слоев сетчатки четко видны и доступны для электрофизиологические записи.
Здесь мы описываем способ изготовления вертикальных участков сетчатки от личиночной тигра саламандры (Ambystoma tigrinum). В то время как этот препарат был первоначально разработан для записи с острыми микроэлектродах 5,6, мы опишем метод для двойного цельноклеточная записи напряжения зажим из фоторецепторов и второго порядков горизонтальных и биполярных клеток, в которых мы оперируем мембранный потенциал фоторецептора одновременно записывая пост- синаптических ответов в горизонтальном или биполярные клетки. Фоторецепторы тигра саламандры значительно больше, чем у млекопитающих, что делает это идеальный препарат, в котором для проведения тего технически сложный экспериментальный подход. Эти эксперименты описаны с глазу на зондировании сигнализации Свойства синаптическую ленты - специализированная структура синаптических найти в только горстка нейронов, в том числе палочек и колбочек, фоторецепторы, который хорошо подходит для поддержания высоких темпов высвобождения нейромедиатора тоником 7 , 8 - и как это способствует уникальный сигнализации свойства этого первого сетчатки синапсе.
протокол
1. Сетчатки Подготовка Ломтики
- Соберите камера (дизайн показано на рисунке 1). Место две капли вакуумной смазки, расположенных ~ 8-10 мм друг от друга, по всей записи камеры, чтобы сформировать канал для superfusate и в котором для встраивания сетчатки ломтиками. Добавьте второй валик жира на несколько миллиметров дальше, за пределы каждой из этих двух шариков жира в качестве дамбы и предельные эффекты. Место небольшой треугольный кусок KimWipe в конце камеры для обеспечения жидкость контактирует с электродом сравнения.
- Нажмите кусок нитроцеллюлозные мембраны (~ 5 х 10 мм; 0,8 поры мкм) плоско против предметное стекло микроскопа на две маленьких шариков вакуумной смазки. Не следует размещать смазки непосредственно под центром нитроцеллюлозной мембране, так как это может предотвратить прилипание сетчатки.
- Чтобы подготовить срез ткани, перерыв двойное лезвие края на 4 части и приложите к одной нарезки руку. Отрежьте тонкий ломтик nitrocellulновления мембраны для того, чтобы передний край лезвия бритвы лежит плоско к записи камеры и, следовательно, сокращает чисто через нитроцеллюлозные мембраны.
- Держите небольшой стакан амфибий солевой раствор (табл. 1) на льду при вскрытии станции.
- Усыпить саламандра путем обезглавливания. Hemisect глава сагиттально и пробковых через спинной мозг. Место половину головы на кусок хлопчатобумажной смоченной солевым амфибий на вершине линолеуме. Другая половина головы может быть обернуто с влажным бумажным полотенцем и хранить при температуре 4 ° C для дальнейшего использования в день.
- Выяснять глаз. Использование маленькие ножницы Vannas, порезать кожу подключения глаза на окружающий орбиту. После освобождения передней части глаза от окружающих тканей орбитальной, тянут глаза скользят вперед и ножниц под глазом, чтобы прорваться через мышцы глаз и зрительного нерва, освобождая глаз с орбиты.
- Поместите энуклеированными глаза на ложе из хлопка налинолеуме. Откажитесь от половины головы. Обрезка избыток орбитальный жир с задней части глаза.
- Сделайте небольшой надрез в центре роговицы с острым хирургическим скальпелем. Удалить роговицы, сдвинув тонких ножниц Vannas в разрез и расширения разреза в радиальном направлении к Ora Serrata. Cut окружности вокруг ора Серрата вращением блока линолеума или хлопок между разрезами.
- После сокращения на всем пути вокруг глаз, удалить роговицей и хрусталиком, выдвинув их из стороны окуляра. Переместить в результате наглазник на твердую поверхность блока линолеума смоченной амфибия физиологическим раствором. Разрезать его на трети с острым лезвием бритвы, с помощью тонкой распиловки движения, чтобы убедиться, что вы сократили все путем склеры.
- Положите одну или две части наглазник на нитроцеллюлозные мембраны с поверхности сетчатки вниз. Погрузите оставшиеся части с дополнительным физиологическим раствором и поместите их в холодильник на ~ 4 ° С.
- Gently нажмите кусок наглазник против нитроцеллюлозные мембраны с тонким пинцетом. Погружение нитроцеллюлозную мембрану и окуляр часть с несколькими каплями холодный солевой амфибий и блоттинга по краям KimWipe помочь сетчатки придерживаться. Еще раз, погрузить окуляр и нитроцеллюлозную мембрану с несколькими каплями холодного амфибия солевым раствором и очистить от склеры / сосудистую оболочку / пигментного эпителия сетчатки, чтобы изолировать сетчатки (которые могут появиться розовый благодаря наличию небеленой родопсина). При необходимости отрежьте зрительного нерва, чтобы освободить сетчатки.
- Если сетчатка не придерживался плотно, стекать с солевым KimWipe тянуть сетчатку более твердо вниз на нитроцеллюлозные мембраны. Замените солевой раствор. Повторите, если это необходимо.
- Заполните камеру с холодным солевым амфибий и передать его на этапе резки ткани. Нарежьте сетчатки и нитроцеллюлозные мембраны на тонкие полоски, работая от одного конца до другого, поворачивая микрометра нониусав 125 мкм шагом. Нажмите на лезвие бритвы мягко, но твердо через сетчатку и нитроцеллюлозные мембраны.
- Передача сетчатки ломтиками, перемещая полоски нитроцеллюлозы мембрану к основным каналом записи камеры. Поднимите полосу мембраны бесплатно, а затем удерживать его на месте во время движения камеры под ней, будучи уверенным, чтобы сохранить ломтики под водой. Вставить краев нитроцеллюлозную мембрану в полосах вакуумной смазки, вращение на 90 градусов, чтобы посмотреть слоев сетчатки.
- Нажмите плоские мембраны нитроцеллюлозы прилегает к поверхности стекла. Даже если нет сетчатки на каждый кусок, место полоски нитроцеллюлозной мембраны через равные промежутки времени (~ 1 мм друг от друга) вдоль всей длины перфузии канал, чтобы помочь разбить поверхностного натяжения и улучшения потока жидкости.
2. Парные Цельноклеточная Recordings
- После того как все кусочки были переданы, перемещать записи камеры до стадии вертикально, фиксированныйстолик микроскопа и прикрепите свинца электрода сравнения. Сосредоточьтесь на ломтики с помощью длинного-рабочее расстояние, погружения в воду, 40-60X цели. Микроскоп должен быть сделан на воздухе таблицы снижают вибрацию и заключен в клетку Фарадея для уменьшения электрических помех.
- Переливать ломтики непрерывно со скоростью 1 мл / мин с амфибия солевой раствор барботировали 100% О 2. Подключите всасывания, убедившись, что приток и отток сбалансированы. Отток можно регулировать путем поворота скошенный конец всасывающей иглы или путем перемещения KimWipe в конце камеру ближе или дальше от оттока иглы. Препарат можно хранить при комнатной температуре или охлаждается с устройством Пельтье или, просто установив пакет со льдом на столик микроскопа.
- Изучить ломтиками при слабом или инфракрасного света и определить пары клеток - фоторецепторов (стержня или конуса) и близлежащих горизонтальных или биполярные клетки - в мишень для цельноклеточная записи. Стержни могут быть яdentified их большие тела клетки и видные стержнеобразную наружные сегменты (рис. 2А). Шишки меньше, чем стержни и имеют маленькие конические наружные сегменты. Биполярные клетки и горизонтальных Somas ячейки во внешнем ряду клеточных тел в внутреннего ядерного слоя (INL; 2В и 2С).
- Перед приготовлением ломтиками, используйте съемник пипетки для производства микропипетки из боросиликатного стекла (1,2 мм наружный диаметр, 0,95 мм внутреннего диаметра со стеклянной нити). Кончик каждой микропипетки должны быть ~ 1-2 мкм в диаметре.
- Использование неметаллических заполнения иглы (например, один изготовлен из 1 мл шприц или Microfil), заполните пипетки с внутриклеточным раствором (таблица 1) и приложить к держатель электрода.
- Поднимите объектива микроскопа незначительно. Расположите фоторецепторов пипеткой под объективным и затем опустите его так, чтобы его конец находится чуть выше ломтиками. Повторите с тОн второй пипетки.
- Отрегулируйте любые смещения в базовых текущий уровень на усилителе. Проверьте сопротивление пипетки с 5-10 мВ деполяризующего импульса. Обычно мы используем пипетки в диапазоне от 10-15 МОм, результат длинный конус вала и низкую осмолярность амфибия решений пипетки. При более высокой осмолярности млекопитающих решений, эти же пипетки проявляют устойчивость значения ~ 8-12 МОм. В то время как мы использовали большие чаевые диаметров с сопротивлением значений 3-4 МОм в растворах амфибия, преимущества, которые дает меньший доступ сопротивления компенсируется большими трудностями в уплотнитель на клеточные мембраны и более быстрому Ранг кальция токов и других вторичных мессенджеров аспектов мер реагирования.
- При применении небольшое положительное давление, положение постсинаптических пипетки так, что она контактирует с горизонтальной или биполярные клетки тела. Затем поместите пресинаптические пипетку так, чтобы он касался тела клетки фоторецепторов стержня или конуса. Записи APPEAR быть более стабильным, когда наконечники связаться внутренний сегмент, а не сомы, особенно в конусах.
- Во время контроля сопротивления, отпустите положительное давление на постсинаптической пипетки. Иногда, освобождение положительное давление достаточно, чтобы сформировать гигаом уплотнение. Если нет, обратитесь нежное всасывание с 1 мл шприца или через рот. После лобового сопротивления выросла до> 100 МОм, применять проведения потенциал -60 мВ. После получения уплотнение гигаом, обнулять любые переходные пипетку емкостью и повторить процедуру для уплотнения фоторецептора пипетки, применяя проведение потенциала -70 мВ.
- Разрыв патч с помощью вашего рта или шприц применять всасывания в каждую ячейку по очереди. Стержни, конусы и биполярные клетки, как правило, разрыв с нежным всасывания. Получение цельноклеточной конфигурацию с горизонтальным клетки могут требовать большего всасывания (т.е. с 3 мл шприц) в сочетании с сильным быстрый импульсов напряжение, подаваемое с "Зап" еeature из усилителя зажим патч. Разрыв мембраны и создании целой клетки конфигурации будут очевидны появление цельноклеточной переходные емкости.
- Подтверждение личности постсинаптической клетки физиологически, применяя вспышку света и доставки ряд ступеней напряжения от -120 до +40 мВ 20 мВ шагом (рис. 3 и 4).
- Чтобы оценить, если пара клетки синаптически связанных, доставки краткого (25-100 мс), 60 мВ шаг деполяризации фоторецептора (до -10 мВ, вблизи пика L-типа напряжения закрытого кальциевых тока) и смотреть для пост-синаптические токи в порядке второго нейрона (рис. 5). Сильный деполяризующие шаг должен вызвать быстрый, преходящий внутрь постсинаптического тока в пост-синаптических горизонтальной или OFF биполярных клеток, вызванной взрывом пузырьков освобождение от конуса (рис. 5).
Результаты
Представитель следы света ответов нейронов в вертикальные срезы сетчатки саламандры показаны на рисунке 3. Конус, горизонтальные ячейки, а OFF биполярной клетки все отображения внешнего тока в ответ на свет начала. Известный входящего тока после вспышки света в горизонтальном и биполярные записи ячейки, вызванного увеличением высвобождение глутамата из фоторецепторов, как они деполяризации в свете смещения. ON биполярного клетка отвечает с входящего тока на свет в результате наступления знак инвертирующий метаботропный рецептора глутамата сигнального каскада и активации TRPM1 каналов 9. Горизонтальные элементы и биполярные клетки можно отличить друг от друга их отношения IV (рис. 4). Горизонтальные клетки обычно имеют линейную или внутренне исправления IV и низким входным сопротивлением (<500 МОм; рис. 4а), а биполярные клетки имеют высокое входное сопротивление(0.5-2 ГОм) и внешне-выпрямительных I - V (рис. 4В) Рисунок 5 показывает репрезентативные результаты по звукам, издаваемым конуса горизонтальной ячейки пары (рис. 5а) и конус-OFF биполярные клетки пары (рис. 5В).. В каждой, деполяризующие конуса до -10 мВ от проведения потенциал -70 мВ вызвало напряжение закрытого кальциевых тока в конус и быстрая внутрь EPSC в горизонтальном или биполярные клетки. Это сильный стимул достаточно, чтобы очистить легко разъемным-пул ~ 20 пузырьков из каждого синаптического ленты, в результате чего EPSC из ~ 47 мкА / лента 10. Горизонтальная EPSC клетки на рисунке 5а 232 пА, предполагая, что он получил 5 лентой контактов из пресинаптических конуса. Аналогичная оценка от 178 пА EPSC в выключенном биполярной клетки (рис. 5В) позволяет предположить, что он получил 4 ленты контактов из пресинаптических конуса.
| амфибия солевые | Пресинаптическая пипетки | Постсинаптические пипетки | |
| NaCl | 116 мМ | 3,5 мМ | 3,5 мМ |
| KCl | 2,5 мМ | ||
| CaCl 2 | 1,8 мМ | 1 мМ | 1 мМ |
| MgCl 2 | 0,5 мМ | 1 мМ | 1 мМ |
| HEPES | 10 мМ | 10 мМ | 10 мМ |
| Глюкоза | 5 мМ | ||
| Cs-глутамата * | 40 мМ | ||
| Cs-глюконат ** | 50 мМ | 90 мМ | |
| Тетраэтиламмонийхлорида | 10 мМ | 10 мМ | |
| АТФ-Mg | 9 мм | 9 мм | |
| GTP | 0,5 мМ | 0,5 мМ | |
| ЭГТА | 5 мМ | 5 мМ | |
| рН *** | 7,8 | 7,2 | 7,2 |
| Осмолярности **** | 245 мосм | 240 мосм | 240 мосм |
* Cs-глутамат получены путем нейтрализации 40 мМ L-глутаминовой кислоты с 40 мМ гидроксида цези в пипетку раствора. ** 1 М запаса Cs-глюконат получены путем нейтрализации раствора CsOH с 45-50% D-глюконовой кислоты. *** РН должен быть отрегулирован с NaOH для внеклеточного раствора и CsOH для решения пипетки. **** Хранение осмолярность растворов пипетки чуть ниже, что внеклеточной решение предотвращает клетки отек и улучшает долговечность записи.
Таблица1. Компоненты и параметры для стандартной внутриклеточных и внеклеточных решения, используемые в настоящем Протоколе.
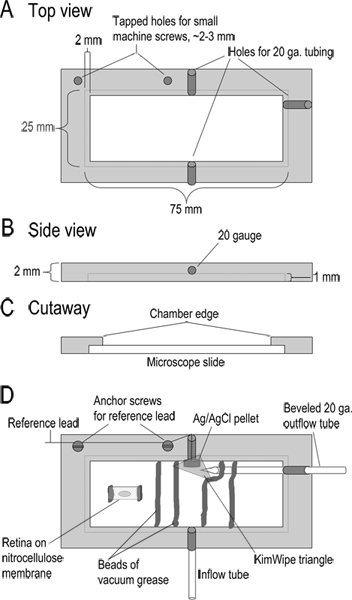
Рисунок 1. Запись камеры дизайна. (AC) сверху, сбоку и в разрезе вид на записи камеры показывающие размеры. Камера изготовлен из 2 мм толщиной кусок акрила. (D) Собранный камеры. Superfusate поступает в камеру через 10 см. Длина трубы тефлоновой (приток трубки; 24LW типа). Superfusate удаляется путем применения мягкого всасывания скошенную 20 калибра металлической трубки на другую сторону камеры. Рядом с этим выходной трубки Ag / AgCl электродом сравнения гранул. Свинца из этой ссылки электрод соединен с опорным входом Headstage. Небольшой треугольник KimWipeнаходится над электродом сравнения, чтобы держать его в контакте с раствором и регулирование потока раствора в выпускной трубе. Основание камера образована путем размещения предметное стекло микроскопа в углубленные края камеры. Слайд удерживается на месте с шарик вакуумной смазки. Полоски нитроцеллюлозную мембрану с сетчатки ломтиками, внедренных в шарики вакуумной смазки, которые образуют канал для решения потока. До проведения ломтиками, 5 х 10 мм кусок нитроцеллюлозные мембраны, прикрепленной к камере с двух маленьких шариков вакуумной смазки. Кусок наглазник находится стекловидное тело вниз на этой мембраны нитроцеллюлозы и поднял далеко, как только сетчатки придерживается. Нажмите здесь, чтобы увеличить рисунок .
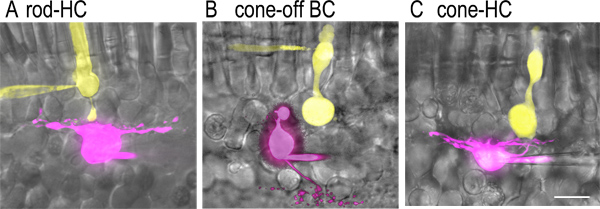
Рисунок 2. Краска кювету с парами в веrtical подготовки срез.) Изображения стержня и синаптически связи горизонтальные клетки, которые были заполнены с контрастными флуоресцентными красителями вводят через патч пипетки при одновременном цельноклеточная записи. Люцифер желтый (2 мг / мл) была включена в решение стержня пипетки (желтый) и sulfarhodamine B (1 мг / мл) был включен в горизонтальное решение пипетки клетки (фиолетовый). Флуоресцентные изображения получены с помощью вращающегося диска конфокальной микроскопии (Perkin Elmer Ultraview LCI), снабженный охлаждением ПЗС-камера (Orca ER) и крепится на неподвижную столик микроскопа (Nikon E600 FN с 60X, 1.0 NA цель погружения в воду). Эти изображения были наложены на яркие образы области соответствующего сетчатки срезов при использовании Adobe Photoshop. B) изображения конуса и синаптически-OFF сочетании биполярной клетки. Биполярной клетки аксона разветвляется во внешнем (S1) sublamina внутренний сетчатый слой недалеко от границы с внутреннего ядерного слоя. С) изображения конуса и синаптически связи горизонтальные клетки. Следует отметить, что конус терминалов значительно больше, чем аксон терминал стержня. Хотя горизонтальные клетки могут быть идентифицированы по продолговатую форму своего тела клетки, клеточные тела включения и выключения типа биполярных клеток в INL не может быть легко отличить перед записью. Можно, однако, цель смещается конуса отъехал биполярных клеток, которые имеют клеточных тел в ОНЛ и можно отличить от конусов отсутствие внутреннего и внешнего сегментов. Масштабная линейка составляет 20 мкм.
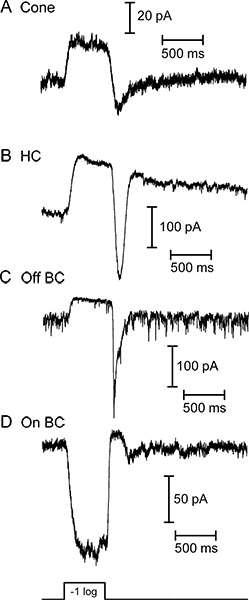
Рисунок 3. Свет, вызвали токов, зарегистрированных под напряжением клеммы из четырех различных нейронов сетчатки в ответ на 500 мс яркие вспышки белого света. Конуса (A), горизонтальные клетки (B), и выключается биполярной ячейки (C) Все ответили на свет с внешним током. (D) на биполярные клетки ответили на тот же раздражитель свет с входящего тока. Исходный шум выставлены от биполярной ячейки (C) отражает постоянное высвобождение синаптических пузырьков в темноте, которая уменьшает, когда фоторецепторы гиперполяризовать в свет. Ответы, полученные от этих четырех клеток было получено в отдельные записи на основе ломтиками подготовленный под белым светом. Интенсивность белого светового раздражителя, используемые в этих примерах получают ответы в горизонтальном и биполярные клетки эквивалентно 580 нм поток фотонов от 1 × 10 5 фотонов / сек / мкм 2.
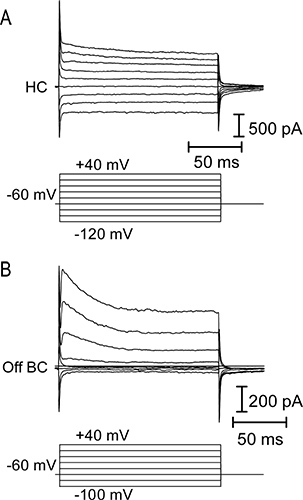
Рисунок 4. Вольт-амперные (IV) отношения чГоризонтальная полоса и от биполярных клеток. (A) Верхняя панель, мембранные токи вызванные серии 150 мс ступеней напряжения от -120 до +40 мВ применяется шагом 20 мВ (нижняя панель) в горизонтальное клетки. Горизонтальные клетки обычно имеют низкое сопротивление на входе и линейные или внутренне исправления IV отношений. (B) IV связь с биполярной клетки в ответ на серию ступеней напряжения. Биполярные клетки имеют более высокое сопротивление на входе и внешне исправления IV, в связи с активацией напряжения закрытого токов калия.
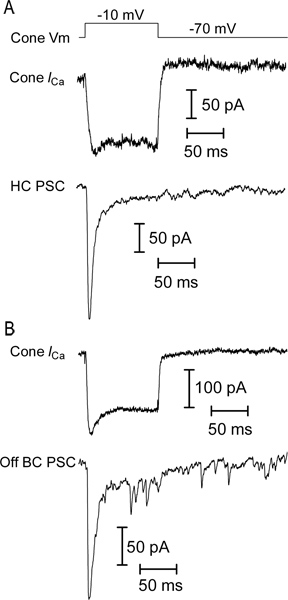
Рисунок 5. Примеры парных данных записи. () Запись конуса напряжения закрытого кальциевых ток (Конус я Ca ) в ответ на шаг 100 мс до -10 мВ от проведения потенциал -70 мВ (конуса V м). Утечки и емкости переходных вычитали использованием P / 8 утечка вычитание протокола. Быстро возбуждающих постсинаптических тока (EPSC; HC PSC) был записан одновременно с горизонтальной ячейки, показывающие, что эти две клетки синаптически сочетании (B) EPSC было записано в ячейке с биполярными в ответ на тот же раздражитель в другом. конуса.
Обсуждение
Сетчатки подготовки срез оказался очень полезным для анализа схем и механизмов, работающих в сетчатке обрабатывать визуальную информацию. Возможность получения записи всего клетки одновременно с пре-и пост-синаптических нейронов было особенно полезным в этом начинании. Парные записи всего клетки гораздо легче достичь, чем с кусочками с телевизором с плоским креплением препаратов сетчатки, потому что различные слои сетчатки подвергаются. Кроме того, из-за их большого нейронов сетчатки, саламандры имеют долгую историю, как сетчатки подготовки и, следовательно, обеспечить особенно хорошо характеризуется моделью системы.
С практикой, здоровым ломтиками сетчатки саламандры могут быть приготовлены на регулярной основе. Несколько ключевых шагов может сделать разницу между успехом и неудачей. 1) Убедитесь, что лезвие установлено на ткани резки так, что она лежит плоско к поверхности стекла и кусочки чисто хотя оба ткани и underlyiнг мембраны нитроцеллюлозы. Если вы сделали чистый срез через нитроцеллюлозные мембраны, вы должны услышать слабый щелчок, лезвие бритвы поражает поверхность стекло. 2) Убедитесь, что сетчатка придерживался нитроцеллюлозные мембраны. В противном случае, сетчатка может плавать от мембраны на любом шаге процедуры. 3) Не подвергайте нарезать кусочками в воздух, как это может повредить многие из поверхностных клеток. 4) Убедитесь, что ломтиками и нитроцеллюлозные мембранные лежать на предметное стекло так, чтобы слои сетчатки являются очевидными под рассекает микроскопом. 5) Баланс темпов superfusate притока и оттока, чтобы избежать переполнения записи камеры. Это предотвращает внезапные изменения в решении уровней, которые могут вызвать резких движений ткани. 6) Выбор здорового пара клеток близко друг к другу. Клетки с гладкой цитоплазме здоровее, чем клетки с зернистой цитоплазмой. Клетки глубже в часть, скорее всего, чтобы сохранить нетронутыми синаптических конконтактов. 7) Убедитесь, что наконечник пипетки не сломаны или задела другую ткань или мусор на пути вниз к клеткам. 8) Проверьте пипетки сопротивление, чтобы он не забит мусором или пузырь, оба из которых могут сделать его трудно получить качество цельноклеточной записи.
Вместо того, чтобы крепления сетчатки к бумаге нитроцеллюлозный фильтр, некоторые исследователи вставлять сетчатки в блоке агар и использовать Vibratome сократить сетчатки ломтиками. Хотя мы еще не пробовали этот подход, Ким и др.. +11 Обсудить преимущества обоих подходов. В их опыт, на основе агара подход является более последовательным выходом плоских ломтиков с хорошо очерченной слоев сетчатки но фильтр бумажных подход дает здоровый фоторецепторов.
Палочки и колбочки отвечают за свет в трансдуцирующих изменения мембранного потенциала. С парных записей, мембранный потенциал стержней или конусы могут быть MANIPULated непосредственно и поэтому способность генерировать свет ответов, в то время как полезный для идентификации типов клеток, могут быть существенными. Поэтому мы часто готовят ломтики в белом свете. Однако, даже когда подготовлено при ярком освещении, саламандра нейронов сетчатки может генерировать большой свет ответов о чем свидетельствуют ответы на рис. 3. Отчасти это связано с относительно большой резервуар хромофора в большой внешний том сегменте, но также может отражать способность клеток к регенерации Мюллер 11-цис-ретиналя для конусов 12. Чтобы получить полностью адаптированных к темноте свет реакций, можно приготовить кусочки при инфракрасном освещении. Для вскрытия под инфракрасным светом, мы придаем GenIII усилители яркости изображения (Nitemate NAV3, Литтон Industries, Темпе, Аризона), чтобы из окуляров рассекает микроскоп и осветить ткани с инфракрасным светодиодным фонариком. Для нарезки и другие процедуры, которые не проводились под рассекает микроскопом, мы используем головке IMAGE усилителя. Для размещения патч пипетки, мы представляем себе срезов при использовании инфракрасных ПЗС-камеры (например, Watec 502H, Watec Инк, Миддлтон, Нью-Йорк), установленный в вертикальное, фиксированное микроскоп. С помощью этих мер предосторожности, можно получить стержень ответов экспонирование одного фотона чувствительность 6, 13.
Одним из ограничений, работающие в сетчатке глаза Ломтики в том, что длинные клеточные процессы больших полей нейронов сетчатки может потерять многих из своих дендритов в процессе резки процедуры. Препараты среза сетчатки, следовательно, более полезны для изучения физиологии клетки, в которых синаптические контакты включают процессов, близких к телу клетки. Земноводных и млекопитающих сетчатка разделяют многие из тех же типов клеток и использовать аналогичными физиологическими механизмами 14-16. В то время как саламандры сетчатки является хорошей моделью для многих аспектов млекопитающих сетчатки, одно важное различие видимому, наличие выделенного пути стержень у млекопитающих, инволюциильфы контакты специализированных клеток-палочек на биполярные клетки AII амакринные 14. Дополнительное ограничение сетчатки саламандры является небольшое количество генетических инструментов, разработанных специально для этого вида. Тем не менее, антитела и реагенты, которые ShRNA целевой хорошо консервативных областей у других видов может быть успешно использован в саламандры, как и многие низкомолекулярные ингибиторы и пептидных реагентов. Кроме того, с некоторыми изменениями в технике, сетчатки ломтики могут быть получены из других видов, в которых некоторые из этих инструментов являются более доступными.
За его полезность для парных цельноклеточная записи, саламандра сетчатки подготовки ломтик также поддаются ряд других подходов. Как обсуждалось выше, сетчатки срезы могут быть использованы для изучения светом реакции в сочетании с различными протоколами напряжение зажим 17. Нейроны сетчатки глаза также могут быть загружены с флуоресцентными красителями, чувствительными к Са 2 +, Cl -, или Na+ Вводится через патч пипетки или ванны-приложений 15,18-20. Флуоресцентный пептид, который связывается с синаптической лента 21 может быть введен через патч пипетки и используется для визуализации ленты 10 или, если конъюгированное с флуоресцеином, для остро и выборочно повреждение ленты 22. Мы также использовали сетчатки ломтиками в комбинации с квантовыми точками для контроля движения отдельных каналов кальция при палочек и колбочек синаптических окончаний 23. Таким образом, вертикальная часть сетчатки является универсальным экспериментального препарата для изучения основных синаптических механизмов и уникальные функции обработки, выполняемой в первом синапсе в визуальном сигнального пути.
Раскрытие информации
Нет конфликта интересов объявлены.
Благодарности
Эта работа финансировалась по исследованиям профилактики слепоты и Национального института здоровья грант EY10542.
Материалы
| Name | Company | Catalog Number | Comments |
| Tissue slicer | Stoelting | 51425 | |
| Double edge razor blades | Ted Pella, Inc | 121-6 | |
| Nitrocellulose membranes | Millipore | AAWP02500 | Type AAWP 0.8 mm pore |
| Borosilicate glass pipettes | World Precision Instruments | TW120F-4 | 1.2mm OD 0.95 mm ID |
| Ag/AgCl pellet | Warner | E206 | |
| MicroFil | World Precision Instruments | MF34G-5 | 34 ga. Filling needle, 67 mm long |
Ссылки
- Ramòn y Cajal, S., Thorpe, S. A., Glickstein, M. . The Structure of the Retina. , (1972).
- Piccolino, M. Cajal and the retina: a 100-year retrospective. Trends Neurosci. 11, 521-525 (1998).
- Hartline, H. K. The response of single optic nerve fibers of the vertebrate eye to illumination of the retina. Am. J. Physiol. 121, 400-415 (1938).
- Kuffler, S. W. Discharge patterns and functional organization of mammalian retina. J. Neurophysiol. 16, 37-68 (1953).
- Werblin, F. S. Transmission along and between rods in the riger salamander retina. J. Physiol. 280, 449-470 (1978).
- Wu, S. M. Synaptic connections between neurons in living slices of the larval tiger salamander retina. J. Neurosci. Meth. 20, 139-149 (1987).
- Heidelberger, R., Thoreson, W. B., Witkovsky, P. Synaptic transmission at retinal ribbon synapses. Prog. Retin. Eye Res. 24, 682-720 (2005).
- Schmitz, F. The making of synaptic ribbons: how they are built and what they do. Neuroscientist. 15, 611-624 (2009).
- Morgans, C. W., Brown, R. L., Duvoisin, R. M. TRPM1: the endpoint of the mGluR6 signal transduction cascade in retinal ON-bipolar cells. Bioessays. 32, 609-614 (2010).
- Bartoletti, T. M., Babai, N., Thoreson, W. B. Vesicle pool size at the salamander cone ribbon synapse. J. Neurophysiol. 103, 419-423 (2010).
- Kim, M. H., Vickers, E., von Gersdorff, H. Patch-clamp capacitance measurements and Ca2+ imaging at single nerve terminals in retinal slices. J. Vis. Exp. (59), e3345 (2012).
- Wang, J. S., Estevez, M. E., Cornwall, M. C., Kefalov, V. J. Intra-retinal visual cycle required for rapid and complete cone dark adaptation. Nat. Neurosci. 12, 295-302 (2009).
- Thoreson, W. B., Tranchina, D., Witkovsky, P. Kinetics of synaptic transfer from rods and cones to horizontal cells in the salamander retina. Neuroscience. 122, 785-798 (2003).
- Wu, S. M. Synaptic organization of the vertebrate retina: general principles and species-specific variations: the Friedenwald lecture. Invest. Ophthalmol. Vis. Sci. 51, 1263-1274 (2010).
- Babai, N., Thoreson, W. B. Horizontal cell feedback regulates calcium currents and intracellular calcium levels in rod photoreceptors of salamander and mouse retina. J. Physiol. 587, 2353-2364 (2009).
- Babai, N., Morgans, C. W., Thoreson, W. B. Calcium-induced calcium release contributes to synaptic release from mouse rod photoreceptors. Neuroscience. 165, 1447-1456 (2010).
- Thoreson, W. B., Burkhardt, D. A. Contrast encoding in retinal bipolar cells: current vs. voltage. Vis. Neurosci. 20, 19-28 (2003).
- Thoreson, W. B., Bryson, E. J., Rabl, K. Reciprocal interactions between calcium and chloride in rod photoreceptors. J. Neurophysiol. 90, 1747-1753 (2003).
- Cadetti, L., Bryson, E. J., Ciccone, C. A., Rabl, K., Thoreson, W. B. Calcium-induced calcium release in rod photoreceptor terminals boosts synaptic transmission during maintained depolarization. Eur. J. Neurosci. 23, 2983-2990 (2006).
- Luo, J., Boosalis, B. J., Thoreson, W. B., Margalit, E. A comparison of optical and electrophysiological methods for recording retinal ganglion cells during electrical stimulation. Curr. Eye Res. 37, 218-227 (2012).
- Zenisek, D., Horst, N. K., Merrifield, C., Sterling, P., Matthews, G. Visualizing synaptic ribbons in the living cell. J. Neurosci. 24, 9752-9759 (2004).
- Snellman, J., Mehta, B., Babai, N., Bartoletti, T. M., Akmentin, W., Francis, A., Matthews, G., Thoreson, W. B., Zenisek, D. Acute destruction of the synaptic ribbon reveals a role for the ribbon in vesicle priming. Nat. Neurosci. 14, 1135-1141 (2011).
- Mercer, A. J., Chen, M., Thoreson, W. B. Lateral mobility of presynaptic L-type calcium channels at photoreceptor ribbon synapses. J. Neurosci. 31, 4397-4406 (2011).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены