Method Article
Введение в твердом носителе мембранный электрофизиологии
В этой статье
Резюме
Здесь мы представляем электрофизиологических метод, основанный на твердом носителе мембран с акцентом на ее приложений для характеристики электрогенных транспортеры мембраны.
Аннотация
Электрофизиологические методы приведены основана на твердом носителе мембраны (SSM), состоящий из octadecanethiol хемосорбированный слой на золотом покрытием сенсорного чипа и фосфатидилхолин монослой на вершине. Этот блок установлен в системе кювету с электродом сравнения, хлорированный серебряная проволока.
После адсорбции в мембранных фрагментов или протеолипосом содержащий мембранный белок, быстрый обмен решение используется, чтобы вызвать транспортный активность мембранного белка. В одном решении протокол обмена два решения, одно не-активирующих и один активизирующий раствор, необходимы. Поток контролируется сжатого воздуха и клапан и трубопровод системы в клетке Фарадея.
Кинетика электрогенных транспортной деятельности получается с помощью емкостной связи между SSM и протеолипосомами или мембранных фрагментов. Способ, таким образом, дает лишь transienT токов. Пиковый ток представляет стационарных транспортной деятельности. Зависит от времени токи транспортера может быть восстановлена схема анализа.
Этот способ особенно подходит для прокариотической или эукариотической транспортеры транспортеры из внутриклеточных мембран, которые не могут быть исследованы зажим патч или напряжение методы зажима.
Введение
Здесь мы показываем новые электрофизиологические подход, основанный на твердом носителе мембраны (SSM) для характеристики электрогенных мембранных белков.
Твердый носитель состоит из тонкого слоя золота на предметное стекло, датчик чипа. Гидрофильные поверхности золота используется для связывания тиоловой группой alcanethiol реагента. После этого selfassembly из фосфатидилхолина monolyer завершает формирование защитного механизма.
Для измерения электрогенных реакции мембранных белков, протеолипосомами или фрагменты мембран, адсорбируются SSM (рис. 1). Белок, содержащий мембрану и ССМ затем образует емкостной связью мембранной системы. Таким образом, заряд транслокации в белок, содержащий мембраны могут быть обнаружены посредством емкостной связи через SSM. Этот метод дает лишь переходные токи. Пиковый ток представляет стационарных транспортной деятельности. Зависит от времени Cu Transporterrrents может быть восстановлено путем анализа схем.
Сенсорный чип смонтирован в систему кюветы (рис. 2). Кювета имеет цилиндрическую кювету объемом 17 мкл (нетто-объем с уплотнительным кольцом установлен). Контактный пружинного контакта создает контакт с усилителем. Выпускной патрубок ввинчивается в верхнюю часть основной части и несет опорный электрод, хлорированный серебряная проволока.
Кюветы устанавливают в клетку Фарадея. Это связано потока текучей среды, который используется, чтобы вызвать транспортный активность мембранного белка в ответ на быстрый обмен раствор (фиг.3). В одном решении протокол обмена два решения, одно не-активирующих и один активизирующий раствор, обязательны для заполнения. Поток контролируется сжатым воздухом с помощью программного обеспечения управления клапаном на компьютере или Выключатели на интерфейсный блок.
протокол
1. Настройка устройства для SSM основе электрофизиологии
Подробности приводятся в двух наших технических публикаций, которые также содержат схемы и фотографии нашей кювет и создали 1, 2. Различные решения обмена конфигурациями и поток протоколов, также обсуждаются в нашем методе бумага 2.
В дальнейшем мы добавим несколько последних усовершенствований и технических деталей, которые имеют прямое отношение к видео-презентации.
Клапан управления и сбора данных
Интерфейсный блок содержит коммерческую USB цифровой выход / аналоговый входной интерфейс (NI USB 6009 National Instruments) и клапан водителей. Она контролирует поток раствора и отвечает за сбор данных. Клапаны обычно управляется с 12 В. Тем не менее, для быстрого переключения клапанов может управляться с напряжением до 18 В. В видео мы используем 12 В источника питания.
Схема клапана доска водителя может работать четыре клапана. Он был изготовлен мастерской Макса Планка Институт биофизики. Клапаны можно управлять с помощью компьютера или вручную с помощью переключателей на передней панели. Последний является удобным для промывки и очистки-процедурами. Во время измерения, интерфейс окна управляется компьютером с помощью управляющего клапана и сбора данных программное обеспечение (2 R Surfe программного обеспечения, IonGate Biosciences).
2. Препараты
В этом разделе различные протоколы для подготовки SSM основе экспериментов электрофизиологии упоминаются.
2.1 Выполнение липидов решение для формирования SSM
- Смешать 25 мкл Октадециламин (5 мг / мл в хлороформе) и 375 мкл Diphytanoylphosphatidylcholine (20 мг / мл в хлороформе) в стеклянный флакон.
- С помощью роторного испарителя и непрерывным потоком газообразного азота, выпаривают хлороформоколо 30 мин.
- Удалить липидов от стенки стеклянного флакона, встряхивая с 500 мкл н-декана. Конечную концентрацию липидов составляет 15 мг / мл с 1:60 (вес / вес) октадециламина.
- Перенесите раствор в пробирку для хранения стекла. Хранить липид раствор при -20 ° С.
2,2 Хлорирование электрода сравнения
Электроды должны быть хлорированный равномерно из-за истирания.
- Удалить остальной старый слой хлорид серебра тонкой наждачной бумагой перед хлорированием процесса.
- Поместите серебряная проволока вместе с платиновым электродом в 1 М раствора соляной кислоты и хлорируют в течение 15 мин при 0,5 мА. После завершения хлорирования, серебряная проволока меняет свой цвет в однородную темно-серый.
2.3 Подготовка моста в полиакриламидном геле
- Готовят раствор, содержащий 100 мМ KPi при рН = 7, 100 мМ KCl и шесть% Акриламида.
- Добавить 0,3% APS (10% со) и 0,6% TEMED и вскоре перемешать раствор с помощью пипетки.
- Сразу же после смешивания раствора, использовать пипетку для введения 30 мкл смеси в пустой контейнер мост геля. Важно, чтобы избежать воздушных пузырей во время инъекции.
- Во время инкубации в течение 20 мин гель полимеризуется.
- После полимеризации гель мост хранится в растворе (100 мМ KPi рН 7, 100 мМ KCl). Чтобы продлить срок службы гель моста раствор хранят при температуре 4 ° С.
2.4 Подготовка измерительной решения
Из-за сильного взаимодействия растворенных веществ с SSM, электрические артефакты генерируются, когда растворов различного состава обмениваются. Таким образом, подготовка решений является важным шагом. Примите следующие меры предосторожности в процессе подготовки решения для минимизации артефактов решения обмена.
- Сделайте не-активация и активация решений от одной партии, отрегулировать рН и ионной силы.
- Высокий фон соль помогает уменьшить артефакты решение обмена.
- Разделить партию раствора в двух томах.
- Добавить активирующее соединение в активирующего раствора. Используйте компенсационные соединения в не-активирующих решение сохранить осмолярности и ионной силы обоих решений как можно более близкими.
- Если растворы хранили при 4 ° С, чтобы убедиться, что все решения до комнатной температуры перед началом измерений, так как даже небольшая разница в температуре может привести к артефактам.
3. SSM основе электрофизиологии эксперимент
Здесь мы представляем типичный протокол для SSM основе электрофизиологических экспериментов.
3.1 Подготовка к установке SSM
В то время как SSM установки не используется трубы заполнены 30% этанола/ Воды, чтобы избежать роста бактерий.
- Промыть система с чистой водой для удаления этанола от трубки до установки кюветы. Замените этанола емкости с водой контейнеров. Использование высокого давления (от 0,6 до 1,0 бар) очистки системы с 20-30 мл воды.
- Повторите процедуру очистки с использованием 100 мМ KPi буфере при рН 7,6 или не активизирующий раствор.
- Убедитесь в том, чтобы не было воздушных подушек внутри гидравлической системы.
3.2 Монтаж кювет
- Установите уплотнительное кольцо для электрода сравнения
- Возьмите гель мост из раствора для хранения и подключить электрода сравнения.
- Prefill выпускной патрубок с не-активирующий буфер, вставьте уплотнительное кольцо и соединить мостом гель для завершения сборки электрода сравнения. Соблюдайте особую осторожность, чтобы не было воздушных пузырьков не на стыке моста геля и выходной поток решением пути.
- Предварительную сборку основной части Cuveтет добавлением контактный пружинный контакт (подключение к усилителю), впускной трубы (соединение с терминалом клапан), уплотнительное кольцо (уплотнение для SSM) и винты.
- С помощью пинцета возьмите сенсорный чип из хранения раствора (10 мМ octadecanethiol в этаноле).
- С помощью пипетки, смыть оставшийся раствор с ок. 5 мл чистого этанола.
- Сушат электрода в атмосфере азота.
- Поместите сенсорный чип точно на базовой части кюветы так, что впускные отверстия основной части кюветы направлено на круговой рабочей области датчика.
- Добавить 1 мкл липидного решение активной области сенсорного чипа. Убедитесь в том, что золотой слой полностью покрывается за счет липидов.
- Сразу после добавления Раствор липида, закройте кювету добавлением предварительно собранный основной части.
- Перед монтажом кювету в клетку Фарадея, убедитесь, что все поверхности полностью высохли.
- КоннЕСТ усилитель с контактом пружинный контакт и впускной трубы к терминалу клапана. Затем установить кювету с помощью винтов внутри клетки Фарадея.
- Винт выпускной патрубок в верхней части кюветы. Наконец подключить выходной трубкой к разъему сети и напряжение генератора с эталонным электродом.
- Сразу после установки кюветы промывают систему с буфером при 0,6 бар. Это приводит к спонтанному образованию SSM.
3.3 Измерение параметров мембраны
Для проверки качества ССМ, емкости и проводимости, оцениваются, используя функцию генератора.
- Используя функцию генератора, применяют 100 мВ напряжения постоянного тока для измерения проводимости.
- Рассчитать проводимость: затухание тока показан процесс зарядки мембранного конденсатора. После того, как конденсатор полностью заряжен измеренной текущей доходности мембранной проводимости с использованием закона Ома. Для простоты мы используем у.е.rrent 1 сек после подачи напряжения для вычисления проводимости G = I / U.
- Применение треугольного переменного напряжения 50 мВ от пика до пика амплитудой и частотой 0,5 Гц для измерения емкости.
- Рассчитать емкость: Амплитуда полученного квадратного текущий волна представляет токи зарядки конденсатора. Емкость С равна передается заряд Q = IΔt деленное AU = 100 мВ. (Аи в два раза приложенном напряжении 50 мВ, потому что разница ток положительной минус отрицательный наклон треугольного напряжения.)
- Мониторинг электрических параметров мембраны неоднократно каждые 10 минут в течение ок. От 30 до 40 мин, до достижения постоянного значения не будут достигнуты. Мытье между ними с KPi буфера при высоком давлении в диапазоне от приблизительно 0,6 до 1 бар.
- Оценка качества SSM: Оптимальные параметры находятся в диапазоне от 0,1 до 0,2 нс и от 2 до 3,5 нФ. Высокой проводимостью выше 0,8 нс, а низкая емкость 1 нФ ниже указываетSSM, что неправильно отформатирован. Высокую емкость выше 4 NF может означать, что активная зона не полностью покрыт SSM.
- Если параметры не в оптимальном режиме, мембраны должны быть отброшены, а другой ССМ подготовлены с использованием свежеприготовленного электрод чипа.
3.4 Проверка для обмена артефактами решения
После мембраны параметры были проверены, измерительные буферы должны быть проверены на артефакты решение обмена.
- Вставьте соответствующие контейнеры решение гидравлической системы.
- Удалить пузырьки воздуха из гидравлической системы, используя ручные клапаны.
- Использование программного обеспечения сбора данных выбрал поток протокола, который вы хотите использовать в вашем эксперименте.
- Отрегулировать давление до 0,6 бар и начала измерений.
- Кроме механических артефактов переключающего клапана, в идеале токов артефакт не должно быть измерено, или они должны быть намного SMAМюллер, чем ожидаемые сигналы транспортного белка. Если артефакты решение обмена наблюдаются, пытаются оптимизировать буфера композиции и / или процедуры подготовки, прежде чем продолжить эксперимент.
3,5 Добавление образца белка
Обычно протеолипосомы или фрагменты мембран хранили замороженными при -80 ° С. В одном измерении аликвоты приблизительно 30 мкл необходимо.
- Промойте SSM с неправительственными организациями, активизирующий раствор.
- Разморозить образец белка на льду.
- Три 10-секундный цикл обработки ультразвуком чередуются с 10 с интервалом охлаждения на льду. Протеолипосомы обрабатывают ультразвуком использованием ультразвуковой ванны. Для фрагментов мембран ультразвукового наконечника (50 Вт, 30 кГц, 1 мм диаметр волновода, интенсивность 20%, 0,5 цикла) используется. После последней стадии обработки ультразвуком не ставят образца вернуться на лед, но внедрить его непосредственно в кювете.
- Открутите выпускной патрубок вместе с электродом сравнения ассmbly.
- С помощью пипетки, аспирация 30 мкл образца белка и смонтировать пипетки с выходным отверстием.
- Откройте ручной клапан в не-активирующие пути в контейнер для отходов и ввести протеолипосомами в объем кюветы. Будьте осторожны, чтобы не вдохнуть воздух в объеме кюветы с датчиком.
- Перед снятием кончиком пипетки, закройте ручной клапан, чтобы предотвратить дальнейшее потока раствора.
- Разрешить протеолипосом адсорбировать на ССМ для инкубации в течение от 1 до 2 часов. Кроме того, можно инкубировать в течение ночи.
3.6 Общий порядок SSM основе эксперимента
- Разминка измерения буферов во времени, при хранении при 4 ° С. Все измерительные буферы должны быть комнатной температуры перед началом измерения, чтобы избежать артефактов.
- При изменении решения очисти прежде внутренность труб решение контейнеры с не-фаззинг ткани, а затем вставьте новые бутылки.
- Перед тем как начать измерение, с помощью ручных клапанов для удаления пузырьков воздуха, которые могли развиться в результате изменения процедуры.
- Отрегулируйте давление непосредственно перед началом измерений. Мы обычно используют давление от 0,6 бар, который в нашем конкретном клапан и трубка конфигурация дает скорость потока приблизительно 1,0 мл / сек.
- Первые несколько измерений может быть осуществлен прямой один за другим и должна быть отклонена до пикового тока остается постоянной. Если решения отличаются рН инкубации в течение по крайней мере 3 мин необходимо регулировать внутреннюю рН протеолипосом перед началом измерения.
- Сейчас создана готов к измерениям. Чтобы уменьшить шум, по крайней мере, три измерения должны быть сделаны и усреднены.
3,7 контрольных измерений
Ранг сигнала во время серии измерений могут произойти из-за деградации белков или потеря адсорбции. Каждый SSM эксперимента я долженNCLUDE Ранг управления. Это делается путем многократных измерений с одинаковым решениям. Минимальный контроль изложение означает одно измерение в начале и один в конце эксперимента, используя те же решения.
Мы рекомендуем делать Ранг управления в условиях, когда вы ожидаете высокий пик амплитуды в эксперименте. Это облегчает для количественной оценки изложение сигнала.
Сигнал изложение может быть определена количественно путем сравнения амплитуды пиков двух элементов управления изложение. Полученное процентное значение может быть использована для коррекции измеряемых сигналов в предположении линейной зависимости время сокращения.
3.8 контроль Артефакт
Если возможно, попытайтесь для проверки результатов путем ингибирования белка, представляющего интерес после эксперимента. Остальные сигналы, вероятно, артефакты решение обмена. Затем сигналы должны быть исправлены для измеренной артефактов.
3.9 После эксперимента
- Промыть системы с 20-30 мл чистой воды и 20-30 мл 30% этанола / воды. Этанольный раствор предотвращает рост бактерий, когда система не используется.
- После этой процедуры очистки, сброса давления из системы и выключите все инструменты.
- Удалите кювету из клетки Фарадея и отключить его. Все части кюветы может быть очищено с водой и чистого этанола, при необходимости, с использованием ультразвуковой ванны.
- Поместите датчик чип в стеклянной стакан с чистого этанола. Обрабатывают ультразвуком химическом стакане в течение от около 1 до 2 мин с использованием ультразвуковой ванны.
- Сушат сенсорный чип в атмосфере азота.
- Храните сенсорный чип вдали от света в 10 мМ Octadecanthiol решение этаноле. После инкубации в течение 30 мин микросхемы датчика готов к повторному использованию.
Результаты
До сих пор SSM основе электрофизиологических был использован для характеристики более 20 транспортеров, в основном, из прокариотических происхождения, например Melb 3, 4 и NhaA PutP 5 (сведены в 6). Но и эукариотических транспортеры из внутриклеточных мембран, например ClC7 7, а также ионные каналы, например, никотиновые рецепторы ацетилхолина 8 были исследованы.
Здесь мы приводим в качестве примера измерения сахара / H +-котранспортера Лейси из кишечной палочки протеолипосом с использованием по меньшей мере 85% правую сторону ориентированных Лейси в LPR из 5 9, 10. Мы ориентируемся на основные шаги, ведущие к минимальной кинетической модели этого транспортного белка.
1. Электрофизиологические характеристики дикого типа кружевные
Первый шаг заключается в общей характеристике электрогенных реакции путем измерения различных значениях рН ( > Рисунок 4), концентраций субстрата (рис. 5) и субстратов. Для проверки техники, K M и ПК значений, приведенных в литературе были воспроизведены.
РН зависимость кружевные показаны два разных электрогенных реакций. Емкостной ток увеличивается при рН 5 и рН 8,5, но и изменяет свою форму. В щелочных условиях устойчивой транспортной состояние наблюдается, а для кислых значениях рН только быстрые реакции электрогенных остается. Чтобы отличить устойчивые сигналы от быстрых реакций электрогенных мы использовали схему анализа реконструировать Transporter токов (рис. 6).
При рН 7 монофазный двухфазный сигнал становится. Это также означает, что существует два различных электрогенных реакции. Оценка из перечисленных заряд (интеграл сигналов), две реакции около 6% и 94% от общей electrogenicity транспортного цикла.
ove_step "> 2. Назначение электрогенных реакцийЧтобы назначить двух электрогенных реакции на конкретные шаги в реакции цикла кружевной, кружевной E325A вариант измеряли (рис. 7). Этот вариант показывает только лактоза обмена, но недостаточна для всех активных видов транспорта, из-за ингибирование протонного выпуска. Сигнал E325A кружевные представляет быстрые переходные и является постоянной для всех измеренных значений рН. Формы и амплитуды сигнала похож на сигнал дикого типа Лейси в кислых условиях. Кроме того, мы наблюдаем небольшую отрицательную фазу после снижения пикового тока, что характерно для быстрых переходных токов, измеренных в емкостной связью систем. Потому лактозы связывание и высвобождение не электрогенных, быстрые переходные должны коррелировать с электрогенных конформационного перехода после лактозы обязательными.
Известно, что протон шаг релиз скорости Limitiнг для кружевных оборот в лактозе градиента концентрации управляемой транспорта. В этом случае мы ожидаем, что увеличение скорости транспорта с щелочной рН, так как протон релиз благоприятствования. Это тот случай, для устойчивого состояния транспортных коррелирует сигнал дикого типа Лейси. Кроме того, он может быть показано измерения рН градиент, который только внутренний рН влияет на устойчивое транспортное состояние Лейси (не опубликовано). Поэтому большой электрогенных реакции могут быть отнесены к протону шаг выпуска.
3. Измерения для кинетического анализа
После идентификации электрогенных реакций и выключать транспортных тарифов были определены с использованием SSM установка с высоким временным разрешением около 4,5 мс. Это возможно только в условиях, когда доминирует одна реакция сигнала. В этом случае константы скорости могут быть получены из переходных токов при рассмотрении разрешение по времени сигналов с использованием итеративного наименьших квадратов де Алгоритм свертки (рис. 8). Определены константы скорости, а также предложенный минимальный кинетической модели (рис. 9), наконец, были использованы для моделирования кинетики Transporter. Моделируется воспроизводят изгибы SSM данные, которые дополнительно доказывает кинетической модели.

Рисунок 1. Адсорбция геометрии протеолипосом на ССМ. SSM формируется на сенсорный чип, структурированный золото покрытием предметное стекло. Для измерения электрогенных реакции мембранных белков, протеолипосомы или мембранные фрагменты адсорбированы на ССМ. Две мембраны образуют емкостной связью системы. Вот почему только переходных токов обнаружены.
tp_upload/50230/50230fig2highres.jpg "/>
Рисунок 2. SSM кювета несет чип датчика и электрода сравнения. Сенсорный чип зажат между кюветы и кюветы головы. Электрод сравнения изолирован от потока на пути солевого мостика полиакриламидном геле.
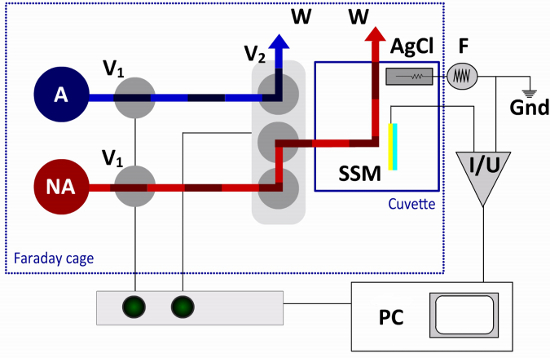
Рисунок 3. Жидкость пути и электрическая схема SSM Setup. В единый протокол обмена решение только одного не активирующие (NA) и один активирующий (A) решения обязательны для заполнения. Поток контролируется двумя 2-ходовой клапан (V1) и один терминал клапана (V2). Терминал клапан переключался между неправительственными организациями и активирующие активирующих решения, направленные одним из решений в кювету и другие решения, чтобы контейнер для отходов (W). Сенсорный чип (SSM) подключен к усилителю (I / U) в то время как эталонный электрод (AgCl) соединен с функционального генератора (F) во внешней электрической цепи. Компьютер (ПК) и интерфейсный блок используется для работы клапана и сбора данных.
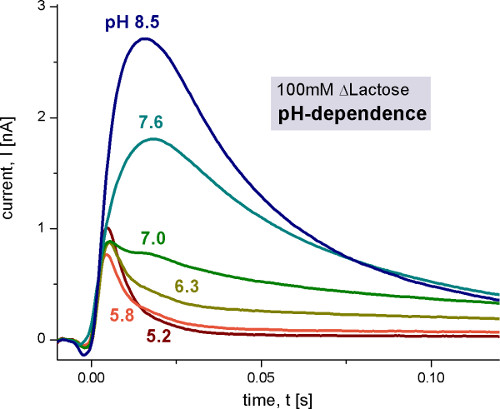
Рисунок 4. Переходных токов, измеряемых с диким типом Лейси протеолипосом после 100 мМ концентрации лактозы скачков при различных значениях рН. Не-активирующий раствор содержал 100 мМ глюкозы, в то время как активирующий раствор содержал 100 мМ лактозы. Все растворы готовили в 100 мМ калий-фосфатном буфере при указанном рН с помощью 1 мМ DTT. Подробности условий измерений в этом и следующих рисунках пожалуйста, обратитесь к 9 и 10.
ftp_upload/50230/50230fig5highres.jpg "/>
Рисунок 5. Средняя нормированная Пик токов, измеряемых с диким типом Лейси протеолипосом после лактоза скачков концентрации при различных концентрациях и рН. К М значений, полученных из гиперболической подходит.
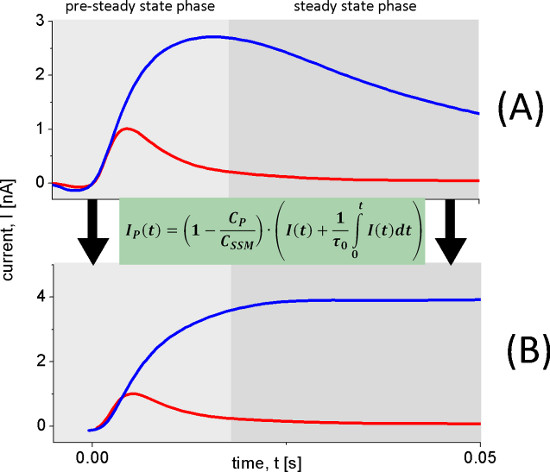
Рисунок 6. Реконструкция транспортер токов. Переходных токов (А) используется для восстановления транспортер тока (B) были измерены с диким типом Лейси протеолипосом после 100 мМ концентрации лактозы скачков при рН 8,5 (голубой луч) и рН 5,2 (красная линия). При рН 8,5 непрерывного оборота наблюдается в то время как при рН 5,2 быстрый электрогенных реакция. Это отчетливо наблюдалась в реконструированном тока (B).
files/ftp_upload/50230/50230fig7.jpg "Alt =" Рисунок 7 "FO: Content-ширина =" 4 дюйма "FO: SRC =" / files/ftp_upload/50230/50230fig7highres.jpg "/>
Рисунок 7. Переходный ток измеряется E325A кружевные протеолипосомами после 100 мМ лактозы скачок концентрации при рН 5,2. Этот кружевной вариант запрещен в протонной шаг выпуске транспортных цикла и поэтому транспортная-дефицитной. Небольшой отрицательный компонент наблюдалось характерное для быстрых переходных токов, измеряемых в емкостной связью системы и вызвано разряда мембраны емкость после быстрого электрогенных реакции. Его постоянная времени π0 определяется емкость и проводимость системы (рис. 1).
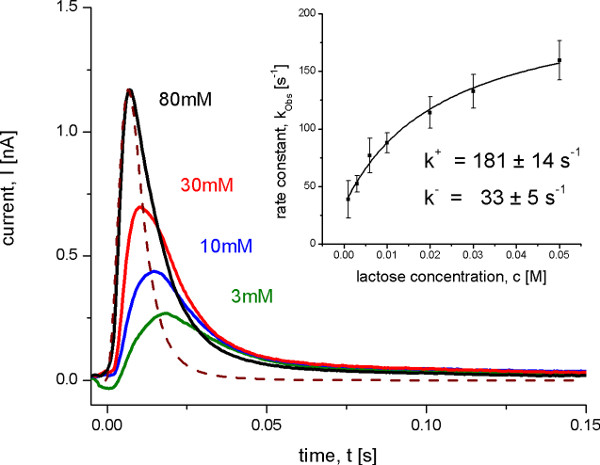
Рисунок 8. Переходных токов, измеренных с диким типом кружевные протеолипосомами AFTEг различных скачков концентрации лактозы при рН 5,2. В этих условиях нет устойчивой транспортной состояние наблюдается, но электрогенных конформационного перехода на лактозу обязательными. Пунктирная линия показывает передаточную функцию представляющий разрешение по времени системы. На вставке показана определения и выключать константы скорости по наблюдаемой скорости постоянной Kobs с гиперболической подходят к данным. Наблюдаемое постоянной скоростью определяли по переходных токов с итерационным методом наименьших квадратов деконволюцией алгоритма 10.
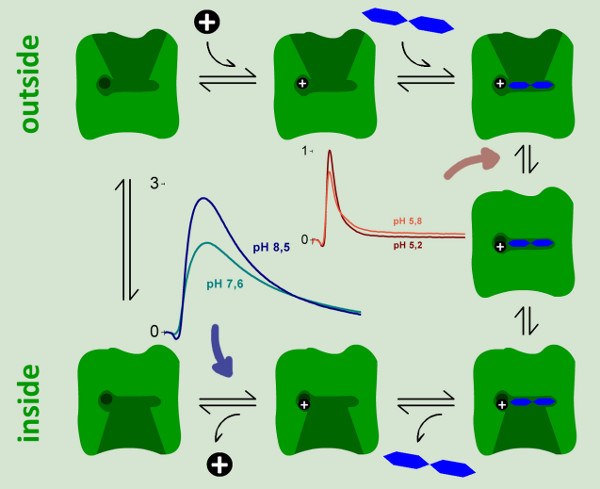
Рисунок 9. Кинетическая модель реакции цикла Лейси. Две электрогенных шаги могут быть идентифицированы и охарактеризованы по SSM измерений. Сильно электрогенных реакции представляющий ~ 94% от общего смещения заряда в реакциицикла наблюдается только при нейтральных и щелочных значениях рН. Это могут быть отнесены к протона шаг релиз (синяя стрелка). Слабо электрогенных шаг наблюдается при кислых значениях рН, когда непрерывный оборот дикого типа Лейси ингибируется. Мы назначенный этой реакции электрогенных конформационного перехода на лактоза связывания, которое представляет 6% от общей перемещение заряда в реакционном цикле.
Обсуждение
1. Преимущества SSM основе электрофизиологических сравнению с традиционными методами
SSM основе электрофизиологии зарекомендовал себя как ценный инструмент электрофизиологических инструментов. Это особенно полезно в тех случаях, когда соглашение электрофизиологии, а именно зажим патч и способы фиксации потенциала, не могут быть применены: Помимо редким исключением бактериальных транспортеров не могут быть исследованы с помощью фиксации потенциала или методов патч зажим из-за малого размера бактерий и потому их трудно выразить в клетках млекопитающих или ооцитов. Но и физиологически значимых млекопитающих транспортеры могут быть исследованы. В этом случае на основе SSM электрофизиологии является привлекательным для перевозчиков из внутриклеточных мембран и для скрининга приложений в лекарственных препаратах из-за своей надежности и ее потенциал для автоматизации.
ССМ-basedUsing обычных электрофизиологии, с разрешением по времени характеристику транспorters является сложной задачей. Поскольку оборот транспортеры низка гигантские патч "или конфигурации" целая клетка "требуется, имеющих по своей сути низким временным разрешением в эксперименте по обмену решение. Осложнения могут быть преодолены использованием фотолитическим релизе подложке. Однако, только ограниченное количество подложки подходит для этого подхода. Здесь быстрый обмен раствора при SSM предлагает уникальную возможность для выполнения электрофизиологических исследований с высоким разрешением по времени использования произвольных подложках.
2. Ограничения и важных шагов
В отличие от зажима патч и методики фиксации потенциала, SSM основе электрофизиологических не может быть использован для применения потенциала. Transporter характеристику поэтому ограничивается видами транспорта, которые не полагаются на мембранный потенциал.
В общем, SSM основе электрофизиологических не имеет ограничений относительно типа (электрогенных) транспортера. Но КЛМетоды усилителя или патч зажим может иметь преимущества, если внутриклеточных компонентов, таких как белки, необходимые для белка функциональности.
Ограничения могут возникнуть, если решение обмена создает большие токи артефакт. Это происходит, когда подложка сильно взаимодействует с SSM, как в случае липофильных соединений. Артефакт управления может быть использован для корректировки измеренных сигналов. Кроме того высоким содержанием соли фона во всех измерений буферы могут быть использованы для уменьшения артефактов. Однако в тех случаях, когда размер артефакт сопоставима с белком сигнал, это почти невозможно выделить белок связанный сигнал от артефакта. К счастью, высокий артефакты необычны в оптимизированным решением.
Есть несколько шагов, которые имеют решающее значение для успешной реализации ССМ-эксперимента на основе электрофизиологии. Подготовка образца белка является наиболее важной частью. Если протеолипосомами используются, убедитесь, что реконовпроституцией способ дает чистое, воспроизводимый образец достаточного LPR и транспортер ориентирована в правильном пути. LPR может быть проверена путем сублимационной перелома электронной микроскопии и ориентации эксперименте ELISA если антитела имеются.
Используйте только SSM, который показывает оптимальные параметры для инкубации образца белка. Инъекций белка еще один важный шаг. Обработка ультразвуком имеет важное значение и пузырьки воздуха следует избегать во время инъекции. После инкубирования пробы измерений сама критическая, потому что пузырьки воздуха удалит адсорбированная образец белка от датчика чипа. Поэтому всегда удаления пузырьков воздуха после изменения решения. Тем не менее сигнал изложение может произойти. Для устранения возможного изложение сигнала, очень важно, чтобы выполнить изложение управления в ходе эксперимента.
3. Специализированные системы
SSM-установки могут быть изменены в соответствии с применением. Кроме того тЗдесь совершенно разные, узкоспециализированные Доступны типы установок.
Существует возможность измерения белка сигналы при асимметричных условиях, например, под градиент рН. Чтобы установить асимметричные композиции буфера внутри и снаружи протеолипосомами третье решение, отдыхая решение, должен быть введен, и это требует двойной конфигурации обмена. Здесь дополнительно трехходовой клапан переключения между не-активирующих и покоя решений не требуется.
Для увеличения времени разрешение системы мы разработали альтернативный путь потока отсутствует терминал клапан, но с использованием другого типа кюветы. Здесь стыке активирующих и не-активирующий раствор расположен внутри кюветы, 3 мм в передней части защитного механизма. Эта установка хорошо подходит для кинетического анализа быстропротекающих процессов транспорта. Это может быть показано, что временное разрешение по цене от 2 мс возможна.
Коммерческая FUlly автоматизированным системам направленных на значительно более высокой пропускной способности для скрининга лекарственных средств. Подвижное устройство собирает решений и вводит их на поверхности сенсора в 96-луночных планшетах в стандартном формате микротитрационных плашек.
Раскрытие информации
Нет конфликта интересов объявлены.
Благодарности
Мы благодарим J. Garcia-Celma, я Смирнова и Р. Kaback за вклад в кружевных измерений и E. Бамберг за поддержку и полезные обсуждения.
Материалы
| Name | Company | Catalog Number | Comments |
| Materials | |||
| Waterbath Sonicator | Bandelin | RK 52 H | |
| Tip Sonicator | Hielscher Ultrasonics GmbH | UP50H | |
| 2-way valve | NResearch, West Caldwell, USA | NR225T011 | |
| Terminal valve | NResearch, West Caldwell, USA | NR225T031 | |
| Manometer | Greisinger electronics | GDH 14 AN | |
| Faraday cage | Max Planck Institute of Biophysics | ||
| Cuvette | Max Planck Institute of Biophysics | ||
| 100 ml solution containers | Kartell | 1623 | |
| O-rings | Seal Science Inc. | ||
| Oscilloscope | Tektronix | TDS 1002 | |
| Reference electrode | Max Planck Institute of Biophysics | ||
| Function generator | Max Planck Institute of Biophysics | ||
| Tubings | SAINT-GOBAIN Performance Plastics | AAC00006 | |
| Sensor chip | Fraunhofer Institut für Schicht und Oberflächentechnik | ||
| Interface box | Max Planck Institute of Biophysics | ||
| Amplifier | Keithley | 427 | |
| Manual cog | Vygon GmbH | 876 | |
| USB analog-to-digital converter | National Instruments | 6009 | |
| Regeants | |||
| 1,2‑Diphytanoyl-sn-glycero-3-Phosphatidylcholine | Avanti Polar Lipids, Inc. | 850356 | |
| Acrylamide/Bis-acrylamide | Sigma Aldrich | A3574 | |
| Ammonium persulfate | Sigma Aldrich | A3678 | |
| D-(+)-Glucose | Sigma Aldrich | G8270 | |
| Dithiothreitol | Sigma Aldrich | 43819 | |
| Ethanol absolut | VWR AnalaR NORMAPUR | 603-002-00-5 | |
| Natural E. coli lipids polar extract | Avanti Polar Lipids, Inc. | 100600 | for LacY reconstitution |
| n-Decane | Sigma Aldrich | D901 | |
| Octadecanethiol | Sigma Aldrich | O1858 | |
| Octadecylamine | Sigma Aldrich | 74750 | |
| Potassium chloride | Merck | 1049360500 | |
| Potassium phosphate dibasic | Sigma Aldrich | P3786 | |
| Potassium phosphate monobasic | Sigma Aldrich | P9791 | |
| Tetramethylethylenediamine | BIO RAD | 1610801 | |
| α-Lactose monohydrate | Sigma Aldrich | L8783 | |
Ссылки
- Seifert, K., Fendler, K., Bamberg, E. Charge transport by ion translocating membrane proteins on solid supported membranes. Biophys. J. 64, 384-391 (1993).
- Schulz, P., Garcia-Celma, J. J., Fendler, K. SSM-based electrophysiology. Methods. 46, 97-103 (2008).
- Garcia-Celma, J. J., et al. Rapid activation of the melibiose permease MelB immobilized on a solid-supported membrane. Langmuir. 24, 8119-8126 (2008).
- Mager, T., Rimon, A., Padan, E., Fendler, K. Transport mechanism and pH regulation of the Na+/H+ antiporter NhaA from Escherichia coli: an electrophysiological study. J. Biol. Chem. 286, 23570-23581 (2011).
- Zhou, A., et al. Charge translocation during cosubstrate binding in the Na+/proline transporter of E.coli. J. Mol. Biol. 343, 931-942 (2004).
- Ganea, C., Fendler, K. Bacterial transporters: charge translocation and mechanism. Biochim. Biophys. Acta. 1787, 706-713 (2009).
- Schulz, P., Werner, J., Stauber, T., Henriksen, K., Fendler, K. The G215R mutation in the Cl-/H+-antiporter ClC-7 found in ADO II osteopetrosis does not abolish function but causes a severe trafficking defect. PLoS ONE. 5, e12585(2010).
- Schulz, P., Dueck, B., Mourot, A., Hatahet, L., Fendler, K. Measuring ion channels on solid supported membranes. Biophys. J. 97, 388-396 (2009).
- Garcia-Celma, J. J., Smirnova, I. N., Kaback, H. R., Fendler, K. Electrophysiological characterization of LacY. Proc. Natl. Acad. Sci. U.S.A. 106, 7373-7378 (2009).
- Garcia-Celma, J. J., Ploch, J., Smirnova, I., Kaback, H. R., Fendler, K. Delineating electrogenic reactions during lactose/H+ symport. Biochemistry. 49, 6115-6121 (2010).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены