Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Method Article
Лигнин вниз-регулирование
В этой статье
Резюме
Двухцепочечной РНК-интерференция (dsRNAi) метод используется для подавляют кукурузы циннамоил коэнзима А редуктазы (ZmCCR1) гена к более низким содержанием лигнина растений. Лигнин понижающая регуляция от клеточной стенки визуализируется с помощью микроскопических анализов и количественно методом Класона. Композиционные изменения в гемицеллюлозы и кристаллической целлюлозы анализируются.
Аннотация
Чтобы облегчить использование лигноцеллюлозной биомассы как альтернативного ресурса биоэнергии, во время биологических процессов конверсии, шаг предварительной обработки необходим, чтобы открыть структуру клеточной стенки растений, повышение доступности клеточной стенки углеводов. Лигнин, полифенольных материал присутствует во многих видах клеточной стенки, как известно, значительное препятствие для доступа фермента. Снижение содержания лигнина до уровня, который не мешает структурной целостности и оборонной системы растения может быть важным шагом для снижения затрат на производство биоэтанола. В этом исследовании, мы генетически подавляется один из биосинтеза связанных генов лигнина, циннамоил-КоА редуктазы (ZmCCR1) через мель техники РНК-интерференции двойной. ZmCCR1_RNAi конструкция была интегрирована в геном кукурузы с использованием метода бомбардировки частицами. Трансгенные растения кукурузы росли нормально по сравнению с контрольными растениями дикого типа, без вterfering с ростом биомассы или защитных механизмов, за исключением показа-коричневого окрашивания в трансгенных растений листовых середине ребра, шелухи, и стеблей. Микроскопические анализы, в сочетании с гистологическим анализом, показали, что лист склеренхимные волокна тоньше, но структура и размер других основных компонентов сосудистой системы не было изменено. Содержание лигнина в трансгенной кукурузы был уменьшен на 7-8.7%, содержание кристаллической целлюлозы был увеличен в ответ на сокращение лигнина и гемицеллюлозы осталась неизменной. Анализы может означать, что поток газа можно было бы сместился с биосинтезе лигнина в биосинтезе целлюлозы. Эта статья очерчивает процедуры, используемые для подавляют содержание лигнина в кукурузе через технологии РНК-интерференции, и анализы клеточной стенки композиционное используется для проверки эффекта изменений на структуру клеточной стенки.
Введение
Производство биотоплива из биомассы лигноцеллюлозы весьма желательно в связи с его нынешней изобилии в США 1, а в случае устойчивого урожая сельскохозяйственных и лесохозяйственных остатков, способность не конкурируют непосредственно для пахотных земель, используемых для пищевой и животного производства кормов. Однако, в отличие зерна кукурузы, которая является основным источником биотоплива в настоящее время, генерируемой в США, лигноцеллюлозные материалы являются значительно более сложными и трудно сломать. В дополнение к длинной цепью углеводов, целлюлозы и гемицеллюлозы, которые являются основными источниками сахара в процессе ферментации лигноцеллюлозных материалов, многих типов клеточных стенок растений также содержат лигнин, в фенилпропаноидного полимера, который обеспечивает прочность, защиту от атаки патогена, и гидрофобность на мобильные стены. В то время как необходимо для роста растений и выживания, лигнин также представляет существенный барьер для успешного ферментативного превращения целлюлозы и hemicelluпроиграть растворимых сахаров. Материалы с высоким содержанием лигнина, как правило, менее желательные материалы как для биотоплива (через пути биологической конверсии) и целлюлозно-бумажной промышленности в связи с негативным воздействием на технологические свойства и качество продукции. Таким образом, генетические манипуляции растительных материалов для сокращения лигнина на уровне, который не вмешивается в растениеводстве структурной прочности и ракетных комплексов может быть важным для снижения издержек производства как для лигноцеллюлозной биотоплива и целлюлозно-бумажной промышленности.
У кукурузы (Zea Mays), лигнин ковалентно сшиты с гемицеллюлозы в первичной клеточной стенки через ферулата и diferulate мостов 2. Лигнин-гемицеллюлоза комплекс связывается с микрофибрилл целлюлозы с помощью водородных связей, образуя сложную матрицу, которая придает целостность и прочность на вторичный клеточной стенки. Механическая прочность клеточных стенок растений во многом определяется типом Lignin субъединиц 3-5. В предыдущих исследованиях, изменяя пропорции лигнина субъединиц не проявляет четкую тенденцию по ферментативной усвояемости 6-11. Тем не менее, снижение содержания лигнина в целом свидетельствуют об улучшении преобразований 12,13 и может быть ключом к повышению усвояемости растительного материала гидролитических ферментов, включая endocellulases, целлобиогидролаз и β-глюкозидаз 14.
Генной инженерии, чтобы регулировать уровень экспрессии транскриптов широко практикуют для улучшения культур черты. Передовые технологии, в том числе анти-смысле 15 и косупрессии 16 технологий, позволяют эффективно понижающей регуляции генов-мишеней. Полный ген нокаут был также достигнут с помощью генных конструкций, кодирующих интронов-сращены РНК со структурой шпильки 17. Кроме того, двухцепочечной РНК-интерференция (dsRNAi) метод, т.е. это мощный и эффективный экспрессии генов СМИтор, который работает либо ориентации деградации транскриптов или перевод репрессии, обеспечивает сильнодействующим средством, чтобы вызвать широкий спектр эффектов подавления на мРНК-мишени 18. Методы молчание генов показать несколько ограничений. Эти методы не точно регулировать уровень транскрипции, и это может привести к неожиданным эффекты глушителей на других гомологичных генов.
В этом методе мы использовали бомбардировку частицами нести dsRNAi конструкции в геном кукурузы. На сегодняшний день, огромный массив видов растений были успешно трансформированы с использованием бомбардировки частицами, Agrobacterium опосредованной трансформации, электропорации и методы микроинъекции. В генетической трансформации кукурузы, метод бомбардировка частицами имеет преимущество перед всеми другими методами, поскольку он является наиболее эффективным. Бомбардировки частицами не зависит от бактерий, поэтому метод свободен от биологических ограничений, таких как размер гена, видов гена илиИгин или завод генотип. Физический трансген система доставки позволяет с высокой молекулярной массы и ДНК множественные гены, которые будут введены в геномов растений и в некоторых случаях в хлоропласты с высокой эффективностью преобразования 19. Снижение лигнин в сосудистой системе листовой середине ребра могут быть визуализированы с помощью сканирующей электронной микроскопии (СЭМ), который является полезным для изучения топографии и состав образцов.
В растений кукурузы, два из редуктазы циннамоил-КоА (ZmCCR1: X98083 и ZmCCR2: Y15069) генов были обнаружены в геном кукурузы 20. Циннамоил-КоА-редуктазы катализирует превращение сложных эфиров hydroxycinnamoyl-КоА в коричные альдегиды. Мы выбрали ген ZmCCR1 вниз-регулировать этот фермент, потому что ген экспрессируется во всех lignifying тканей. В 523 нуклеотиды в конце 3 'гена ZmCCR1 были выбраны для построения, поскольку dsRNAi последовательности, казалось,более разнообразным по сравнению с теми из ZmCCR2. Таким образом, конструкция dsRNAi бы точно связываться только с ZmCCR1, избегая мимо ворот глушителей 21. ZmCCR1_RNAi конструкт был разработан в цитоплазматической экспрессионной системы ImpactVector1.1 тега (IV 1.1), содержащий зеленой ткани специфический промотор, рибулозо-1, 5-бисфосфаткарбоксилазы оксигеназы (RuBisCO).
Для изучения влияния dsRNAi построить на трансгенных растений, содержание лигнина количественно. Класона (кислота нерастворимых в) измерение лигнин, как известно, более точным по сравнению с кислотными методами количественного моющее средство лигнин, который солюбилизации некоторых из лигнина 22. Таким образом, лигнин Класона была измерена в трансгенных стеблей кукурузы. Эта процедура состоит из кислотного гидролиза двухступенчатой который преобразует полимерные углеводы в растворимые моносахаридов 23. Гидролизованный биомасса была затем фракционировали в кислой растворимого и нерастворимого матеALS и кислота нерастворимый лигнин измеряли в соответствии с предыдущих исследований 23,24. В идеале, анализ лигнин должен включать экстракцию водой и этанолом перед стадией гидролиза, с тем, чтобы удалить растворимые материалы, которые могут повлиять на результаты, а также сгорания после гидролиза лигнина остатка с учетом максимального золы, присутствующих в остатке. Без этих шагов, содержание лигнина образца может быть искусственно завышена. Полный метод представлен здесь, однако для наших экспериментов мы не смогли выполнить оба из этих шагов из-за небольшого объема материала, доступного для тестирования
Два других компоненты клеточной стенки, целлюлоза и гемицеллюлоза были также проанализированы в лигнина вниз регулируется трансгенных линий кукурузы. Было сообщено, что трансгенные растения, которые были вниз регулируется в любом их фенилаланиновой аммиак-лиазы (PAL) 25, 4-coumarate: СоА-лигазы (4CL) 26, или коричный вlcohol дегидрогеназы (CAD) 27 показывают рост других структурных компонентов клеточных стенок. В качестве первого шага в наших исследованиях, кристаллическую целлюлозу измеряли с помощью метода Updegraff 28. Этот метод был первоначально разработан для определения целлюлозы в большом количестве клетчатку бактерий и грибков. Вкратце, молотые запасы кукурузы обрабатывали Updegraff реагента (уксусной кислоты: азотная кислота: вода), чтобы удалить гемицеллюлозы, лигнин и xylosans. Кристаллическая целлюлоза была полностью гидролизуется на глюкозу через Saeman гидролиза, добавив H 2 SO 4. Кристаллическую целлюлозу затем анализировали с помощью колориметрического метода, антрон 29. Чтобы проверить, не изменились содержание гемицеллюлозы, моносахаридные экстракты из измельченных стеблей гидролизуют с использованием трифторуксусной кислоты, производные использованием метода алдитол ацетатный, а затем анализировали с помощью газовой хроматографии (ГХ) 30. Подробные процедуры для кристаллического челанализы lulose контент и матричные полисахариды состав описаны в Фостер и др.. (2010) 31.
Здесь мы описываем процедуры, используемые для лигнина вниз регулирования в кукурузе через технологии РНК-интерференции, бомбардировки преобразования частиц и анализа лигнина для ускоренного деконструкции кукурузы лигноцеллюлозной биомассы в ферментации сахаров для биотоплива.
протокол
1. Подготовка dsRNAi конструкции, используемые для понижающей регуляции ZmCCR1
- Генные Дизайн специфические праймеры, включая необходимые сайты рестрикции для принятия dsRNAi построить в нокаут гена ZmCCR1. Два набора праймеров были разработаны для усиления два сегмента фрагмент ZmCCR1 кДНК:. 523 п.о. от нуклеотида 748 до 1271, и 285 п.о. от нуклеотида 986 до 1271 ZmCCR1 кДНК была предоставлена из Аризоны института генома (AGI). Более подробно описаны на рисунке 1.
- Amplify большим фрагментом полимеразной цепной реакции (ПЦР) из шаблона ZmCCR1 кДНК с использованием праймеров ZmCCR1_748F_BglII (5'-AGATCTACATCCTCAAGTACCTGGAC-3 ') и ZmCCR1_1271R_NcoI (5'-CCATGGTTTACACAGCAGGGGAAGGT-3'). Amplify меньший фрагмент (285 п.о.) с использованием праймеров ZmCCR1_986F_BglII (5'-AGATCTGGAAGCAGCCGTACAAGTTC-3 ') и (5R ZmCCR1_1271R_SacI17;-GAGCTCTTTACACAGCAGGGGAAGGT-3 ').
- Индивидуально перевязывать фрагменты в pGEM-T Easy в соответствии с инструкциями изготовителя.
- Выполнение мини-препаративную плазмидную ДНК изоляции из отдельных трансформантов, каждый из которых содержит pGEM-T строит с использованием коммерческого мини-преп плазмиды комплект.
- Дайджест как pGEM-Т :: ZmCCR1 (523 б.п.) и ImpactVector (IV) -1.1 (выражение цитоплазма вектор) и с BglII и NcoI.
- Лигируют большой переваренной геле ZmCCR1 фрагмент (523 б.п.) в переваренной очищают на геле IV-1.1.
- Дайджест pGEM-T :: ZmCCR1 (285 б.п.) и IV-1.1 :: ZmCCR1 (523 б.п.) и с BglII и SacI для того, чтобы вставить небольшой фрагмент в IV-1.1 :: ZmCCR1 (523 б.п.).
- Лигируют небольшой переваренной гель очищают ZmCCR1 фрагмент (285 б.п.) в переваренной очищают на геле IV-1.1 :: ZmCCR1 (523 б.п.).
- Клонировать как 523 б.п. и 285 б.п. фрагментацииTS в IV-1.1, чтобы сделать ZmCCR1 РНК-интерференции построить, который имеет 285 б.п. перевернутой последовательности повторного с 238 б.п. прокладки в середине перевернутых фрагментов повторных (см. Рисунок 1).
- Перевести эту конструкцию в кишечной палочки (E.coli), выращивать их и выполнить изоляцию ДНК размер плазмиды миди-преп получить достаточно ДНК плазмиды для кукурузы генетической трансформации.
2. Кукуруза генетической трансформации
- Подготовка вольфрама частиц
- Наведите 60 мг вольфрама бисера (M10) в 1,5 мл трубки и промыть 1 мл 70% этанола путем встряхивания в течение 2 мин. Выдержите в течение 10 мин при 23 ° С, затем центрифуге при 18894 мкг в течение 2 мин и отбросить супернатант.
- Промыть 3 раза 1 мл 100% этанола, центрифугируют в течение 2 минут и супернатант отбрасывания. Добавить 1 мл стерильного 50% глицерина, чтобы довести концентрацию микрочастиц до 60 мг / мл.
- Подготовка ДНК для бомбардировки
- Plтуз 50 мкл (3 мг) вольфрама гранулы, полученные в 50% глицерине в 1,5 мл трубки. Добавьте 5 мкл (1 мкг) IV-1.1 :: ZmCCR1 РНК-интерференции плазмидной ДНК, 50 мкл 2,5 М CaCl 2 и 20 мкл 0,1 М спермидин. Vortex кратко между каждым добавлением указанных выше реагентов.
- Vortex вольфрама шарик-ДНК смесь коротко и центрифуге при 18894 мкг в течение 30 сек. Слейте супернатант и ресуспендируют гранул в 140 мкл 70% этанола. Удалить жидкость и выбросить. Добавить 140 мкл 100% этанола. Удалить жидкость и выбросить.
- Добавить 48 мкл 100% этанола. Используйте немедленно или хранить на льду в течение до 4 часов до бомбардировки.
- Бомбардировка
- Поместите 3-5 см в диаметре Привет-II эмбриогенный кукурузы каллусах (при условии, от кукурузы трансформации центра Университета штата Айова) в середине 100 мм чашки Петри, содержащие N6OSM СМИ 32 (как osmotium) по крайней мере 4 часа до бомбардировки.
- Подгоэ PSD-1000/He Доставка частиц устройство в соответствии с инструкциями 33 изготовителя.
- Стерилизовать стенки камеры с 70% этанола. Загрузите стерильную 650 фунтов на квадратный дюйм разрыв дисков, в стерильной Кожух. Распространение 5-6 мкл раствора M10-ДНК на поверхности macrocarrier, сухой кратко. Нагрузка macrocarrier и остановки экран на микроносителю запуска сборки.
- Наведите микроносителю запуска сборки и кукурузы каллусах в камере на выбранном расстоянии от экрана остановки (L2 = 6 см) и закрыть дверь. Ускорение в вакууме 27 фунтов на квадратный дюйм против экране проволочной сетки.
- Нажмите кнопку пожарной пока всплески разрыв диска и давление гелия манометр не падает до нуля. Отпустите кнопку огня.
- Выдержите бомбардировке каллусах в чашке Петри, содержащей N6OSM (осмотическое средний) 32 в течение 16 часов в темноте при 27 ° C. Перерыв каллусах в десять штук и трансфер в N6E (каллусогенеза среда) 32 в чашках Петри и выдержать в течение 5 дней ян темноте при 27 ° С.
- Выбор
- Через 5 дней на N6E, передать каллусах на N6S среды (выбор средств массовой информации) 32. Субкультура все каллусы на селективной среде каждые 30 дней в течение 8-12 недель без нарушения структуры Calli.
- Примерно через 8-10 недель, белые быстрорастущие секторы будут расти из Непролиферирующие и частично некротической матери каллусах. Акцизный белые быстрорастущих тканей и субкультура их на свежий селективной среде (N6S) 32 и продолжают инкубировать, как указано выше.
- Регенерация
- Перенести белый и быстро растущий эмбриональных каллусах на среду для регенерации 32 и инкубировать, как указано выше в течение 1 недели. Переключите регенерирующим эмбриогенным каллусах к периоду 16 час дневного света и 8 ч темноте при 25-27 ° С
- Трансфер регенерирующий стреляет на укоренения среды 32 в стеклянную пробирку после 3-4 недель, по-прежнему инкубировать, как указано выше. После существенного гпоявляется развитие OOT, тщательно мыть корни под водопроводной воды, то пересаживать ростки до 4 "горшки с почвой. Покройте горшки с пластиковыми пакетами, чтобы держать влажной. После 2 дней делать небольшие отверстия пластиковые пакеты. После 5-6 дней удалить пластиковые пакеты. Продолжали инкубировать, как указано выше в течение еще 5-6 дней.
- Оранжерея
- Трансфер сеянцы в 18 "горшки с почвой и поддерживать в полном летний Солнечный свет или парникового света. Начальные Регенерированные растения называются Т 0 в то время как первые семена принадлежу к поколению Т 1.
3. Гистологический Анализ
- Закрепите кукурузы листьев средне-ребра в 5 мл 10% нейтральном буферном растворе формалина.
- Процесс и вакуум проникнуть парафином на процессоре ткани, используя процессор ткани.
- Вставить тканей в парафин с использованием вложение станции HistoCentre III.
- Удалить излишки парафина от краев, как только блоккс охлаждаются.
- Образец Раздел на 4-5 мкм с микротоме использованием микротома.
- Наведите разделы по микроскопа и сухой в инкубаторе 56 ° С в течение 2-24 часов. Убедитесь разделы соблюдаться в полной мере слайде.
- Deparaffinize разделы в две смены ксилола в течение 5 мин при 23 ° С
- Сода скользит по две смены 100% этанола в течение 2 мин и две перемены 95% этанола в течение 2 мин при 23 ° С
- Промыть разделы в проточной водопроводной водой в течение 2 мин.
- Пятно с 0,05% толуидиновым синим O в течение 1-2 минут и кратко промыть DDH 2 O.
- Поместите покровное на образцах иммерсионного масла и визуализации с световой микроскопии.
- Сканирующей электронной микроскопии (SEM)
- Закрепить разрезали поперек листа кукурузы средне-ребра в 4% глутарового альдегида и 0,1 М натрий-фосфатный буфер (рН 7,4) при 4 ° С в течение 1-2 часов.
- Сполоснуть образцы в буфере, обезвоженной их вэтанол ряд (25%, 50%, 75% и 95%) в течение 10-15 мин в каждой градации и 100% этанола в течение 10 мин, 3x.
- Высушите обезвоженные разрезали поперек кукурузы листьев средне-ребра в критической точке сушилки с использованием жидкого диоксида углерода в качестве переходного жидкости.
- Установите высушенных образцов на алюминиевых заглушек с помощью высоких требований к вакуум углерода вкладки
- Покрывают кукуруза лист середине ребра установлены на алюминиевых заглушки с золотом (приблизительно 20 нм толщиной) в установке дл покрыти распылением продувают аргоном.
- Изучение образцов покрыли в JEOL JSM-6400V (гексаборид лантана эмиттер электронов) сканирующего электронного микроскопа.
- Цифровые изображения были изображены с помощью Pro программное обеспечение для анализа (версия 3.2).
4. Класона Лигнин Измерение
- Мельница образцы через сито 2 мм.
- С помощью анализатора влажности для определения содержания влаги в каждом образце и записать это значение.
- Взвесить ~ 1,5 г каждого образца и регистрируют массу. EИзвлечь образцы с использованием воды для первой экстракции, с последующим этанола на второй экстракции с использованием либо автоматический съемник растворитель (3 циклов в добыче, ~ 14 мин за один цикл) или аппарате Сокслета (8 час за экстракции). (Примечание: Этот шаг снимает экстрактивные вещества, которые могут конденсироваться при кислотного гидролиза и мешают точного измерения лигнина, увеличивая видимую Класона содержание лигнина.)
- Сушат извлеченные пробы при 45 ° С в течение ночи, а затем дать им остыть в эксикаторе и взвешивают снова.
- Установите инкубатор до 30 ° С. Измерение 0,3 г каждого сухой, извлеченной пробы в скрученной труб высокого давления (трех повторах на образец рекомендуется) и записать весов с точностью до 0,1 мг. Добавьте 3 мл 72% H 2 SO 4 в каждую пробирку давления.
- Смешайте примера с использованием стакан или тефлоновыми стержень. Оставьте перемешайте стержень в трубке, пока вода не добавляется после инкубации.
- Наведите флаконов в инкубаторе себет до 30 ° С и 150 оборотах в минуту в течение 60 мин. Через 1 час добавляют 84 мл деионизированной воды, чтобы разбавить концентрацию кислоты до 4% и смешать с перемешивающим стержнем. Будьте осторожны, чтобы не оставить больших объемов образца по бокам выше ватерлинии флаконе.
- Плотно закрыть фиксаторы на всех флаконах и поместить их в металлическую стойку или больших стаканах. Автоклаве при 121 ° С с использованием жидкого цикл стерилизации в течение 1 часа. Разрешить им остыть до комнатной температуры перед открытием.
- Предварительно пепел фильтрующих тиглей в печи при 575 ° С в течение по меньшей мере 4 часов. Разрешить тигли для охлаждения в эксикаторе в течение по крайней мере часа.
- Вакуумном фильтре раствора из каждой пробирки через отдельный тигле, с помощью резинового переходника, чтобы обеспечить тигель. Используйте деионизированной воды, чтобы ополоснуть все оставшиеся частицы из трубки.
- Сушат лигнина остатка при 105 ° С в течение как минимум 4 часов. Запись веса сухой тигель и остаток.
- При использовании 575 ° C, предварительноОгня образцы над горелку, пока нет никакого дыма или пепла, а затем размещать в печи в течение 24 часов, или при использовании программируемый печи, не предварительно пепел и использовать следующую программу:
- Рампа от комнатной температуры до 105 ° С и удерживать в течение 12 мин.
- Рампа до 250 ° С при 10 ° С / мин и удерживайте в течение 30 мин.
- Рампа до 575 ° С при 20 ° С / мин и удерживайте в течение не менее 180 мин.
- Извлеките тигли из печи и охлаждают в эксикаторе. Взвесьте тигель и пепла.
- Вычислить кислоты нерастворимый остаток, используя следующее уравнение:
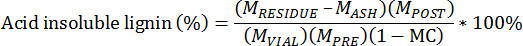
M PRE = масса предварительно извлеченного биомассы
М POST = Масса после добытой биомассы
M VIAL = масса извлеченного биомассы в сосудик добавл
М ОСТАТКИ = Масса тигля и лигнина остаточныхие
М АШ = Масса тигля и золы
MC = Влажность предварительно извлеченного биомассы, полной массе
5. Анализ Углеводы
- Выполните клеток углеводов стены анализирует на основе Фостер и др.. (2010) протокола 31. Короче говоря, Подготовка алкоголя нерастворимого остатка от сублимированного растительного материала. Затем гидролиза материала с трифторуксусной кислоты и соответствовать растворенные производные моносахаридов в соответствующие ацетаты альдита. Анализ эти летучие производные с помощью газовой хроматографии (ГХ), соединенного с четверной масс-спектрометра.
Результаты
Мы показали снижение содержания лигнина в растений кукурузы через RNAi. Метод преобразования бомбардировка частицами дали около 30% эффективности trnasformation. Ген молчание ZmCCR1 последовательно наблюдается в Т0-Т2 поколений. Лигнина снижается трансгены вырос аналогично дикого типа расте?...
Обсуждение
Доступность микробных целлюлазы к клеточной стенки растений полисахариды в основном зависит от степени, в которой они связаны с фенольных полимеров 23. Обменный курс от лигноцеллюлозной биомассы способный к брожению сахар отрицательно коррелирует с лигнина на хранение в растит?...
Раскрытие информации
Нет конфликта интересов объявлены.
Благодарности
Микроскопическая изображений проводилось с помощью услуги в Мичиганском государственном университете Центра перспективных микроскопии. Кукуруза каллуса был приобретен у Transformation Center кукурузы из Университета штата Айова. Авторы хотели бы поблагодарить Джеффри Р. Weatherhead из Научно-исследовательской лаборатории МГУ завод для его технической помощи в области анализа углеводов. Это исследование было щедро финансируется Кукуруза маркетинговой программы Мичигана (CMPM) и Консорциумом по исследованию биотехнологии растений (CPBR).
Материалы
| Name | Company | Catalog Number | Comments |
| N6OSM (Osmotic medium) | Made in-house | ||
| N6E (Callus induction) | Made in-house | ||
| N6S media (Selection media) | Made in-house | ||
| Regeneration medium | Made in-house | ||
| Rooting medium | Made in-house | ||
| 10% Neutral buffered formalin (1 L) | Made in-house | ||
| Bio-Rad PSD-1000/He Particle Delivery device | Hercules, CA, United States | ||
| Zeiss PASCAL confocal laser scanning microscope | Carl Zeiss, Jena, Germany | For brightfield microscopy, the images were recorded using a Zeiss (Jena, Germany) PASCAL confocal laser scanning microscope with a 488 nm excitation mirror, a 560 nm emission filter, and a 505-530 nm emission filter. Image analysis was performed using Laser scanning microscope PASCAL LSM version 3.0 SP3 software. | |
| Excelsior ES Tissue Processor | Thermo Scientific, Pittsburgh, PA, United States | ||
| HistoCentre III Embedding Station | Thermo Scientific, Pittsburgh, PA, United States | ||
| Microtome Model Reichert 2030 | Reichert, Depew, NY, United States | ||
| Emscope Sputter Coater model SC 500 | Ashford, Kent, England | ||
| JEOL JSM-6400V Scanning Electron Microscope | JEOL Ltd., Tokyo, Japan | ||
| Fitzpatrick JT-6 Homoloid mill | Continental Process Systems, Inc., Westmont, IL | ||
| MA35 Moisture Analyzer | Sartorius | ||
| Critical point dryer, Balzers CPD | Leica Microsysstems Inc, Buffalo Grove, IL, United States | ||
| Screw-top high pressure tubes | Ace Glass, Vineland, NJ | #8648-27 | |
| Screw-top high pressure tube plugs | Ace Glass, Vineland, NJ | #5845-47 |
Ссылки
- Ralph, J., Grabber, J. H., Hatfield, R. D. Lignin-ferulate cross-links in grasses - Active incorporation of ferulate polysaccharide esters into ryegrass lignins. Carbohydrate research. , 275-178 (1995).
- Park, S. -. H. . Expediting cellulosic biofuels agenda: Production of high value-low volume co-products and lignin down-regulation of bioenergy crops [Ph.D. thesis]. , (2011).
- Boerjan, W., Ralph, J., Baucher, M. Lignin biosynthesis. Annual review of plant biology. 54, 519-546 (2003).
- Gibson, L. J. The hierarchical structure and mechanics of plant materials. Journal of the Royal Society, Interface / the Royal Society. 9, 2749-2766 (2012).
- Dien, B. S., et al. Enhancing alfalfa conversion efficiencies for sugar recovery and ethanol production by altering lignin composition. Bioresource technology. , 102-6486 (2011).
- Fu, C. X., et al. Downregulation of Cinnamyl Alcohol Dehydrogenase (CAD) Leads to Improved Saccharification Efficiency in Switchgrass. Bioenerg Res. 4, 153-164 (2011).
- Grabber, J. H., Ralph, J., Hatfield, R. D., Quideau, S. p-hydroxyphenyl, guaiacyl, and syringyl lignins have similar inhibitory effects on wall degradability. Journal of agricultural and food chemistry. 45, 2530-2532 (1997).
- Li, X., et al. Lignin monomer composition affects Arabidopsis cell-wall degradability after liquid hot water pretreatment. Biotechnology for biofuels. 3, (2010).
- Mansfield, S. D., Kang, K. Y., Chapple, C. Designed for deconstruction--poplar trees altered in cell wall lignification improve the efficacy of bioethanol production. The New phytologist. 194, 91-101 (2012).
- Studer, M. H., et al. Lignin content in natural Populus variants affects sugar release. Proceedings of the National Academy of Sciences of the United States of America. 108, 6300-6305 (2011).
- Chen, F., Dixon, R. A. Lignin modification improves fermentable sugar yields for biofuel production. Nature. 25, 759-761 (2007).
- Ziebell, A., et al. Increase in 4-coumaryl alcohol units during lignification in alfalfa (Medicago sativa) alters the extractability and molecular weight of lignin. The Journal of biological chemistry. 285, 38961-38968 (2010).
- Park, S. -. H., et al. The quest for alternatives to microbial cellulase mix production: corn stover-produced heterologous multi-cellulases readily deconstruct lignocellulosic biomass into fermentable sugars. Journal of Chemical Technolog., and Biotechnology. 86, 633-641 (2011).
- Mol, J. N., et al. Regulation of plant gene expression by antisense RNA. FEBS letters. 268, 427-430 (1990).
- Adamo, A., et al. Transgene-mediated cosuppression and RNA interference enhance germ-line apoptosis in Caenorhabditis elegans. Proceedings of the National Academy of Sciences of the United States of America. 109, 3440-3445 (2012).
- Smith, N. A., et al. Total silencing by intron-spliced hairpin RNAs. Nature. 407, 319-320 (2000).
- Park, S. -. H., et al. Downregulation of Maize Cinnamoyl-Coenzyme A Reductase via RNA Interference Technology Causes Brown Midrib and Improves Ammonia Fiber Expansion-Pretreated Conversion into Fermentable Sugars for Biofuels. Crop Sci. 52, 2687-2701 (2012).
- Altpeter, F., et al. Particle bombardment and the genetic enhancement of crops: myths and realities. Mol Breeding. 15, 305-327 (2005).
- Pichon, M., Courbou, I., Beckert, M., Boudet, A. M., Grima-Pettenati, J. Cloning and characterization of two maize cDNAs encoding cinnamoyl-CoA reductase (CCR) and differential expression of the corresponding genes. Plant molecular biology. 38, 671-676 (1998).
- Mansoor, S., Amin, I., Hussain, M., Zafar, Y., Briddon, R. W. Engineering novel traits in plants through RNA interference. Trends in plant science. 11, 559-565 (2006).
- Hatfield, R. D., Jung, H. -. J. G., Ralph, J., Buxton, D. R., Weimer, P. J. A comparison of the insoluble residues produced by the Klason lignin and acid detergent lignin procedures. J Sci Food Agr. 65, 51-58 (1994).
- Sluiter, J. B., Ruiz, R. O., Scarlata, C. J., Sluiter, A. D., Templeton, D. W. Compositional analysis of lignocellulosic feedstocks. 1. Review and description of methods. Journal of agricultural and food chemistry. 58, 9043-9053 (2010).
- Sluiter, A., Hames, B., Ruiz, R., Scarlata, C., Sluiter, J., Templeton, D., Crocker, D. Determination of structural carbohydrates and lignin in biomass. Laboratory Analytic Procedure. , (2008).
- Bate, N. J., et al. Quantitative Relationship between Phenylalanine Ammonia-Lyase Levels and Phenylpropanoid Accumulation in Transgenic Tobacco Identifies a Rate-Determining Step in Natural Product Synthesis. Proceedings of the National Academy of Sciences of the United States of America. 91, 7608-7612 (1994).
- Hu, W. J., et al. Repression of lignin biosynthesis promotes cellulose accumulation and growth in transgenic trees. Nature. 17, 808-812 (1999).
- Lapierre, C., et al. Signatures of cinnamyl alcohol dehydrogenase deficiency in poplar lignins. Phytochemistry. 65, 313-321 (2004).
- Updegraff, D. M. Semimicro determination of cellulose in biological materials. Anal Biochem. 32, 420-424 (1969).
- Yemm, E. W., Willis, A. J. The estimation of carbohydrates in plant extracts by anthrone. The Biochemical journal. 57, 508-514 (1954).
- Filomena, A. P., Cherie, W., Geoffrey, B. F., Antony, B. Determining the polysaccharide composition of plant cell walls. Nature. 7, 1590-1607 (2012).
- Foster, C. E., Martin, T. M., Pauly, M. Comprehensive Compositional Analysis of Plant Cell Walls (Lignocellulosic biomass) Part II: Carbohydrates. J. Vis. Exp. (e1837), (2010).
- Department of Agronomy, Iowa State University. Particle bombardment of Hi II immature zygotic embryos and recovery of transgenic maize plants. , (2005).
- Cano-Delgado, A., Penfield, S., Smith, C., Catley, M., Bevan, M. Reduced cellulose synthesis invokes lignification and defense responses in Arabidopsis thaliana. The Plant journal : for cell and molecular biology. 34, 351-362 (2003).
- Boudet, A. M., Kajita, S., Grima-Pettenati, J., Goffner, D. Lignins and lignocellulosics: a better control of synthesis for new and improved uses. Trends in plant science. 8, 576-581 (2003).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены