Method Article
Высок объём шигеллезом-конкретные бактерицидной Assay
В этой статье
Резюме
Здесь мы представляем протокол для измерения активности Shigellacidal антител в сыворотке крови. Сыворотка смешивается с бактериями и экзогенные дополнением, инкубировали, и реакционную смесь покрытием на плитах агара. Жизнеспособные бактерии образуют колоний, которые подсчитываются, используя перечислитель автоматизированных колонии и используется для определения бактерицидный титр.
Аннотация
Бактерицидная анализы сыворотки (SBAs) измеряют функциональной активности антител и были использованы в течение многих десятилетий. SBA непосредственно измерить активность антител убийства путем оценки способности антител в сыворотке для привязки к бактерии и активировать комплемент. Этот активации комплемента приводит к лизис и уничтожение бактерий целевого объекта. Эти анализы являются ценными, поскольку они выходят за рамки количественного определения антител к разъяснению биологических функций, которые эти антитела, что позволяет исследователям изучить роль, которую антитела могут играть в предотвращении инфекции. SBA были использованы для изучения иммунных реакций для многих патогенов человека, но в настоящее время существует нет общепринятой методологии для Shigella . Исторически SBAs были очень трудоемкий, требующий много времени шаги для точного количественного определения живых бактерий. Этот протокол описывает простой, надежный, и высок объём пробирного что меры функциональных антител, специфичных для шигеллы в сыворотке в пробирке. Метод, описанный здесь предлагает много преимуществ над традиционными SBAs, включая использование замороженных бактериальной запасов, 96 хорошо пробирного плиты, системы микро культура и автоматического подсчета колонии. Все эти изменения делают этот assay, менее трудоемкое и более высокой пропускной способностью. Этот протокол является проще и быстрее выполнять, чем традиционные SBAs пока еще с помощью простых технологий и легко доступных реагентов. Протокол успешно применяется в нескольких независимых лабораториях и анализа надежных и воспроизводимых. Assay может использоваться для оценки иммунного ответа в доклинические, а также клинические исследования. Количественная оценка титры антител shigellacidal, до и после воздействия антигена (либо путем иммунизации или инфекции) позволяет для более широкого понимания как функциональных антител, ответы создаются и их вклад защитного иммунитета. Развитие этого стандартизированы, хорошо изученных пробирного значительно может облегчить Shigella вакцины дизайн.
Введение
Шигеллы серотипов, шигеллам Флекснера 2а, 3а S. Флекснера и S. sonnei, демонстрации эпидемиологических распространенности глобально. Диарейных заболеваний вызванных этими Shigella видов воздействия военных, путешественники1и является основной причиной диарейных смерти среди детей в возрасте до 5 лет в развивающихся странах2. Есть в настоящее время не лицензированных вакцин для защиты от шигеллы, однако, есть несколько вакцин на различных этапах развития. Многие из этих вакцин и других профилактических мер в настоящее время в процессе развития, сосредоточить внимание на антитела, вырабатываемые против Shigella липополисахарида (LPS). LPS является привлекательным вакцины-кандидата, потому что это основной поверхностный антиген и природные инфекции с шигеллезом индуцирует LPS-специфические антитела, которые могут быть защитные против повторного заражения серотип конкретным образом. Таким образом успешный Shigella вакцины будет скорее всего нужно быть multi валентных и цели 3-4, которую Shigella серотипов побудить иммунитет против 70-80% глобально циркулирующих штаммов3,4, 5 , 6. это требует, чтобы анализов для оценки вакцин-кандидатов Shigella специфически для нескольких различных серотипов.
Текущий иммунологические анализы для оценки вакцин-кандидатов сосредоточиться на количественной оценки уровня титры антител, но есть несколько хорошо известных анализов для оценки функциональных антител. Изучение функциональной способности антител важно, потому что возбудителя специфические антитела отвечают за борьбу с инфекцией через ряд функциональных механизмов, включая привязки поверхностных антигенов бактерии и предотвращения прилипания к и инфекция эпителиальных клеток, ориентации клетки бактерий или опсонизацию и фагоцитоз и непосредственно убивает привязки и инициирует каскад дополнением патогенов. Прямое уничтожение бактерий антителами происходит, когда антитела связывать поверхности компонентов целевой бактерий и инициировать дополнением Каскад, ведущие к активации многих zymogens, что в конечном итоге результат в порообразования в бактериальных клеток вызывает лизис и бактериальных смерть. Это прямое убийство бактерий, циркулирующих антител и дополнения могут быть важнейшим ранних линию обороны во время инфекции.
Люди естественно инфицированных имеют антитела с shigellacidal активностью в их сера. Эти бактерии Shigella -специфические антитела были обнаружены с помощью традиционных дополнение опосредованной убийство assays 7,8. Это означает, что, возможно, определенную роль для бактерицидной антител в защиту от Shigella. Традиционные бактерицидной анализов просты в их исполнении: Сыворотка инактивированная тепла (чтобы уничтожить эндогенного дополнением деятельности) и смешанные с бактериями интерес. Экзогенные дополнением добавляется к этой смеси на конкретную концентрацию. Реакционную смесь инкубированы для того чтобы позволить для бактериальных убийства и затем покрытием для подтверждения образуя колонии единиц (CFUs). После того, как учитываются CFUs, 50% убийство индекс (KI) может быть рассчитана и SBA титр определено. Хотя эта процедура является относительно простым, эти анализы может быть трудоемким и длительным для выполнения и результаты могут быть крайне непостоянны. Помимо этих ограничений, не хорошо характеризуется функциональных анализов в настоящее время существуют для Shigella. Таким образом мы успешно разработали и квалифицированных простой, высок объём пробирного измерить Shigella бактерицидной активности для трех из наиболее клинически значимых штаммов9. Этот протокол описывает SBA с изменениями, которые повышают эффективность анализа и воспроизводимость. Первым из этих изменений является использование замороженных бактериальных запасов. Производство одноразовых запасов устраняет необходимость культуры свежие бактерии для калибровочных сокращая при этом assay для анализа изменчивости. Другого времени и труда Экономия преимущества этого протокола является использование формата пробирного 96-луночных пластины. Это позволяет для последовательного разбавления проб, так что диапазон концентраций могут быть проверены. Она также позволяет для использования многоканальных пипеток для обшивки образцы на площади Петри. Когда эти площади Петри используются в сочетании с системой культуры, которая производит микро колоний, уменьшается количество агар пластин, необходимых для анализа. Это, в сочетании с свободно доступного программного обеспечения, подсчета колонии, первоначально разработанный для пневмококковой мультиплексных opsonophagocytic убийство пробирного (МЕПА)10, позволяет для быстрый, автоматизированный и надежный колонии перечисления. Все эти усовершенствования значительно сократить время практического анализа и создание высокой пропускной способности системы, позволяя несколько пластин выполняется одновременно.
Хотя этот протокол был оптимизирован для трех из наиболее клинически значимых серотипов шигеллами, SBA описанные здесь могут легко применяться к многих других бактериальных патогенов. В дополнение к возможности использования настоящего Протокола с другими бактериями этот протокол имеет потенциал, чтобы расширить пределы используя только сыворотки в качестве исходного материала, который может включать в себя анализ антител в других соответствующих образцов типов, таких как слизистая образцы, включая слюны и фекальных проб. Использование этот assay расследовать иммунологические реакции после вакцинации может дать более широкие понимание иммунной реакции, порожденные вакцинации, ведущих к рациональной разработки вакцин, и помощь в понимании как естественный иммунитет развивается.
протокол
Этот протокол руководящим советом защиты человеческого субъекта WRAIR. Образцы, используемые в данном исследовании являются пробах сыворотки крови человека как часть WRAIR протокол № 1328, с соблюдением всех институциональных и федеральных правил, регулирующих защиту человеческих субъектов. Образцы были обезличенных, и использование этих анонимных образцов был классифицирован как не человеческого субъекта исследования UAB IRB (протокол № N150115001).
1. Подготовьте Assay реагентов
- Подготовка 1% желатина, добавив 1 г желатина в 100 мл воды. Автоклавы и хранить при комнатной температуре.
- Подготовить раствор TTC (2,3,5-Triphenyltetrazolium хлорид) 100 мг/мл (1, 000 x), добавив 5 g TTC 40 мл воды. Когда TTC полностью растворяется, отрегулируйте громкость до 50 мл с водой и стерильного фильтра с помощью 0,2 мкм фильтром. Хранят раствор при температуре 4 ° C и защищать от света.
Примечание: TTC размечает бактериальных колоний и делает их гораздо легче подсчитать. ТТС раствор имеет небольшой желтый цвет. Если решение TTC разрабатывает красный цвет, отменить и готовить свежие. - Подготовка 10% натрия азид (НАН3) раствор (100 x), добавив 5 g НАН3 40 мл воды. После полного растворения добавьте 50 мл воды. Хранить при комнатной температуре.
ОСТОРОЖНОСТЬЮ: Азид натрия является ядом и могут быть токсичными, если попадает или всасывается через кожу или в глаза. Он может реагировать с свинца и меди сантехника сформировать весьма взрывоопасные азиды. О распоряжении реагентов, содержащие азид натрия заподлицо с большим количеством воды, чтобы предотвратить накопление азид или отменить в мешке биологической. - Подготовьте LBA пластины (LB агар плита), добавив 35 g агар фунтов в 1 Л воды и автоклав. Добавьте 25 мл на каждый квадратный Петри (120 x 120 мм2). Инкубируйте пластины на RT на 10-20 мин разрешить агар затвердеть. Поместите пластины обратно в пластиковые мешки и хранить при 4 ° C до 1 месяца.
- Подготовьте Overlay агар, добавив 7.5 g агар до 1000 мл воды и автоклав. Инкубируйте в 56 ° C водяной бане до тех пор, пока требуется. Прямо перед использованием, добавьте 1 mL 100 мг/мл TTC и 10 мл 10% НАН3 и хорошо перемешать.
Примечание: Каждая пластина LBA нуждается в 25 мл Overlay агара. Оверлея агар могут быть подготовлены до до одного месяца заранее и растаял в микроволновую печь или на горячей плите, необходимые для анализа. Убедитесь, что температура агар ~ 55 ° C до применения плит LBA. - Подготовьте Assay Buffer, добавив 5 мл по 10 x Хэнкс сбалансированный соли раствора (HBSS) с Ca2 +/Mg2 + и 5 мл 1% желатина в 40 мл воды. Хранить при комнатной температуре.
2. подготовить дополнение и целевой бактерий
-
Подготовить ребенка кролика дополнением (BRC)
Примечание: Подробные критерии для дополнения много выбора можно найти здесь: https://www.vaccine.uab.edu/uploads/mdocs/UAB-MOPA.pdf- Получить замороженные BRC и размораживать с холодной проточной водой. Физически смешать BRC каждые ~ 10-20 мин до тех пор, пока полностью разморозить. Не подвергайте BRC неоднократные заморозить циклов оттаивания.
- В то время как BRC оттаивания, ярлык 1,5 мл, 5 мл или 15 мл пробирок. Место помечены трубы на льду для предварительного охлаждения. Аликвота надлежащего объема BRC предварительно охлажденным пробирок (после заполнения, немедленно вернуться в каждую пробирку льда). Хранить аликвоты на ≤-70 ° C в морозильную камеру.
Примечание: Примерно 1 м комплемента необходима для каждого пробирного плиты. Дополнением аликвоты одноместным и следует aliquoted в объемах, соответствующих пробирного макетов. - Подготовить тепло инактивированная BRC, размораживать один Алиготе активных BRC. Подготовьте на водяной бане 56 ° C. После того, как полностью разморожен BRC, перенести его на водяной бане и Инкубируйте 30 мин.
- После инкубации, удалите тепла инактивированная BRC из водяной бани и дайте ему остыть на RT на 10-15 мин смесь энергично и аликвота ~ 150 мкл для 1.5 мл пробирок microcentrifuge. Хранить аликвоты на ≤-10 ° C.
-
Подготовить целевой бактерий фондовой
Примечание: Процедура ниже используется для подготовки 48 аликвоты целевого фонда бактерий; Если необходимо больше аликвоты протокол можно вычислить по маштабу.- Удаление бактерий главной фондовой флакон из морозильника и циклюют замороженных бактериальных поверхность, чтобы удалить небольшое количество льда из флакона на крови агар пластину. Немедленно вернуть мастер запасов флакона в морозильник.
- Полоска этот небольшой Алиготе бактериальной акций на крови агар пластины и накройте крышкой пластины. Инкубируйте пластину вниз на ночь в 37 °C/5% CO2 инкубатора.
- Трансфер ~ 10 изолированных гладкой колоний Тюбик 50 мл, содержащие 30 мл LB отвара. Инкубируйте 3-5 ч при 37 ° C с нежным тряски до тех пор, пока культура бульон имеет ОД600 ~0.6-0,7.
- Урожай верхней 12,5 мл культуры и передать свежие 50 мл трубки. Центрифуга культуры на 15000 x g за 2 мин, с помощью микро центрифугу столешницы. Отменить супернатант и вновь приостановить гранулы в 25 мл 15% стерильный глицерин ЛБ.
- Хорошо перемешайте и отказаться от 0,5 мл аликвоты в микро стерильные 1.5 мл пробирок (~ 48 трубки). Хранить в морозильной камере аликвоты на ≤-70 ° C.
- Подтверждения бактериальной личности, используя агглютинации тест перед использованием.
-
Определение оптимального разрежения фактора для целевой бактерий фондовой
Примечание: Каждый пакет акций целевой бактерий необходимо титруют в условиях анализа для определения разрежения, необходимых для получения ~ 120 CFU/пятно на ФУНТ пластин.- Получить микротитровальных плиту (разбавления плита) и добавить 135 мкл аналитического буфера хорошо 1A. Мкл 120 пробирного масла для скважин 1B - 1H.
- Удаление флакон замороженных целевой бактерий из морозильника и разморозить при комнатной температуре. Добавьте 15ul акций талой бактериальных хорошо 1A сделать десятикратного разрежения бактериальные фондовом.
- Передавать 30 мкл бактериальных решение от хорошо 1A хорошо 1B для выполнения 5 раз серийный разрежения. Далее 5 раз серийных разведений хорошо 1H для в общей сложности 8 разведений (1:10; 1:50; 1: 250; 1:1 250; 1:6 250; 1:31 250; 1:156 250; 1:781 250).
- Получить другой микротитровальных плиты (Assay плита) и добавить 20 мкл аналитического буфера для все хорошо в колонках 1 и 2 в Assay пластины.
- Передача 10 мкл разбавленного бактерий от каждой скважины в колонке 1 пластину разрежения в соответствующий скважин в колонках 1 и 2 пластины Assay. 10 мкл бактерий передается от хорошо 1A пластину разрежения в хорошо 1A и 2A в Assay пластины и т.д.
- Продолжите с assay, как описано в сыворотке бактерицидной Assay (SBA) ниже для управления A и B управления, шаги 3.6-3.12.
- После того, как пластины были инкубировали на льду, используйте многоканальные пипетки с 8 наконечники пятно 10 мкл из скважин в колонке 1 на пластину LBA. Кроме того пятно скважин из столбца 2 на пластину LBA.
- Продолжите с assay, как описано ниже в шагах 3.14-4.6.
- Определить разрежения бактерии, что дает ~ 120 CFU/спот в управления B, будет использоваться этот разрежения в assay.
3. сыворотка бактерицидной Assay (SBA)
Примечание: Описанной ниже процедуры для одной пробирного пластины, но количество пластин Assay может быть увеличена.
- Тепло инактивирует пробы инкубирования образцами в 56 ° C водяной бане 30 мин.
Примечание: Испытательные образцы должны быть инактивированная тепла до испытания отменить любой эндогенного дополнением деятельности. Это может быть сделано накануне пробирного и инактивированных образцов может быть вновь заморозить или хранить при 4 ° C до тех пор, пока тестирование. - Получить пластины пробирного и добавить 20 мкл аналитического буфера столбцы с 1 по 12 строк A через G. добавить 20 мкл аналитического буфера в колонках 1 и 2 строки H, см. таблицу 1.
- Нагрузка 30 мкл каждого образца, в двух экземплярах, строку H пластину Assay. Например лунки 30 мкл пример 1 в скважины, 3 H и 4 H и отказаться от 30 мкл пример 2 Уэллс 5 H и 6 H, и т.д.
-
Выполните вывозимому серийных разведений испытательных образцов с помощью многоканальных дозаторов.
- Удалить в строке G 10 µ образца из скважин 3H - 12H и передать соответствующие скважин и смешайте образец хорошо закупорить вверх и вниз 8 - 10 раз.
- Затем удалите 10 µ из скважин 3G - 12G и передать соответствующие скважин в строке F и хорошо перемешать.
- Далее эти серийных разведений через строку а. После смешивания скважин в строке A, снимите и выбросьте 10 мкл от скважины 3A-12А, так что все скважины содержат 20 мкл.
Примечание: Поскольку 20 мкл сыворотки используется в объеме всего пробирного 80 мкл, существует 4-кратный дополнительного разбавления в assay. Этот разрежения должна приниматься во внимание при расчете SBA титр путем умножения разведения сыворотки на 4. Например если используется начального разбавления 1:2, фактической разбавления тестируется — 1:8.
- Удалите один флакон замороженных целевой бактерий и разморозить при комнатной температуре. Разбавьте бактерий в 20 мл Assay Buffer согласно заранее Оптимальное разведение фактор (этот коэффициент разрежения определялся в раздел 2.3). Добавьте 10 мкл разбавленного бактерий в каждой скважине пробирного пластины с помощью многоканальных дозаторов.
- Удалите один флакон замороженных BRC и один флакон замороженных тепло инактивированная BRC, разморозить при комнатной температуре с холодной проточной водой или место на решетке биологической безопасности кабинета с обдувом воздуха быстро таять.
- Подготовьте 20% раствором тепла инактивированная BRC. Смесь 100 мкл тепла инактивированная BRC с 400 мкл аналитического буфера. 50 мкл этой 20% тепла инактивированная BRC решения для всех скважин в колонке 1 (контролю скважины).
Примечание: Тепло инактивированная BRC используется как элемент управления для наблюдения за убийство неспецифические (NSK) в assay. - Приготовляют раствор 20% из родной BRC. Смешайте 1 мл родной BRC с 4 мл аналитического буфера. Добавьте 50 мкл этой смеси для всех скважин в колонках 2 через 12 (B контроль и испытания скважин образца).
Примечание: Конечная концентрация BRC в реакционной смеси-12,5%. - Кратко смешать Assay пластины, аккуратно покачивая за 10-15 s на тарелку шейкер или mix закупорить вверх и вниз 8 раз с помощью многоканальных дозаторов.
- Положите пластину Assay в микробиологической инкубатора 37 ° C 2 h (без встряхивания).
- Сухой 2 пластины LBA, удаления крышки и поместив пластин лицом вверх в биологической безопасности кабинета за 40-60 мин.
- Когда завершится 2 ч инкубации, переместите Assay плиты для мокрого льда и инкубировать на 10-20 минут, чтобы остановить реакции.
- Использование 12-канальный дозатор, смешайте скважин в строке H и пятно плита 10 мкл реакционной смеси на нижней части пластины LBA. Немедленно наклона пластины и разрешить пятна для запуска на ~1.5-2 см. Повторите эту процедуру для строки, G, F и E, выявления их выше предыдущей строки на табличке LBA. Строка E, F, G и H запятнаны на один LBA плита и строки A, B, C и D запятнаны на второй пластины LBA таким же образом, см. Рисунок 1.
- Инкубируйте LBA пластины при комнатной температуре до тех пор, пока решение адсорбируется в LBA пластины (10-15 мин). Положите крышки на тарелках LBA и поместите пластины для LBA в микробиологической инкубатор вверх вниз для инкубации на ночь (~ 16-18 ч). Инкубировать S. Флекснера 2a и 3a в 29 ° C и инкубировать S. sonnei это 26 ° c.
Примечание: Эти температуры дают меньше «микро колоний» с размерами для точного подсчета колонии счетчика9. - После ночи инкубации добавьте 25 мл Overlay агар (на ~ 55 ° C) содержит 100 мкг/мл TTC и 0.1% НАН3 для каждой пластины LBA.
- Инкубируйте LBA пластины при 37 ° C 2 h разрешить живых бактерий развивать красный цвет, смотрите Рисунок 1 ниже.
- Пластины с помощью цифровой камеры фотографию и передачи изображений на компьютер, где установлена НИСТ интегрированное программное обеспечение колонии перечисление (NICE), см. Рисунок 2.
Примечание: NICE подсчета колонии программное обеспечение доступно на безвозмездной основе. Список Материалов для сведения и инструкции по установке.
4. количество бактериальных колоний
- Ницца программного обеспечения с открытым и ввода Имя оператора, эксперимент информацию и любые пробирного заметки в пустые поля. После ввода этих данных нажмите кнопку сделать .
- Импорт сфотографировали пластины, нажав кнопку Открыть и выбрав правильные файлы с компьютера.
- Отрегулируйте значения параметров анализа, установив количество строк 4 и количество столбцов до 12. Настройте параметр фон -3 Сигма и резолюции до минимума. Смотрите Рисунок 2.
- Перемещение регионов интерес (ROI), щелкнув и перетащив таким образом, чтобы каждый ROI прямо над местом одного образца. Убедитесь, что все бактериальные колонии находятся внутри ROI с не перекрываются образцы. После завершения одной пластиной, дважды нажмите Следующая плита в списке сохраненных данных изображения и отрегулировать ROIs. Смотрите Рисунок 2.
- Когда все пластины были скорректированы, нажмите на зеленую кнопку фото , см. рис. 2 и рис. По завершении подсчета нажмите кнопку Экспорт , чтобы экспортировать данные в формате.xls/.xlsx. Имя и сохраните файл.xls/.xlsx для анализа данных.
- Организовать экспорт данных в формате таблицы так, что счетчики организованы в таблице, представляющие 96-луночных пробирного пластины, см Таблица 2.
5. Вычислите титр SBA (KI) и неспецифические убийства (NSK)
Примечание: SBA титр, или убийство индекс (KI) определяется как обратную величину разрежения сыворотки, которая убивает 50% целевой бактерий.
- Вычислите 50% порогового значения индекса (KI) убивает усреднения CFU активных дополнение контроля скважин (управления B) и деления на 2. Рассчитать средний кое для каждого разведения каждого образца, который был выполнен в двух экземплярах, см. таблицу 3.
- Потому что редко сыворотки разрежения принесут именно это значение KI 50%, это может быть интерполированный из двух последовательных сыворотки разведений, один, который убивает менее 50% и один, который убивает более чем на 50%, см. Рисунок 4. Формула для расчета интерполяцией KI SBA приведен ниже:
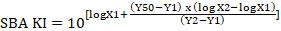
Примечание: Бактерицидный титр, или KI, также может рассчитываться автоматически с помощью программного обеспечения Opsotiter, разработанная ЗАО. Для запроса Opsotiter контакт доктор Луны Nahm или г-н Роб Бертон. Смотрите https://www.vaccine.uab.edu для получения контактной информации. - Вычислить значение NSK, принимая 1 минус в среднем управления B, поделенная на среднее управления а.
Результаты
96-луночных пластины макет, используемый в типичной assay показано в Таблица 1. Эта схема имеет активную дополнение контроля скважин (управления B), тепло инактивированная дополнение контроля скважин (элемент A) и пять образцов в двух экземплярах. Образцы серийно разводили 3 раза вверх пластину от H строки для строки, позволяющий для 8 разведений каждого образца испытываться одновременно. Рисунок 1 показывает две пластины LBA после ночи инкубации и оверлея сложения. Цвет развития имело место и все выжившие колонии отображаются красным цветом. Бактериальные убийство ясно видно для всех образцов в первых трех разведений (строк F-H) и как образцы разводят далее вверх пластину, снижение бактериальной убийство видно где сыворотки менее концентрированным. NICE программного интерфейса можно увидеть на рисунке 2. Микро колонии графов из Ницца программного обеспечения можно увидеть на рисунке 3, и эти отсчеты были организованы в таблице 2. Среднее количество кое для каждого разведения каждого образца вычисляется и значение KI 50% в таблице 3. Это значение 50% KI может применяться к усредненной CFUs для каждого разведения сыворотки для определения значения, необходимые для расчета KI УМБ по формуле, описанные на рис. 4. Окончательный результат анализа показана в таблице 4.
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | |
| A | Элемент управления элемент | Управление B | Разбавление 8 | Разбавление 8 | Разбавление 8 | Разбавление 8 | Разбавление 8 | Разбавление 8 | Разбавление 8 | Разбавление 8 | Разбавление 8 | Разбавление 8 |
| B | Элемент управления элемент | Управление B | Разбавление 7 | Разбавление 7 | Разбавление 7 | Разбавление 7 | Разбавление 7 | Разбавление 7 | Разбавление 7 | Разбавление 7 | Разбавление 7 | Разбавление 7 |
| C | Элемент управления элемент | Управление B | Разбавление 6 | Разбавление 6 | Разбавление 6 | Разбавление 6 | Разбавление 6 | Разбавление 6 | Разбавление 6 | Разбавление 6 | Разбавление 6 | Разбавление 6 |
| D | Элемент управления элемент | Управление B | Разрежения 5 | Разрежения 5 | Разрежения 5 | Разрежения 5 | Разрежения 5 | Разрежения 5 | Разрежения 5 | Разрежения 5 | Разрежения 5 | Разрежения 5 |
| E | Элемент управления элемент | Управление B | Разбавление 4 | Разбавление 4 | Разбавление 4 | Разбавление 4 | Разбавление 4 | Разбавление 4 | Разбавление 4 | Разбавление 4 | Разбавление 4 | Разбавление 4 |
| F | Элемент управления элемент | Управление B | Разбавление 3 | Разбавление 3 | Разбавление 3 | Разбавление 3 | Разбавление 3 | Разбавление 3 | Разбавление 3 | Разбавление 3 | Разбавление 3 | Разбавление 3 |
| G | Элемент управления элемент | Управление B | Разбавление 2 | Разбавление 2 | Разбавление 2 | Разбавление 2 | Разбавление 2 | Разбавление 2 | Разбавление 2 | Разбавление 2 | Разбавление 2 | Разбавление 2 |
| H | Элемент управления элемент | Управление B | Разбавления 1 | Разбавления 1 | Разбавления 1 | Разбавления 1 | Разбавления 1 | Разбавления 1 | Разбавления 1 | Разбавления 1 | Разбавления 1 | Разбавления 1 |
| Пример 1 | Пример 2 | Пример 3 | Пример 4 | Пример 5 | ||||||||
Таблица 1: Assay пластины макета. Колонки 1 и 2 содержат дополнение контроля скважин. Управления A расположен в колонке 1 и тепло инактивированная дополнять элемент управления, содержащий буфер SBA, бактерий и тепло инактивированная дополнения. Управления B расположен в колонке 2 и активной дополнять элемент управления, содержащий буфер SBA, бактерий и дополнения. Столбцы 3-12 содержат образцы сыворотки. Каждый образец выполняется в повторяющихся и серийно разреженных 3 раза из строки H для строки A

Рисунок 1: LBA пластины после разработки цвет. Представитель S. Флекснера 3a микро колонии бактерий на ночь выросли до соответствующего размера. Был добавлен оверлей агар и колониях разработали красный цвет путем уменьшения TTC комплекса в агар оверлея. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.

Рисунок 2: НИСТ интерфейс программного обеспечения комплексной перечислитель колонии (Ницца). Графическое представление NICE программного интерфейса. Регионы интереса (ROI) сосредоточены над колониями для каждого пятна до подсчета. Данные могут быть экспортированы непосредственно из окна хороший. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
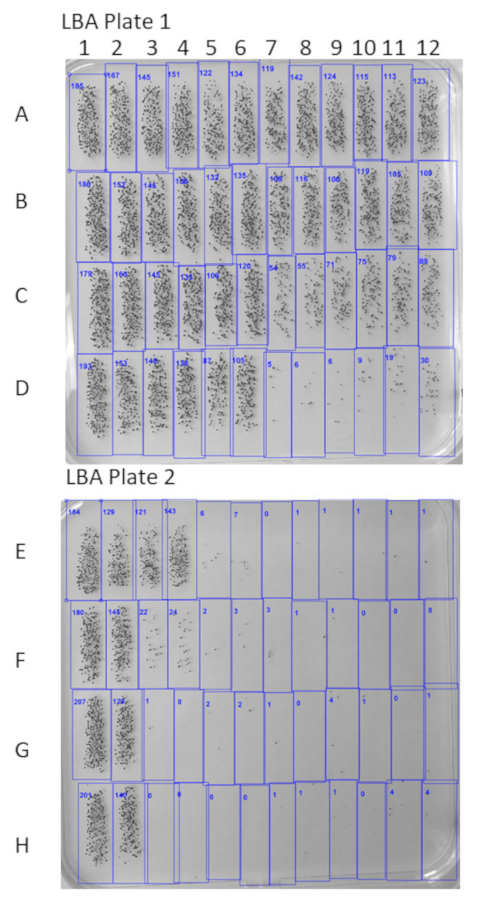
Рисунок 3: LBA плиты подсчитанных в Ницца программного обеспечения. Цветные фотографии изображения загружаются в Ницца программного обеспечения и автоматически подсчитываются колонии формируя единиц (CFUs). Это изображение показывает два представителя LBA пластины с их колонии количество информации. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
| 185 | 167 | 145 | 151 | 122 | 134 | 119 | 142 | 124 | 115 | 113 | 123 | 1:17496 | Разбавление 8 |
| 186 | 152 | 145 | 138 | 132 | 135 | 108 | 116 | 100 | 119 | 105 | 109 | 1:5832 | Разбавление 7 |
| 179 | 160 | 145 | 135 | 109 | 120 | 54 | 55 | 71 | 75 | 79 | 89 | 1:1944 | Разбавление 6 |
| 193 | 153 | 146 | 138 | 87 | 105 | 5 | 6 | 6 | 9 | 19 | 30 | 1:648 | Разрежения 5 |
| 184 | 129 | 121 | 143 | 6 | 7 | 0 | 1 | 1 | 1 | 1 | 1 | 1:216 | Разбавление 4 |
| 180 | 145 | 22 | 24 | 2 | 3 | 3 | 1 | 1 | 0 | 0 | 0 | 1: 72 | Разбавление 3 |
| 207 | 129 | 1 | 0 | 2 | 2 | 1 | 0 | 4 | 1 | 0 | 1 | 1:24 | Разбавление 2 |
| 201 | 140 | 0 | 0 | 0 | 0 | 1 | 1 | 1 | 0 | 4 | 4 | 1:8 | Разбавления 1 |
| Элемент управления элемент | Управление B | Пример 1 | Пример 2 | Пример 3 | Пример 4 | Пример 5 | |||||||
Таблица 2: количество бактериальных колоний. КОЕ графов экспортируются из Ницца программного обеспечения в excel формат. Эти счетчики могут быть организованы в таблицу, бактериальных подсчитывает все дубликаты проб и контроль скважины.
| Элемент управления элемент | Управление B | 148 | 128 | 131 | 120 | 118 | 1:17496 | Разбавление 8 |
| 189 | 147 | 142 | 134 | 112 | 110 | 107 | 1:5832 | Разбавление 7 |
| NSK (1-CtrB/CtrA): 22% | 140 | 115 | 55 | 73 | 84 | 1:1944 | Разбавление 6 | |
| 50% KI (CtrB/2): 73 | 142 | 96 | 6 | 8 | 25 | 1:648 | Разрежения 5 | |
| 132 | 7 | 1 | 1 | 1 | 1:216 | Разбавление 4 | ||
| 23 | 3 | 2 | 1 | 0 | 1: 72 | Разбавление 3 | ||
| 1 | 2 | 1 | 3 | 1 | 1:24 | Разбавление 2 | ||
| 0 | 0 | 1 | 1 | 4 | 1:8 | Разбавления 1 | ||
| Пример 1 | Пример 2 | Пример 3 | Пример 4 | Пример 5 | ||||
Таблица 3: расчет пороговое значение 50% KI и дублировать образец средние. Пороговое значение 50% ки рассчитывалась путем среднее всех управления B скважин и деления на 2. Для каждого разведения каждого образца, который был выполнен в двух экземплярах были рассчитаны средние дубликатов. Также вычисляется значение NSK.

Рисунок 4: схема линейной интерполяции. Количество живых бактерий (ось y) на каждого разведения сыворотки испытания (ось x) печать (бриллианты), и отдельные точки соединены тонкой, пунктирная черная линия. Сплошная и пунктирная горизонтальные линии указывают на 0% и 50% убийств, соответственно. Разведения сыворотки выше (разрежения 5) и ниже (разбавления 4) 50% убийство линии соединены красной линией, и указывается бактерицидный титр (KI). Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
| SBA KI | |
| Пример 1 | 72 |
| Пример 2 | 216 |
| Пример 3 | 1994 |
| Пример 4 | 1994 |
| Пример 5 | 648 |
Таблица 4: SBA результаты показаны бактерицидный титр (KI). Конечные значения SBA KI были определены для каждого образца и показаны. Эти значения вычисляются с помощью средняя CFUs, пороговое значение 50% KI и формулы линейной интерполяции.
Обсуждение
Протокол, описанные здесь демонстрирует функциональной иммунной пробирного оценить shigellacidal активности антител в сыворотке крови. В assay продемонстрировал для этого протокол моноклональных антител специфических для S. Флекснера 3а были используемые9 наряду с управления человеческой сыворотки от предыдущих Shigella вакцины исследование11. Источник сыворотки испытания в этот assay может широко варьироваться от доклинические животных образцы человека клинических образцов, и shigellacidal активности сыворотки образца будет затронуто иммунизации и воздействия, которые человек переживает. Некоторые перекрестной реактивности может ожидать между тесно связанных серотипов, специально S. Флекснера 2a и 3a Флекснера S. но мало перекрестной реактивности был замечен в этих штаммов по сравнению с S. sonnei9. Основу SBA фокусируется на активации комплемента Каскад путем связывания антител антигена. Таким образом обработка реагента BRC является одним из многих критических шагов, участвующих в выполнении настоящего Протокола. BRC был выбран для использования в этом assay из-за его стабильную производительность и низкий уровень NSK в других бактерицидных анализов по12,13,14. Деятельность BRC – температура чувствительных и должны быть соответствующие меры для обеспечения что заморозить циклов сведены к минимуму, что BRC aliquoted на одноместное размещение томов, и что BRC аликвоты оттаяла быстро, непосредственно перед использованием в assay таяния. Согласованность дополнением деятельности повлияет воспроизводимость этот assay. Другой критический шаг, который воздействие пробирного воспроизводимость является производство и разбавления бактериальной запасов. Важно, что перед началом анализа соответствующих разрежения бактериальной запасов определяется, как assay успех в зависимости от последовательного производства элементов A и B имеющие CFU графов в среднем ~ 120 кое на месте. Для того чтобы получить пятна, которые countable программного обеспечения, важно также, что метод, используемый для бактерий пластина выполнена успешно. Осаждение бактериальных решение и наклона пластины, так что места выполнения ~ 2-3 см имеет решающее значение для производства колонии право размер и правильное распределение для точного подсчета Ницца программного обеспечения. Мастеринг все эти шаги будет гарантировать, что точные, последовательные результаты производятся этот протокол
Даже когда все важнейшие шаги выполняются также могут существовать случаи, когда это необходимо для изменения или устранения неполадок Этот протокол. Изменения настоящего протокола для оценки других бактерий может потребоваться оптимизация ночи температуры инкубации пластины LBA, обеспечить формирование микро колоний. Другие штаммы бактерий или антитела источников, отличных от сыворотки, может потребоваться оптимизация дополнением концентрации. NSK ценностей и KIs контроля сывороток также должна контролироваться для обеспечения что assay работает надлежащим образом. NSK следует рост не более 70%. КИ контроля сывороток не должны варьироваться более чем означает ± 2SD. Для достижения успешных и согласованных результатов при использовании данного протокола, будет необходимо выполнить все шаги, как описано здесь, с уделением особого внимания критическим шаги, описанные выше.
Хотя этот протокол заполняет важную потребность в Shigella исследовательского сообщества, это не без его ограничения. Этот протокол основывается на биологических материалов и, таким образом, всегда будут некоторые изменчивости, которую трудно контролировать. Вариации в дополнение деятельности из разных партий и источников может способствовать вариативности в анализов. Чтобы избежать этого, важно правильно обрабатывать дополнением и тестирование новых много дополнения деятельности перед покупкой. Она также может быть полезно для создания пулов дополнением лотов с известной активностью иметь однородную поставок. Этот протокол является простой конструкцией и не требует какого-либо специализированного оборудования и автоматизированных колонии, перечисляя программное обеспечение является свободно доступным. Хотя эта простота является преимуществом, позволяя этот протокол, которые будут использоваться в практически любой лаборатории, она по-прежнему требуют ночь инкубации. Недавние анализы были описаны которые гораздо короче инкубационного требование, но требуют специализированных, подготовительные реагентов15. Другое ограничение этот assay состоит, что в своем нынешнем виде она способна только расследования одного бактериальных видов одновременно. В поле Shigella есть желание создать многовалентных вакцины, и имеющие иммунологические анализы, которые можно оценить патогенов в духе мультиплекс имеет большое значение. Этот assay может быть изменен в будущем, чтобы удовлетворить эту потребность, но в его нынешнем виде, это один plex пробирного.
Хотя этот assay имеет некоторые ограничения, она по-прежнему имеет много преимуществ над существующими или альтернативных методов. Эти преимущества включают в себя множество улучшений, которые объединяются, чтобы сделать выполнение этого метода гораздо менее трудоемкой и более высок объём чем традиционные SBA. Использование замороженных бактериальной запасов, формат пробирного 96-луночных пластины, покрытия на большие площади Петри, окраски колоний, которая позволяет для фотографирования и автоматического подсчета колонии, все помогают сократить материалы и время, необходимое для завершения этого анализа. Этот assay также имеет преимущества перед другими методами высок объём, потому что он не требует никаких специальных реагентов или оборудования. Протокол, в описанный могут быть выполнены с основные реагенты и свободно доступного программного обеспечения, позволяя для его применения в любых условиях лаборатории.
Все преимущества, которые предоставляет этот протокол поддерживает его использование многих будущих расследований. Assay идеально подходит для изучения иммунной реакции после вакцинации или природные инфекции. Это приложение позволяет SBA быть ценным инструментом в исследования в области вакцин, шигеллы и уже используется для оценки иммуногенность вакцины в вакцинах био конъюгат шигеллы , где она продемонстрировала способность этих вакцин для стимулировать производство функциональных антител16. Этот протокол были тщательно протестированы несколькими лабораториями и было показано для получения надежных и воспроизводимых результатов9. Этот протокол также производит сопоставимые результаты, когда же образцы тестируются с помощью других бактерицидных анализов17. Последовательности в данных, генерируемых этот assay, и его совместимости с другими старых методов делает это надежный инструмент для точной оценке бактерицидная активность в образцах сыворотки. Assay также легко могут быть адаптированы для оценки дополнительных образцов типов. В то время как сыворотка легко доступны в взрослых клинических испытаниях, это может быть трудно получить достаточно сыворотки в исследованиях, посвященных младенцев и маленьких детей; один из возможных целевых групп населения Shigella вакцин. В этих испытаниях цельная кровь регулярно собираются на фильтровальной бумаге и сушат. Был некоторые предварительные успех с этим типом типовой формат, используя SBA. В дополнение к цельной крови слизистой образцов (например, слюны, фекальные экстракты и мочи) также являются цели, которая актуальна в исследование вакцин бактерии Shigella . В настоящее время этот протокол был оценен для трех из наиболее клинически значимых серотипов шигеллы , но она также может быть адаптирована для дополнительных Shigella spp., а также других бактериальных патогенов. Будущая работа будет сосредоточена на производстве мультиплекс пробирного многие из те же характеристики, как assay, описанных в настоящем Протоколе. Мультиплексированных пробирного позволит для оценки нескольких серотипов Shigella одновременно, дальнейшее сохранение образца томов и руки на время пробирного. Существует также работа ведется передать этот assay лабораторий по всему миру. Эти глобальные оценки будет генерировать больше данных на отборочный пробу на более широком масштабе исследований, хотя в то же время увеличивая количество микробиологии и иммунологии лабораторий, которые имеют доступ к этой СБА для оценки бактерий и сыворотки образцов собранные из разных мест эндемичных. Описанные здесь проста и высок объём и имеет возможность улучшить иммунологические оценки в поле шигеллы , а также более широкое применение для оценки других бактериальных патогенов.
Раскрытие информации
R.W.K является сотрудником правительства США и таким образом мнения, выраженные в настоящей публикации являются мнениями авторов и не обязательно отражают официальную политику или координата Департамента армии, министерства обороны, ни правительство США.
Благодарности
Эта работа финансировалась за счет гранта от пути к M.H.N. Это исследование было проведено в качестве совместных исследований и разработке соглашения между Walter Reed Army Института исследований и Университет штата Алабама в Бирмингеме.
Материалы
| Name | Company | Catalog Number | Comments |
| Gelatin | Sigma | G9391 | Type B, powder, BioReagent, suitable for cell culture |
| TTC (2,3,5-Triphenyltetrazolium chloride) | Sigma | T8877 | ≥98.0% (HPLC) |
| Sodium azide (NaN3) | Sigma | S2002 | ≥99.5% |
| Baby Rabbit Complement | PelFreez | 31061-3 | 3-4 week old |
| HBSS with Ca2+/Mg2+ | Invitrogen | 14065-56 | Without Phenol Red |
| LB Agar (Lennox) | Sigma | L2897 | Powder microbial growth medium |
| Bacto Agar | BD | 214010 | Powdered, (C12H18O9)n |
| Glycerol | Sigma | G5516 | For molecular biology, ≥99% |
| LB Broth (Lennox) | Sigma | L3022 | Powder microbial growth medium |
| Square Petri Dish | Sigma | Z617679-240EA | 120 mm x 120 mm |
| Assay Plate | Costar | 3799 | 96 well u-bottom plate with lid |
| NICE Software | University of Alabama at Birmingham | ftp://ftp.nist.gov/pub/physics/mlclarke/NICE/ |
Ссылки
- Riddle, M. S., Sanders, J. W., Putnam, S. D., Tribble, D. R. Incidence, etiology, and impact of diarrhea among long-term travelers (US military and similar populations): a systematic review. The American Journal of Tropical Medicine and Hygiene. 74 (5), 891-900 (2006).
- Tickell, K. D., et al. Identification and management of Shigella infection in children with diarrhoea: a systematic review and meta-analysis. The Lancet Global Health. 5 (12), e1235-e1248 (2017).
- Livio, S., et al. Shigella isolates from the global enteric multicenter study inform vaccine development. Clinical Infectious Diseases. 59 (7), 933-941 (2014).
- Barry, E. M., et al. Progress and pitfalls in Shigella vaccine research. Nature Reviews Gastroenterology & Hepatology. 10 (4), 245-255 (2013).
- Noriega, F. R., et al. Strategy for cross-protection among Shigella flexneri serotypes. Infection and Immunity. 67 (2), 782-788 (1999).
- Levine, M. M., Kotloff, K. L., Barry, E. M., Pasetti, M. F., Sztein, M. B. Clinical trials of Shigella vaccines: two steps forward and one step back on a long, hard road. Nature Reviews Microbiology. 5 (7), 540-553 (2007).
- Sayem, M. A., et al. Differential host immune responses to epidemic and endemic strains of Shigella dysenteriae type I. Journal of Health Population and Nutrition. 29 (5), 429-437 (2011).
- Rahman, M. J., et al. Effects of zinc supplementation as adjunct therapy on the systemic immune responses in shigellosis. The American Journal of Clinical Nutrition. 81 (2), 495-502 (2005).
- Nahm, M. H., et al. interlaboratory evaluations, and application of a simple, high-throughput Shigella serum bactericidal assay. mSphere. 3 (3), (2018).
- Burton, R. L., Nahm, M. H. Development and validation of a fourfold multiplexed opsonization assay (MOPA4) for pneumococcal antibodies. Clinical and Vaccine Immunology. 13 (9), 1004-1009 (2006).
- Tribble, D., et al. Safety and immunogenicity of a Shigella flexneri 2a Invaplex 50 intranasal vaccine in adult volunteers. Vaccine. 28 (37), 6076-6085 (2010).
- Kim, H. W., Kim, K. H., Kim, J., Nahm, M. H. A high throughput serum bactericidal assay for antibodies to Haemophilus influenzae type b. BMC Infectious Diseases. 16, 473(2016).
- Maslanka, S. E., et al. Standardization and a multilaboratory comparison of Neisseria meningitidis serogroup A and C serum bactericidal assays. The Multilaboratory Study Group. Clinical Diagnostic Laboratory Immunology. 4 (2), 156-167 (1997).
- Jang, M. S., Sahastrabuddhe, S., Yun, C. H., Han, S. H., Yang, J. S. Serum bactericidal assay for the evaluation of typhoid vaccine using a semi-automated colony-counting method. Microbial Pathogeneis. 97, 19-26 (2016).
- Necchi, F., Saul, A., Rondini, S. Development of a high-throughput method to evaluate serum bactericidal activity using bacterial ATP measurement as survival readout. PLoS One. 12 (2), e0172163(2017).
- Riddle, M. S., et al. Safety and immunogenicity of a candidate bioconjugate vaccine against Shigella flexneri 2a administered to healthy adults: a single blind, randomized phase I study. Clinical and Vaccine Immunology. , (2016).
- Shimanovich, A. A., et al. Functional and Antigen-Specific Serum Antibody Levels as Correlates of Protection against Shigellosis in a Controlled Human Challenge Study. Clinical and Vaccine Immunology. 24 (2), (2017).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены