Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Method Article
Настройка кислотности катализаторов Pt/ CNTs для гидродезоксигенации дифенилового эфира
В этой статье
Резюме
Представлен протокол синтеза HNbWO6, HNbMoO6, HTaWO6 твердой кислоты нанолист модифицированных Pt / CNTs представлен.
Аннотация
Мы представляем метод синтеза HNbWO6, HNbMoO6, HTaWO6 твердой кислоты нанолист модифицированных Pt / CNTs. Путем изменять вес различных нанолистов твердой кислоты, серия Pt/xHMNO6/CNTs с по-разному твердыми кислотными составами (x s 5, 20 wt%;; М. Нб, Та; N и Mo, W) были подготовлены углеродных нанотрубок предварительной обработки, протоненский обмен, твердая кислота отшелушивания, агрегации и, наконец, Pt частиц пропитки. Pt/xHMNO6/CNTs характеризуются рентгеновской дифракцией, сканированием электронной микроскопии, электронноймикроскопией передачи и NH 3-температурной запрограммированной дезорностью. Исследование показало, что HNbWO6 нанолистов были прикреплены на CNTs, с некоторыми краями нанолистов изогнутые в форме. Кислотная прочность поддерживаемых катализаторов Pt увеличивается в следующем порядке: Pt/CNTs lt; Pt/5HNbWO6/CNTslt; Pt/CNTs 6 /CNTs. Кроме того, была исследована каталитическая гидроконверсия из лигнина, полученного из состава модели: дифениловый эфир с использованием синтезированного катализатора Pt/20HNbWO 6.
Введение
Многие промышленные процессы для производства химических веществ связаны с использованием вакозной неорганической кислоты. Одним из типичных примеров является обычный h2SO4 процесс гидратации циклонексана для производства циклонгексанола. Этот процесс включает в себя двухфазную систему, с циклогексаном, намиеваемым в органической фазе, а продукт циклонгексанола находится в кислой ваквозной фазе, что затрудняет процесс разделения путем простой дистилляции. Помимо трудностей в разделении и восстановлении, неорганическая кислота также является высокотоксичной и коррозионной для оборудования. Иногда, использование неорганической кислоты генерирует побочные продукты, которые снизят урожайность продукта и следует избегать. Например, обезвоживание 2-циклофексен-1-ol для производства 1,3-циклогексадиена с использованием H2SO4 приведет к полимеризации побочных продуктов1. Таким образом, многие промышленные процессы смещаются в сторону использования твердой кислоты катализаторов. Различные воды терпимых твердых кислот используются для решения вышеупомянутой проблемы и максимизировать урожайность продукта, такие как использование H'SM-5 и Amberlyst-15. Было показано, что использование высококремнии H'SM-5 цеолита заменяет H2SO4 в производстве циклонексанола из бензола2. Так как цеолит присутствует в нейтральной ваквойной фазе, продукт будет переходить исключительно к органической фазе, тем самым упрощая процесс разделения. Однако, из-за Льюиса кислотно-кислотного образования аддуктовых молекул к кислотным участкам Льюиса, цеолитические материалы по-прежнему демонстрировали более низкую селективность из-за присутствия неактивных участков3. Среди всех этих твердых кислот, Nb2O5 является одним из лучших кандидатов, которые содержат как Льюис и Br'nsted кислоты сайтов. Кислотность Nb2O5NH2O эквивалентна 70% H2SO4 раствору, из-за присутствия лабильных протонов. Кислотность Брюнстед, сравнимая с протоникными цеолитными материалами, очень высока. Эта кислотность превратится в кислотность Льюиса после ликвидации воды. При наличии воды Nb2O5 образует тетраэдрал NbO4-H2O аддукты, которые могут снизить кислотность Льюиса. Тем не менее, Льюис кислоты сайты по-прежнему эффективны, поскольку NbO4 тетраэдрал по-прежнему имеют эффективные положительные заряды4. Такое явление было успешно продемонстрировано при преобразовании глюкозы в 5-(гидроксиметил) фураля (HMF) и аллиляции бензальдегида с тетрааллиловым олова в воде5. Таким образом, водоустойчивые катализаторы играют решающую роль в преобразовании биомассы в возобновляемые источники энергии, особенно в тех случае, когда преобразования проводятся в экологически химых растворителях, таких как вода.
Среди многих экологических доброкачественных твердой кислоты катализаторов, функционализованные углеродные наноматериалы с использованием графена, углеродных нанотрубок, углеродных нановолокон, мезопорных углеродных материалов играют важную роль в валоризации биомассы из-за настраиваемый пористость, чрезвычайно высокая специфическаяплощадь поверхности, и отличная гидрофобность 6,7. Сульфонированные производные являются особенно стабильными и высокоактивными протоникическими каталитическими материалами. Они могут быть подготовлены либо путем неполной карбонизации сульфонированных ароматических соединений8 или путем сульфонации неполностью карбонизированных сахаров9. Они оказались очень эффективными катализаторами (например, для этерификации высших жирных кислот) с активностью, сопоставимой с использованием жидкости H2SO4. Графены и CNT являются углеродными материалами с большой площадью поверхности, отличными механическими свойствами, хорошей кислотно-кислотной устойчивостью, равномерной разложением размеров пор, а также устойчивостью к осаждению кокса. Сульфонированный графен был найден для эффективного катализировать гидролиз этил ацетата10 и бифункциональные катализаторы графена было установлено, чтобы облегчить один горшок преобразования левуллиной кислоты в -валеролактон11. Бифункциональные металлы, поддерживаемые на CNTs, также являются очень эффективными катализаторами для применения в преобразовании биомассы12,13, таких как высоко селективное аэробное окисление HMF до 2,5-диформилфуна над VO2-PANI/CNT катализатор14.
Воспользовавшись уникальными свойствами твердой кислоты Nb2O5, функционализированных CnT и двухфункционального металла, поддерживаемых на CnT, мы сообщаем о протоколе для синтеза серии Нанолист на основе Nb (Ta) нанолиста нанолиста Pt/CNT с высоким площадь поверхности методом агрегации нанолистов. Кроме того, мы продемонстрировали, что Pt/20HNbWO6/CNTs, в результате синергетический эффект хорошо рассеялись частиц Pt и сильных кислотных участков, полученных из HNbWO6 нанолистов, демонстрируют лучшую активность и селективность в преобразовании лигнин полученных моделей соединений в топливе путем гидродеоксигенации.
протокол
ВНИМАНИЕ: Для надлежащих методов обработки, свойств и токсичности химических веществ, описанных в настоящем документе, обратитесь к соответствующим данным данных о безопасности материалов (MSDS). Некоторые из используемых химических веществ являются токсичными и канцерогенными, и необходимо проявлять особую осторожность. Наноматериалы потенциально могут представлять опасность для безопасности и последствия для здоровья. Следует избегать вдыхания и контакта с кожей. Необходимо соблюдать меры предосторожности, такие как выполнение синтеза катализатора в капоте дыма и оценка производительности катализатора с помощью автоклавных реакторов. Необходимо носить средства индивидуальной защиты.
1. Предварительная обработка СНТ13
- Погрузите 1,0 г CNT в 50 мл азотной кислоты в стакан 100 мл.
- Сножайте раствор при 25 градусах по Цельсию на 1,5 ч для удаления поверхностных примесей и усиления якорного эффекта катализатора.
- Перенесите раствор в круглую нижнюю колбу 100 мл.
- Рефлюкс раствора в смеси азотной кислоты (65%) и серной кислоты (98%) при 60 градусах по Цельсию на ночь. Установите коэффициент громкости на уровне 3:1. Это создаст дефекты поверхности на CNTs.
- Фильтр решение для получения многостенных углеродных нанотрубок твердых. Вымойте твердый с деионированной водой.
- Высушите твердую на 80 градусов по Цельсию в течение 14 ч.
2. Приготовление HNbWO6 нанолистов твердой кислоты15 по протонному обмену с последующим отшелушиванием
- Смешайте стоихиометрические количества Ли2CO3 (0,9236 г) и оксидов металла Nb2O5 (3,3223 г) и WO3 (5,7963 г) при молярном соотношении 1:1:2.
- Calcine твердой смеси при 800 градусах по Цельсию в течение 24 ч с одним промежуточным шлифовальные.
- Поместите 10,0 г порошка LiNbWO6 в 200 мл 2 М HNO3 водного раствора при 50 градусах По Цельсию и перемешайте раствор нуючку в течение 5 дней (120 ч) с одной заменой кислоты на 60 ч.
- Обмен кислотной жидкости каждый день и повторить шаг 2.3.
- Фильтр твердых и мыть твердые с деионизированной водой 3x.
- Высушите твердую на уровне 80 градусов цельсия за ночь.
- Добавьте 25 вт.% TBAOH (тетра (n-butylammonium) гидроксида) раствор 150 мл деионизированного водного раствора с 2,0 г протонного соединения, полученного в шаге 2,6, пока рН не достигнет 9,5 - 10,0.
- Перемешать вышерастворяемый раствор в течение 7 дней.
- Centrifuge выше раствор и собирать супернатант решение, которое содержит рассеянные нанолисты.
3. Приготовление нанолистов твердой кислоты HNbMO6
ПРИМЕЧАНИЕ: Процедура аналогична процедуре шага 2, за исключением первого и третьего этапов.
- Смешайте стоихиометрические количества Ли2CO3 и оксидов металла Nb2O5 и MOO3 в молярном соотношении 1:1:2.
- Calcine выше твердых смесей при 800 градусах Цельсия в воздухе в течение 24 ч с одной промежуточной шлифовки.
- Поместите 10,0 г порошка LiNbMoO6 в 200 мл 2 М HNO3 aqueous раствора при 50 градусах По Цельсию и перемешайте раствор нуючку в течение 5 дней (120 ч) с одной заменой кислоты на 60 ч.
4. Приготовление нанолистов твердой кислоты HTaWO6
ПРИМЕЧАНИЕ: Процедура аналогична процедуре шага 2, за исключением первого и третьего этапов.
- Смешайте стоихиометрические количества Ли2CO3 и оксидов металла Ta2O5 и WO3 в соотношении моляров 1:1:2.
- Calcine выше твердых смесей при 900 градусов по Цельсию в воздухе в течение 24 ч с одной промежуточной шлифовки.
- Поместите 10,0 г порошка LiTaWO6 в 200 мл 2 М HNO3 водного раствора при 50 градусах Цельсия и перемешайте раствор нуючку в течение 5 дней (120 ч) с одной заменой кислоты на 60 ч.
5. Подготовка HNbWO6/MWCNTs методом агрегации нанолистов
- Добавьте 2,0 г многостенных CNT, полученных в шаге 1, к раствору 100 мл нанолистов HNbWO6 в круглую нижнюю колбу размером 250 мл.
- Добавьте 100 мл 1,0 М HNO3 aqueous раствора в круглую нижнюю колбу dropwise. Это позволит агрегировать образцы нанолистов.
- Продолжайте перемешивать раствор при 50 градусах по Цельсию в течение 6 ч.
- Фильтр твердых и мыть твердые с деионизированной водой 3x.
- Высушите твердую на уровне 80 градусов цельсия за ночь.
- Взвесьте высушенное твердое тело и запишите % нагрузку твердой кислоты на MWCNT.
6. Подготовка Pt/20HNbWO6/CNTs методом пропитки
- Растворите H2PtCl6Х2O в воду (1,0 г/100 мл).
- Пропитка как подготовленных нанолистов модифицированных материалов CNTs с 1,34 мл вышеупомянутого вавого раствора Pt.
- Сушите материалы cnT нанолистых на уровне 80 градусов по Цельсию и кальцинировать материалы при 400 градусах по Цельсию в течение 3 ч.
- Получить Nb (Ta) на основе твердой кислоты нанолисты модифицированных Катализаторов Pt / CNTs.
7. Гидродеоксигенация ароматического эфира, полученного из лигнина
ПРИМЕЧАНИЕ: Выбранный лигнин-производный ароматический эфир дифенил эфир в этом эксперименте. Выбранный ароматический эфир, полученный из лигнина, является дифениловым эфиром в этом эксперименте. Активность Pt/20HTaWO6/CNTs (88,8% конверсии, не показано в настоящей работе) ниже, чем Pt/20HNbWO6/CNTs (99,6%), таким образом, урожайность циклогексануменьшаета уменьшается. Таким образом, хотя, более высокая селективность циклонексана была получена в течение Pt/20HTaWO6/ CNTs, более низкое преобразование дифенилэфира ограничивает его использование. Использование соответствующего защитного оборудования и дымового капота для выполнения реакции с использованием канцерогенных реагентов.
- Разбавить 0,05 грамма катализатора в 5 миллилитров кварцевого песка. Загрузите раствор посередине стационарного реактора между двумя подушками кварцевой шерсти.
- Уменьшите катализатор в H2 (40 мл/мин) при 300 градусах по Цельсию в течение 2 ч.
- Насос дифенил эфира сырья (в том числе 5,0 Вт.% реактивант в n-декан и 2,0 wt.% n-dodecane в качестве внутреннего стандарта для анализа газовой хроматографии) в стационарный реактор кровати с различными темпами потока (0,05-0,06 мл / мин)
- Сбор продуктов в разное пространство разное время определяется как соотношение между массой катализатора W (g) и скоростью потока субстрата F (г/мин).
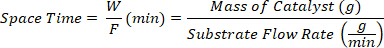
- Определите жидкие продукты по ГК (HP-5, 30 м х 0,32 мм х 0,25 мм) с 5977A MSD и анализируйте офлайн по газовой хроматографии (GC 450, FID, КАпиллярная колонка FFAP 30 м х 0,32 мм х 0,25 мм).
- Определить конверсию реагентов(conv.%), селективность по отношению к продукту I (Si %), и выход продукта i (Yi %) используя следующие уравнения:
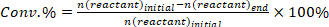 (1)
(1)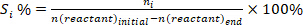 (2)
(2)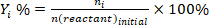 (3)
(3)
Результаты
Рентгеновская дифракционная модели (XRD) были изучены для предшественника LiNbWO6 и соответствующего протонного обмена катализатора образца HNbWO6 для определения фазы (Рисунок1 и Рисунок 2). NH3-температура запрограммирована desorption (N...
Обсуждение
Предварительная обработка ЦНТ азотной кислотой значительноувеличивает специфическую площадь поверхности (S BET). Сырые CNT имеют определенную площадьповерхности 103 м 2/г, в то время как после обработки площадь поверхности была увеличена до 134 м 2/г. Таким образом, такая пре...
Раскрытие информации
Нам нечего раскрывать.
Благодарности
Работа, описанная в настоящем документе, была полностью поддержана грантом Совета по исследовательским грантам Специального административного района Гонконг, Китай (UGC/FDS25/E09/17). Мы также с благодарностью признательны Национальному фонду естественных наук Китая (21373038 и 21403026) за предоставление аналитических инструментов для характеристики катализатора и стационарного реактора для оценки производительности катализатора. Д-р Hongxu Ци хотел бы поблагодарить за научно-исследовательские помощники, предоставленные Научно-исследовательских грантов Совета Гонконга (UGC/FDS25/E09/17).
Материалы
| Name | Company | Catalog Number | Comments |
| Carbon nanotubes (multi-walled) | Sigma Aldrich | 724769 | |
| Nitric acid (65%) | Sigma Aldrich | V000191 | |
| sulphuric acid (98%) | MERCK | 100748 | |
| Lithium carbonate (>99%) | Aladdin | L196236 | |
| Niobium pentaoxide (99.95%) | Aladdin | N108413 | |
| Tungsten trioxide (99.8%) | Aladdin | T103857 | |
| Molybdenum trioxide (99.5%) | Aladdin | M104355 | |
| Tantalum oxide (99.5%) | Aladdin | T104746 | |
| Chloroplatinic acid hexahydrate, ≥37.50% Pt basis | Sigma Aldrich | 206083 | |
| tetra (n-butylammonium) hydroxide 30-hydrate | Aladdin | D117227 | |
| Diphenyl ether, 98% | Aladdin | D110644 | |
| 2-Bromoacetophenone,98% | Aladdin | B103328 | |
| Diethyl ether,99.5% | Sinopharm | 10009318 | |
| n-Decane,98% | Aladdin | D105231 | |
| n-Dodecane,99% | Aladdin | D119697 | |
| Autoclave Reactor | CJF-0.05—0.1L (Dalian Tongda Equipment Technology Development Co., Ltd) | ||
| Tube furnace | SK2-1-10/12 (Luoyang Huaxulier Electric Stove Co., Ltd) |
Ссылки
- Jensen, J. L., Uaprasert, V., Fujii, C. R. Acid-Catalyzed Hydration of Dienes. 2. Changes in Activity Coefficient Ratios, Enthalpy, and Entropy as a Function of Sulfuric Acid Concentration. Journal of Organic Chemistry. 41 (10), 1675-1680 (1976).
- Ishida, H., Ono, M., Kaji, S., Watanabe, A. Synthesis of 1,3-Cyclohexadiene through Liquid Phase Dehydration of 2-Cyclohexen-1-ol in Aqueous Solution using Zeolite Catalyst. Nippon Kagaku Kaishi. 4, 267-275 (1997).
- Ishida, H. Liquid-phase hydration process of cyclohexene with zeolites. Catalysis Surveys from Japan. , 241-246 (1997).
- Ushikubo, T., Iizuka, T., Hattori, H., Tanabe, K. Preparation of highly acidic hydrated niobium oxide. Catalysis Today. 16, 291-295 (1993).
- Nakajima, K., et al. Nb2O5.nH2O as a heterogeneous catalyst with water-tolerant Lewis acid sites. Journal of the American Chemical Society. 133 (12), 4224-4227 (2011).
- Lam, E., Luong, J. H. T. Carbon Materials as Catalyst Supports and Catalysts in the Transformation of Biomass to Fuels and Chemicals. ACS Catalysis. 4 (10), 3393-3410 (2014).
- Sudarsanam, P., et al. Functionalised heterogeneous catalysts for sustainable biomass valorisation. Chemical Soceity Review. 47 (22), 8349-8402 (2018).
- Hara, M., et al. A carbon material as a strong protonic acid. Angewandte Chemie International Edition English. 43 (22), 2955-2958 (2004).
- Toda, M., et al. Biodiesel made with sugar catalyst. Nature. 438 (7065), (2005).
- Ji, J., et al. Sulfonated graphene as water-tolerant solid acid catalyst. Chemical Science. 2 (3), 484-487 (2011).
- Wang, Y., et al. Graphene-Based Metal/Acid Bifunctional Catalyst for the Conversion of Levulinic Acid to γ-Valerolactone. ACS Sustainable Chemistry & Engineering. 5 (2), 1538-1548 (2016).
- Ma, Q., et al. Catalytic depolymerization of lignin for liquefied fuel at mild condition by rare earth metals loading on CNT. Fuel Processing Technology. , 220-225 (2017).
- Rahzani, B., Saidi, M., Rahimpour, H. R., Gates, B. C., Rahimpour, M. R. Experimental investigation of upgrading of lignin-derived bio-oil component anisole catalyzed by carbon nanotube-supported molybdenum. RSC Advances. 7 (17), 10545-10556 (2017).
- Guo, Y., Chen, J. Bicomponent Assembly of VO2and Polyaniline-Functionalized Carbon Nanotubes for the Selective Oxidation of Biomass-Based 5-Hydroxymethylfurfural to 2,5-Diformylfuran. ChemPlusChem. 80 (12), 1760-1768 (2015).
- He, J., et al. Characterization of HNbMoO6, HNbWO6 and HTiNbO5 as solid acids and their catalytic properties for esterification reaction. Applied Catalysis A: General. , 145-152 (2012).
- Tagusagawa, C., Takagaki, A., Hayashi, S., Domen, K. Characterization of HNbWO6 and HTaWO6 Metal Oxide Nanosheet Aggregates As Solid Acid Catalysts. Journal of Physical Chemistry C. 113, 7831-7837 (2009).
- Niwa, M., Katada, N., Sawa, M., Murakami, Y. Temperature-Programmed Desorption of Ammonia with Readsorption Based on the Derived Theoretical Equation. Journal of Physical Chemistry. 99, 8812-8816 (1995).
- Leiva, K., et al. Conversion of guaiacol over supported ReOx catalysts: Support and metal loading effect. Catalysis Today. , 228-238 (2017).
- Deng, W., Liu, M., Tan, X., Zhang, Q., Wang, Y. Conversion of cellobiose into sorbitol in neutral water medium over carbon nanotube-supported ruthenium catalysts. Journal of Catalysis. 271 (1), 22-32 (2010).
- Huang, B., Huang, R., Jin, D., Ye, D. Low temperature SCR of NO with NH3 over carbon nanotubes supported vanadium oxides. Catalysis Today. 126 (3-4), 279-283 (2007).
- Takagaki, A., Tagusagawa, C., Hayashi, S., Hara, M., Domen, K. Nanosheets as highly active solid acid catalysts for green chemical syntheses. Energy & Environmental Science. 3 (1), 82-93 (2010).
- Hu, L. -. F., et al. Structure and photocatalytic performance of layered HNbWO6nanosheet aggregation. Journal of Nanophotonics. 9 (1), (2015).
- Geim, A. K. Graphene: Status and Prospects. Science. 324, 1530-1534 (2009).
- Golberg, D., et al. Boron Nitride Nanotubes and Nanosheets. ACS Nano. 4 (6), 2979-2993 (2010).
- Wilson, J. A., Yoffe, A. D. The transition metal dichalcogenides discussion and interpretation of the observed optical, electrical and structural properties. Advances in Physics. 18 (73), 193-335 (1969).
- Ma, R., Sasaki, T. Nanosheets of oxides and hydroxides: Ultimate 2D charge-bearing functional crystallites. Advanced Materials. 22 (45), 5082-5104 (2010).
- Pope, T. R., Lassig, M. N., Neher, G., Weimar Iii, R. D., Salguero, T. T. Chromism of Bi2WO6 in single crystal and nanosheet forms. Journal of Materials Chemistry C. 2 (17), 3223-3230 (2014).
- Yu, Y., et al. Controlled scalable synthesis of uniform, high-quality monolayer and few-layer MoS2 films. Scientific Reports. 3, 1866 (2013).
- Prasomsri, T., Shetty, M., Murugappan, K., Román-Leshkov, Y. Insights into the catalytic activity and surface modification of MoO3 during the hydrodeoxygenation of lignin-derived model compounds into aromatic hydrocarbons under low hydrogen pressures. Energy & Environmental Science. 7 (8), 2660-2669 (2014).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены