Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Biology
ターゲティングされたのsRNAのファージ媒介送達はにおける遺伝子発現をノックダウンするために構築します
We describe a method to knock down gene expression in a growing population of E. coli cells using sequence-targeted sRNA expression cassettes delivered by an M13 phagemid vector.
RNA媒介性ノックダウンは広く、遺伝子発現を制御するために使用されます。技術のこの多目的ファミリーは、任意の順序で合成し、サイレンシングを対象とした遺伝子を補完するように設計することができ、短いRNA(のsRNA)を利用します。 sRNA直接多くの細胞型に導入されるか、または種々のベクターを使用することができる構築ので、遺伝子発現は、面倒な遺伝子改変することなく、生細胞内で抑制することができます。最も一般的なRNAノックダウン技術、RNA干渉(RNAi)は、標的mRNAの内因性RNA誘導サイレンシング複合体(RISC)媒介する配列認識および切断を利用します。この技術の応用は、したがって、RISC発現生物、主に真核生物に限定されています。最近では、RNAの生物工学の新世代は、RNAを介して遺伝子発現を制御するための代替メカニズムを開発している、などの細菌で可能RNA媒介遺伝子ノックダウンを行いました。ここでは、遺伝子EXPRESをサイレンシングするための方法を説明しますE.でシオン機能的にRNAiを似ている大腸菌 。このシステムでは、合成ファージミドは、任意の配列を標的とするように設計することができるのsRNAを発現するように設計されています。発現構築物は、 大腸菌の集団に送達されます安定してプラスミドとして複製することができ、その後、非溶解性M13ファージによる大腸菌細胞、。アンチセンス認識及び標的mRNAのサイレンシングはE.に対して内因性HFQタンパク質によって媒介されます大腸菌 。このプロトコルは、アンチセンスのsRNAを設計するファージミドベクターを構築し、M13バクテリオファージにファージミドのパッケージング、感染のために生きた細胞集団を調製し、感染そのものを実行するためのメソッドを含んでいます。蛍光タンパク質mKate2及び抗生物質耐性遺伝子、クロラムフェニコールアセチルトランスフェラーゼ(CAT)は、代表的なデータを生成し、ノックダウン効果を定量化するために標的化されます。
RNA媒介遺伝子ノックダウンは、2段階で進行します。まず、RNA分子は、研究の細胞株または生物体に導入されます。第二に、内因性RNA結合タンパク質は、RNA標的の認識を容易にし、消音効果をもたらします。すべてのRNAノックダウン技術は簡単に関心のある特定のターゲットに適合するように製造することができる合成sRNAsのカスタマイズ可能な性質、恩恵を受ける。しかし、RNAの取り込みおよびサイレンシングの分子の詳細は、どこで、どのようにRNAのノックダウンを適用することができる拘束、モデル系全体に広く変化します。
線虫では、二本鎖RNA(dsRNA)分子は、培地中またはdsRNAを発現する大腸菌の集団とワームを供給することによって直接導入することができます大腸菌細胞を1,2。 ショウジョウバエにおいて、RNAiは、dsRNA 3で胚をマイクロインジェクションすることによって達成することができる、または単に培地4へのdsRNAを添加することにより細胞株で実施しました。哺乳動物細胞株において、合成低分子干渉RNA(siRNA)は、エレクトロポレーション1,2,5により生細胞に送達するリポソーム3,6にパッケージ化、又はDNAプラスミドベクター4,7から発現され得ます。 RNA種が細胞質ゾルに到達すると、RNAi経路は、該dsRNAを処理対象のアンチセンス認識を容易にし、ホストに依存して、翻訳抑制、mRNA分解、またはヘテロクロマチンの形成を触媒するためにRISC複合体に依存しています。
そのため、これらの要件のため、古典的なRNAiは、唯一の効率的外因性RNAを取り上げ、RISCまたはRISCライクな活性を発現する生物で行うことができます。注目すべきことに、このモデル細菌E.を除外しますRNAi経路を欠いている大腸菌 、。しかし、合成生物学の最近の進歩は、配信の問題とサイレンシングの問題の両方を解決するためのツールを提供しています。
このプロトコルでは、のsRNA構築物を大腸菌で発現されますリーに送達DNAベクターから大腸菌M13ファージミド/ヘルパーシステムを用いて細胞をレイムス。ファージミドは、複製のファージ由来のf1を原点とする任意のプラスミドです。ヘルパープラスミドは、この場合M13KOに、ウイルス粒子を生成するのに必要なすべての機械を運び、それ自体は複製およびパッケージングのために有能ではありません。ファージミドおよびヘルパープラスミドを同時形質転換された場合、単独のファージミドは、パッケージ化され、分泌され、f1の原点に複製されます。ベクトル化ファージミドは、ライブE.に感染する能力がありますF線毛を介した大腸菌 。
このシステムでは、サイレンシング効果は、標的結合配列を有する骨格配列を組み合わせたカスタムのsRNAカセットによって産生されます。標的結合配列は、典型的には、リボソーム結合部位(RBS)で、mRNA標的に対するアンチセンス24塩基対です。 Naおよび同僚8によって開発された足場のシーケンスは、MICC、Eに内因性の小さな調節RNAから抽出HFQ結合モチーフが含まれています大腸菌 。 HFQタンパク質は、RNA-RNAバインディンを刺激しますgであり、mRNA分解、RNAiの中でRISCに似たこのシステムの役割を提供する。 図1のsRNAカセット構造、ファージミドベクトル化、およびサイレンシング機構を備えたファージ媒介のsRNAノックダウンのための完全なスキームを、示しています。
大腸菌における遺伝子発現を調節する方法として大腸菌 、のsRNAサイレンシングは、簡単、迅速かつ汎用性があります。対象とE.大腸菌は、ファージミドを伝播するとのsRNAを表現超えて負荷がかかりません。これは、より大きな異種構築物の発現は、細胞資源9に負担することができます合成生物学や基礎研究の文脈で関連している可能性があります。新しいターゲットとのファージミドは、単一のPCRにより生産され、ファージミド転換の1日後に収穫することができます。最後に、ほぼすべてのmRNAを標的とすることができます。 (標準プラスミド上)のsRNA規制カセットは> 90%8典型的な抑制レベルと代謝に種々の標的に作用することが示されています。
10をカセットを使用して、以前の作業を拡張したものです。まず、パッケージ化されたファージミドは、Eのバッチ培養に導入され、 coli細胞と蛍光タンパク質mKate2の発現を抑制するために使用されます。その後の蛍光の変化をリアルタイムでモニターされます。第二に、CAT遺伝子をノックダウンする寒天プレート上での表現型クロラムフェニコール耐性を減少させることが示されています。両方の場合において、ファージミド自体は感染率は、独立して、ノックダウン効率を測定することができるように、GFPマーカーを運びます。
1.ミドベクターの設計と建設のsRNAサイレンシングカセットベアリング
- sRNAサイレンシングカセット8のデノボ設計
- mRNAの完全な配列は、DNA配列データベースを使用してサイレンシングされるように特定します。標的配列を生成するには、開始コドン( 例えば、ATG)で始まる位置1から24に、コード配列の最初の24塩基対の点に注意してください。
注:他のサイトまたはmRNAのセグメントが8をターゲットとしているときにサイレンシングはあまり効率的です。 - sRNAカセットのためのガイド配列を生成するために、標的配列の逆相補してください。クロラムフェニコールアセチルトランスフェラーゼ(CAT)のためのTARGETとGUIDEシーケンスの例については、 表1を参照してください。
- 292 bpの完全なのsRNA発現カセットを設計するには、シリーズのPRプロモーター、ガイド配列、HFQタンパク質結合ドメインおよびT1 / TE転写ターミネーター配列( 表2)を配置します。
- ターゲットベクターへのsRNAカセットのクローニングを容易にするための選択肢の追加のクローニングサイトを追加します。
- 商業遺伝子合成を介して、完全なのsRNAカセットまたは類似の方法を取得し、機能f1の複製起点11を有する任意のファージミドベクターにそれをクローン。最終的なファージミドベクターの完全な配列のための情報のサポートを参照してください。
- mRNAの完全な配列は、DNA配列データベースを使用してサイレンシングされるように特定します。標的配列を生成するには、開始コドン( 例えば、ATG)で始まる位置1から24に、コード配列の最初の24塩基対の点に注意してください。
- PCRベースの部位特異的突然変異誘発12を使用して、既存のsRNA発現カセットによって標的とされる配列を変更します
- 既存のsRNA発現カセットに24 bpのガイド配列を特定します。注:この作業で使用される注釈付きpAB.001プラスミドは、補足的なシーケンスファイルとして提供されています。
- 前方デザインと新しい24 bpのガイド配列に隣接する既存のsRNAカセットとの相同性の短い領域とリバースプライマー。商業オリゴヌクレオチド合成によりプライマーを取得します。
注:部位特異的突然変異誘発のためのプライマー設計はdepicですテッドは、 図2の正確なプライマーの鋳型配列を表3に提供されます。 - Eの5ミリリットルの文化を準備テンプレートのsRNA発現ファージミドを保有する大腸菌 。適切な抗生物質を含むLB培地中で、振盪しながら37℃で一晩細胞を増殖させます。
- DNAミニプレップキットまたは類似の方法12を用いて、5ミリリットル細菌培養からテンプレートのsRNA発現ファージミドを抽出し、精製します。
- テンプレートのsRNA発現ファージミドと高忠実度のポリメラーゼ、前方と1とリバースプライマー( 表4)を持つものを使用して、2つのPCR反応を準備します。ポリメラーゼサプライヤー( 表5)によって推奨されるようにPCR条件を使用してください。単一プライマー反応が指数関数的増幅が生じないという事実を考慮するために、標準的な反応よりも高い10-50xするテンプレートの濃度を高めます。
- マイクロチューブに2以上のPCR反応を兼ね備えています。 Annea沸騰水浴中で98°Cに加熱し、L製品。すぐに水浴中でマイクロチューブを配置した後、熱源を除去し、浴をゆっくりと1〜2時間かけて室温に戻すことができます。
- 突然変異していないテンプレートのsRNA発現ファージミドを除去するために、1μlを添加します。混合物にDpnIの制限酵素と1時間、または完全な消化のためにメーカーが推奨する時間、37℃でインキュベートします。
DpnIのは、唯一のメチル化標的部位を消化する、ホストに複製ファージミドではなく、PCR産物上に存在する:注意してください。 - トランスフォーム13化学的コンピテントE.を購入または準備アニールPCR産物の1-5μlを持つ大腸菌 。適切な抗生物質を含むLB寒天プレート上で選択メッキにより形質転換株の単一コロニーを分離します。
- 正しいガイド配列の組込みを確認するために、コロニーPCRによって得られたコロニーをスクリーニングします。 200μlのピペットチップを用いて、CO単一の形質転換コロニーからの細胞の少量をllect。マークとは、確認後、下流の使用のためにオリジナルのコロニーを維持します。
- マイクロチューブにヌクレアーゼフリー水50μlに採取した細胞を追加します。ピペッティングにより混和します。
- ベンチトップの熱サイクラーまたは沸騰水浴を用いて、2分間95℃に加熱することによって細胞を溶解。
- DNAテンプレートとして熱溶解した細胞の1μLを使用してファージミド地域をPCR増幅します。 PCR条件およびサーモプロトコルは、 表6および7に設けられています。検証プライマー配列の補助pAB.001シーケンスファイルを参照してください。
- 正しいガイド配列の組込みを確認するために、PCR産物を配列決定。
- Eの5ミリリットルの培養物に接種配列検証のsRNA発現ファージミドを保有する大腸菌クローン。選択LB培地中、振盪しながら37℃で一晩細胞を増殖させます。
- グリセロールストックを準備します配列検証したクローンの。スクリューキャップクライオチューブに60%グリセロールの250μlに一晩培養物750μlのを追加します。
- 無期限に-80℃でグリセロールストックを保管してください。一晩培養物の残りの部分は、手順2でのsRNA発現ファージミドのソースとして使用することができます。
M13パッケージ化ファージミド株式の2生産と収穫
- Eの5ミリリットルの文化を準備sRNA発現ファージミドを保有する大腸菌 。適切な抗生物質を含むLB培地中で、振盪しながら37℃で一晩細胞を増殖させます。注:のsRNA発現ファージミドは、ステップ1.1.5で説明したようにデノボクローニングして得られた、または変更された既存のファージミドから、ステップ1.2.16で収穫することができます。
- 同様に、Eの5ミリリットルの文化を準備M13KO7ヘルパープラスミドを有する大腸菌 。選択LB培地中、振盪しながら37℃で一晩細胞を増殖させます。
- sRNA expressioを抽出し、精製DNA抽出キット又は類似の方法12を用いて、nは、ファージミドとヘルパープラスミド。
- Cotransformは、購入または1μlののsRNA発現ファージミドとヘルパープラスミドのそれぞれと13の化学的にコンピテント大腸菌を用意しました。両方の構築のための選択的抗生物質を含むLB寒天上にプレーティングすることにより共形質転換体のために選択します。
- 選択的抗生物質を含むLB中で同時形質転換株の単一コロニーから10ミリリットル文化を準備します。 8-12時間または一晩振とうしながら37℃でインキュベートします。
- 10分間、3300×gで文化を遠心。 0.2μmのフィルターを通して上清およびフィルタを収集します。注意:メディア流出の場合には、感染性ファージ粒子を破壊するために希薄漂白剤(0.5%)でエリアを清掃してください。
- 4℃でパッケージ化されたファージミドろ液を保管してください。注:サンプルは、活性の損失なしに数日から数週間維持することができます。
サイレンシングのためのF +標的細胞の調製
- サイレンシングの標的とされる細胞はF線毛14を表現するかどうかを確認します。 F線毛がすでに存在する場合は、手順4に進みます。
注:Eの一般的な実験室株を大腸菌は、それらのゲノムまたはプラスミド上のF線毛の存在を示すために、F +またはF 'と注釈されています。 - EのF +株を取得大腸菌などTOP10F 'として。
注:ターゲット株は共役後のF-プラスミドドナーから分離するために、ユニークな耐性マーカーを保有することを確認してください。 - F +株との結合により、F線毛を導入するために、標的株とF-プラスミドドナー14の両方の5ミリリットルの文化を準備します。適切な抗生物質を含むLB培地中で、振盪しながら37℃で一晩細胞を増殖させます。
- 次の日、両株1希釈する:選択LBの5ミリリットルで100を振とうしながら37℃で培養を継続します。
- OPTを測定することにより、細胞の増殖期を決定しますベンチトップ型分光光度計を用いて600 nmの(OD 600)での文化のiCalの密度。培養物を0.3のOD 600まで、約2時間、細胞を対数増殖期15を示し、達成されます。
- マイクロ遠心チューブに3結合反応を準備:0.5ミリリットルF-プラスミドドナー+ 0.5ミリリットル標的株、0.5ミリリットルF-プラスミドドナー+ 0.5ミリリットルのLB培地(陰性対照)および0.5ミリリットル標的株+ 0.5ミリリットルのLB培地(ネガティブコントロール)。結合は振盪しながら37℃で2時間進行させます。
- プレートF-プラスミド(典型的には、テトラサイクリン)と標的株に特異的な抗生物質を選択的LB寒天上の各結合反応を100μl。どちらのドナーまたはレシピエント株は、両方の抗生物質耐性を発現することを確認するために、ネガティブコントロール反応をプレート。
サイレンシングのためにパッケージ化されたファージミド4.感染
- LBのメディ5mlの培養液中にF +標的細胞の単一コロニーを接種適切な抗生物質を含みます。振盪しながら37℃で一晩インキュベートします。
- 翌日、1 F +標的細胞を希釈:選択LB培地の5ミリリットルで100、振とうしながら37℃で培養を続けます。
- ベンチトップ型分光光度計を用いて600 nmの(OD 600)での培養物の光学密度を測定することによって、細胞の増殖期を決定します。培養物を0.3のOD 600まで、約2時間、細胞を対数増殖期15を示し、達成されます。注:F線毛の発現と感染効率は、対数期で最も高いです。
- 標的集団の約99%の感染を達成するために、100:1の体積比で標的細胞に(ステップ2.6)からM13パッケージファージミドを加えます。感染は30〜60分間振盪しながら37℃で進行させます。
- 選択の方法に応じたsRNAサイレンシング表現型をアッセイ。
注:蛍光タンパク質標的の場合、消音効果を定量化することができます直接蛍光法10による。あるいは、表現型のアッセイは、遺伝子ノックダウン8の表現型の影響を観察するために使用することができます。 - 手順1.2.14-1.2.16次のsRNAを発現するファージミドホストのグリセロールストックを準備します。注:ファージミドは、無期限に宿主株に伝播すると、従来のプラスミドに抗生物質類似して維持することができます。
液体媒体中mKate2蛍光のサイレンシング
図1は、のsRNAカセットの設計、ファージミドベクトル化、およびサイレンシング機構を備えたこの研究に記載のsRNA媒介ノックダウンのためのスキームを示します。プロトコル1.2に続いて、プラスミドpAB.001ののsRNAサイレンシングカセットはmKateを標的とするように変更されました。 sRNAカセットは、合成さやファージミドLitmus28i_J23115-B0032-GFP、モニカ・オルティスとドリューENDY 11からの贈り物にクローニングしました。このファージミドは、成功した感染を追跡できるように、GFP発現およびカナマイシン耐性のマーカーを運びます。パッケージ化されたファージミドの株式は、プロトコル2に従って調製しました。
Eの微分恒常的に発現、染色体に組み込まれmKate2マーカーを保有する大腸菌 K12 MG1655は、コンジュゲーションによってファージ感染のために準備されました対数期中期およびファージミド感染後のプロトコル4.次の導入ファージミドに成長させたプロトコル3.細胞を、以下のFプラスミドドナー株と、200μlの培養物を、蛍光プレートリーダーに移し、蛍光を24時間継続的に監視しました。
図3は mKate2発現に対するのsRNA媒介サイレンシングの効果を示しています。抗mKate2ファージミドを感染させた株は、バックグラウンドを超える検出可能mKate2蛍光を示しませんでした。対照的に、この株は、ファージミドの成功した取り込みを示す、GFPマーカーを発現しました。非感染対照細胞はmKate2蛍光なくGFPを生成しました。抗mKate2ターゲティングドメインは、CATを標的配列と置換した付加的な制御は、mKate2蛍光に影響を及ぼしませんでした。
寒天プレート上のクロラムフェニコール抵抗性のサイレンシング
sRNAサイレンシングカセットはCATを標的とするように製造されたプロトコル1.1、続いて1 ">恒常的に発現し、染色体に組み込まれたCATのマーカーを保有する大腸菌 K12 MG1655の誘導体をのために調製した:「キープtogether.within-ページ= foの「コンテンツ。プロトコル3.細胞以下のF-プラスミドドナー株との結合によってファージ感染は、対数期中期まで増殖させ、ファージミドは、37℃でのインキュベーションの1時間後にプロトコル4.以下の導入、感染した細胞を連続希釈しでプレートしましたクロラムフェニコール濃度。プレート範囲を一晩インキュベートし、そしてそれぞれのクロラムフェニコール濃度で耐性細胞の割合は、コロニー形成単位(CFUの)次の日をカウントすることによって決定しました。図4は、クロラムフェニコール耐性表現型上のsRNA媒介サイレンシングの効果を示しています。 mKate2をターゲットファージミドを感染させた非感染細胞、または細胞は、に耐性でした試験した全ての濃度で、クロラムフェニコール。対照的に、CATを標的とファージミドに感染した細胞は、低クロラムフェニコール濃度で減少生存率を示し、ほぼ99%が高濃度で殺します。アンピシリンを加え、ファージミドを運ぶ細菌のみを選択するためには、検出不可能なレベルにクロラムフェニコールの生存率を減少させました。これは、ファージ感染からの脱出が10をサイレンシング脱出する一般的な経路であることを示す以前の研究と一致しています。
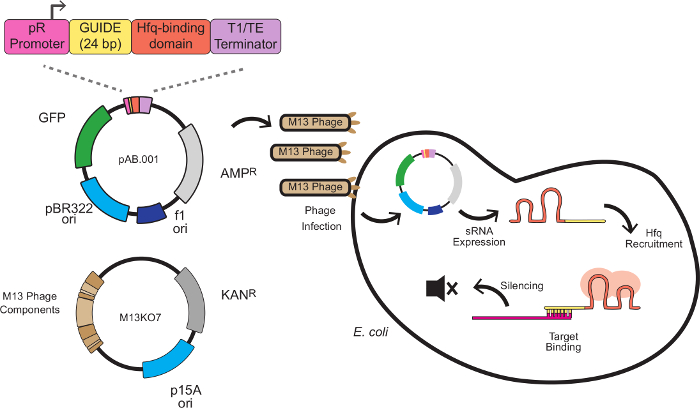
図1: 大腸菌 における遺伝子サイレンシング sRNA発現カセットを持つ 大腸菌は、M13 ファージで配信のsRNAカセットは、4つのモジュールから構成されています。PRプロモーター(バクテリオファージラムダ由来構成的プロモーター)、24 bpの標的ドメイン、HFQ結合ドメインは、MICCから抽出および転写ターミネーター8 、Eに感染することができますsRNA式が始まるF線毛を発現する大腸菌 。 sRNAは、その後、(赤で示されている)HFQタンパク質を動員し、翻訳抑制とmRNA分解の結果、リボソーム結合部位の近くにアンチセンスmRNA標的に特異的に結合する。 この図の拡大版をご覧になるにはこちらをクリックしてください。
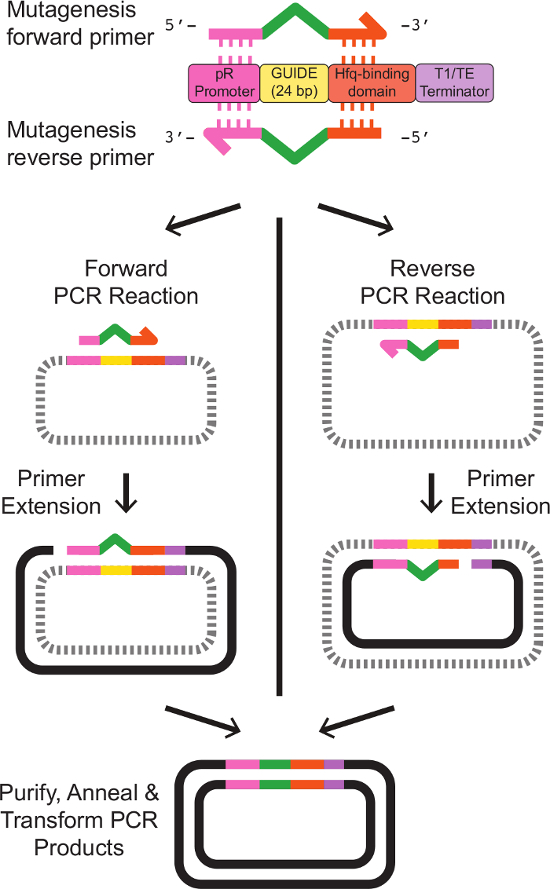
図2:プライマー設計とのsRNAターゲットサイトの部位特異的突然変異誘発は、2つのプライマーを、既存のsRNAカセットへの部分的な相同性を有するように設計されています。フォワードプライマーは、続いて、5 '末端にPRプロモーターに20 bpの相同性を含有します新しいガイド配列を表す24塩基対、3 '末端にHFQ結合ドメインへ、次いで18 bpの相同。逆方向プライマーは、新しいガイド配列の逆相補体に隣接する既存のsRNAカセットと相同性の領域を有するフォワードプライマーの正確な逆相補体、です。正確なプライマー配列を表3に示す。フォワードおよびリバースプライマーを用いた個別の単一プライマーPCR反応は、所望の改変配列を有する直鎖、一本鎖DNAを生成します。前方と希望の修正のsRNAカセットを担持する二本鎖プラスミドDNAでクリーンアッププロトコールに記載されているように、結果に続いて、反応生成物を逆にアニールする。 この図の拡大版をご覧になるにはこちらをクリックしてください。
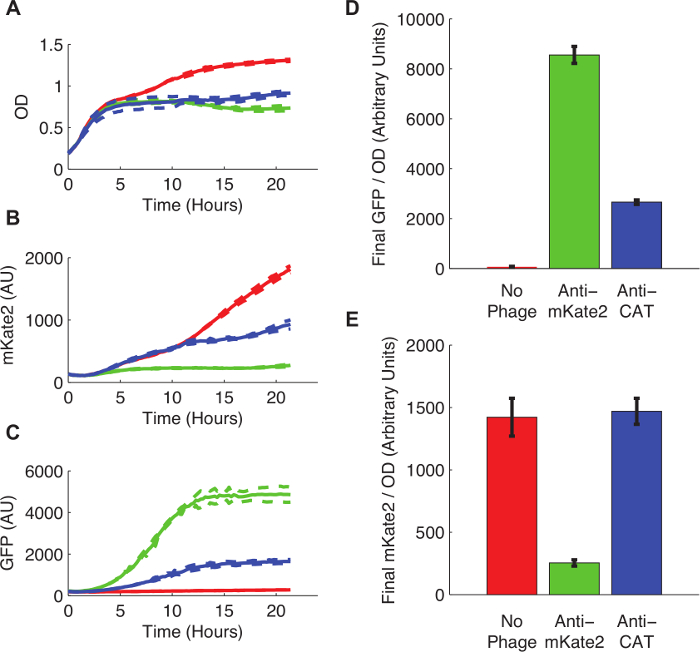
図3:K染色体に組み込まれmKate2蛍光レポーターのnockdown。E. mKate2を発現している大腸菌 MG1655 K12は、未処理(赤色の線やバー)左抗mKate2ファージミド(緑色の線やバー)に感染し、またはCAT(青い線やバー)を標的と対照ファージミドを感染させたいずれかでした。 (A)未処理E.大腸菌は、ファージ感染への代謝コストを示す、より高い飽和密度まで成長しました。点線は3反復の標準偏差を示します。 (B)mKate2信号抗mKate2近バックグラウンドレベルに低下したのではなく、コントロール株で、歪みを処理しました。また、ファージミドによって運ば(C)GFP蛍光は、わずかファージミド処置コントロールで検出可能でした。 (D、E)の最終蛍光読み取り成長の24時間は、ODに標準化した後。 GFPシグナルは、ファージミドの感染を示す、未処理の対照には存在しなかったが、また、実質的に抗CAT pを以下に低減しますhagemid治療。これは、ファージミドのオフターゲット効果を示すことができます。 mKate2信号は、未処理対照と比較して、抗mKate2ファージミド処理により減少しました。 CAT-制御目標ファージミドはmKate2の蛍光に対する効果を示しませんでした。エラーバーは3反復の標準偏差を表す。 この図の拡大版をご覧になるにはこちらをクリックしてください。
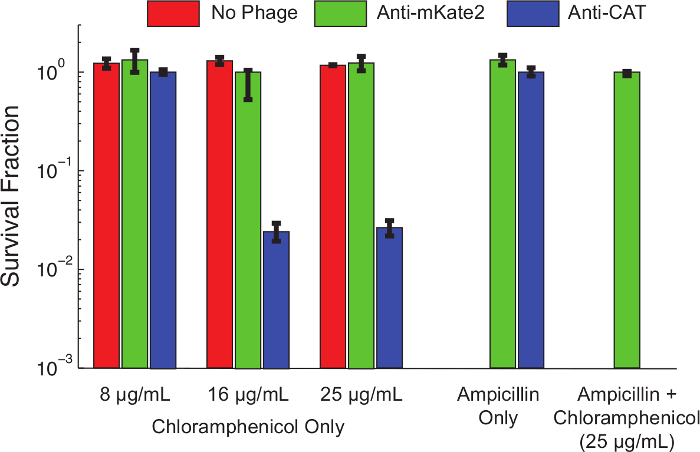
図4:CATのノックダウンは、遺伝的に耐性人口にクロラムフェニコール感受性を復元E.。染色体に統合されたCAT遺伝子を発現する大腸菌 MG1655 K12はmKate2(緑のバー)を標的とする対照ファージミドで処理した未処理(赤色バー)、左、または抗CATのsRNA(青いバー)を発現するファージミドを用いて処理しました。感染の1時間後、指示されたアリ上の生存率ibioticsは段階希釈およびプレーティングすることによって評価しました。対照処理は影響を受けなかった一方で抗CATミドで処理された株が大幅に、より高い濃度でクロラムフェニコールにより(> 90%)を殺害しました。培養プレートにアンピシリンを追加すると、積極ファージミド感染のために選択し、非感染細胞を排除します。これらの条件下では、何のクロラムフェニコール耐性コロニーを、抗CAT処置後に観察されませんでした。これは、ほとんどの生存者が感染の故障ではなく、サイレンシングの失敗を表していることを示しています。エラーバーは3反復の標準偏差を表す。 この図の拡大版をご覧になるにはこちらをクリックしてください。
| CAT標的配列 | 5 ' - ATGGAGAAAAAAATCACTGGATAT - 3' |
| CATのガイド配列 | 5 ' - ATATCCAGTGATTTTTTTCTCCAT - 3' |
表1:CAT遺伝子のための例示TARGETとガイド配列は、逆相補関係に注意してください。
| PRプロモーター | TAACACCGTGCGTGTTGACTATTTTACCTCTGGCGGTGATAATGGTTGC | ||||
| ガイド配列 | ATATCCAGTGATTTTTTTCTCCAT | ||||
| HFQ結合ドメイン | TTTCTGTTGGGCCATTGCATTGCCACTGATTTTCCAACATATAAAAAGACAAGCCCGAACAGTCGTCCGGGCTTTTTT TCTCGAG | ||||
| T1 / TEターミネーター | CTCGAGCCAGGCATCAAATAAAACGAAAGGCTCAGTCGAAAGACTGGGCCTTTCGTTTTATCTGTTTTTGTCGGTGAA CGCTCTCTACTAGAGTCACACTGGCTCACCTTCGGGTGGGCCTTTCTGCGTTTATA | ||||
表2:のsRNAカセットのシーケンス成分それぞれの配列は、5'-3 'に書き込まれます。完全なカセットがために、これらの4つの要素を連結したものですと292塩基対を含みます。
| フォワードプライマー | 5 ' - CTGGCGGTGATAATGGTTGC [GUIDE] TTTCTGTTGGGCCATTGC - 3' |
| リバースプライマー | 5 ' - GCAATGGCCCAACAGAAA [TARGET] GCAACCATTATCACCGCCAG - 3' |
表3:プライマーの設計既存のガイド要素を変更するためのフォワードプライマーは、PRプロモーターの最後の20bp、新しいガイド配列、およびHFQ結合ドメインの最初の18塩基対を含んでいます。標的配列は、ガイド配列の正確な逆相補体です。逆方向プライマーは、フォワードプライマーの正確な逆相補体です。
表4:シングルプライマー突然変異誘発PCRの推奨条件。
| ステップ | 一時 | 時間 |
| 最初の変性 | 98°C | 30秒 |
| 30サイクル | 98°C | 10秒 |
| 55°C | 30秒 | |
| 72°C | 120秒 | |
| 最終的な拡張 | 72°C | 300秒 |
| ストレージ | 10°C |
表5:シングルプライマー突然変異誘発PCRのためにサーモプロトコル推奨。
| 成分 | ボリューム |
| テンプレートDNA | 1μlの |
| 10μMのフォワードプライマー | 0.5μlの |
| 10μMのリバースプライマー | 0.5μlの |
| Taq 2Xマスターミックス | 25μlの |
| ヌクレアーゼフリーウォートR | 23μlの |
| 全容積 | 50μlの |
表6:シーケンスの検証PCRの推奨条件。
| ステップ | 一時 | 時間 |
| 最初の変性 | 95°C | 30秒 |
| 30サイクル | 95°C | 30秒 |
| 55°C | 30秒 | |
| 68°C | 30秒 | |
| 最終的な拡張 | 68°C | 300秒 |
| ストレージ | 10°C |
表7:推奨サーモプロシーケンス検証PCR用トコール。
本発明の方法は、非標的対照と比較してmKateの蛍光レベルで80%の削減を達成しました。これは完全なサイレンシングが観察され、百分の50から90の効率が16,17典型的であるされていない他のRNAノックダウンの方法、に沿ったものです。表現型レベルでは、CAT-標的ノックダウンは著しくクロラムフェニコール耐性を減衰し、いくつかの条件の下でそれを除去することができました。
ノックダウン表現型はわずか数時間後に感染( 図3B)の後に集団レベルで検出可能でした。これは、ファージに基づく配信の重要な特徴を示しています。高いノックダウン周波数は、従来、遺伝子改変することなく、バッチ培養で直接得ることができます。プラスミド形質転換またはゲノム統合を用いた従来の遺伝的修飾とは異なり、ファージ感染は、人口が単一の孤立コロニーから再成長されることを必要としません。これは、ファージ感染の影響がEXPLORにすることができます18、または遺伝的に混合自然集団19におけるバイオフィルムのような既存の空間構造を持つ複雑な空間ダイナミクス11、と集団で編。
この方法における重要なステップは、高力価でパッケージ化されたファージミドの製造です。ファージ粒子の生産に関連する代謝負担がファージミド生産菌株における突然変異またはプラスミドの損失率の高さにつながる可能性があります。ファージミド生産菌株は、単一の同時形質転換コロニーから直接培養し、冷蔵ではない、凍結またはファージ収穫前に継代培養することをお勧めします。 E.にファージミドおよびヘルパープラスミドを導入する際に同時形質転換の効率が低いことも観察することができます同時に大腸菌 。この場合には、より高い効率が次にファージミドを用いたその後の形質転換のためのヘルパープラスミドを有するコンピテント細胞を調製し、第1のヘルパープラスミドを形質転換することにより得ることができます。
PHAgemid感染またはのsRNA発現はまた、標的細胞上の検出可能な代謝負担を課し、そしていくつかの表現型の摂動をもたらすことができます。例えば、mKate2蛍光の減少は、細胞はCAT( 図3)を標的とファージミドを感染させた場合にも観察されました。 M13での感染は、Eにおける全身ストレス反応を誘発すると考えられていません20 コリが、間接的に転写パターンを変更することができます。代わりに、ファージミドに含まれるGFPまたはアンピシリン耐性マーカーはmKate2発現と成長9を軽減、携帯リソースの競合があります。最後に、のsRNAカセット自体がグローバルHFQタンパク質を滴定することによって遺伝子発現プロファイルを変更、またはオフ標的mRNAサイレンシングを介してあります。オフターゲット効果は、in vivoでのRNAi 21-23を標的化するのに共通しているが、彼 らは体系的に、このシステムのために調査するには至っていません。
この方法の1つの制限は、感染EFFIということですciencyは、いくつかの非感染細菌の集団に固執することができ、100%未満です。この作業の結果とそれ以前の作品10は、非感染細胞は、最終的な人口の1から10パーセントを表していることを示唆し、観察nonsilenced表現型のほとんどを担っています。 M13-抵抗への経路の様々な線毛式24の最も一般的な突然変異の損失で、知られています。これらの制限を考慮して、コントロールが高い感染率とノックダウン効率を確認するために使用されるべきです。
いくつかのアプリケーションのための別の潜在的な制限は、ヘルパーファージを汚染時折転送です。 M13K07は、突然変異したパッケージングシグナルを含んでいますが、それは、ファージ生産と最初の感染イベント25を超えたファージの継続的な普及のためのコンピテントセルで、その結果、低周波数でのファージキャプシド中にパッケージングし、感染した集団に転送することができます。ヘルパーファージへの変更が有効であることが判明しました減少したファージ生産26の費用であるが、時には、非特異的なパッケージングを減らすことで。
操作されたバクテリオファージは、Eのための必要不可欠なツールとなっています人口増加への新しい遺伝子の迅速な配信を可能にする大腸菌合成生物学、。最近の研究では、27を経路抗生物質耐性を抑制するために細胞間通信回路11または発現された転写因子を生産しています。ここで紹介するプロトコルは、プログラムされたRNAを介して細菌生理学の制御を可能にするツールの成長のコレクションに追加されます。ヌクレアーゼ活性を排除するために変異したときCRISPR-CASヌクレアーゼは、RNA誘導型遺伝子標的17,28で転写を抑制することが示されています。これとは対照的に、のsRNAサイレンシングは、翻訳レベルで動作し、外因性タンパク質の発現を必要としません。次世代バイオテクノロジーは、複雑なフェノをプログラムするために、ファージ媒介送達での転写および翻訳制御を団結させることができますリアルタイムでタイプ。
The authors have nothing to disclose.
この仕事のための資金は、パリベッテンコートIGEMチームのサポートに財団ベッテンコートシュエーラーによって提供されました。我々は、技術支援やアドバイスをINSERM U1001研究ユニットとシャンタルLottonに感謝します。ファージミドLitmus28i_J23115-B0032-GFPは、モニカ・オルティスとスタンフォード大学のドリューENDYによって提供されました。
| Name | Company | Catalog Number | Comments |
| Plasmid Miniprep Kit | Qiagen | 27104 | |
| DpnI Enzyme | NEB | R0176S | |
| Phusion High Fidelity Polymerase | NEB | M0530S | |
| Taq 2x Master Mix | NEB | M0270L | |
| M13KO7 Helper Phage | NEB | N0315S | |
| DH5α Competent Cells | Life Technologies | 18265-017 | |
| TOP10F' Cells | Life Technologies | C3030-03 | |
| LB Broth | Sigma | L3022-250G | |
| Ampicillin | Sigma | A9393-5G | |
| Kanamycin | Sigma | 60615-5G | |
| Chloramphenicol | Sigma | C0378-5G | |
| Tetracycline | Sigma | 87128-25G |
- Ohkumo, T., Masutani, C., Eki, T., Hanaoka, F. Use of RNAi in C. elegans. RNAi. , 129-137 (2008).
- Fire, A., Xu, S., Montgomery, M. K., Kostas, S. A., Driver, S. E., Mello, C. C. Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans. Nature. 391 (6669), 806-811 (1998).
- Iordanou, E., Chandran, R. R., Blackstone, N., Jiang, L. RNAi interference by dsRNA injection into Drosophila embryos. J Vis Exp. (50), e2477 (2011).
- Ramadan, N., Flockhart, I., Booker, M., Perrimon, N., Mathey-Prevot, B. Design and implementation of high-throughput RNAi screens in cultured Drosophila cells. Nat Protoc. 2 (9), 2245-2264 (2007).
- Tsong, T. Y. Electroporation of cell membranes. Biophys J. 60 (2), 297-306 (1991).
- Kim, W. J., Chang, C. -. W., Lee, M., Kim, S. W. Efficient siRNA delivery using water soluble lipopolymer for anti-angiogenic gene therapy. J Control Release. 118 (3), 357-363 (2007).
- Shi, Y. Mammalian RNAi for the masses. Trends Genet. 19 (1), 9-12 (2003).
- Na, D., Yoo, S. M., Chung, H., Park, H., Park, J. H., Lee, S. Y. Metabolic engineering of Escherichia coli using synthetic small regulatory RNAs. Nat Biotechnol. 31 (2), 170-174 (2013).
- Ceroni, F., Algar, R., Stan, G. -. B., Ellis, T. Quantifying cellular capacity identifies gene expression designs with reduced burden. Nat Methods. 12 (5), 415-418 (2015).
- Libis, V. K., Bernheim, A. G., et al. Silencing of Antibiotic Resistance in E. coli with Engineered Phage Bearing Small Regulatory RNAs. ACS Synth Biol. 3 (12), 1003-1006 (2014).
- Ortiz, M. E., Endy, D. Engineered cell-cell communication via DNA messaging. J Biol Eng. 6 (1), 16 (2012).
- Edelheit, O., Hanukoglu, A., Hanukoglu, I. Simple and efficient site-directed mutagenesis using two single-primer reactions in parallel to generate mutants for protein structure-function studies. BMC Biotechnol. 9 (1), 61 (2009).
- Chung, C. T., Miller, R. H. Preparation and storage of competent Escherichia coli cells. Recombinant DNA Part I. , 621-627 (1993).
- Phornphisutthimas, S., Thamchaipenet, A., Panijpan, B. Conjugation in Escherichia coli. Biochem Mol Biol Educ. 35 (6), 440-445 (2007).
- Sezonov, G., Joseleau-Petit, D., D'Ari, R. Escherichia coli Physiology in Luria-Bertani Broth. J Bacteriol. 189 (23), 8746-8749 (2007).
- Mittal, V. Improving the efficiency of RNA interference in mammals. Nat Rev Genet. 5 (5), 355-365 (2004).
- Qi, L. S., Larson, M. H., et al. Repurposing CRISPR as an RNA-guided platform for sequence-specific control of gene expression. Cell. 152 (5), 1173-1183 (2013).
- Lu, T. K., Collins, J. J. Dispersing biofilms with engineered enzymatic bacteriophage. Proc Natl Acad Sci USA. 104 (27), 11197-11202 (2007).
- Yosef, I., Manor, M., Kiro, R., Qimron, U. Temperate and lytic bacteriophages programmed to sensitize and kill antibiotic-resistant bacteria. Proc Natl Acad Sci USA. 112 (23), 7267-7272 (2015).
- Karlsson, F., Malmborg-Hager, A. -. C., Albrekt, A. -. S., Borrebaeck, C. A. K. Genome-wide comparison of phage M13-infected vs. uninfected Escherichia coli. Can J Microbiol. 51 (1), 29-35 (2005).
- Senthil-Kumar, M., Mysore, K. S. Caveat of RNAi in plants: the off-target effect. Methods in molecular biology. 744, 13-25 (2011).
- Jackson, A. L., Linsley, P. S. Recognizing and avoiding siRNA off-target effects for target identification and therapeutic application. Nat Rev Drug Discov. 9 (1), 57-67 (2010).
- Cho, S. W., Kim, S., et al. Analysis of off-target effects of CRISPR/Cas-derived RNA-guided endonucleases and nickases. Genome Res. 24 (1), 132-141 (2014).
- Hagens, S., Blasi, U. Genetically modified filamentous phage as bactericidal agents: a pilot study. Lett Appl Microbiol. 37 (4), 318-323 (2003).
- Kasman, L. M., Kasman, A., Westwater, C., Dolan, J., Schmidt, M. G., Norris, J. S. Overcoming the phage replication threshold: a mathematical model with implications for phage therapy. J Virol. 76 (11), 5557-5564 (2002).
- Chasteen, L., Ayriss, J., Pavlik, P., Bradbury, A. R. M. Eliminating helper phage from phage display. Nucleic Acids Res. 34 (21), e145 (2006).
- Lu, T. K., Collins, J. J. Engineered bacteriophage targeting gene networks as adjuvants for antibiotic therapy. Proc Natl Acad Sci USA. 106 (12), 4629-4634 (2009).
- Bikard, D., Jiang, W., Samai, P., Hochschild, A., Zhang, F., Marraffini, L. A. Programmable repression and activation of bacterial gene expression using an engineered CRISPR-Cas system. Nucleic Acids Res. 41 (15), 7429-7437 (2013).
Tags
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved