Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Immunology and Infection
Visualisering af trækul Agar Resazurin Assay til Semi-kvantitativ, Medium-throughput Tælling af mykobakterier
The charcoal agar resazurin assay (CARA) is a semi-quantitative, medium-throughput method to assess activity of test agents against mycobacteria that are replicating, non-replicating, or both. The CARA permits rapid evaluation of time- and concentration-dependent activity and identifies parameters to pursue by colony forming unit (CFU) assays.
Der er et presserende behov for at opdage og fremskridt antiinfektionsmidler der forkorter varigheden af tuberkulose (TB) behandling. Mycobacterium tuberculosis, det ætiologiske agens for tuberkulose, er refraktære over for hurtig og varig kemoterapi på grund af tilstedeværelsen af baciller, der udviser fænotypisk resistens. Den c harcoal en gar r esazurin en ssay (CARA) blev udviklet som et redskab til at karakterisere aktive molekyler opdaget af high-throughput screening kampagner mod at kopiere og ikke-replikerende M. tuberculosis. Inddragelse af aktivt kul i bakteriologisk agar medium hjælper afbøde virkningerne af forbindelsen fremførsel, og fjerner kravet om at pre-fortynde celler før spotting på CARA mikroplader. Efter en 7-10 dages inkubationsperiode ved 37 ° C, reduktion af resazurin af mycobakterielle mikrokolonier vokser på overfladen af CARA mikropladebrøndene tillader semikvantitativ assessment af bakterieantal via fluorometri. Den CARA registrerer cirka en 2-3 log 10 forskel i antallet af bakterier og forudser en minimal baktericid koncentration fører til ≥99% bakteriel kill (MBC ≥99). CARA hjælper med at afgøre, om et molekyle er aktiv på baciller, der er replikerende, ikke-replikerende, eller begge dele. Pilot eksperimenter ved hjælp af CARA lette identifikationen af hvilken koncentration af test agent og tidspunkt for sammensatte eksponering kræver yderligere evaluering af kolonidannende enhed (CFU) analyser. Desuden kan CARA forudsige, om replikerende aktive er baktericide eller bakteriostatiske.
Mycobacterium tuberculosis, det ætiologiske agens for tuberkulose, kan overleve i en vært i en latent tilstand, der er refraktære over for antibiotika udryddelse. Fænotypisk (ikke-genetiske) modstand fra M. tuberculosis under infektion menes at skyldes til dels, at populationer af ikke-replikerende bacilli 1,2. Klasse I persisters viser fænotypisk resistens opstår via sjældne stokastiske mekanismer blandt store bestande af narkotika sensitive celler 3,4. Klasse II persisters er gjort ikke-replikerende med faktorer på vært immunitet, herunder eksterne spændinger i mikromiljøer opstået under infektion. Vi har for nylig udviklet en in vitro model af klasse II ikke-replikerende vedholdenhed at efterligne betingelser konfronteret med M. tuberculosis i aktiverede makrofager og granulomer. Den multi-stress model af klasse II vedholdenhed omfatter betingelser, at langsom vækst, såsom en fedtsyre kulstofkilde, og helt halt vækst, såsom mild surhedsgrad (pH 5,0), hypoxi (1% O 2), nitrogenoxid og andre reaktive kvælstof mellemprodukter 5-9. Storstilet screening ansætte denne multi-stress model af ikke-replikation og andre klasse II ikke-replikerende modeller, har givet forskellige molekyler, hvis aktivitet er rettet mod ikke-replikerende tilstand 5-7,9-18. De samme ikke-replikerende skærme afslørede også en kategori af molekyler, der besidder aktivitet over for både replikerende og ikke-replikerende baciller, betegnes "dobbelt aktive" 7,10,12,19,20.
Antibakteriel lægemiddelforskning i hit-til-lead fase indebærer omfattende karakterisering af kandidat molekyler til at vælge kundeemner til hit ekspansion, foreløbig farmakologiske karakterisering, target identifikation, og de foreløbige in vivo undersøgelser af effekten. Som et første skridt, er anti-infektiøse klassificeret efter deres bakteriostatisk eller baktericidt virkningsmekanisme og hvis bakteriedræbende, whether bakteriel drab er tids- og / eller koncentrationsafhængig. Den kolonidannende enhed (CFU) assay er den klassiske, guld standardmetode at behandle disse spørgsmål. I CFU-assayet, er bakterier udsættes for et testmiddel, hvorefter aliquoter fjernet, serielt fortyndet, og alikvoter af fortyndinger spredes på fast bakteriologisk medium og inkuberet til at tillade væksten af overlevende celler. Endelig er bakteriekolonier optalt. Den CFU-assayet kræver store antal af mikrotiterplader til fortynding celler og agar-indeholdende Petri-plader for at optælle overlevende kolonier. CFU assay for langsomt voksende mykobakterier er hæmmet af deres langsomme generationstid (18-24 timer), hvilket kræver ca. 3 uger for kolonier vises på plader. Desuden er inkubator plads ofte begrænset i specialiserede biosikkerhed-niveau-3 anlæg.
Mens besværlige, CFU-analyser er den gyldne standard til at karakterisere effekten af ikke-replikerende og dual-aktive molekyler på mycobacteria. Ikke-replikerende analyser er underlagt høje falsk-positive satser så mange er koblet til replikere assays til vurdering cellulær levedygtighed 6-8. For eksempel kan en forbindelse, der har potent aktivitet mod replikerende M. tuberculosis (en "replikerende aktiv"), kan ikke dræbe i ikke-replikerende assay, men kan stadig dræbe i kraft af overførsel fra den ikke-replikerende fase af assay til inddrivelse fase af analysen, der udføres under forhold, der understøtter replikation ( "replikering betingelser"). Forbindelse fremførsel yderligere komplicerer analysen af to aktive molekyler, hvilket gør det vanskeligt at skelne, om aktiviteten blev replikerende, ikke-replikerende, eller dual.
For at løse de problemer, der er beskrevet ovenfor, vi udviklede c harcoal en gar r esazurin en ssay (CARA) til hurtig, semikvantitativ tælling af mycobakterielle arter såsom M. tuberculOSIS, M. bovis BCG og M. smegmatis 7 (figur 1 og 2). I pufferopløsninger in vitro, aktiveret kul afsondrer hurtigt fleste standard lægemidler, der anvendes til behandling af tuberkulose 7. Aktivt kul i CARA mikroplader binder forbindelser, der kan bære over et assay mikroplade, og dette træk ved CARA fjerner kravet til serielt fortynde assay brøndindholdet før tælling 7,21,22. Antallet af mycobakterielle mikrokolonier på agaroverfladen af CARA mikroplader skønnes ved tilsætning af resazurin, et blåt farvestof, hvis reducerede form resorufin, er en lyserød molekyle, hvis fluorescens måles med en spektrofotometri 23. CARA mikroplader inkuberes i 1-2 dage for M. smegmatis og 7-10 dage for langsomt voksende mycobakterier såsom M. tuberculosis og M. bovis BCG. Den CARA har et smalt dynamikområde på ~ 2-3 log 10 diffeærbødighed i CFU. Når det bruges i stedet for en CFU-assay, et enkelt CARA mikroplade erstatter ca. fem plader med 96 brønde anvendes til serielle fortyndinger og 120 tri-stil agarplader anvendes til plettering. Fortolkning af Cara data hjælper vejlede efterfølgende studier ved at bestemme hvilken inkubation tider og sammensatte koncentrationer for at teste i mere besværlige CFU-baserede analyser.
1. Fremstilling af CARA mikroplader
- Autoclave 900 ml Middlebrook 7H11 agar indeholdende 0,2% glycerol og 0,4% aktivt kul i en 2 L Erlenmeyer-kolbe, eller alternativt 450 ml i en 1 L bægerglas. Medtag en stor autoklaverbar omrører i kolben eller bæger. Dæk åbningen af kolben eller bægeret med aluminiumsfolie og tillægger glas med autoklave tape.
- Cool at røre (ca. 55-65 ° C) på en magnetomrører indstillet til en lav hastighed for at opretholde trækul i suspension.
- Udføre alle efterfølgende trin aseptisk i et bio hætte, der har en magnetomrører.
- Fjern folie. Tilsæt 100 ml OADC-supplement (OADC supplement, når de anvendes ved 10%, udbytte endelige koncentrationer på 0,2% dextrose, 0,5% albumin, 0,085% NaCl, 0,0005% oliesyre og 0,4 mg / ml catalase medier) til 2 L Erlenmeyer-kolbe eller 50 ml OADC til 1 L bægerglas, og fortsæt opblanding.
- Hvis du bruger en Erlenmeyerkolbe, hæld ca. 25-40 ml 7H11-OADC-trækul i en steril reagens reservoir. Hvis der anvendes bægeret, er det ikke nødvendigt at anvende et reagens reservoir.
- Fyld en 96-brønds mikroplade med 200 pl / brønd af 7H11-OADC-trækul fra reagenset reservoir eller bægerglas. Arbejde hurtigt for at undgå agar størkning og indførelse af bobler. Undgå sprøjt fast medium uden for brøndene, som kan være en kilde til svampeangreb. Ved hjælp af en multikanal pipette, bruge et sæt af 12 filter tips til overførsel af 7H11-OADC-trækul til de 8 rækker (AH) af 96 brønde.
BEMÆRK: Mediet størkner hurtigt. For at undgå tilstopning pipettespidser, ændre dem ofte. - Alternativt, hæld CARA mikroplader bruge en P1000 elektronisk multikanal pipette med filter tips til at hjælpe med at forberede en lang række plader.
BEMÆRK: På grund af den lave volumen af mikropladebrøndene, agar i CARA mikroplader størkner i løbet af minutter hælde. - Place stakke af CARA mikroplader i genlukkelige plast bags for at undgå udtørring.
- Store CARA mikroplader ved 4 ° C.
2. Opsætning Replikering og ikke-replikerende MIC 90 Analyser
- Podes M. tuberculosis, M. bovis BCG eller M. smegmatis ved en OD 580 af 0,01-0,1 og udvide til midt-log-fase (OD 580 ~ 0,5) i Middlebrook 7H9-ADN (Middlebrook 7H9 indeholdende 0,2% glycerol, 0,2% dextrose , 0,5% albumin, og 0,085% NaCl) eller 7H9-OADC (Middlebrook 7H9 indeholdende 0,2% glycerol og 10% OADC supplement).
- Grow M. tuberculosis og M. bovis BCG som ~ 20 ml stående kulturer i celle kultur flasker og M. smegmatis med rystning i polypropylen rundbundet (4 ml kultur) eller 50 ml koniske centrifugerør (10-20 ml kultur). Inkuber patogene mycobakterier ved 37 ° C med 20% O2 og 5% CO2, og M. smegmatis ved 37 ° C med 20% O2.
- Opsæt en minimal-hæmmendekoncentration (MIC 90) -stil eksperiment under replikerende og ikke-replikerende betingelser (figur 2).
BEMÆRK: testmidler sædvanligvis analyseret i duplikater eller firdobbelte at tillade test 4, eller 2 forbindelser henholdsvis pr 96-brønds mikroplade. For eksempel i en plade med 96 brønde, én testmiddel kan analyseres i rækker AD og en anden i rækker EH. Den DMSO (køretøj) er i kolonne 1, 2 og 12, og testen agent fortyndingsrække løber fra kolonne 3 (laveste koncentration) til kolonne 11 (højeste koncentration). MIC 90 -stil assays anvender typisk 2-fold fortyndingsrække. Der er mange ikke-replikerende modeller til rådighed for mykobakterier 14-16,18,24,25 og til illustrative formål, bruger vi en multi-stress model af ikke-replikation 6,8,9.- For replikerende assayet, distribuere 200 pi celler i 7H9-ADN ved en OD 580 på 0,01 i alle hullerne på en klar bund, vævskulturbehandlet 96-brønds plade. <li> For de ikke-replikerende assay vaskes celler to gange i phosphatbufret saltvand (PBS) indeholdende 0,02% tyloxapol, og resuspender celler i ikke-replikerende medium (0,05% KH 2 PO 4, 0,05% MgSO4, 0,005% ferriammoniumcitrat , 0,0001% ZnCl2, 0,1% NH4Cl, 0,5% BSA, 0,085% NaCl, 0,02% tyloxapol, 0,05% butyrat; pH justeret til 5,0 med 2 N NaOH).
- Fortynd celler til en OD 580 på 0,1 i ikke-replikerende medium og tilsæt NaNO2 fra en frisk fremstillet 1 M stamopløsning til en slutkoncentration på 0,5 mM.
- Fordel 200 pi celler ved en OD 580 på 0,1 i alle hullerne på en klar bund, vævskulturbehandlet 96-brønds plade.
BEMÆRK: fremstilling af forbindelse fortyndinger som 100-fold stamopløsninger i DMSO. Således er en typisk MIC plade at afprøve virkningen af et molekyle i en slutkoncentration 0,4-100 ug / ml ville kræve stamopløsninger af 0,04-10 mg / ml i DMSO.
- Tilsæt 2 pi dilutions af test agent 1 i rækkerne AE og 2 pi fortyndinger af test agent 2 i rækker EH. Bland grundigt.
- Tilsæt 2 pi vehikelkontrol (sædvanligvis DMSO) i kontrolbrønde, kolonne 1, 2, 12 (rækker Ah). Bland grundigt.
- For hvert eksperiment, omfatte mindst én positiv kontrol såsom rifampicin fra 0,004 til 1 ug / ml (replikerende assay) og / eller 0,08 til 20 ug / ml (ikke-replikerende assay).
BEMÆRK: Anvendelse af 6-brom-1H-indazol-3-amin 9 ved 0,1 til 25 ug / ml anbefales som en kontrol forbindelse, der har selektiv, NaNO2 -afhængige aktivitet i multi-stress model af ikke-replikation. - For replikerende assays inkuberes mikroplader ved 37 ° C ved 20% O2 og 5% CO2 i 7 dage (M. tuberculosis og M. bovis BCG) eller 1-48 timer (M. smegmatis). For multi-stress model af ikke-replikation, inkuberes mikroplader i 7 dage ved 37 ° C ved 1% O2 og 5% CO2 (<em> M. tuberkulose og M. bovis BCG).
3. Podning af CARA mikroplader
- På tidspunkter, hvor CARA vil blive anvendt som en udlæsning, omhyggeligt resuspender godt indhold MIC 90-stil assayplade anvendelse af en p200 multikanalpipette sat til 50-75 pi. Pipette op og ned mindst 5-10 gange og forsigtigt swirl de godt indhold i en cirkulær bevægelse ved hjælp af pipettespidser.
- Overfør 10 pi assay godt indhold til CARA mikropladen. Sørg for, at rækkefølgen af godt indhold på assaypladen matcher rækkefølgen af såvel indholdet af CARA mikropladen. Undgå stænk i overførslerne, og sørg de 10 pi er plettet i midten af CARA mikropladebrøndene. Bekræft 10 pi absorberer ind i CARA mikropladen.
BEMÆRK: Der er ingen fortyndinger kræves forud for spotting celler på CARA mikroplader. - Bind stakke af CARA mikroplader med plade tape ogderefter anbringes i en genlukkelig plasticpose. Inkuber CARA mikroplader ved 37 ° C med 20% O2 (M. smegmatis) eller 1% O2 og 5% CO2 (M. tuberculosis og M. bovis BCG).
- For M. tuberculosis og M. bovis BCG, replikerende analyser: inkuberes i 7 dage; for M. tuberculosis og M. bovis BCG ikke-replikerende assays, inkuberes i 10 dage; for M. smegmatis, replikerende analyser, inkuberes i 1-2 dage; for M. smegmatis, ikke-replikerende analyser, inkuberes 2-3 dage.
BEMÆRK: Times er skøn og kan ændres i overensstemmelse hermed for forskellige replikerende, ikke-replikerende, og stress betingelser.
4. Udvikling CARA mikroplader
- Udvikle CARA mikroplader når en film af bakterievækst, eller større, makroskopiske kolonier, er synlige på de negative (køretøj) kontrolbrønde.
BEMÆRK: Efter længere tids inkubation CARA mikropladebrøndene oftesynes tørt og vi anbefaler forudgående befugtning godt indhold med sterilt PBS. Dette tjener til at forhindre, at trækul fra absorbere resazurin, hvilket kan føre til lav fluorescens eller brønd-til-brønd variation. - Anvendelse af et enkelt sæt af 12 P200 tips med en multikanalpipette, dispensere 40 pi sterilt PBS langs siden af brøndene og lade PBS at fordele hen over toppen af de agar / bakterielle mikrokolonier.
- Forbered CARA fremkaldelsesreagens ved blanding 5 mg resazurin (0,01% endelig) og 50 ml 5% Tween80 i PBS. Vortex og sterilt filter.
BEMÆRK: En alternativ CARA fremkaldelsesreagens kan fremstilles ved at blande kommercielt tilberedt resazurin flydende opløsning ved 1: 1 (vol / vol) med 10% Tween80 i PBS. - Der tilsættes 50 pi frisk fremstillet CARA fremkaldelsesreagens til hver brønd af Cara mikroplade med en 12-kanals pipette. Rock plader frem og tilbage et par gange for at hjælpe distribuere reagens tværs af agar og bakterielle mat i hver brønd.
- Placer pladerne ina genlukkelig plasticpose og inkuberes ved 37 ° C i mindst 30 min for M. smegmatis og 45-60 min for M. tuberculosis eller M. bovis BCG.
BEMÆRK: Hvis bilen kontrolbrønde udebliver lyserød inden for den første time, pladerne kan genbruges sække og inkuberes i længere perioder. - Før læsning fluorescens, placere CARA mikroplader i et biosikkerhed hætte i 15 minutter ved stuetemperatur med deres låg fjernet. Når du bruger BSL3 spektrofotometre uden for en biosikkerhed kabinet, overholde en optisk kvalitet PCR mærkat over pladen og slutter tæt ved at trykke forsigtigt på mærkaten overflade med en blød papirserviet.
- Bestem fluorescens via top læses med excitation ved 530 nm og emission ved 590 nm. Det er ikke nødvendigt at slukke pladen.
5. Data Analysis
- Plot inhibitorkoncentration på X-aksen på en log 10 skala og fluorescens på Y-aksen på en lineær skala. Brug en scatterplot ansætte en kurve passer som "log inhibitor versus respons-variabel hældning (4 parametre)". Plot datapunkter som betyder ± standardafvigelse.
Forventede CARA resultaterne er beskrevet i figur 2 og opsummeret i tabel 1. For replikerende celler er CARA løbe parallelt med en standard MIC 90 assays, og for ikke-replikerende assays er CARA løbe parallelt med en tilpasset MIC 90 assay, der er koblet til en udvækst fase. Koncentrationen af testmiddel, som resulterer i svigt i Cara-fluorescens til at stige over baggrundsniveauer er Cara-MBC ≥99 (figur 3a). Den "≥99" sænket angiver, at Cara-MBC giver en estimeret koncentration af test agent, der giver anledning til ≥2 log 10 bakteriel kill (≥99% kill).
Den flydende bouillon MIC 90 assay er ude af stand til at skelne mellem baktericid og bakteriostatisk aktivitet, og denne sondring skal løses ved en CFU-analysen. Vedkonvention, den tærskel, der adskiller baktericid fra bakteriostatisk aktivitet for langsomt voksende mykobakterier er ca. 2-3 log 10 kill over 7 dage 7,26. Da det dynamiske område af CARA er også 2-3 log 10 kill kan CARA give et skøn over baktericid eller bakteriostatisk aktivitet. Den CARA nemt identificerer nogle replikerende aktive som bakteriostatisk grund af svigt af disse forbindelser til at falde CARA fluorescens til baggrundsniveauer (figur 2). Men nogle forbindelser med bakteriostatisk aktivitet mod replikere M. tuberculosis har en potent post-antibiotisk effekt, hvilket betyder, at de fortsætter med at hæmme genvækst af bakterier i opsvingsfasen selv i fravær af forbindelse fremførsel. Denne effekt kan være svært at genkende i CARA-analysen. Forbindelser mistænkes for at udøve en post-antibiotisk effekt, hvis de udviser en "statisk vindue", defineret som en> 4-fold højredrejning between MIC og CARA kurver (figur 3b). Den statiske vindue angiver, at et molekyle aktive over replikerende M. tuberculosis kan være bakteriostatisk stedet for baktericid. I nogle tilfælde, de statiske windows er først efter inspektion af en udvidet Y-aksen for Cara fluorescens (figur 3c og 3d).
CARA og MIC 90 data er normalt afbildet sammen (figur 4). Repræsentative data for replicating- og ikke-replikerende-aktive molekyler testet af MIC 90 og CARA er vist i figur 4. Der er 4 store aktivitet klasser for molekyler: 1) replikerende bakteriedræbende (demonstreret med isoniazid, figur 4a); 2) replikerende bakteriostatisk (demonstreret med linezolid, figur 4b); 3) ikke-replikerende baktericide (demonstreret med oxyphenbutazon, figur 4c); og, 4) replicating-aktiv (bakteriostatisk eller baktericid) og ikke-replikerende baktericide (påvist med PA-824, figur 4d). Vigtigere, 4a og 4b viser, at mens isoniazid og linezolid synes at have aktivitet mod ikke-replikerende bakterier ved MIC 90 assay CARA antyder, at de er inaktive under de ikke-replikerende betingelser testet. For at teste anvendeligheden af Cara forudsige et molekyles tids- og koncentrationsafhængig virkning, replikerende M. smegmatis blev udsat for stigende koncentrationer af rifampicin (figur 5a - d), og på forskellige tidspunkter mellem 1-24 timer blev alikvoter plettet på CARA plader. Disse data indikerede, at rifampicin udøvede en virkning så tidligt som 1 time (figur 5a), vises stigende baktericid aktivitet mellem 3 og 24 timer (figur 5b-d), og dræbte ≥2-3 log10 ved ~ 10 pg / ml ved 24 timer (figur 5d). Et lignende eksperiment testning firdobbelte af en vehikelkontrol og 9 lægemiddelkoncentrationer, og ved 4 tidspunkter, ville være uoverkommelige ved en standard CFU-baseret assay.
, CARA har således en rolle i lægemiddelforskning som et medium-throughput, hurtig mekanisme til at identificere et molekyles aktivitet profil. CARA forudsigelser bør nøje evalueres ved hjælp af en standard CFU assay. Tilsætning af 0,4% aktivt kul til petriskåle til CFU analyse kan hjælpe med at forbedre korrelation til CARA data, og kan resultere i en mere præcis CFU tællinger, størrelsen af korrektionen generelt er proportional med forbindelsens styrke 21,22.
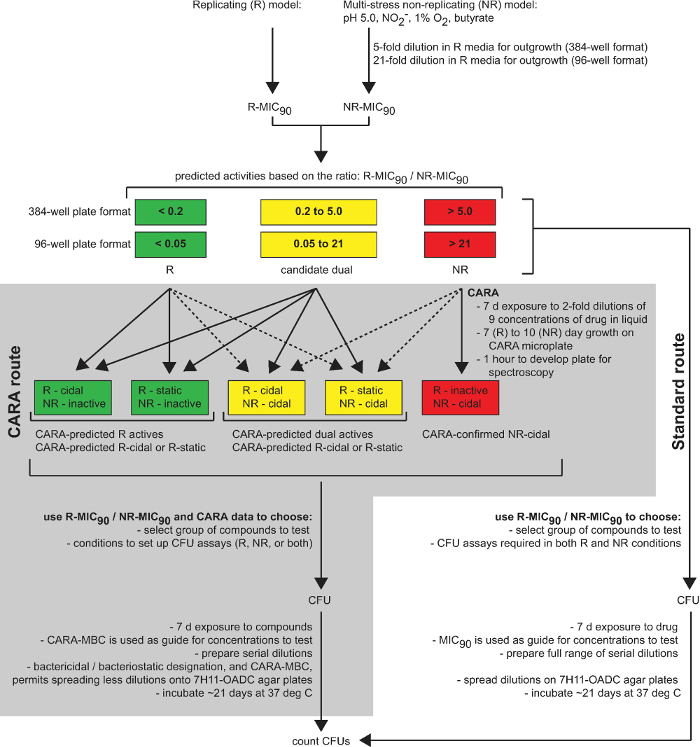
Figur 1: CARA er en prædiktiv redskab inden for lægemiddelforskning. Dette diagram opsummerer anvendeligheden af CARA som enmellemstadium mellem screening stof (enkelt punkt screening, cherry-picking, og dosis-respons-assays) og tidskrævende hit-til-lead assays (CFU-analyser og target identifikation). [Tilpasset med tilladelse fra Gold et al., Antimicrobial Agents and kemoterapi, 2015 7] Klik her for at se en større version af dette tal.
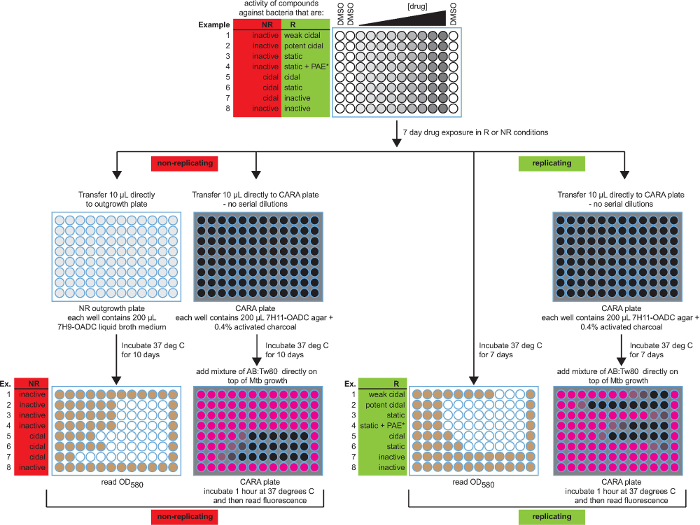
Figur 2: Skematisk af bouillon MIC 90 assay og CARA med forventede resultater. Både MIC 90 og CARA resultaterne præsenteres for 8 mulige aktiviteter. Den farvekodning til MIC 90 mikropladebrøndene er hvid (ingen vækst) og brun (vækst), og for CARA mikroplader er sort (ingen fluorescens) og pink (resorufin fluorescens). Dataene er hypotetiske. [Tilpasset med tilladelse fra Gold et al., Antimicrobial Agents and kemoterapi, 2015 7] Klik her for at se en større version af dette tal.
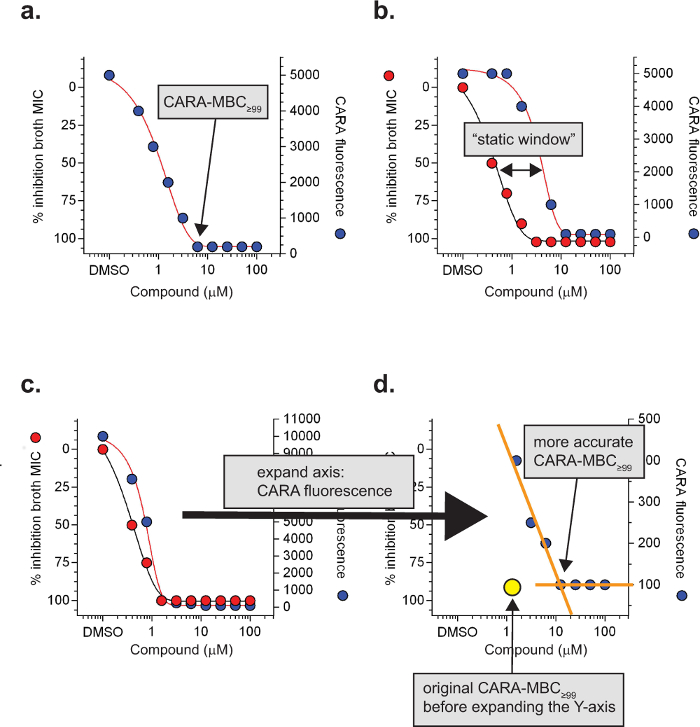
Figur 3: Specialiseret CARA begreber og definitioner. Den minimale baktericide koncentration af et molekyle der resulterer i baggrundsniveauer af CARA fluorescens er CARA-MBC ≥99 (a). Under replikerende betingelser, en ≥4 gange forskubning af Cara-MBC ≥99 til højre for MIC 90 indikerer ofte bakteriostatisk aktivitet og kaldes en "statisk vindue" (b). For molekyler med en potent post-antibiotisk effekt, kan statiske vinduer være vanskelig at observere (c) og kræverudvidelse af Y-aksen (CARA fluorescens) at visualisere (d). Dataene er hypotetiske. [Tilpasset med tilladelse fra Gold et al., Antimicrobial Agents and kemoterapi, 2015 7] Klik her for at se en større version af dette tal.
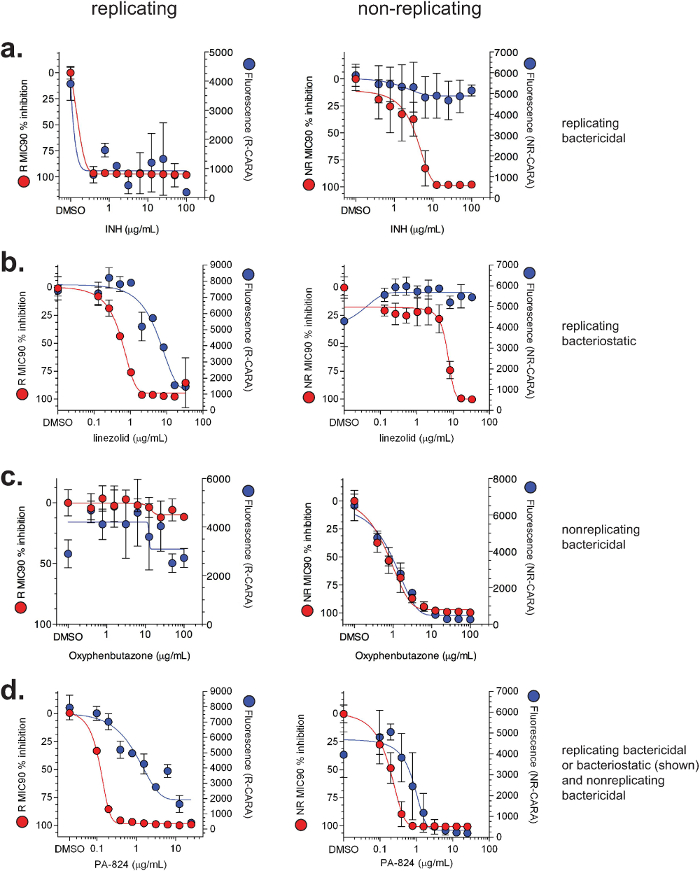
Figur 4: Illustrative MIC 90 og CARA resultater for udvalgte forbindelser. Data for MIC 90 (rød) og CARA (blå) er demonstreret for (a) isoniazid (INH), (b) linezolid, (c) oxyphenbutazon, og (d) PA-824. Vildtype M. tuberculosis H37Rv blev udsat for forbindelserne i 7 dage under standard replikerende betingelser eller multi-stress model af ikke-replikation 7-9. MIC 90 assays og CARA blev udført som vist i figur 2. [Tilpasset med tilladelse fra Gold et al., Antimicrobial Agents and kemoterapi, 20157]Klik her for at se en større version af dette tal.
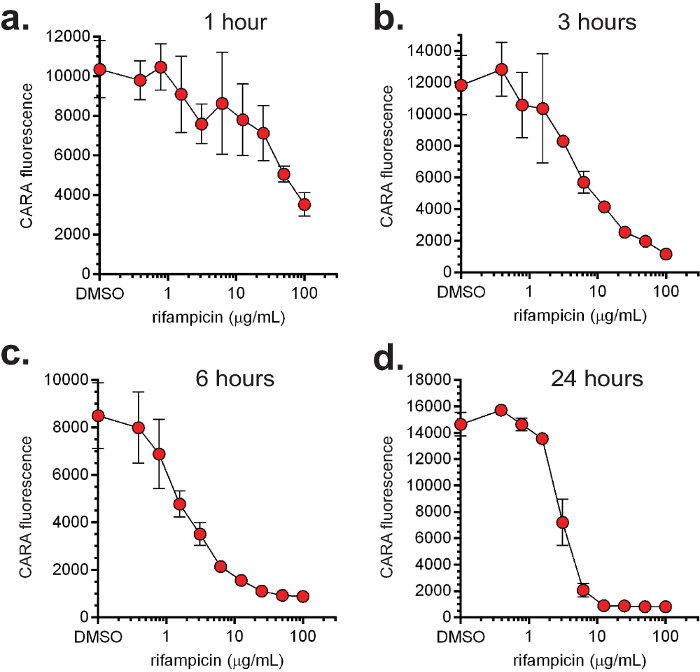
Figur 5: dosis- og tidsafhængig aktivitet af rifampicin. Den ikke-patogene, hurtigt voksende M. smegmatis blev udsat for stigende koncentrationer af rifampicin under replikerende betingelser og portioner blev udtaget til CARA ved 1 (a), 3 (b), 6 (c) og 24 (d) hr. [Tilpasset med tilladelse fra Gold et al., Antimicrobial Agents and kemoterapi, 2015 7].com / filer / ftp_upload / 54.690 / 54690fig5large.jpg "target =" _ blank "> Klik her for at se en større version af dette tal.
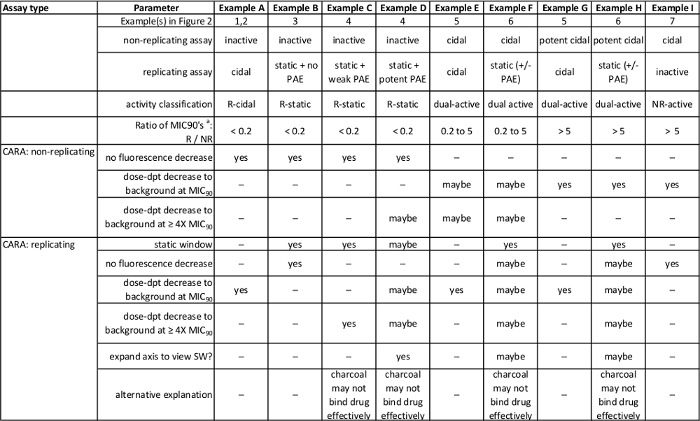
Tabel 1: Sammenfatning af forventede resultater i figur 2. [Tilpasset med tilladelse fra Gold et al., Antimicrobial Agents and kemoterapi, 2015 7] Klik her for at se en større version af denne tabel.
Den CARA blev oprindeligt udviklet til at afhjælpe en flaskehals i forløber ikke-replikerende eller dual-aktive molekyler 7. Den CARA fungerer som et mellemtrin mellem koncentration-respons bekræftelse af primære screening hits og CFU assays (figur 1). Da en enkelt CARA plade kan erstatte mange mikrotiterplader skal udarbejde serielle fortyndinger, og agar-holdige Petri-plader, der anvendes til at optælle overlevende bakterier, CARA giver en simpel anordning til hurtigt at vurdere et molekyle aktivitet og teste flere variabler på én gang, herunder sammensatte koncentration og tid for udsættelse for forbindelsen.
I en CFU-assay, foruden serielle fortyndinger, der ofte spænder op til 10 6 fold, agarpladen fortynder typisk molekyler ved yderligere ~ 800-fold (10 pi onto 8 ml i en tri-stil petriskål). Vores to-trins, multi-stress screeningsassay for forbindelser er aktive på ikke-replikerende M. tukulose har en fremførsel faktor 5-fold, dvs. en forbindelse til stede i den ikke-replikerende fase af assayet er til stede ved en femtedel den oprindelige koncentration i udvækst (replikerende) fase af assayet 6-9. De CARA formindsker fremførsel virkninger ved sekvestrering små molekyler med aktivt kul. Størstedelen af tuberkulose lægemidler og kliniske kandidater binder aktivt kul hurtigt og fuldstændigt, med undtagelse af aminoglycosid streptomycin 7. Inddragelse af aktivt kul i agarplader for CFU assays forhindrede bakterievækst hæmning, eller bakteriel dræbe, ved i op TMC207 og PA-824 7,21,22. Således i kraft af inkorporering aktivt kul i bakteriologisk agar, CARA er ikke afhængig af serielle fortyndinger af celler og testmiddel.
Den CARA kan hjælpe med at forudsige bakteriostatisk eller baktericidt konsekvenser af replikerende aktive og bakteriedræbende effekt af ikke-replikerende aktive. I ggeneraldirektøren, at CARA bruges parallelt med standard MIC 90 analyser. Den intelligente magt CARA kommer fra sammenligne MIC 90 og CARA resultater (Figur 2 og tabel 1). Når det bruges til at studere anti-mycobakterielle midler kan CARA præcist forudsige aktivitet, der er replikerende baktericide (figur 4a), replikerende bakteriostatiske (figur 4b), ikke-replikerende baktericide (figur 4c), eller dual aktiv (figur 4d). Den CARA tillader også enkel vurdering af en forbindelse aktivitet på tværs af både dosis og tid. CFU assays alene kræver en stor indsats og materiale til at vurdere aktiviteten af en forbindelse over et bredt område af doser og tidspunkter, men opgaven bliver håndterbar når CARA resultater indsnævre række betingelser til dem, hvori forbindelsen er påviseligt aktiv (figur 5 ).
Mens Cara har anvendelighed i at studere virkningen af enNTI-infektiøse på mycobakterier, assayet har begrænsninger. Den CARA har en smal dynamikområde (2-3 log 10), og kan ikke være passende for betingelser, hvor man foregriber kan der ikke være mere end 2 til 3 log 10 bakteriel dræbe. CARA forudsigelser kræver yderligere undersøgelse ved hjælp af en mere stringent og præcis metode til at optælle antallet af bakterier, såsom en CFU-analysen. Den post-antibiotisk effekt af nogle antiinfektionsmidler, såsom PAS, kan forvirre CARA som en prædiktiv værktøj til at skelne mellem forbindelser med baktericid og bakteriostatisk aktivitet mod replikerende M. tuberculosis 7.
Der er to anbefalinger til at forbedre kvaliteten af CARA. For det første skal man hælde CARA mikroplader hurtigt før agar størkner, og samtidig opretholde volumetrisk præcision og undgå sprøjt uden for mikrobrønde. Uanset antallet af plader, der kræves, anbefaler vi at gøre 0,5 til 1 L batches af medium til at hjælpe opretholde medium i flydende form, så længe den nødvendige tid til at hælde plader. Ændring tips ofte, mens fylde mikroplader med medium undgår at bruge delvist tilstoppede tip. For det andet må man minimere kunstig variation i fluorescens mellem replikater. Mycobakterielle mikrokolonier, især til patogene mycobakterier såsom M. tuberculosis, ofte vokser uregelmæssigt. For eksempel kan mikrokolonier vokser på agaroverfladen variere i størrelse, form, højde, eller kan strække sig op til de indvendige vægge af mikropladebrønde. En af udfordringerne er at dække alle baciller ensartet med udviklingslandene reagens. En anden hurdle er, at efter forlænget inkubering ved 37 ° C, kan det faste bakteriologisk medium af Cara mikroplader bliver tør og tilbøjelige til at absorbere fremkaldelsesreagens. Da aktivt kul kan binde resazurin og slukke fluorescens 7, kan der være godt til-brønd variation som følge tørre brønde absorberer resazurin fremkalderopløsning og den aktiverede Charcoal quenching resazurin fluorescens. Pre-befugtning af overfladen af alle Cara mikropladebrønde med PBS umiddelbart før tilsætning af fremkaldelsesreagens afbøder begge disse problemer - fremkaldelsesreagens vil nå alle mycobakterielle kolonier ens, og resazurin forbliver sikkert over aktivt kul. Den CARA kan have applikationer i at identificere og karakterisere fænotyper af mycobakterielle mutanter, eller i medium-throughput drug discovery analyser for andre bakteriearter.
Der er ingen interessekonflikter at afsløre.
Vi er taknemmelige for Kristin Burns-Huang til ekspert gennemgang af manuskriptet og J. David Warren (Weill Cornell Medical College) for kemi bistand samtidig udvikle den CARA. Dette arbejde blev støttet af TB Drug Accelerator Program af Bill og Melinda Gates Foundation, Abby og Howard P. Milstein Program i Translationel Medicin og et NIH TB Research Unit (U19 AI111143). Institut for Mikrobiologi og Immunologi er støttet af William Randolph Hearst Foundation. SSK blev støttet af NIH tilskud K08AI108799.
| Name | Company | Catalog Number | Comments |
| Middlebrook 7H9 | Beckton Dickinson | 271310 | |
| Middlebrook 7H11 | Beckton Dickinson | 298810 | |
| Middlebrook OADC | Beckton Dickinson | 212351 | |
| BSA, heat shock | Roche | 3118958001 | |
| activated charcoal | Sigma | C5510 | |
| PBS, Dulbecco's Ca2+ and Mg2+ free | Life Technologies / Invitrogen | 14190-144 | |
| tween 80 | Sigma | P8074 | |
| tyloxapol | Sigma | T8761 | |
| sodium nitrite | Sigma | 2252 | |
| rifampicin | Sigma | R3501 | |
| 6-bromo-1H-indazol-3-amine | Alfa Aesar | H34095 | |
| potassium phosphate monobasic | Sigma | P0662 | |
| magnesium sulfate, heptahydrate | Sigma | M1880 | |
| ferric ammonium citrate | Sigma | F5879 | |
| zinc sulfate, heptahydrate | Sigma | Z0251 | |
| ammonium chloride | Sigma | A9434 | |
| butyric acid, liquid | Sigma | B103500 | |
| resazurin powder | Sigma | R7017 | |
| sodium chloride | J.T. Baker | 4058-01 | |
| prepared resazurin solution | Invitrogen | DAL1100 | |
| PCR stickers | Denville | B1212-5 | |
| spectrophotometer | Molecular Devices | M5 | |
| 96-well, tissue culture treated microplates | Corning | 3595 | |
| reagent reservoirs | VWR | 89094-678 | |
| resealable plastic bags | VWR | 395-94602 | |
| 14 mL Polypropylene round-bottom tubes | Corning | 352059 | |
| 50 mL conical centrifuge tube | Corning | 352070 | |
| 75 cm2 Cell culture flask | Corning | 431464U | |
| clear, flat bottom tissue culture treated 96-well microplate | Costar | 3595 | |
| Prism 6 for OS X | GraphPad | http://www.graphpad.com/scientific-software/prism/ |
- Nathan, C. Fresh approaches to anti-infective therapies. Sci. Transl. Medicine. 4 (140), 140-142 (2012).
- Gomez, J. E., McKinney, J. D. M. tuberculosis persistence, latency, and drug tolerance. Tuberculosis (Edinb). 84, 29-44 (2004).
- Balaban, N. Q., Merrin, J., Chait, R., Kowalik, L., Leibler, S. Bacterial persistence as a phenotypic switch. Science. 305, 1622-1625 (2004).
- Bigger, J. Treatment of staphylococcal infections with penicillin by intermittent sterilisation. Lancet. , 497-500 (1944).
- Bryk, R., et al. Selective killing of nonreplicating mycobacteria. Cell Host Microbe. 3, 137-145 (2008).
- Gold, B., et al. Nonsteroidal anti-inflammatory drug sensitizes Mycobacterium tuberculosis to endogenous and exogenous antimicrobials. Proc. Natl. Acad. Sci. U.S.A. 109, 16004-16011 (2012).
- Gold, B., et al. Rapid, semi-quantitative assay to discriminate among compounds with activity against replicating or non-replicating Mycobacterium tuberculosis. Antimicrob. Agents Chemother. 59, 6521-6538 (2015).
- Gold, B., Warrier, T., Nathan, C., Parish, T., Roberts, D. . Mycobacteria Protocols, Methods in Molecular Biology. 1285, 293-315 (2015).
- Warrier, T., et al. Identification of Novel Anti-mycobacterial Compounds by Screening a Pharmaceutical Small-Molecule Library against Nonreplicating Mycobacterium tuberculosis. ACS Infect. Dis. , 580-585 (2015).
- Zheng, P., Chem, J. .. M. e. d. .., et al. Synthetic Calanolides with Bactericidal Activity Against Replicating and Nonreplicating Mycobacterium tuberculosis. J. Med. Chem. , (2014).
- Darby, C. M., et al. Whole cell screen for inhibitors of pH homeostasis in Mycobacterium tuberculosis. PLoS One. 8, e68942 (2013).
- Darby, C. M., Nathan, C. F. Killing of non-replicating Mycobacterium tuberculosis by 8-hydroxyquinoline. J. Antimicrob. Chemother. 65, 1424-1427 (2010).
- de Carvalho, L. P., Darby, C. M., Rhee, K., Nathan, C. Nitazoxanide Disrupts Membrane Potential and Intrabacterial pH Homeostasis of Mycobacterium tuberculosis. ACS Med. Chem. Lett. 2, 849-854 (2011).
- Xie, Z., Siddiqi, N., Rubin, E. J. Differential antibiotic susceptibilities of starved Mycobacterium tuberculosis isolates. Antimicrob. Agents Chemother. 49, 4778-4780 (2005).
- Grant, S. S., et al. Identification of novel inhibitors of nonreplicating Mycobacterium tuberculosis using a carbon starvation model. ACS Chem. Biol. 8, 2224-2234 (2013).
- Zhang, M., et al. Streptomycin-starved Mycobacterium tuberculosis 18b, a drug discovery tool for latent tuberculosis. Antimicrob. Agents Chemother. 56, 5782-5789 (2012).
- Mak, P. A., et al. A high-throughput screen to identify inhibitors of ATP homeostasis in non-replicating Mycobacterium tuberculosis. ACS Chem. Biol. 7, 1190-1197 (2012).
- Cho, S. H., et al. Low-oxygen-recovery assay for high-throughput screening of compounds against nonreplicating Mycobacterium tuberculosis. Antimicrob. Agents Chemother. 51, 1380-1385 (2007).
- Franzblau, S. G., et al. Comprehensive analysis of methods used for the evaluation of compounds against Mycobacterium tuberculosis. Tuberculosis (Edinb). 92, 453-488 (2012).
- Rebollo-Lopez, M. J., et al. Release of 50 new, drug-like compounds and their computational target predictions for open source anti-tubercular drug discovery. PLoS One. 10, e0142293 (2015).
- Tasneen, R., et al. Contribution of the nitroimidazoles PA-824 and TBA-354 to the activity of novel regimens in murine models of tuberculosis. Antimicrob. Agents Chemother. 59, 129-135 (2015).
- Grosset, J. H., et al. Assessment of clofazimine activity in a second-line regimen for tuberculosis in mice. Am. J. Respir. Crit. Care Med. 188, 608-612 (2013).
- Shiloh, M. U., Ruan, J., Nathan, C. Evaluation of bacterial survival and phagocyte function with a fluorescence-based microplate assay. Infect. Immun. 65, 3193-3198 (1997).
- Wang, F., et al. Identification of a small molecule with activity against drug-resistant and persistent tuberculosis. Proc. Natl. Acad. Sci. U.S.A. 110, E2510-E2517 (2013).
- Wayne, L. G., Hayes, L. G. An in vitro model for sequential study of shiftdown of Mycobacterium tuberculosis through two stages of nonreplicating persistence. Infect. Immun. 64, 2062-2069 (1996).
- Barry, A. L., et al. . Methods for determining bactericidal activity of antimicrobial agents: approved guideline. 19, (1999).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved