Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Immunology and Infection
Visualisierung des Charcoal Agar Resazurin-Assay für Semi-quantitative, Mitteldurch Auszählung von Mykobakterien
The charcoal agar resazurin assay (CARA) is a semi-quantitative, medium-throughput method to assess activity of test agents against mycobacteria that are replicating, non-replicating, or both. The CARA permits rapid evaluation of time- and concentration-dependent activity and identifies parameters to pursue by colony forming unit (CFU) assays.
Es besteht ein dringender Bedarf zu entdecken, und die Fortschritte Antiinfektiva, die die Dauer der Tuberkulose (TB) Behandlung zu verkürzen. Mycobacterium tuberculosis, dem Erreger der Tuberkulose, ist resistent gegen rasche und dauerhafte Chemotherapie aufgrund der Anwesenheit von Bazillen phänotypische Medikamentenresistenz aufweisen. Die c harcoal ein GAR r esazurin eine ssay (CARA) wurde als ein Werkzeug entwickelt , aktive Moleküle durch Hochdurchsatz - Screening - Kampagnen gegen die Replikation und nicht-replizierende M. tuberculosis entdeckt zu charakterisieren. Die Aufnahme von Aktivkohle in bakteriologischer Agar-Medium hilft, die Auswirkungen der Verbindung Übertrag zu mindern, und beseitigt die Erfordernis Zellen auf CARA Mikrotiterplatten vor Spek vorab verdünnen. Nach einer 7-10 Tage Inkubationsdauer bei 37 ° C ermöglicht die Reduktion von Resazurin durch mykobakterielle Mikrokolonien auf der Oberfläche der CARA Mikrotitervertiefungen wachsenden semi-quantitative assessment von Bakterienzahlen über Fluorometrie. Die CARA erkennt etwa eine 2-3 log 10 Unterschied in der Bakterienzahlen und prognostiziert eine minimale bakterizide Konzentration führt zu ≥99% Bakterienabtötung (MBC ≥99). Die CARA hilft festzustellen, ob ein Molekül auf Bazillen aktiv ist, die, nicht replizierenden oder beide zu replizieren. Pilotversuche die CARA mit erleichtern die Identifizierung von denen Konzentration der Testmittel und die Zeit der Verbindung Exposition erfordern weitere Auswertung von koloniebildende Einheit (CFU) Assays. Darüber hinaus kann die CARA vorhersagen, ob die Replikation Wirkstoffe bakterizide bzw. bakteriostatische sind.
Mycobacterium tuberculosis, dem Erreger der Tuberkulose, kann in einem Wirt in einem latenten Zustand überleben, die Antibiotika - Ausrottung resistent ist. Phänotypische (nicht-genetischen) Widerstand von M. tuberculosis während der Infektion wird angenommen , daß dies zu sein, teilweise , um Populationen von nicht-replizierende Bazillen 1,2. Klasse I persisters phänotypische Medikamentenresistenz unter großen Populationen von Drogenempfindlichen Zellen 3,4 entstehen über seltene stochastischen Mechanismen anzeigt. Klasse II persisters sind nicht replizierenden durch Faktoren der Wirtsimmunität gemacht, einschließlich der externen Belastungen in Mikroumgebungen während der Infektion auftreten. Kürzlich entwickelten wir ein in - vitro - Modell der Klasse II nicht replizierenden Persistenz Bedingungen von M. tuberculosis in aktivierten Makrophagen und Granulome konfrontiert zu imitieren. Die Multi-Belastungsmodell der Klasse II Persistenz umfasst Bedingungen, dass ein langsames Wachstum, wie beispielsweise einer Fettsäure Kohlenstoffquelle und vollständig halt Wachstum, wie milde Säure (pH 5,0), Hypoxie (1% O 2) und Stickoxid und andere reaktive Stickstoffzwischenprodukte 5-9. Groß angelegte Screening dieses Multi-Stress - Modell von nicht-Replikation verwendet wird , und andere Klasse II nicht replizierenden Modelle hat diverse Moleküle ergeben , deren Aktivität gegenüber dem nicht-replizierenden Zustand gerichtet ist 5-7,9-18. Die gleichen nicht-replizierenden Bildschirme zeigte auch eine Kategorie von Molekülen , die sowohl replizierende und nicht-replizierende Bazillen Aktivität gegen besitzen, als "dual Aktiv" 7,10,12,19,20.
Antibakteriell Wirkstoffforschung in der Treffer-to-Lead - Phase beinhaltet umfassende Charakterisierung von Kandidatenmolekülen führt zur Treffer Expansion, vorläufige pharmakologische Charakterisierung, Zielidentifizierung und vorläufige Wirksamkeit in vivo Studien zur Auswahl. Als erster Schritt werden Antiinfektiva durch ihre bakteriostatische oder bakterizide Wirkmechanismus klassifiziert und, wenn bakterizid, whether Bakterienabtötung ist zeit- und / oder konzentrationsabhängig. Die Kolonie bildende Einheit (CFU) Assay ist die klassische, Goldstandard Methode, um diese Fragen zu beantworten. In der CFU-Assay werden die Bakterien auf einem Testmittel ausgesetzt, wonach Aliquots entfernt werden, seriell verdünnt, und Aliquots der Verdünnungen werden auf festen bakteriologischen Medium verteilt und inkubiert Wachstum der überlebenden Zellen zu ermöglichen. Schließlich werden Bakterienkolonien gezählt. Die CFU-Test erfordert eine große Anzahl von Mikrotiterplatten Zellen und Agar enthaltenden Petriplatten zu verdünnen überlebenden Kolonien aufzuzählen. Die CFU-Assay für langsam wachsende Mykobakterien durch ihre langsame Generationszeit (18-24 Stunden) behindert, die etwa 3 Wochen erfordert für Kolonien auf Platten zu erscheinen. Darüber hinaus wird Inkubator Raum oft in spezialisierten Biosicherheit-Level-3-Anlagen beschränkt.
Während umständlich, CFU-Assays sind der Goldstandard, die Auswirkungen von nicht-replizierenden und Dual-aktive Moleküle auf mycobacter zu charakterisierenia. Nicht-replizierende Assays unterliegen hohen Fehlalarmquote , so viele sind mit Assays replizierende zelluläre Lebensfähigkeit 6-8 zu bewerten. Zum Beispiel kann eine Verbindung , die eine starke Aktivität gegen replizierende M. tuberculosis (ein "Replizieren aktiv") kann fehlschlagen , während der nicht-replizierenden Assay zu töten, kann aber aufgrund der Übertrag von der nicht-replizierenden Phase des noch töten Test auf der Erholungsphase des Assays, die unter Bedingungen durchgeführt wird, die Replikation ( "replizieren von Bedingungen") zu unterstützen. Verbindung tragen über erschwert die weitere Analyse der dualen aktiven Molekülen, so dass es schwierig zu unterscheiden, ob Aktivität zu replizieren, nicht replizierenden oder Dual.
Um die Probleme anzugehen oben beschrieben, entwickelten wir das c harcoal ein GAR r eine ssay (CARA) für eine schnelle, semi-quantitative Zählung von mycobakteriellen Spezies, wie M. tubercul esazurinosis, M. bovis BCG und M. smegmatis 7 (1 und 2). In Pufferlösungen in vitro, Aktivkohle sequesters schnell die meisten Standard Drogen verwendet , um Tuberkulose 7 zu behandeln. Aktivkohle in CARA Mikrotiterplatten bindet Verbindungen , die aus einem Assay Mikrotiterplatten - Übertrag kann, und dieses Merkmal der CARA eliminiert die Anforderung zu seriell Assay gut Inhalt vor der Zählung 7,21,22 verdünnen. Die Anzahl der mykobakteriellen Mikrokolonien auf der Agar - Oberfläche von CARA Mikrotiterplatten durch Zugabe von Resazurin geschätzt wird, einen blauen Farbstoff, dessen reduzierte Form, Resorufin, ist ein rosa Molekül , dessen Fluoreszenz durch Spektrophotometrie 23 gemessen wird. CARA Mikrotiterplatten für 1-2 Tage inkubiert werden für M. smegmatis und 7-10 Tage für langsam wachsende Mycobakterien wie M. tuberculosis und M. bovis BCG. Die CARA hat einen schmalen Dynamikbereich von ~ 2-3 log 10 verschierenz in CFU. Wenn anstelle eines CFU-Assay verwendet wird, ersetzt eine einzige CARA Mikrotiterplatte etwa fünf 96-Well-Platten für serielle Verdünnungen verwendet, und 120 tri-Stil für das Plattieren verwendet Agarplatten. Die Interpretation der CARA Daten hilft nachfolgende Studien führen, durch die Inkubationszeiten und Konzentrationen der Verbindung zu testen, in mühsamer CFU-basierte Assays zu bestimmen.
1. Herstellung von CARA Mikrotiterplatten
- Autoklaven 900 ml Middlebrook 7H11-Agar, enthaltend 0,2% Glycerin und 0,4% Aktivkohle in einem 2 l-Erlenmeyerkolben oder alternativ 450 ml in einem 1 l Becherglas. Fügen Sie eine große autoklavierbar Rührstab im Kolben oder Becher. Decken Sie die Öffnung des Kolbens oder Becher mit Aluminiumfolie und heften sich an Glas mit Autoklav-Band.
- Kühl (ca. 55-65 ° C) auf einer magnetischen Rührplatte bei niedriger Geschwindigkeit zu halten, die Holzkohle in Suspension eingestellt zu berühren.
- Führen Sie alle nachfolgenden Schritte aseptisch in einer Biosicherheits Haube, die eine magnetische Rührplatte hat.
- Folie entfernen. 100 ml OADC Supplement (OADC ergänzen, wenn sie bei 10% verwendet, Ausbeuten endgültigen Medienkonzentrationen von 0,2% Dextrose, 0,5% Albumin, 0,085% NaCl, 0,0005% Ölsäure und 0,4 mg / ml Katalase) mit dem 2 L Erlenmeyerkolben oder 50 ml OADC zum 1 L-Becherglas und Mischen fortzusetzen.
- Wenn ein Erlenmeyerkolben mit, gießen etwa 25-40 ml 7H11-OADC-Kohle in ein steriles Reaktionsmittelreservoir. Wenn das Becherglas verwendet wird, ist es nicht notwendig, ein Reaktionsmittelreservoir zu verwenden.
- Füllen Sie eine 96-Well-Mikroplatten mit 200 ul / Vertiefung 7H11-OADC-Kohle aus dem Reagenzienbehälter oder Becher. Arbeiten Sie schnell Agar Erstarrung und Einführung von Blasen zu vermeiden. Vermeiden festen Medium außerhalb der Vertiefungen spritzt, so dass eine Quelle für Pilzkontamination sein kann. Mit Hilfe einer Mehrkanalpipette, verwenden Sie einen Satz von 12 Filterspitzen für den Transfer von 7H11-OADC-Holzkohle auf die 8 Zeilen (AH) der 96-Well-Platte.
HINWEIS: Das Medium erstarrt schnell. Um zu vermeiden, Pipettenspitzen zu verstopfen, ändern sie häufig. - Alternativ gießen CARA Mikrotiterplatten eine p1000 elektronische Mehrkanalpipette mit Filterspitzen mit der Vorbereitung zahlreiche Platten zu unterstützen.
HINWEIS: Aufgrund des geringen Volumens von Mikrotitervertiefungen, die Agar in CARA Mikrotiterplatten erstarrt innerhalb von Minuten zu gießen. - Platz Stapel von CARA Mikrotiterplatten in wiederverschließbaren Plastik bags zu vermeiden auszutrocknen.
- Store CARA Mikrotiterplatten bei 4 ° C.
2. Einrichten von Replizieren und nicht-replizierende MIC 90 Assays
- Beimpfen von M. tuberculosis, M. bovis BCG oder M. smegmatis bei einer OD 580 von 0,01 bis 0,1 und erweitern bis zur mittleren logarithmischen Phase (OD 580 ~ 0,5) in Middlebrook 7H9-ADN (Middlebrook 7H9 0,2% Glycerin, 0,2% Dextrose , 0,5% Albumin und 0,085% NaCl) oder 7H9-OADC (Middlebrook 7H9 0,2% Glycerol und 10% OADC Ergänzung enthält).
- Wachsen M. tuberculosis und M. bovis BCG als ~ 20 ml - Kulturen in Zellkulturflaschen stehen und M. smegmatis mit Schütteln in Polypropylen mit rundem Boden (4 ml Kultur) oder 50 ml konischen Zentrifugenröhrchen (10-20 ml Kultur). Inkubieren pathogene Mykobakterien bei 37 ° C mit 20% O 2 und 5% CO 2 und M. smegmatis bei 37 ° C mit 20% O 2.
- Richten Sie eine minimal-hemmendenKonzentration (MIC 90) -Stil Experiment unter replizierende und nicht-replizierende Bedingungen (Abbildung 2).
HINWEIS: Testmittel sind in der Regel in Duplikate oder vierfach getestet 4 Tests zu ermöglichen, oder 2-Verbindungen, jeweils pro 96-well Mikrotiterplatten. Beispielsweise in einer 96-Well-Platte kann ein Testmittel in Reihen AD und anderen in Reihen EH werden getestet. Die DMSO (Vehikel) ist in den Spalten 1, 2 und 12 und das Testmittel Verdünnungsreihe läuft von Spalte 3 (niedrigste Konzentration), bis Spalte 11 (höchste Dichte). MIC 90 -Stil Assays verwenden typischerweise 2-fache Verdünnungsreihe. Es gibt zahlreiche nicht-replizierenden Modelle für Mykobakterien 14-16,18,24,25 und zu illustrativen Zwecken, wir sind ein Multi-Stress - Modell von nicht-Replikation 6,8,9 verwenden.- Für den replizierenden Assay verteilen 200 ul Zellen in 7H9-ADN bei einer OD 580 von 0,01 in alle Vertiefungen einer klaren Boden, Gewebekultur behandelt 96-Well - Platte. <li> Für das nicht-replizierende Assay, wasche zweimal Zellen in phosphatgepufferter Salzlösung (PBS) 0,02% Tyloxapol enthält, und resuspendieren Zellen in nicht-replizierenden Medium (0,05% KH 2 PO 4, 0,05% MgSO 4, 0,005% Eisenammoniumcitrat 0,0001% ZnCl 2, 0,1% NH 4 Cl, 0,5% BSA, 0,085% NaCl, 0,02% Tyloxapol 0,05% Butyrat, pH auf 5,0 mit 2 N NaOH eingestellt).
- Verdünnte Zellen bis zu einer OD 580 von 0,1 in nicht-replizierenden Medium und füge NaNO 2 aus einer frisch hergestellten 1 M Vorrat zu einer Endkonzentration von 0,5 mM.
- Verteilen Sie 200 ul Zellen bei einer OD 580 von 0,1 in alle Vertiefungen einer klaren Boden, Gewebekultur behandelt 96-Well - Platte.
HINWEIS: Bereiten Verbindung Verdünnungen als das 100-fache Stammlösungen in DMSO. Damit die Wirkung eines Moleküls in einer Endkonzentration eine typische MIC Platte 0,4-100 & mgr; g / ml würde Stammlösungen von 0,04 bis 10 mg / ml in DMSO Tests erfordern.
- In 2 ul disungen von Testmittel 1 in Reihen AE und 2 ul-Verdünnungen von Testmittels 2 in Reihen EH. Gründlich durchmischen.
- Fügen Sie 2 ul Fahrzeugsteuerung (üblicherweise DMSO) in Kontrollvertiefungen, die Spalten 1, 2, 12 (Zeilen AH). Gründlich durchmischen.
- Für jedes Experiment enthalten mindestens eine positive Kontrolle, wie Rifampicin 0,004-1 ug / ml (replizierende assay) und / oder 0,08 bis 20 & mgr; g / ml (nicht replizierenden assay).
HINWEIS: Die Verwendung von 6-Brom-1H-indazol-3-amin 9 bei 0,1 bis 25 & mgr; g / ml wird als Kontrollverbindung empfohlen , die eine selektive hat, NaNO 2 -abhängigen Aktivität in dem Mehrspannungsmodell von nicht-Replikation. - Assays für die Replikation, inkubieren bei 20% O 2 und 5% CO 2 für 7 Tage (M. tuberculosis und M. bovis BCG) oder 1-48 h (M. smegmatis) bei 37 ° C Mikrotiterplatten. Für die Multi-Belastungsmodell von nicht-Replikation inkubieren Mikrotiterplatten für 7 Tage bei 37 ° C bei 1% O 2 und 5% CO 2 (<em> M. tuberculosis und M. bovis BCG).
3. Inokulation von CARA Mikrotiterplatten
- Zu den Zeitpunkten , in denen die CARA wird als Auslese verwendet werden, resuspendieren sorgfältig und Inhalt des MIC 90 -Stil Assayplatte eine p200 mehrkanaligen Pipette in 50-75 ul eingestellt werden. Pipette nach oben und unten mindestens 5-10 mal und behutsam schwenken, die auch Inhalte in einer kreisförmigen Bewegung der Pipettenspitzen.
- Transfer 10 ul Assay-Well-Inhalt an die CARA Mikrotiterplatte. Stellen Sie sicher, dass die Reihenfolge der gut Inhalte auf der Testplatte, die Reihenfolge der gut Inhalt der CARA Mikrotiterplatte entspricht. Vermeiden Sie Spritzer während der Transfers und stellen Sie sicher, dass die 10 & mgr; l in die Mitte der CARA Mikrotitervertiefungen gesichtet werden. Bestätigen Sie die 10 & mgr; l absorbiert in die CARA Mikrotiterplatte.
HINWEIS: Es gibt keine Verdünnungen vor erforderlich, um Zellen auf der CARA Mikrotiterplatten Spek. - Bind Stapel von CARA Mikrotiterplatten mit Plattenband undanschließend in einen wiederverschließbaren Plastikbeutel. Inkubieren CARA - Mikrotiterplatten bei 37 ° C mit 20% O 2 (M. smegmatis) oder 1% O 2 und 5% CO 2 (M. tuberculosis und M. bovis BCG).
- Für M. tuberculosis und M. bovis BCG, Assays zu replizieren: Inkubation für 7 Tage; für M. tuberculosis und M. bovis BCG nicht replizierenden Assays, Inkubation für 10 Tage; für M. smegmatis, Assays zu replizieren, Inkubation für 1-2 Tage; für M. smegmatis, 2-3 Tage nicht replizierenden Assays inkubiert.
Hinweis: Die Zeiten sind Schätzungen und können dementsprechend für verschiedene replizierenden, nicht replizierenden und Stressbedingungen geändert werden.
4. Entwicklung von CARA Micro
- Entwickeln Sie die CARA Mikrotiterplatten, wenn ein Film von Bakterienwachstum, oder größere, makroskopische Kolonien sind sichtbar auf die negativen (Fahrzeug) Kontrollvertiefungen.
HINWEIS: Nach längerer Inkubation, Mikrotiterplatten CARA Brunnen ofttrocken erscheinen, und wir empfehlen Vorbenetzung auch Inhalte mit sterilem PBS. Dies dient dazu, die Kohle absorbiert Resazurin zu verhindern, was zu einer geringen Fluoreszenz oder auch zu gut Variation führen kann. - Mit einem einzigen Satz von 12 p200 Spitzen mit einer Mehrkanalpipette, verzichtet werden 40 ul sterilem PBS entlang der Seite der Vertiefung und lassen Sie die PBS über die Oberseite der Agar / bakteriellen Mikrokolonien zu verteilen.
- Bereiten CARA Entwicklungsreagens durch Mischen von 5 mg Resazurin (0,01% Endkonzentration) und 50 ml 5% Tween80 in PBS. Vortex und Sterilfilter.
HINWEIS: 1 (vol / vol) mit 10% Tween80 in PBS: Eine alternative CARA Entwicklungsreagens kann durch Vermischen kommerziell hergestellten flüssigen Lösung Resazurin auf 1, hergestellt werden. - Zugeben von 50 ul frisch hergestelltem CARA Entwicklungsreagens zu jeder Vertiefung der Mikrotiterplatte CARA eine 12-Kanal Pipette. Rock-Platten hin und her ein paar Mal Reagenz in jeder Vertiefung über den Agar und Bakterienmatte verteilen zu helfen.
- Legen Sie die Platten ina wiederverschließbaren Plastikbeutel und Inkubation mindestens 30 min für M. bei 37 ° C für smegmatis und 45-60 min für M. tuberculosis oder M. bovis BCG.
HINWEIS: Wenn die Fahrzeugkontrollvertiefungen nicht rosa innerhalb der ersten Stunde zu drehen, können die Platten neu verpackt und für längere Zeit inkubiert werden. - Vor der Fluoreszenz Lesen, legen CARA Mikrotiterplatten in einem Bio-Sicherheitshaube für 15 Minuten bei Raumtemperatur mit entfernt ihren Deckeln. Wenn außerhalb eines Biosicherheitsschrank BSL3 Spektralphotometer verwenden, haften fest mit einer optischen Qualität PCR-Aufkleber über die Platte und die Dichtung mit einem weichen Papiertuch sanft auf dem Aufkleber Oberfläche drücken.
- Bestimmen Fluoreszenz via oben mit einer Anregung bei 530 nm und Emission bei 590 nm abgelesen. Es ist nicht notwendig zu leeren die Platte.
5. Datenanalyse
- Plot Inhibitorkonzentration auf der X-Achse auf einer log - Skala 10 und die Fluoreszenz auf der Y-Achse auf einer linearen Skala. Verwenden Sie ein StreuGrundstück eine Kurve passen, wie zB "log-Hemmers gegen Antwort variable Steigung (4 Parameter)" verwendet wird. Plot Datenpunkte als Mittelwert ± Standardfehler.
Antizipierte CARA Ergebnisse sind in Figur 2 und in Tabelle 1 zusammengefasst beschrieben. Für Zellen replizieren, wird die CARA parallel zu einem Standard - MIC 90 Tests laufen, und für nicht-replizierende Assays wird die CARA parallel mit einem angepassten MIC 90 - Test ausführen, die ein Auswuchs Phase gekoppelt ist. Die Konzentration der Testmittel , das in Ausfall von CARA-Fluoreszenz führt über Hintergrundgehalte steigen die CARA-MBC ≥99 (Abbildung 3a). Die "≥99" Index zeigt an, dass die CARA-MBC eine geschätzte Konzentration des Testmittels liefert, die zu ≥2 log 10 Bakterienabtötung (≥99% kill) gibt.
Die flüssige Nährlösung MIC 90 - Test ist nicht in der Lage zwischen bakterizide und bakteriostatische Aktivität zu unterscheiden und diese Unterscheidung ist von einem CFU - Assay gelöst werden. DurchKonvention, die Schwelle , die für langsam wachsende Mykobakterien ist etwa 2-3 log 10 Kill über 7 Tage 7,26 bakterizide von bakteriostatische Aktivität unterscheidet. Da der Dynamikbereich des CARA auch töten 2-3 log 10 ist, kann die CARA eine Schätzung der bakterizide oder bakteriostatische Aktivität liefern. Die CARA identifiziert leicht einige replizierende Wirkstoffe als bakteriostatisch durch den Ausfall dieser Verbindungen CARA Fluoreszenz zu Hintergrundwerten (Abbildung 2) zu verringern. Allerdings haben einige Verbindungen mit bakteriostatischen Aktivität gegen replizierende M. tuberculosis eine starke Post-Antibiotika - Wirkung, was bedeutet , dass sie auch weiterhin während der Erholungsphase auch in Abwesenheit der Verbindung carry-over Nachwachsen von Bakterien zu hemmen. Dieser Effekt kann schwierig sein, in der CARA-Assay zu erkennen. Die Verbindungen werden im Verdacht, eine post-antibiotische Wirkung ausüben, wenn sie einen "statischen Fenster" angezeigt werden, definiert als> 4-fache Verschiebung nach rechts between die MIC und CARA - Kurven (Abbildung 3b). Das statische Fenster zeigt an, dass ein Molekül , aktiv gegen die Replikation von M. tuberculosis bakteriostatisch sein kann anstelle der bakteriziden. In einigen Fällen sind die statischen Fenster offensichtlich nur nach Überprüfung eines erweiterten Y-Achse für CARA Fluoreszenz (3c und 3d).
CARA und MIC 90 Daten werden in der Regel zusammen aufgetragen (Abbildung 4). Repräsentative Daten für replicating- und nicht-replizierende aktiven Moleküle durch MIC getestet 90 und CARA sind in Abbildung 4 dargestellt. Es gibt vier Hauptaktivitätsklassen für Moleküle: 1) replizierende bakterizid (gezeigt mit Isoniazid, 4a); 2) Replizieren bakteriostatische (gezeigt mit Linezolid, 4b); 3) nicht-replizierenden bakterizid (gezeigt mit Oxyphenbutazon, 4c); und 4) replicating aktive (bakteriostatisch oder bakterizid) und nicht-replizierende bakterizid (gezeigt mit PA-824, 4d). Wichtig ist , Figuren 4a und 4b zeigen , dass während Isoniazid und Linezolid angezeigt durch den MIC 90 - Assay Aktivität gegen nicht-replizierenden Bakterien zu haben, das CARA schlägt sie unter den nicht-replizierenden Bedingungen getestet inaktiv sind. Die Nützlichkeit der CARA Um zu testen , die in einem Molekül der zeit- und konzentrationsabhängige Wirkung der Vorhersage, M. smegmatis replizieren ausgesetzt war Konzentrationen von Rifampicin (5a - d) zu erhöhen und zu verschiedenen Zeiten zwischen 24.01 h wurden Aliquots getupft auf CARA Platten. Diese Daten zeigten , dass Rifampicin einen Einfluss ausgeübt bereits 1 h (5a) angezeigt Erhöhung bakterizide Aktivität zwischen 3 und 24 h (Figuren 5b-d) und getötet ≥2-3 log 10 bei ~ 10 & mgr; g / ml nach 24 h (5d). Ein ähnliches Experiment testet vierfach eines Fahrzeugsteuerung und 9 Arzneimittelkonzentrationen und bei 4 Zeitpunkte, würde durch einen Standard CFU-basierten Assay prohibitiv sein.
Somit hat die CARA eine Rolle in der Wirkstoffforschung als Medium-Throughput, schnellen Mechanismus eines Moleküls Aktivitätsprofil zu identifizieren. CARA Prognosen rigoros werden sollte mit einem Standard-CFU-Test bewertet. Die Zugabe von 0,4% Aktivkohle auf Petri - Platten für CFU - Analyse helfen Korrelation zu CARA Daten verbessern kann, und in genaueren CFU Zählungen führen können, im allgemeinen die Größe der Korrektur zu der Verbindung Potenz 21,22 proportional ist.
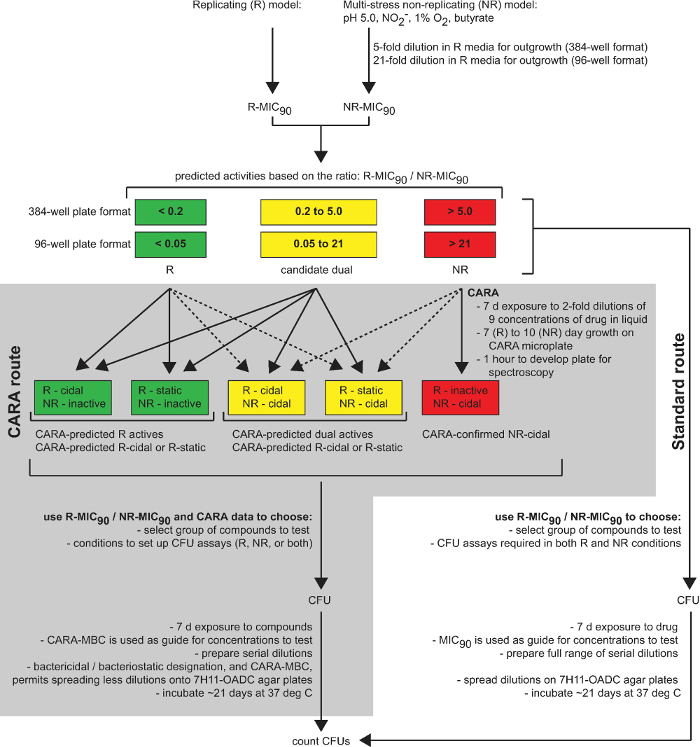
Abbildung 1: Die CARA ist eine prädiktive Werkzeug in der Wirkstoffforschung. Dieses Diagramm fasst den Nutzen der CARA alsZwischenstufe zwischen Wirkstoff-Screening (Single-Point-Screening, Rosinenpicken und Dosis-Wirkungs-Assays) und zeitraubend Hit-to-Lead-Assays (CFU-Assays und Zielidentifizierung). [Adaptiert mit Erlaubnis von Gold et al., Antimicrobial Agents and Chemotherapy, 2015 7] Bitte hier klicken , um eine größere Version dieser Figur zu sehen.
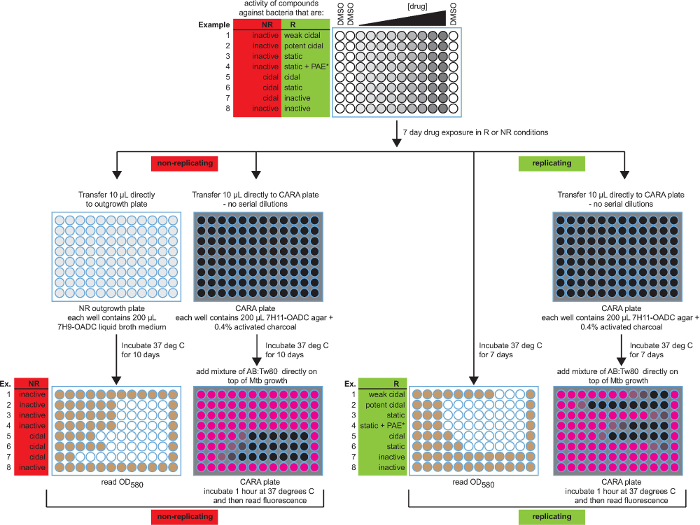
Abbildung 2: Schematische Darstellung der Brühe MIC 90 - Assay und CARA mit erwarteten Ergebnissen. Beide MIC 90 und CARA Ergebnisse werden für die 8 möglichen Aktivitäten vorgestellt. Die Farbcodierung für MIC 90 Mikrotitervertiefungen ist weiß (kein Wachstum) und braun (Wachstum) und für CARA Mikrotiterplatten ist schwarz (keine Fluoreszenz) und Rosa (Resorufin Fluoreszenz). Die Daten sind hypothetisch. [Adaptiert mit Erlaubnis von Gold et al., Antimicrobial Agents and Chemotherapy, 2015 7] Bitte hier klicken , um eine größere Version dieser Figur zu sehen.
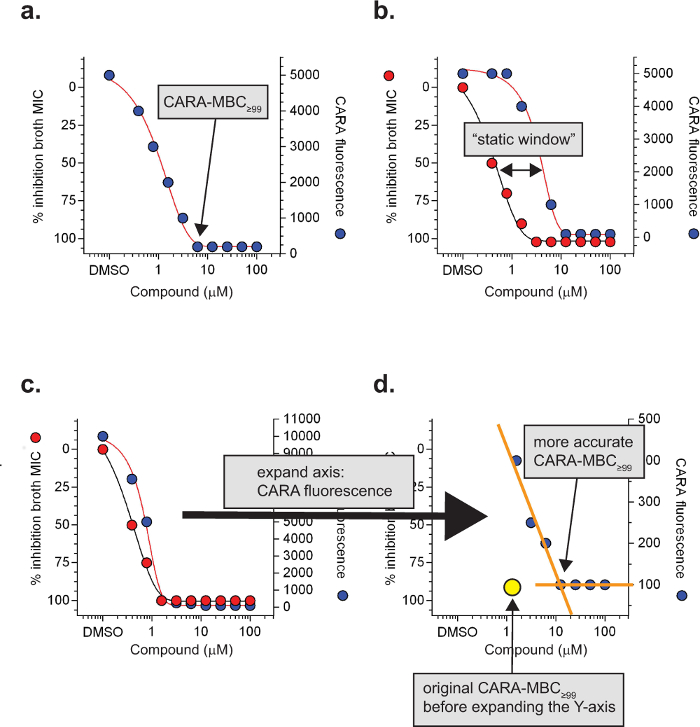
Abbildung 3: Specialized CARA Begriffe und Definitionen. Die Minimale bakterizide Konzentration eines Moleküls , was zu Hintergrundwerten von CARA Fluoreszenz ist das CARA-MBC ≥99 (a). Unter Replizieren Bedingungen zeigt eine ≥4 fache Verschiebung der CARA-MBC ≥99 nach rechts des MIC 90 oft bakteriostatische Aktivität und ist ein "statisches Fenster" (b) bezeichnet. Bei Molekülen mit einem potenten post-antibiotische Wirkung kann statische Fenster schwierig sein, (c) beobachten und erfordernExpansion der Y-Achse (CARA Fluoreszenz) sichtbar zu machen (d). Die Daten sind hypothetisch. [Adaptiert mit Erlaubnis von Gold et al., Antimicrobial Agents and Chemotherapy, 2015 7] Bitte hier klicken , um eine größere Version dieser Figur zu sehen.
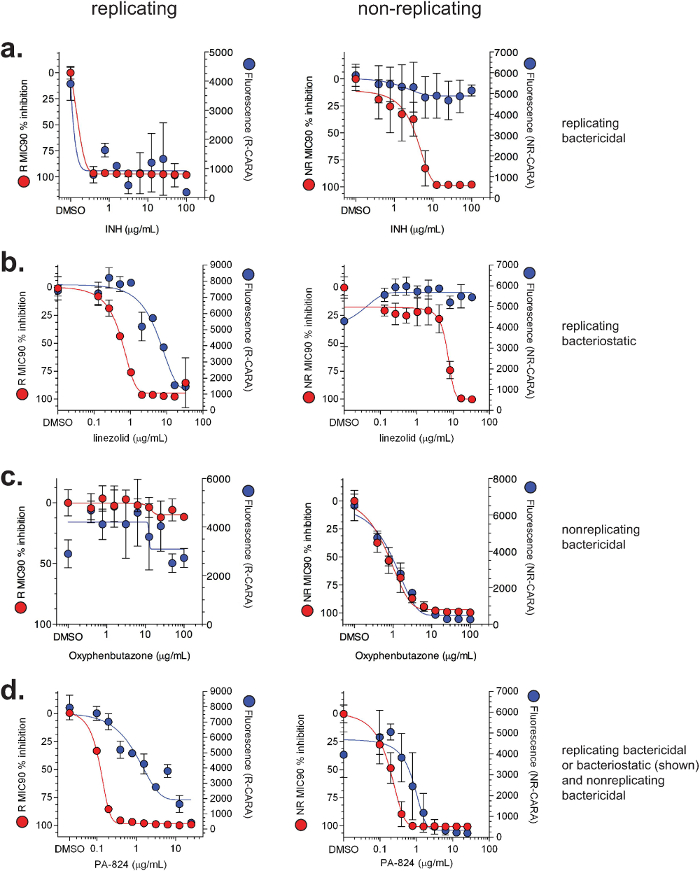
Abbildung 4: Illustrative MIC 90 und CARA - Ergebnisse für ausgewählte Verbindungen. Daten für MIC 90 (rot) und CARA (blau) für (a) Isoniazid (INH), (b) Linezolid, (c) Oxyphenbutazon gezeigt, und (d) PA-824. Wildtyp M. tuberculosis H37Rv wurde 7 Tage unter Standard replizierenden Bedingungen oder der Multi-Stress - Modell von Nicht-Replikation 7-9 Verbindungen ausgesetzt. MIC 90 - Assays und CARA wurden wie in Abbildung 2 gezeigt , durchgeführt. [Adaptiert mit Erlaubnis von Gold et al., Antimicrobial Agents and Chemotherapy, 20157]Bitte hier klicken , um eine größere Version dieser Figur zu sehen.
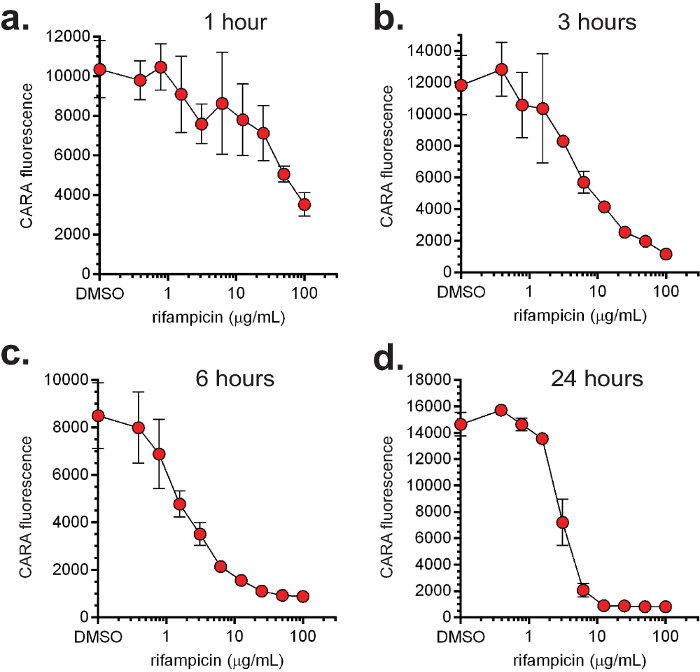
Abbildung 5: dosis- und zeitabhängige Aktivität von Rifampicin. Der nicht-pathogene, schnell wachsende M. smegmatis wurde bei Konzentrationen von Rifampicin ausgesetzt unter Bedingungen zu replizieren , und Aliquote wurden zur Steigerung der 1 (a) für CARA abgetastet, 3 (b), 6 (c) und 24 (d) hr. [Adaptiert mit Erlaubnis von Gold et al., Antimicrobial Agents and Chemotherapy, 2015 7].com / files / ftp_upload / 54690 / 54690fig5large.jpg "target =" _ blank "> Bitte hier klicken, um eine größere Version dieser Figur zu sehen.
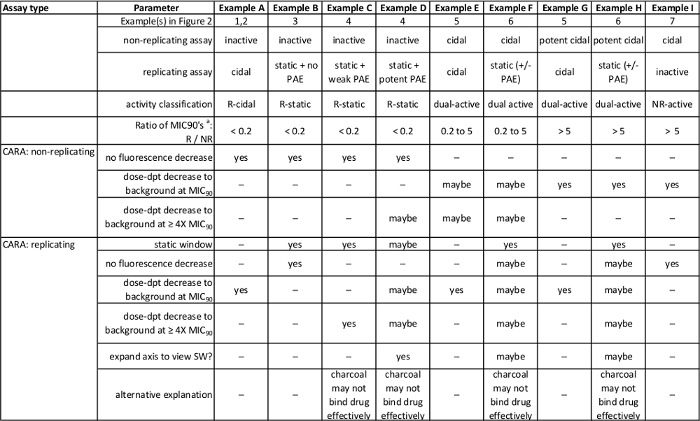
Tabelle 1: Zusammenfassung der erwarteten Ergebnisse in Abbildung 2. [Adaptiert mit Erlaubnis von Gold et al., Antimicrobial Agents and Chemotherapy, 2015 7] Bitte hier klicken , um eine größere Version dieser Tabelle anzuzeigen.
Die CARA wurde ursprünglich entwickelt , 7 einen Engpass in voran nicht replizierenden oder Dual-aktive Moleküle zu lindern. Das CARA dient als Zwischenschritt zwischen Konzentrations-Wirkungs - Bestätigung von primären Screening - Hits und CFU - Assays (Abbildung 1). Da eine einzelne CARA Platte zahlreiche Mikrotiterplatten erforderlich ersetzen kann, um serielle Verdünnungen herzustellen und Agar-haltigen Platten Petri verwendet überlebenden Bakterien aufzuzählen, stellt die CARA ein einfaches Mittel, um schnell zu einem Molekül der Aktivität zu bewerten und mehrere Variablen auf einmal zu testen, einschließlich Verbindungskonzentration und die Zeit der Exposition gegenüber der Verbindung.
In einem CFU - Assay, zusätzlich zur seriellen Verdünnungen, die 10 6 -fach Bereich bis oft die Agarplatte verdünnt typischerweise Moleküle durch eine zusätzliche ~ 800-fachen (10 & mgr; l auf 8 ml in einem tri-Petriplatte). Unsere zweistufigen, Multi-Stress Screening - Test für Verbindungen , die aktiv auf nicht-replizierenden M. tuberkulose hat einen Übertrag Faktor 5-fach, dh eine Verbindung , die in der nicht-replizierende Stufe des Assays auf ein Fünftel der ursprünglichen Konzentration in dem Auswuchs (Replizieren) Phase des Assays 6-9 vorhanden ist. Die CARA mildert Carry-Over-Effekte durch kleine Moleküle mit Aktivkohle zu maskieren. Die Mehrzahl der tuberculosis Medikamente und klinische Kandidaten binden Kohle schnell aktiviert und vollständig, mit Ausnahme der Aminoglykosid Streptomycin 7. Die Aufnahme von Aktivkohle in Agarplatten für CFU - Assays bakterielle Wachstumshemmung verhindert oder Bakterienabtötung durch übertragene TMC207 und PA-824 7,21,22. Somit aufgrund von Aktivkohle in der bakteriologischen Agar enthält, ist das CARA nicht abhängig von seriellen Verdünnungen von Zellen und Testmittel.
Die CARA kann bakteriostatische oder bakterizide Wirkung von replizierenden Wirkstoffe und bakterizide Wirkung von nicht-replizierenden Wirkstoffe helfen vorherzusagen. in general, die CARA ist parallel mit Standard - MIC 90 - Assays verwendet. Die Vorhersagekraft des CARA kommt aus dem Vergleich MIC 90 und CARA Ergebnisse (Abbildung 2 und Tabelle 1). Bei der Verwendung zur antimykobakteriellen Mittel studieren, kann die CARA genau Aktivität vorhersagen , die bakterizid (4a) repliziert wird , replizieren bakteriostatisch (Abbildung 4b), nicht-replizierenden bakterizid (4c) oder Dual - aktiv (4d). Die CARA erlaubt auch eine einfache Auswertung der Tätigkeit eines Verbindung über beide Dosis und Zeit. CFU - Assays erfordern allein viel Aufwand und Material Aktivität einer Verbindung über einen weiten Bereich von Dosierungen und Zeiten zu beurteilen, aber die Aufgabe wird überschaubar , wenn CARA Ergebnisse den Bereich von Bedingungen, wie sie verengen , in denen die Verbindung nachweislich aktiv ist (Abbildung 5 ).
Während die CARA hat Dienstprogramm, um die Wirkung eines in das StudiumNTI-infectives auf Mykobakterien, hat der Test Einschränkungen. Das CARA hat einen schmalen Dynamikbereich (2-3 log 10) und kann für Bedingungen , unter denen man erwartet , es nicht geeignet sein, nicht mehr als 2 bis 3 log 10 Bakterienabtötung ist. CARA Prognosen erfordern weitere Studie eine strengere und genaue Methode zur Bakterienzahlen, wie eine CFU-Assay aufzuzählen. Die post-antibiotische Wirkung einiger Antiinfektiva, wie PAS, die CARA als prädiktiver Werkzeug zwischen den Verbindungen mit bakterizide und bakteriostatische Wirkung gegen replizierende M. tuberculosis 7 zu unterscheiden verwechseln.
Es gibt zwei Empfehlungen, die Qualität der CARA zu verbessern. Zuerst muss man CARA gießen Mikrotiterplatten schnell vor den Agar sich verfestigt, während die volumetrische Genauigkeit beibehalten und außerhalb von Mikrotitervertiefungen Spritzwasser zu vermeiden. Unabhängig von der Anzahl von Platten erforderlich ist, empfehlen wir, 0,5 bis 1 L Chargen des Mediums, um die m aufrechtzuerhaltenedium in flüssiger Form für die Dauer der Zeitplatten zu gießen erforderlich. Ändern Spitzen häufig während mit mittlerer Füllung Mikrotiterplatten vermeidet teilweise verstopft Tipps. Zweitens muss eine artifactual Variabilität in der Fluoreszenz zwischen den Replikaten minimieren. Mykobakteriellen Mikrokolonien, insbesondere für pathogene Mycobakterien wie M. tuberculosis, wachsen häufig erratisch. Zum Beispiel können Mikrokolonien auf der Agaroberfläche wachsen variieren in Größe, Form, Höhe oder kann an den Innenwänden der Mikrotitervertiefungen erstrecken. Eine Herausforderung ist es, alle Bazillen gleichmäßig mit dem Entwicklungs Reagenz zu decken. Eine weitere Hürde ist, dass nach einer längeren Inkubation bei 37 ° C, der Feststoff bakteriologischen Medium der CARA Mikrotiterplatten trocken werden können und anfällig für die Entwicklung von Reagenz absorbiert. Da Aktivkohle binden Resazurin und löschen Fluoreszenz 7, kann es zu trockenen Brunnen durch gut-zu-gut Variante sein , die Resazurin Entwicklungslösung zu absorbieren und die aktivierte Charcoal Abschrecken Resazurin Fluoreszenz. Vorbenetzung sofort die Oberfläche aller CARA Mikrotitervertiefungen mit PBS vor dem Entwicklungs Reagenz Zugabe mildert diese beiden Probleme - das Entwicklungsreagens alle mykobakteriellen Kolonien gleichermaßen zu erreichen, und das Resazurin bleibt sicher oberhalb der Aktivkohle. Die CARA kann Anwendungen bei der Identifizierung und Phänotypen von Mykobakterien-Mutanten oder in mittlerem Durchsatz Drug Discovery-Assays für andere Bakterienarten zu charakterisieren.
Es gibt keine Interessenkonflikte offen zu legen.
Wir sind dankbar, dass Kristin Burns-Huang-für Expertensicht des Manuskripts und J. David Warren (Weill Cornell Medical College) für die Unterstützung der Chemie, während die CARA entwickeln. Diese Arbeit wurde von der TB Drug-Accelerator-Programm von der Bill und Melinda Gates-Stiftung, die Abby und Howard P. Milstein Programm in Translational Medicine, und ein NIH TB Research Unit (U19 AI111143) unterstützt. Die Abteilung für Mikrobiologie und Immunologie wird durch die William Randolph Hearst Foundation unterstützt. SSK wurde von NIH Zuschusses K08AI108799 unterstützt.
| Name | Company | Catalog Number | Comments |
| Middlebrook 7H9 | Beckton Dickinson | 271310 | |
| Middlebrook 7H11 | Beckton Dickinson | 298810 | |
| Middlebrook OADC | Beckton Dickinson | 212351 | |
| BSA, heat shock | Roche | 3118958001 | |
| activated charcoal | Sigma | C5510 | |
| PBS, Dulbecco's Ca2+ and Mg2+ free | Life Technologies / Invitrogen | 14190-144 | |
| tween 80 | Sigma | P8074 | |
| tyloxapol | Sigma | T8761 | |
| sodium nitrite | Sigma | 2252 | |
| rifampicin | Sigma | R3501 | |
| 6-bromo-1H-indazol-3-amine | Alfa Aesar | H34095 | |
| potassium phosphate monobasic | Sigma | P0662 | |
| magnesium sulfate, heptahydrate | Sigma | M1880 | |
| ferric ammonium citrate | Sigma | F5879 | |
| zinc sulfate, heptahydrate | Sigma | Z0251 | |
| ammonium chloride | Sigma | A9434 | |
| butyric acid, liquid | Sigma | B103500 | |
| resazurin powder | Sigma | R7017 | |
| sodium chloride | J.T. Baker | 4058-01 | |
| prepared resazurin solution | Invitrogen | DAL1100 | |
| PCR stickers | Denville | B1212-5 | |
| spectrophotometer | Molecular Devices | M5 | |
| 96-well, tissue culture treated microplates | Corning | 3595 | |
| reagent reservoirs | VWR | 89094-678 | |
| resealable plastic bags | VWR | 395-94602 | |
| 14 mL Polypropylene round-bottom tubes | Corning | 352059 | |
| 50 mL conical centrifuge tube | Corning | 352070 | |
| 75 cm2 Cell culture flask | Corning | 431464U | |
| clear, flat bottom tissue culture treated 96-well microplate | Costar | 3595 | |
| Prism 6 for OS X | GraphPad | http://www.graphpad.com/scientific-software/prism/ |
- Nathan, C. Fresh approaches to anti-infective therapies. Sci. Transl. Medicine. 4 (140), 140-142 (2012).
- Gomez, J. E., McKinney, J. D. M. tuberculosis persistence, latency, and drug tolerance. Tuberculosis (Edinb). 84, 29-44 (2004).
- Balaban, N. Q., Merrin, J., Chait, R., Kowalik, L., Leibler, S. Bacterial persistence as a phenotypic switch. Science. 305, 1622-1625 (2004).
- Bigger, J. Treatment of staphylococcal infections with penicillin by intermittent sterilisation. Lancet. , 497-500 (1944).
- Bryk, R., et al. Selective killing of nonreplicating mycobacteria. Cell Host Microbe. 3, 137-145 (2008).
- Gold, B., et al. Nonsteroidal anti-inflammatory drug sensitizes Mycobacterium tuberculosis to endogenous and exogenous antimicrobials. Proc. Natl. Acad. Sci. U.S.A. 109, 16004-16011 (2012).
- Gold, B., et al. Rapid, semi-quantitative assay to discriminate among compounds with activity against replicating or non-replicating Mycobacterium tuberculosis. Antimicrob. Agents Chemother. 59, 6521-6538 (2015).
- Gold, B., Warrier, T., Nathan, C., Parish, T., Roberts, D. . Mycobacteria Protocols, Methods in Molecular Biology. 1285, 293-315 (2015).
- Warrier, T., et al. Identification of Novel Anti-mycobacterial Compounds by Screening a Pharmaceutical Small-Molecule Library against Nonreplicating Mycobacterium tuberculosis. ACS Infect. Dis. , 580-585 (2015).
- Zheng, P., Chem, J. .. M. e. d. .., et al. Synthetic Calanolides with Bactericidal Activity Against Replicating and Nonreplicating Mycobacterium tuberculosis. J. Med. Chem. , (2014).
- Darby, C. M., et al. Whole cell screen for inhibitors of pH homeostasis in Mycobacterium tuberculosis. PLoS One. 8, e68942 (2013).
- Darby, C. M., Nathan, C. F. Killing of non-replicating Mycobacterium tuberculosis by 8-hydroxyquinoline. J. Antimicrob. Chemother. 65, 1424-1427 (2010).
- de Carvalho, L. P., Darby, C. M., Rhee, K., Nathan, C. Nitazoxanide Disrupts Membrane Potential and Intrabacterial pH Homeostasis of Mycobacterium tuberculosis. ACS Med. Chem. Lett. 2, 849-854 (2011).
- Xie, Z., Siddiqi, N., Rubin, E. J. Differential antibiotic susceptibilities of starved Mycobacterium tuberculosis isolates. Antimicrob. Agents Chemother. 49, 4778-4780 (2005).
- Grant, S. S., et al. Identification of novel inhibitors of nonreplicating Mycobacterium tuberculosis using a carbon starvation model. ACS Chem. Biol. 8, 2224-2234 (2013).
- Zhang, M., et al. Streptomycin-starved Mycobacterium tuberculosis 18b, a drug discovery tool for latent tuberculosis. Antimicrob. Agents Chemother. 56, 5782-5789 (2012).
- Mak, P. A., et al. A high-throughput screen to identify inhibitors of ATP homeostasis in non-replicating Mycobacterium tuberculosis. ACS Chem. Biol. 7, 1190-1197 (2012).
- Cho, S. H., et al. Low-oxygen-recovery assay for high-throughput screening of compounds against nonreplicating Mycobacterium tuberculosis. Antimicrob. Agents Chemother. 51, 1380-1385 (2007).
- Franzblau, S. G., et al. Comprehensive analysis of methods used for the evaluation of compounds against Mycobacterium tuberculosis. Tuberculosis (Edinb). 92, 453-488 (2012).
- Rebollo-Lopez, M. J., et al. Release of 50 new, drug-like compounds and their computational target predictions for open source anti-tubercular drug discovery. PLoS One. 10, e0142293 (2015).
- Tasneen, R., et al. Contribution of the nitroimidazoles PA-824 and TBA-354 to the activity of novel regimens in murine models of tuberculosis. Antimicrob. Agents Chemother. 59, 129-135 (2015).
- Grosset, J. H., et al. Assessment of clofazimine activity in a second-line regimen for tuberculosis in mice. Am. J. Respir. Crit. Care Med. 188, 608-612 (2013).
- Shiloh, M. U., Ruan, J., Nathan, C. Evaluation of bacterial survival and phagocyte function with a fluorescence-based microplate assay. Infect. Immun. 65, 3193-3198 (1997).
- Wang, F., et al. Identification of a small molecule with activity against drug-resistant and persistent tuberculosis. Proc. Natl. Acad. Sci. U.S.A. 110, E2510-E2517 (2013).
- Wayne, L. G., Hayes, L. G. An in vitro model for sequential study of shiftdown of Mycobacterium tuberculosis through two stages of nonreplicating persistence. Infect. Immun. 64, 2062-2069 (1996).
- Barry, A. L., et al. . Methods for determining bactericidal activity of antimicrobial agents: approved guideline. 19, (1999).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved