Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Immunology and Infection
Visualisering av Charcoal Agar Resazurin analyse for Semi-kvantitativ, Medium-throughput telling av mykobakterier
The charcoal agar resazurin assay (CARA) is a semi-quantitative, medium-throughput method to assess activity of test agents against mycobacteria that are replicating, non-replicating, or both. The CARA permits rapid evaluation of time- and concentration-dependent activity and identifies parameters to pursue by colony forming unit (CFU) assays.
Det er et presserende behov for å oppdage og utvikle seg antiinfektiva som forkorter varigheten av tuberkulose (TB) behandling. Mycobacterium tuberculosis, det etiologiske middel av TB, er upåvirkelig for rask og vedvarende kjemoterapi på grunn av tilstedeværelsen av bacilli utviser fenotypiske medikamentresistens. Den c harcoal en gar r esazurin en ssay (CARA) ble utviklet som et verktøy for å karakterisere aktive molekyler oppdaget av high-throughput screening kampanjer mot replikere og ikke-reproduserende M. tuberculosis. Inkludering av aktivt kull i bakteriologiske agar medium bidrar til å redusere effekten av sammensatte carry-over, og eliminerer behovet for å pre-fortynne celler før spotting på CARA mikro. Etter en 7-10 dagers inkuberingsperiode ved 37 ° C, reduksjon av resazurin av mykobakterielle mikrokolonier som vokser på overflaten over Cara mikroplate brønnene tillater semikvantitativ assevurdering av bakterietall via fluorometri. Den CARA oppdager omtrent en 2-3 log 10 forskjell i bakterietall og spår en minimal bakteriedrepende konsentrasjon fører til ≥99% bakteriell drepe (MBC ≥99). Cara på å avgjøre hvorvidt et molekyl som er aktiv på basiller som er replikere, ikke-replikerende, eller begge deler. Pilot eksperimenter med Cara lette identifiseringen av hvilken konsentrasjon av testmiddel og tid av forbindelse eksponering kreve ytterligere evaluering av kolonidannende enhet (CFU) analyser. I tillegg kan CARA forutsi om replikere Actives er bakteriedrepende eller bakteriostatisk.
Mycobacterium tuberculosis, den agens av tuberkulose, kan overleve i en vert i en latent tilstand som ikke kan behandles med antibiotika utrydding. Fenotypiske (ikke-genetisk) motstand av M. tuberculosis under infeksjon antas å skyldes, delvis, til populasjoner av ikke-reproduserende basiller 1,2. Oppstå i klasse I persisters viser fenotypisk resistens via sjeldne stokastiske mekanismer blant store grupper av narkotika sensitive celler 3,4. Klasse II persisters gjengis ikke-reproduserende av faktorer av verten immunitet, inkludert ytre påkjenninger i microenvironments oppstått under infeksjon. Vi har nylig utviklet en in vitro modell av klasse II ikke-reproduserende utholdenhet for å etterligne forholdene konfrontert med M. tuberculosis i aktiverte makrofager og granulomer. Den multi-stress modell av klasse II persistens omfatter forutsetning av at langsom vekst, slik som en fettsyre karbonkilde, og helt halt vekst, såsom mild syre (pH 5,0), hypoksi (1% O 2), og nitrogenoksid og andre reaktive nitrogenmellomprodukter 5-9. Storskala screening ved anvendelse av denne multi-stress modell av ikke-replikasjon, og andre klasse II ikke-reproduserende modeller, har resultert i forskjellige molekyler hvis aktivitet er rettet mot den ikke-reproduserende tilstand 5-7,9-18. De samme ikke-reproduserende skjermer også avdekket en kategori av molekyler som innehar aktivitet mot både replikere og ikke-replikerende basiller, kalt "dual aktive" 7,10,12,19,20.
Antibakteriell stoffet funnet i hit-til-ledelsen fase innebærer omfattende karakterisering av kandidatmolekyler for å velge leder for hit ekspansjon, foreløpig farmakologisk karakterisering, mål identifikasjon, og foreløpige studier in vivo effekt. Som et tidlig trinn blir antiinfektiva klassifisert etter deres bakteriostatisk eller bakteriedrepende virkningsmekanisme, og hvis bakteriedrepende, whether bakteriell kill er tids- og / eller konsentrasjonsavhengig. Den kolonidannende enhet (CFU) analysen er den klassiske, gull standard metode for å håndtere disse spørsmålene. I CFU-analysen, blir bakterier utsettes for en testmiddel, hvoretter alikvoter fjernes, fortynnet i serie, og alikvoter av fortynninger er spredt på fast bakteriologiske medium og inkubert for å tillate vekst av overlevende celler. Endelig er bakteriekolonier nummerert. CFU-assay krever et stort antall mikrotiterplater for å fortynne cellene og agar inneholdende Petri-plater for å telle overlevende kolonier. CFU-analysen for langsomtvoksende mykobakterier er hemmet av sin langsomme generasjon tid (18-24 timer), noe som krever omtrent 3 uker for kolonier som skal vises på platene. Videre er inkubatorplass ofte begrenset i spesialiserte biosikkerhet-nivå-3 anlegg.
Mens tungvint, CFU analysene er gullstandarden for å karakterisere virkningen av ikke-reproduserende og dual-aktive molekyler på mycobacteria. Ikke-reproduserende analyser er underlagt høye falske positive priser som mange er koplet til replikere analyser for å vurdere cellulær levedyktighet 6-8. For eksempel kan en forbindelse som har sterk aktivitet mot replikere M. tuberculosis (en "replikerende aktiv") kan mislykkes i å drepe i løpet av den ikke-reproduserende assay, men kan likevel drepe i kraft av overheng fra den ikke-reproduserende fase av analyse for å restitusjonsfasen av forsøket, som er utført under betingelser som støtter replikasjon ( "replikerende forhold"). Forbindelse bære over ytterligere kompliserer analyse av to aktive molekyler, noe som gjør det vanskelig å skille hvorvidt aktiviteten ble replikerende, ikke-replikerende, eller dobbel.
For å løse problemene som er beskrevet ovenfor, har vi utviklet c harcoal en gar r esazurin en ssay (CARA) for rask, semi-kvantitativ telling av mykobakterielle arter som M. tuberculosis, M. bovis BCG og M. smegmatis 7 (figur 1 og 2). I bufferløsninger in vitro, aktivt kull sequesters raskt meste av standard legemidler som brukes til behandling av tuberkulose 7. Aktivt kull i CARA mikro binder forbindelser som kan bære over fra en analyse mikro, og denne funksjonen av CARA eliminerer kravet om å serielt fortynne analysen vel innholdet før telling 7,21,22. Antallet mykobakterielle mikrokoloniene på agaroverflaten av CARA mikroplater blir estimert ved tilsetning av resazurin, et blått fargestoff, som har redusert form, resorufin, er en rosa molekyl hvis fluorescens blir målt ved en spektrofotometri 23. CARA mikro inkuberes i 1-2 dager for M. smegmatis og 7-10 dager for langsomt voksende mykobakterier som M. tuberculosis og M. bovis BCG. Den CARA har et smalt dynamisk område på ~ 2-3 log 10 diffeRence i CFU. Når den brukes i stedet for en CFU assay, erstatter en enkelt CARA mikro omtrent fem 96-brønners plater som brukes til serie-fortynninger og 120 tri-stil agarplater som brukes for plettering. Tolkning av CARA data hjelper veilede senere studier ved å bestemme hvilke inkubasjon tider og sammensatte konsentrasjoner for å teste i mer arbeidskrevende CFU-baserte analyser.
1. Utarbeidelse av CARA Mikro
- Autoklaver 900 ml Middlebrook 7H11 agar inneholdende 0,2% glycerol og 0,4% aktivt kull i en 2 liters Erlenmeyer-kolbe, eller alternativt, 450 ml i en 1-liters begerglass. Ta med en stor autoklaverrørepinne i kolben eller beger. Dekke åpningen av flasken eller beger med aluminiumsfolie og fester seg til glass med autoklav tape.
- Avkjøl til berøring (ca. 55-65 ° C) på en magnetisk røreplate innstilt på en lav hastighet for å opprettholde den trekull i suspensjon.
- Utfør alle påfølgende trinn aseptisk i en biosikkerhet hette som har en magnetisk røreplate.
- Fjern folien. Tilsett 100 ml OADC supplement (OADC supplement, når de anvendes på 10%, utbytter sluttkonsentrasjoner på 0,2% dekstrose, 0,5% albumin, 0,085% NaCl, 0,0005% oljesyre, og 0,4 mg / ml katalase media) til 2 liter Erlenmeyer kolbe eller 50 ml OADC til 1 liter begerglass, og fortsette blanding.
- Hvis du bruker en Erlenmeyerkolbe, hell ca 25-40 ml 7H11-OADC-trekull i et sterilt reagens reservoar. Ved hjelp av begerglasset, er det ikke nødvendig å bruke et reagens reservoaret.
- Fyll en 96-brønns mikroplate med 200 ul / brønn av 7H11-OADC-trekull fra reagensreservoaret eller beger. Arbeid raskt for å unngå agar størkning og introduksjon av bobler. Unngå spruting fast medium utsiden av brønnene, slik som kan være en kilde til soppforurensning. Ved hjelp av en multikanal pipette, bruke ett sett med 12 filter tips for overføring av 7H11-OADC-kull til 8 p (AH) av 96-brønns plate.
MERK: Mediet stivner raskt. For å unngå tilstopping pipettespisser, endre dem ofte. - Alternativt, hell CARA mikro bruker en P1000 elektronisk multikanalspipette med filter tips som skal bistå med en rekke plater.
MERK: På grunn av lavt volum av mikroplate brønnene, agar i CARA mikro stivner i løpet av minutter helle. - Plasser bunker med CARA mikro i lukkbare plast bags å unngå uttørking.
- Oppbevares CARA mikro ved 4 ° C.
2. Sette opp Replikere og ikke-reproduserende MIC 90 Analyser
- Vaksinere M. tuberculosis, M. bovis BCG eller M. smegmatis på en OD 580 av 0,01-0,1 og utvide til midt-log fase (OD 580 ~ 0,5) i Middlebrook 7H9-ADN (Middlebrook 7H9 inneholder 0,2% glycerol, 0,2% dekstrose , 0,5% albumin, og 0,085% NaCl) eller Brook 7H9-OADC (Middlebrook 7H9 inneholdende 0,2% glycerol og 10% supplement OADC).
- Grow M. tuberculosis og M. bovis BCG som ~ 20 ml stående kulturer i cellekulturflasker og M. smegmatis med risting i polypropylen rund bunn (4 ml kultur) eller 50 ml konisk sentrifugerør (10-20 ml kultur). Inkuber patogene mykobakterier ved 37 ° C med 20% O2 og 5% CO2, og M. smegmatis ved 37 ° C med 20% O2.
- Sett opp en minimal-hemmendekonsentrasjon (MIC 90) -stil eksperiment henhold replikere og ikke-reproduserende forhold (figur 2).
MERK: Testmidler blir vanligvis analysert i duplikat eller quadruplicates for å tillate testing 4, eller 2-forbindelser, henholdsvis per 96-brønns mikroplate. For eksempel, i en 96-brønners plate, en testmiddel kan bli analysert i rader AD og en annen i rader EH. DMSO (bærer) er i kolonne 1, 2 og 12, og testmidlet fortynningsserie går fra kolonne 3 (laveste konsentrasjon) til kolonne 11 (høyeste konsentrasjon). MIC 90 -stil analyser bruker vanligvis to ganger fortynning serien. Det er mange ikke-reproduserende modeller tilgjengelig for mykobakterier 14-16,18,24,25 og veiledende, vi bruker en multi-stress-modellen av ikke-replikering 6,8,9.- For replikerende analysen, distribuere 200 ul celler i Brook 7H9-ADN ved en OD 580 på 0,01 i alle brønner av en klar bunn, vevskultur behandlede 96-brønns plate. <li> For den ikke-reproduserende assay, vaskes cellene to ganger i fosfatbufret saltvann (PBS) inneholdende 0,02% tyloksapol, og resuspender cellene i ikke-reproduserende medium (0,05% KH 2PO 4, 0,05% MgSO4, 0,005% jern-III-ammoniumcitrat , 0,0001% ZnCl2, 0,1% NH4CI, 0,5% BSA, 0,085% NaCl, 0,02% tyloksapol, 0,05% butyrat, pH ble justert til 5,0 med 2 N NaOH).
- Fortynn cellene til en OD 580 på 0,1 i ikke-reproduserende medium og tilsett NaNO2 fra en nyfremstilt 1M lager til en sluttkonsentrasjon på 0,5 mM.
- Fordel 200 ul celler til en OD 580 på 0,1 i alle brønner av en klar bunn, vevskultur behandlede 96-brønns plate.
MERK: Forbered sammensatte fortynninger som 100-fold stamløsninger i DMSO. Dermed vil en typisk MIC plate testing av virkningen av et molekyl ved en sluttkonsentrasjon 0,4 til 100 pg / ml ville kreve stamløsninger av 0,04 til 10 mg / ml i DMSO.
- Tilsett 2 mL av dinologi av testmiddel 1 i rader AE og 2 mL fortynninger av testmiddel 2 i rader EH. Bland grundig.
- Tilsett 2 mL bærerkontroll (vanligvis DMSO) i kontrollbrønnene, kolonnene 1, 2, 12 (rader AH). Bland grundig.
- For hvert eksperiment, omfatter minst en positiv kontroll som rifampicin fra 0,004 til 1 ug / ml (replikerende assay) og / eller 0,08 til 20 ug / ml (ikke-reproduserende assay).
MERK: Anvendelse av 6-brom-1 H-indazol-3-amin 9 ved 0,1 til 25 ug / ml anbefales som en kontrollforbindelse som har selektiv, NaNO2 -avhengig aktivitet i multi-stress modell av ikke-replikasjon. - For replikerende assays, inkubere mikroplater ved 37 ° C med 20% O2 og 5% CO2 i 7 dager (M. tuberculosis og M. bovis BCG) eller 1-48 hr (M. smegmatis). For multi-stress modell av ikke-replikasjon, inkuber mikro i 7 dager ved 37 ° C ved 1% O2 og 5% CO2 (<em> M. tuberkulose og M. bovis BCG).
3. Inokulering av CARA Mikro
- På tidspunkter der CARA vil bli brukt som en lese-out, nøye resuspender vel innholdet i MIC 90 -stil analyseplaten ved hjelp av en P200 multikanalspipette satt til 50-75 mikroliter. Pipette opp og ned minst 5-10 ganger og virvle brønn innholdet i en sirkulær bevegelse ved hjelp pipettespissene.
- Overfør 10 mL av analysen vel innhold til CARA mikro. Sørg for at rekkefølgen av brønn innholdet på analyseplaten stemmer overens med rekkefølgen av brønn innholdet i CARA mikro. Unngå sprut under transport og sørge for at de 10 mL er oppdaget i midten av CARA mikroplate brønnene. Bekreft 10 pl absorberer inn i CARA mikro.
MERK: Det er ingen fortynninger som kreves før spotting celler på CARA mikroplater. - Bind stabler av CARA mikroplater med plate tape ogderetter plassere i en plastpose som kan forsegles. Inkuber CARA mikroplater ved 37 ° C med 20% O 2 (M. smegmatis) eller 1% O2 og 5% CO2 (M. tuberculosis og M. bovis BCG).
- For M. tuberculosis og M. bovis BCG, replikere analyser: ruge i 7 dager; for M. tuberculosis og M. bovis BCG ikke-reproduserende analyser, inkuberes i 10 dager; for M. smegmatis, replikere analyser, inkuber i 1-2 dager; for M. smegmatis, ikke-reproduserende analyser, inkuber 2-3 dager.
MERK: Tidene er estimater og kan endres tilsvarende for annen replikere, ikke-reproduserende, og spenningstilstander.
4. Utvikle CARA Mikro
- Utvikle CARA mikro når en film av bakterievekst, eller større, makroskopiske kolonier, er synlige på negative (vehicle) kontrollbrønner.
MERK: Etter langvarig inkubasjon, CARA mikroplate brønnene oftevises tørr og vi anbefaler forvanning godt innhold med sterilt PBS. Dette tjener til å hindre at kull fra å absorbere resazurin, noe som kan føre til lav fluorescens eller brønn-til-brønn variasjon. - Ved hjelp av et enkelt sett med 12 P200 tips med en multikanal pipette, fordeles 40 ul steril PBS langs siden av brønnene og la PBS for å fordele over toppen av agar / bakterielle mikrokoloniene.
- Forbered CARA utvikle reagens ved å blande 5 mg resazurin (0,01% sluttkonsentrasjon) og 50 ml 5% Tween80 i PBS. Vortex og sterilt filter.
MERK: En alternativ CARA fremkallingsmiddel kan fremstilles ved å blande kommersielt forberedt resazurin flytende oppløsning ved 1: 1 (vol / vol) med 10% Tween80 i PBS. - Tilsett 50 pl av ferskt tilberedte CARA utvikle reagens til hver brønn på CARA mikroplate ved hjelp av en 12-kanals pipette. Rock plater frem og tilbake noen ganger for å bidra til å fordele reagens over agar og bakterielle matte i hver brønn.
- Plasser platene jegna plastpose som kan forsegles og inkuberes ved 37 ° C i minst 30 min for M. smegmatis og 45-60 min for M. tuberculosis eller M. bovis BCG.
MERK: Dersom kjøretøyet kontrollbrønner klarer å bli rosa i løpet av den første timen, platene kan gjen Bagasje og inkubert i lengre perioder av gangen. - Før du leser fluorescens, plasserer CARA mikro i en biosikkerhet hette i 15 minutter ved romtemperatur med sine lokkene fjernet. Når du bruker BSL3 spektrofotometre utenfor en biosikkerhet kabinett, holder en optisk kvalitet PCR klistremerke over platen og slutter tett ved å trykke forsiktig på klistre overflaten med en myk papirhåndkle.
- Bestem fluorescens via toppen lese med eksitasjon ved 530 nm og emisjon ved 590 nm. Det er ikke nødvendig å blank plate.
5. Data Analysis
- Plot inhibitor konsentrasjon på X-aksen på en log skala 10 og fluorescens på Y-aksen på en lineær skala. Bruk en scatterTomten ansette en kurve passer eksempel "logg hemmer versus respons variabel helning (4 parametre)". Plot datapunkter som betyr ± standardfeil.
Forventede CARA Resultatene er beskrevet i figur 2 og oppsummert i tabell 1. For replikerende celler, blir Cara kjøres parallelt med en standard MIC 90 analyser, og for ikke-replikerende analyser, blir Cara drives i parallell med et tilpasset MIC 90 assay som er koplet til en utvekst fase. Den konsentrasjon av testmiddel som resulterer i svikt av CARA-fluorescens å stige over bakgrunnsnivået er Cara-MBC ≥99 (figur 3a). Den "≥99" senket indikerer at CARA-MBC gir en beregnet konsentrasjon av testmiddel som gir opphav til ≥2 log 10 bakteriell drepe (≥99% kill).
Den flytende buljong MIC 90-analysen er i stand til å skille mellom bakteriedrepende og bakteriostatisk aktivitet og dette skillet må løses ved en CFU analysen. Avkonvensjonen, terskelen som skiller bakteriedrepende fra bakteriostatisk aktivitet for saktevoksende mykobakterier er ca 2-3 log 10 drap i løpet av 7 dager 7,26. Siden det dynamiske område for Cara er også 2-3 log 10 drepe, kan Cara tilveiebringe et estimat av baktericid eller bakteriostatisk aktivitet. Den CARA lett identifiserer noen replikere aktive som bakteriostatisk til som følge av disse forbindelsene for å redusere CARA fluorescens bakgrunnsnivå (figur 2). Men noen forbindelser med bakteriostatisk aktivitet mot replikerende M. tuberculosis har en potent post-antibiotisk virkning, noe som betyr at de fortsetter å hemme gjenvekst av bakterier under gjenvinningsfasen, selv i fravær av forbindelse overheng. Denne effekten kan være vanskelig å gjenkjenne i Cara analysen. Forbindelser er mistenkt for å utøve en post-antibiotisk virkning hvis de viser en "statisk vindu", definert som en> 4-gangers forskyvning til høyre between MIC og CARA kurver (figur 3b). Den statiske vinduet indikerer at et molekyl aktive mot replikere M. tuberculosis kan være bakteriostatisk stedet for bakteriedrepende. I noen tilfeller, de statiske vinduene er synlig etter inspeksjon av et ekspandert Y-aksen for CARA fluorescens (figur 3c og 3d).
CARA og MIC 90 data er vanligvis plottet sammen (figur 4). Representative data for replicating- og ikke-replikerende-aktive molekyler som ble testet ved MIC 90 og CARA er vist i figur 4. Det er 4 store aktivitet klasser for molekyler: 1) replikere bakteriedrepende (demonstrert med isoniazid, figur 4a); 2) replikere bakteriostatisk (demonstrert med linezolid, figur 4b); 3) ikke-reproduserende bakteriedrepende (demonstrert med oksyfenbutason, figur 4c); og 4) replicating-aktiv (bakteriostatisk eller bakteriedrepende) og ikke-reproduserende bakteriedrepende (demonstrert med PA-824, figur 4d). Viktigere, Figurene 4a og 4b viser at mens isoniazid og linezolid synes å ha aktivitet mot ikke-replikerende bakterier av MIC-analysen 90, antyder Cara de er inaktive under de ikke-replikerende testede betingelser. For å teste anvendeligheten av Cara i å forutsi et molekyl som er tids- og konsentrasjonsavhengig effekt, replikerende M. smegmatis ble utsatt for økende konsentrasjoner av rifampicin (figurene 5a - d), og på forskjellige tidspunkter mellom 1-24 timer ble aliquoter flekket på CARA plater. Disse data indikerte at rifampicin utøves en påvirkning så tidlig som i 1 time (figur 5a), viste økt baktericid aktivitet mellom 3 og 24 timer (figurene 5b-d), og drepte ≥2-3 log 10 på ~ 10 pg / ml ved to4 timer (figur 5d). Et lignende eksperiment testing quadruplicates av en bærerkontroll og 9 medikamentkonsentrasjoner, og ved 4 tidspunkter, ville være prohibitive ved en standard CFU-baserte analysen.
Således har CARA en rolle i medisiner som et medium-throughput, hurtig mekanisme for å identifisere et molekyl aktivitetsprofil. CARA spådommer bør strengt evaluert ved hjelp av en standard CFU analysen. Tilsetningen av 0,4% aktivkull til Petri-plater for CFU-analysen kan bidra til å forbedre korrelasjon til CARA data, og kan gi en mer nøyaktig CFU tellinger, størrelsen av korreksjonen generelt å være proporsjonal med forbindelsens styrke 21,22.
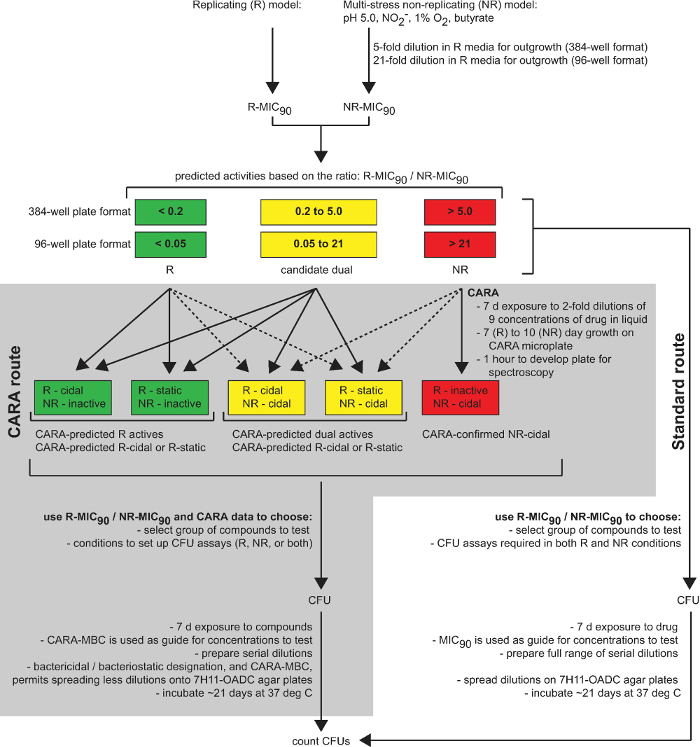
Figur 1: CARA er en prediktiv verktøy i medisiner. Dette diagrammet oppsummerer nytten av CARA som enmellomstadium mellom narkotika screening (single point screening, cherry-picking, og dose-respons-analyser) og tidkrevende hit-til-bly-analyser (CFU-analyser og målet identifikasjon). [Hentet med tillatelse fra Gold et al., Antimicrobial Agents and Chemotherapy 2015 7] Klikk her for å se en større versjon av dette tallet.
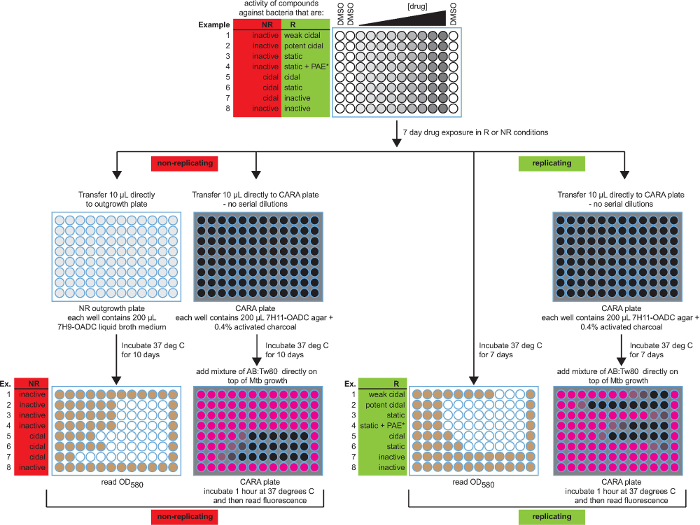
Figur 2: Skjematisk av kjøttkraft MIC 90 analysen og CARA med forventede resultater. Begge MIC 90 og CARA resultatene blir presentert for 8 mulige aktiviteter. Den fargekoding for MIC 90 mikroplate brønnene er hvit (ingen vekst) og brun (vekst), og for CARA mikro er svart (ingen fluorescens) og rosa (resorufin fluorescens). Dataene er hypotetisk. [Tilpasset med tillatelse fra Gold et al., Antimicrobial Agents and Chemotherapy 2015 7] Klikk her for å se en større versjon av dette tallet.
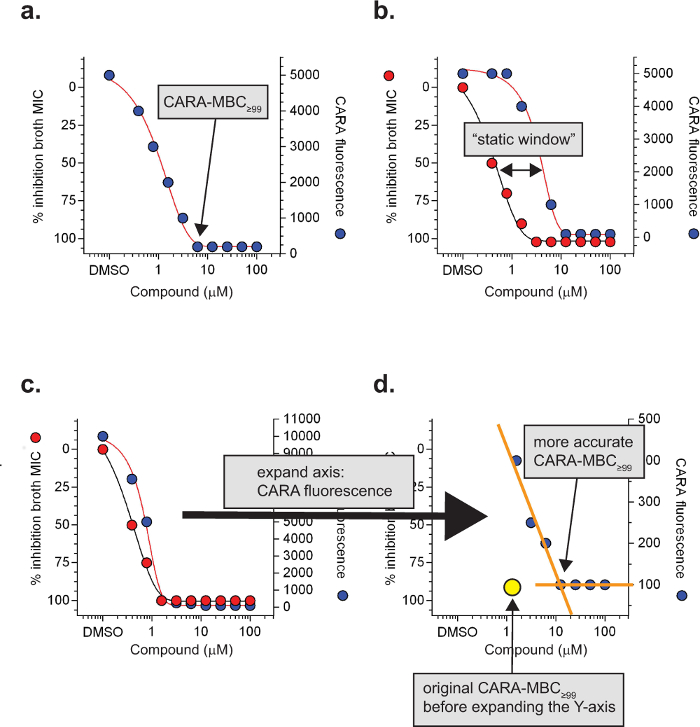
Figur 3: Spesielle CARA begreper og definisjoner. Den minimale baktericide konsentrasjonen av et molekyl som fører til bakgrunnsnivåer av CARA fluorescens er Cara-MBC ≥99 (a). Under replikerende betingelser, en ≥4 gangers forskyvning av Cara-MBC ≥99 til høyre for MIC 90 indikerer ofte bakteriostatisk aktivitet, og som kalles en "statisk-vindu" (b). For molekyler med en potent post-antibiotiske virkning, kan statiske vinduer være vanskelig å observere (c) og kreverutvidelse av Y-aksen (CARA fluorescens) for å visualisere (d). Dataene er hypotetisk. [Hentet med tillatelse fra Gold et al., Antimicrobial Agents and Chemotherapy 2015 7] Klikk her for å se en større versjon av dette tallet.
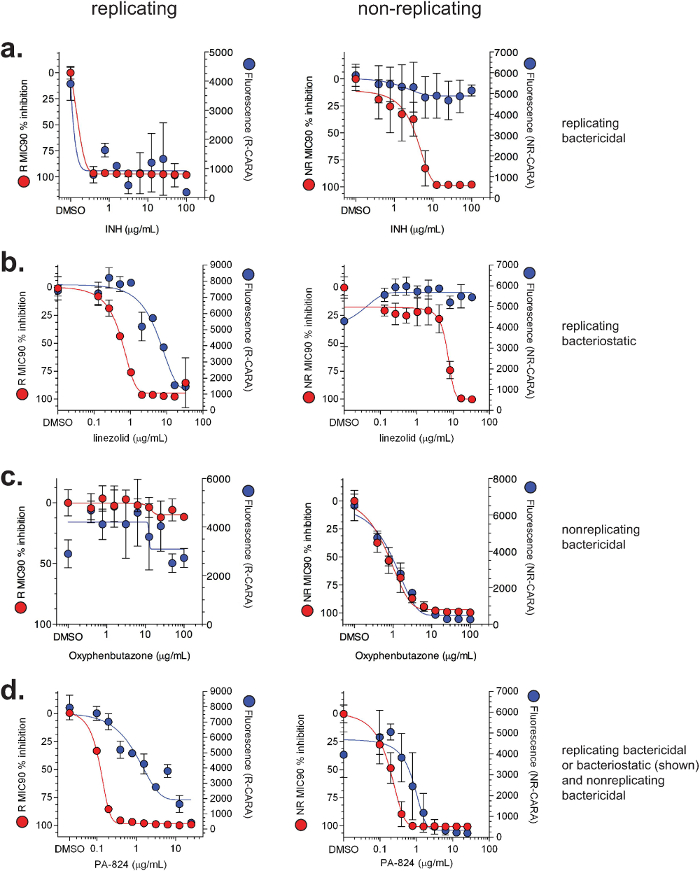
Figur 4: Illustrasjons MIC 90 og CARA resultater for utvalgte forbindelser. Data for MIC 90 (rød) og CARA (blå) er vist for (a) isoniazid (INH), (b) linezolid, (c) oksyfenbutazon, og (d) PA-824. Villtype M. tuberculosis H37Rv ble eksponert for forbindelsene i 7 dager under standardbetingelser Replikere eller multi-stress modell av ikke-replikasjon 7-9. MIC 90-analyser og CARA ble utført som vist i figur 2. [Hentet med tillatelse fra Gold et al., Antimicrobial Agents and Chemotherapy 20157]Klikk her for å se en større versjon av dette tallet.
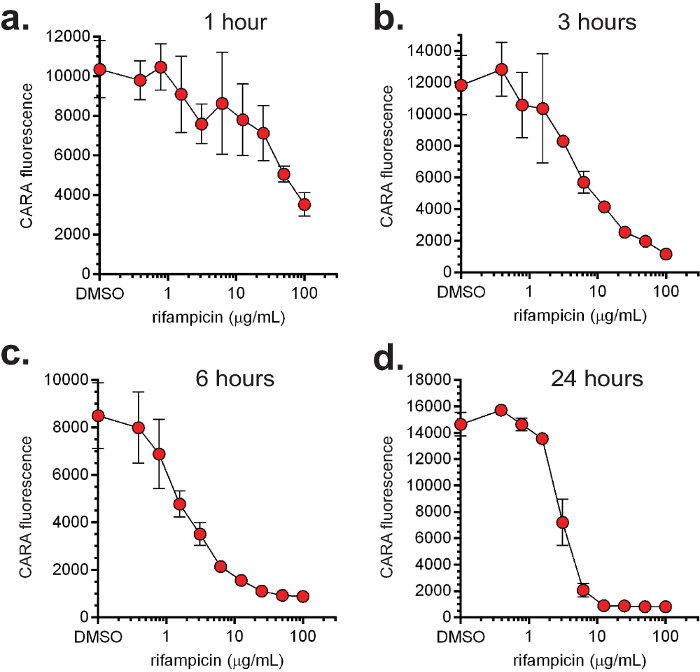
Figur 5: dose- og tidsavhengig aktivitet av rifampicin. Den ikke-patogene, hurtigvoksende M. smegmatis ble utsatt for økende konsentrasjoner av rifampicin i henhold replikerende betingelser og prøver ble samlet inn for CARA ved 1 (a), 3 (b), 6 (c) og 24 (d) hr. [Hentet med tillatelse fra Gold et al., Antimicrobial Agents and Chemotherapy 2015 7].com / filer / ftp_upload / 54690 / 54690fig5large.jpg "target =" _ blank "> Klikk her for å se en større versjon av dette tallet.
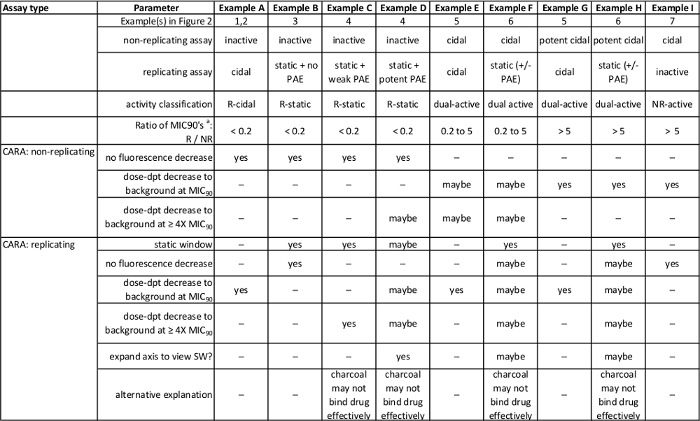
Tabell 1: Oversikt over forventede resultater i figur 2. [Hentet med tillatelse fra Gold et al., Antimicrobial Agents and Chemotherapy 2015 7] Klikk her for å se en større versjon av denne tabellen.
Den CARA ble opprinnelig utviklet for å lindre en flaskehals i framdrift ikke-reproduserende eller dual-aktive molekyler 7. Cara tjener som et mellomliggende trinn mellom konsentrasjon-respons bekreftelse av primære screening treff og CFU-analyser (figur 1). Siden en enkelt CARA plate kan erstatte mange mikrotiterplater forpliktet til å utarbeide serielle fortynninger, og agar-holdige Petri plater som brukes til å nummerere overlevende bakterier, gir en enkel måte å vurdere raskt et molekyl aktivitet og teste flere variabler samtidig, inkludert sammensatte konsentrasjon av CARA og eksponeringstiden til forbindelsen.
I en CFU-analyse, i tillegg til serielle fortynninger som ofte strekker seg opp til 10 6-doble, agarplaten fortynner typisk molekyler ved en ytterligere ~ 800-fold (10 ul ut mot 8 ml i en tri-stil Petri-plate). Våre to-trinns, multi-stress screening test for forbindelser aktive på ikke-reproduserende M. tuberculosis har et overheng faktor av 5-ganger, det vil si en forbindelse som er tilstede i den ikke-reproduserende trinn av analysen er til stede ved en femtedel den opprinnelige konsentrasjon i utveksten (replikerende) fase av analysen 6-9. Cara reduserer bære-over effekter av avsette små molekyler med aktivt kull. Flertallet av tuberkulose og kliniske kandidater binder aktivert trekull raskt og fullstendig, med unntak av streptomycin 7 aminoglykosider. Inkludering av aktivt kull i agarskåler for CFU analyser forhindret bakterieveksthemming, eller bakteriell drepe, etter gjennomført-over TMC207 og PA-824 7,21,22. Således, i kraft av å inkorporere aktivkull i den bakteriologiske agar, er Cara ikke avhengig av seriefortynninger av celler og testmiddel.
Den CARA kan bidra til å forutsi bakteriostatisk eller bakteriedrepende virkningen av replikere aktive og bakteriedrepende virkningen av ikke-reproduserende aktive. i gGenerell in, Cara er brukt i parallell med standard MIC 90 analyser. Den prediktive kraften i CARA kommer fra sammenligne MIC 90 og resultater CARA (figur 2 og tabell 1). Når den brukes til å studere anti-mycobakterielle midler, kan Cara nøyaktig forutsi aktiviteten som replikerer bakteriedrepende (figur 4a), replikere bakteriostatisk (figur 4b), ikke-reproduserende baktericid (figur 4c), eller dobbel aktiv (figur 4d). Den CARA tillater også enkel evaluering av en forbindelses aktivitet på tvers av både dose og tid. CFU-analyser alene krever mye arbeid og materiale for å vurdere aktiviteten av en forbindelse over et vidt område av doser og tidspunkter, men oppgaven blir overkommelig når CARA resultater begrense det område av betingelser for slike hvor forbindelsen er beviselig aktiv (Figur 5 ).
Mens Cara har anvendelse i å studere virkningen av enNTI infeksjons på mykobakterier, har analysen begrensninger. Den CARA har et smalt dynamisk område (2-3 log 10), og kan ikke være egnet for forholdene der man forventer det kan ikke være mer enn 2-3 log 10 bakteriell drepe. CARA spådommer krever videre studier ved hjelp av en mer stringent og nøyaktig metode for å telle bakterietall, for eksempel en CFU analysen. Den post-antibiotisk effekt av enkelte antiinfektiva som PAS, kan forvirre CARA som en prediktiv verktøy for å skille mellom forbindelser med bakteriedrepende og bakteriostatisk aktivitet mot replikere M. tuberculosis 7.
Det er to anbefalinger for å bedre kvaliteten på CARA. Først må man helle CARA mikroplater raskt før de agar størkner, og samtidig opprettholde volumetrisk nøyaktighet og å unngå sprut utenfor mikrobrønnene. Uavhengig av antall plater som kreves, anbefaler vi å lage 0,5 til 1 L grupper av medium for å opprettholde medium i flytende form i løpet av den tid som kreves for å helle platene. Endre tips ofte mens du fyller mikro med medium unngår å bruke delvis tilstoppede tips. For det andre må man redusere kunstig variasjon i fluorescens mellom replikater. Mykobakterielle mikrokolonier, særlig for patogene mykobakterier slik som M. tuberculosis, ofte blir uberegnelig. For eksempel kan mikrokolonier som vokser på agaroverflaten variere i størrelse, form, høyde, eller kan strekke seg opp til de indre vegger av mikroplatebrønner. En utfordring er å dekke alle basiller jevnt med utviklings reagens. Et annet hinder er at etter forlenget inkubering ved 37 ° C, kan det faste bakteriologiske medium av Cara mikroplater blir tørr og utsatt for å absorbere det fremkallende reagens. Siden aktivt kull kan binde resazurin og slukke fluorescensen 7, kan det være godt-til-brønn variasjon på grunn av tørre brønner absorbere den resazurin fremkallingsløsningen og det aktiverte Charcoal slukke resazurin fluorescens. Pre-fukte overflaten av alle CARA mikroplate brønnene med PBS umiddelbart før du legger den tredje reagent demper begge disse problemene - utviklings reagent vil nå alle mykobakterielle kolonier likt, og resazurin forblir trygt over aktivt kull. Den CARA kan ha programmer i å identifisere og karakterisere fenotyper av mykobakterielle mutanter, eller i medium-throughput drug discovery-analyser for andre bakteriearter.
Det er ingen interessekonflikter å avsløre.
Vi er takknemlige for Kristin Burns-Huang for sakkyndig vurdering av manuskriptet og J. David Warren (Weill Cornell Medical College) for kjemi assistanse mens utvikle CARA. Dette arbeidet ble støttet av TB Drug Accelerator Program av Bill og Melinda Gates Foundation, Abby og Howard P. Milstein Program i translasjonell medisin, og en NIH TB Research Unit (U19 AI111143). Avdeling for mikrobiologi og immunologi støttes av William Randolph Hearst Foundation. SSK ble støttet av NIH stipend K08AI108799.
| Name | Company | Catalog Number | Comments |
| Middlebrook 7H9 | Beckton Dickinson | 271310 | |
| Middlebrook 7H11 | Beckton Dickinson | 298810 | |
| Middlebrook OADC | Beckton Dickinson | 212351 | |
| BSA, heat shock | Roche | 3118958001 | |
| activated charcoal | Sigma | C5510 | |
| PBS, Dulbecco's Ca2+ and Mg2+ free | Life Technologies / Invitrogen | 14190-144 | |
| tween 80 | Sigma | P8074 | |
| tyloxapol | Sigma | T8761 | |
| sodium nitrite | Sigma | 2252 | |
| rifampicin | Sigma | R3501 | |
| 6-bromo-1H-indazol-3-amine | Alfa Aesar | H34095 | |
| potassium phosphate monobasic | Sigma | P0662 | |
| magnesium sulfate, heptahydrate | Sigma | M1880 | |
| ferric ammonium citrate | Sigma | F5879 | |
| zinc sulfate, heptahydrate | Sigma | Z0251 | |
| ammonium chloride | Sigma | A9434 | |
| butyric acid, liquid | Sigma | B103500 | |
| resazurin powder | Sigma | R7017 | |
| sodium chloride | J.T. Baker | 4058-01 | |
| prepared resazurin solution | Invitrogen | DAL1100 | |
| PCR stickers | Denville | B1212-5 | |
| spectrophotometer | Molecular Devices | M5 | |
| 96-well, tissue culture treated microplates | Corning | 3595 | |
| reagent reservoirs | VWR | 89094-678 | |
| resealable plastic bags | VWR | 395-94602 | |
| 14 mL Polypropylene round-bottom tubes | Corning | 352059 | |
| 50 mL conical centrifuge tube | Corning | 352070 | |
| 75 cm2 Cell culture flask | Corning | 431464U | |
| clear, flat bottom tissue culture treated 96-well microplate | Costar | 3595 | |
| Prism 6 for OS X | GraphPad | http://www.graphpad.com/scientific-software/prism/ |
- Nathan, C. Fresh approaches to anti-infective therapies. Sci. Transl. Medicine. 4 (140), 140-142 (2012).
- Gomez, J. E., McKinney, J. D. M. tuberculosis persistence, latency, and drug tolerance. Tuberculosis (Edinb). 84, 29-44 (2004).
- Balaban, N. Q., Merrin, J., Chait, R., Kowalik, L., Leibler, S. Bacterial persistence as a phenotypic switch. Science. 305, 1622-1625 (2004).
- Bigger, J. Treatment of staphylococcal infections with penicillin by intermittent sterilisation. Lancet. , 497-500 (1944).
- Bryk, R., et al. Selective killing of nonreplicating mycobacteria. Cell Host Microbe. 3, 137-145 (2008).
- Gold, B., et al. Nonsteroidal anti-inflammatory drug sensitizes Mycobacterium tuberculosis to endogenous and exogenous antimicrobials. Proc. Natl. Acad. Sci. U.S.A. 109, 16004-16011 (2012).
- Gold, B., et al. Rapid, semi-quantitative assay to discriminate among compounds with activity against replicating or non-replicating Mycobacterium tuberculosis. Antimicrob. Agents Chemother. 59, 6521-6538 (2015).
- Gold, B., Warrier, T., Nathan, C., Parish, T., Roberts, D. . Mycobacteria Protocols, Methods in Molecular Biology. 1285, 293-315 (2015).
- Warrier, T., et al. Identification of Novel Anti-mycobacterial Compounds by Screening a Pharmaceutical Small-Molecule Library against Nonreplicating Mycobacterium tuberculosis. ACS Infect. Dis. , 580-585 (2015).
- Zheng, P., Chem, J. .. M. e. d. .., et al. Synthetic Calanolides with Bactericidal Activity Against Replicating and Nonreplicating Mycobacterium tuberculosis. J. Med. Chem. , (2014).
- Darby, C. M., et al. Whole cell screen for inhibitors of pH homeostasis in Mycobacterium tuberculosis. PLoS One. 8, e68942 (2013).
- Darby, C. M., Nathan, C. F. Killing of non-replicating Mycobacterium tuberculosis by 8-hydroxyquinoline. J. Antimicrob. Chemother. 65, 1424-1427 (2010).
- de Carvalho, L. P., Darby, C. M., Rhee, K., Nathan, C. Nitazoxanide Disrupts Membrane Potential and Intrabacterial pH Homeostasis of Mycobacterium tuberculosis. ACS Med. Chem. Lett. 2, 849-854 (2011).
- Xie, Z., Siddiqi, N., Rubin, E. J. Differential antibiotic susceptibilities of starved Mycobacterium tuberculosis isolates. Antimicrob. Agents Chemother. 49, 4778-4780 (2005).
- Grant, S. S., et al. Identification of novel inhibitors of nonreplicating Mycobacterium tuberculosis using a carbon starvation model. ACS Chem. Biol. 8, 2224-2234 (2013).
- Zhang, M., et al. Streptomycin-starved Mycobacterium tuberculosis 18b, a drug discovery tool for latent tuberculosis. Antimicrob. Agents Chemother. 56, 5782-5789 (2012).
- Mak, P. A., et al. A high-throughput screen to identify inhibitors of ATP homeostasis in non-replicating Mycobacterium tuberculosis. ACS Chem. Biol. 7, 1190-1197 (2012).
- Cho, S. H., et al. Low-oxygen-recovery assay for high-throughput screening of compounds against nonreplicating Mycobacterium tuberculosis. Antimicrob. Agents Chemother. 51, 1380-1385 (2007).
- Franzblau, S. G., et al. Comprehensive analysis of methods used for the evaluation of compounds against Mycobacterium tuberculosis. Tuberculosis (Edinb). 92, 453-488 (2012).
- Rebollo-Lopez, M. J., et al. Release of 50 new, drug-like compounds and their computational target predictions for open source anti-tubercular drug discovery. PLoS One. 10, e0142293 (2015).
- Tasneen, R., et al. Contribution of the nitroimidazoles PA-824 and TBA-354 to the activity of novel regimens in murine models of tuberculosis. Antimicrob. Agents Chemother. 59, 129-135 (2015).
- Grosset, J. H., et al. Assessment of clofazimine activity in a second-line regimen for tuberculosis in mice. Am. J. Respir. Crit. Care Med. 188, 608-612 (2013).
- Shiloh, M. U., Ruan, J., Nathan, C. Evaluation of bacterial survival and phagocyte function with a fluorescence-based microplate assay. Infect. Immun. 65, 3193-3198 (1997).
- Wang, F., et al. Identification of a small molecule with activity against drug-resistant and persistent tuberculosis. Proc. Natl. Acad. Sci. U.S.A. 110, E2510-E2517 (2013).
- Wayne, L. G., Hayes, L. G. An in vitro model for sequential study of shiftdown of Mycobacterium tuberculosis through two stages of nonreplicating persistence. Infect. Immun. 64, 2062-2069 (1996).
- Barry, A. L., et al. . Methods for determining bactericidal activity of antimicrobial agents: approved guideline. 19, (1999).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved