Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Immunology and Infection
Método de muestreo hisopo para la Detección de norovirus humano en superficies
A macrofoam based sampling methodology was developed and evaluated for the detection and quantification of norovirus on environmental hard surfaces.
norovirus humanos son una causa principal de la epidemia y la gastroenteritis esporádica en todo el mundo. Debido a que la mayoría de las infecciones se propagan ya sea directamente a través de la ruta de persona a persona o indirectamente a través de las superficies ambientales o alimentos, fómites contaminados y superficies inanimadas son vehículos importantes para la propagación del virus durante los brotes de norovirus.
Desarrollamos y evaluamos un protocolo utilizando hisopos macroespuma para la detección y tipificación de los norovirus humanos de las superficies duras. En comparación con hisopos con punta de fibra o toallitas antiestáticas, hisopos macroespuma permiten la recuperación de virus (rango de 1,2 a 33,6%) de las superficies de asiento de inodoro de hasta 700 cm 2. El protocolo incluye los pasos para la extracción del virus de los hisopos y una mayor concentración del ARN viral usando columnas de centrifugación. En total, 127 (58,5%) de 217 muestras de frotis que habían sido recogidos de las superficies en los cruceros y centros de atención a largo plazo donde había estado la gastroenteritis por norovirusinformaron dado positivo por norovirus GII por RT-qPCR. De estos 29 (22,8%) podría ser genotipo con éxito. En conclusión, la detección de norovirus en superficies ambientales utilizando el protocolo que hemos desarrollado puede ayudar a determinar el nivel de contaminación del medio ambiente durante los brotes, así como la detección de virus cuando las muestras clínicas no están disponibles; también puede facilitar el seguimiento de la eficacia de las estrategias de remediación.
Norovirus humanos son una causa principal de la epidemia y la gastroenteritis aguda esporádica en todo el mundo 1, 2, 3. El virus es muy contagioso y la transmisión ocurre a través de la interacción persona directa a persona o indirectamente por contacto con alimentos contaminados, agua o superficies ambientales. Los norovirus se pueden desprender durante períodos prolongados y prolongan la supervivencia del virus en las superficies ambientales se ha documentado 1, 2, 3. Duran....
1. torunda de muestreo en el campo
- Use un par de guantes limpios.
- Medir el tamaño de la zona de muestreo sin tocar la superficie usando una cinta de medición o una regla. Tratar de estimar el área con la mayor precisión posible y llenar un formulario de informe (Cuadro 1).
- Compruebe el kit de raspado de posibles fugas y bolsas de transporte de muestras de etiquetas y kits de hisopos.
- Mueva el hisopo por el área de muestreo como sigue: un golpe en la direcci?.......
La Figura 1 presenta un diagrama de flujo del protocolo de muestreo hisopo. Este protocolo consiste en cuatro pasos principales; 1) la recogida de muestras, 2) de almacenamiento de muestras y el transporte, 3) la purificación de ARN viral y la concentración y 4) ensayo de RT-qPCR y genotipado.
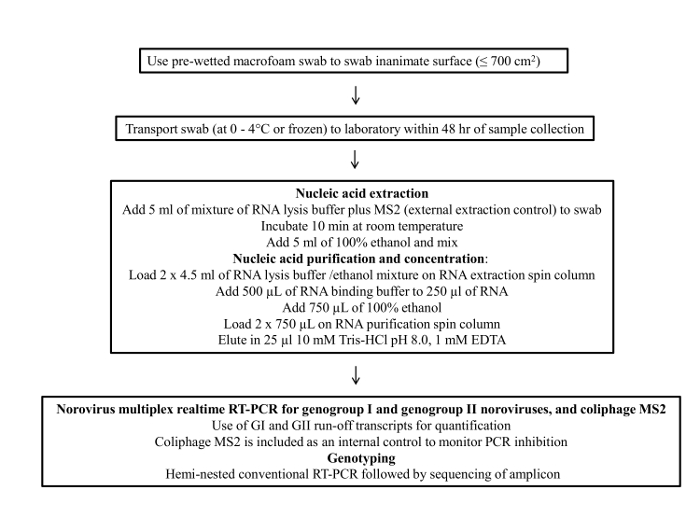
Figura 1: Diagrama de flujo del prot.......
Los norovirus tienen una dosis infecciosa humana 50% entre 18 y 10 3 20 partículas de virus. Por lo tanto, incluso la contaminación de bajo nivel de las superficies puede suponer un riesgo para la salud pública. Se evaluaron varios aspectos del protocolo de muestreo hisopo incluyendo: 1) diferentes materiales de hisopo, 2) hisopos de condiciones de almacenamiento durante el transporte, 3) la concentración de ARN viral, y 4) colífagos MS2 como el control de la extracción interna. .......
| Name | Company | Catalog Number | Comments | |
| Generic name for kits | ||||
| Macrofoam swab | Premoistened EnviroMax Swab kit | Puritan | 2588060PFUW | |
| RNA Lysis buffer | CDC UNEX buffer | Microbiologics | Cat No MR0501 | |
| RNA extraction spin column | Midi column | Omega Biotek | Cat No R6664-02 | |
| RNA purification spin column | Zymol RNA Clean and Concentrator kit | Zymo Research | Cat No R1016 | |
| Real time RT-PCR kit | AgPath kit One-Step RT-PCR Kit | Life Technologies | Cat No 4387391 | |
| Conventional RT-PCR kit | Qiagen one step RT-PCR kit | Qiagen kit | Cat No 210212 | |
| Gel extraction kit | Qiagen QIAquick gel extraction kit | Qiagen kit | Cat No 28704 or 28706 | |
| Coliphage MS2 | ATCC | Cat No 15597-B1 | ||
| RNA run-off transcripts | Bacteriophage MS2 (ATCC No. 15597-B1) can be cultivated using Escherichia coli (E.coli) Famp (ATCC No. 700891). | |||
| Realtime PCR platform | Applied Biosystems | Model ABI 7500 | GI and GII RNA run off transcripts were quantified spectrophotometrically at A260, diluted in diethyl pyrocarbonate-treated water to 1 × 106 copies/ μl, and stored at −80°C with 1.0 U /μl RNasin (Promega, Madison, WI). | |
| Optical 96-well reaction plate | Thermo Scientific | Cat No 4316813 | ||
| MicroAmp Clear Adhesive Film | Thermo Scientific | Cat No 4306311 |
- Isakbaeva, E. T., et al. Norovirus transmission on cruise ship. Emerg. Infect. Dis. 11, 154-158 (2005).
- Lopman, B. A., Gastañaduy, P., Park, G. W., Hall, A. J., Parashar, U. D., Vinjé, P. Environmental transmission of norovirus gastroenteritis. Curr. Opin. Virol. 2 (1), 1-7 (2011).
- Malek, M., et al. Outbreak of norovirus infection among river rafters associated with packaged delicatessen meat, Grand Canyon, 2005. Clin Infect Dis. 48 (1), 31-37 (2009).
- Atmar, R. L., et al. Norwalk virus shedding after experimental human infection. Emerg. Infect. Dis. 14 (10), 1553-1557 (2008).
- Glass, R. I., Parashar, U. D., Estes, M. K. Norovirus gastroenteritis. N. Engl. J. Med. 361 (18), 1776-1785 (2009).
- Park, G. W., et al. Evaluation of a New Environmental Sampling Protocol for Detection of Human Norovirus on Inanimate Surfaces. Appl. Environ. Microbiol. 81 (17), 5987-5992 (2015).
- Barker, J., Jones, M. V. The potential spread of infection caused by aerosol contamination of surfaces after flushing a domestic toilet. J. Appl. Microbiol. 99, 339-347 (2005).
- Tung-Thompson, G., Libera, D. A., Koch, K. L., de Los Reyes, F. L., Jaykus, L. A. Aerosolization of a Human Norovirus Surrogate, Bacteriophage MS2, during Simulated Vomiting. PloS one. 10, 0134277 (2015).
- Atmar, R. L., et al. Determination of the 50% human infectious dose for Norwalk virus. J. Infect. Dis. 209 (7), 1016-1022 (2014).
- Petrignani, M., van Beek, J., Borsboom, G., Richardus, J. H., Koopmans, M. Norovirus introduction routes into nursing homes and risk factors for spread: a systematic review and meta-analysis of observational studies. J. Hosp. Infect. 89 (3), 163-178 (2015).
- . Centers for Disease Control Prevention. Norovirus outbreak in an elementary school--District of Columbia, February 2007. MMWR. Morb. Mortal. Wkly. Rep. 56 (51-52), 1340-1343 (2008).
- Cheesbrough, J. S., Barkess-Jones, L., Brown, D. W. Possible prolonged environmental survival of small round structured viruses. J. Hosp. Infect. 35, 325-326 (1997).
- Julian, T. R., Tamayo, F. J., Leckie, J. O., Boehm, A. B. Comparison of surface sampling methods for virus recovery from fomites. Appl. Environ. Microbiol. 77, 6918-6925 (2011).
- Taku, A., et al. Concentration and detection of caliciviruses from food contact surfaces. J. Food. Prot. 65, 999-1004 (2002).
- Scherer, K., Ellerbroek, L., Schulenburg, J., Johne, R., Klein, G. Application of a swab sampling method for the detection of norovirus and rotavirus on artifically contaminated food and environmental surfaces. Food. Environ. Virol. 1 (42), 42-49 (2009).
- Herzog, A. B., et al. Evaluation of sample recovery efficiency for bacteriophage P22 on fomites. Appl. Environ. Microbiol. 78, 7915-7922 (2012).
- Vega, E., et al. CaliciNet: A Novel Surveillance Network for Norovirus Gastroenteritis Outbreaks in the United States. Emerging Infectious Diseases. 17 (8), 1389-1395 (2011).
- Rolfe, K. J., et al. An internally controlled, one-step, real-time RT-PCR assay for norovirus detection and genogrouping. J Clin Virol. 39 (4), 318-321 (2007).
- Kittigul, L., et al. Norovirus GII-4 2006b variant circulating in patients with acute Thailand during a 2006-2007 study. J. Med. Virol. 82 (5), 854-860 (2010).
- Teunis, P. F., et al. Norwalk virus: how infectious is it. J. Med. Virol. 80 (8), 1468-1476 (2008).
- Wollants, E., et al. Evaluation of a norovirus sampling method using sodium dodecyl sulfate/EDTA-pretreated chromatography paper strips. J. Virol. Methods. 122, 45-48 (2004).
- Weir, M. H., Shibata, T., Masago, Y., Cologgi, D., Rose, J. B. The Effect of Surface Sampling and Recovery of Viruses and Non-Spore Forming Bacteria on a QMRA Model for Fomites. Environ. Sci. Technol. 50 (11), 5945-5952 (2016).
- . Microbiology of food and animal feed-Horizontal method for determination of hepatitis A virus and norovirus in food using real-time RT-PCR. International Organization for Standardization (ISO). , (2013).
- Huslage, K., Rutala, W. A., Sickbert-Bennett, E., Weber, D. J. A quantitative approach to defining "high-touch" surfaces in hospitals. Infect. Control. Hosp. Epidemiol. 31 (8), 850-853 (2010).
- Wu, H. M., et al. A norovirus outbreak at a long-term-care facility: the role of environmental surface contamination. Infect. Control. Hosp. Epidemiol. 26 (10), 802-810 (2005).
- Ikner, L. A., Gerba, C. P., Bright, K. R. Concentration and recovery of viruses from water: a comprehensive review. Food Environ. Virol. 4 (2), 41-67 (2012).
- Gallimore, C. I., et al. Environmental monitoring for gastroenteric viruses in a pediatric primary immunodeficiency unit. J. Clin. Microbiol. 44 (2), 395-399 (2006).
- Ganime, A. C., et al. Dissemination of human adenoviruses and rotavirus species A on fomites of hospital pediatric units. Am J Infect Control. , (2016).
- Verani, M., Bigazzi, R., Carducci, A. Viral contamination of aerosol and surfaces through toilet use in health care and other settings. Am J Infect Control. 42 (7), 758-762 (2014).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved