Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Medicine
Das Chick Chorioallantoic Membrane In Vivo Modell zur Beurteilung der perineuralen Invasion bei Kopf- und Halskrebs
Perineurale Invasion ist ein aggressiver Phänotyp für Kopf- und Halsplattenkarzinome und andere Tumoren. Das Küken-Chorioallanto-Membranmodell wurde zur Untersuchung von Angiogenese, Krebsinvasion und Metastasierung verwendet. Hier zeigen wir, wie dieses Modell genutzt werden kann, um die perineurale Invasion in vivo zu bewerten.
Perineurale Invasion ist ein Phänotyp, bei dem Krebs die Nerven umgibt oder eindringt. Es ist verbunden mit schlechten klinischen Ergebnissen für Kopf und Hals Plattenepithelkarzinom und andere Krebsarten. Mechanistische Studien haben gezeigt, dass das molekulare Übersprechen zwischen Nerven und Tumorzellen vor der physikalischen Interaktion auftritt. Es gibt nur wenige In-vivo-Modelle, um die perineurale Invasion zu untersuchen, insbesondere um die frühe Progression zu untersuchen, bevor physikalische Nerven-Tumor-Wechselwirkungen auftreten. Das Küken-Chorioallanto-Membranmodell wurde verwendet, um die Krebsinvasion zu untersuchen, da die Kellermembran des Chorionepithels die des menschlichen Epithelgewebes imitiert. Hier haben wir das Küken-Chorioallanto-Membranmodell umfunktioniert, um die perineurale Invasion zu untersuchen, die Dorsalwurzelganglien der Rate und die Plattenepithelkarzinomzellen des menschlichen Kopfes und Deshalses auf das Chorionepithel zu pfropfen. Wir haben gezeigt, wie dieses Modell nützlich sein kann, um die Fähigkeit von Krebszellen zu bewerten, in vivo in neuronales Gewebe einzudringen.
Perineurale Invasion (PNI) ist ein unteruntersuchter Phänotyp bei Krebs, der mit einem hohen Krankheitsrezidiv und einem schlechten Überleben bei Patienten mit Kopf- und Halsplattenzellkarzinom (HNC)1assoziiert ist. PNI ist mikroskopisch als Tumorzellen innerhalb oder um die Nervendefiniert 2,3. Wenn PNI nachgewiesen wird, erhalten Patienten wahrscheinlich adjuvante Therapien wie elektive Nackensektion und/oder Strahlentherapie4,5. Diese Therapien sind jedoch aggressiv und nicht PNI-spezifisch. Tatsächlich gibt es keine Therapie, um PNI zu blockieren, vor allem, weil die Mechanismen, die Nerven-Tumor-Wechselwirkungen zugrunde liegen, immer noch schlecht verstanden werden.
Verschiedene molekulare Mechanismen wurden in die Anziehung von Nerventumoren involviert; Tumoren und Stromalzellen setzen Neuropeptide und Wachstumsfaktoren frei, um die Neuritogenese zu fördern6,7. Wenn sie in vitro kultiviert werden, haben HNC-Zellen und dorsale Wurzelganglien (DRG) beide eine robuste Reaktion; Auswirkungen auf Tumorzellinvasion und Neuritogenese können nach ein paar Tagen in Kultur6,8,9gesehen werden. Es fehlt jedoch an geeigneten In-vivo-Modellen, um Tumor-Nerven-Wechselwirkungen vor der Invasion zu rekapitulieren. Hier stellen wir ein in vivo PNI-Modell vor, um frühe Wechselwirkungen zwischen HNC-Zellen und Nerven zu untersuchen6. Wir passten das Küken-Chorioallanto-Membran-Modell (CAM) an, um eine neuronale Komponente einzuschließen, indem wir ein DRG in das CAM transplantierten, gefolgt von einem Transplantat von Krebszellen, um eine innervierte Tumormikroumgebung nachzuahmen.
Das CAM-Modell wurde erfolgreich verwendet, um die Invasion von Zellen durch die Kellermembran zu bewerten, nachahmt frühe invasive Stadien von Karzinomen und Melanom10,11,12. Das CAM besteht aus dem oberen Chorionepithel, dem dazwischen liegenden Mesenchym und dem unteren allantoischen Epithel. Das Chorionepithel ist dem menschlichen Epithel10,13 strukturell ähnlich, da die kollagen-IV-reiche Kellermembran die Kellermembran simuliert, die das mundliche Epithel vom darunter liegenden Bindegewebe trennt. Da die ersten Tumortransplantate 191314im CAM durchgeführt wurden, wurden viele Anpassungen der Methode entwickelt, um die Beurteilung der Angiogenese15,16,17, Tumorprogression und Metastasen18. Wichtig ist, dass sich die Technik der Transplantation von Tumoren auf das CAM kaum verändert hat, aber die Anwendungen entwickeln sich ständig weiter. Es wurden Assays mit zunehmender Komplexität veröffentlicht, darunter das Arzneimittelscreening19, Knochengewebe-Engineering20und Nanopartikel-basierte Krebsmedikamente21.
Unser Labor verwendet ein CAM-DRG-Modell, bei dem ein Säugetier-DRG isoliert und auf die Oberfläche des oberen CAM gepfropft wird. Nachdem das DRG in das CAM integriert wurde, werden HNC-Zellen in der Nähe des DRG transplantiert und dürfen mit dem DRG interagieren, bevor das gesamte In-vivo-System geerntet und analysiert wird. Wichtig ist, dass das System eine ex-vivo visuelle Beobachtung sowohl des DRG als auch des Tumors durch Fluoreszenzkennzeichnung von DRG- und Tumorzellen ermöglicht. Dieses Protokoll umfasst mehrere Schritte mit unterschiedlicher Komplexität, die innerhalb von 17 Tagen durchgeführt werden, von der Brut von Eiern bis zur Ernte des CAM (Abbildung 1). Zellen, die verschiedene Proteine von Interesse exemittieren, können in diesem Modell getestet werden, um die molekularen Pfade aufzuklären, die für die Nerveninvasion bei Krebs verantwortlich sind, und auch für das Screening von Medikamenten, um die neuronale Invasion direkt ins Visier zu nehmen. Zellen, die mit einem Kandidatenmedikament vorbehandelt wurden, können auf das CAM transplantiert und das Auftreten von PNI im Vergleich zu unbehandelten Kontrollen untersucht werden. Tatsächlich wurde das CAM-Modell für das Arzneimittelscreening als Zwischenschritt zwischen In-vitro-Studien und präklinischen In-vivo-Studien an Nagetieren19verwendet.
Das experimentelle Design wird mit der Hypothese variieren. Wenn beispielsweise die Rolle eines bestimmten Proteins auf PNI getestet wird, würde die experimentelle Gruppe DRG umfassen, die mit Tumorzellen transplantiert wird, die das Protein überexzitieren, während die Kontrollgruppe DRG mit Zellen umfassen sollte, die stabil mit leerem Vektor transfiziert sind. Verschiedene experimentelle Entwürfe können verwendet werden, um spezifische Fragen zu beantworten.
Ethik-Erklärung: Alle Experimente mit Ratten in diesem Protokoll werden in Übereinstimmung mit den IACUC-Regeln (Institutional Animal Care and Use Committee) unserer Institution durchgeführt. Versuche mit Eiern in dieser Studie sind von der IACUC-Verordnung ausgenommen.
1. Ei-Inkubation (geschätztes Timing: 5 min, Tag Null)
- Erregerfreie befruchtete kommerzielle Lohmann White Leghorn Eier erhalten, vorzugsweise am ersten Tag nach der Befruchtung. Inkubieren Sie sechs Eier pro Versuchsgruppe in einem Eibefeuchter-Inkubator bei 38 °C und 54% Luftfeuchtigkeit für 8 Tage mit stündlicher Rotation. Verwenden Sie die regelmäßige Rotation der Eier, um zu verhindern, dass der Embryo an den Eimembranen klebt.
HINWEIS: Bewahren Sie die Eier vor der Inkubation in einem 18 °C-Kühlschrank auf, um die Embryoentwicklung für maximal 1 Woche zu stoppen.
2. Ernte und Vorbereitung von DRGs (geschätzter Zeitpunkt: 2 h, Tag 8)
HINWEIS: Experimente mit Mäusen und Ratten bedürfen der Genehmigung durch die (IACUC). In einigen Ländern bedarf die Verwendung von Hühnereiern ebenfalls der Genehmigung.
- Holen Sie sich sechs bis sieben Wochen alte Sprague Dawley Ratten (200 g Gewicht), um DRGs zu extrahieren.
HINWEIS: Eine Ratte sollte 40 Gebärmutterhals- und Thorax-DRGs ergeben. Maus-DRG integriert sich ebenfalls in das CAM, aber die Bedingungen für diese Art müssen unabhängig optimiert werden. - In einem laminaren Strömungsschrank ernten DRGs aus zervikalen und thorakalen Regionen nach dem Protokoll für die Maus-DRG-Extraktion, das an anderer Stelle veröffentlicht wurde22. Folgen Sie Abbildung 2, um eine Orientierung zum Ernten von DRGs zu erhalten.
- Euthanisieren Sie die Ratte durch Herzpunktion nach Verabreichung von Ketamin / Xylazin intraperitoneal injiziert. Reinigen Sie die Rattenhaut mit 70% Ethanol und entfernen Sie die Rattenwirbelsäule mit einer Schere. Führen Sie keine zervikale Dislokation durch, da dies die zervikalen DRGs beschädigen würde.
- Trennen Sie die Zervix-, Brust- und Lendenbereiche mit derselben Schere, wobei sie der schematischen anatomischen Darstellung und den Bruttobildern in Abbildung 2A-Dfolgen. Legen Sie die Wirbelsäulenabschnitte in eine 10 cm große Kulturschale mit 1x PBS, um gewebenass zu halten.
- Mit einer empfindlichen Knochenschere öffnen Sie die Wirbelknochen in den dorsalen und ventralen Aspekten und trennen Sie die Wirbelsäule in zwei seitliche Hälften (Abbildung 2E-F). Legen Sie die Gewebeteile in eine saubere 10 cm Schale mit frischen 1x PBS.
- Mit Zangen das Rückenmark vorsichtig von den Wirbelknochen lösen, um die DRGs zu visualisieren (Abbildung 2G).
- Mit feinen Zangen, die unter jedem DRG gehalten werden, greifen Sie es und ziehen Sie es aus der Knochenhöhle heraus, in der sie untergebracht ist. Halten Sie die DRG nicht direkt, da dies zu Gewebeschäden führt. Trimmen Sie die Axonbündel nicht aus dem DRG (Abbildung 2H).
HINWEIS: Vermeiden Sie die Verwendung von Lenden-DRGs, da diese die Integration in das CAM reduziert haben. Befolgen Sie für den Standort der DRG-Region die schematische Illustration und die groben anatomischen Bilder in Abbildung 2A-D.
- Unmittelbar nach der Ernte jedes DRG in DMEM-Kulturmedium mit 2% Penicillin/Streptomycin (Pen/Strep) und 10% hitzeinaktiviertem Fetal Bovine Serum (FBS) ergänzen, um eine bakterielle Kontamination der DRGs zu verhindern. Gruppieren Sie alle DRGs in den gleichen 6 cm Kulturgericht mit 4 ml Kulturmedium.
- Nach der Ernte aller DRGs, übertragen Sie sie auf ein neues Kulturgericht mit DMEM-Kulturmedium, ergänzt mit 2% Pen/Strep plus 10% FBS und enthält 1,25 g/ml roten Fluoreszenzfarbstoff. Inkubieren Sie für 1 h im Zellkultur-Inkubator. Bereiten Sie während dieser Zeit die Eier auf die DRG vor, wie unten beschrieben (Schritt 3).
ANMERKUNG: Das Intervall zwischen der Ernte von DRGs und der Fertigstellung der Fluoreszenzkennzeichnung sollte ausreichen, um die Eier vorzubereiten; DRGs können für ein paar Stunden im Inkubator aufbewahrt werden.
3. Vorbereitung von Eiern für die DRG-Veredelung (geschätzter Zeitpunkt: 1 h für ein Dutzend Eier, Tag 8)
- In einem laminaren Strömungsschrank das Licht verdünnen und die Eier transleuchten, um die Lebensfähigkeit und embryonale Phase zu überprüfen. Auszuschließen Eier mit schlechter Gefäßbildung, nicht befruchtete Eier oder Eier, die nicht mit Tag 8 nach der Befruchtung übereinstimmen. Halten Sie das Ei vorsichtig mit dem natürlich vorkommenden Luftsack in Richtung der Lichtquelle (Abbildung3A).
- Markieren Sie mit einem Bleistift die Eierschale, um die Öffnungen zu erhalten (Abbildung 3A-B).
- Identifizieren Sie zunächst die Befestigung des sich entwickelnden Embryos an das CAM als ein dunkles bewegliches Gefäß, das an der Eimembran befestigt ist, und markieren Sie diesen Bereich, um Eingriffe in dieser Region zu vermeiden.
- Wählen Sie zweitens den Betriebsfensterbereich als gut vaskularisierten Bereich von mindestens 2 cm vom Embryo-Anhang aus und zeichnen Sie einen Kreis mit einem Durchmesser von 1,5 cm. Etwa 1 cm vom Betriebsfenster entfernt, zeichnen Sie ein 0,5 cm großes Quadrat in einem weniger vaskularisierten Bereich.
- Drittens: Ziehen Sie den Luftsackbereich, um ihn aus dem Einsatzbereich auszuschließen. Markieren Sie die Mitte des Luftsacks mit einem Kreuz.
- Mit einem Drehwerkzeug und Gravurbohrer, 3 mm Durchmesser, bohren Sie die Eierschale in das markierte Quadrat (Abbildung 3C). Verwenden Sie stumpfe Zangen, um die Eierschale zu entfernen, ohne die äußere Eierschalenmembran (die weiße Membran direkt unter der Schale) zu entfernen (Abbildung 3D). Arbeiten Sie sorgfältig, um eine versehentliche Perforation dieser Membran zu vermeiden.
- Mit dem gleichen Bohrer wie in Schritt 3.3, machen Sie eine punktgenaue Perforation im markierten Kreuz im Luftsackbereich, um Luftstrom in das Ei zu ermöglichen (Abbildung 3E). Achten Sie darauf, nicht zu viel Druck auf das Ei auszuüben, um zu vermeiden, zu brechen oder zu beschädigen.
- Legen Sie 30 L HBSS in die quadratische Öffnung, über die intakte äußere Eierschalenmembran (Abbildung 3E). Mit einer 30-G-Spritzennadel eine punktgenaue Perforation in der äußeren Membran in diesem quadratischen Bereich (Abbildung3F) machen
- Legen Sie das Ei in die Lichtquelle, um den Luftsack zu visualisieren. Drücken Sie auf eine Augentropfen-Gummilampe und legen Sie sie in die kleine Perforation im Luftsackbereich (Schritt 3.4). Druck in der Glühbirne loslassen, bis Sie die Trennung der beiden Membranen im Betriebsfensterbereich sehen (Abbildung 3G); Wiederholen Sie diesen Schritt so oft, wie Sie benötigen, um eine vollständige Trennung der Membranen im Betriebsfensterbereich zu erreichen.
- Wiederholen Sie die Schritte 3.1-3.6 für alle Eier.
- Mit dem gleichen Bohrer wie in Schritt 3.3, bohren Sie das kreisförmige Betriebsfenster, um darauf zu achten, die äußere Eierschalenmembran nicht zu brechen (Abbildung 3H). Reinigen Sie die Eieroberfläche, indem Sie vorsichtig ein Klebeband kleben, um alle losen Partikel zu entfernen.
- Mit stumpfer Zange die Eierschale aus dem gebohrten Bereich entfernen (Abbildung 3I-J). Als nächstes, mit den gleichen Zangen, entfernen Sie die äußere Eihülle Membran (Abbildung 3K), achten Sie darauf, keine kleinen Schalenpartikel in das Ei einzuführen, um die Kontamination zu minimieren.
- Identifizieren Sie das CAM ungefähr in 1 cm Tiefe von der Eioberfläche. Bedecken Sie jedes geöffnete Ei vorübergehend mit Paraffinwachsmembran, um eine Kontamination zu vermeiden (Abbildung 3L).
- Wiederholen Sie die Schritte 3.8-3.10 für alle Eier. Legen Sie die Eier ohne Rotation wieder in den Eierbrutkasten, bis die DRGs zur Veredelung bereit sind.
4. Grafting DRG auf dem CAM (geschätzter Zeitpunkt: 40 min, Tag 8)
- Bereiten Sie eine 6 cm Kulturschale mit HBSS Medium vor, um die DRGs vor der Implantation zu waschen. Bringen Sie die vorbereiteten Eier in den Zellkultur-Laminar-Flow-Schrank. Entfernen Sie die Paraffinmembran aus dem Ei (Abbildung 4A).
- Mit feinen sterilen Zangen, greifen Sie vorsichtig ein DRG aus dem Inneren des Kulturmediums. Tauchen Sie es in das HBSS-Medium ein, um das überschüssige Medium zu entfernen, das den Fluoreszenzfarbstoff enthält. Halten Sie die DRG sehr sanft; Andernfalls bleibt es bei der Zange.
- Legen Sie das DRG auf das CAM, achten Sie darauf, die Membran nicht zu durchstechen (Abbildung 4B-C). Verwenden Sie bei Bedarf ein weiteres Zangenpaar, um das DRG beim Auflegen auf dem CAM von der Spitze der Zange zu lösen.
HINWEIS: Das Halten des DRG mit HBSS-Medium wird auch das Ablösen von den Zangen erleichtern. - Bedecken Sie das Ei mit einem sterilen transparenten Filmverband. Bedecken Sie alle Fenster und Einstiche in der Eierschale, um eine bakterielle Kontamination zu vermeiden (Abbildung 4D).
- Nach der Pfropfung von DRGs in allen Eiern die Eier in einem Befeuchtungsbrutschrank bei 38 °C und 54% Luftfeuchtigkeit für 2 Tage, ohne Rotation, inkubieren.
5. Transplantation tumorzellen auf dem CAM (geschätztes Timing: 1 h 30 min, Tag 10)
- Bei 48 h vor der Transplantation der Zellen, Platte die Zellen in Kulturplatten benötigt. Berechnen Sie 0,5 bis 1 x 106 Zellen pro Ei für UM-SCC-1-Zellen, um dreidimensionale Tumoren im CAM zu erzeugen. Beachten Sie, dass die Zellnummer je nach Zelllinie variieren kann.
- Aspirieren Medium und dmEM Kulturmedium ergänzt mit 1% Pen/Strep plus 10% FBS und 2,5 g/ml grünen Fluoreszenzfarbstoff. 1 h bei 37 °C im Zellkultur-Inkubator inkubieren. Überprüfen Sie dann die Fluoreszenzintensität auf dem Mikroskop, aspirieren Medium, waschen einmal mit 1x PBS, und fügen Sie 0,25% Trypsin für bis zu 10 min. Neutralisieren Trypsin mit DMEM ergänzt Medium.
- Zentrifuge bei 250 x g für 4 min, um ein Zellpellet zu bilden. DMEM-Medium aspirieren und in HBSS wieder aufsetzen, um den überschüssigen Fluoreszenzfarbstoff zu waschen. Zählen Sie Zellen mit einem Hämozytometer.
- Bringen Sie die Eier in die Zellkultur laminare Flussschrank. Öffnen Sie mit Schere und Zange den transparenten Folienverband, der das Ei bedeckt (Abbildung 4E-F).
- Zentrifugieren Sie die berechnete Anzahl der Zellen erneut, aspirieren Sie das HBSS-Medium und setzen Sie es bei einer Endkonzentration von 0,5 bis 1x106 Zellen pro 5 l des gleichen Mediums wieder aus (Abbildung4G). Bereiten Sie die benötigte Menge für die Gesamtanzahl der Eier (5 L zellsuspension pro Ei) vor.
- Legen Sie 5 l Zelllösung auf das CAM, ca. 2 mm vom DRG entfernt (Abbildung 4H). Halten Sie einheitliche Abstände zwischen dem DRG und den Zellen. Achten Sie sehr darauf, das Ei nicht zu stören, um die Ausbreitung der Zellen zu minimieren.
HINWEIS: Um mit der Zellimplantation zu beginnen, wählen Sie Eier aus, auf denen die CAM-Oberfläche optisch trocken ist. Wenn die Oberfläche zu nass ist, können sich Zellen ausbreiten und keine regelmäßigen Tumoren bilden. - Bedecken Sie das Ei mit einem neuen Filmdressing wie in Schritt 4.4. Die Zellen in allen Eiern begrapfen. Die Eier in einem Befeuchtungsbrutschrank bei 38 °C und 54% Luftfeuchtigkeit 7 Tage lang ohne Rotation bebrüten.
6. Ernte des CAM (geschätzter Zeitpunkt: 1 h für Dutzend Eier, Tag 17)
- Bereiten Sie 6-Well-Platten mit 4% PFA (Paraformaldehyd) pH7.0, eine gut pro Ei, 2 ml pro Brunnen.
- Bringen Sie die Eier auf eine Laborbank. Mit einer Anziehnadel, die an einer Spritze befestigt ist, um den Filmverband zu perforieren, lassen Sie etwa 300 l PFA über das CAM fallen, um das CAM leicht zu versteifen und so den Ernteprozess zu erleichtern. Wiederholen Sie dies für alle Eier.
- Mit einer Schere die obere Hälfte der Eierschale (wo sich das Betriebsfenster befindet) mit dem cam daran zu entfernen (Abbildung 4I). Reduzieren Sie die Größe dieser Hälfte auf ca. 3 cm im Durchmesser, wobei der Teil des CAM, in dem DRG- und Tumorzellen in der Mitte transplantiert wurden , beibehalten wird (Abbildung 4J). Greifen Sie das CAM mit feiner Zange und lösen Sie es von der Eierschale, während Sie es in das PFA legen. Richten Sie die DRG und Krebszellen nach oben (Abbildung 4K-L).
HINWEIS: Der Bereich von 3 cm sollte sowohl die DRG als auch die Zellen enthalten. Das DRG ist leicht als kleiner Klumpen am CAM zu sehen, aber Tumorzellen sind manchmal bei grober Untersuchung schwer zu identifizieren. - Alternativ, mit einer Schere, verbreitern Sie das Operationsfenster entfernen die Eischale von der Oberseite des Eis, während die CAM an Ort und Stelle zu halten; ca. 1 cm über das Betriebsfenster hinaus entfernen (Abbildung 4M) und die DRG und die Zellen auf dem CAM identifizieren (Abbildung 4N-O). Mit feinen Zangen halten Sie das CAM an einer der Kanten und heben Sie es sanft an. Mit scharfen zarten Scheren, schneiden Sie das CAM vorsichtig, um eine kreisförmige Fläche zu entfernen, ca. 3 cm im Durchmesser (Abbildung4P), und legen Sie das CAM in PFA mit DRG und Krebszellen nach oben.
HINWEIS: Vermeiden Sie das Dehnen oder Halten des CAM mit Zangen an mehreren Stellen, um Gewebeschäden zu minimieren, die Mikroskopieartefakte erzeugen können. - Platzieren Sie jede CAM-Membran in einem Brunnen (Abbildung 4L). Greifen Sie vorsichtig die Ränder des CAM, um das im PFA geöffnete Gewebe zu verteilen, oder schütteln Sie die Platte sanft, bis das CAM entfaltet ist, um Faltenartefakte zu vermeiden.
- Euthanisieren Sie den Embryo (Tag 17) durch schnelle Enthauptung. Fixieren Sie die geernteten Gewebe in PFA für 4 h bei Raumtemperatur. Nach der Fixierung PFA durch 1x PBS ersetzen und Gewebe in PBS bei 4 °C lagern, bis es zum Schnitt in Paraffin eingebettet ist. Vermeiden Sie Eine Überfixierung, die die empfindliche Gefäße des CAM beschädigt.
- Mit einem Fluoreszenz-Stereomikroskop fotografieren Sie die Membranen innerhalb von 2 Tagen nach der Ernte, um zu vermeiden, dass fluoreszierende Signale verloren geht.
Wenn diese Methode optimiert ist, verfügt sie über eine nahezu 100%ige DRG-Integration im CAM. Repräsentative Ergebnisse der DRG-Integration sind in Abbildung 5A-Bdargestellt. Die Integration von DRG in das CAM ist wichtig, da es dem DRG-Gewebe während des Experiments lebenserhaltend ist. Mikroskopisch wird die DRG im Bindegewebe des CAM (H&E-Färbung) gesehen. Blutgefäße sind oft im DRG-Gewebe zu sehen, was darauf hindeutet, dass die CAM-Blutversorgung das transplantierte Gewebe nährt. Implantierte Tumoren werden auch auf dem CAM von H&E identifiziert; Je nachdem, wie viel Invasion vorhanden ist, können Tumore mit keiner bis zu zahlreichen Tumorinseln vorhanden sein, die in das Bindegewebe eindringen (Abbildung 5C-D). Die repräsentative Abbildung 5E-F zeigt das geerntete CAM auf Hellfeld-Bildgebung und zusammengeführte Fluoreszenz. UM-SCC-1-Zellen, die den Galanin-Rezeptor 2 überexzättieren, zeigten eine erhöhte Invasion der DRG im Vergleich zu Kontrollzellen (Abbildung 5G-H). Krebs-DRG-Wechselwirkung wird beobachtet, als Krebszellen eine richtungsweisende Invasion in Richtung der DRG darstellen (Abbildung 5H).
Die Datenanalyse wird auf unterschiedliche Weise durchgeführt. Die richtungsweisende Invasion von Krebszellen in Richtung der DRG wird als dichotome Variable beobachtet und die Anzahl der Eier, die dieses Invasionsmuster darstellen, wird in jeder Gruppe gezählt. Statistische Unterschiede zwischen Gruppen werden anhand eines Binomialtests von Proportionen berechnet. Die Nähe zwischen Krebszellen und DRG und Tumorbereich werden mit ImageJ6 gemessen und Unterschiede zwischen den Gruppen werden mit dem Schüler-t-Test bewertet. Um die Genauigkeit bei der ImageJ-Analyse zu gewährleisten, sollten alle Bilder aus demselben Experiment auf gleiche Licht- und Belichtungseinstellungen aufgenommen werden. Nach der Anpassung des Bildschwellenwerts und der Helligkeit aller Bilder nach denselben Kriterien wird das Werkzeug "Partikel analysieren" verwendet, um den Tumorbereich zu messen, und das lineare Messwerkzeug misst Tumor-DRG-Abstände. Es ist wichtig, die konstante Einstellung der Größe der analysierten Partikel für alle Bilder über verschiedene Gruppen hinweg zu verwenden. In einigen Fällen werden Tumore dicker und können manuell mit einem digitalen Bremssattel gemessen werden, was eine Volumenmessung ermöglicht.
Die Verwendung von Abschnitten aus paraffinintegriertem CAM-Gewebe, H&E-Färbung oder Immunhistochemie für Epithelzellen (Anti-Cytokeratin-Antikörper reaktiv für menschliche Arten) kann durchgeführt werden, was eine Bewertung der Invasion im Bindegewebe ermöglicht. Invasion wird als Anzahl der Tumorinseln im Bindegewebe pro Ei quantifiziert. Immunfluoreszenz für Kollagen IV kann verwendet werden, um die Kellermembran hervorzuheben. Auch bei Verwendung von GFP-markierten Krebszellen wird die Identifizierung dieser Zellen in den Gewebeabschnitten ohne Immunhistochemie für Cytokeratin erleichtert. Metastasen- und Angiogeneseanalysen in CAM-Experimenten werden an anderer Stelle diskutiert10,17.
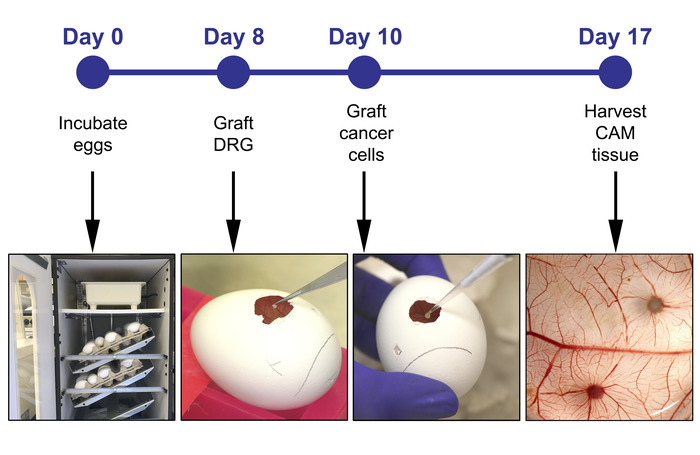
Abbildung 1: Zeitachse des Experiments einschließlich der wichtigsten Schritte an den Tagen 0, 8, 10 und 17. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
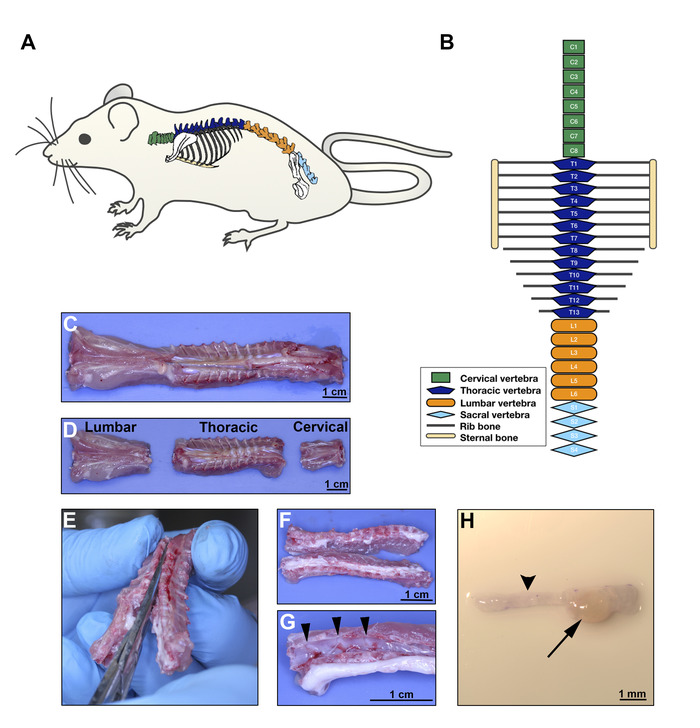
Abbildung 2: DRG-Extraktion am 8. Tag . A. Ratte schaltplantisch, der die anatomische Position der Wirbelsäule veranschaulicht. B. Diagramm der Rattenwirbelkonfiguration, das verschiedene Körperregionen zeigt; grün für Gebärmutterhals, dunkelblau für Brust, Orange für Lendenwirbel und hellblau für Sakrale. C-D. Ventraler Aspekt der Brustwirbelsäule nach chirurgischer Exzision; Trennung der Regionen, wie in Bdargestellt. E. Zerlegung der Wirbel, um den Rückenmarkskanal zu öffnen, die Wirbelkörper in zwei seitliche Abschnitte mit den DRGs zu trennen. Abschnitt sollte durch den dorsalen und ventralen Aspekt jedes Wirbelknochens an der Mittellinie schneiden. F. Grosser Aspekt der geöffneten Brustwirbelsäule. G. Nachdem das Rückenmark verschoben wurde, sind DRGs in den Wirbelkanälen gut sichtbar (Pfeilspitzen, die auf 3 DRGs zeigen). H. Stereomikroskopisches Bild eines DRG (Pfeil) mit den entsprechenden Axonbündeln (Pfeilkopf). Skalenbalken: C, D, Fund G, 1 cm; H, 1 mm. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
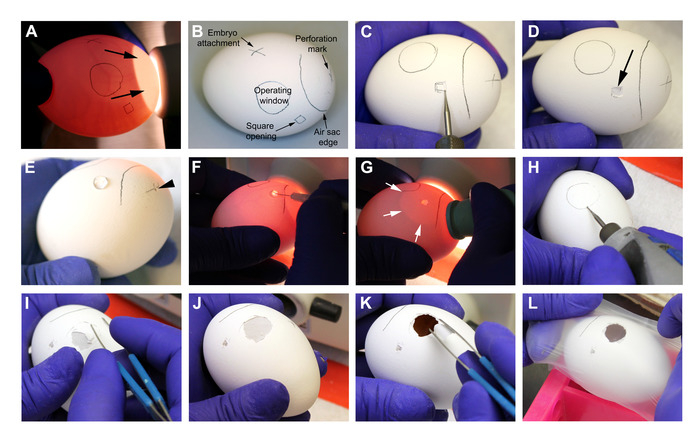
Abbildung 3: Zubereitung der Eier am 8. Tag. A-B. Identifizierung der Eivaskulatur und Markierungen vor dem Eingriff. Pfeile auf A zeigen auf den natürlich vorkommenden Luftsack. C-D. Bohren und Öffnen der Eierschale auf der quadratischen Öffnungsmarke. Pfeil auf D zeigt auf die intakte äußere Eierschalenmembran, nachdem die Schale mit Hilfe von stumpfen Zangen entfernt wurde. E. Das markierte Kreuz auf dem Luftsack wird mit dem Bohrer perforiert, um Luftinjederzeit in das Ei (Pfeilkopf) zu ermöglichen. 30 L HBSS-Medium wird auf die äußere Eierschalenmembran auf der quadratischen Öffnung gelegt. F. Mit einer feinen Spritzennadel wird die äußere Eischalenmembran an der Stelle perforiert, an der zuvor das HBSS platziert wurde. G. Druck wird auf eine Gummi-Augentropfenlampe ausgeübt, während sie an der Perforation befestigt wird, die auf den Luftsack gebohrt wird. Wenn der Fingerdruck freigesetzt wird, wird Luft gesaugt, wodurch ein künstlicher Luftsack (weiße Pfeile) erzeugt wird, der sich bis zum Betriebsfenster erstrecken sollte. H. Die Ränder des Betriebsfensters werden in einer fast parallelen Position zur Eierschale gebohrt, um eine versehentliche Perforation zu vermeiden. I-J. Entfernung der Eierschale mit stumpfer Zange. K. Entfernen Sie die äußere Eischalenmembran mit stumpfer Zange, wobei Sie darauf achten, keine Partikel auf das CAM einzuführen (beobachtet bei 1 cm unter der Oberfläche). L. Eier werden vorübergehend mit einer Paraffinwachsmembran bedeckt und wieder in den Brutkasten gelegt. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
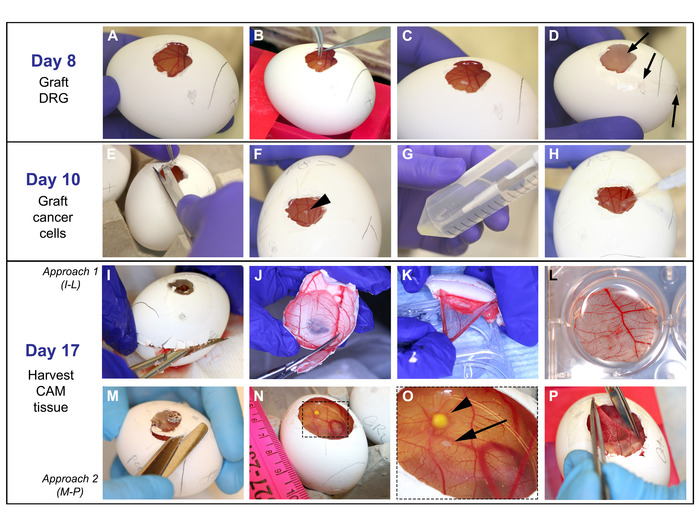
Abbildung 4: Grafting von DRG, Zellen und Ernte von CAM: Am Tag 8: A. CAM leicht nach Paraffinwachs-Membranentfernung beobachtet. B-C. Mit feiner Zange wird DRG auf das CAM gelegt. D. Ei wird mit Filmdressing überzogen und in den Brutkasten gelegt; Pfeile zeigen auf die abgedeckten Öffnungen. Am 10. Tag: E-F. Filmverband wird entfernt und DRG befindet sich (Pfeilkopf auf F). G-H. 5 l Zelllösung werden in einem Abstand von 2 mm zum DRG auf das CAM abgeworfen. Am 17. Tag: I-L und M-P zeigen zwei unterschiedliche Ansätze, die für die Ernte des CAM verwendet werden. I. Die Eierschale wird mit einer feinen Schere geöffnet, die auf dem Luftsack beginnt, bis die obere Hälfte des Eis entfernt ist. J. Die Eierschale, die das CAM enthält, ist auf ca. 3 cm verkleinert. K-L. Mit feiner Zange wird CAM von der Eierschale gelöst und in PFA gelegt. M-O. Die Erweiterung des Operationsfensters wird durchgeführt, um die DRG- und Krebszellen auf dem CAM zu visualisieren. Pfeilspitze zeigt auf den Tumor und Pfeil zeigt auf das DRG. P. Das CAM wird mit feinen Zangen erfasst, mit einer scharfen Schere ausgeschnitten und in PFA platziert, wie in Lgezeigt. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
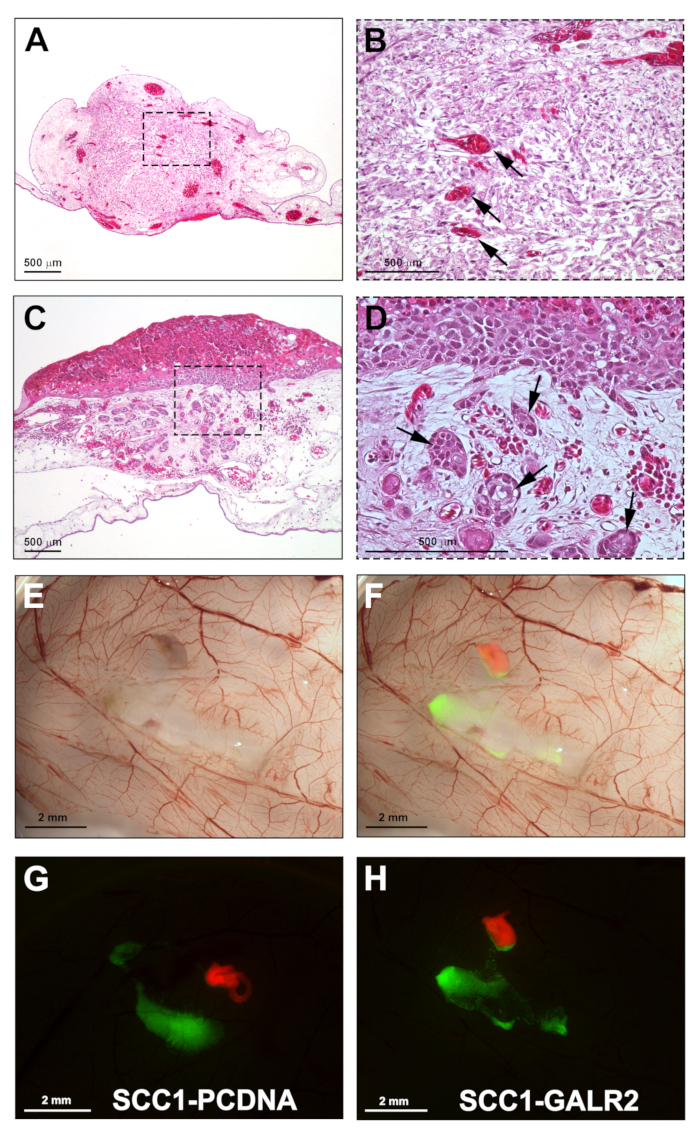
Abbildung 5: Repräsentative Ergebnisse. A. H&E-Abschnitt, der die Integration der DRG in das CAM zeigt. B. Höhere Vergrößerung von A; Zeigt CAM-Blutgefäße in der DRG. C. UM-SCC-1-Zellen, die auf das CAM gepfropft und vier Tage nach der Transplantation geerntet wurden (H&E-Färbung). D. Höhere Vergrößerung von C zeigt invasive Tumorinseln im CAM-Bindegewebe (Pfeile). E. Gross esteroskopisches Bild des CAM mit UM-SCC-1-GALR2-Zellen und Ratten-DRG, geerntet am 17. Tag. F. Zusammengeführte Fluoreszenz- und Hellfeldbilder, die die DRG mit roter und krebserregender Zelle mit grüner Kennzeichnung hervorheben. G-H. Fluoreszenz-Stereomikroskopie des CAM mit DRG und UM-SCC-1-GALR2 im Vergleich zu Kontrollzellen transplantiert, was die richtungsweisende Invasion von UM-SCC-1-GALR2-Zellen in die DRG (H) veranschaulicht. Skalenbalken: A-D, 500 m; E-H, 2 mm. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
| schritt | problem | grund | lösung | ||||||
| 3.2.1 | Die Embryo-Anhaftung konnte nicht identifiziert werden. | Befestigungsposition ist schwer zu sehen, während Ei noch ist. | Drehen Sie das Ei schnell seitlich, um ein langes Gefäß an der Eimembran befestigt zu sehen. | ||||||
| 3.3 & 3.8 | Perforation der äußeren Eierschalenmembran beim Bohren. | Falsche Positionierung des Bohrers. | Positionieren Sie den Bohrer beim Bohren fast parallel zur Eierschale. Wenn die Membran in Schritt 3.3 perforiert wird, ist es nicht erforderlich, eine weitere Perforation mit Nadel durchzuführen, wie in Schritt 3.5 angegeben. Wenn Blutungen auftreten, entsorgen Sie das Ei. | ||||||
| 4.3 | DRG bleibt an der Zange. | DRG ist trocken. | Nass DRG wieder in HBSS und/oder verwenden Sie eine feine Nadel, um DRG von Zangen zu lösen. | ||||||
| 5.2 | Zellen sind nicht perfekt mit fluoreszierendem Farbstoff gekennzeichnet. | Inkubationszeit. Einige Zellen benötigen mehr Zeit für die Beschriftung. | Halten Sie Zellen für eine zusätzliche Stunde in den Medien mit Fluoreszenzfarbstoff. | ||||||
| 5,6 | Luftblase auf dem Zellabfall. | Mit der gesamten Flüssigkeit in der Pipettenspitze. | Laden Sie 1 L mehr als das gewünschte Volumen und verwenden Sie nicht die endgültige L der Pipette bei der Implantation von Zellen. Dadurch werden Luftblasen im Zellmix vermieden. | ||||||
| 6.3 | DrG oder Zellen können bei der Ernte des CAM nicht identifiziert werden. | Kleine DRG, DRG wurde verdrängt, Krebszellen verbreiten sich. | Wenn DRG nicht gesehen wird, ernten Sie eine größere Fläche des CAM und legen Sie in einen größeren Behälter zur Fixierung. Überprüfen Sie DRG und Zellposition unter Fluoreszenz in einem Stereomikroskop, und trimmen Sie das CAM dann auf eine kleinere Größe für die Paraffineinbettung. | ||||||
Tabelle 1: Fehlerbehebungstabelle
Das hier vorgestellte CAM-DRG-In-vivo-Modell befasst sich mit den Defiziten früherer Modelle, indem es die Nerven-Tumor-Interaktion vor der physischen Invasion des Nervs durch Tumorzellen demonstriert. Die meisten In-vivo-Studien von PNI konzentrieren sich auf Tumorausbreitung und Hemmung der motorischen Funktion, und hängen von der direkten Injektion von Tumorzellen in Ischiasnerven23,24,25. Die Ischiasnerveninjektion ist ein In-vivo-Modell von PNI, bei dem Krebszellen in einen Schiasnerv der Maus oder Der Ratte injiziert werden, wo der Tumor anschließend wächst. Injektionsmodelle sind nützlich, um destruktive Tumorprogression und Schmerzen zu zeigen, die aus Tumorzellen innerhalb der Nerven entstehen. Das Ischiasnervenmodell eignet sich auch für die Untersuchung von Faktoren, die es Krebszellen ermöglichen, im Nerv zu gedeihen, aber es fehlt die Fähigkeit, die frühe Phase von PNI zu bewerten, weil es Zellen direkt in den Nerv einführt, unter Umgehung von Nervenscheiden. In einem anderen Ansatz wurden chirurgisch implantierte orthotopische Tumortransplantate verwendet, um die Bedeutung von adrenergen und cholinergen Nervenfasern bei der Förderung der Prostatakrebsprogression zu charakterisieren, was auf eine herausragende Rolle der Nerven bei der Tumorprogression hindeutet. 26. Dieses Modell bestand aus chemischer Ablation von murinen sympathischen und parasympathischen Nerven. Die parasympathischen Fasern infiltrierten Tumorgewebe, ein Prozess im Zusammenhang mit PNI, aber das Modell wurde nicht speziell verwendet, um physikalische Wechselwirkungen zwischen dem Nerv und Tumor zu bewerten. Das CAM-DRG-Modell ermöglicht die Untersuchung von Wechselwirkungen zwischen Nerven und Krebs während PNI. Darüber hinaus sind murine Modelle im Vergleich zum CAM-Modell teuer und zeitaufwändig. Wir empfehlen die Verwendung des CAM-DRG-Modells für mechanistische Studien von PNI.
Einige Vorteile des CAM-DRG-Ansatzes sind die Bewertung von PNI und anderen Phänotypen, wie Tumorwachstum, Metastasierung und Angiogenese. Die Identifizierung menschlicher DNA am unteren CAM und/oder in der Leber kann zum Nachweis von Metastasen menschlicher Krebszelllinien10verwendet werden, einem empfindlicheren experimentellen Ansatz im Vergleich zu Gewebeschnitt und Färbung, der möglicherweise keine kleinen Metastasen offenbart.
Die CAM-DRG-Methode hat einige Einschränkungen, einschließlich des kurzen Beobachtungszeitrahmens. Das Immunsystem des Embryos ist physiologisch aktiv am Tag 1827, wenn Abstoßung und ein entzündlicher Prozess stattfinden können, die die experimentelle Zeit begrenzen. Es ist auch wichtig, den Abstand bei der Transplantation von Tumorzellen in der Nähe des DRG zu berücksichtigen; größere DRG-Krebsentfernungen könnten die molekularen Wechselwirkungen zwischen Tumorzellen und Nerven beeinträchtigen oder den physischen Kontakt zwischen beiden Komponenten des Modells verzögern. Auch wenn die Embryonen älter sind als in diesem Protokoll vorgesehen, könnten Embryobewegungen die Tumorzellen verdrängen. Daher ist es wichtig, Eier zu verwenden, die mit Tag 10 nach der Befruchtung für die Zelltransplantation übereinstimmen.
Da das Immunsystem vor dem 18.Tagnicht vollständig entwickelt ist, ähnelt die Tumormikroumgebung im CAM der der immunsuppressierten murinen Modelle, die häufig für Krebsstudien verwendet werden. Daher ist dieses Modell nicht nützlich, um die Rolle von Immunzellen bei der Tumorprogression zu bewerten. Eine weitere Einschränkung ist die eingeschränkte Verfügbarkeit von Reagenzien für Hühnerarten wie Antikörper, Zytokine und Primer.
Die genaue Durchführung dieses Protokolls erfordert Übung; Es kann jedoch von einem Labormitglied ohne Notwendigkeit für eine spezialisierte Kerneinrichtung durchgeführt werden. Das Bohren der Eierschale erfordert Eine Schulung. Üben auf Lebensmitteleiern (nicht befruchtet) wird empfohlen, bevor Sie dieses Modell zum ersten Mal versuchen. Ein hohes embryonales Überleben und Erfolg des Modells können erreicht werden, wenn einige kritische Schritte zur Vermeidung einer Infektion befolgt werden: angemessene Antibiotikaprophylaxe von DRGs in 2% Pen/Strep, Arbeiten in einem laminaren Strömungsschrank und Vermeidung der Dispersion von Eischalenpartikeln auf das CAM. Es ist auch wichtig, stabile Luftfeuchtigkeit während der gesamten Inkubationszeit des Eis zu halten. Wir empfehlen, die Anzahl der Eier pro Gruppe zu erhöhen, bis die Technik gemeistert ist. Die häufigsten Probleme für unerfahrenes Laborpersonal sind die Eikontamination und die ungenaue Technik bei der Zelltransplantation.
Die DRG-Ernte erfordert auch Eine Schulung; Praxis bei der Ernte von DRGs für In-vitro-Experimente8 vor dem Versuch des In-vivo-Modells wird empfohlen. Die In-vitro-DRG-Kultur ist eine Gelegenheit, die Bedingungen zu optimieren und die Technik zu verbessern, um die Dauer der DRG-Extraktion zu verkürzen. Besondere Aufmerksamkeit ist der Erntetechnik beim Greifen der DRG mit Zangen erforderlich. Die DRG sollte nicht direkt gehalten werden; Druck unter ihm aufgebracht werden. Wir empfehlen die Verwendung von Lupe, um das DRG während der Extraktion besser zu visualisieren.
Wichtig ist, dass bei der ersten Ausführung dieses Modells alle Bedingungen für die gewünschte Zelllinie optimiert werden sollten. Dieses Modell wurde für Ratten-DRG und die HNC-Zelllinie UM-SCC-1 optimiert. Die Verwendung von Maus-DRG und anderen Krebszelltypen kann eine Optimierung erfordern. Mit einer höheren Konzentration von transplantierten Zellen neigen Tumoren dazu, dicker und steifer zu werden, was Tumormessungen erleichtert. Unter Berücksichtigung mehrerer Eier für jede Gruppe und einer angemessenen Konzentration von Zellen für jedes Ei können für jedes Experiment mehrere Millionen Zellen erforderlich sein. Um die Planung zu erleichtern, sollte die Kenntnis der Verdoppelungszeit der Zellen berücksichtigt werden. Für einige wichtige Schritte in diesem Protokoll wird eine Fehlerbehebungstabelle bereitgestellt (Tabelle 1).
Die Autoren erklären keine konkurrierenden Interessen.
Diese Arbeit wurde durch die NIH/NIDCR-Stipendien DE027551 und DE022567 (NJD) unterstützt.
| Name | Company | Catalog Number | Comments |
| 0.25% Trypsin-EDTA (1x) | Gibco | # 25200-056 | |
| ACE light source | SCHOTT North America, Inc. | Used to transilluminate the eggs | |
| CellTracker Green CMFDA fluorescent dye | Life Technologies | # C7025 | Reconstitute 50µg in 20µL of DMSO and stock at -20oC. Use 1µL of stock solution/mL of culture medium. |
| CellTracker Red CMTPX fluorescent dye | Life Technologies | # C34552 | Reconstitute 50µg in 40µL of DMSO and stock at -20oC. Use 1µL of stock solution/mL of culture medium |
| Cordless rotary tool | DREMEL | # 866 | Used to drill the egg shell |
| DMEM (1x) | Gibco | # 11965-092 | Dulbeecco`s Modified Eagle Medium |
| DMSO | Fisher Bioreagents | # BP231-100 | Dimethyl Sulfoxide |
| Dumont # 5 fine forceps | Fine Science Tools (FST) | # 11254-20 | Used to harvest DRG |
| Egg incubator | GQF Digital Sportsman | # 1502 | Egg incubator equipped with automatic rotator, digital thermostat, temperature and humidity controls |
| Engraving cutter | DREMEL | # 108 | Used to drill the egg shell |
| Extra fine Graefe forceps, curved | Fine Science Tools (FST) | # 11151-10 | Used to graft DRG onto the CAM on day 8 and to harvest CAM tissue on day 17 |
| Extra fine Graefe forceps, straight | Fine Science Tools (FST) | # 11150-10 | Used to graft DRG onto the CAM on day 8 and to harvest CAM tissue on day 17 |
| Fertilized Lohmann White Leghorn eggs | Fertilized eggs at early fertilization days, preferably on first day post-fertilization. Eggs used in this protocol are from Michigan State University Poultry Farm. | ||
| Filter Forceps | EMD Millipore | # XX6200006P | Blunt forceps used to remove the egg shell |
| Fine surgical straight sharp scissor | Fine Science Tools (FST) | #14060-09 | Used to harvest the CAM tissue on day 17 |
| HBSS (1x) | Gibco | # 14025-092 | Hank`s Balanced Salt Solution |
| HI FBS | Gibco | # 10082-147 | Heat-inactivated Fetal Bovine Serum |
| Paraffin wax membrane | Parafilm laboratory film | # PM-996 | Used to temporarily cover the egg openings until DRG grafting on day 8 |
| PBS (1x) pH 7.4 | Gibco | # 10010-023 | Phosphate Buffered Saline |
| Pen/Strep | Gibco | # 15140-122 | 10,000 Units/mL Penicilin, 10,000 µg/mL Streptomycin |
| PFA (paraformaldehyde solution) | Sigma-Aldrich | # P6148-1KG | Dilute in water to make a 4% PFA solution |
| Sprague Dawley rats (females) | Charles River laboratories | Strain code: 001 | 6-7 weeks old (190-210g in weight) |
| Tegaderm Transparent Film Dressing | 3M | # 9505W | Sterile, 6x7cm, used to cover the egg openings during incubation |
- Schmitd, L. B., Scanlon, C. S., D'Silva, N. J. Perineural Invasion in Head and Neck Cancer. Journal of dental research. 97 (7), 742-750 (2018).
- Liebig, C., Ayala, G., Wilks, J. A., Berger, D. H., Albo, D. Perineural invasion in cancer: a review of the literature. Cancer. 115 (15), 3379-3391 (2009).
- Schmitd, L. B., et al. Redefining Perineural Invasion: Integration of Biology With Clinical Outcome. Neoplasia (New York, N.Y). 20 (7), 657-667 (2018).
- Chinn, S. B., et al. Impact of perineural invasion in the pathologically N0 neck in oral cavity squamous cell carcinoma. Otolaryngology--head and neck surgery : official journal of American Academy of Otolaryngology-Head and Neck Surgery. 149 (6), 893-899 (2013).
- Tai, S. K., Li, W. Y., Yang, M. H., Chu, P. Y., Wang, Y. F. Perineural invasion in T1 oral squamous cell carcinoma indicates the need for aggressive elective neck dissection. The American journal of surgical pathology. 37 (8), 1164-1172 (2013).
- Scanlon, C. S., et al. Galanin modulates the neural niche to favour perineural invasion in head and neck cancer. Nature communications. 6, 6885 (2015).
- Amit, M., et al. Upregulation of RET induces perineurial invasion of pancreatic adenocarcinoma. Oncogene. 36 (23), 3232-3239 (2017).
- Huyett, P., Gilbert, M., Liu, L., Ferris, R. L., Kim, S. A Model for Perineural Invasion in Head and Neck Squamous Cell Carcinoma. Journal of visualized experiments : JoVE. (119), (2017).
- Ayala, G. E., et al. In vitro dorsal root ganglia and human prostate cell line interaction: redefining perineural invasion in prostate cancer. The Prostate. 49 (3), 213-223 (2001).
- Liu, M., et al. The Histone Methyltransferase EZH2 Mediates Tumor Progression on the Chick Chorioallantoic Membrane Assay, a Novel Model of Head and Neck Squamous Cell Carcinoma. Translational oncology. 6 (3), 273-281 (2013).
- Busch, C., Krochmann, J., Drews, U. The chick embryo as an experimental system for melanoma cell invasion. PloS one. 8 (1), e53970 (2013).
- Li, M., et al. The In Ovo Chick Chorioallantoic Membrane (CAM) Assay as an Efficient Xenograft Model of Hepatocellular Carcinoma. Journal of visualized experiments : JoVE. (104), (2015).
- Ota, I., Li, X. Y., Hu, Y., Weiss, S. J. Induction of a MT1-MMP and MT2-MMP-dependent basement membrane transmigration program in cancer cells by Snail1. Proceedings of the National Academy of Sciences of the United States of America. 106 (48), 20318-20323 (2009).
- Murphy, J. B. TRANSPLANTABILITY OF TISSUES TO THE EMBRYO OF FOREIGN SPECIES : ITS BEARING ON QUESTIONS OF TISSUE SPECIFICITY AND TUMOR IMMUNITY. The Journal of experimental medicine. 17 (4), 482-493 (1913).
- Ribatti, D., Nico, B., Vacca, A., Presta, M. The gelatin sponge-chorioallantoic membrane assay. Nature. 1 (1), 85-91 (2006).
- Auerbach, R., Arensman, R., Kubai, L., Folkman, J. Tumor-induced angiogenesis: lack of inhibition by irradiation. International journal of cancer. 15 (2), 241-245 (1975).
- Banerjee, R., et al. The G protein-coupled receptor GALR2 promotes angiogenesis in head and neck cancer. Molecular cancer therapeutics. 13 (5), 1323-1333 (2014).
- Ossowski, L., Reich, E. Experimental model for quantitative study of metastasis. Cancer research. 40 (7), 2300-2309 (1980).
- Nowak-Sliwinska, P., Segura, T., Iruela-Arispe, M. L. The chicken chorioallantoic membrane model in biology, medicine and bioengineering. Angiogenesis. 17 (4), 779-804 (2014).
- Moreno-Jimenez, I., et al. The chorioallantoic membrane (CAM) assay for the study of human bone regeneration: a refinement animal model for tissue engineering. Scientific reports. 6, 32168 (2016).
- Vu, B. T., et al. Chick chorioallantoic membrane assay as an in vivo model to study the effect of nanoparticle-based anticancer drugs in ovarian cancer. Scientific reports. 8 (1), 8524 (2018).
- Sleigh, J. N., Weir, G. A., Schiavo, G. A simple, step-by-step dissection protocol for the rapid isolation of mouse dorsal root ganglia. BMC research notes. 9, 82 (2016).
- Cavel, O., et al. Endoneurial macrophages induce perineural invasion of pancreatic cancer cells by secretion of GDNF and activation of RET tyrosine kinase receptor. Cancer research. 72 (22), 5733-5743 (2012).
- Guo, K., et al. Interaction of the sympathetic nerve with pancreatic cancer cells promotes perineural invasion through the activation of STAT3 signaling. Molecular cancer therapeutics. 12 (3), 264-273 (2013).
- Deborde, S., et al. An In Vivo Murine Sciatic Nerve Model of Perineural Invasion. Journal of visualized experiments : JoVE. (134), (2018).
- Magnon, C., et al. . Autonomic nerve development contributes to prostate cancer progression. 341 (6142), 1236361 (2013).
- Ribatti, D. Chick embryo chorioallantoic membrane as a useful tool to study angiogenesis. International review of cell and molecular biology. 270, 181-224 (2008).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved