Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Medicine
ממברנה של צ'יק כוראלאנטוניק במודל Vivo להערכת הפלישה לתוך הראש ולסרטן הצוואר
הפלישה הנקבים הוא פנוטיפ אגרסיבי הראש והצוואר קרצינומה של תאים וגידולים אחרים. מודל הממברנה של האפרוח שימש ללימוד אנגיוגנזה, הפלישה לסרטן וגרורות. כאן אנו מדגימים כיצד מודל זה יכול להיות מנוצל כדי להעריך את הפלישה הנקבים בvivo.
הפלישה הנקבים היא פנוטיפ שבו הסרטן מקיף או פולש לעצבים. זה קשור התוצאה הקלינית הירודה של הראש והצוואר קרצינומה של תאים סרטניים אחרים. מחקרים מכניסטיים הראו כי הוצלב המולקולרי בין העצבים לתאי הגידול מתרחש לפני האינטראקציה הפיזית. יש רק כמה מודלים vivo לחקר הפלישה הנקבים, במיוחד כדי לחקור התקדמות מוקדמת, לפני אינטראקציות פיזיות הגידול הפיזי להתרחש. מודל ממברנה של האפרוח שימש לחקר הפלישה לסרטן, כי קרום המרתף של האפיתל הוריוני מחקה את זה של רקמת האפיתל האנושי. כאן אנו מחדש את מודל ממברנה האפרוח כוראלאלי לחקור הפלישה הנקבים, השתלת עכברוש בסיס שורש והראש האנושי הצוואר קרצינומה של תאים סרטניים על האפיתל כוריוני. הדגמנו כיצד מודל זה יכול להיות שימושי כדי להעריך את היכולת של תאים סרטניים לפלוש רקמות עצביות vivo.
הפלישה הנקבים (PNI) הוא הפנוטיפ מתחת למחקר בסרטן, אשר קשורה להישנות מחלות גבוהות הישרדות עניים בחולים עם הראש והצוואר קרצינומה של תאים קשקשיים (HNC)1. Pni הוא הגדיר מיקרוסקופיסטית כמו תאים סרטניים בתוך או מסביב לעצבים2,3. כאשר pni מזוהה, המטופלים צפויים לקבל טיפולים שדון כגון ניתוח בחירה בצוואר ו/או טיפול בקרינה4,5. עם זאת, טיפולים אלה הם אגרסיביים, ולא PNI ספציפי. למעשה, אין טיפול כדי לחסום PNI, בעיקר בגלל המנגנונים הבסיסיים אינטראקציות הגידול העצבי עדיין מובנים בצורה גרועה.
מנגנונים מולקולריים שונים היו מעורבים במשיכה הגידול העצבי; גידולים ותאים סטרומה שחרור נוירופפטידים וגורמי גדילה כדי לקדם neuritogenesis6,7. כאשר מתורבתים יחד בתוך מבחנה, תאים HNC ו גנגוליה שורש (DRG) שניהם יש תגובה חזקה; ההשפעות על הפלישה תא הגידול neuritogenesis ניתן לראות לאחר כמה ימים בתרבות6,8,9. עם זאת, יש חוסר מתאים במודלים vivo כדי לחבר בין אינטראקציות הגידול-עצבי לפני פלישה. כאן אנו מציגים מודל PNI vivo ללמוד אינטראקציות מוקדמות בין התאים HNC והעצבים6. התאמתי את הקרום הנשי הממברנה (CAM) מודל לכלול מרכיב עצבי, השתלת DRG ב-CAM, ואחריו השתל של תאים סרטניים לחקות מיקרוסביבה innervated הגידול.
מודל פקה שימש בהצלחה כדי להעריך את הפלישה של תאים דרך קרום המרתף, חיקוי בשלבים פולשנית מוקדם של קרצינומות ומלנומה10,11,12. CAM מורכב אפיתל כוריוני עליון, מהתערב mesenchyme, ו אפיתל allantoic נמוכה. האפיתל כוריוני הוא מבחינה מבנית דומה האפיתל האנושי10,13 בגלל קרום קולגן-IV-המרתף מדמה את קרום המרתף המפריד האפיתל אוראלי מרקמת החיבור הבסיסית. מאז שתלי הגידול הראשון בוצעו במצלמת ב 191314, עיבודים רבים של השיטה פותחו כדי לאפשר הערכה של אנגיוגנזה15,16,17, התקדמות הגידול, ו מיכלבן 18 והכי חשוב, הטכניקה של גידולים השתלה על המצלמה השתנתה מעט מאוד, אבל היישומים מתפתחים ברציפות. Assays של המורכבות הגוברת פורסמו, כולל הקרנת סמים19, רקמת עצם הנדסה20, ו מבוססי תרופות נגד סרטן21.
המעבדה שלנו משתמשת מודל CAM-DRG שבו DRG היונקים הוא מבודד מושתל על פני השטח של CAM העליון. לאחר DRG הופך משולבים ב-CAM, התאים HNC מושתלים ליד DRG ומותר לקיים אינטראקציה עם DRG לפני כולה במערכת vivo הוא נקצרו ונותחו. חשוב מכך, המערכת מאפשרת התבוננות חזותית לשעבר vivo של DRG ו הגידול על ידי תיוג הזריחה של DRG ותאים סרטניים. פרוטוקול זה כולל מספר שלבים עם רמות שונות של מורכבות שבוצעו בתוך 17 ימים, מתוך הביצים הדגירה כדי לקצור את מצלמת הסרט (איור 1). תאים המבטאים חלבונים שונים של ריבית ניתן נבדק במודל זה כדי להבהיר את מסלולים מולקולריים האחראים לפלישת העצבים בסרטן, וגם עבור תרופות הקרנה ישירות היעד הפלישה העצבית. תאים שטופלו מראש עם התרופה המועמד יכול להיות מושתל על CAM ואת המופע של PNI נחקר בהשוואה פקדים מטופלים. למעשה, מודל CAM שימש להקרנה התרופה כצעד ביניים בין מחקרים מחוץ למחקר וניסויים פרה-קליניים vivo מכרסמים ב19.
התכנון הניסיוני ישתנה עם ההשערה. למשל, אם בודקים את התפקיד של חלבון מסוים על PNI, הקבוצה הניסיונית תכלול DRG מושתל עם תאי הגידול מבטאים את החלבון, בעוד קבוצת הביקורת צריך לכלול DRG עם תאים באופן מאוד מנוכר עם וקטור ריק. ניתן להשתמש במספר עיצובים ניסיוניים שונים כדי לטפל בשאלות ספציפיות.
הצהרת האתיקה: כל הניסויים המשתמשים בחולדות בפרוטוקול זה נעשים בהתאם ל-IACUC (ועדת הטיפול המוסדי והשימוש בבעלי חיים) מהמוסד שלנו. ניסויים עם ביצים במחקר זה פטורים מרגולציה IACUC.
1. דגירה הביצית (משוער העיתוי: 5 דקות, יום אפס)
- קבל-מסחרי המופרית ללא מסחר הוליסטי לבן לגהורן ביצים, רצוי ביום הראשון לאחר ההפריה. דגירה שש ביצים לכל קבוצה ניסיונית בתוך מחולל ביצה לפני החממה ב 38 ° c ו 54% לחות עבור 8 ימים עם סיבוב שעה. השתמשו בסיבוב רגיל של הביצים כדי למנוע מהעובר לדבוק בקרום הביצה.
הערה: לפני דגירה, לשמור את הביצים במקרר 18 ° c כדי לעצור את התפתחות העובר למשך שבוע מקסימום 1.
2. קציר והכנת DRGs (עיתוי משוער: 2 h, יום 8)
הערה: ניסויים עם עכברים וחולדות דורשים אישור של (IACUC). במדינות מסוימות, השימוש בביצים עוף דורש גם אישור.
- לקבל שישה עד שבע חולדות בשבוע בן הזוג משחק (~ 200 g במשקל) כדי לחלץ DRGs.
הערה: עכברוש אחד צריך להניב ~ 40 בצוואר הרחם ו DRGs החזה הצווארי. עכבר DRGS גם משתלב CAM, אולם התנאים עבור מין זה צריך להיות ממוטב באופן עצמאי. - בארון זרימה למינארי, המסיק מאזורי הצוואר והחזה בעקבות הפרוטוקול להפקת DRGS העכבר שפורסם במקום אחר22. עקוב אחר איור 2 לאוריינטציה כיצד לקצור drgs.
- המתת החסד על ידי ניקוב הלב לאחר הממשל של קטמין/Xylazine הזריק intraperitoneally. נקה את העור עכברוש עם 70% אתנול ולהסיר את עמוד השדרה חולדה באמצעות מספריים. אין לבצע פריקה צוואר הרחם כי זה יפגע DRGs צוואר הרחם.
- הפרידו את האזורים הצווארי, בית החזה והמותניים עם אותו מספריים, בעקבות הייצוג האנטי-אטומי ותמונות ברוטו שסופקו באיור 2A-D. מניחים את מקטעי עמוד השדרה בצלחת התרבות 10 ס מ עם 1x PBS כדי לשמור על הרקמות רטובות.
- בעזרת מספריים של עצם עדינה, פתחו את עצמות החוליות בהיבטים הצדדיים והגטים, המפרידים בין עמוד השדרה לשני חצאים לרוחב (איור 2E-F). מניחים את מקטעי הרקמה בצלחת 10 ס"מ נקי עם חדש 1x PBS.
- באמצעות מלקחיים, לנתק בעדינות את חוט השדרה מן העצמות החוליות כדי להמחיש את DRGs (איור 2G).
- עם מלקחיים עדינים החזיק מתחת כל DRG, לתפוס אותו ולמשוך אותו החוצה מחלל העצם שבו הוא תקוע. אין להחזיק את ה-DRG ישירות כי זה יגרום נזק לרקמות. אין לחתוך את החבילות אקסון מ-drg (איור 2h).
הערה: הימנע משימוש ב-DRGs המותני מאז אלה הפחיתו אינטגרציה ב-CAM. למיקום האזור DRG, עקבו אחר האיור הסכמטי והדימויים האנטומיים הדוחים באיור 2A-D.
- מיד לאחר הקציר, מקום כל DRG לתוך בינוני התרבות DMEM שיושלם עם 2% פניצילין/סטרפטומיצין (עט/דלקת) ו 10% חום מופעל סרום העוברי (FBS) כדי לסייע למנוע זיהום חיידקי של Drg. Group כל Drg באותו 6 ס מ צלחת תרבות עם 4 מ ל של תרבות בינונית.
- לאחר איסוף כל DRGs, להעביר אותם לצלחת תרבות חדשה עם בינוני התרבות DMEM בתוספת 2% עט/דלקת פלוס 10% FBS והמכיל 1.25 μg/mL של צבע פלורסנט אדום. מודטה עבור 1 h בחממה תרבות התא. במהלך הזמן הזה, הכן את הביצים לקבל את ה-DRG כמתואר להלן (שלב 3).
הערה: המרווח בין הקציר DRGs והשלמת תיוג פלואורסצנטית צריך להספיק כדי להכין את הביצים; ניתן לשמור את הדראגים. לכמה שעות בחממה
3. הכנת ביצים להשתלת DRG (עיתוי משוער: 1 h עבור תריסר ביצים, יום 8)
- בארון זרימה למינארי, עמעם את האור והדליקו את הביצים כדי לבדוק את הכדאיות ואת השלב העובריים. לא לכלול ביצים עם ואצלב עני, ביצים לא מופרות, או ביצים לא עקבי עם יום 8 פוסט הפריה. החזיקו את הביצה בעדינות עם שק האוויר הטבעי המתרחש לעבר מקור האור (איור 3A).
- עם עיפרון, סמן את מעטפת הביצה כדי לקבל את הפתחים (איור 3A-B).
- ראשית, לזהות את הקובץ המצורף של העובר המתפתח ל-CAM כמו כלי נע כהה המצורפת קרום הביצה ולסמן אזור זה כדי למנוע התערבויות באזור זה.
- שנית, בחרו באזור חלון ההפעלה כאזור ואצלב לפחות 2 ס מ מהעובר המצורף וציירו מעגל בקוטר 1.5 ס מ. כ 1 ס מ מחלון ההפעלה, לצייר כיכר 0.5 ס מ באזור הvascularized פחות.
- שלישית, צייר את אזור שק האוויר כדי להוציא אותו מאזור הפעולה. תסמן את אמצע. שק האוויר עם צלב
- עם כלי רוטרי ומקדחה חריטה, 3 מ"מ קוטר, לקדוח את קליפת הביצה בכיכר מסומן (איור 3C). השתמש מלקחיים קהה להסיר את פגז ביצה מבלי להסיר את קרום פגז הביצית החיצונית (הקרום הלבן ממש מתחת למעטפת) (איור 3D). עבוד בזהירות כדי למנוע ניקוב מקרי של קרום זה.
- באמצעות התרגיל אותו כמו בשלב 3.3, לעשות ניקוב מדויק בצלב מסומן באזור שק האוויר כדי לאפשר זרימת אוויר לתוך הביצה (איור 3E). להיזהר לא להחיל יותר מדי לחץ על הביצה, כדי למנוע שבירת או להזיק לו.
- מקום 30 μL של HBSS בפתח הכיכר, מעל קרום מעטפת ביצה החיצוני שלמים (איור 3E). עם מחט של 30 גרם מזרק, לעשות ניקוב מדויק בקרום החיצוני באזור זה מרובע (איור 3F).
- מניחים את הביצה במקור האור כדי להמחיש את שק האוויר. להפעיל לחץ על הנורה הגומי טפטפת ולמקם אותו חירור קטן שנעשה באזור שק האוויר (שלב 3.4). שחרר לחץ על הנורה עד שתראה את הפרדת שני הקרומים באזור חלון ההפעלה (איור 3G); חזור על שלב זה פעמים רבות ככל שתצטרך כדי להשיג הפרדה מלאה של הקרומים באזור חלון ההפעלה.
- חזור על שלבים 3.1-3.6 עבור כל הביצים.
- באמצעות התרגיל אותו כמו בשלב 3.3, לקדוח את חלון ההפעלה המעגלית נזהר לא לקרוע את קרום פגז ביצה החיצונית (איור 3H). נקו את משטח הביצה על ידי הדבקה עדינה של סרט דביק כדי להסיר את כל החלקיקים הרופפים.
- עם מלקחיים קהה, להסיר את קליפת הביצה מאזור הקדח (איור 3I-J). הבא, עם מלקחיים אותו, להסיר את קרום פגז ביצה חיצונית (איור 3K), להיות זהירים לא להחדיר חלקיקים פגז קטן בתוך הביצה כדי למזער את הזיהום.
- זהה את מצלמת ה-CAM בעומק של 1 ס מ ממשטח הביצה. מכסים כל ביצה נפתחה זמנית עם קרום שעווה פרפין כדי למנוע זיהום (איור 3L).
- חזור על שלבים 3.8-3.10 עבור כל הביצים. הניחו את הביצים חזרה בחממה ללא סיבוב עד שה-DRGs יהיו מוכנים להשתלת.
4. השתלת מצלמה (עיתוי משוער: 40 דקות, יום 8)
- להכין צלחת תרבות 6 ס מ עם מדיום HBSS, כדי לשטוף את DRGs לפני השרשה. הביאו את הביצים המוכנות לתרבית התאים לארון הזרימה המבינארי. הסירו את קרום הפרפין מהביצה (איור 4A).
- עם מלקחיים סטריליים בסדר, לתפוס בעדינות אחד DRG מתוך מדיום התרבות. טבול אותו במדיום HBSS כדי להסיר את עודפי המדיום המכילים את צבע הפלורסנט. החזיקו את ה-DRG בעדינות רבה; אחרת, זה יהיה לדבוק הלקחיים.
- מניחים את DRG על מצלמת, להיזהר לא ניקוב קרום (איור 4B-C). במקרה הצורך, להשתמש בזוג אחר של מלקחיים כדי לעזור לנתק את DRG מהקצה של מלקחיים בעת הצבת אותו על CAM.
הערה: שמירה על DRG רטוב עם מדיום HBSS גם להקל על התנתקות מן המלקחיים. - כסו את הביצה בעזרת הקרנת סרט שקוף סטרילי. לכסות את כל החלונות ודקירות עשה במעטפת הביצה כדי למנוע זיהום חיידקי (איור 4D).
- לאחר השתלת DRGs בכל הביצים, מודיית את הביצים בתוך מחולל לחות בחממה ב 38 ° c ו 54% לחות עבור 2 ימים, ללא סיבוב.
5. השתלת תאי גידול במצלמת הסרט (עיתוי משוער: 1 h 30 דקות, יום 10)
- ב 48 h לפני השתלת התאים, צלחת התאים הדרושים בלוחות התרבות. חישוב 0.5 כדי 1 x 106 תאים לכל ביצה עבור UM-scc-1 תאים על מנת ליצור גידולים תלת מימדיים של המצלמה. שים לב שמספר התאים עשוי להשתנות בהתאם לקו התאים.
- מולחים בינונית ולהוסיף בינונית תרבות DMEM דיום בתוספת 1% עט/דלקת פלוס 10% FBS ו 2.5 μg/mL של צבע פלורסנט ירוק. דגירה של 1 h ב 37 ° c בחממה תרבות התא. לאחר מכן, בדוק את עוצמת הקרינה על המיקרוסקופ, מאחד בינוני, לשטוף פעם אחת עם 1 x PBS, ולהוסיף 0.25% טריפסין עד 10 דקות. לנטרל טריפסין עם DMM בתוספת מדיום.
- צנטריפוגה ב 250 x g עבור 4 דקות כדי ליצור גלולה תא. מנקה בינונית DMEM דיום ו-להשעות מחדש ב HBSS כדי לשטוף את צבע פלורסנט עודף. ספירת תאים באמצעות הומוציטומטר.
- הביאו את הביצים לתרבית. התאים לארון הזרימה עם מספריים ומלקחיים, לפתוח את הסרט שקוף ההלבשה המכסה את הביצה (איור 4E-F).
- צנטריפוגה את המספר המחושב של תאים שוב, מביס את המדיום HBSS ולהשעות מחדש בריכוז הסופי של 0.5 אל 1x106 תאים לכל 5 μl של אותו מדיום (איור 4g). הכינו את הסכום הדרוש למספר הכולל של ביצים (5 μL של השעיית תאים לכל ביצה).
- מקום 5 μL של פתרון התא על מצלמת, כ 2 מ"מ מ DRG (איור 4H). שמור על מרחקים אחידים בין התאים DRG. להיזהר מאוד לא להפריע את הביצה כדי למזער את התפשטות התאים.
הערה: כדי להתחיל השרשה תא, לבחור ביצים שמשטח CAM יבש באופן חזותי. אם המשטח רטוב מדי, התאים יכולים להתפשט ולא ליצור גידולים רגילים. - לכסות את הביצה עם התחבושת הסרט החדש כמו בשלב 4.4. להשתיל את התאים בכל הביצים. מודיית את הביצים בתוך מחולל לחות בחממה ב 38 ° c ו 54% לחות עבור 7 ימים, ללא סיבוב.
6. לאסוף את המצלמה (עיתוי משוער: 1 h עבור תריסר ביצים, יום 17)
- הכינו לוחיות 6-היטב עם 4% (פאראפורמלדהיד) pH 7.0, אחד טוב לכל ביצה, 2 מ ל לכל היותר.
- . תביא את הביצים לספסל מעבדה באמצעות מחט המצורפת מזרק כדי לנקב את הסרט ההלבשה, ירידה סביב 300 μL של התחתית על גבי CAM כדי להתקשות מעט מצלמת CAM, ובכך להקל על תהליך הקציר. . חזור על זה עבור כל הביצים
- עם מספריים, להסיר את החצי העליון של פגז ביצה (שם חלון ההפעלה ממוקם) עם CAM מצורף אליו (איור 4I). להקטין את הגודל של חצי זה עד כ 3 ס מ בקוטר, שמירה על החלק של CAM שבו DRG ותאים סרטניים היו מושתלים במרכז (איור 4J). לתפוס את מצלמת עם מלקחיים עדינים ולנתק אותו מקליפת הביצה תוך הצבת אותו לתוך המעלה למעלה. האוריינט התאים DRG ו סרטן הפונה כלפי מעלה (איור 4K-L).
הערה: שטח 3 ס מ צריך לכלול גם את התאים DRG ו. DRG הוא ראה בקלות כמו גוש קטן מצורף על CAM, אולם תאים סרטניים הם לפעמים קשה לזהות במבחן ברוטו. - לחילופין, עם מספריים, להרחיב את חלון ההפעלה הסרת פגז ביצה מלמעלה של הביצה תוך שמירה על מצלמת מקום; להסיר כ 1 ס מ מעבר לחלון ההפעלה (איור 4M) ולזהות את drg ואת התאים על מצלמת (איור 4m-O). עם מלקחיים עדינים עדין, החזיקו את מצלמת המצלמה באחת הקצוות והרימו אותה בעדינות. עם מספריים עדינים חדים, בעדינות לחתוך את CAM כדי להסיר אזור עגול, כ 3 ס מ קוטר (איור 4P), ומניחים את מצלמת המשחק בחצי המשחק עם התאים drg ו סרטן פונה כלפי מעלה.
הערה: הימנע מתיחה או החזקת CAM עם מלקחיים במקומות מרובים כדי למזער את הנזק לרקמות שעשויות ליצור חפצי מיקרוסקופ. - מניחים כל קרום CAM אחד טוב (איור 4L). לתפוס בעדינות את הקצוות של מצלמת לפזר את הרקמה לפתוח בתוך התחתית או בעדינות לנער את הצלחת עד מצלמת הפרש, כדי למנוע חפצים לקפל.
- המתת חסד העובר (יום 17) על ידי עריפת ראש מהירה. לתקן את הרקמות שנקטפו בכיתה 4 h בטמפרטורת החדר. לאחר הקיבעון, להחליף את הג באמצעות 1x PBS ולאחסן רקמות ב-PBS ב-4 ° c עד הטבעה פרפין לצורך שיבוץ. למנוע קיבעון מעל כי יהיה נזק הvascuלטורה עדינה של מצלמת.
- באמצעות stereomicroscope ניאון, לצלם את הקרומים בתוך 2 ימים לאחר הקציר כדי למנוע אובדן של אותות פלורסנט.
כאשר ממוטב, שיטה זו יש בקרבת 100% DRG אינטגרציה ב-CAM. תוצאות מייצגות של אינטגרציה DRG מוצגים באיור 5A-B. השילוב של DRG ב-CAM חשוב מאז הוא מספק הכדאיות של רקמת DRG במהלך הניסוי. באופן מיקרוקטאני, DRG הוא ראה בתוך רקמת החיבור של CAM (H & E כתם). כלי הדם נראים לעתים קרובות בתוך רקמת DRG, מציע כי אספקת הדם פקה מטפחת הרקמה המושתלים. גידולים מושתלים מזוהים גם על ידי מצלמת H & E; בהתאם לכמות הפלישה הנוכחית, גידולים עשויים להופיע עם אף אחד איי הגידול רבים הפולשים רקמת החיבור (איור 5C-D). הדמות הייצוגית 5E-F מראה את מצלמת מצלמה שנאספה על דימות ברייטפילד הדמיה וזריחה ממוזג. UM-SCC-1 תאים המבטא Galanin קולטן 2 הציג פלישה מוגברת של DRG בהשוואה לתאי בקרה (איור 5G-H). האינטראקציה של סרטן-DRG נצפתה כתאים סרטניים המציגים פלישה כיוונית לכיוון DRG (איור 5H).
ניתוח נתונים מבוצע בדרכים שונות. הפלישה כיוונית של תאים סרטניים לכיוון DRG הוא נצפתה כמשתנה דיכוטומי ומספר ביצים המציגות דפוס זה של הפלישה נספר בכל קבוצה. הבדלים סטטיסטיים בין קבוצות מחושבים באמצעות בדיקה בינומית של פרופורציות. הקרבה בין תאים סרטניים DRG, ואזור הגידול נמדד באמצעות ImageJ6 והבדלים בין קבוצות מוערך באמצעות מבחן t של הסטודנט. כדי להבטיח דיוק בניתוח ImageJ, כל התמונות מאותו ניסוי צריכות להילקח על הגדרות אור וחשיפה שוות. לאחר התאמת סף התמונה ואת הבהירות של כל התמונות באמצעות אותם קריטריונים, הכלי לנתח חלקיקים משמש למדידת אזור הגידול והכלי מדידה ליניארי מודד מרחקים הגידול-DRG. חשוב להשתמש בכיוונון קבוע של גודל החלקיקים שנותחו עבור כל התמונות בין קבוצות שונות. במקרים מסוימים, גידולים לגדול עבה ניתן למדוד באופן ידני עם caliper דיגיטלי, המאפשר מדידת נפח.
באמצעות מקטעים של פרפין מוטבע רקמת מצלמת, H & E כתם או אימונוהיסטוכימיה עבור תאים אפיתל (נוגדן אנטי ציטוקרטין מגיב למין האנושי) ניתן לבצע, המאפשר הערכה של פלישה בתוך רקמת החיבור. הפלישה היא בכמת כמו מספר איי הגידול ברקמת החיבור לכל ביצה. Immunofluorescence עבור קולגן IV ניתן להשתמש כדי להדגיש את קרום המרתף. גם, אם שימוש בתאי סרטן המסומנים ב-GFP, זיהוי תאים אלה בסעיפים הרקמה הוא הקלה ללא אימונוהיסטוכימיה עבור ציטוקרטין. גרורות וניתוח אנגיוגנזה בניסויי קאם נדונים במקום אחר10,17.
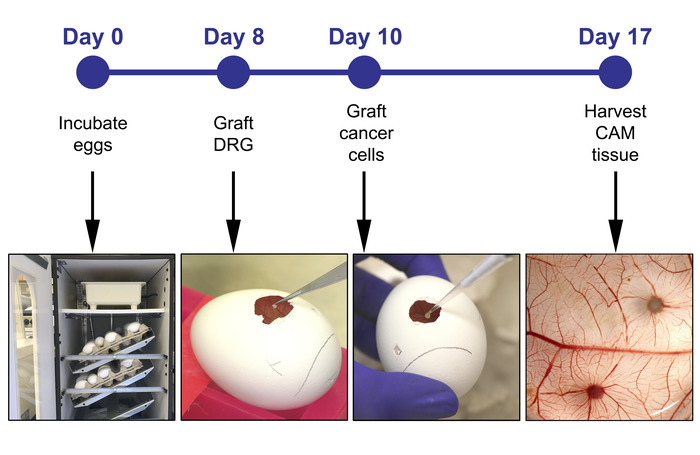
איור 1: הניסוי ציר הזמן כולל את השלבים העיקריים בימים 0, 8, 10 ו -17. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
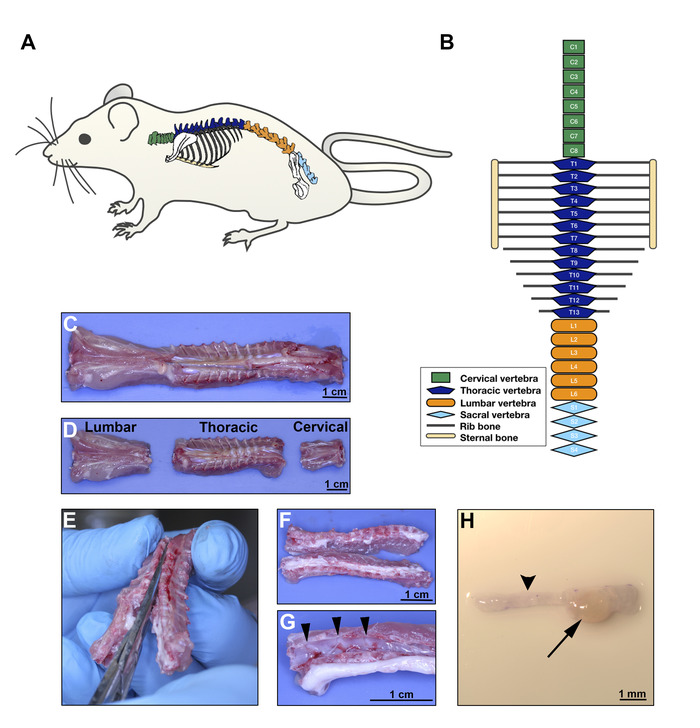
איור 2: חילוץ DRG ביום 8 . א. תרשים סכימטי הממחישות את המיקום האנטומי של עמוד השדרה. ב. דיאגרמת התצורה של חוליות החולדה המציגה אזורי גוף שונים; ירוק לצוואר הרחם, כחול כהה לחזה, כתום למותניים וכחול בהיר לחוליות סאקרל. C-D. ההיבט הגחוני של עמוד השדרה לאחר כריתה כירורגית; הפרדת האזורים כמודגם ב- B. ה. ניתוח החוליות כדי לפתוח את תעלת חוט השדרה, הפרדת הגופים החוליות לשני סעיפים צדדיים המכילים את drgs. סעיף צריך לחתוך את ההיבט הגייתי והגייתי של כל עצם החוליות באמצע הקו. ו. היבט גולמי של עמוד השדרה הפתוח של החזה. G. לאחר חוט השדרה הוא העקורים, drgs הם גלויים בקלות בתעלות החוליות (החצים מצביעים 3 drgs). H. Stereomicroscopic תמונה של drg אחד (חץ) עם חבילות אקסון המקביל (ראש החץ). סרגלי קנה מידה: C, D, F, ו- G, 1 ס מ; H, 1 מ"מ לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
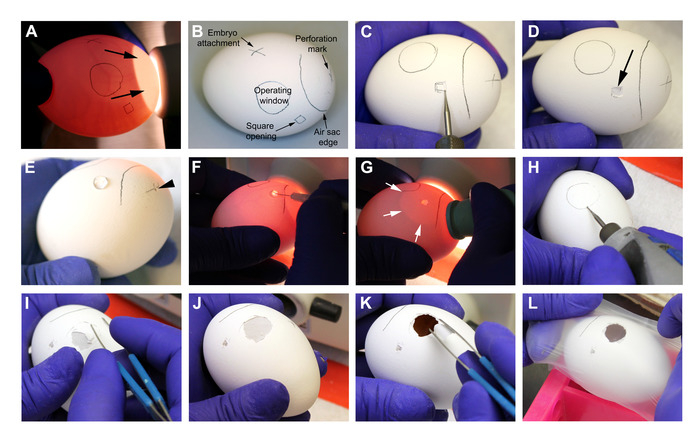
איור 3: הכנת הביצים ביום 8. א-ב. זיהוי של ביצית והסימנים לפני ההליך. חיצים על הנקודה. לגבי שק האוויר הטבעי C-D. קידוח ופתיחה של קליפת הביצה על סימון הפתיחה המרובע. חץ על D נקודות על קרום ביצה חיצונית ללא שינוי לאחר הסרת המעטפת בעזרת מלקחיים קהה. ה. הצלב המסומן על שק האוויר מחורר את המקדחה כדי לאפשר זרימת אוויר לתוך הביצה (ראש החץ). 30 μL של מדיום HBSS ממוקם על קרום קליפת הביצה החיצונית בפתח הכיכר. F. עם מחט מזרק קנס, קרום הביצה פגז החיצוני מחורר שבו HBSS הוצב בעבר. G. הלחץ מוחל על הנורה טפטפת גומי תוך הצמדת אותו חירור קדח על האוויר שק. כאשר הלחץ אצבע משוחרר, האוויר הוא שאבק, יצירת שק אוויר מלאכותי (חצים לבנים) כי צריך להאריך לחלון ההפעלה. ח. הקצוות של חלון ההפעלה מקדעות בתנוחה כמעט מקבילה למעטפת הביצה, כדי למנוע ניקוב מקרי. . איי. ג'יי הסרת קליפת הביצה עם מלקחיים בוטים. K. להסיר את קרום פגז ביצה חיצונית עם מלקחיים קהה, להיות זהירים לא להחדיר חלקיקים על CAM (נצפתה ב ̴1 ס מ מתחת לפני השטח). L. ביצים מכוסים באופן זמני עם קרום שעווה פרפין ולשים חזרה בחממה. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
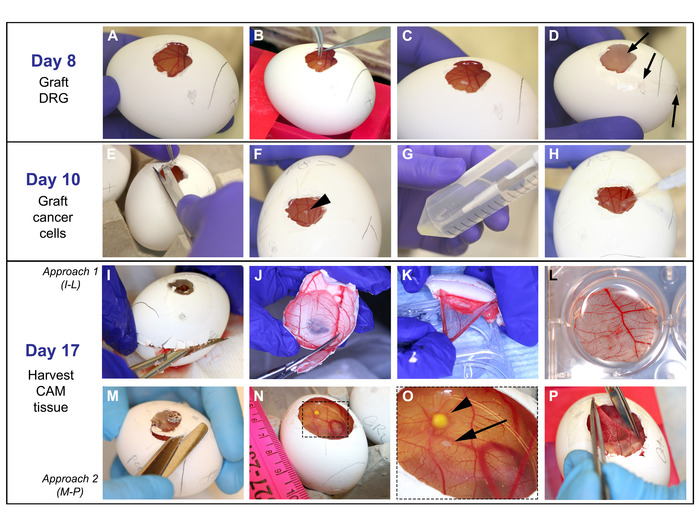
איור 4: השתלה של DRG, תאים, וקציר של קאם: ביום 8: A. קאם נצפתה בקלות לאחר הסרת פרפין קרום השעווה. . בי. סי עם מלקחיים עדינים, DRG ממוקם על CAM. ד. ביצה מכוסה ברוטב הסרט ומכניסים לחממה; חצים מצביעים על הפתחים המכוסים. ביום 10: E-F. ההלבשה הסרט מוסרת ו DRG ממוקם (חץ ראש על F). G-H. 5 μL של פתרון התא הוא ירד על מצלמת במרחק של ~ 2 מ"מ מ DRG. ביום 17: I-L ו -M-P להדגים שתי גישות שונות המשמשים למסוק את CAM. I. מעטפת ביצה נפתח עם מספריים קנס החל על שק האוויר קדח מחורר עד המחצית העליונה של הביצה מוסרת. J. ביצה פגז המכיל את מצלמת הוא מופחת בגודל של כ 3 ס"מ. K-L. עם מלקחיים עדינים, קאם מנותקת מקליפת הביצה וממוקמת בתוך ההמעטה. . אנימבין הרחבת חלון ההפעלה מבוצעת כדי להמחיש את התאים DRG ו סרטן על מצלמת. ראש החץ מצביע על הגידול חץ מצביע על DRG. P. THE מצלמת הוא נתפס עם מלקחיים עדינים, לגזור עם מספריים חדה, והניח בתוך כלפי מראה ב L. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
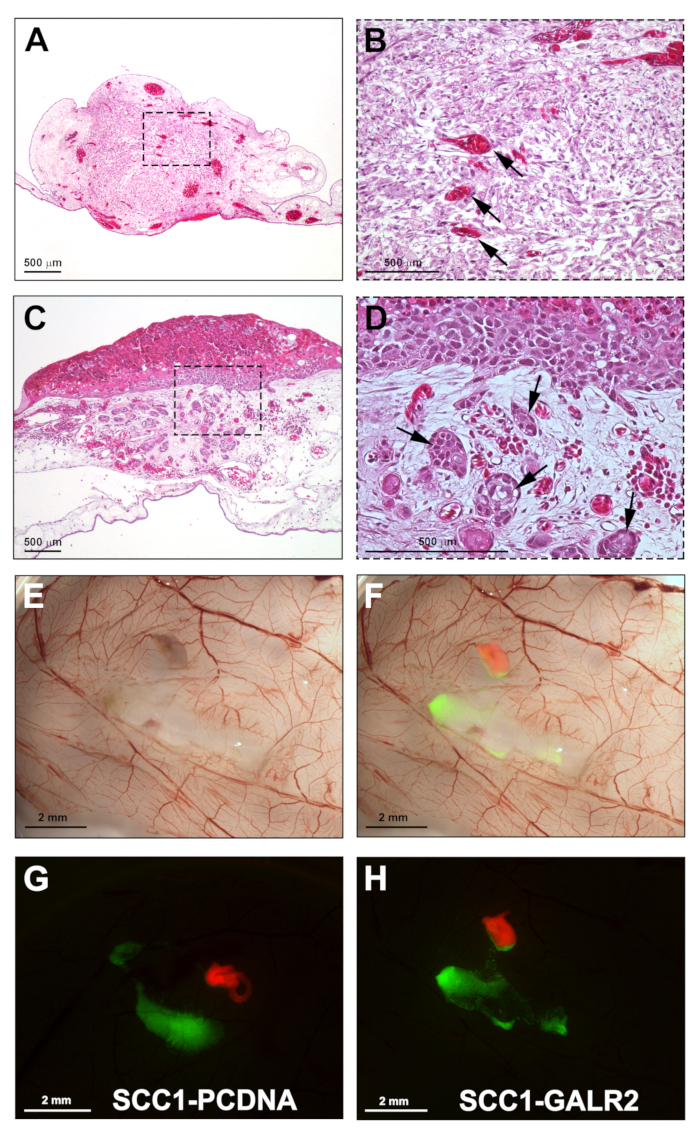
איור 5: תוצאות מייצגות. במקטע A. H &Amp; E המציג שילוב של DRG ב-CAM. ב. הגדלה גבוהה יותר של A; חיצים להראות מצלמת כלי הדם של DRG. C. UM-scc-1 תאים הושתל על מצלמת וקצרו ארבעה ימים לאחר השתלה (H & E כתם). ד. הגדלה גבוהה יותר של C מציג איי גידול פולשנית ברקמת החיבור של CAM (חיצים). E. stereomicroscopic התמונה של מצלמת הGALR2 המושתלים עם UM-scc-1-תאים ועכבר drg, שנקטפו ביום 17. F. ממוזג ותמונות ברייטפילד הדגשת ה-drg המסומן בתאים אדומים וסרטניים המסומנים בירוק. G-H. Stereomicroscopy פלואורסצנטית של מצלמת מצוידים DRG ו-UM-SCC-1-GALR2 לעומת תאים בקרה, הממחישות הפלישה של אום-SCC-1-GALR2 תאים DRG (H). סרגלי קנה מידה: A-D, 500 μm; E-H, 2 ממ. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
| צעד | עיה | סיבה | פתרון | ||||||
| 3.2.1 | אין אפשרות לזהות את הקובץ המצורף לעובר. | קשה לראות את תנוחת ההחזקה בזמן שהביצה עדיין ממשיכה. | לסובב את הביצה במהירות הצידה כדי להיות מסוגל לראות כלי ארוך מוצמד קרום הביצה. | ||||||
| 3.3 & 3.8 | חירור של קרום קליפת הביצה החיצונית בזמן הקידוח. | . מיקום לא נכון של התרגיל | הצב את התרגיל כמעט במקביל למעטפת הביצה בזמן הקידוח. אם הממברנה מנוקב בשלב 3.3, אין צורך לבצע חירור נוסף עם מחט כאמור בשלב 3.5. . אם הדימום יתרחש, מחק את הביצה | ||||||
| 4.3 | . DRG נדבק למלקחיים | DRG יבש. | DRG רטוב שוב ב HBSS ו/או להשתמש מחט קנס כדי לעזור לנתק DRG מ מלקחיים. | ||||||
| 5.2 | תאים אינם מתויגים באופן מושלם עם צבע פלורסנט. | . זמן דגירה תאים מסוימים דורשים יותר זמן לתווית. | שמור על תאים למשך שעה נוספת במדיה עם צבע פלורסנט. | ||||||
| 5.6 | . בועת אוויר על טיפת התאים | משתמש בכל הנוזלים. בקצה הפיפטה | טען 1μL יותר מאמצעי האחסון הרצוי ואל תשתמש ב-μL הסופי של הפיפטה בעת השתלת תאים. זה ימנע בועות האוויר בתערובת התאים. | ||||||
| 6.3 | אין אפשרות לזהות את התאים DRG או לאחר איסוף המצלמה. | קטן DRG, DRG יש נעקרו, תאים סרטניים להתפשט. | אם DRG לא נראה, הקציר שטח גדול יותר של מצלמת ומקום לתוך מיכל גדול יותר עבור קיבעון. בדוק DRG ומיקום התא תחת הזריחה במיקרוסקופ סטריאו, ולאחר מכן לקצץ את מצלמת בגודל קטן יותר עבור הטבעה פרפין. | ||||||
טבלה 1: הטבלה ' פתרון בעיות '
The CAM-DRG ב vivo מודל הציג כאן כתובות החסרונות של הדגמים הקודמים על ידי הוכחת אינטראקציה של גידול עצבי לפני פלישה פיזית של העצב על ידי תאים סרטניים. רוב במחקרים vivo של pni להתמקד על התפשטות הגידול ועיכוב של תפקוד המנוע, תלוי בהזרקה ישירה של תאים סרטניים לתוך עצבי הירך23,24,25. הזרקת העצב הסימתי הוא מודל vivo של PNI שבו תאים סרטניים מוזרק לתוך עכבר או עצב מגיד עכברוש שבו הגידול לאחר מכן גדל. מודלים הזרקה שימושיים כדי להציג התקדמות הגידול הרסני כאב וכתוצאה מתאי הגידול בתוך העצבים. המודל העצבי מתאים גם למחקר של גורמים המאפשרים תאים סרטניים לשגשג בעצב אבל חסר את היכולת להעריך את השלב המוקדם של PNI, כי הוא מציג תאים ישירות לתוך העצב, לעקוף נרתיקים עצביים. בגישה שונה, מושתל בניתוח שתלי הגידול אורתוטופית שימשו כדי לאפיין את החשיבות של אדררורגיות וסיבי עצב cholinergic בקידום התקדמות סרטן הערמונית, ובכך מציע תפקיד בולט של עצבים התקדמות הגידול 26. מודל זה כללה אבלציה כימית של עצבים מורקיים ומעורר חמלה פאראסימפתטית. הסיבים הפאראסימפתטית חדרו לרקמות הגידול, תהליך הקשור PNI, אבל המודל לא היה משמש במיוחד כדי להעריך את האינטראקציות הפיזיות בין העצב לבין הגידול. מודל CAM-DRG מאפשר חקירה של אינטראקציות בין העצב והסרטן במהלך PNI. יתר על כן, מודלים murine הם יקרים וגוזלת זמן בהשוואה למודל CAM. אנו ממליצים להשתמש בדגם CAM-DRG למחקרים מכניסטיים של PNI.
כמה יתרונות לגישה CAM-DRG כוללים הערכה של PNI ופנוטיפים אחרים, כגון גידול גידול, גרורות, ואנגיוגנזה. זיהוי של ה-DNA האנושי על מצלמת התחתון ו/או בכבד יכול לשמש לאיתור גרורות של שורות התאים של סרטן האדם10, גישה ניסיונית יותר רגיש בהשוואה לסקר רקמות וכתמים, אשר עשוי לא לחשוף גרורות קטנות.
לשיטת CAM-DRG יש מספר מגבלות, כולל מסגרת זמן התבוננות קצרה. המערכת החיסונית של העובר הוא פעיל מבחינה פיזיולוגית על ידי יום 1827, כאשר דחייה ותהליך דלקתי עשוי להתרחש, הגבלת זמן ניסיוני. חשוב גם לשקול את המרחק כאשר השתלת תאים סרטניים קרוב DRG; מרחקים גדולים יותר DRG-cancer עלול לפגוע באינטראקציות המולקולריות בין תאי הגידול והעצב, או יכול לעכב את המגע הפיזי בין שני המרכיבים של המודל. כמו כן, אם העוברים ישנים יותר מאשר האמור בפרוטוקול זה, תנועות העובר עלול לתפוס את תאי הגידול. לכן, חשוב להשתמש בביצים עקבית עם יום 10 לאחר הפריה עבור השתלת תאים.
מאז המערכת החיסונית אינה מפותחת לגמרי לפני יום 1827, הסביבה מיקרוסביבתית של מצלמת דומה לזה של מודלים מורקיים החיסוני משמש לעתים קרובות ללימודי סרטן. לכן, מודל זה אינו שימושי כדי להעריך את התפקיד של תאים חיסוניים בהתקדמות הגידול. מגבלה נוספת היא הזמינות המוגבלת של ריאגנטים למיני עוף, כגון נוגדנים, ציטוקינים וצבעי יסוד.
ביצוע מדויק של פרוטוקול זה דורש תרגול; עם זאת, זה יכול להיעשות על ידי חבר מעבדה ללא צורך במתקן הליבה המקצועית. קידוח מעטפת הביצית דורש הכשרה. מומלץ להתאמן על ביצי מכולת (לא מופרות) לפני שמנסים לבצע מודל זה בפעם הראשונה. הישרדות עובריים גבוהה והצלחה של המודל יכול להיות מושגת אם כמה צעדים קריטיים כדי למנוע זיהום מלווה: מניעה אנטיביוטי מתאים של DRGs ב 2% עט/דלקת, עובד בארון הזרם למינארי, והימנעות הפיזור של חלקיקים פגז ביצה על המצלמה. זה גם חיוני כדי לשמור על לחות יציבה במהלך הזמן דגירה הביצית הכוללת. אנו ממליצים להגדיל את מספר הביצים לכל קבוצה עד שתהיה שליטה בטכניקה. הבעיות השכיחות ביותר עבור אנשי מעבדה לא מנוסים הם זיהום ביצים טכניקה מדויקת עבור השתלת תאים.
קציר DRG גם דורש הכשרה; מומלץ לאסוף DRGs לניסויים בתחום החוץ הגופית8 לפני שמנסים לvivo במודל. תרבות DRG מתורבת היא הזדמנות למטב את התנאים ולשפר את הטכניקה כדי לקצר את משך החילוץ DRG. תשומת לב מיוחדת לאסוף טכניקה נדרשת כאשר אוחז את DRG עם מלקחיים. אין להחזיק את ה-DRG ישירות; לחץ צריך להיות מיושם מתחתיו. אנו ממליצים להשתמש בעדשת מגדלת כדי להמחיש טוב יותר את DRG במהלך החילוץ.
חשוב מכך, בעת ביצוע מודל זה בפעם הראשונה, כל התנאים צריכים להיות ממוטבים עבור קו התא הרצוי. מודל זה היה אופטימיזציה עבור עכברוש DRG ו קו HNC תא UM-SCC-1. השימוש בעכבר DRG וסוגים אחרים של תאים סרטניים עשויים לדרוש אופטימיזציה. עם ריכוז גבוה יותר של תאים מושתלים, גידולים נוטים לצמוח עבה יותר stiffer, אשר מקלה על מדידות הגידול. התחשבות בביצים מרובות עבור כל קבוצה וריכוז מתאים של תאים עבור כל ביצה, כמה מיליוני תאים עשויים להידרש עבור כל ניסוי. כדי להקל על תכנון, הידע של זמן ההכפלה של התאים יש לקחת בחשבון. עבור חלק מהשלבים הקריטיים בפרוטוקול זה, מסופקת טבלת פתרון בעיות (טבלה 1).
המחברים לא מצהירים על אינטרסים מתחרים.
עבודה זו נתמכת על ידי NIH/נדבך מענקים DE027551 ו-DE022567 (NJD).
| Name | Company | Catalog Number | Comments |
| 0.25% Trypsin-EDTA (1x) | Gibco | # 25200-056 | |
| ACE light source | SCHOTT North America, Inc. | Used to transilluminate the eggs | |
| CellTracker Green CMFDA fluorescent dye | Life Technologies | # C7025 | Reconstitute 50µg in 20µL of DMSO and stock at -20oC. Use 1µL of stock solution/mL of culture medium. |
| CellTracker Red CMTPX fluorescent dye | Life Technologies | # C34552 | Reconstitute 50µg in 40µL of DMSO and stock at -20oC. Use 1µL of stock solution/mL of culture medium |
| Cordless rotary tool | DREMEL | # 866 | Used to drill the egg shell |
| DMEM (1x) | Gibco | # 11965-092 | Dulbeecco`s Modified Eagle Medium |
| DMSO | Fisher Bioreagents | # BP231-100 | Dimethyl Sulfoxide |
| Dumont # 5 fine forceps | Fine Science Tools (FST) | # 11254-20 | Used to harvest DRG |
| Egg incubator | GQF Digital Sportsman | # 1502 | Egg incubator equipped with automatic rotator, digital thermostat, temperature and humidity controls |
| Engraving cutter | DREMEL | # 108 | Used to drill the egg shell |
| Extra fine Graefe forceps, curved | Fine Science Tools (FST) | # 11151-10 | Used to graft DRG onto the CAM on day 8 and to harvest CAM tissue on day 17 |
| Extra fine Graefe forceps, straight | Fine Science Tools (FST) | # 11150-10 | Used to graft DRG onto the CAM on day 8 and to harvest CAM tissue on day 17 |
| Fertilized Lohmann White Leghorn eggs | Fertilized eggs at early fertilization days, preferably on first day post-fertilization. Eggs used in this protocol are from Michigan State University Poultry Farm. | ||
| Filter Forceps | EMD Millipore | # XX6200006P | Blunt forceps used to remove the egg shell |
| Fine surgical straight sharp scissor | Fine Science Tools (FST) | #14060-09 | Used to harvest the CAM tissue on day 17 |
| HBSS (1x) | Gibco | # 14025-092 | Hank`s Balanced Salt Solution |
| HI FBS | Gibco | # 10082-147 | Heat-inactivated Fetal Bovine Serum |
| Paraffin wax membrane | Parafilm laboratory film | # PM-996 | Used to temporarily cover the egg openings until DRG grafting on day 8 |
| PBS (1x) pH 7.4 | Gibco | # 10010-023 | Phosphate Buffered Saline |
| Pen/Strep | Gibco | # 15140-122 | 10,000 Units/mL Penicilin, 10,000 µg/mL Streptomycin |
| PFA (paraformaldehyde solution) | Sigma-Aldrich | # P6148-1KG | Dilute in water to make a 4% PFA solution |
| Sprague Dawley rats (females) | Charles River laboratories | Strain code: 001 | 6-7 weeks old (190-210g in weight) |
| Tegaderm Transparent Film Dressing | 3M | # 9505W | Sterile, 6x7cm, used to cover the egg openings during incubation |
- Schmitd, L. B., Scanlon, C. S., D'Silva, N. J. Perineural Invasion in Head and Neck Cancer. Journal of dental research. 97 (7), 742-750 (2018).
- Liebig, C., Ayala, G., Wilks, J. A., Berger, D. H., Albo, D. Perineural invasion in cancer: a review of the literature. Cancer. 115 (15), 3379-3391 (2009).
- Schmitd, L. B., et al. Redefining Perineural Invasion: Integration of Biology With Clinical Outcome. Neoplasia (New York, N.Y). 20 (7), 657-667 (2018).
- Chinn, S. B., et al. Impact of perineural invasion in the pathologically N0 neck in oral cavity squamous cell carcinoma. Otolaryngology--head and neck surgery : official journal of American Academy of Otolaryngology-Head and Neck Surgery. 149 (6), 893-899 (2013).
- Tai, S. K., Li, W. Y., Yang, M. H., Chu, P. Y., Wang, Y. F. Perineural invasion in T1 oral squamous cell carcinoma indicates the need for aggressive elective neck dissection. The American journal of surgical pathology. 37 (8), 1164-1172 (2013).
- Scanlon, C. S., et al. Galanin modulates the neural niche to favour perineural invasion in head and neck cancer. Nature communications. 6, 6885 (2015).
- Amit, M., et al. Upregulation of RET induces perineurial invasion of pancreatic adenocarcinoma. Oncogene. 36 (23), 3232-3239 (2017).
- Huyett, P., Gilbert, M., Liu, L., Ferris, R. L., Kim, S. A Model for Perineural Invasion in Head and Neck Squamous Cell Carcinoma. Journal of visualized experiments : JoVE. (119), (2017).
- Ayala, G. E., et al. In vitro dorsal root ganglia and human prostate cell line interaction: redefining perineural invasion in prostate cancer. The Prostate. 49 (3), 213-223 (2001).
- Liu, M., et al. The Histone Methyltransferase EZH2 Mediates Tumor Progression on the Chick Chorioallantoic Membrane Assay, a Novel Model of Head and Neck Squamous Cell Carcinoma. Translational oncology. 6 (3), 273-281 (2013).
- Busch, C., Krochmann, J., Drews, U. The chick embryo as an experimental system for melanoma cell invasion. PloS one. 8 (1), e53970 (2013).
- Li, M., et al. The In Ovo Chick Chorioallantoic Membrane (CAM) Assay as an Efficient Xenograft Model of Hepatocellular Carcinoma. Journal of visualized experiments : JoVE. (104), (2015).
- Ota, I., Li, X. Y., Hu, Y., Weiss, S. J. Induction of a MT1-MMP and MT2-MMP-dependent basement membrane transmigration program in cancer cells by Snail1. Proceedings of the National Academy of Sciences of the United States of America. 106 (48), 20318-20323 (2009).
- Murphy, J. B. TRANSPLANTABILITY OF TISSUES TO THE EMBRYO OF FOREIGN SPECIES : ITS BEARING ON QUESTIONS OF TISSUE SPECIFICITY AND TUMOR IMMUNITY. The Journal of experimental medicine. 17 (4), 482-493 (1913).
- Ribatti, D., Nico, B., Vacca, A., Presta, M. The gelatin sponge-chorioallantoic membrane assay. Nature. 1 (1), 85-91 (2006).
- Auerbach, R., Arensman, R., Kubai, L., Folkman, J. Tumor-induced angiogenesis: lack of inhibition by irradiation. International journal of cancer. 15 (2), 241-245 (1975).
- Banerjee, R., et al. The G protein-coupled receptor GALR2 promotes angiogenesis in head and neck cancer. Molecular cancer therapeutics. 13 (5), 1323-1333 (2014).
- Ossowski, L., Reich, E. Experimental model for quantitative study of metastasis. Cancer research. 40 (7), 2300-2309 (1980).
- Nowak-Sliwinska, P., Segura, T., Iruela-Arispe, M. L. The chicken chorioallantoic membrane model in biology, medicine and bioengineering. Angiogenesis. 17 (4), 779-804 (2014).
- Moreno-Jimenez, I., et al. The chorioallantoic membrane (CAM) assay for the study of human bone regeneration: a refinement animal model for tissue engineering. Scientific reports. 6, 32168 (2016).
- Vu, B. T., et al. Chick chorioallantoic membrane assay as an in vivo model to study the effect of nanoparticle-based anticancer drugs in ovarian cancer. Scientific reports. 8 (1), 8524 (2018).
- Sleigh, J. N., Weir, G. A., Schiavo, G. A simple, step-by-step dissection protocol for the rapid isolation of mouse dorsal root ganglia. BMC research notes. 9, 82 (2016).
- Cavel, O., et al. Endoneurial macrophages induce perineural invasion of pancreatic cancer cells by secretion of GDNF and activation of RET tyrosine kinase receptor. Cancer research. 72 (22), 5733-5743 (2012).
- Guo, K., et al. Interaction of the sympathetic nerve with pancreatic cancer cells promotes perineural invasion through the activation of STAT3 signaling. Molecular cancer therapeutics. 12 (3), 264-273 (2013).
- Deborde, S., et al. An In Vivo Murine Sciatic Nerve Model of Perineural Invasion. Journal of visualized experiments : JoVE. (134), (2018).
- Magnon, C., et al. . Autonomic nerve development contributes to prostate cancer progression. 341 (6142), 1236361 (2013).
- Ribatti, D. Chick embryo chorioallantoic membrane as a useful tool to study angiogenesis. International review of cell and molecular biology. 270, 181-224 (2008).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved