Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Medicine
Чик Chorioallantoic Membrane In Vivo Модель для оценки perineural вторжение в голову и шею рака
Периневрального вторжения является агрессивным фенотипом для головы и шеи плоскоклеточной карциномы и других опухолей. Модель хориоаллантоической мембраны была использована для изучения ангиогенеза, рака и метастазов. Здесь мы демонстрируем, как эта модель может быть использована для оценки периневрального вторжения in vivo.
Периневрневенное вторжение является фенотипом, в котором рак окружает или вторгается в нервы. Это связано с плохим клиническим исходом для головы и шеи плоскоклеточной карциномы и других видов рака. Механистические исследования показали, что молекулярный перекрестный разговор между нервами и опухолевыми клетками происходит до физического взаимодействия. Есть только несколько моделей in vivo для изучения периневрального вторжения, особенно для исследования раннего прогрессирования, прежде чем физические нервные опухоли взаимодействия происходят. Модель хориоаллантоической мембраны была использована для изучения вторжения рака, потому что мембрана в подвале хорионического эпителия имитирует эпитилию человека. Здесь мы перепрофилировали цыпленок chorioallantoic мембранной модели для расследования периневрального вторжения, прививки крыс ывата корневой ганглии и головы человека и шеи плоскоклеточной клетки карциномы на хорионический эпителий. Мы продемонстрировали, как эта модель может быть полезна для оценки способности раковых клеток вторгаться в нервную ткань in vivo.
Периневрального вторжения (PNI) является недостаточно изученным фенотипом при раке, который связан с высокой рецидивом заболевания и плохой выживаемостью у пациентов с плоскоклеточной карциномой головы и шеи (HNC)1. PNI определяется микроскопически как опухолевые клетки внутри или вокруг нервов2,3. Когда PNI обнаружен, пациенты, скорее всего, получить адъювантной терапии, такие как факультативное вскрытие шеи и / или лучевой терапии4,5. Тем не менее, эти методы лечения являются агрессивными, а не PNI-специфических. В самом деле, нет терапии, чтобы блокировать PNI, в первую очередь потому, что механизмы, лежащие в основе нервно-опухолевых взаимодействий по-прежнему плохо изучены.
Различные молекулярные механизмы были вовлечены в нервно-опухолевого притяжения; опухоли и стромальные клетки релиз нейропептидов и факторов роста для содействия неуритогенез6,7. При культивировании вместе in vitro, клетки HNC и дорсальные корневые ганглии (DRG) оба имеют надежный ответ; влияние на вторжение опухолевых клеток и неуритогенез можно увидеть через несколько дней в культуре6,8,9. Тем не менее, существует отсутствие соответствующих моделей in vivo для повторения взаимодействия опухоли и нерва до вторжения. Здесь мы представляем in vivo PNI модель для изучения ранних взаимодействий между клетками HNC и нервами6. Мы адаптировали модель хориоаллантоической мембраны (CAM), чтобы включить нейронный компонент, прививку DRG в CAM, а затем трансплантат раковых клеток, чтобы имитировать иннерватированную микросреду опухоли.
Модель CAM была успешно использована для оценки вторжения клеток через мембрану подвала, имитируя ранние инвазивные стадии карциномы и меланомы10,11,12. CAM состоит из верхнего хорионического эпителия, вмешиваясь мезенхим, и нижней аллантоической эпителия. Хорионический эпителий структурно похож на человеческий эпителий10,13 в том, что коллаген-IV богатых подвале мембраны имитирует подвал мембраны, которая отделяет устные эпителия от основной соединительной ткани. Так как первые опухолевые трансплантаты были выполнены в CAM в 191314, многие адаптации метода были разработаны, чтобы позволить для оценки ангиогенеза15,16,17, прогрессирование опухоли, и метастаз18. Важно отметить, что техника прививки опухолей на CAM изменилась очень мало, но приложения постоянно развиваются. Анализы растущей сложности были опубликованы, в том числе скрининг аткан19, костной ткани инженерных20, и наночастицы на основе противораковых препаратов21.
Наша лаборатория использует модель CAM-DRG, в которой млекопитающее DRG изолировано и привито на поверхности верхнего CAM. После того, как DRG становится включенвв в CAM, клетки HNC прививаются вблизи DRG и позволяют взаимодействовать с DRG до того, как вся система in vivo будет собрана и проанализирована. Важно отметить, что система позволяет ex-vivo визуальное наблюдение как DRG и опухоли флуоресценции маркировки DRG и опухолевых клеток. Этот протокол включает в себя несколько шагов с различными уровнями сложности выполняется в течение 17 дней, от инкубации яиц для сбора CAM (Рисунок 1). Клетки, выражающие различные белки, представляющие интерес, могут быть протестированы в этой модели, чтобы выяснить молекулярные пути, ответственные за вторжение нерва в рак, а также для скрининга препаратов непосредственно целевой нейронной вторжения. Клетки предварительно обработанные с наркотиком кандидата могут быть привиты на CAM и появление PNI исследовали по сравнению с необработанным контроля. В самом деле, модель CAM была использована для скрининга наркотиков в качестве промежуточного шага между in vitro исследований и доклинических испытаний in vivo у грызунов19.
Экспериментальная конструкция будет варьироваться в зависимости от гипотезы. Например, при тестировании роли конкретного белка на ПНИ, экспериментальная группа будет включать DRG привитых с опухолевыми клетками, перевыражающими белок, в то время как контрольная группа должна включать DRG с клетками, стабилизированными пустым вектором. Для решения конкретных вопросов можно использовать несколько различных экспериментальных проектов.
Заявление об этике: Все эксперименты с использованием крыс в этом протоколе проводятся в соответствии с правилами IACUC (Институциональный комитет по уходу за животными и использованию) нашего учреждения. Эксперименты с яйцами в этом исследовании освобождаются от регулирования IACUC.
1. Инкубация яйцеклеток (оценочное время: 5 мин, ноль дня)
- Получить без патогена оплодотворенные коммерческие яйца Lohmann Белый Leghorn, предпочтительно в первый день после оплодотворения. Инкубировать шесть яиц на экспериментальную группу в яйцеук увлажняющий инкубатор при 38 градусах Цельсия и 54% влажности в течение 8 дней с почасовым вращением. Используйте регулярное вращение яйцеклеток, чтобы предотвратить прилипание эмбриона к яйцеклеткам.
ПРИМЕЧАНИЕ: Перед инкубации, держать яйца в холодильнике 18 градусов по Цельсию, чтобы остановить развитие эмбриона в течение максимум 1 недели.
2. Урожай и подготовка DRGs (оценочное время: 2 ч, день 8)
ПРИМЕЧАНИЕ: Эксперименты с мышами и крысами требуют одобрения со стороны (IACUC). В некоторых странах использование куриных яиц также требует одобрения.
- Получить шесть-семь недельных Крыс Sprague Dawley (200 г в весе) для извлечения DRGs.
ПРИМЕЧАНИЕ: Одна крыса должна дать 40 цервикальных и грудных DRGs. Мышь DRG также интегрируется в CAM, однако условия для этого вида должны быть оптимизированы самостоятельно. - В ламинарном шкафу потока, урожай DRGs из шейки матки и грудной области после протокола для мыши DRG извлечения опубликованы в другом месте22. Следуйте на рисунке 2 для ориентации на то, как собирать DRGs.
- Эвтанизировать крысу путем прокола сердца после введения кетамина/ ксилазина вводят интраперитоне. Очистите крысиную кожу с 70% этанола и удалить позвоночник крысы с помощью ножниц. Не выполняйте вывих шейки матки, потому что это повредит ШЕЙки матки DRGs.
- Отделите цервикальные, грудные и поясничные области теми же ножницами, следуя схематичному анатомическому представлению и грубым изображениям, представленным на рисунке 2A-D. Поместите секции позвоночника в 10 см культуры блюдо с 1x PBS держать ткани мокрые.
- С тонкими ножницами кости, открыть позвоночных костей в области позвоночника и вентрал аспекты, отделяя позвоночник в двух боковых половинок(рисунок 2E-F). Поместите секции тканей в чистую 10 см блюдо со свежим1x PBS.
- Используя щипцы, осторожно отсоедините спинной мозг от костей позвонка, чтобы визуализировать DRGs(рисунок 2G).
- С тонкими щипцы провел под каждым DRG, схватить его и вытащить его из полости кости, в которой он подал. Не держите DRG непосредственно, потому что это приведет к повреждению тканей. Не обрезайте аксонные пучки от DRG(рисунок 2H).
ПРИМЕЧАНИЕ: Избегайте использования поясничных DRGs, поскольку они сократили интеграцию в CAM. Для расположения региона DRG следуйте схематической иллюстрации и грубым анатомическим изображениям на рисунке 2A-D.
- Сразу же после сбора урожая, поместите каждый DRG в DMEM культуры среды дополнены 2% пенициллина / стрептомицина (Pen/Strep) и 10% тепло-инактивированных фетальной сыворотки крупного рогатого скота (FBS), чтобы помочь предотвратить бактериальное загрязнение DRGs. Группа всех DRGs в том же 6 см культурное блюдо с 4 мл культуры среды.
- После сбора урожая всех DRGs, передать их в новую культуру блюдо с DMEM культуры среды дополнены 2% Перо / Strep плюс 10% FBS и содержащие 1,25 мкг /мл красного флуоресцентного красителя. Инкубировать 1 ч в инкубаторе клеточной культуры. В течение этого времени, подготовить яйца, чтобы получить DRG, как описано ниже (шаг 3).
ПРИМЕЧАНИЕ: Интервал между сбором DRGs и завершением флуоресценции маркировки должно быть достаточно, чтобы подготовить яйца; DRGs можно хранить в течение нескольких часов в инкубаторе.
3. Приготовление яиц для прививки DRG (оценочное время: 1 ч для десятка яиц, день 8)
- В ламинарной шкафки потока, тусклый свет и transilluminate яйца, чтобы проверить на жизнеспособность и эмбриональной фазы. Исключить яйца с плохой сосуды, неоплодотворенные яйца или яйца, не соответствующие 8-му дню после оплодотворения. Держите яйцо осторожно с естественным воздушным мешком к источнику света(рисунок 3A).
- Карандашом отметьте яичную скорлупу, чтобы получить отверстия(рисунок 3A-B).
- Во-первых, определить привязанность развивающегося эмбриона к CAM как темный движущийся сосуд, прикрепленный к яйцеклетке мембраны и пометить эту область, чтобы избежать вмешательства в этой области.
- Во-вторых, выберите область операционного окна в качестве хорошо васкуляризированной области не менее 2 см от крепления эмбриона и нарисуйте круг диаметром 1,5 см. Примерно 1 см от операционного окна, рисовать 0,5 см квадрат в менее васкуляризованной области.
- В-третьих, нарисуйте область воздушного мешка, чтобы исключить его из зоны операции. Отметьте середину воздушного мешка крестом.
- С роторным инструментом и гравюры дрель, 3 мм в диаметре, просверлить яичную скорлупу в отмеченном квадрате(рисунок 3C). Используйте тупые щипки, чтобы удалить яичную скорлупу, не снимая наружную мембрану яичной скорлупы (белая мембрана прямо под оболочкой) (Рисунок 3D). Работайте тщательно, чтобы избежать случайной перфорации этой мембраны.
- Используя ту же дрель, что и в шаге 3.3, сделайте точечную перфорацию в отмеченном кресте в области воздушного мешка, чтобы позволить поток воздуха в яйцо(рисунок 3E). Будьте осторожны, чтобы не применять слишком много давления на яйцо, чтобы избежать нарушения или повреждения его.
- Поместите 30 кЛ HBSS в квадратное отверстие, над нетронутой внешней мембраной яичной скорлупы(рисунок 3E). С 30-G шприц иглы, сделать точечную перфорацию во внешней мембране в этой квадратной области(рисунок 3F).
- Поместите яйцо в источник света, чтобы визуализировать воздушный мешок. Нанесите давление на резиновую лампу eyedropper и поместите его в небольшую перфорацию, сделанную в области воздушного мешка (шаг 3.4). Отпустите давление в луковице, пока не увидите разделение двух мембран в области операционного окна(рисунок3G); повторить этот шаг столько раз, сколько вам нужно для достижения полного разделения мембран в области операционного окна.
- Повторите шаги 3.1-3.6 для всех яиц.
- Используя ту же дрель, что и в шаге 3.3, просверлите круглое операционное окно, стараясь не разрывать наружную мембрану яичной скорлупы(рисунок 3H). Очистите поверхность яйца, аккуратно наклеив клейлентую ленту, чтобы удалить все свободные частицы.
- С тупыми щипками, удалить яичную скорлупу из пробуренной области(рисунок 3I-J). Далее, с теми же щипцы, удалить наружную мембрану яичной скорлупы(Рисунок 3K), стараясь не вводить мелкие частицы оболочки внутри яйца, чтобы свести к минимуму загрязнение.
- Определите CAM примерно на глубине 1 см от поверхности яйца. Обложка каждого открыл яйцо временно с парафином восковой мембраны, чтобы избежать загрязнения(Рисунок 3L).
- Повторите шаги 3.8-3.10 для всех яиц. Поместите яйца обратно в яйцо инкубатор без вращения до DRGs готовы к прививке.
4. Прививка DRG на CAM (оценочное время: 40 мин, день 8)
- Приготовьте блюдо культуры 6 см со средой HBSS, чтобы вымыть DRGs перед имплантацией. Принесите подготовленные яйца в ламинарную камеру культуры клеток. Удалите парафиновую мембрану из яйцеклетки(рисунок 4A).
- С тонкими стерильными щипками, аккуратно схватить один DRG изнутри культуры среды. Окуните его в среду HBSS, чтобы удалить избыток среды, которая содержит флуоресцентный краситель. Держите DRG очень осторожно; в противном случае, он будет придерживаться щипки.
- Поместите DRG на CAM, стараясь не проколоть мембрану(рисунок 4B-C). При необходимости используйте другую пару щипцы, чтобы помочь отделить DRG от кончика щипцы при размещении его на CAM.
ПРИМЕЧАНИЕ: Сохранение DRG мокрой с HBSS среды также облегчит отрыв от щипцы. - Накройте яйцо стерильной прозрачной пленкой. Обложка все окна и проколы, сделанные в яичной скорлупе, чтобы избежать бактериального загрязнения(Рисунок 4D).
- После прививки DRGs во всех яйцах, инкубировать яйца в увлажняющий инкубатор при 38 градусах Цельсия и 54% влажности в течение 2 дней, без вращения.
5. Прививка опухолевых клеток на CAM (оценочное время: 1 ч 30 мин, день 10)
- На 48 h перед прививкой клеток, пластины клетки, необходимые в культуре пластин. Рассчитайте от 0,5 до 1 х 106 клеток на яйцо для UM-SCC-1 клеток для того, чтобы генерировать трехмерные опухоли в CAM. Имейте в виду, что число клеток может варьироваться в зависимости от клеточной линии.
- Аспирсредо среды и добавить DMEM культуры среды дополнены 1% Перо / Strep плюс 10% FBS и 2,5 мкг /мл зеленого флуоресцентного красителя. Инкубировать в течение 1 ч при 37 градусах Цельсия в инкубаторе клеточной культуры. Затем проверьте интенсивность флуоресценции на микроскопе, аспирной среде, промойте один раз с 1x PBS, и добавить 0,25% трипсина на срок до 10 мин. Нейтрализуйте трипсин с DMEM дополненной средой.
- Центрифуга на 250 х г в течение 4 мин, чтобы сформировать клетку гранулы. Аспирировать DMEM средних и повторно приостановить в HBSS для мытья избыточного флуоресцентного красителя. Подсчитайте клетки с помощью гемоситометра.
- Принесите яйца в ламинарной лампы культуры клеток. С ножницами и щипками, откройте прозрачную пленку, которая покрывает яйцо(рисунок 4E-F).
- Центрифуге рассчитывается количество клеток снова, аспирировать hBSS среды и повторно приостановить на конечной концентрации 0,5 до 1x106 ячеек на 5 qL той же среде (Рисунок 4G). Подготовьте количество, необходимое для общего количества яиц (5 кЛ клеточной суспензии на яйцо).
- Поместите 5 злятого раствора на CAM, около 2 мм от DRG(рисунок 4H). Держите равномерное расстояние между DRG и клетками. Будьте очень осторожны, чтобы не беспокоить яйцо, чтобы свести к минимуму распространение клеток.
ПРИМЕЧАНИЕ: Для начала имплантации клеток выберите яйца, на которых поверхность CAM визуально сухая. Если поверхность слишком влажная, клетки могут распространяться и не образуют регулярных опухолей. - Обложка яйцо с новой пленкой соусом, как в шаге 4.4. Привягайте клетки во все яйца. Инкубировать яйца в увлажняющем инкубаторе при 38 градусах Цельсия и 54% влажности в течение 7 дней, без вращения.
6. Сбор CAM (оценочный срок: 1 ч для десятка яиц, день 17)
- Приготовьте 6-колодные пластины с 4% ПФА (параформальдегид) pH7.0, один хорошо на яйцо, 2 мл на хорошо.
- Принесите яйца на лабораторную скамейку. Использование иглы, прикрепленной к шприцу, чтобы перфорировать пленку соусом, падение около 300 ЗЛ PFA над CAM слегка ужесточить CAM, тем самым облегчая процесс сбора урожая. Повторите это для всех яиц.
- Ножницами удалите верхнюю половину яичной скорлупы (где расположено рабочее окно) с прикрепленным к ней CAM(рисунок 4I). Уменьшите размер этой половины до приблизительно 3 см в диаметре, сохраняя часть CAM, где DRG и опухолевые клетки были привиты в центре(рисунок 4J). Возьмитесь за CAM с тонкими щипками и отсоедините его от яичной скорлупы, поместив его в PFA. Ориентируйте DRG и раковые клетки, обращенные вверх(рисунок 4K-L).
ПРИМЕЧАНИЕ: Область 3 см должна включать как DRG, так и клетки. DRG легко рассматривать как небольшой кусок прилагается на CAM, однако опухолевые клетки иногда трудно определить на валовом экзамене. - Кроме того, с ножницами, расширить операционное окно удаления яичной скорлупы из верхней части яйца, сохраняя CAM на месте; удалить примерно 1 см за пределами операционного окна(рисунок 4M) и определить DRG и клетки на CAM (рисунок4N-O). С тонкими тонкими щипками, держите CAM на одном из краев и осторожно поднимите его. С острыми тонкими ножницами, аккуратно вырезать CAM, чтобы удалить круговую область, примерно 3 см в диаметре(рисунок 4P), и место CAM в PFA с DRG и раковых клеток, обращенных вверх.
ПРИМЕЧАНИЕ: Избегайте растяжения или проведения CAM с щипками в нескольких местах, чтобы свести к минимуму повреждение тканей, которые могут генерировать микроскопии артефактов. - Поместите каждую имбрану CAM в одну скважину(рисунок 4L). Аккуратно схватить края CAM для распространения ткани открыты в PFA или осторожно встряхнуть пластину, пока CAM разворачивается, чтобы избежать сложить артефактов.
- Эвтанизировать эмбрион (день 17) путем быстрого обезглавливания. Исправьте собранные ткани в PFA в течение 4 ч при комнатной температуре. После фиксации замените PFA 1x PBS и храните ткани в PBS при 4 градусах По Цельсия до встраивания в парафин для секции. Избегайте чрезмерной фиксации, которая повредит деликатную сосудку CAM.
- Используя стереомикроскоп флуоресценции, сфотографируйте мембраны в течение 2 дней после сбора урожая, чтобы избежать потери флуоресцентных сигналов.
При оптимизации этот метод имеет около 100% интеграции DRG в CAM. Репрезентативные результаты интеграции DRG показаны на рисунке 5A-B. Интеграция DRG в CAM имеет важное значение, поскольку она обеспечивает жизнеспособность ткани DRG во время эксперимента. Микроскопически, DRG рассматривается в соединительной ткани CAM (H и E пятно). Кровеносные сосуды часто видели внутри ткани DRG, предполагая, что CAM кровоснабжения является воспитание привитых тканей. Имплантированные опухоли также идентифицируются на CAM H и E; в зависимости от того, сколько вторжения присутствует, опухоли могут представлять ни с одним из многочисленных островов опухоли вторжения соединительной ткани(Рисунок 5C-D). Представитель Рисунок 5E-F показывает собранный CAM на ярком поле изображения и слилась флуоресценции. UM-SCC-1 клетки overexpressing Галанин рецептор 2 представлены увеличение вторжения DRG по сравнению с контрольными клетками(Рисунок 5G-H). Рак-DRG взаимодействия наблюдается как раковые клетки, представляющие направленное вторжение к DRG(Рисунок 5H).
Анализ данных выполняется по-разному. Направленное вторжение раковых клеток к DRG наблюдается как дихотомическая переменная, и количество яиц, представляющих эту модель вторжения, учитывается в каждой группе. Статистические различия между группами рассчитываются с помощью биномиального теста пропорций. Близость между раковыми клетками и DRG, и область опухоли измеряются с помощью ImageJ6 и различия между группами оцениваются с помощью т-теста студента. Для обеспечения точности с помощью анализа ImageJ все изображения из одного и того же эксперимента должны быть сделаны на одинаковом освещении и настройках экспозиции. После корректировки порога изображения и яркости всех изображений с использованием одних и тех же критериев, инструмент анализа частиц используется для измерения области опухоли, а линейный инструмент измерения измеряет расстояния опухоли-DRG. Важно использовать постоянную установку размера частиц, анализируемых для всех изображений в разных группах. В некоторых случаях опухоли становятся толще и могут быть измерены вручную с помощью цифрового калибра, что позволяет измерять объем.
Использование разделов парафина встроенных CAM ткани, Н И E пятно или иммуногистохимия для эпителиальных клеток (анти-цитокератин антитела реактивной для человеческого вида) может быть выполнена, что позволяет оценить вторжение в соединительной ткани. Вторжение количественно, как количество опухолевых островов в соединительной ткани на яйцо. Иммунофлуоресценция для коллагена IV может быть использована для выделения мембраны подвала. Кроме того, при использовании GFP помечены раковые клетки, идентификация этих клеток в секциях тканей облегчается без иммуногистохимии для цитокератина. Метастаз и ангиогенез анализ в CAM эксперименты обсуждаются в другом месте10,17.
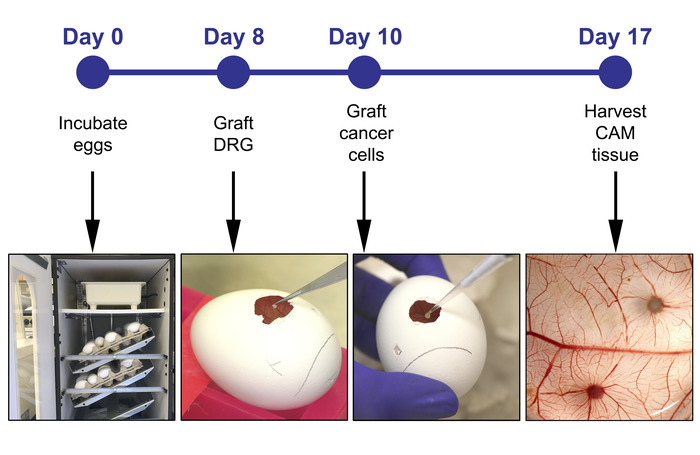
Рисунок 1: Временная шкала эксперимента, включающая основные шаги в дни 0, 8, 10 и 17. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
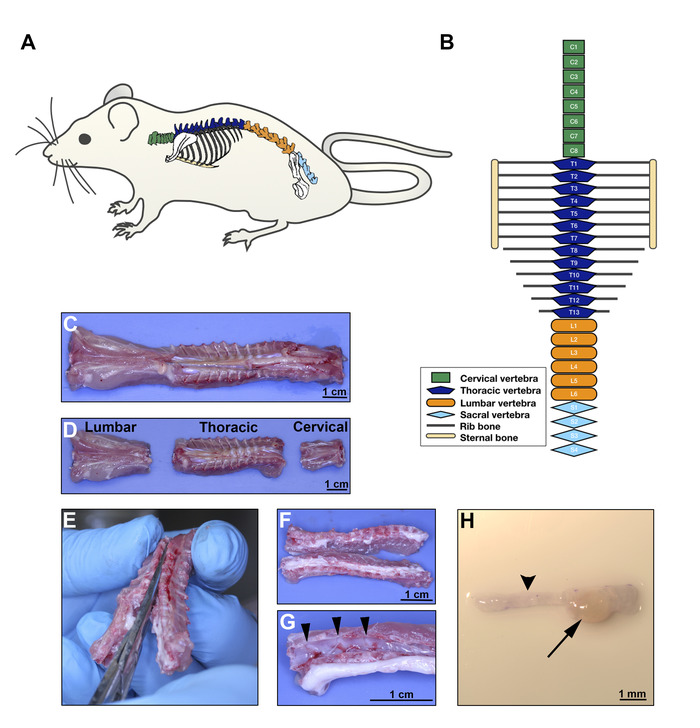
Рисунок 2: добыча DRG на 8-й день . A. Крыса схематика, иллюстрирующая анатомическое расположение позвоночника. B. Диаграмма конфигурации крысиных позвонков, показывающая различные области тела; зеленый для шейки матки, темно-синий для грудной клетки, оранжевый для поясничных и светло-голубой для крестцовых позвонков. C-D. Вентральный аспект крысиного позвоночника после хирургического иссечения; разделение регионов, как показано в B. E.Рассечение позвонков, чтобы открыть канал спинного мозга, разделяя позвонков органов на два боковых разделов, содержащих DRGs. Раздел должен прорезать спинной и вентральный аспект каждой позвоночной кости в средней линии. F. Валовой аспект открытого грудного отдела позвоночника. G. После того, как спинной мозг смещен, DRGs легко видны в позвоночных каналах (стрелка головы указывая 3 DRGs). H. Стереомикроскопическое изображение одного DRG (стрелка) с соответствующими аксонными пучками (стрелка головка). Шкала баров: C, D, F, и G, 1 см; H, 1 мм. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
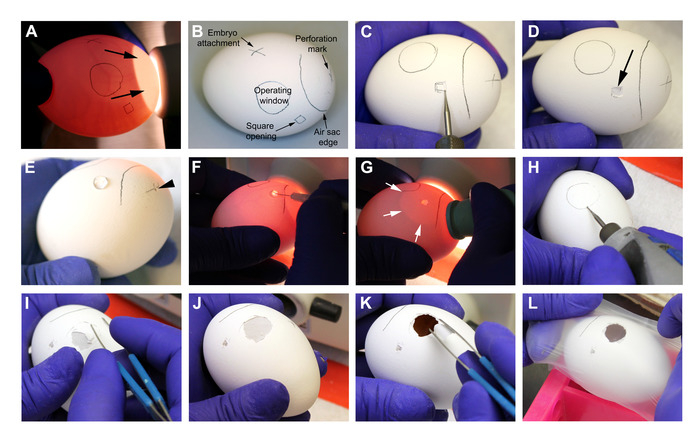
Рисунок 3: Приготовление яиц на 8-й день. А-Б. Идентификация сосуды яичных и маркировки до процедуры. Стрелки на точке естественно происходящих воздушный мешок. C-D. Бурение и открытие яичной скорлупы на квадратной отметке открытия. Стрелка на D указывает на нетронутую внешнюю мембрану яичной скорлупы после удаления скорлупы с помощью тупых щипушек. E. Отмеченный крест на воздушном мешке перфорирован с дрелью, чтобы позволить поток воздуха в яйцо (стрелка головы). 30 зЛ среды HBSS помещается на внешнюю мембрану яичной скорлупы на квадратном открытии. F. С тонкой шприцевой иглой, внешняя мембрана яичной скорлупы перфорирована там, где ранее был помещен HBSS. G. Давление наносится на резиновую лампу eyedropper при присоединении его к перфорации, пробуренной на воздушном мешке. Когда давление пальца высвобождается, воздух пылесосится, создавая искусственный воздушный мешок (белые стрелки), который должен распространяться на операционное окно. H. Края рабочего окна просверливаются в почти параллельном положении с яичной скорлупой, чтобы избежать случайной перфорации. I-J. Удаление яичной скорлупы тупыми щипками. K. Удалите наружную мембрану яичной скорлупы тупыми щипками, стараясь не вводить частицы на CAM (наблюдаемый на 1 см ниже поверхности). Яйца L. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
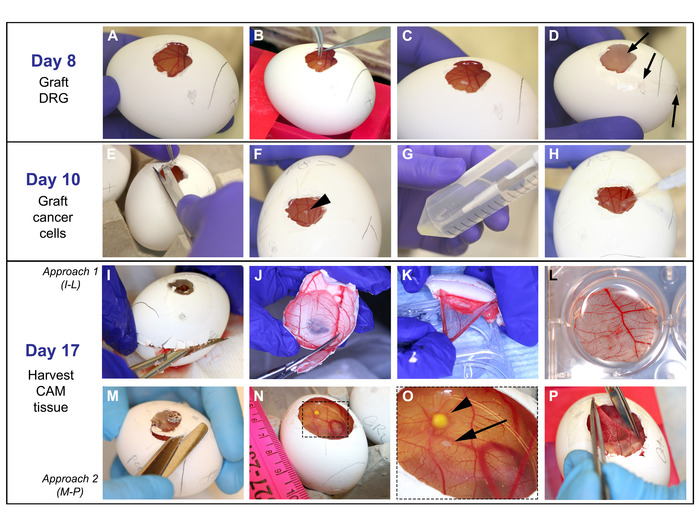
Рисунок 4: Прививка DRG, клетки, и уборка CAM: На 8-й день: A. CAM легко наблюдается после удаления парафиновой восковой мембраны. B-C. С тонкими щипками, DRG помещается на CAM. D. Яйцо покрывается пленочным соусом и помещается в инкубатор; стрелки указывают на отверстия, которые покрыты. На 10-й день: E-F. Пленка повязка удаляется и DRG находится (стрелка головка на F). G-H. 5 qL клеточного раствора сбрасывается на CAM на расстоянии 2 мм от DRG. На 17-й день: I-L и M-P демонстрируют два различных подхода, используемых для сбора CAM. I. Яичная скорлупа открывается тонким ножницами, начиная с воздушного мешка пробуренной перфорации до тех пор, пока верхняя половина яйца не будет удалена. J. Яичная оболочка, содержащая CAM уменьшается в размерах примерно до 3 см. K-L. С тонкими щипками, CAM отделяется от яичной скорлупы и помещается в PFA. М-О. Расширение операционного окна выполняется для визуализации DRG и раковых клеток на CAM. Стрелка указывает на опухоль, а стрелка указывает на DRG. P. CAM схватил с тонкими щипками, вырезать с острыми ножницами, и помещен ы в PFA, как показано в L. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
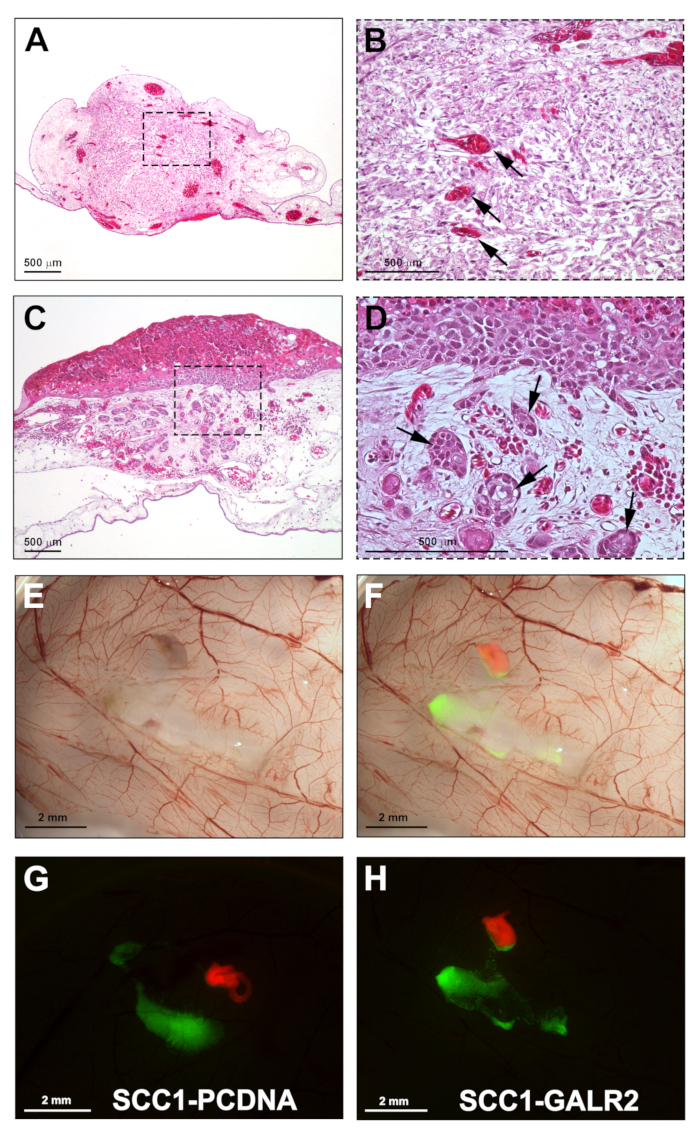
Рисунок 5: Результаты представитель. A. Н И Е раздел, показывающий интеграцию DRG в CAM. B. Высшее увеличение A; стрелки показывают CAM кровеносные сосуды в DRG. C. UM-SCC-1 клетки привиты на CAM и собрали через четыре дня после прививки (H и E пятно). D. Высшее увеличение C, показывающее инвазивные опухолевые острова в соединительной ткани CAM (стрелки). E. Гросс стереомикроскопическое изображение CAM, привитого с UM-SCC-1-GALR2 клеток и крыс DRG, собранные на 17-й день. F.Слияние флуоресценции и ярко-поле изображения подчеркнув DRG помечены красным цветом и раковые клетки помечены зеленым цветом. G-H. Флуоресценция стереомикроскопия CAM привитых с DRG и UM-SCC-1-GALR2 против контрольных элементов, иллюстрирующие направленное вторжение UM-SCC-1-GALR2 клеток в DRG (H). Шкала баров: A-D, 500 мкм; E-H, 2 мм. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
| Шаг | Проблема | Причина | Решение | ||||||
| 3.2.1 | Невозможно определить привязанность эмбриона. | Положение привязанности трудно увидеть в то время как яйцо все еще. | Поверните яйцо быстро боком, чтобы иметь возможность увидеть длинный сосуд, прикрепленный к яйцеклетке мембраны. | ||||||
| 3.3 и 3.8 | Перфорация наружной мембраны яичной скорлупы во время бурения. | Неправильное позиционирование сверла. | Расположите сверло почти параллельно яичной скорлупе во время бурения. Если мембрана перфорирована в шаге 3.3, нет необходимости выполнять дальнейшую перфорацию с помощью иглы, как указано в шаге 3.5. Если кровотечение происходит, отбросить яйцо. | ||||||
| 4,3 | DRG прилипает к щипкам. | DRG сухой. | Влажный DRG снова в HBSS и / или использовать тонкую иглу, чтобы помочь отделить DRG от щипцы. | ||||||
| 5.2 | Клетки не идеально помечены флуоресцентным красителем. | Время инкубации. Некоторые клетки требуют больше времени для маркировки. | Держите клетки в течение дополнительного часа в средствах массовой информации с флуоресцентным красителем. | ||||||
| 5.6 | Воздушный пузырь на клеточной капле. | Использование всей жидкости в наконечнике пипетки. | Загрузите на 1 л больше, чем желаемый объем, и не используйте окончательный КЛ пипетки при имплантации клеток. Это позволит избежать пузырьков воздуха в клетках смеси. | ||||||
| 6,3 | Невозможно определить DRG или клетки при сборе CAM. | Малый DRG, DRG получил смещения, раковые клетки распространения. | Если DRG не видел, урожай большей площади CAM и место в большой контейнер для фиксации. Проверьте DRG и положение клеток под флуоресценцией в стерео микроскоп, а затем обрезать CAM до меньшего размера для встраивания парафина. | ||||||
Таблица 1: Таблица для устранения неполадок
Представленная здесь модель CAM-DRG in vivo устраняет дефицит предыдущих моделей, демонстрируя нервно-опухолевое взаимодействие до физического вторжения нерва опухолевыми клетками. Большинство in vivo исследования PNI сосредоточиться на распространении опухоли и ингибирование двигательной функции, и зависит от прямого впрыска опухолевых клеток в седализаторы23,24,25. Инъекции седалищного нерва является in vivo модель PNI, где раковые клетки вводятся в мышь или крысиный седалищный нерв, где опухоль впоследствии растет. Инъекционные модели полезны, чтобы показать разрушительное прогрессирование опухоли и боль в результате опухолевых клеток в нервах. Седалитовый нерв модель также подходит для изучения факторов, которые позволяют раковые клетки процветать в нерва, но не хватает способности оценить раннюю фазу PNI, потому что он вводит клетки непосредственно в нерв, минуя нервных оболочек. В другом подходе, хирургически имплантированные ортотопические опухолевые трансплантаты были использованы для характеристики важности адренергических и холинергических нервных волокон в содействии прогрессированию рака простаты, тем самым предлагая заметную роль нервов в прогрессии опухоли 26. Эта модель состояла из химической абляции мурин симпатических и парасимпатических нервов. Парасимпатические волокна проникли опухолевых тканей, процесс, связанный с PNI, но модель не была специально использована для оценки физических взаимодействий между нервом и опухолью. Модель CAM-DRG позволяет проводить исследование взаимодействий между нервом и раком во время PNI. Кроме того, модели murine являются дорогостоящими и трудоемкими по сравнению с моделью CAM. Мы предлагаем использовать модель CAM-DRG для механистических исследований ПНИ.
Некоторые преимущества подхода CAM-DRG включают оценку ПНИ и других фенотипов, таких как рост опухоли, метастаз и ангиогенез. Идентификация ДНК человека на нижнем CAM и / или в печени может быть использована для обнаружения метастазов человеческих раковых клеток линий10, более чувствительный экспериментальный подход по сравнению с тканей секции и окрашивания, которые не могут выявить небольшие метастазовые.
Метод CAM-DRG имеет некоторые ограничения, включая короткий срок наблюдения. Иммунная система эмбриона физиологически активна к18-27дню, когда может происходить отторжение и воспалительный процесс, ограничивающий экспериментальное время. Важно также учитывать расстояние при прививке опухолевых клеток, близких к DRG; большие расстояния DRG-рака могут ухудшить молекулярные взаимодействия между опухолевыми клетками и нервом, или может задержать физический контакт между обоими компонентами модели. Кроме того, если эмбрионы старше, чем предусмотрено в этом протоколе, эмбрион движения могут вытеснить опухолевые клетки. Поэтому важно использовать яйца в соответствии с днем 10 после оплодотворения для клеточной прививки.
Так как иммунная система не полностью развита до дня 1827, микроокружение опухоли в CAM похож на иммунодепрессированных моделей мурин часто используется для исследований рака. Поэтому эта модель не полезна для оценки роли иммунных клеток в прогрессировании опухоли. Другим ограничением является ограниченное наличие реагентов для видов кур, таких как антитела, цитокины и грунтовки.
Точное выполнение этого протокола требует практики; однако это может быть сделано сотрудником лаборатории без необходимости в специализированном базовом учреждении. Бурение яичной скорлупы требует обучения. Практика на продуктовых (неоплодотворенных) яйца рекомендуется, прежде чем пытаться эту модель в первый раз. Высокая эмбриональная выживаемость и успех модели могут быть достигнуты, если будут предприняты некоторые критические шаги, чтобы избежать инфекции: соответствующая антибиотикопрофилактика DRGs в 2% Pen/Strep, работающая в ламинарном шкафу потока, и избегающая рассеивания частиц яичной скорлупы на CAM. Также важно поддерживать стабильную влажность во время общего времени инкубации яйцеклеток. Мы рекомендуем увеличить количество яиц на группу до тех пор, пока техника не будет освоена. Наиболее частыми проблемами для неопытного персонала лаборатории являются заражение яйцами и неточная методика прививки клеток.
Сбор урожая DRG также требует профессиональной подготовки; практика в сборе DRGs для экспериментов в пробирке8 перед попыткой in vivo модель рекомендуется. Культура in vitro DRG – это возможность оптимизировать условия и улучшить технику сокращения продолжительности добычи DRG. Особое внимание требуется технике уборки при захвате DRG с помощью щипцев. DRG не должно проводиться непосредственно; под ним следует применять давление. Мы рекомендуем использовать увеличительное линза для лучшей визуализации DRG во время извлечения.
Важно отметить, что при первом выполнении этой модели все условия должны быть оптимизированы для нужной клеточной линии. Эта модель была оптимизирована для крыс DRG и hnC клеточной линии UM-SCC-1. Использование мыши DRG и других типов раковых клеток может потребовать оптимизации. С более высокой концентрацией привитых клеток, опухоли, как правило, растут толще и жестче, что облегчает измерения опухоли. Принимая во внимание несколько яиц для каждой группы и соответствующую концентрацию клеток для каждого яйца, несколько миллионов клеток может потребоваться для каждого эксперимента. Для облегчения планирования следует принимать во внимание информацию о времени удвоения клеток. Для некоторых критических шагов в этом протоколе предусмотрена таблица устранения неполадок(таблица 1).
Авторы не заявляют о каких-либо конкурирующих интересах.
Эта работа была поддержана NIH/NIDCR гранты DE027551 и DE022567 (NJD).
| Name | Company | Catalog Number | Comments |
| 0.25% Trypsin-EDTA (1x) | Gibco | # 25200-056 | |
| ACE light source | SCHOTT North America, Inc. | Used to transilluminate the eggs | |
| CellTracker Green CMFDA fluorescent dye | Life Technologies | # C7025 | Reconstitute 50µg in 20µL of DMSO and stock at -20oC. Use 1µL of stock solution/mL of culture medium. |
| CellTracker Red CMTPX fluorescent dye | Life Technologies | # C34552 | Reconstitute 50µg in 40µL of DMSO and stock at -20oC. Use 1µL of stock solution/mL of culture medium |
| Cordless rotary tool | DREMEL | # 866 | Used to drill the egg shell |
| DMEM (1x) | Gibco | # 11965-092 | Dulbeecco`s Modified Eagle Medium |
| DMSO | Fisher Bioreagents | # BP231-100 | Dimethyl Sulfoxide |
| Dumont # 5 fine forceps | Fine Science Tools (FST) | # 11254-20 | Used to harvest DRG |
| Egg incubator | GQF Digital Sportsman | # 1502 | Egg incubator equipped with automatic rotator, digital thermostat, temperature and humidity controls |
| Engraving cutter | DREMEL | # 108 | Used to drill the egg shell |
| Extra fine Graefe forceps, curved | Fine Science Tools (FST) | # 11151-10 | Used to graft DRG onto the CAM on day 8 and to harvest CAM tissue on day 17 |
| Extra fine Graefe forceps, straight | Fine Science Tools (FST) | # 11150-10 | Used to graft DRG onto the CAM on day 8 and to harvest CAM tissue on day 17 |
| Fertilized Lohmann White Leghorn eggs | Fertilized eggs at early fertilization days, preferably on first day post-fertilization. Eggs used in this protocol are from Michigan State University Poultry Farm. | ||
| Filter Forceps | EMD Millipore | # XX6200006P | Blunt forceps used to remove the egg shell |
| Fine surgical straight sharp scissor | Fine Science Tools (FST) | #14060-09 | Used to harvest the CAM tissue on day 17 |
| HBSS (1x) | Gibco | # 14025-092 | Hank`s Balanced Salt Solution |
| HI FBS | Gibco | # 10082-147 | Heat-inactivated Fetal Bovine Serum |
| Paraffin wax membrane | Parafilm laboratory film | # PM-996 | Used to temporarily cover the egg openings until DRG grafting on day 8 |
| PBS (1x) pH 7.4 | Gibco | # 10010-023 | Phosphate Buffered Saline |
| Pen/Strep | Gibco | # 15140-122 | 10,000 Units/mL Penicilin, 10,000 µg/mL Streptomycin |
| PFA (paraformaldehyde solution) | Sigma-Aldrich | # P6148-1KG | Dilute in water to make a 4% PFA solution |
| Sprague Dawley rats (females) | Charles River laboratories | Strain code: 001 | 6-7 weeks old (190-210g in weight) |
| Tegaderm Transparent Film Dressing | 3M | # 9505W | Sterile, 6x7cm, used to cover the egg openings during incubation |
- Schmitd, L. B., Scanlon, C. S., D'Silva, N. J. Perineural Invasion in Head and Neck Cancer. Journal of dental research. 97 (7), 742-750 (2018).
- Liebig, C., Ayala, G., Wilks, J. A., Berger, D. H., Albo, D. Perineural invasion in cancer: a review of the literature. Cancer. 115 (15), 3379-3391 (2009).
- Schmitd, L. B., et al. Redefining Perineural Invasion: Integration of Biology With Clinical Outcome. Neoplasia (New York, N.Y). 20 (7), 657-667 (2018).
- Chinn, S. B., et al. Impact of perineural invasion in the pathologically N0 neck in oral cavity squamous cell carcinoma. Otolaryngology--head and neck surgery : official journal of American Academy of Otolaryngology-Head and Neck Surgery. 149 (6), 893-899 (2013).
- Tai, S. K., Li, W. Y., Yang, M. H., Chu, P. Y., Wang, Y. F. Perineural invasion in T1 oral squamous cell carcinoma indicates the need for aggressive elective neck dissection. The American journal of surgical pathology. 37 (8), 1164-1172 (2013).
- Scanlon, C. S., et al. Galanin modulates the neural niche to favour perineural invasion in head and neck cancer. Nature communications. 6, 6885 (2015).
- Amit, M., et al. Upregulation of RET induces perineurial invasion of pancreatic adenocarcinoma. Oncogene. 36 (23), 3232-3239 (2017).
- Huyett, P., Gilbert, M., Liu, L., Ferris, R. L., Kim, S. A Model for Perineural Invasion in Head and Neck Squamous Cell Carcinoma. Journal of visualized experiments : JoVE. (119), (2017).
- Ayala, G. E., et al. In vitro dorsal root ganglia and human prostate cell line interaction: redefining perineural invasion in prostate cancer. The Prostate. 49 (3), 213-223 (2001).
- Liu, M., et al. The Histone Methyltransferase EZH2 Mediates Tumor Progression on the Chick Chorioallantoic Membrane Assay, a Novel Model of Head and Neck Squamous Cell Carcinoma. Translational oncology. 6 (3), 273-281 (2013).
- Busch, C., Krochmann, J., Drews, U. The chick embryo as an experimental system for melanoma cell invasion. PloS one. 8 (1), e53970 (2013).
- Li, M., et al. The In Ovo Chick Chorioallantoic Membrane (CAM) Assay as an Efficient Xenograft Model of Hepatocellular Carcinoma. Journal of visualized experiments : JoVE. (104), (2015).
- Ota, I., Li, X. Y., Hu, Y., Weiss, S. J. Induction of a MT1-MMP and MT2-MMP-dependent basement membrane transmigration program in cancer cells by Snail1. Proceedings of the National Academy of Sciences of the United States of America. 106 (48), 20318-20323 (2009).
- Murphy, J. B. TRANSPLANTABILITY OF TISSUES TO THE EMBRYO OF FOREIGN SPECIES : ITS BEARING ON QUESTIONS OF TISSUE SPECIFICITY AND TUMOR IMMUNITY. The Journal of experimental medicine. 17 (4), 482-493 (1913).
- Ribatti, D., Nico, B., Vacca, A., Presta, M. The gelatin sponge-chorioallantoic membrane assay. Nature. 1 (1), 85-91 (2006).
- Auerbach, R., Arensman, R., Kubai, L., Folkman, J. Tumor-induced angiogenesis: lack of inhibition by irradiation. International journal of cancer. 15 (2), 241-245 (1975).
- Banerjee, R., et al. The G protein-coupled receptor GALR2 promotes angiogenesis in head and neck cancer. Molecular cancer therapeutics. 13 (5), 1323-1333 (2014).
- Ossowski, L., Reich, E. Experimental model for quantitative study of metastasis. Cancer research. 40 (7), 2300-2309 (1980).
- Nowak-Sliwinska, P., Segura, T., Iruela-Arispe, M. L. The chicken chorioallantoic membrane model in biology, medicine and bioengineering. Angiogenesis. 17 (4), 779-804 (2014).
- Moreno-Jimenez, I., et al. The chorioallantoic membrane (CAM) assay for the study of human bone regeneration: a refinement animal model for tissue engineering. Scientific reports. 6, 32168 (2016).
- Vu, B. T., et al. Chick chorioallantoic membrane assay as an in vivo model to study the effect of nanoparticle-based anticancer drugs in ovarian cancer. Scientific reports. 8 (1), 8524 (2018).
- Sleigh, J. N., Weir, G. A., Schiavo, G. A simple, step-by-step dissection protocol for the rapid isolation of mouse dorsal root ganglia. BMC research notes. 9, 82 (2016).
- Cavel, O., et al. Endoneurial macrophages induce perineural invasion of pancreatic cancer cells by secretion of GDNF and activation of RET tyrosine kinase receptor. Cancer research. 72 (22), 5733-5743 (2012).
- Guo, K., et al. Interaction of the sympathetic nerve with pancreatic cancer cells promotes perineural invasion through the activation of STAT3 signaling. Molecular cancer therapeutics. 12 (3), 264-273 (2013).
- Deborde, S., et al. An In Vivo Murine Sciatic Nerve Model of Perineural Invasion. Journal of visualized experiments : JoVE. (134), (2018).
- Magnon, C., et al. . Autonomic nerve development contributes to prostate cancer progression. 341 (6142), 1236361 (2013).
- Ribatti, D. Chick embryo chorioallantoic membrane as a useful tool to study angiogenesis. International review of cell and molecular biology. 270, 181-224 (2008).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved