Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Medicine
Imaging Funktioner af systemisk sklerose-associeret interstitiel lungesygdom
Her præsenterer vi praktiske anbefalinger til udførelse af thorax høj opløsning computertomografi til diagnosticering og vurdering af systemisk sklerose-relaterede interstitielle lungesygdom.
Tidlig diagnosticering af systemisk skleroserelateret interstitiel lungesygdom (SSc-ILS) er vigtig for at gøre det muligt at administrere behandlingen med minimal forsinkelse. Men diagnosticering af SSc-ILS er udfordrende, fordi de vigtigste symptomer er ikke-specifikke. Høj opløsning computertomografi (HRCT) af brystet er anerkendt som en følsom billeddannelse metode til diagnosticering og vurdering af SSc-ILS. Eksponering af patienter for ioniserende stråling kan betragtes som en begrænsning, selv om der kan tages metodologiske skridt til at moderere dette. Vi præsenterer praktiske anbefalinger til udførelse af HRCT-scanninger og fortolkning af resultaterne. De vigtigste funktioner i SSc-ILD på HRCT omfatter en ikke-specifik interstitiel lungebetændelse (NSIP) mønster med perifere jord-glas opaciteter og omfattende trækkraft bronchiectasis. På trods af ligheder mellem SSc-ILD og idiopatisk lungefibrose (IPF) kan HRCT bruges til at skelne mellem disse betingelser: I SSc-ILS sammenlignet med IPF er der en større andel af opaciteten i jordglas, og fibrosen er mindre grov. En forstørret, luftfyldt spiserøret med diameter >10 mm, der tyder på esophageal dysmotilitet ses almindeligvis i SSc-ILS. Pulmonal arterie størrelse større end den tilstødende stigende aorta antyder sameksistente pulmonal hypertension. Knuder skal overvåges på grund af den øgede risiko for lungekræft. En stor grad af sygdom på MENCT (≥20%) eller en høj fibrose score tyder på en øget risiko for dødelighed. HRCT er centralt for diagnosticering af SSc-ILS, og serielle vurderinger kan være nyttige til overvågning af sygdomsprogression eller behandlingsrespons.
Systemisk sklerose (SSc) er en kompleks, heterogen, autoimmun sygdom. Det kan manifesteres som vaskulopati, Raynauds fænomen og fibrose i huden og indre organer1. SSc er klassificeret i undertyper som følger: begrænset kutan, diffus kutan, sinus sklerodermi (uden hud involvering), og SSc overlapper syndrom1.
SSc er ikke nedarvet i mendelian mode, men genetiske faktorer synes at påvirke modtagelighed for sygdommen. Incidensen varierer mellem etniske grupper og øges blandt personer medsygdommens slægtshistorie 2,3. Der synes også at være miljømæssige risikofaktorer, idet høj eksponering for silica eller organiske opløsningsmidler synes at øge forekomsten af SSc4. Den globale udbredelse af SSc er omkring 1 ud af 10.0001. Flere kvinder end mænd er påvirket af SSc, med rapporterede kvindelige: mandlige nøgletal spænder mellem 3:1 og 8:1, og aldersgruppen med den højeste forekomst af sygdommen er 45-54 år5.
Lungen er det næstmest berørte viscerale organ hos patienter med SSc6. Der er to primære pulmonale manifestationer af SSc: interstitiel lungesygdom (ILD), og pulmonal hypertension7. ILS er normalt fibrotisk; det forekommer hos ca. 80 % af patienterne med SSc og er mere almindeligt hos diffus kutan sklerodermi end i den begrænsede form af sygdommen1,8. Pulmonal hypertension kan manifestere sig som isoleret pulmonal arteriel hypertension (PAH, som har en prævalens på 13-35% i SSc) eller pulmonal hypertension som følge af venstre ventrikel involvering / diastolisk dysfunktion eller ILD / hypoxæmi7. Antistofprofiler varierer mellem patienter med SSc-ILS og patienter med SSc-PAH. For eksempel er tilstedeværelsen af anti-Scl-70 antistoffer forbundet med SSc-ILD8,mens anticentromere antistoffer er mere almindelige hos SSc-patienter med PAH end hos dem uden PAH9.
Symptomerne på SSc-ILS omfatter dyspnø, hoste, brystsmerter og træningsbegrænsning. ILS er en stor bidragyder til sygelighed i SSc10,11,12. Som en konsekvens, årlige all-cause sundhedsudgifter er blevet rapporteret til at være højere hos patienter med SSc-ILS end i dem med SSc og ingen ILD: $ 31.285-55.446 versus $ 18.513-23.268, henholdsvis13.
SSc-ILS er den hyppigste årsag til dødelighed hos patienter med SSc, der tegner sig for 30-35% af dødsfaldene i denne gruppe10,14. Median overlevelse blandt patienter med SSc-ILS er blevet rapporteret til at være 5-8 år10,15; til sammenligning overlever ca. 76 % af den samlede befolkning med SSc i mere end 10 år fra sygdomsdebut16. Signifikante prædiktorer for dødelighed i SSc-ITTE omfatter alder, tvungen vital kapacitet (FVC), baseline diffusing kapacitet i lungerne for kulilte (DLCO), omfanget af sygdom på høj opløsning computertomografi (HRCT), tilstedeværelse af pulmonal hypertension og niveauer af Kerbs von den Lungren 6 (KL-6) antigen17,18.
Tidlig diagnose er vigtig for at gøre det muligt at administrere behandlingen med minimal forsinkelse, og hos patienter med en progressiv fænotype kan sygdomsprogressionen potentielt blive bremset. Men diagnosticering af SSc-ILS er udfordrende, fordi ikke-specifikke symptomer på hoste, dyspnø og træthed kan forveksles med andre aspekter af SSc, såsom hjertesygdom og muskel- og skeletbesvær. Evalueringer til diagnosticering af id'er omfatter: klinisk præsentation, historie, rygestatus, lungefunktion, billeddannelse, og i nogle tilfælde lungebiopsi. Bekræftelse af SSc-ILD diagnose kræver flere undersøgelser, som ofte anvendes i kombination19. De hyppigst anvendte vurderinger omfatter lungefunktionstest og HRCT20,21,22,23. Andre billeddannelsesmetoder, såsom brystrastring og strålingsbesparende billeddannelse (f.eks. magnetisk resonansscanning [MRI], lungeultrault) kan også anvendes22. Pulmonale funktionstest bruges til at vurdere alvorligheden af ILS og overvåge dens kurs. Brugen af lungefunktionstest alene er dog til begrænset brug til diagnosticering af SSc-ILD24,25. HRCT af brystet betragtes som den mest følsomme ikke-invasive middel til at lette differentialdiagnose af SSc-ILD19. Baseline HRCT resultater, samt ændringer over tid, kan bruges til at forudsige det fremtidige forløb af lungesygdom og potentielle respons på terapi26.
Eksponering for stråling med MENCT betragtes undertiden som en begrænsende faktor for regelmæssig screening27,28; begrænsning af antallet af skiver er en potentiel metode til at reducere strålingsrisikoen, og dosis kan også reduceres ved at reducere enten spændingen eller strømmen29,30,31. Alternativt kan der overvejes forskellige vurderingsmetoder. For eksempel synes MR-scanning at have et vist potentiale for evaluering og opfølgning af ILS-patienter22. I en undersøgelse med T2-vægtede MR-billeder med respiratorisk synkronisering blev HRCT udført parallelt som "guldstandarden"-vurderingen. 100 % følsomhed og 60 % specificitet blev rapporteret med MR-scanning til bestemmelse af tilstedeværelsen af ILS32. I en anden undersøgelse33blev der rapporteret om en lignende aftale mellem MR og MENCT i forbindelse med påvisning og kategorisering af ILS . På trods af de lovende resultater, MR er i øjeblikket en forskning metode, og det er endnu ikke klar til generaliseret klinisk brug.
Her giver vi et praktisk overblik over fortolkningen af billeddannelsesresultater med fokus på HRCT, til diagnosticering af lungeinddragelse i SSc, fastlæggelse af prognose og også udforskning af fremtidige udviklinger, der kan forbedre billeddannelsesmetoder og fortolkning af resultater. HRCT-billeder fra repræsentative sager er inkluderet i papiret.
1. HRCT-scanning
- Udfør volumetrisk HRCT erhvervelse scanning af brystet36. Kontrastmidler er ikke påkrævet36,37.
- Der opskaffes følgende erhvervelser med parametre vist i tabel 136,37.
- Anskaf en supine inspiratory scanning (volumetrisk) fra lunge apices til lungebasen.
- Anskaf en supine expiratory scan (sekventiel med 10-20 mm huller) fra 2 cm under lunge apices til lungebasen.
- Anskaf en tilbøjelig inspiratorisk valgfri (sekventiel med 10-20 mm huller) fra carinaen til lungebasen.
- Giv patienten vejrtrækningsinstruktioner før hver erhvervelse36,37. For en inspiratorisk scanning, siger "Tag i en dyb indånding .... og lad det ud. Tag i en anden dyb indånding .... og lad det ud. Tag i en anden dyb indånding, og hold vejret i. Hold vejret"37.
- Få inspiratoriske scanninger ved fuld inspiration35,36.
- Brug den tyndeste kollimation, den korteste rotationstid og den højeste tonehøjde for at sikre, at bevægelsesfrie billeder opnås36. Foreslåede scanningsparametre er beskrevet i tabel 137.
- For optimal kvalitet af volumetriske scanninger, få tynde sektion (<2 mm) billeder med høj-rumlig opløsning rekonstruktion35,36.
- Gennemgå scanninger umiddelbart efter erhvervelse og gentag, hvis enten bevægelse artefakt er til stede eller utilstrækkelig inspiration har fundet sted37.
2. Rapportering
- Udarbejde en fortolkningsrapport.
- Del rapporten og HRCT billeder med patientens pleje team og tilføje dem til patientens sygejournaler.
Diagnose
De vigtigste elementer i SSc-ILD på HRCT omfatter almindeligvis et ikke-specifikt interstitielt lungebetændelsesmønster (NSIP) med perifere jordglasopaciteter og omfattende trækkraft bronchiectasis (figur 1 og figur 2). Opaciteter i glas har en bred ætiologi og er ofte ikke-specifikke40,41,42. Central overvægt eller perifer fordeling med subpleural sparing er meget tyder på NSIP (Figur 3).
Typisk, ILD mønstre i HRCT billeder omfatter reticulations med arkitektonisk forvrængning resulterer i trækkraft bronchiectasis / bronkiolectasis (i overensstemmelse med en fibrotisk form for NSIP). Trækkraft bronchiectasis og trækkraft bronkiolectasis er ofte de fremherskende træk ved SSc-ILS (Figur 4)43. Yderligere fund kan omfatte honeycombing (Figur 5; mere almindelig i begrænsede former for SSc), interlobular septal fortykkelse og intralobular linjer, og micronodules40,44. Honeycombing refererer til grupperede cystiske luftrum med typisk ensartet diameter (~ 3-10 mm) med tykke, veldefinerede vægge31. Honeycombing og trækkraft bronchiectasis er centrale elementer i sædvanlige interstitielle lungebetændelse (UIP) på HRCT. Selv om dette mønster er mest almindeligt forbundet med idiopatisk lungefibrose (IPF), prototypen fibrosing ILS med en progressiv fænotype, kan det undertiden ses hos patienter med SSc-ILS10. For nylig er der identificeret adskillige tegn hos patienter med forbindelsesrelateret vævssygdomsrelateret ILD (herunder SSc-ILD) og UIP-mønsteret på HRCT, men ikke hos patienter med IPF. Disse er den lige kant tegn (dvs. isolering af fibrose til lungebunde med skarp afgrænsning i kraniokaudalen plan uden væsentlig forlængelse langs de laterale margener af lungerne på koronale billeder), honeycombing fremherskende (eller sprudlende) tegn (> 70% af fibrotiske dele af lungerne), og den forreste øvre lap tegn (dvs. koncentration af fibrose inden for det forreste aspekt af de øverste lapper, med relativ besparelse af de andre aspekter af de øverste lapper, og samtidig lavere lap involvering)45. Tegnet lige kant er også blevet forbundet med NSIP-patologi46, som er det vigtigste CT-mønster i SSc-ILD10.
Forstørret luftfyldt spiserøret observeres hyppigt hos patienter med SSc (Figur 6)47,48,49 og hos patienter med SSc-ILS47,48. Selv om der ikke er nogen accepteret øvre aldersgrænse, hvor en udvidet spiserøret ikke længere kan bidrage til at differentiere SSc-ILS og IPF, en udvidet spiserøret kan være vanskeligere at fortolke hos patienter over 65 år på grund af stigende forekomst af esophageal motilitet lidelser. Mediastinal lymfadenopati (normalt reaktiv), hvor den korte akse af lymfeknuden overstiger 10 mm, observeres også ofte hos patienter med SSc-ILD47,50. Lungearteriestørrelse større end den tilstødende stigende aorta antyder samtidig pulmonal hypertension (Figur 6), selv hos patienter uden fibrotisk lungesygdom51,,52,53. Områder af konsolidering tyder overlejret infektion, aspiration, organisere lungebetændelse, blødning eller malignitet. Knuder skal overvåges på grund af den øgede risiko for lungekræft i SSc-ILD7; den mest almindelige primære kræftform, der opstår hos patienter med SSc-ILS, er adenocarcinom7,54.
SSc-I deler en række kliniske, mekanistiske og patologiske ligheder med IPF15,55. Nogle radiologiske funktioner gør det dog muligt at differentiere disse to id'er15,45. I SSc-ILS, sammenlignet med IPF, er der en større andel af jord-glas opacitet og fibrose er mindre grov. I tilfælde af UIP i SSc, honeycombing kan observeres i mere end 70% af fibrotisk-lungevæv ─ den sprudlende honeycombing tegn56,57. Desuden er fire-hjørner tegn (også kendt som den forreste øvre lap tegn) er betydeligt mere udbredt i SSc-ILD end i IPF; dette er et mønster af inflammation og/eller fibrose, der er omdrejningspunkt eller uforholdsmæssigt involveret i de bilaterale anterolaterale overlapper og posterosuperior nedre kamre58.
Røntgenbilleder af brystkassen kan i første omgang detektere ILS. de tilbyder dog ikke tilstrækkelig kontrastopløsning til pålidelig diagnose. Hos røntgenbilleder af brystet fra patienter med SSc-ILS er det hyppigste mønster basal dominerende reticulation59. Yderligere funktioner kan omfatte synlige bronchiectasis, volumen tab og honeycombing. Som med HRCT kan tilstedeværelsen af en udvidet luftfyldt spiserøret være nyttig til at støtte diagnosen SSc-ILD47.
Prognose
Flere forskellige billeddiagnostiske fund har vist sig at være forbundet med prognose i SSc-ILD. Dødelighedsrisikoen er rapporteret at være højere hos patienter med en sygdomsudstrækning på mindst 20 % på HRCT (10 års overlevelse var henholdsvis 43 % mod 67 % hos patienter med sygdomsudstrækning over under tærsklen på 20 %)60. Tilsvarende har en høj fibrose score på HRCT (baseret på omfanget af reticulation og honeycombing) været forbundet med øget dødelighed61. Store esophageal diametre er forbundet med øget ILS sværhedsgrad og nedsat DLCO48. Lungetæthed og lungearteriediameter kan potentielt anvendes til at forudsige risikoen for pulmonal hypertension62. Edb, kvantitative CT-parametre kunne også udnyttes til at identificere patienternes risiko for lungefunktion tilbagegang eller dødelighed. En undersøgelse viste, at omfanget af ILS, kvantificeret fra HRCT, kunne anvendes til at forudsige faldet i FVC over 12 måneder63. I en anden undersøgelse gav kvantitative c.ium CT-parametre dødelighedsrisikoresultater, der var i overensstemmelse med kliniske forudsigelsesmodeller64. På trods af deres tilsyneladende potentiale, imaging-baserede biomarkører er i øjeblikket bedst betragtes på et befolkningsniveau som deres kliniske nytte hos de enkelte patienter er ikke blevet etableret.
Behandlingsrespons
Cyclophosphamid og mycophenolat mofetil giver beskedne fordele hos patienter med SSc-ILS. I den skelsættende Sklerodermi Lunge undersøgelse I, cyclophosphamid behandling førte til langsommere progression af fibrose sammenlignet med placebo65. For nylig, Sklerodermi Lung Study II rapporterede lignende effekt og forbedret tolerabilitet med mycophenolat mofetil i sammenligning med cyclophosphamid66. Der er dog fortsat behov for bedre behandlingsmuligheder for patienter med SSc-ILS. De behandlinger, der i øjeblikket undersøges, omfatter monoklonale antistoffer (f.eks. rituximab, abituzumab), antifibrotiske midler (f.eks. nintedanib, pirfenidon), den direkte thrombinhæmmer dabigatran, proteasomhæmmende ningshæmmende stoffer og hæmatopoietisk stamcelletransplantation19,67.
Seriel HRCT-scanninger, der viser sygdomsprogression hos en patient med SSc-IS
HRCT-vurderinger, der udføres på forskellige tidspunkter, kan anvendes til at undersøge sygdomsprogression. Figur 7 viser to sæt aksiale og koronale bryst HRCT billeder taget 10 år fra hinanden i en patient med SSc-ILD. Den oprindelige aksiale og koronale billeder (Figur 7A,B) fra brystet HRCT viser basilar fremherskende jord-glas opacitet og reticulation med mild trækkraft bronchiectasis og subpleural skåne i overensstemmelse med NSIP i denne patient med SSc. Sidstnævnte sæt af billeder (Figur 7C, D) taget 10 år senere, viser øget reticulation og trækkraft bronkiolectasis på lungebaser med fald i jord-glas opacitet på aksial og koronal (Figur 7C, D) billeder fra brystet CT i overensstemmelse med mild forværring af lungefibrose. Seriel HRCT-scanninger kan også bruges til at overvåge behandlingsrespons68,69,70; Dette blev påvist i Sklerodermi-lungeundersøgelse II, hvor computerstøttede diagnosescorer baseret på HRCT-scanninger blev anvendt til at sammenligne effekten af cyclophosphamid med mykophenolatmofetil hos patienter med SSc-ILS68.
| Fase | Detektor kollimation | Spænding (kV) | Nuværende (mAs) | Skan interval | Pitch | Rotation | Rørstrøm Graduering |
| Supine inspiratoriske | Spiralformet 1,2 mm | 120 (kan sænkes) | 230 (kan sænkes) | Nielsen | ~1,0 | 0,5 sekunder eller hurtigere | På |
| Supine expiratory | Aksial 2 x 1,0 mm | 120 | 150 | 20 mm | Nielsen | 1,0 sekunder | På |
| Tilbøjelig inspiratorisk | Aksial 2 x 1,0 mm | 120 | 150 | 20 mm | Nielsen | 1,0 sekunder | På |
Tabel 1: Parametre for erhvervelse af computertomografi37. Ikke relevant.
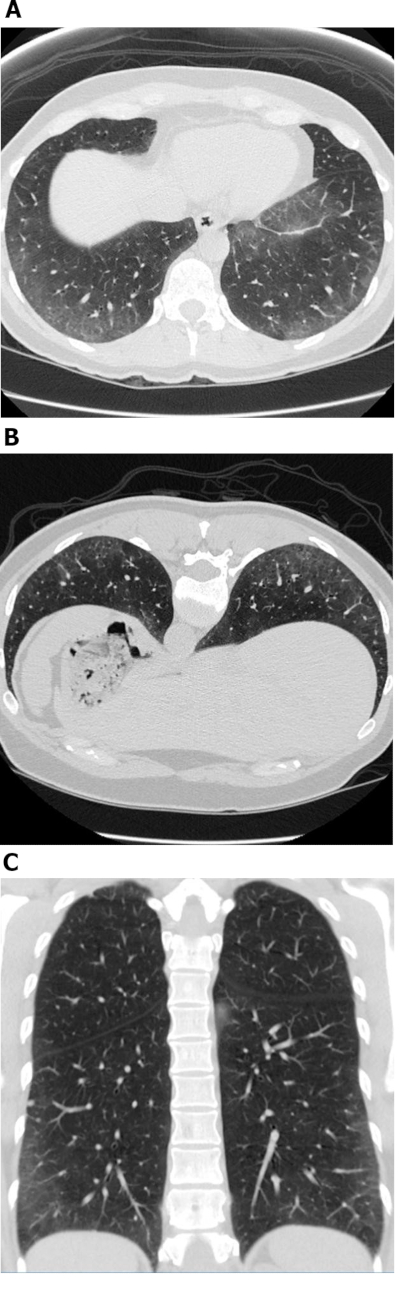
Figur 1: Systemisk sklerose med et cellulært NSIP-sygdomsmønster. Aksial (A), tilbøjelige (B) og koronale (C) høj opløsning computertomografi billeder alle viser omfattende perifere og basale fremherskende jord-glas opaciteter; disse er typiske observationer med NSIP. Manglen på trækkraft bronchiectasis tyder på en cellulær NSIP mønster af sygdom. NSIP = ikke-specifik interstitiel lungebetændelse. Klik her for at se en større version af dette tal.
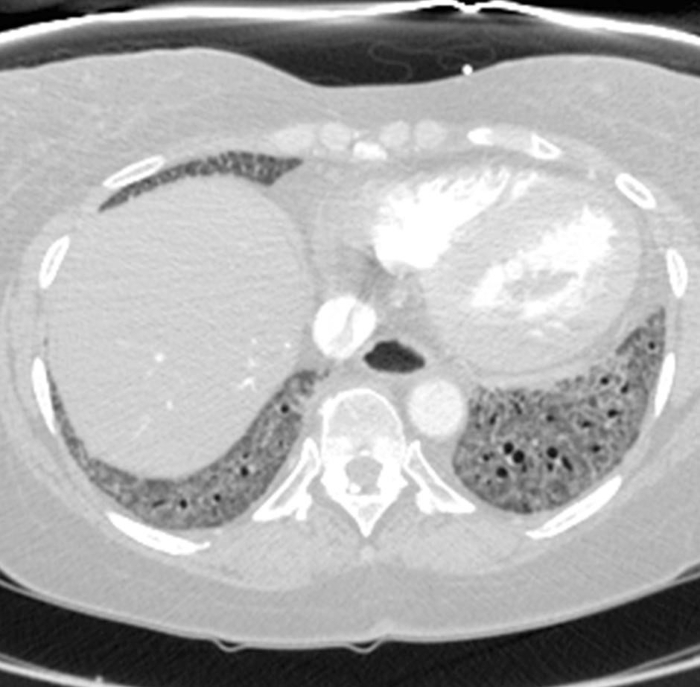
Figur 2: Systemisk sklerose med et fibrotisk ikke-specifikt interstitielt lungebetændelsesmønster af sygdom. Aksial computertomografi billede viser omfattende, basal-fremherskende jord-glas opacities med tilhørende trækkraft bronchiectasis. Især spiserøret viser markant dilatation; dette er typisk for sklerodermi. Klik her for at se en større version af dette tal.
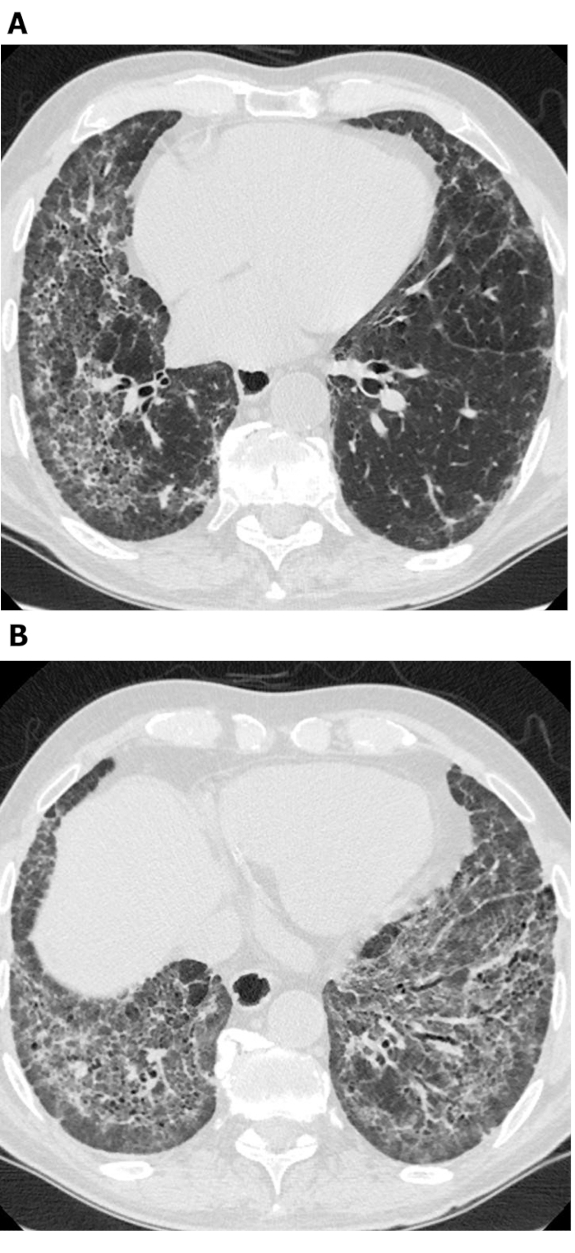
Figur 3: Systemisk sklerose med et fibrotisk NSIP-mønster. Aksial høj opløsning computertomografi billeder (A og B) viser omfattende jord-glas opaciteter, reticulation, arkitektonisk forvrængning og trækkraft bronchiectasis. Især subpleural besparelse er indlysende; dette er typisk for NSIP og ses i omkring 50% af alle tilfælde. NSIP = ikke-specifik interstitiel lungebetændelse. Klik her for at se en større version af dette tal.
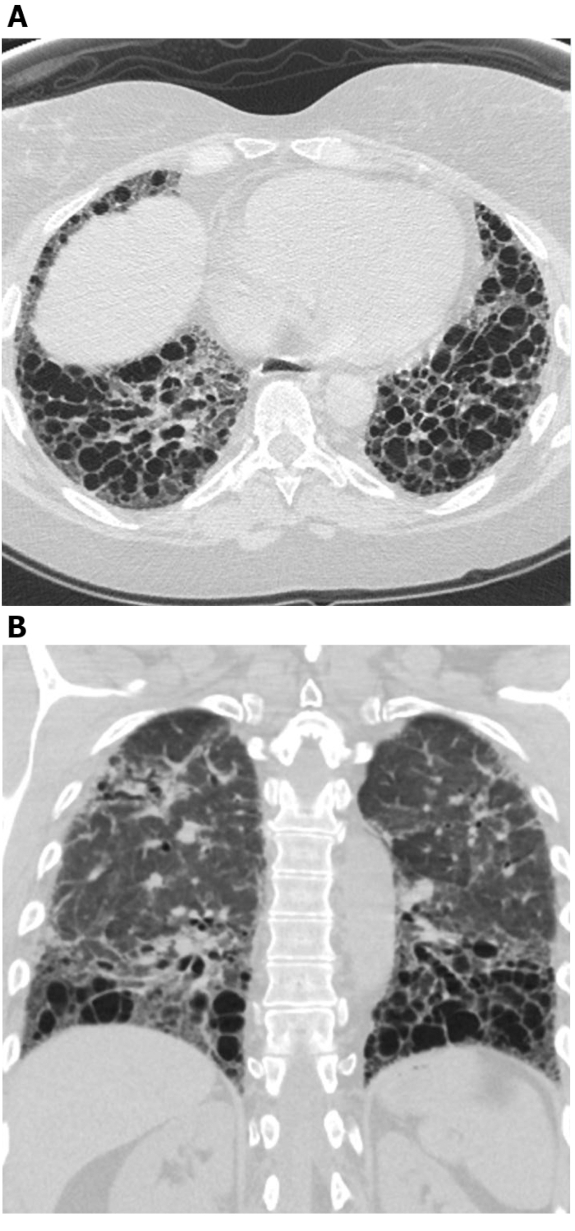
Figur 4: Systemisk sklerose med sprudlende trækkraft bronchiectasis. Aksial (A) og koronal (B) høj opløsning computertomografi billeder viser omfattende midterste og nedre lungezone fremherskende trækkraft bronchiectasis. Mens dette kan forveksles med honeycombing, cystisk områder forbinde med hinanden og skåne den umiddelbare subpleural lunge; dette er typisk for bronchiectasis. Klik her for at se en større version af dette tal.
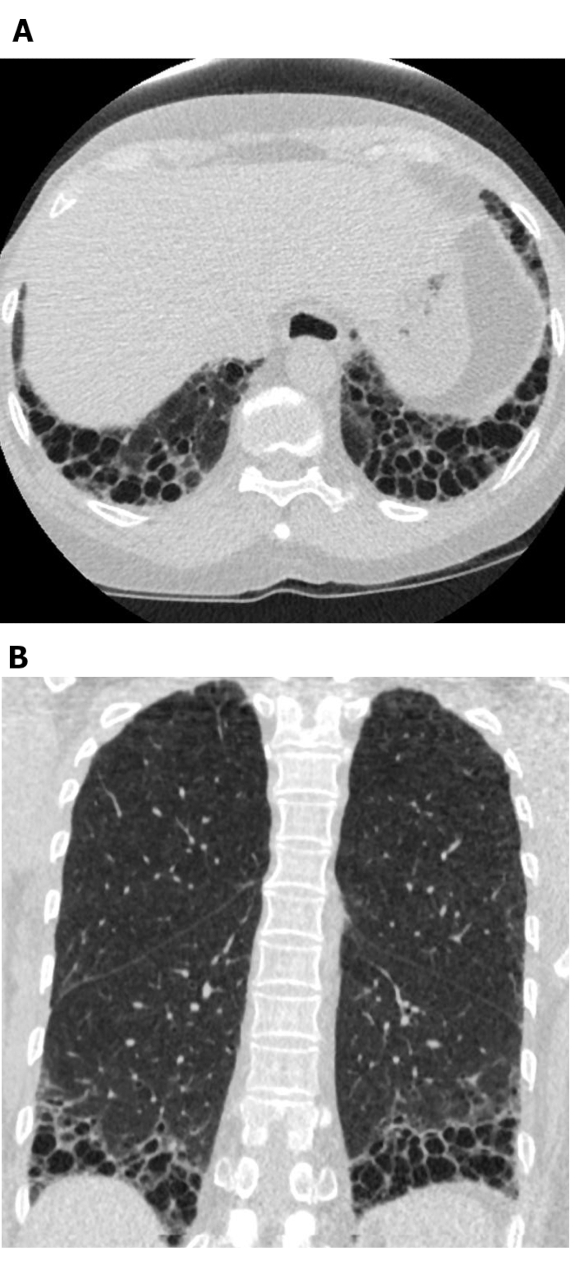
Figur 5: Systemisk sklerose med et UIP-mønster af lungefibrose. Aksial (A) og koronale (B) computertomografi billeder viser perifere og basale fremherskende honeycombing og trækkraft bronchiectasis i overensstemmelse med den typiske UIP mønster af lungefibrose. Bemærk den udvidede spiserøret (kan henføres til sklerodermi) og den "sprudlende" honeycombing (hvilket tyder på ILD relateret til bindevævssygdom snarere end idiopatisk lungefibrose). UIP = sædvanlig interstitiel lungebetændelse. Klik her for at se en større version af dette tal.
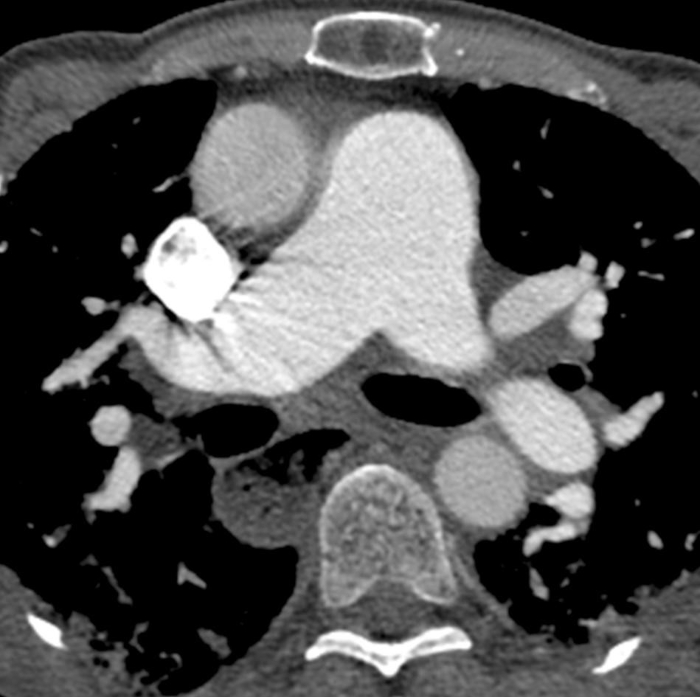
Figur 6: Systemisk sklerose med pulmonal hypertension og udvidet spiserøret. Kontrast-forbedret bryst computertomografi viser markant udvidelse af pulmonal stammen, med en større måling end den tilstødende stigende aorta, der tyder på underliggende pulmonal hypertension. Spiserøret er markant udvidet; dette kan henføres til sklerodermi. Klik her for at se en større version af dette tal.
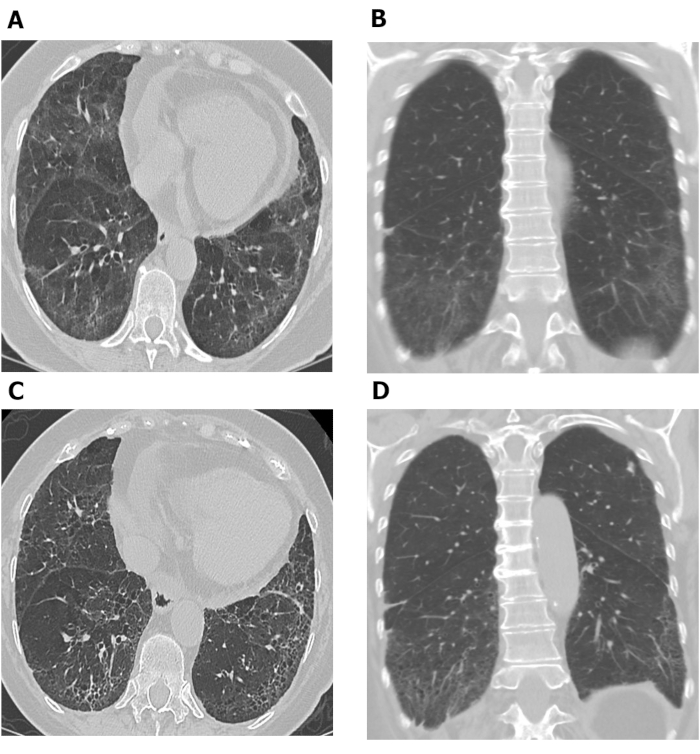
Figur 7: Seriel bryst HRCT billeder viser progression af lungefibrose hos patient med SSc-ILD. Aksial (A) og koronale (B) billeder fra brystet HRCT viser basilar fremherskende jord-glas opacitet og reticulation med mild trækkraft bronchiectasis og subpleural besparelse i overensstemmelse med ikke-specifikke interstitielle lungebetændelse hos denne patient med SSc. Efter 10 år, øget reticulation og trækkraft bronkiolectasis på lungebaser med fald i jord-glas opacitet er observeret på aksial (C) og koronale (D) brystet HRCT billeder, i overensstemmelse med mild forværring af lungefibrose. HRCT = computertomografi med høj opløsning; SSc-ILD = systemisk sklerodermi-associeret interstitiel lungesygdom. Klik her for at se en større version af dette tal.
Mens HRCT er i øjeblikket den endelige billeddannelse metode til diagnosticering og vurdering af SSc-ILS, det bruger ioniserende stråling og er relativt dyrt. Røntgenbilleder af brystkassen kan foretages i stedet, selv om disse ikke fremmer differentialdiagnosticering i samme omfang som HRCT, og en normal røntgenbillede af brystet eliminerer ikke muligheden for ILS. Måske den bedste brug af røntgenbilleder af brystet er at overvåge for progressiv sygdom mellem HRCT scanninger og for udelukkelse af komplicerende sygdom, såsom infektiøs lungebetændelse, i forbindelse med akut forværring af symptomer.
En opfattet begrænsning af HRCT er stråling. Som beskrevet tidligere, nye metoder til at gennemføre CT-scanninger kan gøre det muligt stråling eksponering, der skal reduceres31,og desuden, nuværende CT-scannere giver en række avancerede teknikker, der giver mulighed for i fremtiden at sænke stråling eksponering for næsten bryst røntgenbillede niveauer. Alternativt kan billeddannelsesmetoder såsom MR- eller lungeultralyd potentielt anvendes for at undgå at udsætte patienten for stråling i fremtiden32,,71,,72,73. Vi mener, at selv om der er fordele og risici i forbindelse med billedbehandlingsudnyttelse, opvejer fordelene ved CT i diagnosticering og patienthåndtering langt de potentielle risici.
Billeddata, især HRCT, giver uden tvivl de vigtigste oplysninger, der gør det muligt at diagnosticere SSc-ILS. En detaljeret overvejelse af mønstre og karakteristika ved HRCT-scanninger er normalt tilstrækkelig til at skelne SSc-I fra andre lungesygdomme med den fordel, at man undgår behovet for en invasiv biopsiprocedure.
Visuel vurdering af HRCT-scanninger indfører en vis subjektivitet og muligheden for variation mellem observatører. Computerbaserede metoder til fortolkning af MENCT-scanninger er blevet undersøgt som en mulig metode til at forbedre nøjagtigheden63,74. F.eks. kan kvantitative tilgange til vurdering af lungefibrose eller sygdomsniveauet anvendes til at vurdere behandlingsrespons68,70,75. Men, disse metoder er ikke almindeligt anvendt i daglig klinisk praksis på dette tidspunkt.
Vi håber, at de oplysninger, der præsenteres i dette manuskript vil tjene som en praktisk vejledning til at hjælpe læger med at bruge HRCT scanninger til diagnosticering SSc-ILD og bestemme prognose. Forbedrede metoder til at opnå billeder og til tolkning har potentiale til at reducere patienternes eksponering for stråling og forbedre diagnostisk/prognostisk nøjagtighed.
Jonathan Chung erklærer ingen potentielle interessekonflikter med hensyn til den beskrevne forskning, forfatterskab, og / eller offentliggørelse af denne artikel; Christopher Walker erklærer modtagelsen af royalties fra Amirsys (Elsevier); og Stephen Hobbs erklærer modtagelsen af royalties fra Elsevier og Wolters Kluwer Health. Open Access offentliggørelse af denne artikel er sponsoreret af Boehringer Ingelheim Pharmaceuticals, Inc.
Forfatteren(e) opfylder kriterierne for forfatterskab som anbefalet af International Committee of Medical Journal Editors (ICMJE). Forfatterne modtog ingen direkte kompensation i forbindelse med udviklingen af videoen. Medicinsk skrivning støtte til video script blev leveret af Leon Newman, ph.d., af GeoMed, en Ashfield selskab, som blev indgået og finansieret af Boehringer Ingelheim Pharmaceuticals, Inc. (BIPI). BIPI fik mulighed for at gennemgå den endelige video for medicinsk og videnskabelig nøjagtighed samt intellektuelle ejendomsrettigheder overvejelser.
Forfatterne opfylder kriterierne for forfatterskab som anbefalet af International Committee of Medical Journal Editors (ICMJE). Forfatterne modtog ingen direkte kompensation i forbindelse med udviklingen af manuskriptet. Skriftlig bistand blev ydet af Ken Sutor, BSc, af GeoMed, en Ashfield selskab, en del af UDG Healthcare plc, som blev indgået og finansieret af Boehringer Ingelheim Pharmaceuticals, Inc. (BIPI). BIPI fik mulighed for at gennemgå manuskriptet for medicinsk og videnskabelig nøjagtighed samt hensyn til intellektuel ejendomsret.
| Name | Company | Catalog Number | Comments |
| CT scanners | Philips | NA | Multiple |
- Denton, C. P., Khanna, D. Systemic sclerosis. Lancet. 390 (10103), 1685-1699 (2017).
- Arnett, F. C., et al. Familial occurrence frequencies and relative risks for systemic sclerosis (scleroderma) in three United States cohorts. Arthritis & Rheumatism. 44 (6), 1359-1362 (2001).
- Barnes, J., Mayes, M. D. Epidemiology of systemic sclerosis: incidence, prevalence, survival, risk factors, malignancy, and environmental triggers. Current Opinion in Rheumatology. 24 (2), 165-170 (2012).
- Marie, I., Gehanno, J. F. Environmental risk factors of systemic sclerosis. Seminars in Immunopathology. 37 (5), 463-473 (2015).
- Silman, A. J. Epidemiology of scleroderma. Annals of the Rheumatic Diseases. 50, 846-853 (1991).
- Scholand, M. B., et al. Interstitial lung disease in systemic sclerosis: diagnosis and management. Rheumatology. 1, 008 (2012).
- Solomon, J. J., et al. Scleroderma lung disease. European Respiratory Review. 22 (127), 6-19 (2013).
- Walker, U. A., et al. Clinical risk assessment of organ manifestations in systemic sclerosis: a report from the EULAR Scleroderma Trials And Research group database. Annals of the Rheumatic Diseases. 66 (6), 754-763 (2007).
- Hinchcliff, M., Fischer, A., Schiopu, E., Steen, V. D., Investigators, P. Pulmonary hypertension assessment and recognition of outcomes in scleroderma (PHAROS): baseline characteristics and description of study population. The Journal of Rheumatology. 38 (10), 2172-2179 (2011).
- Giacomelli, R., et al. Interstitial lung disease in systemic sclerosis: current and future treatment. Rheumatology International. 37 (6), 853-863 (2017).
- Sanchez-Cano, D., et al. Interstitial lung disease in systemic sclerosis: data from the spanish scleroderma study group. Rheumatology International. 38 (3), 363-374 (2018).
- Silver, K. C., Silver, R. M. Management of systemic-sclerosis-associated interstitial lung disease. Rheumatic Diseases Clinics of North America. 41 (3), 439-457 (2015).
- Fischer, A., Kong, A. M., Swigris, J. J., Cole, A. L., Raimundo, K. All-cause healthcare costs and mortality in patients with systemic sclerosis with lung involvement. The Journal of Rheumatology. 45 (2), 235-241 (2018).
- Tyndall, A. J., et al. Causes and risk factors for death in systemic sclerosis: a study from the EULAR Scleroderma Trials and Research (EUSTAR) database. Annals of the Rheumatic Diseases. 69 (10), 1809-1815 (2010).
- Herzog, E. L., et al. Review: interstitial lung disease associated with systemic sclerosis and idiopathic pulmonary fibrosis: how similar and distinct. Arthritis & Rheumatology. 66 (8), 1967-1978 (2014).
- Rubio-Rivas, M., Royo, C., Simeon, C. P., Corbella, X., Fonollosa, V. Mortality and survival in systemic sclerosis: systematic review and meta-analysis. Seminars in Arthritis and Rheumatism. 44 (2), 208-219 (2014).
- Stock, C., et al. Serum KL-6 as a marker of disease progression in SSc-ILD. European Respiratory Journal. 52, (2018).
- Winstone, T. A., et al. Predictors of mortality and progression in scleroderma-associated interstitial lung disease: a systematic review. Chest. 146 (2), 422-436 (2014).
- Khanna, D., et al. Ongoing clinical trials and treatment options for patients with systemic sclerosis-associated interstitial lung disease. Rheumatology (Oxford). 58 (4), 567-579 (2019).
- Behr, J., Furst, D. E. Pulmonary function tests. Rheumatology (Oxford). 47, 65-67 (2008).
- Hax, V., et al. Clinical algorithms for the diagnosis and prognosis of interstitial lung disease in systemic sclerosis. Seminars in Arthritis and Rheumatism. 47 (2), 228-234 (2017).
- Molberg, O., Hoffmann-Vold, A. M. Interstitial lung disease in systemic sclerosis: progress in screening and early diagnosis. Current Opinion in Rheumatology. 28 (6), 613-618 (2016).
- Raghu, G., Goldman, L., Schafer, A. I. Interstital lung disease. Goldman-Cecil Medicine. , 575-588 (2016).
- Showalter, K., et al. Performance of forced vital capacity and lung diffusion cutpoints for associated radiographic interstitial lung disease in systemic sclerosis. The Journal of Rheumatology. 45 (11), 1572-1576 (2018).
- Suliman, Y. A., et al. Brief report: pulmonary function tests: high rate of false-negative results in the early detection and screening of scleroderma-related interstitial lung disease. Arthritis & Rheumatology. 67 (12), 3256-3261 (2015).
- Roth, M. D., et al. Predicting treatment outcomes and responder subsets in scleroderma-related interstitial lung disease. Arthritis & Rheumatology. 63 (9), 2797-2808 (2011).
- Kalra, M. K., Maher, M. M., Rizzo, S., Kanarek, D., Shepard, J. A. Radiation exposure from chest CT: issues and strategies. Journal of Korean Medical Science. 19 (2), 159-166 (2004).
- Siegel, J. A., Pennington, C. W., Sacks, B., Welsh, J. S. The birth of the illegitimate linear no-threshold model: an invalid paradigm for estimating risk following low-dose radiation exposure. American Journal of Clinical Oncology. 41 (2), 173-177 (2018).
- Frauenfelder, T., et al. Screening for interstitial lung disease in systemic sclerosis: performance of high-resolution CT with limited number of slices: a prospective study. Annals of the Rheumatic Diseases. 73 (12), 2069-2073 (2014).
- Kubo, T., et al. Radiation dose reduction in chest CT: a review. American Journal of Roentgenology. 190 (2), 335-343 (2008).
- Nguyen-Kim, T. D. L., et al. The impact of slice-reduced computed tomography on histogram-based densitometry assessment of lung fibrosis in patients with systemic sclerosis. Journal of Thoracic Disease. 10 (4), 2142-2152 (2018).
- Muller, C. S., Warszawiak, D., Paiva, E. D. S., Escuissato, D. L. Pulmonary magnetic resonance imaging is similar to chest tomography in detecting inflammation in patients with systemic sclerosis. Revista Brasileira de Reumatologia English Edition. 57 (5), 419-424 (2017).
- Pinal-Fernandez, I., et al. Fast 1.5 T chest MRI for the assessment of interstitial lung disease extent secondary to systemic sclerosis. Clinical Rheumatology. 35 (9), 2339-2345 (2016).
- Sverzellati, N. Highlights of HRCT imaging in IPF. Respiratory Research. 14, 3 (2013).
- Lynch, D. A., et al. Diagnostic criteria for idiopathic pulmonary fibrosis: a Fleischner Society White Paper. The Lancet Respiratory Medicine. 6 (2), 138-153 (2018).
- Raghu, G., et al. Diagnosis of idiopathic pulmonary fibrosis. An official ATS/ERS/JRS/ALAT clinical practice guideline. American Journal of Respiratory and Critical Care Medicine. 198 (5), 44-68 (2018).
- . Exam: CT thorax for interstitial lung disease Available from: https://www.pulmonaryfibrosis.org/docs/default-source/medical-community-documents/ct-chest-for-ild-protocol.pdf?sfvrsn=0 (2019)
- Doyle, T. J., Hunninghake, G. M., Rosas, I. O. Subclinical interstitial lung disease: why you should care. American Journal of Respiratory and Critical Care Medicine. 185 (11), 1147-1153 (2012).
- Peroni, D. G., Boner, A. L. Atelectasis: mechanisms, diagnosis and management. Paediatric Respiratory Reviews. 1 (3), 274-278 (2000).
- Branley, H. M. Pulmonary fibrosis in systemic sclerosis: diagnosis and management. Respiratory Medicine CME. 3, 10-14 (2010).
- Engeler, C. E., Tashjian, J. H., Trenkner, S. W., Walsh, J. W. Ground-glass opacity of the lung parenchyma: a guide to analysis with high-resolution CT. American Journal of Roentgenology. 160 (2), 249-251 (1993).
- Goldin, J. G., et al. High-resolution CT scan findings in patients with symptomatic scleroderma-related interstitial lung disease. Chest. 134 (2), 358-367 (2008).
- Strollo, D., Goldin, J. Imaging lung disease in systemic sclerosis. Current Rheumatology Reports. 12 (2), 156-161 (2010).
- Pandey, A. K., et al. Significance of various pulmonary and extrapulmonary abnormalities on HRCT of the chest in scleroderma lung. Indian Journal of Radiology and Imaging. 23 (4), 304-307 (2013).
- Chung, J. H., et al. CT Features of the usual interstitial pneumonia pattern: differentiating connective tissue disease-associated interstitial lung disease from idiopathic pulmonary fibrosis. American Journal of Roentgenology. 210 (2), 307-313 (2018).
- Zhan, X., et al. Differentiating usual interstitial pneumonia from nonspecific interstitial pneumonia using high-resolution computed tomography: the "Straight-edge Sign". Journal of Thoracic Imaging. 33 (4), 266-270 (2018).
- Farrokh, D., Abbasi, B., Fallah-Rastegar, Y., Mirfeizi, Z. The extrapulmonary manifestations of systemic sclerosis on chest high resolution computed tomography. Tanaffos. 14 (3), 193-200 (2015).
- Salaffi, F., et al. Relationship between interstitial lung disease and oesophageal dilatation on chest high-resolution computed tomography in patients with systemic sclerosis: a cross-sectional study. La Radiologia Medica. 123 (9), 655-663 (2018).
- Vonk, M. C., et al. Oesophageal dilatation on high-resolution computed tomography scan of the lungs as a sign of scleroderma. Annals of the Rheumatic Diseases. 67 (9), 1317-1321 (2008).
- Chowaniec, M., Skoczynska, M., Sokolik, R., Wiland, P. Interstitial lung disease in systemic sclerosis: challenges in early diagnosis and management. Reumatologia. 56 (4), 249-254 (2018).
- McCall, R. K., Ravenel, J. G., Nietert, P. J., Granath, A., Silver, R. M. Relationship of main pulmonary artery diameter to pulmonary arterial pressure in scleroderma patients with and without interstitial fibrosis. Journal of Computer Assisted Tomography. 38 (2), 163-168 (2014).
- Pandey, A. K., et al. Predictors of pulmonary hypertension on high-resolution computed tomography of the chest in systemic sclerosis: a retrospective analysis. Canadian Association of Radiologists Journal. 61 (5), 291-296 (2010).
- Raymond, T. E., Khabbaza, J. E., Yadav, R., Tonelli, A. R. Significance of main pulmonary artery dilation on imaging studies. Annals of the American Thoracic Society. 11 (10), 1623-1632 (2014).
- Colaci, M., et al. Lung cancer in scleroderma: results from an Italian rheumatologic center and review of the literature. Autoimmunity Reviews. 12 (3), 374-379 (2013).
- Distler, O., et al. Design of a randomised, placebo-controlled clinical trial of nintedanib in patients with systemic sclerosis-associated interstitial lung disease (SENSCIS). Clinical and Experimental Rheumatology. 35 (4), 75-81 (2017).
- Desai, S. R., et al. CT features of lung disease in patients with systemic sclerosis: comparison with idiopathic pulmonary fibrosis and nonspecific interstitial pneumonia. Radiology. 232 (2), 560-567 (2004).
- Mira-Avendano, I., et al. Interstitial lung disease and other pulmonary manifestations in connective tissue diseases. Mayo Clinic Proceedings. 94 (2), 309-325 (2019).
- Walkoff, L., White, D. B., Chung, J. H., Asante, D., Cox, C. W. The four corners sign: a specific imaging feature in differentiating systemic sclerosis-related interstitial lung disease from idiopathic pulmonary fibrosis. Journal of Thoracic Imaging. 33 (3), 197-203 (2018).
- Kotnur, M. R., Suresh, P., Reddy, V. S., Sharma, T., Salim, N. A. Systemic sclerosis with multiple pulmonary manifestations. Journal of Clinical & Diagnostic Research. 10 (6), 16-17 (2016).
- Goh, N. S., et al. Interstitial lung disease in systemic sclerosis: a simple staging system. American Journal of Respiratory and Critical Care Medicine. 177 (11), 1248-1254 (2008).
- Takei, R., et al. Radiographic fibrosis score predicts survival in systemic sclerosis-associated interstitial lung disease. Respirology. 23 (4), 385-391 (2018).
- Bakker, M. E., et al. Lung density and pulmonary artery diameter are predictors of pulmonary hypertension in systemic sclerosis. Journal of Thoracic Imaging. 32 (6), 391-397 (2017).
- Khanna, D., et al. Predictors of lung function decline in scleroderma-related interstitial lung disease based on high-resolution computed tomography: implications for cohort enrichment in systemic sclerosis-associated interstitial lung disease trials. Arthritis Research & Therapy. 17, 372 (2015).
- Ariani, A., et al. Quantitative chest computed tomography is associated with two prediction models of mortality in interstitial lung disease related to systemic sclerosis. Rheumatology (Oxford). 56 (6), 922-927 (2017).
- Goldin, J., et al. Treatment of scleroderma-interstitial lung disease with cyclophosphamide is associated with less progressive fibrosis on serial thoracic high-resolution CT scan than placebo: findings from the scleroderma lung study. Chest. 136 (5), 1333-1340 (2009).
- Tashkin, D. P., et al. Mycophenolate mofetil versus oral cyclophosphamide in scleroderma-related interstitial lung disease (SLS II): a randomised controlled, double-blind, parallel group trial. The Lancet Respiratory Medicine. 4 (9), 708-719 (2016).
- Distler, O., et al. Nintedanib for Systemic Sclerosis-Associated Interstitial Lung Disease. New England Journal of Medicine. 380, 2518-2528 (2019).
- Cappelli, S., et al. Interstitial lung disease in systemic sclerosis: where do we stand. European Respiratory Review. 24 (137), 411-419 (2015).
- Goldin, J. G., et al. Longitudinal changes in quantitative interstitial lung disease on CT after immunosuppression in the Scleroderma Lung Study II. Annals of the American Thoracic Society. 5 (11), 1286-1295 (2018).
- Wangkaew, S., Euathrongchit, J., Wattanawittawas, P., Kasitanon, N. Correlation of delta high-resolution computed tomography (HRCT) score with delta clinical variables in early systemic sclerosis (SSc) patients. Quantitative Imaging in Medicine and Surgery. 6 (4), 381-390 (2016).
- Kim, H. J., et al. Transitions to different patterns of interstitial lung disease in scleroderma with and without treatment. Annals of the Rheumatic Diseases. 75 (7), 1367-1371 (2016).
- Tardella, M., et al. Ultrasound B-lines in the evaluation of interstitial lung disease in patients with systemic sclerosis: cut-off point definition for the presence of significant pulmonary fibrosis. Medicine (Baltimore). 97 (18), 0566 (2018).
- Hassan, R. I., et al. Lung ultrasound as a screening method for interstitial lung disease in patients with systemic sclerosis. Journal of Clinical Rheumatology. , (2018).
- Wang, Y., Gargani, L., Barskova, T., Furst, D. E., Cerinic, M. M. Usefulness of lung ultrasound B-lines in connective tissue disease-associated interstitial lung disease: a literature review. Arthritis Research & Therapy. 19 (1), 206 (2017).
- Ariani, A., et al. Quantitative CT indexes are significantly associated with exercise oxygen desaturation in interstitial lung disease related to systemic sclerosis. The Clinical Respiratory Journal. 11 (6), 983-989 (2017).
- Kim, H. J., et al. Quantitative texture-based assessment of one-year changes in fibrotic reticular patterns on HRCT in scleroderma lung disease treated with oral cyclophosphamide. European Radiology. 21 (12), 2455-2465 (2011).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved