Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Medicine
Bildeegenskaper ved systemisk sklerose-assosiert interstitiell lungesykdom
Her presenterer vi praktiske anbefalinger for å utføre thorax høyoppløselig computertomografi for diagnost ing og vurdering av systemisk skleroserelatert interstitiell lungesykdom.
Tidlig diagnose av systemisk skleroserelatert interstitiell lungesykdom (SSc-ILD) er viktig for at behandlingen skal kunne administreres med minimal forsinkelse. Diagnostising av SSc-ILD er imidlertid utfordrende fordi viktige symptomer ikke er spesifikke. Høyoppløselig computertomografi (HRCT) på brystet er anerkjent som en sensitiv bildemetode for diagnosting og vurdering av SSc-ILD. Eksponering av pasienter for ioniserende stråling kan betraktes som en begrensning, selv om metodiske skritt kan tas for å moderere dette. Vi presenterer praktiske anbefalinger for å utføre HRCT-skanninger og tolke resultatene. Viktige funksjoner i SSc-ILD på HRCT inkluderer et ikke-spesifikt interstitiell pneumoni (NSIP) mønster med perifere bakkeglassforstyrrelser og omfattende trekkraft bronkiektasi. Til tross for likheter mellom SSc-ILD og idiopatisk lungefibrose (IPF), kan HRCT brukes til å skille mellom disse forholdene: i SSc-ILD sammenlignet med IPF er det en større andel av jordglasstetthet og fibrose er mindre grov. En utvidet, luftfylt spiserør med diameter > 10 mm, noe som tyder på esophageal dysmotilitet er ofte sett i SSc-ILD. Pulmonal arterie størrelse større enn tilstøtende stigende aorta antyder samtidig pulmonal hypertensjon. Knuter må overvåkes på grunn av økt risiko for lungekreft. Et stort omfang av sykdom ved HRCT (≥20 %) eller en høy fibrose score antyder en økt risiko for dødelighet. HRCT er sentral for å diagnostisere SSc-ILD, og serielle vurderinger kan være nyttige for å overvåke sykdomsprogresjon eller behandlingsrespons.
Systemisk sklerose (SSc) er en kompleks, heterogen, autoimmun sykdom. Det kan manifesteres som vaskulopati, Raynauds fenomen og fibrose i huden og indre organer1. SSc er klassifisert i undertyper som følger: begrenset kutan, diffus kutan, sinus sklerodermi (uten hudinvolvering), og SSc overlapping syndrom1.
SSc er ikke arvet i mendelian mote, men genetiske faktorer synes å påvirke mottakelighet for sykdommen. Forekomsten varierer mellom etniske grupper og økes blant personer med en familiehistorie av sykdommen2,3. Miljømessige risikofaktorer synes også å eksistere, med høy eksponering for silika eller organiske løsemidler som ser ut til å øke forekomsten av SSc4. Den globale utbredelsen av SSc er rundt 1 av 10.0001. Flere kvinner enn menn påvirkes av SSc, med rapporterte kvinner:mannlige forhold mellom 3:1 og 8:1, og aldersgruppen med høyest forekomst av sykdommen er 45-54 år5.
Lungen er det nest mest berørte viscerale organet hos pasienter med SSc6. Det er to hovedpulmonal manifestasjoner av SSc: interstitiell lungesykdom (ILD), og pulmonal hypertensjon7. ILD er vanligvis fibrotisk; det forekommer hos ca 80% av pasientene med SSc og er mer vanlig i diffust kutan sklerodermi enn i den begrensede formen av sykdommen1,8. Pulmonal hypertensjon kan manifestere seg som isolert pulmonal arteriell hypertensjon (PAH, som har en prevalens på 13–35 % i SSc) eller pulmonal hypertensjon som følge av venstre ventrikulær involvering/diastolisk dysfunksjon eller ILD/hypoksemi7. Antistoffprofiler varierer mellom pasienter med SSc-ILD og de med SSc-PAH. For eksempel er tilstedeværelsen av anti-Scl-70 antistoffer forbundet med SSc-ILD8, mens anticentromere antistoffer er mer vanlig hos SSc-pasienter med PAH enn hos de uten PAH9.
Symptomene på SSc-ILD inkluderer dyspné, hoste, brystsmerter og treningsbegrensning. ILD er en viktig bidragsyter til sykelighet i SSc10,11,12. Som en konsekvens har årlige all-cause helsekostnader blitt rapportert å være høyere hos pasienter med SSc-ILD enn hos de med SSc og ingen ILD: $ 31 285-55 446 versus $ 18 513-23 268, henholdsvis13.
SSc-ILD er den viktigste årsaken til dødelighet hos pasienter med SSc, og står for 30–35 % av dødsfallene i denne gruppen10,,14. Median overlevelse blant pasienter med SSc-ILD er rapportert å være 5–8 år10,,15; til sammenligning overlever ca. 76% av den totale befolkningen med SSc i mer enn 10 år fra sykdomsutbrudd16. Signifikante prediktorer for dødelighet i SSc-ILD inkluderer alder, tvungen vital kapasitet (FVC), lungemengdekapasitet ved baseline for karbonmonoksid (DLCO), sykdomsomfang på høyoppløselig computertomografi (HRCT), tilstedeværelse av pulmonal hypertensjon og nivåer av Kerbs von den Lungren 6 (KL-6) antigen17,,18.
Tidlig diagnose er viktig for at behandlingen skal kunne administreres med minimal forsinkelse, og hos pasienter med progressiv fenotype kan sykdomsprogresjonen potensielt reduseres. Diagnostising av SSc-ILD er imidlertid utfordrende fordi ikke-spesifikke symptomer på hoste, dyspné og tretthet kan forveksles med andre aspekter ved SSc, som hjertesykdom og muskel-skjelettinvolvering. Evalueringer for diagnosting av ILDer inkluderer: klinisk presentasjon, historie, røykestatus, lungefunksjon, bildebehandling, og i noen tilfeller lungebiopsi. Bekreftelse av SSc-ILD diagnose krever flere undersøkelser, som ofte brukes i kombinasjon19. De mest brukte vurderingene inkluderer lungefunksjonstester og HRCT20,,21,22,,23. Andre bildemetoder, som brystradiografi og strålingssparende avbildning (f.eks. magnetisk resonansavbildning [MR], lunge ultralyd) kan også brukes22. Lungefunksjonstester brukes til å vurdere alvorlighetsgraden av ILD og overvåke kurset. Bruk av lungefunksjonstester alene er imidlertid av begrenset bruk for diagnosting av SSc-ILD24,25. HRCT av brystet er sett på som den mest følsomme ikke-invasive måten å tilrettelegge differensial diagnose av SSc-ILD19. Baseline HRCT resultater, samt endringer over tid, kan brukes til å forutsi fremtidig løpet av lungesykdom og potensiell respons på terapi26.
Eksponering for stråling med HRCT anses noen ganger som en begrensende faktor for regelmessig screening27,,28; begrense antall skiver er en potensiell metode for å redusere strålingsrisikoen, og dosen kan også reduseres ved å redusere enten spenningen eller strømmen29,,30,31. Alternativt kan ulike vurderingsmetoder vurderes. Mr ser for eksempel ut til å ha et potensial for evaluering og oppfølging av ILD-pasienter22. I en studie ved hjelp av T2-vektede MR-bilder med respiratorisk synkronisering, ble HRCT utført parallelt som "gullstandard"-vurderingen; 100 % følsomhet og 60 % spesifisitet ble rapportert med MR for å bestemme tilstedeværelsen av ILD32. Lignende avtale mellom MR og HRCT i deteksjon og kategorisering av ILD ble rapportert i en annen studie33. Til tross for de lovende resultatene, er MR for tiden en forskningsmetodikk, og det er ennå ikke klart for generalisert klinisk bruk.
Her gir vi en praktisk oversikt over tolkningen av bilderesultater, med fokus på HRCT, for å diagnostisere lungeinvolvering i SSc, bestemme prognose, og også utforske fremtidige utviklinger som kan forbedre bildemetoder og tolkning av resultater. HRCT-bilder fra representative saker er inkludert i avisen.
1. HRCT-skanning
- Utfør volumetrisk HRCT-anskaffelsesskanning av brystet36. Kontrastmidler er ikke nødvendig36,37.
- Få følgende anskaffelser med parametere som vises i tabell 136,37.
- Få en liggende inspiratorisk skanning (volumetrisk) fra lungebilder til lungebasen.
- Få en liggende ekspiratorisk skanning (sekvensiell med 10–20 mm hull) fra 2 cm under lungebilder til lungebasen.
- Få en utsatt inspiratorisk valgfri (sekvensiell med 10–20 mm hull) fra karina til lungebasen.
- Gi pusteinstruksjoner til pasienten før hvert oppkjøp36,37. For en inspiratorisk skanning, si "Ta i et dypt åndedrag .... og la det ut. Ta inn et nytt dypt åndedrag .... og slipp det ut. Ta inn et nytt dypt åndedrag, og hold pusten i. Hold pusten"37.
- Få inspiratoriske skanninger med full inspirasjon35,36.
- Bruk den tynneste collimation, korteste rotasjonstid og høyeste tonehøyde for å sikre at bevegelsesfrie bilder oppnås36. Foreslåtte skanneparametere er beskrevet i tabell 137.
- For optimal kvalitet på volumetriske skanninger, få tynne snitt (<2 mm) bilder med høy romlig oppløsning rekonstruksjon35,,36.
- Gjennomgå skanninger umiddelbart etter oppkjøpet og gjenta hvis enten bevegelse artefakt er til stede eller utilstrekkelig inspirasjon har skjedd37.
2. Rapportering
- Klargjør en tolkende rapport.
- Del rapporten og HRCT-bildene med pasientens omsorgsteam og legg dem til i pasientens medisinske journaler.
Diagnose
Viktige funksjoner i SSc-ILD på HRCT inkluderer vanligvis et ikke-spesifikt interstitiell pneumoni (NSIP) mønster med perifere bakkeglassforstyrrelser og omfattende trekkraft bronkiektasi (figur 1 og figur 2). Jordglass opacities har en bred etiologi og er ofte ikke-spesifikke40,41,42. Sentral overvekt eller perifer distribusjon med subpleural sparing er svært tankevekkende for NSIP (figur 3).
Vanligvis, ILD mønstre i HRCT bilder inkluderer reticulations med arkitektonisk forvrengning resulterer i trekkraft bronkiektasi /bronchiolectasis (i samsvar med en fibrotisk form for NSIP). Faktisk trekkraft bronkiektasi og trekkraft bronkieolectasis er ofte de dominerende funksjonene i SSc-ILD (Figur 4)43. Ytterligere funn kan omfatte honeycombing (Figur 5; mer vanlig i begrensede former for SSc), interlobulære septal fortykning og intralobulære linjer, og mikronodules40,44. Honeycombing refererer til grupperte cystiske luftrom med typisk konsistent diameter (~ 3–10 mm) med tykke, veldefinerte vegger31. Honeycombing og trekkraft bronkiektasi er viktige trekk ved vanlig interstitiell lungebetennelse (UIP) på HRCT. Selv om dette mønsteret er oftest forbundet med idiopatisk lungefibrose (IPF), prototypen fibrosing ILD med en progressiv fenotype, kan det noen ganger ses hos pasienter med SSc-ILD10. Nylig har flere tegn blitt identifisert hos pasienter med bindevevssykdomsrelatert ILD (inkludert SSc-ILD) og UIP-mønsteret på HRCT, men ikke hos personer med IPF. Dette er det rette kanttegnet (dvs. isolering av fibrose til lungebasene med skarp avgrensning i kraniokaudalt plan uten betydelig forlengelse langs lungenes sidemarginer på koronale bilder), honeycombing dominerende (eller sprudlende) tegn (> 70% av fibrotiske deler av lungene), og anterior øvre lobe tegn (dvs. konsentrasjon av fibrose innenfor det fremre aspektet av de øvre fliker, med relativ sparing av de andre aspektene av de øvre fliker, og samtidig lavere lobe involvering)45. Det rette kanttegnet har også vært forbundet med NSIP patologi46, som er det viktigste CT-mønsteret i SSc-ILD10.
Utvidet luftfylt spiserør observeres ofte hos pasienter med SSc (figur 6)47,,48,,49 og hos pasienter med SSc-ILD47,48. Selv om det ikke er akseptert øvre aldersgrense der en utvidet spiserør ikke lenger kan bidra til å skille SSc-ILD og IPF, kan en utvidet spiserør være vanskeligere å tolke hos pasienter over 65 år på grunn av økende forekomst av esophageal motilitetsforstyrrelser. Mediastinal lymfadenopati (vanligvis reaktiv), hvor den korte aksen av lymfeknuten overstiger 10 mm, observeres også ofte hos pasienter med SSc-ILD47,50. Pulmonal arterie størrelse større enn tilstøtende stigende aorta antyder samtidig pulmonal hypertensjon (figur 6), selv hos pasienter uten fibrotisk lungesykdom51,52,53. Områder av konsolidering tyder på overliggende infeksjon, aspirasjon, organisering av lungebetennelse, blødning eller malignitet. Knuter må overvåkes på grunn av økt risiko for lungekreft i SSc-ILD7; den vanligste primære kreften som oppstår hos pasienter med SSc-ILD er adenokarsinom7,54.
SSc-ILD deler en rekke kliniske, mekanistiske og patologiske likheter med IPF15,,55. Noen radilogiske funksjoner tillater imidlertid differensiering av disse to ILDene15,45. I SSc-ILD, sammenlignet med IPF, er det en større andel av bakken-glass opase og fibrose er mindre grov. I tilfeller av UIP i SSc, kan honeycombing observeres i mer enn 70% av fibrotisk-lungevevet ─ det frodige honeycombing-tegnet56,57. I tillegg er firehjørnertegnet (også kjent som det fremre øvre lobetegnet) betydelig mer vanlig i SSc-ILD enn i IPF; Dette er et mønster av betennelse og/eller fibrose fokalt eller uforholdsmessig involverer bilaterale anterolateral øvre fliker og bakre lavere fliker58.
Brystradiografier kan i utgangspunktet oppdage ILD; Men de tilbyr ikke nok kontrastoppløsning for pålitelig diagnose. I brystradiografier fra pasienter med SSc-ILD er det hyppigste mønsteret basal dominerende reticulation59. Ytterligere funksjoner kan omfatte synlig bronkiektasi, volumtap og honeycombing. Som med HRCT kan tilstedeværelsen av en utvidet luftfylt spiserør være nyttig for å støtte diagnosen SSc-ILD47.
Prognose
Flere ulike bildefunn har vist seg å være forbundet med prognose i SSc-ILD. Dødelighetsrisiko er rapportert å være høyere hos pasienter med en sykdomsgrad på minst 20 % på HRCT (10-års overlevelse var henholdsvis 43 % versus 67 %hos pasienter med sykdomsgrad over versus 20 % terskel)60. Tilsvarende har en høy fibrose score på HRCT (basert på omfanget av reticulation og honeycombing) vært forbundet med økt dødelighet61. Store spiserediameter er forbundet med økt ILD-alvorlighetsgrad og redusert DLCO48. Lungetetthet og pulmonal arteriediameter kan potensielt brukes til å forutsi risikoen for pulmonal hypertensjon62. Datastyrte, kvantitative CT-parametere kan også utnyttes for å identifisere pasientenes risiko for nedgang i lungefunksjon eller dødelighet. En studie antydet at omfanget av ILD, kvantifisert fra HRCT, kunne brukes til å forutsi nedgangen i FVC over 12 måneder63. I en annen studie ga kvantitative bryst-CT-parametere dødelighetsrisikoresultater som var i samsvar med kliniske prediksjonsmodeller64. Til tross for deres tilsynelatende potensial, er bildebaserte biomarkører for tiden best vurdert på populasjonsnivå, da deres kliniske nytte hos individuelle pasienter ikke er fastslått.
Respons på behandling
Cyklofosfamid og mykofenolatmofetil gir beskjeden nytte hos pasienter med SSc-ILD. I landemerket Sklerodermi Lungestudie I førte cyklofosfamidbehandling til langsommere progresjon av fibrose sammenlignet med placebo65. Mer nylig rapporterte Scleroderma Lung Study II lignende effekt og forbedret tolerabilitet med mykofenolatmofetil sammenlignet med cyklofosfamid66. Det er imidlertid fortsatt behov for bedre behandlingstilbud for pasienter med SSc-ILD. Behandlinger som for tiden undersøkes inkluderer monoklonale antistoffer (f.eks. rituksimab, abituzumab), antifibrotiske midler (f.eks. nintedanib, pirfenidon), den direkte trombinhemmeren dabigatran, den proteasome inhibitoren bortezomib og hematopoietisk stamcelletransplantasjon19,,67.
Seriell HRCT-skanninger som viser sykdomsprogresjon hos en pasient med SSc-ILD
HRCT-vurderinger som utføres på ulike tidspunkter, kan brukes til å undersøke sykdomsprogresjon. Figur 7 viser to sett med aksiale og koronale hrct-bilder i brystet tatt 10 år fra hverandre hos en pasient med SSc-ILD. De første aksiale og koronale bildene(figur 7A,B)fra brystet HRCT viser basilær dominerende bakkeglass tetthet og reticulation med mild trekkraft bronkiektasi og subpleural sparing i samsvar med NSIP i denne pasienten med SSc. Det siste settet med bilder (Figur 7C, D) tatt 10 år senere, viser økt reticulation og trekkraft bronchiolectasis på lungebasene med reduksjon i bakken-glass tetthet på aksial og koronar (Figur 7C,D) bilder fra brystet CT i samsvar med mild forverring av lungefibrose. Seriell HRCT-skanninger kan også brukes til å overvåke behandlingsresponsen68,,69,,70; dette ble demonstrert i Sklerodermi lungestudie II, hvor dataassistert diagnosescore basert på HRCT-skanninger ble brukt til å sammenligne effekten av cyklofosfamid med mykofenolatmofetil hos pasienter med SSc-ILD68.
| Fase | Detektor koasjonering | Spenning (kV) | Gjeldende (mAs) | Skanne Intervall | Pitch | Rotasjon | Rørstrøm Modulering |
| Supine inspiratorisk | Spiralformet 1,2 mm | 120 (kan senkes) | 230 (kan senkes) | N/a | ~1.0 (1,0) | 0,5 sekunder eller raskere | På |
| Supine ekspiratorisk | Aksial 2 x 1,0 mm | 120 | 150 | 20 mm (20 mm) | N/a | 1,0 sekunder | På |
| Utsatt inspiratorisk | Aksial 2 x 1,0 mm | 120 | 150 | 20 mm (20 mm) | N/a | 1,0 sekunder | På |
Tabell 1: Dataerte parametere for tomografianskaffelse37. I/T = ikke aktuelt.
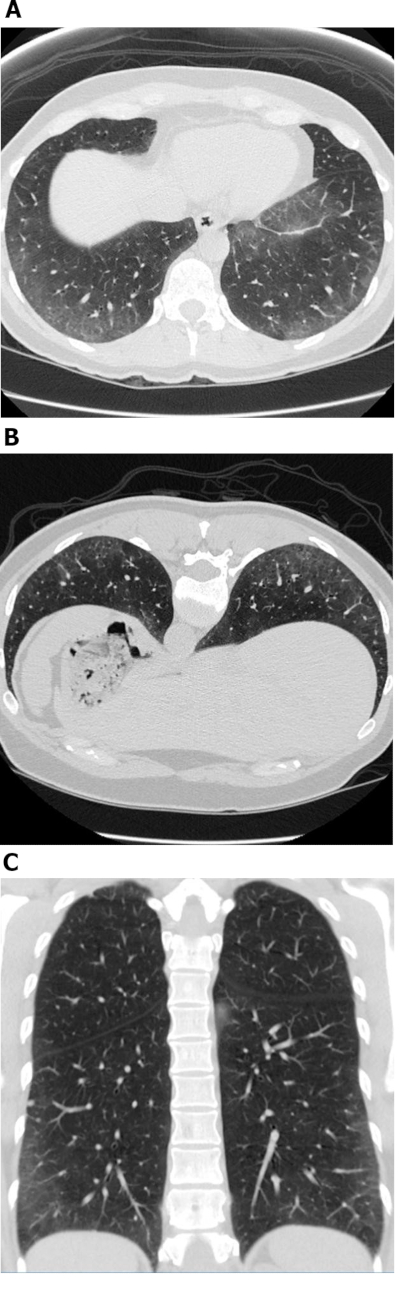
Figur 1: Systemisk sklerose med et cellulært NSIP sykdomsmønster. Aksial (A), utsatt (B) og koronal (C) høyoppløselige datatomografibilder viser alle omfattende perifere og basale dominerende bakkeglassforstyrrelser; dette er typiske observasjoner med NSIP. Mangelen på trekkraft bronkiektasi er antydet av et cellulært NSIP sykdomsmønster. NSIP = ikke-spesifikk interstitiell lungebetennelse. Vennligst klikk her for å se en større versjon av dette tallet.
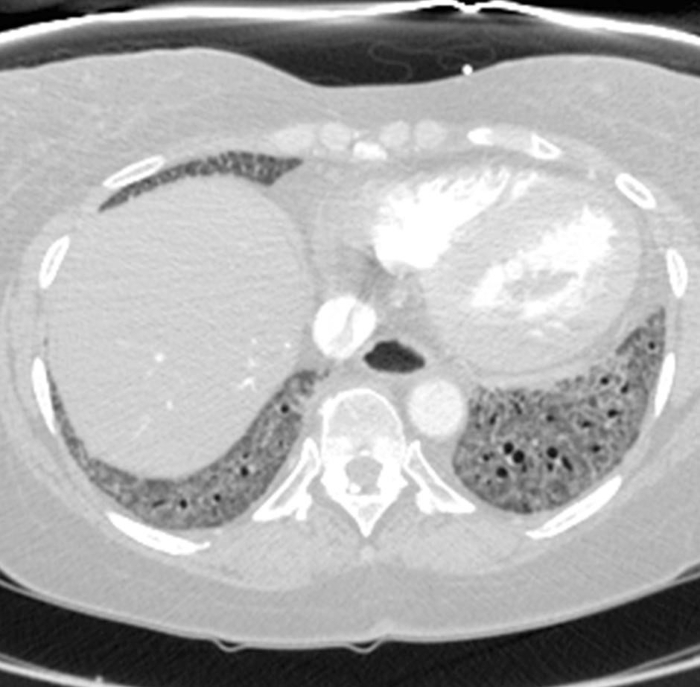
Figur 2: Systemisk sklerose med et fibrotisk ikke-spesifikt interstitiell lungebetennelsemønster av sykdom. Aksial computertomografi bildet viser omfattende, basal-dominerende bakken-glass opacities med tilhørende trekkraft bronkiektasi. Spesielt viser spiserøret merket utvidelse; dette er typisk for sklerodermi. Vennligst klikk her for å se en større versjon av dette tallet.
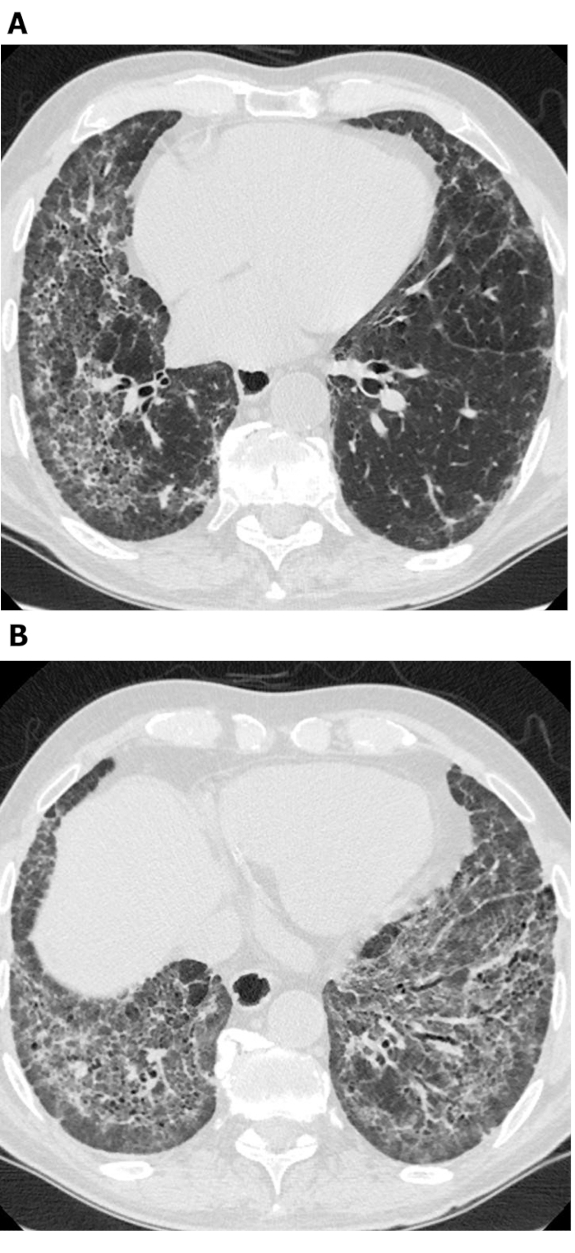
Figur 3: Systemisk sklerose med et fibrotisk NSIP-mønster. Aksiale datatomografibilder med høy oppløsning (A og B) viser omfattende opacities i bakkeglass, reticulation, arkitektonisk forvrengning og trekkraft bronkiektasi. Spesielt er subpleural sparing tydelig; Dette er typisk for NSIP og ses i ca 50% av alle tilfeller. NSIP = ikke-spesifikk interstitiell lungebetennelse. Vennligst klikk her for å se en større versjon av dette tallet.
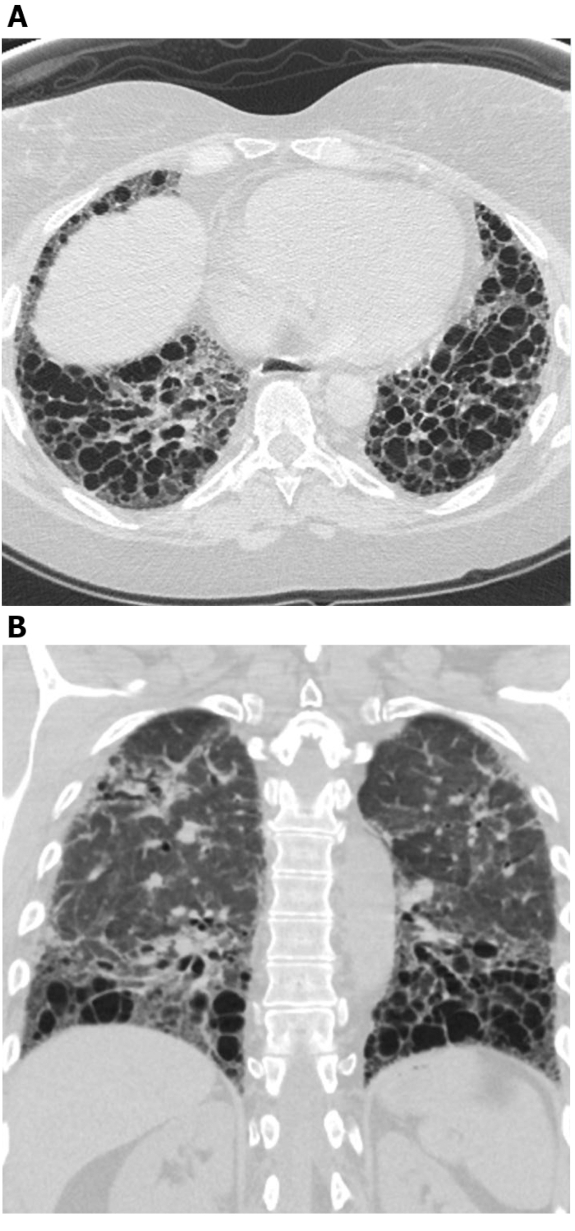
Figur 4: Systemisk sklerose med overstrømmende grepet bronkiektasi. Aksial (A) og koronal (B) høyoppløselige dataografibilder viser omfattende mellom- og nedre lungesone dominerende trekkraft bronkiektasi. Selv om dette kan forveksles med honeycombing, forbinder de cystiske områdene med hverandre og sparer den umiddelbare subpleurallungen; dette er typisk for bronkiektasi. Vennligst klikk her for å se en større versjon av dette tallet.
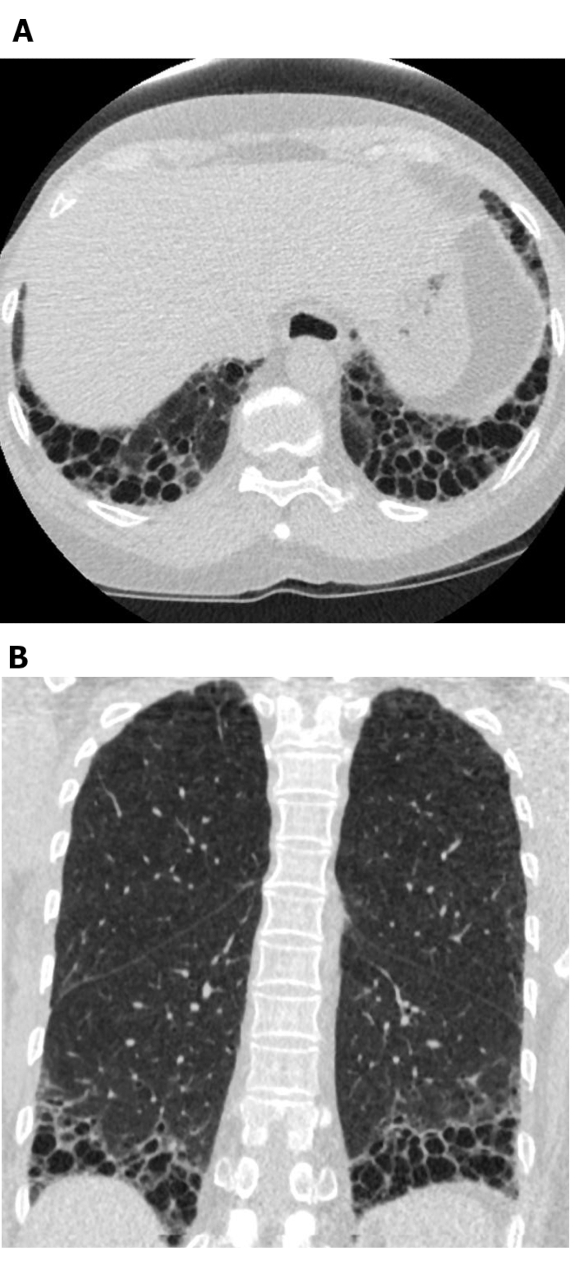
Figur 5: Systemisk sklerose med et UIP-mønster av lungefibrose. Aksial (A) og koronal (B) datatomografibilder viser perifere og basale dominerende honeycombing og trekkraft bronkiektasi i tråd med det typiske UIP-mønsteret av lungefibrose. Legg merke til den utvidede spiserøret (som kan tilskrives sklerodermi) og den "sprudlende" honeycombing (noe som tyder på ILD relatert til bindevevssykdom i stedet for idiopatisk lungefibrose). UIP = vanlig interstitiell lungebetennelse. Vennligst klikk her for å se en større versjon av dette tallet.
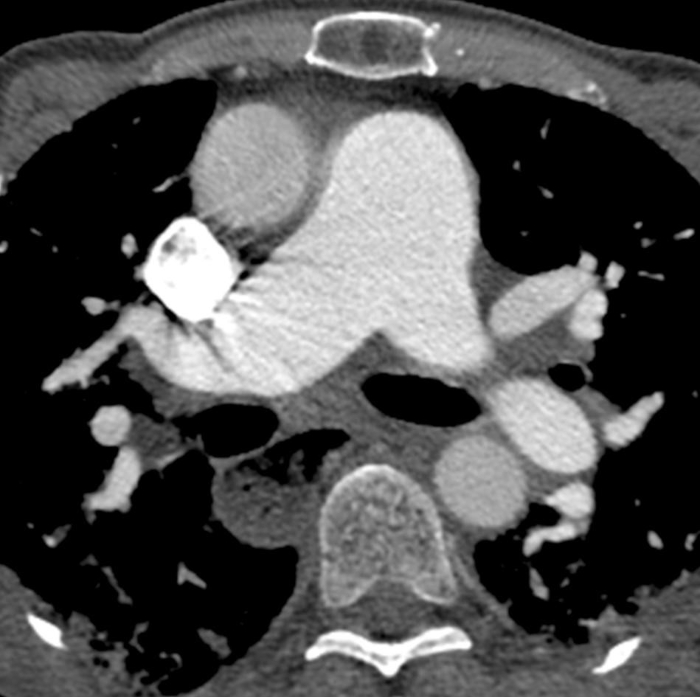
Figur 6: Systemisk sklerose med pulmonal hypertensjon og utvidet spiserør. Kontrastforbedret bryst computertomografi viser markert utvidelse av lungestammen, med en større måling enn tilstøtende stigende aorta som antyder underliggende pulmonal hypertensjon. Spiserøret er markert utvidet; dette kan tilskrives sklerodermi. Vennligst klikk her for å se en større versjon av dette tallet.
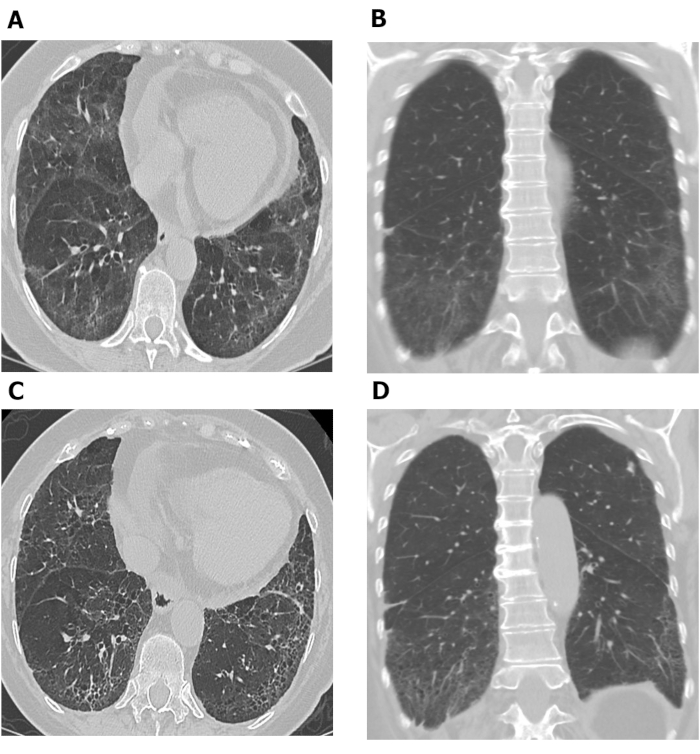
Figur 7: HRCT-bilder i seriebrystet som viser progresjon av lungefibrose hos pasient med SSc-ILD. Aksial (A) og koronære (B) bilder fra brystet HRCT viser basilær dominerende jordglass tetthet og reticulation med mild trekkraft bronkiektasi og subpleural sparing i samsvar med ikke-spesifikk interstitiell lungebetennelse i denne pasienten med SSc. Etter 10 år observeres økt reticulation og trekkraft bronkielektase ved lungebasene med reduksjon i jordglasstetthet på aksial (C) og koronale (D) bryst HRCT-bilder, i samsvar med mild forverring av lungefibrose. HRCT = datatomografi med høy oppløsning; SSc-ILD = systemisk sklerodermi-assosiert interstitiell lungesykdom. Vennligst klikk her for å se en større versjon av dette tallet.
Mens HRCT for tiden er den definitive bildemetoden for diagnostisering og vurdering av SSc-ILD, bruker den ioniserende stråling og er relativt dyr. Brystradiografier kan gjennomføres i stedet, selv om disse ikke letter differensialdiagnose i samme grad som HRCT, og en normal brystradiografi eliminerer ikke muligheten for ILD. Kanskje den beste bruken av brystradiografier er å overvåke for progressiv sykdom mellom HRCT-skanninger og for utelukkelse av kompliserende sykdom, som smittsom lungebetennelse, i innstillingen av akutt forverring av symptomer.
En oppfattet begrensning av HRCT er strålingseksponering. Som beskrevet tidligere, nye metoder for å gjennomføre CT-skanninger kan gjøre stråling eksponering for å bli redusert31, og videre, nåværende CT skannere gi en rekke avanserte teknikker som gir muligheten i fremtiden for å redusere stråling eksponering for nesten brystet radiografi nivåer. Alternativt kan bildemetoder som MR eller lunge ultralyd potensielt brukes til å unngå å utsette pasienten for stråling i fremtiden32,71,72,73. Vi tror at selv om det er risiko-nytte-hensyn forbundet med bildebehandlingsutnyttelse, oppveier fordelene med CT i diagnose og pasientbehandling langt de potensielle risikoene.
Bildedata, spesielt HRCT, gir uten tvil den viktigste informasjonen for å muliggjøre diagnose av SSc-ILD. Detaljert vurdering av mønstrene og egenskapene til HRCT-skanninger er vanligvis tilstrekkelig til å skille SSc-ILD fra andre lungesykdommer, med fordelen av å unngå behovet for en invasiv biopsiprosedyre.
Visuell vurdering av HRCT-skanninger introduserer en grad av subjektivitet og muligheten for interobservatørvariasjon. Databaserte metoder for HRCT-skanningstolkning har blitt undersøkt som en mulig tilnærming til å forbedre nøyaktigheten63,,74. For eksempel kan kvantitative tilnærminger til vurdering av lungefibrose eller sykdomsomfanget brukes til å vurdere behandlingsrespons68,70,75. Disse metodene er imidlertid ikke mye brukt i daglig klinisk praksis på dette tidspunktet.
Vi håper informasjonen som presenteres i dette manuskriptet vil fungere som en praktisk veiledning for å hjelpe leger med å bruke HRCT-skanninger for diagnosting av SSc-ILD og fastsettelse av prognose. Forbedrede metoder for å skaffe bilder og for å tolke skanninger har potensial til å redusere pasientenes eksponering for stråling og forbedre diagnostisk /prognostisk nøyaktighet.
Jonathan Chung erklærer ingen potensielle interessekonflikter med hensyn til den beskrevne forskningen, forfatterskapet og/eller publiseringen av denne artikkelen; Christopher Walker erklærer mottak av royalties fra Amirsys (Elsevier); og Stephen Hobbs erklærer mottak av royalties fra Elsevier og Wolters Kluwer Health. Open Access-publisering av denne artikkelen er sponset av Boehringer Ingelheim Pharmaceuticals, Inc.
Forfatteren(e) oppfyller kriteriene for forfatterskap som anbefalt av International Committee of Medical Journal Editors (ICMJE). Forfatterne fikk ingen direkte kompensasjon knyttet til utviklingen av videoen. Medisinsk skriftlig støtte til videomanuset ble gitt av Leon Newman, PhD, av GeoMed, et Ashfield-selskap, som ble kontrahert og finansiert av Boehringer Ingelheim Pharmaceuticals, Inc. (BIPI). BIPI fikk anledning til å gjennomgå den endelige videoen for medisinsk og vitenskapelig nøyaktighet samt hensyn til immaterielle rettigheter.
Forfatterne oppfyller kriteriene for forfatterskap som anbefalt av International Committee of Medical Journal Editors (ICMJE). Forfatterne fikk ingen direkte kompensasjon knyttet til utviklingen av manuskriptet. Skriveassistanse ble gitt av Ken Sutor, BSc, av GeoMed, et Ashfield-selskap, en del av UDG Healthcare plc, som ble kontrahert og finansiert av Boehringer Ingelheim Pharmaceuticals, Inc. (BIPI). BIPI fikk anledning til å gjennomgå manuskriptet for medisinsk og vitenskapelig nøyaktighet samt hensyn til immaterielle rettigheter.
| Name | Company | Catalog Number | Comments |
| CT scanners | Philips | NA | Multiple |
- Denton, C. P., Khanna, D. Systemic sclerosis. Lancet. 390 (10103), 1685-1699 (2017).
- Arnett, F. C., et al. Familial occurrence frequencies and relative risks for systemic sclerosis (scleroderma) in three United States cohorts. Arthritis & Rheumatism. 44 (6), 1359-1362 (2001).
- Barnes, J., Mayes, M. D. Epidemiology of systemic sclerosis: incidence, prevalence, survival, risk factors, malignancy, and environmental triggers. Current Opinion in Rheumatology. 24 (2), 165-170 (2012).
- Marie, I., Gehanno, J. F. Environmental risk factors of systemic sclerosis. Seminars in Immunopathology. 37 (5), 463-473 (2015).
- Silman, A. J. Epidemiology of scleroderma. Annals of the Rheumatic Diseases. 50, 846-853 (1991).
- Scholand, M. B., et al. Interstitial lung disease in systemic sclerosis: diagnosis and management. Rheumatology. 1, 008 (2012).
- Solomon, J. J., et al. Scleroderma lung disease. European Respiratory Review. 22 (127), 6-19 (2013).
- Walker, U. A., et al. Clinical risk assessment of organ manifestations in systemic sclerosis: a report from the EULAR Scleroderma Trials And Research group database. Annals of the Rheumatic Diseases. 66 (6), 754-763 (2007).
- Hinchcliff, M., Fischer, A., Schiopu, E., Steen, V. D., Investigators, P. Pulmonary hypertension assessment and recognition of outcomes in scleroderma (PHAROS): baseline characteristics and description of study population. The Journal of Rheumatology. 38 (10), 2172-2179 (2011).
- Giacomelli, R., et al. Interstitial lung disease in systemic sclerosis: current and future treatment. Rheumatology International. 37 (6), 853-863 (2017).
- Sanchez-Cano, D., et al. Interstitial lung disease in systemic sclerosis: data from the spanish scleroderma study group. Rheumatology International. 38 (3), 363-374 (2018).
- Silver, K. C., Silver, R. M. Management of systemic-sclerosis-associated interstitial lung disease. Rheumatic Diseases Clinics of North America. 41 (3), 439-457 (2015).
- Fischer, A., Kong, A. M., Swigris, J. J., Cole, A. L., Raimundo, K. All-cause healthcare costs and mortality in patients with systemic sclerosis with lung involvement. The Journal of Rheumatology. 45 (2), 235-241 (2018).
- Tyndall, A. J., et al. Causes and risk factors for death in systemic sclerosis: a study from the EULAR Scleroderma Trials and Research (EUSTAR) database. Annals of the Rheumatic Diseases. 69 (10), 1809-1815 (2010).
- Herzog, E. L., et al. Review: interstitial lung disease associated with systemic sclerosis and idiopathic pulmonary fibrosis: how similar and distinct. Arthritis & Rheumatology. 66 (8), 1967-1978 (2014).
- Rubio-Rivas, M., Royo, C., Simeon, C. P., Corbella, X., Fonollosa, V. Mortality and survival in systemic sclerosis: systematic review and meta-analysis. Seminars in Arthritis and Rheumatism. 44 (2), 208-219 (2014).
- Stock, C., et al. Serum KL-6 as a marker of disease progression in SSc-ILD. European Respiratory Journal. 52, (2018).
- Winstone, T. A., et al. Predictors of mortality and progression in scleroderma-associated interstitial lung disease: a systematic review. Chest. 146 (2), 422-436 (2014).
- Khanna, D., et al. Ongoing clinical trials and treatment options for patients with systemic sclerosis-associated interstitial lung disease. Rheumatology (Oxford). 58 (4), 567-579 (2019).
- Behr, J., Furst, D. E. Pulmonary function tests. Rheumatology (Oxford). 47, 65-67 (2008).
- Hax, V., et al. Clinical algorithms for the diagnosis and prognosis of interstitial lung disease in systemic sclerosis. Seminars in Arthritis and Rheumatism. 47 (2), 228-234 (2017).
- Molberg, O., Hoffmann-Vold, A. M. Interstitial lung disease in systemic sclerosis: progress in screening and early diagnosis. Current Opinion in Rheumatology. 28 (6), 613-618 (2016).
- Raghu, G., Goldman, L., Schafer, A. I. Interstital lung disease. Goldman-Cecil Medicine. , 575-588 (2016).
- Showalter, K., et al. Performance of forced vital capacity and lung diffusion cutpoints for associated radiographic interstitial lung disease in systemic sclerosis. The Journal of Rheumatology. 45 (11), 1572-1576 (2018).
- Suliman, Y. A., et al. Brief report: pulmonary function tests: high rate of false-negative results in the early detection and screening of scleroderma-related interstitial lung disease. Arthritis & Rheumatology. 67 (12), 3256-3261 (2015).
- Roth, M. D., et al. Predicting treatment outcomes and responder subsets in scleroderma-related interstitial lung disease. Arthritis & Rheumatology. 63 (9), 2797-2808 (2011).
- Kalra, M. K., Maher, M. M., Rizzo, S., Kanarek, D., Shepard, J. A. Radiation exposure from chest CT: issues and strategies. Journal of Korean Medical Science. 19 (2), 159-166 (2004).
- Siegel, J. A., Pennington, C. W., Sacks, B., Welsh, J. S. The birth of the illegitimate linear no-threshold model: an invalid paradigm for estimating risk following low-dose radiation exposure. American Journal of Clinical Oncology. 41 (2), 173-177 (2018).
- Frauenfelder, T., et al. Screening for interstitial lung disease in systemic sclerosis: performance of high-resolution CT with limited number of slices: a prospective study. Annals of the Rheumatic Diseases. 73 (12), 2069-2073 (2014).
- Kubo, T., et al. Radiation dose reduction in chest CT: a review. American Journal of Roentgenology. 190 (2), 335-343 (2008).
- Nguyen-Kim, T. D. L., et al. The impact of slice-reduced computed tomography on histogram-based densitometry assessment of lung fibrosis in patients with systemic sclerosis. Journal of Thoracic Disease. 10 (4), 2142-2152 (2018).
- Muller, C. S., Warszawiak, D., Paiva, E. D. S., Escuissato, D. L. Pulmonary magnetic resonance imaging is similar to chest tomography in detecting inflammation in patients with systemic sclerosis. Revista Brasileira de Reumatologia English Edition. 57 (5), 419-424 (2017).
- Pinal-Fernandez, I., et al. Fast 1.5 T chest MRI for the assessment of interstitial lung disease extent secondary to systemic sclerosis. Clinical Rheumatology. 35 (9), 2339-2345 (2016).
- Sverzellati, N. Highlights of HRCT imaging in IPF. Respiratory Research. 14, 3 (2013).
- Lynch, D. A., et al. Diagnostic criteria for idiopathic pulmonary fibrosis: a Fleischner Society White Paper. The Lancet Respiratory Medicine. 6 (2), 138-153 (2018).
- Raghu, G., et al. Diagnosis of idiopathic pulmonary fibrosis. An official ATS/ERS/JRS/ALAT clinical practice guideline. American Journal of Respiratory and Critical Care Medicine. 198 (5), 44-68 (2018).
- . Exam: CT thorax for interstitial lung disease Available from: https://www.pulmonaryfibrosis.org/docs/default-source/medical-community-documents/ct-chest-for-ild-protocol.pdf?sfvrsn=0 (2019)
- Doyle, T. J., Hunninghake, G. M., Rosas, I. O. Subclinical interstitial lung disease: why you should care. American Journal of Respiratory and Critical Care Medicine. 185 (11), 1147-1153 (2012).
- Peroni, D. G., Boner, A. L. Atelectasis: mechanisms, diagnosis and management. Paediatric Respiratory Reviews. 1 (3), 274-278 (2000).
- Branley, H. M. Pulmonary fibrosis in systemic sclerosis: diagnosis and management. Respiratory Medicine CME. 3, 10-14 (2010).
- Engeler, C. E., Tashjian, J. H., Trenkner, S. W., Walsh, J. W. Ground-glass opacity of the lung parenchyma: a guide to analysis with high-resolution CT. American Journal of Roentgenology. 160 (2), 249-251 (1993).
- Goldin, J. G., et al. High-resolution CT scan findings in patients with symptomatic scleroderma-related interstitial lung disease. Chest. 134 (2), 358-367 (2008).
- Strollo, D., Goldin, J. Imaging lung disease in systemic sclerosis. Current Rheumatology Reports. 12 (2), 156-161 (2010).
- Pandey, A. K., et al. Significance of various pulmonary and extrapulmonary abnormalities on HRCT of the chest in scleroderma lung. Indian Journal of Radiology and Imaging. 23 (4), 304-307 (2013).
- Chung, J. H., et al. CT Features of the usual interstitial pneumonia pattern: differentiating connective tissue disease-associated interstitial lung disease from idiopathic pulmonary fibrosis. American Journal of Roentgenology. 210 (2), 307-313 (2018).
- Zhan, X., et al. Differentiating usual interstitial pneumonia from nonspecific interstitial pneumonia using high-resolution computed tomography: the "Straight-edge Sign". Journal of Thoracic Imaging. 33 (4), 266-270 (2018).
- Farrokh, D., Abbasi, B., Fallah-Rastegar, Y., Mirfeizi, Z. The extrapulmonary manifestations of systemic sclerosis on chest high resolution computed tomography. Tanaffos. 14 (3), 193-200 (2015).
- Salaffi, F., et al. Relationship between interstitial lung disease and oesophageal dilatation on chest high-resolution computed tomography in patients with systemic sclerosis: a cross-sectional study. La Radiologia Medica. 123 (9), 655-663 (2018).
- Vonk, M. C., et al. Oesophageal dilatation on high-resolution computed tomography scan of the lungs as a sign of scleroderma. Annals of the Rheumatic Diseases. 67 (9), 1317-1321 (2008).
- Chowaniec, M., Skoczynska, M., Sokolik, R., Wiland, P. Interstitial lung disease in systemic sclerosis: challenges in early diagnosis and management. Reumatologia. 56 (4), 249-254 (2018).
- McCall, R. K., Ravenel, J. G., Nietert, P. J., Granath, A., Silver, R. M. Relationship of main pulmonary artery diameter to pulmonary arterial pressure in scleroderma patients with and without interstitial fibrosis. Journal of Computer Assisted Tomography. 38 (2), 163-168 (2014).
- Pandey, A. K., et al. Predictors of pulmonary hypertension on high-resolution computed tomography of the chest in systemic sclerosis: a retrospective analysis. Canadian Association of Radiologists Journal. 61 (5), 291-296 (2010).
- Raymond, T. E., Khabbaza, J. E., Yadav, R., Tonelli, A. R. Significance of main pulmonary artery dilation on imaging studies. Annals of the American Thoracic Society. 11 (10), 1623-1632 (2014).
- Colaci, M., et al. Lung cancer in scleroderma: results from an Italian rheumatologic center and review of the literature. Autoimmunity Reviews. 12 (3), 374-379 (2013).
- Distler, O., et al. Design of a randomised, placebo-controlled clinical trial of nintedanib in patients with systemic sclerosis-associated interstitial lung disease (SENSCIS). Clinical and Experimental Rheumatology. 35 (4), 75-81 (2017).
- Desai, S. R., et al. CT features of lung disease in patients with systemic sclerosis: comparison with idiopathic pulmonary fibrosis and nonspecific interstitial pneumonia. Radiology. 232 (2), 560-567 (2004).
- Mira-Avendano, I., et al. Interstitial lung disease and other pulmonary manifestations in connective tissue diseases. Mayo Clinic Proceedings. 94 (2), 309-325 (2019).
- Walkoff, L., White, D. B., Chung, J. H., Asante, D., Cox, C. W. The four corners sign: a specific imaging feature in differentiating systemic sclerosis-related interstitial lung disease from idiopathic pulmonary fibrosis. Journal of Thoracic Imaging. 33 (3), 197-203 (2018).
- Kotnur, M. R., Suresh, P., Reddy, V. S., Sharma, T., Salim, N. A. Systemic sclerosis with multiple pulmonary manifestations. Journal of Clinical & Diagnostic Research. 10 (6), 16-17 (2016).
- Goh, N. S., et al. Interstitial lung disease in systemic sclerosis: a simple staging system. American Journal of Respiratory and Critical Care Medicine. 177 (11), 1248-1254 (2008).
- Takei, R., et al. Radiographic fibrosis score predicts survival in systemic sclerosis-associated interstitial lung disease. Respirology. 23 (4), 385-391 (2018).
- Bakker, M. E., et al. Lung density and pulmonary artery diameter are predictors of pulmonary hypertension in systemic sclerosis. Journal of Thoracic Imaging. 32 (6), 391-397 (2017).
- Khanna, D., et al. Predictors of lung function decline in scleroderma-related interstitial lung disease based on high-resolution computed tomography: implications for cohort enrichment in systemic sclerosis-associated interstitial lung disease trials. Arthritis Research & Therapy. 17, 372 (2015).
- Ariani, A., et al. Quantitative chest computed tomography is associated with two prediction models of mortality in interstitial lung disease related to systemic sclerosis. Rheumatology (Oxford). 56 (6), 922-927 (2017).
- Goldin, J., et al. Treatment of scleroderma-interstitial lung disease with cyclophosphamide is associated with less progressive fibrosis on serial thoracic high-resolution CT scan than placebo: findings from the scleroderma lung study. Chest. 136 (5), 1333-1340 (2009).
- Tashkin, D. P., et al. Mycophenolate mofetil versus oral cyclophosphamide in scleroderma-related interstitial lung disease (SLS II): a randomised controlled, double-blind, parallel group trial. The Lancet Respiratory Medicine. 4 (9), 708-719 (2016).
- Distler, O., et al. Nintedanib for Systemic Sclerosis-Associated Interstitial Lung Disease. New England Journal of Medicine. 380, 2518-2528 (2019).
- Cappelli, S., et al. Interstitial lung disease in systemic sclerosis: where do we stand. European Respiratory Review. 24 (137), 411-419 (2015).
- Goldin, J. G., et al. Longitudinal changes in quantitative interstitial lung disease on CT after immunosuppression in the Scleroderma Lung Study II. Annals of the American Thoracic Society. 5 (11), 1286-1295 (2018).
- Wangkaew, S., Euathrongchit, J., Wattanawittawas, P., Kasitanon, N. Correlation of delta high-resolution computed tomography (HRCT) score with delta clinical variables in early systemic sclerosis (SSc) patients. Quantitative Imaging in Medicine and Surgery. 6 (4), 381-390 (2016).
- Kim, H. J., et al. Transitions to different patterns of interstitial lung disease in scleroderma with and without treatment. Annals of the Rheumatic Diseases. 75 (7), 1367-1371 (2016).
- Tardella, M., et al. Ultrasound B-lines in the evaluation of interstitial lung disease in patients with systemic sclerosis: cut-off point definition for the presence of significant pulmonary fibrosis. Medicine (Baltimore). 97 (18), 0566 (2018).
- Hassan, R. I., et al. Lung ultrasound as a screening method for interstitial lung disease in patients with systemic sclerosis. Journal of Clinical Rheumatology. , (2018).
- Wang, Y., Gargani, L., Barskova, T., Furst, D. E., Cerinic, M. M. Usefulness of lung ultrasound B-lines in connective tissue disease-associated interstitial lung disease: a literature review. Arthritis Research & Therapy. 19 (1), 206 (2017).
- Ariani, A., et al. Quantitative CT indexes are significantly associated with exercise oxygen desaturation in interstitial lung disease related to systemic sclerosis. The Clinical Respiratory Journal. 11 (6), 983-989 (2017).
- Kim, H. J., et al. Quantitative texture-based assessment of one-year changes in fibrotic reticular patterns on HRCT in scleroderma lung disease treated with oral cyclophosphamide. European Radiology. 21 (12), 2455-2465 (2011).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved