Einsatz des Kapillaraerosolgenerators bei der kontinuierlichen Produktion von kontrolliertem Aerosol für nicht-klinische Studien
In diesem Artikel
Zusammenfassung
Das Protokoll beschreibt die Einstellungen und die Verwendung eines Kapillaraerosolgenerators für die kontinuierliche Produktion von kontrolliertem Aerosol aus einer flüssigen Lösung mit mehreren Spezies, die für die stetige großvolumige Aerosolabgabe (z. B. In-vivo-Inhalationsstudien ) geeignet ist.
Zusammenfassung
Der Kapillaraerosolgenerator (CAG) wird mit dem Prinzip der thermischen Flüssigkeitsverdampfung durch Erwärmung von E-Liquid in der Anfangsphase betrieben, gefolgt von Keimbildung und Kondensation, die durch ein Gemisch aus Luftstrom reguliert werden, um Aerosole zu erzeugen, wie z.B. in einer elektronischen Zigarette (EC). Das CAG ist besonders nützlich bei der kontinuierlichen Erzeugung von Aerosolen großer Volumina, z. B. bei In-vivo-Inhalationstoxikologiestudien , bei denen die Verwendung von ECs nicht möglich ist. Die thermischen Auswirkungen der Erzeugung von Aerosol aus dem CAG sind in Bezug auf die in einer EC angewendete Temperatur ähnlich, so dass die Forscher die Dämpfe von E-Liquids in großem Maßstab und Reproduzierbarkeit beurteilen können. Da der Betrieb des CAG es den Benutzern ermöglicht, kritische Parameter wie die Durchflussrate von E-Liquid, Heiztemperaturen und Verdünnungsluftströme zu steuern, können Forscher verschiedene E-Liquid-Formulierungen in einem gut kontrollierten Gerät testen. Es wird gezeigt, dass Eigenschaften, wie die Größe der Aerosolpartikel, mit dem Luftdurchsatz in Bezug auf den E-Liquid-Durchfluss und die E-Liquid-Zusammensetzung reguliert werden. Die CAG ist jedoch bei der Bewertung allgemeiner EG-bezogener Fragen, wie z. B. der Überhitzung ihrer Elemente, begrenzt. Wir wollen zeigen, dass das CAG Aerosol erzeugen kann, das reproduzierbar und kontinuierlich ist, indem wir die chemischen und physikalischen Aerosoleigenschaften mit einer ausgewählten E-Liquid-Formulierung bewerten. Das Protokoll beschreibt die Betriebsparameter des Flüssigkeitsdurchflusses, der Verdünnungsluftdurchflussraten und der Betriebsverfahren, die zur Optimierung der Aerosolkonzentration und Partikelgröße erforderlich sind, die für eine in vivo toxikologische Studie erforderlich sind. Durch die Präsentation der repräsentativen Ergebnisse des Protokolls und die Diskussion der Herausforderungen und Anwendungen der Arbeit mit einem CAG zeigen wir, dass CAG reproduzierbar eingesetzt werden kann. Die Technologie und das Protokoll, die aus früheren Arbeiten entwickelt wurden, dienen als Grundlage für zukünftige Innovationen für laborgesteuerte Untersuchungen zur Aerosolerzeugung.
Einleitung
Gängige E-Liquids enthalten eine Mischung aus Propylenglykol, Glycerin, Wasser, Nikotin und ausgewählten Geschmacksrichtungen. Die Zusammensetzung eines von einem EC-Gerät erzeugten Aerosols hängt nicht nur von der flüssigen Formulierung ab, sondern auch vom Material, dem Design und den Eigenschaften des Geräts. Folglich können viele EG-Produkte eine große Variabilität der Aerosolabgabe1 verursachen, einschließlich der gerätespezifischen Erzeugung erhöhter Konzentrationen unerwünschter Bestandteile, der Variation des Puffvolumens, der Änderung des Luftstroms aufgrund blockierter Lüftungslöcher und des "trockenen Puffens" (wenn der Flüssigkeitsbehälter fast leer ist, was zu einer Überhitzung des Geräts führt, da ein Teil der gelieferten Energie nicht für die Flüssigkeitsverdampfung verwendet wird)2 . Darüber hinaus würde das Aufladen, Nachfüllen und Reinigen von EC-Geräten während langfristiger Inhalationsstudien zu einem enormen zusätzlichen Hindernis für die Logistikwerden 3. Aus diesen Gründen sollten andere Aerosolgeneratoren für die großtechnische Produktion von Aerosolen und die ordnungsgemäße Bewertung flüssiger Formulierungen in Betracht gezogen werden, wobei gerätebedingte Schwankungen der Aerosolzusammensetzung vermieden und die Arbeitsbelastung verringertwerden sollte 4,5. Dennoch sollten geräteerzeugte Aerosole Teil der Risikobewertungsstrategien bleiben, da die Konzentrationen bestimmter Bestandteile in EG-Produkten aufgrund der Heiz-/Kühlungsbesonderheiten der Produkte höher sein könntenals in laborgesteuerten standardisierten Aerosolgeneratoren 6,7,8.
Aufgrund der begrenzten Informationen über die derzeit verfügbaren regulatorischen Anforderungen entwickeln sich die Bewertungsmethoden für die potenzielle Toxizität von Aerosolen, die von elektronischen Zigaretten erzeugt werden, (EC) nochweiter 9,10,11. Eine genaue In-vitro- und In-vivo-Bewertung erfordert jedoch die Erzeugung gut charakterisierter und reproduzierbarer Aerosolvolumina im Laufe der Zeit. Die Herstellung von Aerosol aus einem EC-Gerät mit einem kontrollierten Puffregime wäre sicherlich der repräsentativste Prozess aus Sicht des Benutzerverbrauchs. Für Studien zur regulatorischen Toxizität, unter Berücksichtigung einer Vielzahl möglicher flüssiger Formulierungen, die Benutzer häufig selbst herstellen können, und gleichzeitig unter Änderung einiger Produkteigenschaften (z. B. gelieferte Energie) ist die Verwendung von EC-Produkten für die Durchführung von toxikologischen Langzeitstudien mit wiederholter Exposition nicht nur eine Herausforderung, sondern auch potenziell unzureichend.
Der Kapillaraerosolgenerator (CAG), der von Philip Morris 12,13 entwickelt und von der Virginia Commonwealth University14 weiterentwickelt wurde, arbeitet nach dem Prinzip, einen heißen Dampfstrahl aus einer elektrisch beheizten Kapillare zu erzeugen, der anschließend mit Umgebungsluft abgekühlt wird, was zur Bildung von Partikelkernen und anschließender Kondensation führt, was zur Aerosolbildung führt. Da die gleichen physikalischen Prozesse zur Aerosolbildung in ECs führen (abgesehen von der Abgabe der Flüssigkeit an die Kapillare durch eine Pumpe im CAG, die in einem EC üblicherweise durch Kapillarkräfte ersetzt wird, die auf das ableitende Material wirken, das die Flüssigkeit aus dem Reservoir in der EC zieht), sind die Eigenschaften von CAG-erzeugten Aerosolen denen von EC-Aerosolen14 sehr ähnlich (Abbildung 1 ). Das CAG ermöglicht die Produktion großer Aerosolmengen mit geringen Handhabungsanforderungen. Es eignet sich daher besonders für In-vivo-Inhalationsstudien.
Das CAG ist ein Laborgerät, das aus einem beheizten Kapillarrohr besteht, das einfach mit einem Temperaturregler und über eine Peristaltikpumpe mit einem Flüssigkeitsreservoir verbunden ist (Abbildung 2A). Die Kapillare (160 mm, 21 G, Edelstahl) wird durch vier Heizelemente beheizt, die alle in einen Aluminiumblock eingebettet sind (Abbildung 2B). Die Temperatur wird typischerweise auf 250-275 °C eingestellt, um die Spulenerwärmungsbedingungen eines EC-Geräts15 nachzuahmen. Die durch die Kapillare gepumpte Flüssigkeit wird erhitzt und in heißen Dampf umgewandelt, der aus der Spitze der Kapillare austritt. Die CAG-Baugruppe (Abbildung 2C) benötigt zusätzliche Elemente, um den erzeugten Dampf mit kalter Luft zu mischen und ein Aerosol zu bilden. Das abrupte Mischen des heißen, übersättigten Dampfes mit einem kalten Luftstrom führt zu Keimbildung und anschließender Kondensation, was zur Aerosolbildung führt (Abbildung 2C). In unserem CAG-Design (Abbildung 3) kühlt ein zusätzlicher beheizter Luftstrom zunächst den äußeren Körper ab und zirkuliert anschließend entlang der Heizblöcke, um den Luftstrom zu erwärmen, wodurch gleichzeitig die Kondensation des Flüssigkeitsrückstroms an der Spitze der Kapillare verhindert und der Dampfstrahlbruch stabilisiert wird. Darüber hinaus erzeugt es eine unerwünschte Abschirmung von heißen Dämpfen und beeinflusst so den Keimbildungsprozess. Aus diesem Grund sollte der für diesen Luftstrom angewendete Durchfluss minimal sein und dem Zweck der Anwendung entsprechen. Dieser Luftstrom wird in diesem Manuskript als "beheizter Luftstrom" bezeichnet, obwohl verstanden werden muss, dass dieser Strom passiv von den Heizblöcken und nicht absichtlich vom Benutzer erwärmt wird.
Der Kühlluftdurchsatz hat einen starken Einfluss auf die Größe der erzeugten Aerosolpartikel. Bei der Aerosolproduktion für In-vivo-Inhalationsstudien bestimmt der Verdünnungsluftstrom die Expositionsdosis und muss möglicherweise weiter verdünnt werden, bevor die Expositionskammer erreicht wird. Neben der chemischen Zusammensetzung von Aerosolen ist es wichtig, die Aerosolpartikelgrößenverteilung (PSD) zu charakterisieren, um sicherzustellen, dass das erzeugte Aerosol dem von ECs erzeugten Aerosol ähnelt und innerhalb des von den OECD-Leitsätzen empfohlenen Inhalationspartikelgrößenbereichs liegt (oft parametrisiert durch die Annahme der logarithmischen Normalität von PSD mit einem aerodynamischen Massendurchmesser [MMAD] und einer geometrischen Standardabweichung [GSD]).
Der MMAD der erzeugten Aerosole kann je nach Gerätedesign, physikalisch-chemischen Flüssigkeitseigenschaften der Formulierung (z. B. Dichte, Viskosität und Oberflächenspannung), Luftdurchsatz und Temperatur, die thermodynamische Bedingungen diktiert14,16,17 stark variieren. Bei In-vivo-Expositionsexperimenten besteht der Luftstrom im Allgemeinen aus konditionierter, gefilterter Luft bei 22 ± 2 °C und 60 % ± 5 % relativer Luftfeuchtigkeit. Das erzeugte Aerosol kann dann je nach Studienbedarf weiter verdünnt werden, um Zielkonzentrationen in der Testatmosphäre zu erreichen. Es wird dann über Glasrohrleitungen in die Belichtungskammer geliefert, um den Filtrationsverlust zu verringern. In den hier vorgestellten Ergebnissen werden die Temperatur- und Luftstromeinstellungen festgelegt, um zu zeigen, dass das CAG für die kontinuierliche Produktion eines kontrollierten Aerosols mit konsistenter und inhalierbarer PSD und definierten Konzentrationen für In-vivo-Inhalationsstudien verwendet werden kann.
Im Protokoll beschreiben wir, wie man: 1) das CAG zusammenstellt, 2) Parameter bestimmt, die zur Erzeugung von Aerosol aus dem CAG erforderlich sind, 3) Aerosolerzeugung durchführt und 4) physikalische und chemische Bestandteile analysiert, die im Aerosol von Interesse sind. Für diese Vorläufe betrachten wir eine flüssige Lösung, die auf einer Mischung von aerosolbildenden Komponenten basiert: Propylenglykol (PG), Glycerin (VG), Wasser und Nikotin in vorgeschriebenen Massenanteilen. Schließlich werden wir Beispieldaten für die Bewertung einer komplexen Multispezies-Mischung teilen, die in unseren Experimenten erzeugt wurde (einschließlich der oben genannten Bestandteile, die mit zusätzlichen Geschmacksbestandteilen gemischt werden). Wir werden die Gesamtergebnisse und Herausforderungen sowie die Anwendbarkeit dieses experimentellen Ansatzes für die Bewertung solcher Mischungen diskutieren.
Protokoll
1. CAG-Systemmontage
- Montage der CAG
- Platzieren Sie die Kapillare in der Kapillarnut der Aluminiumheizblöcke, wobei das Ausgangsende um ca. 5 mm hervorsteht.
- Ziehen Sie die Schrauben der beiden Hälften der Aluminium-Heizblöcke leicht an.
- Montieren Sie die Heizelemente (a) und das Thermoelement (b) in den Aluminiumheizblöcken (c), wobei die Drähte durch die hintere Aluminiumkappe (d) ragen (Abbildung 4A).
- Stellen Sie sicher, dass die Drähte der Heizelemente mit einem Adapter verbunden sind und stellen Sie sicher, dass sie gerade sind.
- Montieren Sie das innere PEEK-Rohr (g) mit dem äußeren SS-Rohr (e). Stellen Sie sicher, dass die 2 x 4 mm Steckverschraubungen (f) fest am äußeren SS-Rohr (e) befestigt sind (Abbildung 4B).
- Legen Sie O-Ringe (3 x 30 mm) auf die beiden Rillen des inneren PEEK-Rohrs (g) und setzen Sie das innere PEEK-Rohr (g) vom vorderen Ende in das äußere SS-Rohr (e) ein.
- Legen Sie die montierten Aluminium-Heizelemente auf die hintere SS-Rückseite (i), wobei die hintere Aluminiumkappe der SS-Rückseite zugewandt ist, und schieben Sie die innere PEEK/äußere SS-Rohrbaugruppe über die Aluminium-Heizelemente, um sie fest mit der SS-Rückseite (i) zu verbinden (Abbildung 4C).
- Legen Sie die Aluminium-Frontkappe (h) über das Aluminium-Heizelement im inneren PEEK-Rohr. Stellen Sie sicher, dass die Kapillare leicht aus der Aluminium-Frontkappe herausragt. Installieren Sie die drei SS-Spindeln (j) um die SS-Rückwand und ziehen Sie sie fest an.
- Platzieren Sie den PEEK-Adapter (k) über der Innenfront des PEEK-Rohrs. Stellen Sie sicher, dass der PEEK-Adapter auf die vordere Nut des PEEK-Innenrohrs passt. Platzieren Sie den 25 mm Scheduler (l) über dem PEEK-Adapter und durch die drei SS-Gewindespindeln. Ziehen Sie die Muttern über dem Scheduler von Hand fest, sodass der PEEK-Adapter fest sitzt (Abbildung 4D).
- Verbinden Sie die Heizelemente mit dem Temperaturregler und die Kapillare mit der Peristaltikpumpe und der Testflüssigkeitslösung.
- Schließen Sie die Druckluft für den beheizten Luftstrom über die 2 x 4 mm Push-in-Armaturen an das CAG an (Abbildung 4B, [f]).
- Montieren Sie das CAG an das Glasstück und schließen Sie die CAG-Kühlung und die ersten Verdünnungsluftströme (Prozessluft; Abbildung 3). Fügen Sie bei Bedarf einen zweiten Verdünnungsdurchflusseintrag sowie Aerosolprobenahmeanschlüsse und einen regulatorischen T-Übergang hinzu (Abbildung 5).
- CAG-Reinigungsverfahren
- Entfernen Sie die CAG aus der CAG-Glasbaugruppe und reinigen Sie das Glas mit trockenen Tüchern, bis das Glas sichtbar trocken ist.
- Beobachten Sie die Kapillarabgabe des CAG auf Verstopfung. Wenn eine Partikelablagerung am Ausgang der Kapillare beobachtet werden kann, ändern Sie die Kapillare. Wenn Sie eine reduzierte Aerosolabgabe bemerken, ersetzen Sie die Kapillare durch eine neue.
- Zerlegen Sie den CAG gemäß den Schritten 1.1.9 bis 1.1.1.
- Setzen Sie die CAG gemäß den Schritten 1.1.1 bis 1.1.9 wieder zusammen, sobald die Kapillare geändert wurde.
2. Berechnung der CAG-Aerosolkonzentration und -verdünnung
- Theoretische Berechnung der TDF
- Berechnen Sie den TDF basierend auf der Konzentration der flüssigen Formulierung (hier Stammlösung/-konzentration genannt) und dem LFR:
TDF: Gesamtverdünnungsluftstrom (L/min)
CLagerbestand: Lagerkonzentration 2%, w/w)
LFR: Flüssigkeitsdurchfluss (g/min)
C-Ziel: Zielkonzentration (μg/L) - Bei Verwendung einer Lösung mit 2% (w/w) Nikotin, mit einer Ziel-Nikotinaerosolkonzentration von 15 μg/L und einem LFR von 0,35 g/min, wird davon ausgegangen, dass 100% Ausbeute wie folgt sein wird:
- Berechnen Sie den TDF basierend auf der Konzentration der flüssigen Formulierung (hier Stammlösung/-konzentration genannt) und dem LFR:
- Theoretische Berechnung von LFR
- Berechnen Sie den LFR basierend auf der Konzentration der flüssigen Stammlösung und des TDF:
LFR: Flüssigkeitsdurchfluss (g/min)
C-Ziel: Zielkonzentration (μg/L)
TDF: Gesamtverdünnungsluftstrom (L/min)
CLagerbestand: Lagerkonzentration (%, w/w) - Bei Verwendung einer Lösung mit 2% (w/w) Nikotin, mit einer Ziel-Nikotinaerosolkonzentration von 15 μg/L und einer TDF von 300 l/min, wird davon ausgegangen, dass eine Ausbeute von 100% wie folgt sein wird:
- Berechnen Sie den LFR basierend auf der Konzentration der flüssigen Stammlösung und des TDF:
- Berechnung des tatsächlichen Ertrags (%) auf Basis experimenteller Daten
- Basierend auf den oben genannten theoretischen Berechnungen führen Sie die ersten technischen Läufe durch, um die tatsächliche Konzentration der Aerosolbestandteile (CActual) zu quantifizieren und die tatsächliche Ausbeute (AY) des CAG-Aerosols zu erhalten. Führen Sie eine weitere Feinabstimmung der Aerosolkonzentration durch, indem Sie die gleichen Berechnungen für die Einstellung von TDF oder LFR verwenden.
AY: tatsächlicher Ertrag (%)
CIst: tatsächliche Konzentration des Aerosolbestandteils (μg/L)
TDF: Gesamtverdünnungsluftstrom (L/min)
CLagerbestand: Lagerkonzentration (%, w/w)
LFR: Flüssigkeitsdurchfluss (g/min) - Die Verwendung einer Lösung, die 2% (w/w) Nikotin enthält, mit einer gemessenen Nikotinaerosolkonzentration von 15 μg/l, TDF von 320 l/min und LFR von 0,35 g/min führt zu folgendem Nikotin-AY:
- Basierend auf den oben genannten theoretischen Berechnungen führen Sie die ersten technischen Läufe durch, um die tatsächliche Konzentration der Aerosolbestandteile (CActual) zu quantifizieren und die tatsächliche Ausbeute (AY) des CAG-Aerosols zu erhalten. Führen Sie eine weitere Feinabstimmung der Aerosolkonzentration durch, indem Sie die gleichen Berechnungen für die Einstellung von TDF oder LFR verwenden.
3. CAG-Aerosolerzeugung
- Beginn der Aerosolerzeugung
- Wiegen und notieren Sie den Wert der Testflüssigkeit, des Magnetrührers und der Flasche auf 0,01 g genau. Flüssige Bestandsformulierungen werden mit den in Tabelle 1 beschriebenen Komponenten hergestellt.
- Geben Sie die entsprechenden Luftstromeinstellungen (±5%) an (Abbildung 5):
Druckluft für beheizten Durchfluss: 2 l/min
Kühlstrom: 10 l/min
Erster Verdünnungsstrom: 150 L/min
Zweiter Verdünnungsstrom: 160 l/min
Abfallstrom: 172 l/min - Stellen Sie den Temperaturregel-Sollwert am digitalen Temperaturregler auf 250 °C und beginnen Sie mit der Erwärmung des CAG.
- Legen Sie die flüssige Stammlösung mit einem magnetischen Rührstab auf einen Magnetrührer. Setzen Sie das Einlassrohr der Peristaltikpumpe in die Testlösung ein.
- Schalten Sie die Peristaltikpumpe ein und stellen Sie den Durchfluss auf den LFR ±5% (g/min) ein.
- Wenn die CAG-Temperatur 250 ± 1 °C erreicht, beginnen Sie mit der Aerosolerzeugung, indem Sie die Peristaltikpumpe starten, um Testflüssigkeit an die CAG abzugeben.
- Überprüfen Sie, ob das Aerosol in der Nähe der Kapillarspitze erzeugt wird und erfassen Sie die Zeit, die zur Berechnung des Massendurchflusses erforderlich ist. Wenn kein Aerosol erzeugt wird, überprüfen Sie alle Geräte und Einstellungen erneut. Wenn immer noch kein Aerosol erzeugt wird, ist es sehr wahrscheinlich, dass die Kapillare blockiert ist und ersetzt werden muss.
- Während der Aerosolerzeugung
- Lassen Sie die Flüssigkeit, die im Glasaufbau kondensiert, alle 60 Minuten ab, um eine konstante und stabile Aerosolerzeugung zu gewährleisten.
- Stoppen der Aerosolerzeugung
- Entfernen Sie den Schlauch aus der Testlösungsflasche und schalten Sie die Testflüssigkeit auf deionisiertes Wasser um und notieren Sie die Zeit für die Berechnung des Massenstroms.
- Warten Sie, bis Wasserdampf aus der Kapillare austritt, schalten Sie den Temperaturregler aus und lassen Sie die Peristaltikpumpe mindestens 10 Minuten eingeschaltet, um die Kapillare zu spülen und zu reinigen.
- Wiegen und erfassen Sie den Wert der Prüfflüssigkeit und -flasche auf 0,01 g genau und berechnen Sie den Massenstrom anhand der folgenden Gleichung:
- Schalten Sie die Druckluft aus, die als erwärmter Durchfluss verwendet wird.
- Falls erforderlich, entfernen Sie die CAG aus der Baugruppeneinrichtung, reinigen Sie die Glasröhre mit trockenen Tüchern und bauen Sie die CAG wieder zusammen.
4. Analytische Bestimmung der Bestandteile
HINWEIS: Die Aerosolprobenahme erfolgt an zwei Positionen: a) am unverdünnten Aerosol (sowohl die erste Verdünnungsluft als auch der zweite Verdünnungsstrom werden während der unverdünnten Probenahme abgeschaltet) und b) am verdünnten Aerosol mit allen bereitgestellten Verdünnungen (Abbildung 5). An jeder der Probenahmepositionen stehen bis zu drei Probenahmeanschlüsse zur Verfügung, a und b, die die gleichzeitige Erfassung von ACM ermöglichen, sowie andere Geräte/Sonden zur Analyse von Aerosoleigenschaften. Die Probenahmeleitung wird senkrecht zur Aerosolströmungsrichtung installiert und mit einer Vakuumpumpe verbunden, die es ermöglicht, ein bestimmtes Aerosolvolumen (abhängig von der Pumpendurchflussrate und der Probendauer) zu ziehen.
- Bestimmung der gesammelten Aerosolmasse (ACM)
HINWEIS: Die partikuläre Phase des Aerosols wird auf einem Glasfaser-Filterpad eingeschlossen (Durchmesser: 44 mm, Partikelgrößenretention: 1,6 μm). ACM-Gewichte vor und nach der Probenahme werden mit Filterhaltern gemessen, um Wägeverluste durch Verdampfung flüchtiger Komponenten zu minimieren.- Legen Sie einen Filter in den Filterhalter und setzen Sie die Filterkappen ein.
- Wiegen Sie den Filterhalter vor der Probenentnahme auf 0,0001 g mit dem Filter und dokumentieren Sie das Gewicht.
- Schließen Sie den Filterhalter, der den Filter enthält, an den Aerosolstrom an und starten Sie die Probenentnahme.
- Wiegen Sie den Filter nach der Probenentnahme mit dem Filterhalter und den Kappen und dokumentieren Sie das Endgewicht.
- Berechnen Sie den ACM anhand der folgenden Formel:
ACM: Konzentration von ACM (μg/L)
Wb: Gewicht des Filters und des Filterhalters vor der Probenahme (g) auf 0,0001 g
Wa: Gewicht des Filters und des Filterhalters nach Probenahme (g) auf 0,0001 g
V-Aerosol: Volumen des Aerosols (L), das durch den Filter strömt, berechnet mit:
Probenahmezeit (min) x Probenahmedurchfluss (L/min) - Entfernen Sie das Filterpad aus dem Filterhalter und legen Sie es in eine 25 ml Glasdurchstechflasche mit 5 ml Ethanol. Extrahieren Sie das ACM, indem Sie das Filterpad an einem Laborschüttler für 30 min bei 400 U / min schütteln.
- Zentrifen Sie das 25 ml Glasfläschchen für 5 min bei 290 x g und sammeln Sie den Überstand zur Quantifizierung von PG/VG und der partikulären Phase von Nikotin.
- Bestimmung der Nikotin- (oder Geschmacks-) Konzentration
HINWEIS: Das Aerosol wird auf einer Probensäule eingeschlossen, die speziell verarbeitete breitporige Kieselgur enthält, eine chemisch inerte Matrix für den Einsatz in einem pH-Bereich von 1 bis 13 (Abbildung 6).- Bereiten Sie die Probensäule innerhalb von 15 Minuten vor, bevor Sie mit der Extraktion der Aerosolproben beginnen.
- Um die Nikotinkonzentrationen zu bestimmen, fügen Sie 2 ml 0,5 M Schwefelsäure hinzu. Um Aromen zu bestimmen, fügen Sie 2 ml Isopropanol hinzu.
- Überprüfen Sie den Probenahmefluss.
- Schalten Sie die Vakuumpumpe ein und überprüfen Sie mit der kalibrierten Durchflussvorrichtung, die eine Genauigkeit von bis zu 1 ccm / min bietet, die Durchflussrate mit einer an die Probenahmeleitung angeschlossenen Probensäule. Stellen Sie den Durchfluss mit dem Nadelventil auf den Bereich von 700 ccm/min ± 5% ein.
- Schalten Sie die Vakuumpumpe aus.
- Musterkollektion
- Fügen Sie die beiden Adapter entsprechend ihrer Einlass- und Auslassseite zur Probensäule hinzu (Abbildung 6). Schließen Sie das Rohr über den Auslassadapter an die Vakuum-Probenahmeleitung an.
- Schließen Sie die Probensäulenbaugruppe über den Einlassadapter an den Probenahmeanschluss an.
- Starten Sie die Probenentnahme durch Einschalten der Vakuumpumpe.
- Notieren Sie sich die Startzeit der Probenahme.
- Nach einer voreingestellten Probenahmezeit, 10 min an der unverdünnten Probenahmestelle A und 30 min an der verdünnten Probenahmestelle B, schaltet die Vakuumpumpe aus und zeichnet die Uhrzeit auf.
- Entfernen Sie die Beispielspalte aus dem Sampling-Port.
- Entfernen Sie die Adapter von der Probensäule und versiegeln Sie die Probensäule mit einer Filmmembran, um Verluste durch Verdampfung oder Kontamination zu vermeiden. Beschriften Sie die Beispielspalte entsprechend dem entsprechenden Beispielnamen.
- Lagern Sie die versiegelte Probensäule bis zur Analyse im Kühlschrank (2-8 °C).
- Bestimmung der Carbonylkonzentrationen
HINWEIS: Carbonyle werden auf einem Glasfilterpad eingeschlossen, das in Reihe mit einem Mikroimpinger verbunden ist, der mit 2,4-Dinitrophenylhydrazin (DNPH) gefüllt ist, das in Acetonitril gelöst ist.
- Bereiten Sie die Probensäule innerhalb von 15 Minuten vor, bevor Sie mit der Extraktion der Aerosolproben beginnen.
- Vorbereitung für das Fangen
- Füllen Sie den Mikroimpinger mit 10 ml 15 mM DNPH in Acetonitril.
- Bereiten Sie ein Filterpad vor (siehe Absatz 4.1).
- Probenahmefluss überprüfen
- Schalten Sie die Vakuumpumpe ein und überprüfen Sie die Durchflussrate der Probenahmelinie mit einer kalibrierten Durchflussvorrichtung, die eine Genauigkeit von 1 ccm / min bietet. Stellen Sie den Durchfluss mit dem Nadelventil auf den Bereich von 700 ccm/min ± 5% ein.
- Schalten Sie die Vakuumpumpe aus.
- Probenahme
- Schließen Sie den mit dem Mikroimpinger verbundenen Filterhalter an den Probenahmeanschluss an.
- Schließen Sie die Vakuum-Probenahmeleitung an den Auslass des Mikro-Impingers an.
- Starten Sie die Probenentnahme durch Einschalten der Vakuumpumpe.
- Notieren Sie sich die Startzeit der Probenahme.
- Nach einer voreingestellten Probenahmezeit, 10 min an der unverdünnten Probenahmestelle a und 30 min an der verdünnten Probenahmestelle b, schalten Sie die Vakuumpumpe aus und zeichnen Sie die Zeit auf.
- Trennen Sie die Probenahmefalle vom Probenahmeanschluss.
- Entleeren Sie den Impinger in ein Glasfläschchen. Füllen Sie die DNPH-Lösung auf 10 ml mit Acetonitril auf.
- Bestimmen Sie das Gewicht des Filterpads und extrahieren Sie es in der DNPH-Acetonitril-Lösung durch Schütteln. Entsorgen Sie das Filterpad nach der Extraktion.
- Nehmen Sie ein 1 ml Aliquot der Carbonyl-DNPH-Lösung und fügen Sie 50 μL Pyridin hinzu, um die Lösung zu stabilisieren.
- Lagern Sie die Aliquots bis zur Analyse in einem Gefrierschrank bei ≤-12 °C.
- Füllen Sie den Mikroimpinger mit 10 ml 15 mM DNPH in Acetonitril.
Ergebnisse
Reproduzierbarkeit von CAG-Aerosolen
Um die Reproduzierbarkeit des CAG-erzeugten Aerosols zu demonstrieren, wurde eine flüssige Basislösung, die PG, VG, Nikotin, Wasser und Ethanol (71,72%, 17,93%, 2%, 5,85% bzw. 2,5%) enthielt, über 10 separate Aerosolerzeugungsläufe verwendet. Die Aerosolisierungs- und Probenahmeparameter sind in Tabelle 2 zusammengefasst. Die chemische Charakterisierung der CAG-erzeugten Aerosole bestätigte die hohe Reproduzierbarkeit der mit dem System erzielten Ergebnisse. Unter den gleichen Wärme-, Kühl- und Verdünnungsluftströmen sowie den gleichen Probenahmebedingungen waren die Konzentrationen von ACM, Nikotin, VG und PG über die Aerosolerzeugungsläufe stabil, mit einer relativen Standardabweichung von 2,48%, 3,28%, 3,43% bzw. 3,34% von ACM, Nikotin, VG und PG (Abbildung 7).
Die Konzentrationen von acht Carbonylen - nämlich Acetaldehyd, Aceton, Acrolein, Butyraldehyd, Crotonaldehyd, Formaldehyd, Methylethylketon und Propionaldehyd - wurden während drei aufeinanderfolgender CAG-Aerosolerzeugungsläufe gemessen. Wie bei Aerosolen, die unter konstanten kontrollierten Bedingungen erzeugt werden, erwartet wurden, blieben die Ausbeuten aller Carbonylanalyten niedrig (Tabelle 3) und erreichten nicht die Grenzen der Quantifizierung (LOQ) der Analysemethode für die meisten Verbindungen. Nur Acetaldehyd und Formaldehyd hatten Ausbeuten über dem LOQ. Die Formaldehydkonzentrationen in der verdünnten Aerosolprobe zeigten eine hohe Variabilität (±32%) aufgrund der Flüchtigkeit dieses Analyten sowie Ausbeuten nahe dem LOQ. Die Daten bestätigten das Fehlen von flüssigen thermischen Abbauprodukten in CAG-erzeugten Aerosolen. Die Zugabe einer Mischung von Aromen hatte einen Einfluss auf die Carbonylzusammensetzung des Aerosols. Im vorliegenden Fall waren die Ausbeuten an Acetaldehyd und Butyraldehyd in dem verdünnten Aerosol, das in die Expositionskammer gelangen sollte, drastisch von Werten nahe dem LOQ auf 2,06 bzw. 1,56 μg/L erhöht. Diese Daten unterstreichen die Wirkung der Zusammensetzung der Aromamischung auf die Aerosolzusammensetzung und betonen die Notwendigkeit, die potenzielle Toxizität bestimmter Aromastoffe in einer E-Liquid-Formulierung in einem frühen Stadium vor der endgültigen Bewertung in In-vivo-Langzeitexpositionsstudien zu untersuchen.
PSD der CAG-erzeugten Aerosole
Die PSD der CAG-erzeugten Aerosole wurde unter verschiedenen Kühl- und ersten Verdünnungsströmen gemessen, um den Einfluss dieser Bedingungen auf die physikalischen Eigenschaften des Aerosols zu bewerten, das aus der flüssigen Basislösung erzeugt wird, die nur PG, VG, Wasser und Nikotin enthält. Dieses Verfahren ist unerlässlich, um geeignete Bedingungen für die Herstellung von Aerosolen mit Partikelgrößen im lungengängigen Bereich zu identifizieren.
In der vorliegenden Studie wurden Kühl- und erste Verdünnungsströme in Schritten von 10 l/min modifiziert, um das gleiche Gesamtvolumen des Aerosolflusses beizubehalten (Tabelle 4). Der Flüssigkeitsstrom (0,5 ml/min), der beheizte Durchfluss (2 l/min) und der zweite Verdünnungsstrom (150 l/min) wurden konstant gehalten. An der verdünnten Probenahmestelle b wurden Aerosolproben entnommen (Abbildung 5). PSD wurde unter Verwendung eines aerodynamischen Partikelgrößenmessers bestimmt, der Partikelgrößen von 0,5 bis 20 μm bei einer Probendurchflussrate von 5 l / min misst und für die Verwendung mit Geräten entsprechend verdünnt wurde. Die MMAD und GSD wurden vom aerodynamischen Partikelgrößenmesser für jeden Aerosolerzeugungslauf gemeldet.
Die Erhöhung des Kühlstroms und die gleichzeitige Abnahme des ersten Verdünnungsstroms wirkten sich auf die Größe der Aerosolpartikel aus (Tabelle 4). Der größte Einfluss auf die Partikelgröße wurde beobachtet, wenn der Kühlstrom von 10 auf 20 L/min und der erste Verdünnungsstrom von 160 auf 150 L/min geändert wurde. Der MMAD hat sich unter diesen Bedingungen von 1,47 auf 4,03 μm mehr als verdoppelt. Die durchschnittliche Aerosolpartikelgröße wuchs mit den zunehmenden Abkühlungsraten weiter, wenn auch in niedrigeren Verhältnissen als die zwischen 10 und 20 l/min beobachteten. Die Verteilung des aerodynamischen Durchmessers der Aerosolpartikel wurde deutlich in Richtung größerer Durchmesser verschoben, wenn man die bei einem Kühlstrom von 10 l/min erzeugten Aerosole mit denen vergleicht, die bei 20-50 l/min erzeugt werden (Abbildung 8).
Fangeffizienz von E-Liquid-Aromen
Wie bereits erwähnt, sind verschiedene flüssige Bestandteile aufgrund ihrer Flüchtigkeit in Abhängigkeit von den lokalen thermodynamischen Bedingungen kontinuierlich anfällig für den Gas-Flüssig-Stofftransfer. Darüber hinaus haben analytische Methoden eine gewisse Fähigkeit, solche Bestandteile einzufangen. Tatsächliche Ausbeutemessungen ermöglichen es uns, die Fähigkeit chemischer Methoden zum genauen Nachweis und zur Quantifizierung ausgewählter Bestandteile zu messen (z. B. aufgrund ihres Kondensationspotenzials oder ihrer Reaktionen erreichen einige Bestandteile möglicherweise nicht ihr Ziel, d. H. Die Expositionskammer im Falle von Inhalationsstudien). Daher ist es bei der Beurteilung verschiedener aromatisierter E-Liquid-Formulierungen unerlässlich, die effizienteste Fangmethode für die chemische Beurteilung des Aerosols bestimmen zu können. Anschließend können wir so die Übertragungsrate für jeden Bestandteil messen, die durch die oft vorhandenen Verluste durch den Aerosoltransport vom Ort der Erzeugung zur Expositionskammer bestimmt wird. Im vorliegenden Fall wurde eine zusätzliche Studie mit einer Flüssigkeit durchgeführt, die eine Mischung von Aromastoffen enthielt. Das Aerosol wurde mit den in Tabelle 2 aufgeführten CAG-Parametern erzeugt und nach der Verdünnung eingeschlossen (Position b, Abbildung 5), wobei die Probenahmedurchflussrate für 30 min auf 0,7 l/min festgelegt war. Das Trapping wurde an Probenahmesäulen durchgeführt, die mit 2 ml Isopropanol vorkonditioniert waren. Die Kartuschen wurden kurz nach Abschluss der Fangphase mit Isopropanol eluiert, bis 20 ml der Lösung zurückgewonnen waren. Wir fanden heraus, dass die Fangeffizienz im Allgemeinen für jeden Geschmacksbestandteil untersucht und bestimmt werden sollte.
Für 70% der untersuchten Geschmacksbestandteile hatten wir Rückgewinnungsraten >60%, was gut mit den Siedepunkten (Volatilität) der Aromen korrelierte. Diese Tatsache impliziert, dass inhalative toxikologische Studien, die komplexe Gemische enthalten, mit besonderem Augenmerk auf die Übertragung und Abgabe von Aerosol an die Expositionsstelle durchgeführt werden sollten.
Abbildung 1: Funktionsprinzip des Kapillaraerosolgenerators (CAG). Die Flüssigkeit wird in eine elektrisch beheizte Kapillare gepumpt, die Ausbrüche von heißen übersättigten Dämpfen liefert, die durch den Luftstrom abgekühlt werden, was zu plötzlicher Keimbildung und Kondensation führt, was zur Aerosolbildung führt. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
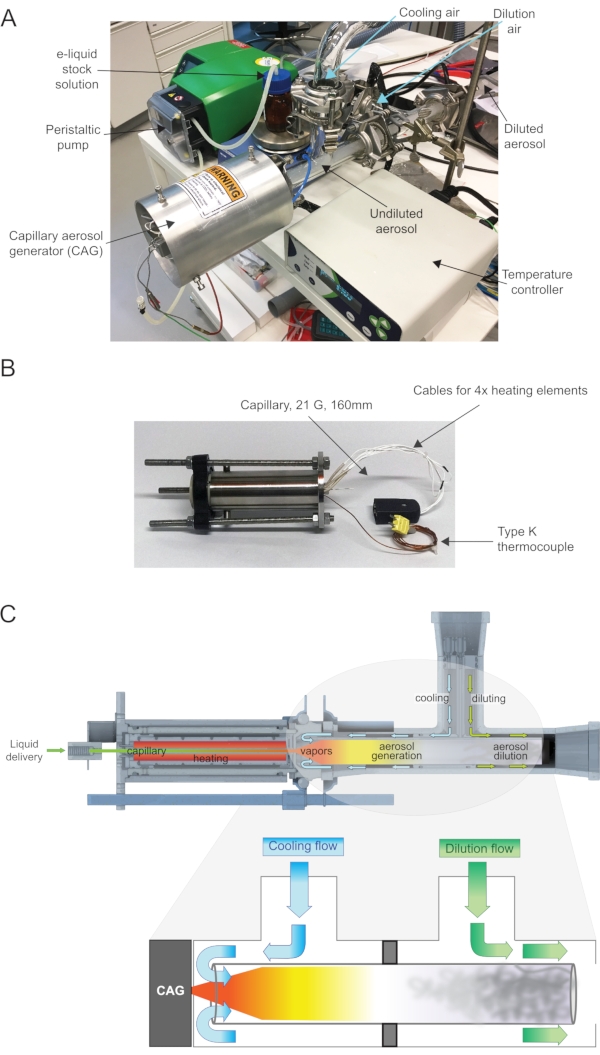
Abbildung 2: Typischer CAG-Versuchsaufbau und Schlüsselelemente . (A) Allgemeine Ansicht der CAG-Baugruppe, die die Peristaltikpumpe zeigt, die die flüssige Materiallösung mit dem CAG, dem Verdünnungsluftkanal und dem Aerosolbildungsprozess verbindet. (B) Detailansicht des CAG mit Kapillar- und Heizelementen. (C) Querschnittsansicht des CAG-Baugruppen-Aerosolerzeugungsaufbaus. Details zu den Kühl- und Verdünnungsluftströmen. Die Glasröhre hat zwei separate Fächer. Der Kühlstrom wird in Richtung des CAG gedrückt und tritt in Kontakt mit dem flüssig erzeugten Dampf ein, um das Aerosol zu erzeugen. Der Verdünnungsstrom wird in Richtung des gebildeten Aerosols gedrückt, um dieses zu verdünnen. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
Abbildung 3: Details des CAG-Geräts: Querschnittsansicht. Der Heizstrom wird um die Heizelemente herum eingeführt, um den externen CAG-Körper zu kühlen, die Kondensation des Flüssigkeitsrückflusses an der Spitze der Kapillare zu verhindern und den Dampfstrahlausbruch zu stabilisieren. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.

Abbildung 4: CAG-Baugruppe Die Kapillare und das Heizelement (A) werden in ein PEEK-Innenrohr eingeführt, und diese Baugruppe wird in ein äußeres Edelstahlrohr (B) geschoben. Die Baugruppe ist gekappt und mit Edelstahl-Gewindespindeln (C,D) fest auf einer Stütze befestigt. Die Kapillare, die aus dem hinteren Ende herausragt, ist über Schläuche mit der Peristaltikpumpe und der flüssigen Formulierung verbunden. Abkürzungen: SS, Edelstahl. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
Abbildung 5: CAG-Aerosolerzeugungseinstellungen für In-vivo-Expositionsexperimente . Die Aerosolprobenahme für die Analyse erfolgt an zwei Positionen: (a) unverdünntes Aerosol - der erste Verdünnungsschritt wird während der Probenahme abgeschaltet; b) verdünntes Aerosol kurz vor dem Betreten der Expositionskammer. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.

Abbildung 6: Beispielspalte mit angeschlossenen Adaptern. Vor der Probenahme wird die Probensäule mit 0,5 M Schwefelsäure für die Nikotinanalyse oder Isopropanol für die Aromaanalyse vorkonditioniert. Der Einlassadapter wird an den CAG-erzeugten Aerosolstrom und der Auslassadapter an die Vakuumpumpe angeschlossen. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
Abbildung 7: Charakterisierung und Reproduzierbarkeit von CAG-erzeugten Aerosolen. Die Konzentration von ACM-, Nikotin-, PG- und VG-Konzentrationen über 10 separate experimentelle Aerosolerzeugung läuft mit derselben flüssigen Basislösung. ACM, 1105,45 ± 27,4 μg/l; Nikotin, 20,16 ± 0,7 μg/L; VG, 227,15 ± 7,8 μg/L; PG, 656,59 ± 22,0 μg/L. Fehlerbalken stellen die Standardabweichung dar. Abkürzungen: ACM, aerosol collected mass; PG, Propylenglykol; VG, Glycerin. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
Abbildung 8: Änderungen in der Partikelgrößenverteilung von Aerosol, das unter verschiedenen Kühldurchflussraten erzeugt wird. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
| BASIS (PG/VG/N) | GESCHMACK (PG/VG/N/F) | |
| Bestandteil | PG/VG/N (g/1000g) | PG/VG/N/F (g/1000g) |
| Benzoesäure | 3.33 | 3.33 |
| PG | 240.00 | 238.91 |
| Wasser | 150.00 | 150.00 |
| Milchsäure | 3.33 | 3.33 |
| Essigsäure | 3.33 | 3.33 |
| Gemischte Geschmacksmischung | 0.00 | 1.20 |
| Glyzerin | 560.01 | 559.90 |
| Nikotin | 40.00 | 40.00 |
| Summe | 1000.00 | 1000.00 |
Tabelle 1: Formulierungskomponenten für E-Liquid-Stoffe18
| Aerosolisierungsprotokoll | Sampling-Protokoll | ||||
| Parameter | Unverdünnt | Verdünnt | Parameter | Unverdünnter Standort A | Verdünnte Position B |
| CAG-Temperatur (°C) | 250 | ||||
| Pumpendurchfluss (mL/min) | 0.5 | 0.5 | Probenahmezeit (min) | 10 | 30 |
| Beheizter Luftstrom (L/min) | 2 | 2 | Probenahmefluss (ACM) (L/min) | 0.7 | 1.5 |
| Kühlluftstrom (L/min) | 10 | 10 | Probenahmestrom Extrelut (L/min) | 0.7 | 0.7 |
| 1. Luftverdünnung (L/min) | NA | 150 | Probenahmestrom Carbonyle (L/min) | 0.7 | 0.7 |
| 2. Luftverdünnung (L/min) | NA | 160 | |||
| Abfall (L/min) | NA | 172 | |||
Tabelle 2: Parameter der Aerosolerzeugung, -verdünnung und -probenahme
| Carbonyle | Basisflüssigkeit (PG/VG/Nikotin) | Geschmack Stammlösung hohe Konzentration mit Nikotin (PG / VG / Nikotin / Aromen) | ||
| Unverdünnte Aerosolprobe μg/L | Verdünnte Aerosolprobe μg/L | Unverdünnte Aerosolprobe μg/L | Verdünnte Aerosolprobe μg/L | |
| Acetaldehyd | 0,834 ± 0,096 | 0.119* | 45.346 ± 1.134 | 2.058 ± 0.202 |
| Aceton | < LOC | < LOC | < LOC | < LOC |
| Acrolein | < LOC | < LOC | < LOC | < LOC |
| Butyraldehyd | < LOC | < LOC | 36,475 ± 0,996 | 1,557 ± 0,179 |
| Crotonaldehyd | < LOC | < LOC | 0,052 ± 0,001 | < LOC |
| Formaldehyd | 0,731 ± 0,072 | 0,072 ± 0,023 | 0,158 ± 0,007 | 0,026 ± 0,004 |
| Methylethylketon | < LOC | < LOC | 0,570 ± 0,015 | < LOC |
| Propionaldehyd | < LOC | < LOC | 0,085 ± 0,001 | < LOC |
Tabelle 3: Bestimmung von Carbonylen im CAG-erzeugten Aerosol. Durchschnittswerte aus drei Aerosolerzeugungen laufen mit der gleichen flüssigen Basislösung allein und mit einer Aromamischung. Nur eine Stichprobe über drei Durchläufe hatte Werte, die größer waren als die untere Quantifizierungsgrenze (LOQ) der Methode.
| Einstellungen (L/min) | Durchmesser der Aerosoltröpfchen | ||
| Kühlfluss | 1. Verdünnungsstrom | MMAD (μm) | GSD |
| 10 | 160 | 1,47 ± 0,04 | 2,07 ± 0,01 |
| 20 | 150 | 4,03 ± 0,18 | 2,13 ± 0,04 |
| 30 | 140 | 4,74 ± 0,04 | 1,89 ± 0,02 |
| 40 | 130 | 5,35 ± 0,04 | 1,80 ± 0,01 |
| 50 | 120 | 5,23 ± 0,03 | 1,76 ± 0,01 |
Tabelle 4: Bestimmung der Aerosolpartikelgröße (Tröpfchendurchmesser) unter verschiedenen Luftströmungsbedingungen. Abkürzungen: MMAD, Mass Median Aerodynamic Diameter; GSD, geometrische Standardabweichung.
Diskussion
Die Erzeugung von Aerosolen mit CAG trägt dazu bei, die Variabilität von EC-Geräte-spezifischen Aerosolisierungsprozessen zu reduzieren, was eine objektive und kontrollierbare Bewertung der aerosolisierten E-Liquid-Formulierung selbst ermöglicht. Es hat sich gezeigt, dass CAG-erzeugte Aerosole repräsentativ für die von ECs7 erzeugten Aerosole sind. Sie können reproduzierbar mit der gleichen Zusammensetzung und den gleichen Eigenschaften erzeugt werden und eignen sich daher besonders für in vivo Langzeitexpositionsstudien, die große Mengen an Aerosol über einen langen Zeitraum erfordern8.
Das CAG-Setup ist relativ einfach zu montieren und einfach zu warten. Die Betriebsparameter wie der Flüssigkeitsdurchsatz und die jeweiligen Luftdurchflussraten bleiben jedoch für die Herstellung von kontrolliertem Aerosol kritisch, was eine Methodenoptimierung entsprechend dem Zweck der Anwendung des CAG-erzeugten Aerosols erfordert.
Die in der aktuellen Studie vorgestellten Ergebnisse zeigen, dass der Kühlluftdurchsatz einen deutlichen Einfluss auf die Größenverteilung von Aerosolpartikeln hat. Der Kühlluftstrom hat einen direkten Einfluss nicht nur auf die Keimbildung der erzeugten Dämpfe, sondern auch auf die Kondensation, da der Innenschlauch, in den das erzeugte Aerosol fließt, abgekühlt wird. Darüber hinaus ist das dichte Aerosol anfällig für erhebliche Gerinnungseffekte. Zusammengenommen sind diese Prozesse komplex und ihre Wechselwirkung und ihr Einfluss auf die Aerosolbildung sind für die spezifischen E-Flüssigkeiten, Temperaturen und Strömungen eher schwer zu verallgemeinern. Die zusätzliche Zusammensetzung des Luftstroms (trocken oder mit einem festen Prozentsatz relativer Luftfeuchtigkeit befeuchtet) - insbesondere der Wassergehalt - beeinflusst Wärme und Massenaustausch, was nicht nur zu einem modulierten Kondensationswachstum von Aerosolpartikeln, sondern auch zu Wandkondensation führt. Daher gelten Änderungen an den Parametern dieser Methode als Verwendungszweck in Bezug auf die Kontrolle der PSD17,19.
Das Vorhandensein von Chemikalien mit geringer Löslichkeit oder hohen Siedepunkten könnte die Wirksamkeit von CAG-erzeugtem Aerosol aufgrund von Ausfällungen innerhalb der Kapillare und Verstopfung der Kapillare im Laufe der Zeit einschränken. Abhängig von den im Aerosol vorhandenen Chemikalien muss die Temperatur für den Betrieb des CAG angepasst werden, um den Dampf zu erzeugen. Darüber hinaus sollte die Stabilität der flüssigen Formulierung regelmäßig bewertet werden. Die Zugabe von Bestandteilen, einschließlich Aromen, mit unterschiedlichen Siedepunkten hat einen Einfluss auf die endgültige Aerosolzusammensetzung14 und die Gas-Flüssig-Partitionierung. Es kann notwendig sein, die Kapillartemperatur und den Wärmeluftstrom anzupassen, um einen Rückfluss und eine Ablagerung von Flüssigkeiten in der Nähe der heißen Kapillare zu verhindern, was aufgrund der langen Dauer der Retention der Flüssigkeit bei einer hohen Temperatur zur Erzeugung unkontrollierter Produkte des thermischen Abbaus (z. B. Carbonyle) führen könnte. Darüber hinaus hat die Kontrolle der Temperatur, die zur Erzeugung des Dampfes in der Kapillare verwendet wird, einen Einfluss darauf, wo sich der Dampf in der Kapillare zu bilden beginnt - je höher die Temperatur, desto früher wird der Dampf gebildet. Bei einer höheren Kapillartemperatur dauert es länger, bis der aus der Kapillare austretende Dampf durch den Kühlluftstrom abgekühlt wird, und beginnt daher, sich zu keimen und zu einem Aerosol zu kondensieren, das weiter von der Kapillarspitze entfernt ist, wodurch ein Rückflusseffekt vermiedenwird 19.
Aktuelle e-Liquid-In-vivo-Toxikologiestudien sind bei der Reproduktion von E-Zigaretten-Aerosolen aufgrund der logistischen Komplexität, um die erforderliche Aerosolskala zu erfüllen, begrenzt, wie in einer OECD TG 413-Studie20. Das in dieser Studie vorgestellte Protokoll gibt einen Überblick über den CAG-Aufbau und die Einstellungen, die bei Philip Morris International für die Aerosolerzeugung in in vivo-Langzeitexpositionsstudien verwendet werden18. Diese Daten können als guter Ausgangspunkt für die weitere Feinabstimmung in einer anderen Laborumgebung (z. B. Drug-Delivery-Systeme21) oder für die Anpassung an spezifische Anforderungen einer bestimmten Studie dienen.
Offenlegungen
Die hier beschriebene Methode sowie die spezifische CAG-Baugruppe wurden zur Bewertung von Aerosolen aus E-Liquids entwickelt, um die Anforderungen von In-vivo-Expositionsstudien zu erfüllen. Alle Autoren sind Mitarbeiter von Philip Morris International (PMI) oder haben im Rahmen vertraglicher Vereinbarungen für PMI gearbeitet. Philip Morris International ist die einzige Finanzierungsquelle und Sponsor dieser Studie.
Materialien
| Name | Company | Catalog Number | Comments |
| Aluminium front cap | Mecanique Buri S.A., La Chaux-de Fonds, Switzerland | Custom Built | Purpose built, 1 x |
| Aluminium heating block, groove diameter 0.4mm | Phil Gunn Machine Co., Inc, VA, USA | B-505432 | 2 x |
| Aluminium rear cap | Mecanique Buri S.A., La Chaux-de Fonds, Switzerland | Custom Built | 1 x |
| Cambridge glass filter pads | GE Healthcare UK Limited | 9703-9654 | 44 mm diameter |
| Capillary 21 G SS, 160 mm | Phil Gunn Machine Co., Inc, VA, USA | 304H21RW | 1 x |
| Dry wipes | Contec Inc. , SC, USA | Prosat Wipes saturated with isopropyl alcohol | cleaning material |
| Flowmeter | TSI, Shoreview, MI, USA | 4100 Series, 0-20 L/min | or equivalent |
| Gilibrator-2 calibrator | Sensidyne, St-Petersburg FL, USA | Gilian Gilibrator-2 | Air flow calibrator |
| Glass Couplings | Labo Service, Kontich, Belgium | QVF | |
| Glass piping | Labo Service, Kontich, Belgium | QVF | Pipe 25 and 40 mm |
| Heating elements | Phil Gunn Machine Co., Inc, VA, USA | LDC01864 | 4 x |
| High heat grease | Lubriplate Lubricant Company, NJ, USA | High temperature multipurpose grease | CAG maintenance |
| Inner PEEK tube | Mecanique Buri S.A., La Chaux-de Fonds, Switzerland | Custom Built | 1 x |
| Magnetic stirrer | IKA-Werke GmbH & Co. KG, Staufen, Germany | C-MAG HS 4 | or equivalent |
| Micro impingers | Labo Service, Kontich, Belgium | Custom Built | |
| Outer SS tube | Mecanique Buri S.A., La Chaux-de Fonds, Switzerland | Custom Built | 1 x |
| PEEK adaptor | Mecanique Buri S.A., La Chaux-de Fonds, Switzerland | Custom Built | Purpose built, 1 x |
| Peristaltic pump | Watson-Marlow Fluid Technology Group, Falmouth, UK | Watson-Marlow 530 U | or equivalent |
| Push-in fitting | Festo Pte Ltd | NPQM-DK-M5-Q4-P10 | 1 x |
| Sample Column Extrelut NT3 cartridge | Merk Sigma-Aldrich | 115095 | |
| SS 25 mm assembly cap | Mecanique Buri S.A., La Chaux-de Fonds, Switzerland | Custom Built | Purpose built, 1 x |
| SS M8 lead screw | Mecanique Buri S.A., La Chaux-de Fonds, Switzerland | Custom Built | 3 x |
| SS M8 nut | Mecanique Buri S.A., La Chaux-de Fonds, Switzerland | Custom Built | 3 x |
| SS rear backing | Mecanique Buri S.A., La Chaux-de Fonds, Switzerland | Custom Built | Purpose built, 1 x |
| Temperature controller | Cole Parmer GmbH, Wertheim, Germany | Digi-Sense TC 9600 | or equivalent |
| Thermocouple type K | RS Components GmbH, Wädenswil, Switzerland | 814-0147 | 1 x |
Referenzen
- Williams, M., Talbot, P. Variability among electronic cigarettes in the pressure drop, airflow rate, and aerosol production. Nicotine and Tobacco Research. 13 (12), 1276-1283 (2011).
- Farsalinos, K. E., Voudris, V., Poulas, K. E-cigarettes generate high levels of aldehydes only in 'dry puff' conditions. Addiction. 110 (8), 1352-1356 (2015).
- Werley, M. S., et al. Toxicological assessment of a prototype e-cigaret device and three flavor formulations: a 90-day inhalation study in rats. Inhalation Toxicology. 28 (1), 22-38 (2015).
- Werley, M. S., et al. Non-clinical safety and pharmacokinetic evaluations of propylene glycol aerosol in Sprague-Dawley rats and Beagle dogs. Toxicology. 287 (1-3), 76-90 (2011).
- Werley, M. S., et al. Prototype e-cigarette and the capillary aerosol generator (CAG) comparison and qualification for use in subchronic inhalation exposure testing. Aerosol Science and Technology. 50 (12), 1284-1293 (2016).
- Williams, M., Villarreal, A., Bozhilov, K., Lin, S., Talbot, P. Metal and silicate particles including nanoparticles are present in electronic cigarette cartomizer fluid and aerosol. PLoS One. 8 (3), 57987 (2013).
- Bekki, K., Uchiyama, S., Ohta, K., Inaba, Y., Kunugita, N. Carbonyl compounds generated from electronic cigarettes. International Journal of Environmental Research and Public Health. 11 (11), 11192-11200 (2014).
- Flora, J. W., et al. Characterization of potential impurities and degradation products in electronic cigarette formulations and aerosols. Regulatory Toxicology and Pharmacology. 74, 1-11 (2016).
- Tobacco Products Directive. Directive 2014/40/EU of the European Parliament and of the Council on 3 April 2014 Available from: https://ec.europa.eu/health/sites/health/files/tobacco/docs/dir_201440_en.pdf (2014)
- Farsalinos, K. E., Le Houezec, J. Regulation in the face of uncertainty: the evidence on electronic nicotine delivery systems (e-cigarettes). Risk Management and Healthcare Policy. 8, 157-167 (2015).
- McNeill, A., Brose, L., Calder, R., Bauld, L., Robson, D. Evidence review of e-cigarettes and heated tobacco products 2018. A report commissioned by Public Health England. Public Health England. , (2018).
- Howell, T. M., Sweeney, W. R. Aerosol and a method and apparatus for generating an aerosol. US Patent. , (1998).
- Dutra, L. M., Grana, R., Glantz, S. A. Philip Morris research on precursors to the modern e-cigarette since 1990. Tobacco Control. 26, 97-105 (2017).
- Gupta, R., Hindle, M., Byron, P. R., Cox, K. A., McRae, D. D. Investigation of a novel Condensation Aerosol Generator: solute and solvent effects. Aerosol Science and Technology. 37 (8), 672-681 (2003).
- Geiss, O., Bianchi, I., Barrero-Moreno, J. Correlation of volatile carbonyl yields emitted by e-cigarettes with the temperature of the heating coil and the perceived sensorial quality of the generated vapours. International Journal of Hygiene and Environmental Health. 219 (3), 268-277 (2016).
- Hong, J. N., Hindle, M., Byron, P. R. Control of particle size by coagulation of novel condensation aerosols in reservoir chambers. Journal of Aerosol Medicine. 15 (4), 359-368 (2002).
- Taylor, G., Warren, S., McRae, D., Venitz, J. Human deposition and exposure studies with propylene glycol aerosols produced using the CAG technology platform. Respiratory Drug Delivery. 1, 183-190 (2006).
- Wong, E. T., et al. A 6-month inhalation toxicology study in Apoe -/- mice demonstrates substantially lower effects of e-vapor aerosol compared with cigarette smoke in the respiratory tract. Archive of Toxicology. 95 (5), 1805-1829 (2021).
- Shen, X., Hindle, M., Byron, P. R. Effect of energy on propylene glycol aerosols using the capillary aerosol generator. International Journal of Pharmaceutics. 275 (1-2), 249-258 (2004).
- Phillips, B., et al. Toxicity of the main electronic cigarette components, propylene glycol, glycerin, and nicotine, in Sprague-Dawley rats in a 90-day OECD inhalation study complemented by molecular endpoints. Food and Chemical Toxicology. 109, 315-332 (2017).
- Hindle, M., Cox, K. A., Gupta, R. Adding pharmaceutical flexibility to the capillary aerosol generator. Proceedings of Respiratory Drug Delivery IX. (Volume III). , 247-253 (2004).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten