Method Article
Istituzione e manutenzione di scarafaggi americani gnotobiotici (Periplaneta americana)
In questo articolo
Riepilogo
Questo protocollo viene utilizzato per stabilire e mantenere gli scarafaggi americani gnotobiotici (Periplaneta americana) sterilizzando in superficie i casi di uova (oothecae) prima della schiusa. Questi insetti gnotobiotici contengono i loro endosombionti Blattabacterium trasmessi verticalmente ma hanno fegato axenico.
Abstract
Gli animali gnotobiotici sono un potente strumento per lo studio dei controlli sulla struttura e la funzione del microbioma. Presentato qui è un protocollo per la creazione e il mantenimento di scarafaggi americani gnotobiotici (Periplaneta americana). Questo approccio include controlli di sterilità integrati per il controllo di qualità continuo. Gli insetti gnotobiotici sono definiti qui come scarafaggi che contengono ancora il loro endosimbiont trasmesso verticalmente (Blattabacterium) ma mancano di altri microbi che normalmente risiedono sulla loro superficie e nel loro tratto digestivo. Per questo protocollo, i casi di uova (oothecae) vengono rimossi da una colonia di stock (non sterilizzale) e sterilizzati in superficie. Una volta raccolte e sterilizzate, le ootecae vengono incubate a 30 °C per circa 4−6 settimane sull'agar dell'infusione cervello-cuore (BHI) fino a quando non si schiudono o vengono rimosse a causa della contaminazione. Le ninfe tratteggiate vengono trasferite in un pallone Erlenmeyer contenente un pavimento BHI, acqua sterile e cibo sterile per topi. Per garantire che le ninfe non alloggino microbi che non sono in grado di crescere su BHI nelle condizioni date, una misura aggiuntiva di controllo qualità utilizza polimorfismo di lunghezza dei frammenti di restrizione (RFLP) per testare i microbi nonendosimicbiotici. Le ninfe gnotobiotiche generate utilizzando questo approccio possono essere inoculate con comunità microbiche semplici o complesse e utilizzate come strumento negli studi sul microbioma intestinale.
Introduzione
Gli animali gnotobiotici hanno dimostrato di essere strumenti inestimabili per gli studi sul microbioma1,2,3. Gli animali privi di germi e a flora definita hanno permesso di inucidazione delle interazioni ospite-microbo, comprese le risposte immunologiche dell'ospite, la maturazione epiteliale intestinale e il metabolismo ospite1,4,5,6,7. Gli animali gnotobiotici inoculati con una comunità semplificata hanno anche aiutato in una comprensione più completa delle interazioni microbo-microbo in una comunità intestinale, in particolare nello svelare l'alimentazione incrociata e le relazioni antagonistiche8,9,10,11. L'attuale sistema modello preferito per gli studi sul microbioma intestinale dei mammiferi è il modello murino. Sebbene questo sistema sia stato vitale nelle scoperte sopra descritte, una lacuna fondamentale è il costo. Attrezzature specializzate e tecnici altamente qualificati sono necessari per stabilire e mantenere una struttura gnotobiotica. Questo, in combinazione con una cura extra che deve essere data ad ogni aspetto del mantenimento degli animali gnotobiotici, fa sì che un animale gnotobiotico costi da dieci a venti volte di più per riprodursi rispetto a un animale standardmodello 12. A causa dei costi elevati, molti ricercatori potrebbero non essere in grado di permettersi un modello murino gnotobiotico. Inoltre, mentre i modelli murini possono essere la scelta più ampiamente accettata per gli studi che cercano di tradurre in salute umana, ci sono ancora molte differenze fisiologiche e morfologiche tra budella umana e topo13. Chiaramente nessun modello singolare è sufficiente per rispondere al numero sempre crescente di domande riguardanti i molti aspetti del microbioma intestinale.
I modelli di insetti sono un'alternativa più economica a causa del loro minor costo di manutenzione rispetto alle specie di mammiferi. Un'ampia ricerca senza germi e gnotobiotica in una varietà di specie di insetti ha portato allo sviluppo di più modelli comunemente usati. Zanzare e Drosophila sono modelli comuni per il lavoro privo di germi a causa della loro rilevanza per le malattie globali e la trattabilità genetica14,15. Un altro sistema di modelli emergenti è quello dell'apemellifera ( Apis mellifera), data la sua importanza nella ricerca sull'impollinazione e lasocialità 16. Tuttavia, molti di questi insetti comunemente usati mancano della complessità tassonomica osservata nelle comunità intestinali dei mammiferi17,limitando la loro capacità di modellare interazioni di ordine superiore. Non solo la totale diversità dei microbi trovati nell'intestino degli scarafaggi americani è più simile ai mammiferi, ma molti dei microbi presenti nell'intestino scarafaggio appartengono a famiglie e filla che si trovano comunemente nel microbiota intestinale di mammiferi e umani18. Il broncio posteriore dello scarafaggio è anche funzionalmente analogo all'intestino crasso dei mammiferi, in quanto è una camera di fermentazione densamente piena di batteri per aiutare nell'estrazionedei nutrienti 19,20. Infine, la natura onnivora degli scarafaggi consente una diversità di regimi dietetici che non sarebbe possibile con gli specialisti dietetici.
Gli scarafaggi americani possono essere un utile sistema modello per comprendere le comunità microbiche intestinali negli organismi superiori, ma lo stato dello scarafaggio come parassita rende anche questo sistema rilevante per il controllo dei parassiti21. Sfruttare la conoscenza fondamentale dell'influenza della comunità intestinale sulla salute e la fisiologia degli scarafaggi aiuta a sviluppare nuove tecniche per la gestione dei parassiti.
L'obiettivo di questo metodo è quello di delineare una descrizione completa della creazione e del mantenimento di scarafaggi americani gnotobiotici (Periplaneta americana), ma questo protocollo potrebbe essere utilizzato per generare ninfe di qualsiasi scarafaggio oviparo. Include un metodo per una raccolta efficiente e non invasiva di ootece mature e una tecnica non distruttiva per monitorare lo stato gnotobioticodegli insetti 22,23,24. Mentre i precedenti metodi per raggiungere e mantenere gli scarafaggi gnotobiotici descrivono la raccolta di ootheca23,24,25,26,27, la maturità dell'ootheca viene interpretata in termini di spunti specifici per specie (in Blattella germanica22,24,25), o non esplicitamente descritta27,28, rendendo difficile l'implementazione per chi non ha familiarità con il sistema. Poiché il metodo qui descritto utilizza ootecae cadute naturalmente, l'errore di rimuovere prematuramente le uova è assente. Questo protocollo contiene metodi di controllo della qualità dipendenti dalla cultura e indipendenti dalla cultura, e il metodo dipendente dalla coltura non richiede il sacrificio degli insetti. Infine, questo metodo riunisce le informazioni di più studi di scarafaggi gnotobiotici per creare un unico protocollo completo con tutte le informazioni necessarie per raggiungere e mantenere gli scarafaggi gnotobiotici.
Protocollo
1. Preparazione dei materiali
- Mantenimento delle colture di scarafaggi stock
NOTA: Ci sono molti modi per allevare questi robusti insetti. Le specifiche sulla fornitura di riparo e acqua possono essere diverse a seconda dei materiali accessibili (ad esempio, cartoni per uova invece di tubi di cartone). Il seguente protocollo di sterilizzazione funzionerà per qualsiasi configurazione del serbatoio di magazzino.- Stendere abbastanza letti in trucioli di legno in un serbatoio di pesce da 37,85 L (10 galloni) per coprire il fondo del serbatoio con circa 1 pollice di biancheria da letto. Preparare l'alloggiamento tagliando il cartone (piatto) a 2 x 4 in pezzi. Inserire pezzi di cartone in tubi di cartone (ad esempio tubi di carta igienica) e impilare i tubi ad un'estremità del serbatoio(figura 1).
- Spalmare un sottile strato di vaselina sui primi due pollici dell'interno del serbatoio per evitare la fuga degli insetti.
NOTA: Assicurarsi di rivestire correttamente l'interno degli angoli del serbatoio. - Aggiungi scarafaggi trasferendo tubi di cartone (occupati) da un precedente serbatoio di magazzino, scuotendoli per rilasciare i loro abitanti. Per ogni trasferimento, spostare 100−200 scarafaggi a età mista e a sesso misto. Aggiungere cibo per cani (20−30 pezzi), monitorare la quantità di cibo per cani nel serbatoio e ricaricare quando è basso.
- Alleva un piatto d'acqua.
- Riempire un piccolo contenitore di plastica riutilizzabile con acqua distillata doppia (ddH2O). Tagliare spugne e fori di cellulosa nel coperchio del contenitore del cibo all'incirca della stessa dimensione.
NOTA: Le spugne di cellulosa impediscono agli scarafaggi di annegare nel piatto d'acqua.
- Riempire un piccolo contenitore di plastica riutilizzabile con acqua distillata doppia (ddH2O). Tagliare spugne e fori di cellulosa nel coperchio del contenitore del cibo all'incirca della stessa dimensione.
- Inserire spugne nei fori nel coperchio e posizionare il coperchio sul contenitore riempito. Posizionare il contenitore nel serbatoio e ricaricare quando è basso. Coprire il serbatoio con un panno di cotone e fissarlo in posizione con una fascia elastica.
- Quando i serbatoi iniziano ad accumulare quantità eccessive di frass e carcasse di insetti, imposta nuovi serbatoi e trasferisci scarafaggi.
NOTA: i carri armati vengono in genere trasferiti ogni 6 mesi. Tutti gli scarafaggi /uova rimanenti nei serbatoi di stoccaggio dismessa vengono eutanasiati congelando a -20 °C per 1 h e il contenuto del serbatoio di stoccaggio viene quindi trasferito in un sacchetto autoclave e autoclavato (1 h, ciclo di gravità) prima dello smaltimento. I serbatoi di magazzino vengono sterilizzati con candeggina al 2% tra un uso e l'altro.
- Disinfettare un contenitore secondario.
NOTA: Questo contenitore non include un filtro, ma consente invece lo scambio d'aria gratuito.- Spruzzare l'interno sia del coperchio che del fondo con candeggina al 2% e lasciare in ammollo per 10 minuti. Pulire la candeggina con un tovagliolo di carta pulito.
- Spruzzare l'interno del coperchio e del fondo con etanolo al 70% e asciugare con un tovagliolo di carta pulito. Sostituire il coperchio fino all'uso.
- Fai inclinazioni e fiasche BHI per incubare uova e ospitare ninfe.
- Preparare BHI secondo le istruzioni del pacchetto, aggiungendo il 2% di agar. Far bollire la soluzione BHI-agar fino a quando non viene chiarita.
- Per le inclinazioni, trasferire aliquote da 5 ml a provette e tappo in vetro da 18 mm x 150 mm. Sterilizzare tramite autoclave (tempo di sterilizzazione = 20 min, ciclo liquido). Posizionare tubi autoclavati con un angolo di 45° per raffreddarsi in inclinazioni. Una volta solidificato, conservare in frigorifero fino all'uso per evitare l'essiccazione.
- Per i contenitori, trasferire aliquote da 10 ml di soluzione di agar BHI bollita in mastri Erlenmeyer da 250 mL per coprire completamente il fondo del pallone. Coprire il pallone con un foglio e sterilizzare tramite autoclave (20 min, ciclo liquido). Lasciare raffreddare e raffreddare i contenitori autoclavati fino all'uso per evitare l'essiccazione.
NOTA: non è necessario alcun filtro dell'aria per questa configurazione. Il coperchio del foglio è sufficiente per consentire lo scambio di gas prevenendo al contempo la contaminazione dal flusso all'aperto.
- Sterilizzare tramite autoclave: chow di ratto autoclavabile suddiviso in mezze dimensioni (~ pezzi da 1/2 pollice) in un becher coperto di fogli (tempo di sterilizzazione = 1 h, ciclo di gravità), ddH2O in una bottiglia limitata (tempo di sterilizzazione = 20 minuti, ciclo liquido) e forcep in un becher coperto di fogli (tempo di sterilizzazione = 20 minuti, ciclo di gravità).
NOTA: Non riempire es oltre il becher chow del ratto. I pellet si gonfieranno nell'autoclave. - Alleva un carro armato del "reparto maternità".
NOTA: Questo serbatoio contiene gli stessi materiali dei serbatoi di stoccaggio (tubi di cartone, piatti d'acqua con spugne, cibo per cani, biancheria da letto a cippato; vedi figura 1) e deve essere vuoto di scarafaggi a meno che non venga trasferito per la raccolta delle ootece (vedi sezione 2). - Umidificare un'incubatrice preparando un becher pieno di soluzione di cloruro di sodio supersaturo (NaCl). Preparare questa soluzione aggiungendo 37 g di NaCl per 100 mL di ddH2O e mescolando fino allo scioglimento.
NOTA: In genere, 500 mL di soluzione di sale saturo in genere umidificano un incubatore con dimensioni della camera 51 cm x 46 cm x 46 cm (H x W x D) per circa un mese prima di aggiungere più acqua.
2. Raccolta di oothecae
- Trasferire le femmine (in qualsiasi numero, a maggior dire per gli esperimenti pianificati) che trasportano oothecae (Figura 2) dal serbatoio di stoccaggio al "reparto maternità" utilizzando le forcep per spostare tubi di cartone che contengono femmine gravide.
- Se un tubo di carboard contiene più insetti oltre alla femmina gravita, prima scuoti il tubo in un contenitore di plastica aggiuntivo arato con vaselina, quindi incoraggia l'insetto bersaglio a risalire nel solo tubo di cartone.
- Trasferisci le femmine nel serbatoio di scorta una volta che hanno lasciato cadere le loro oothecae. Recupera le ootece dalla lettiera nel serbatoio con le forcep.
NOTA: Le oothecae vengono spesso eliminate entro 24 ore dal trasferimento della femmina.
3. Pulizia delle ootecae
- Aggiungere ootecae a un tubo di centrifuga da 5 ml contenente 3 ml di solfato di dodecil solfato di sodio (SDS). Vortice per 10 s. Ripetere per un secondo passaggio di lavaggio con un tubo di centrifuga contenente SDS fresco.
NOTA: Possono essere utilizzate fino a cinque ootecae per 3 mL di SDS. - Utilizzando una delicata salvietta per compiti, strofinare delicatamente la superficie di ogni ooteca per rimuovere eventuali detriti. È possibile aggiungere più SDS per facilitare una pulizia accurata. Mettere le ootece pulite in una barca di pesatura fino a quando non sono pronte per la sterilizzazione.
NOTA: Il protocollo può essere messo in pausa qui, ma lasciare le ootece in ambienti a bassa umidità per lunghi periodi di tempo (da giorni a settimane) li farà disidratare e perderà vitalità.
4. Sterilizzazione e incubazione delle ootecae
- Acqua sterile aliquota per risciacquo post-sterilizzazione. Per sterilizzare ogni ooteca, riempire due tubi di centrifuga da 1,5 ml con 1 ml di acqua sterile.
- Aggiungere 10 μL di concentrato (32%) soluzione di stock di acido peracetico a 3,2 ml di ddH2O in un tubo di centrifuga da 5 ml per creare una soluzione allo 0,1% per la sterilizzazione. Cappuccio e invertire più volte per mescolare.
ATTENZIONE: L'acido peracetico è dannoso a contatto con la pelle o i polmoni. Diluire in una cappa dei fumi.
NOTA: Questo deve essere fatto lo stesso giorno della sterilizzazione. Se diluita in anticipo, la soluzione si decompone rapidamente e quindi non sterilizza correttamente. Fino a cinque ootece pulite possono essere sterilizzate in 3,2 mL di acido diluito. - Posizionare (fino a cinque) ootece pulite nella soluzione di acido peracetico allo 0,1% per 5 min. Invertire il tubo più volte ogni 60 s.
- In una cappa a flusso laminare, utilizzare forcep sterili per trasferire ciascuna ooteca al proprio tubo di centrifuga con acqua di risciacquo sterile aliquota (fase 4.1). Invertire più volte per mescolare. Ripetere per un secondo risciacquo, quindi trasferire ogni ooteca risciacquata sulla propria inclinazione BHI utilizzando forcep sterili.
- Posizionare le inclinazioni nel contenitore secondario sterilizzato. Spostare il contenitore nell'incubatore umidificato a 30 °C per 4−5 settimane fino alla schiusa.
NOTA: Le inclinazioni possono essere tenute in posizione verticale da un piccolo porta provetta o da un becher medio/piccolo. - Controllare regolarmente le inclinazioni (1−2 volte a settimana). Se la crescita fungina o batterica della colonia appare sull'agar, rimuovere l'inclinazione contaminata. Quando il punto di tempo di quattro settimane si avvicina, controllare le inclinazioni ogni giorno.
NOTA: Una volta tratteggiate, le ninfe possono sopravvivere fino a diverse settimane solo su BHI ma non cresceranno in modo ottimale.
5. Mantenimento delle ninfe gnotobiotiche
- In una cappa di flusso laminare, trasferire aseticamente un pellet di chow di ratto sterilizzato in un pallone BHI preparato (dal passo 1.3.3) con forcep sterili. Come controllo di sterilità, posizionare il pallone nel contenitore secondario in un incubatore di 30 °C per 24 ore e non utilizzare se appare la crescita.
- Aggiungere ninfe al pallone BHI con pellet di cibo sterile. Scuoterli dalla loro inclinazione BHI e lasciarli cadere nel pallone in un cappuccio di flusso laminare.
NOTA: Le ninfe non hanno trazione sulle pareti di vetro della provetta. Scuotere il tubo per farli cadere dall'inclinazione e quindi ribaltare il tubo per consentire loro di scivolare giù per il vetro nel pallone è efficace. Mentre le ninfe possono essere trasferite usando le forcep, il rischio di lesioni mortali è elevato. - Ninfe d'acqua con 300 μL di acqua sterile una volta alla settimana in una cappa di flusso laminare tubazione direttamente sul pavimento BHI del pallone.
- Quando le feci delle ninfe iniziano a coprire il pavimento BHI, trasferire in un nuovo pallone BHI, aggiungendo il chow di ratto sterilizzato con 24 ore di anticipo (per verificare la sterilità) come nel passaggio 5.1.
6. Controllo di qualità della sterilità
- Rimuovere una ninfa dal pallone BHI da sacrificare per un controllo di qualità indipendente dalla cultura dello stato gnotobiotico tramite polimorfismo di restrizione della lunghezza del frammento (RFLP). Per fare questo, versare la ninfa in un tubo di centrifuga sterile (simile al trasferimento ninfa dal passo 5.1) o posizionare un applicatore di legno sterile nel pallone e attendere che una ninfa inizi a salire, quindi trasferirlo nel tubo di centrifuga.
- Aggiungere 0,5 ml di 1x soluzione salina tamponata di fosfato (PBS) alla ninfa nel tubo di centrifuga e omogeneizzare con una micropestola sterile fino a quando tutti i pezzi di grandi dimensioni non vengono scomposti. Vortice bene.
- Estrarre il DNA dall'omogeneato di ninfe utilizzando un kit di estrazione del DNAbatterico (Table of Materials)come segue.
- Centrifugare la ninfa omogeneizzata per 10 min a 5.000 x g e rimuovere il supernatante. Preriscaldare uno shaker termico a 37 °C.
- Aggiungere 100 μL di 1x Tris-EDTA e vortice per rimorsi completamente il pellet. Aggiungere 10 μL di lisozima e mescolare, seguito da un'incubazione di 30 minuti (senza scuotimento) nello shaker termico preriscaldato a 37 °C.
- Aggiungere 25 mg di perline di vetro ai campioni e vortice alla velocità massima per 5 minuti. Preriscaldare lo shaker termico a 55 °C.
- Lasciare depositare le perline prima di trasferire il supernatante in un nuovo tubo di centrifuga da 1,5 ml con 100 μL di tampone proteica k e 20 μL di proteinasi K. Vortex da mescolare accuratamente.
- Incubare, con scuotimento a 600 giri/min, in uno shaker termico a 55 °C per 60 min. Centrifuga a 10.000 x g per 2 min e trasferisci il supernatante in un nuovo tubo di centrifuga da 1,5 ml. Preriscaldare lo shaker termico a 65 °C. Iniziare a preriscaldare il tampone di eluizione in un forno di ibridazione a 65 °C.
- Aggiungere 220 μL di etanolo al 100%. Vortice alla velocità massima per 20 s. Rompere qualsiasi precipitato visibile tubazione su e giù 10x.
- Inserire una colonna di DNA in un tubo di raccolta da 2 ml e trasferire il campione nella colonna, incluso qualsiasi precipitato che potrebbe aver formato. Centrifugare a 10.000 x g per 1 min, scartare il filtrato dal tubo di raccolta e sostituire il tubo di raccolta.
- Aggiungere 500 μL di tampone di legame alla colonna e centrifugare a 10.000 x g per 1 min. Scartare il filtrato dal tubo di raccolta e sostituire il tubo di raccolta.
- Aggiungere 700 μL di tampone di lavaggio del DNA alla colonna e centrifugare a 10.000 x g per 1 min. Scartare il filtrato dal tubo di raccolta e sostituire il tubo di raccolta. Ripetere per un secondo passaggio di lavaggio.
- Centrifugare la colonna vuota per 2 minuti per asciugarla, trasferendo la colonna in un nuovo tubo di centrifuga da 1,5 ml in seguito. Aggiungere 50 μL di tampone di eluizione preriscaldato direttamente alla matrice della colonna di DNA e incubare a 65 °C per 5 min.
- Centrifuga a 10.000 x g per 1 minuto per elutare. Quantificare il DNA estratto nel filtrato tramite spettrofotometria o fluorometria.
- Amplificare e digerire l'intero gene 16S. Visualizzare i frammenti usando l'elettroforesi del gel.
- Utilizzare 12,5 μL di mix master 2x, 0,5 μL di ogni primer 1492R (5′-GGTTACCTTGTTACGACTT) e 27F (5'-AGAGTTTGATCCTGGCTCAG), 5 ng di DNA e acqua di grado molecolare per un volume di reazione totale di 25 μL.
- Eseguire il seguente programma termociclometro: 94 °C per 60 s; seguito da 35 cicli di 94 °C per 30 s, 50 °C per 45 s, 68 °C per 90 s; seguito da 68 °C per 5 min.
- Purificare il prodotto di reazione a catena della polimerasi (PCR) utilizzando un kit di purificazione del DNA(Table of Materials).
- Aggiungere 120 μL di tampone purificante al prodotto PCR e al vortice da mescolare. Centrifugare brevemente per raccogliere goccioline all'interno del coperchio. Inserire una colonna di DNA in un tubo di raccolta da 2 ml, trasferire il liquido nella colonna preparata e centrifugare a ≥13.000 x g per 1 min.
- Scartare il filtrato e sostituire il tubo di raccolta. Aggiungere 700 μL di tampone di lavaggio del DNA e centrifuga a ≥13.000 x g per 1 min. Scartare il filtrato e sostituire il tubo di raccolta. Ripetere per un secondo passaggio di lavaggio.
- Centrifugare la colonna vuota per 2 minuti per asciugare e trasferire la colonna in un nuovo tubo di centrifuga da 1,5 ml. Aggiungere 50 μL di tampone di eluizione preriscaldato direttamente alla matrice della colonna di DNA e incubare a temperatura ambiente per 2 minuti.
- Centrifuga a 10.000 x g per 1 minuto per elutare. Quantificare il DNA estratto in filtrato tramite spettrofotometria o fluorometria.
- Aggiungere 1 μg di prodotto PCR purificato a 5 μL di tampone di digestione, 10 unità RsaI e acqua di grado molecolare per un volume di reazione totale di 50 μL. Mescolare pipettando su e giù e incubando a 37 °C per 60 min.
- Separare il prodotto digerito tramite elettroforesi gel eseguendo 20 μL di DNA digerito su un gel di agarosio al 2%. Visualizza il gel per confermare lo stato gnotobiotico.
NOTA: Gli insetti gnotobiotici dovrebbero provocare solo bande a 402 bp, 201 bp e uno striscio da 163 a 148 bp, basato sulla sequenza 16S rDNA dell'endosimbionte, Blattabacterium. Tutte le bande extra viste nel gel sono indicative di contaminare le specie microbiche.
7. Tracciamento asettico della crescita ninfa
- Registra la lunghezza del corpo per tenere traccia della crescita delle ninfe misurando gli insetti attraverso il pavimento BHI traslucido del pallone.
NOTA: Le ninfe possono essere posizionate a 4 °C per 15 minuti per rallentare il loro movimento, rendendole così più facili da misurare.
Risultati
I serbatoi di serie sono impostati come illustrato nella figura 1. Le femmine "incinte" sono identificate dall'ootheca attaccata all'addome posteriore, come nella figura 2. L'incubazione di ootecae su agar BHI consente il controllo della qualità gnotobiotico in modo non distruttivo. In alcuni casi, la sterilizzazione non ha successo e la crescita appare intorno alle ootecae come nella figura 3B. Queste ootecae devono essere rimosse e scartate. Nelle nostre mani, è stato osservato un tasso medio di fallimento del 10% per la sterilizzazione (n = 51). Le ootecae si schiudono in media 34 giorni dopo la sterilizzazione senza crescita sul mezzo, come si vede nella figura 3A. Abbiamo osservato tassi tipici di schiusa del 41% (n = 46) per le ooteca sterilizzate e non contaminate, con una media di 11 ninfe per ootheca. Le ninfe più grandi vengono trasferite a mastri BHI ricoperti di foglio, come nella figura 4. Il foglio previene la contaminazione e le ninfe hanno spazio per crescere. RFLP del 16S rDNA da una ninfa omogeneizzata viene utilizzato per confermare lo stato gnotobiotico. Le ninfe gnotobiotiche sono state osservate crescere ad un ritmo più lento rispetto alle loro controparti non sterili, come rappresentato figura 5. La figura 6 mostra i risultati degli insetti gnotobiotici con successo e delle ninfe standard (nonsterili).
Sebbene questo test non abbia ancora identificato la contaminazione in assenza di un risultato di coltura positivo, questo passaggio è stato effettuato regolarmente durante esperimenti critici per escludere la presenza di microbi contaminanti sensibili all'ossigeno o fastidiosi. La crescita più lenta è stata osservata negli scarafaggi gnotobiotici rispetto agli insetti standard / nonsterili.

Figura 1: Configurazione della cultura delle scorte di scarafaggi.
I tubi di cartone possono essere visti impilati all'estremità del serbatoio. Cibo e acqua sono entrambi vicino alla parte anteriore del serbatoio. Il coperchio in stoffa di cotone e la fascia elastica sono stati rimossi per la visibilità. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 2: Uno scarafaggio americano "incinta".
La freccia indica l'ootheca. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 3: Immagini di ninfe gnotobiotiche tratteggiate con successo e ootecae sterilizzate senza successo su inclinazioni BHI.
Le ootece sono state sterilizzate e incubate come descritto in questo protocollo. (A) La mancanza di crescita microbica sull'inclinazione BHI indica che gli insetti sono privi di organismi culturabili. (B) Le ootecae su inclinazioni che vengono alla formazione di colonie devono essere scartate come contaminate. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 4: Apparecchio di allevamento gnotobiotico.
Gli insetti sono tenuti in contenitori sterili coperti da un coperchio di lamina per prevenire la contaminazione. Il contenitore secondario (coperchio verde) viene sterilizzato con candeggina al 2% seguita dal 70% di etanolo. Il flusso d'aria non è limitato nel contenitore secondario. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 5: Dati rappresentativi sul tasso di crescita che confrontano le lunghezze corporee delle ninfe gnotobiotiche e non estere. Entrambi i gruppi di insetti sono stati nutriti con dieta autoclavata dei roditori. Gli insetti gnotobiotici (qui: n = 105) sono tenuti su BHI come descritto. Gli insetti nonsterili (qui: n = 50) vivono in fiasche con biancheria da letto in trucioli di legno autoclavati con piccoli piatti per l'acqua. Le ninfe nonsterili crescono ad un tasso medio di 0,059 mm/giorno, mentre le ninfe gnotobiotiche crescono a 0,028 mm/giorno (p < 0,0001). Clicca qui per visualizzare una versione più grande di questa figura.
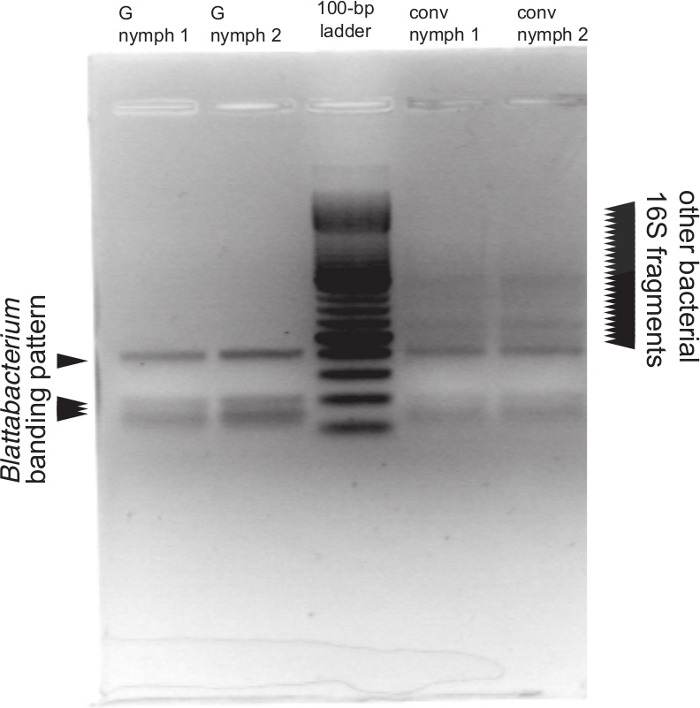
Figura 6: Immagine in gel rappresentativa dei risultati RFLP per il controllo di qualità.
Gli ampliconi genetici dell'intero 16S sono stati digeriti con RsaI. Il DNA per PCR è stato estratto da ninfe omogeneizzate in 1x PBS. Le corsie "G nymph" corrispondono alle ninfe gnotobiotiche, mentre le corsie "conv nymph" corrispondono a controparti convenzionali e nonsterili. Sulla base del digest di restrizione virtuale, l'endosymbiont (Blattabacterium) dovrebbe avere bande delle dimensioni di 402 bp, 206 bp e 163 bp, con uno striscio di bande tra 163 bp e 148 bp. Un insetto gnotobiotico dovrebbe mostrare solo il modello di bande blattabacterium. Si prevede che una comunità batterica mista abbia uno striscio di bande di varie dimensioni, etichettate qui come "altri frammenti batterici 16S". Clicca qui per visualizzare una versione più grande di questa figura.
Discussione
Altri metodi che descrivono la generazione di scarafaggi gnotobiotici non hanno descritto la raccolta delle ootece o usato benchmark specifici per altre specie di scarafaggi per indicare quando le oothecae potrebbero essere rimosse dalla madre23,25,26. Originariamente, le oothecae venivano raccolte dalla lettiera a cippato nei serbatoi di stoccaggio, con conseguente bassissimo tasso di schiusa (~10%) rispetto alle ootecae nonsterilizzate (47%)29. Ciò è probabilmente dovuto al fatto che le ootece non otecae non ohatched si accumulano nel tempo nella gabbia e non c'è modo di verificare l'età o la vitalità dell'ootheca. L'attuazione dell'approccio del "reparto maternità" consente la raccolta di oothecae appena depositate di età nota. Ciò facilita ulteriormente la pianificazione sperimentale, in quanto il ricercatore può anticipare i probabili tempi di schiusa per le singole oothecae. Un'altra modifica rispetto ai protocolli iniziali e pubblicati include l'incubazione di ootece e ninfe in camere semi-sigillate contenenti anche una soluzione di cloruro di sodio supersaturo. La presenza della soluzione mantiene un'umidità relativa di circa il 75%30. Le ootece vengono regolarmente incubate a 30 °C, il che ha dimostrato di ridurre al minimo il numero di giorni necessari per l'incubazione, massimizzando al contempo la vitalità degli embrioni e il numero di ninfe prodotte per ootheca31. Dopo la schiusa, le ninfe gnotobiotiche vengono regolarmente coltivate sul banco a temperatura ambiente e condizioni ambientali di laboratorio, anche se le camere controllate dall'umidità vengono nuovamente utilizzate per esperimenti critici. Dopo aver insociato queste modifiche alla raccolta e all'incubazione dell'ootheca, i tassi di schiusa sono aumentati a circa il 41% (n = 51), senza includere le ootecae rimosse a causa della contaminazione. Un potenziale percorso per un'ulteriore ottimizzazione dei tassi di tratteggio può includere l'estensione del tempo tra la raccolta dell'ootheca e la sterilizzazione. La cuticola della custodia dell'uovo potrebbe non essere completamente abbronzata alrilascio iniziale 32e quindi può essere permeabile alle soluzioni utilizzate durante la sterilizzazione entro 24 ore dalla caduta.
Il protocollo di sterilizzazione con acido peracetico 0,1% è stato adattato da Doll etal. Altri studi hanno documentato tecniche alternative per sterilizzare le ootecae23,26. I tassi di contaminazione si basano sul metodo non distruttivo di incubazione delle ootecae su un'inclinazione BHI. Questo approccio è altamente vantaggioso in quanto consente una rapida identificazione e rimozione delle ootecae contaminate. La maggior parte dei protocolli precedenti testa gli organismi culturabili placcando feci o ninfe omogeneate su mezzi batteriologici e controllando lacrescita 22,23,25,27,28,33. In almeno un caso, il metodo per testare lo stato gnotobiotico non è stato descritto completamente26. Tranne Clayton che ha aggiunto una piccola lastra di supporto di test di sterilità alle bottigliedi allevamento 24, metodiprecedenti 22,23 ha ospitato insetti gnotobiotici su supporti batteriologici solo per brevi periodi di tempo per valutare inizialmente il protocollo di sterilizzazione.
L'alloggiamento continuo delle ninfe risultanti su un mezzo BHI come misura integrata di controllo della qualità consente di monitorare il loro stato gnotobiotico in tempo semi-reale, una tecnica che non si vede nella maggior parte deimetodi precedenti 22,23. Questo è particolarmente utile per esperimenti a lungo termine che richiedono l'accesso a ninfe gnotobiotiche. Se il pavimento BHI sotto le ninfe appare contaminato dalla crescita batterica o fungina, il pallone deve essere scartato. Questo tipo di contaminazione si verifica tipicamente quando si scoprono i mambi alle ninfe d'acqua, ma può anche derivare dalle feci nel caso di ootece o cibo non sufficientemente sterilizzati. L'uso di una cappa di flusso laminare durante l'irrigazione migliora il tasso di contaminazione causato dalla scoperta di fiasche.
Poiché non tutti gli organismi contaminanti possono crescere aerobicamente su mezzo BHI, è necessario un metodo aggiuntivo indipendente dalla coltura per i test di sterilità. Un approccio potenziale è la microscopia27, ma questo approccio può essere ad alta intensità di lavoro. Altri protocolli utilizzano tecniche basate su sequenze per rilevare organismi che possono sfuggire allacoltura 14,23,27,28. Tuttavia, tali approcci sono spesso costosi e difficili da interpretare, poiché i risultati degli approcci di sequenziamento ad alta produttività possono essere facilmente influenzati dalla contaminazione a basso livello dei reagenti34 e dal salto con i codici abarre 35. Invece, è stato sviluppato un nuovo approccio che utilizza l'amplificazione PCR del gene 16S rRNA in combinazione con il polimorfismo di lunghezza dei frammenti di restrizione per visualizzare sia l'endosimbionte che qualsiasi simbionte intestinale contaminante. Questa tecnica include un controllo PCR interno, poiché il gene 16S del Blattabacteriumè stato sequenziato, e il suo modello di bande dovrebbe essere presente sia negli insetti gnotobiotici che in quello nonsterile. Poiché il modello di restrizione dell'endosimbionte può essere previsto dalla sua sequenza genomica36, non è necessario sequenziare gli ampliconi o i frammenti di restrizione, a meno che non si desideri l'identificazione di qualsiasi contaminante. L'attuale versione di questo protocollo richiede che una ninfa venga sacrificata per PCR/RFLP, ma questa tecnica potrebbe essere utilizzata anche sulle feci come misura non distruttiva. Tuttavia, non includerà un controllo integrato, poiché le feci non dovrebbero contenere molto Blattabacterium.
Un ulteriore componente facilmente modificabile ma critico dell'allevamento di animali gnotobiotici è la dieta. Mentre l'agar BHI può servire come fonte di cibo temporaneo per gli insetti, è stato scoperto che si traduce in notevoli deficit di crescita tra le ninfe se usato come unica fonte di cibo per lunghi periodi. Mentre sono state provate diete diverse, il chow di ratto autoclavabile è raccomandato come dieta di routine per il mantenimento degli insetti gnotobiotici. Diete non specificamente formulate per la sterilizzazione erano spesso difficili da rendere completamente sterili, e molte diete animali da laboratorio sterili o autoclavabili hanno mostrato una rapida crescita fungina in condizioni non sterili. Questa tendenza a degradarsi in condizioni nonsterili li rese inadatti all'uso in esperimenti che confrontavano direttamente insetti gnotobiotici e nongnotobiotici. La dieta raccomandata consente l'uso di una dieta coerente tra ninfe gnotobiotiche e standard, facilitando il confronto delle caratteristiche - come i tassi di crescita - tra i due gruppi.
Come altri hanno osservato27, le ninfe gnotobiotiche crescono più lentamente delle loro controparti nonsterili. Un confronto tra le lunghezze corporee di gnotobiotiche (n = 105) e ninfe nonsterili (n = 50) alimentate allo stesso modo, la dieta autoclavata dei roditori e mantenuta a temperatura ambiente rivela che le ninfe nonsterili crescono in media 0,059 mm/giorno, mentre le ninfe gnotobiotiche crescono di 0,028 mm/giorno (p < 0,0001)(Figura 5). La presenza di microbiota intestinale in P. americana ha dimostrato di alterare il tasso metabolico degli insetti37, e si ritiene che le comunità intestinali in generale influenzino l'assorbimentodei nutrienti 38,39. Queste ragioni supportano le differenze osservate nel tasso di crescita delle ninfe gnotobiotiche e nonsterili.
Una possibile limitazione a questa tecnica è che le ninfe gnotobiotiche potrebbero non raggiungere la maturità sessuale, poiché le coorti sterili più antiche hanno più di 10 mesi e hanno raggiunto solo la settima instar (su 10; 11 essendo età adulta) come approssimata dalla lunghezza del corpo40. Queste coorti più antiche non sono nella dieta del ratto autoclavato, ma mangiano invece chow di ratto irradiato, una dieta che contiene troppa umidità per nutrirsi di coorti nonsterili senza un'eccessiva crescita della muffa. Le ninfe nonsterili con una dieta nonsterilizzata di cibo per cani hanno raggiunto l'età adulta dopo 9−10 mesi in condizioni di laboratorio (temperatura ambiente e umidità). Le coorti di ninfe gnotobiotiche e non sterili sul chow di ratto condiviso e autoclavato hanno attualmente meno di 7 mesi, gli insetti non sterili sono stimati al settimo instar (media: 16,7 mm) mentre gli insetti sterili sono stimati al quinto instar (media: 11,2 mm). Di conseguenza, non possiamo ancora verificare se i nostri scarafaggi gnotobiotici possono riprodursi con successo. Tuttavia, data la facilità con cui possono essere stabilite nuove coorti gnotobiotiche utilizzando questo approccio, questo metodo mostra grandi promesse anche in assenza di una riproduzione comprovata di insetti gnotobiotici.
In conclusione, questo protocollo fornisce uno strumento versatile che consente ai ricercatori di microbioma di utilizzare la propria "struttura" gnotobiotica a basso costo utilizzando materiali di laboratorio comuni. Questo approccio può essere utilizzato per generare scarafaggi gnotobiotici per esperimenti che esaminano il ruolo del microbiota nel plasmare il comportamento dell'ospite, l'immunità, lo sviluppo e le risposte allo stress21,26,27. Questi insetti gnotobiotici possono anche essere inoculati con comunità sintetiche o xenobiotiche e successivamente utilizzati come soggetti per studi sul microbioma intestinale23,28. Inoltre, elementi di questo approccio, incluso l'uso di camere di incubazione batteriologiche rivestite di mezzi come controllo di sterilità integrato, sono generalizzabili ad altri sistemi modello e possono facilitare il mantenimento di routine degli animali gnotobiotici in strutture su piccola scala.
Divulgazioni
Gli autori non hanno conflitti di interesse da rivelare.
Riconoscimenti
Questa pubblicazione è stata sostenuta dal National Institute of General Medical Sciences del National Institutes of Health con il numero di premio R35GM133789. Il contenuto è di esclusiva responsabilità degli autori e non rappresenta necessariamente la visione ufficiale degli Istituti Nazionali di Sanità. Gli autori vorrebbero riconoscere Josey Dyer per aver tracciato i tassi di sterilizzazione, i tassi di schiusa e i tassi di crescita degli scarafaggi gnotobiotici.
Materiali
| Name | Company | Catalog Number | Comments |
| 2X master mix | New England BioLabs | M0482 | OneTaq MasterMix |
| Autoclavable rat chow | Zeigler | NIH-31 Modified Auto | |
| Bacterial DNA extraction kit | Omega Bio-Tek | D-3350 | E.Z.N.A. Bacterial DNA kit; includes lysozyme, glass beads, proteinase K, buffers (proteinase K, binding, wash, elution), DNA columns, 2-mL collection tube |
| binding buffer | Omega Bio-Tek | PD099 | included in Omega Biotek's bacterial DNA extraction kit ("HBC" buffer) |
| brain-heart infusion (BHI) broth | Research Products International | B11000 | |
| Delicate task wipes | KimWipe | JS-KCC-34155-PK | KimWipes |
| DNA purification kit | Omega Bio-Tek | D6492 | E.Z.N.A. Cycle Pure kit; D6493 may also be used; includes buffers (purifying ,wash, elution) |
| elution buffer | Omega Bio-Tek | PDR048 | included in Omega Biotek's bacterial DNA extraction kit |
| glass beads | Omega Bio-Tek | n/a | included in Omega Biotek's bacterial DNA extraction kit |
| Hybridization oven | UVP | 95-0330-01 | we use a hybridization oven for preheating elution buffer, but a water bath could probably also be used |
| Laminar flow biological safety cabinet | NuAire, Inc. | NU-425-400 | Protocol refers to this as "laminar flow hood" for brevity |
| lysozyme | Omega Bio-Tek | n/a | included in Omega Biotek's bacterial DNA extraction kit |
| peracetic acid stock solution (32%) | Sigma-Aldrich | 269336 | |
| Petroleum jelly | Vaseline | n/a | |
| proteinase K buffer | Omega Bio-Tek | PD061 | included in Omega Biotek's bacterial DNA extraction kit ("TL buffer") |
| purifying buffer | Omega Bio-Tek | PDR042 | included in Omega Biotek's CyclePure kit ("CP" buffer) |
| RsaI | New England BioLabs | R0167 | Includes CutSmart (digestion) buffer |
| Secondary container | n/a | n/a | a plastic container with a lid (such as a Kritter Keeper) works well for this (25cm long x 15cm wide x 22cm high); it should be large enough to fit BHI slants and test tubes |
| spectrophotometer | ThermoFisher | ND-2000 | Catalog info is for NanoDrop2000 |
| thermal shaker | Eppendorf | EP5386000028 | Thermomixer R |
| Tris-EDTA | Fisher | BP1338-1 | 10 nm Tris, 1 mM EDTA, pH 8 |
| wash buffer | Omega Bio-Tek | PDR044 | included in Omega Biotek's bacterial DNA extraction kit ("DNA wash" buffer) |
| Woodchip bedding | P.J. Murphy Forest Products | Sani-Chips |
Riferimenti
- Yi, P., Li, L. The germfree murine animal: An important animal model for research on the relationship between gut microbiota and the host. Veterinary Microbiology. 157 (1-2), 1-7 (2012).
- Nature Biotechnology. Laying better plans for mice. Nature Biotechnology. 31 (4), 263-263 (2013).
- Nicklas, W., Keubler, L., Bleich, A. Maintaining and Monitoring the Defined Microbiota Status of Gnotobiotic Rodents. ILAR Journal. 56 (2), 241-249 (2015).
- Faith, J. J., Ahern, P. P., Ridaura, V. K., Cheng, J., Gordon, J. I. Identifying Gut Microbe-Host Phenotype Relationships Using Combinatorial Communities in Gnotobiotic Mice. Science Translational Medicine. 6 (220), 11 (2014).
- Moon, C., et al. Vertically transmitted faecal IgA levels determine extra-chromosomal phenotypic variation. Nature. 521 (7550), 90-93 (2015).
- Eun, C. S., et al. Induction of Bacterial Antigen-Specific Colitis by a Simplified Human Microbiota Consortium in Gnotobiotic Interleukin-10-/- Mice. Infection and Immunity. 82 (6), 2239-2246 (2014).
- Cherbuy, C., et al. Microbiota matures colonic epithelium through a coordinated induction of cell cycle-related proteins in gnotobiotic rat. American Journal of Physiology: Gastrointestinal and Liver Physiology. 299 (2), 348-357 (2010).
- Van Den Abbeele, P., et al. Arabinoxylans and inulin differentially modulate the mucosal and luminal gut microbiota and mucin-degradation in humanized rats. Environmental Microbiology. 13 (10), 2667-2680 (2011).
- Stecher, B., Berry, D., Loy, A. Colonization resistance and microbial ecophysiology: using gnotobiotic mouse models and single-cell technology to explore the intestinal jungle. FEMS Microbiology Reviews. 37 (5), 793-829 (2013).
- Sugahara, H., et al. Probiotic Bifidobacterium longum alters gut luminal metabolism through modification of the gut microbial community. Scientific Reports. 5 (1), 13548 (2015).
- Martín, R., Bermúdez-Humarán, L. G., Langella, P. Gnotobiotic Rodents: An In Vivo Model for the Study of Microbe-Microbe Interactions. Frontiers in Microbiology. 7, 409 (2016).
- Mallapaty, S. Gnotobiotics: getting a grip on the microbiome boom. Lab Animal. 46 (10), 373-377 (2017).
- Nguyen, T. L. A., Vieira-Silva, S., Liston, A., Raes, J. How informative is the mouse for human gut microbiota research. Disease Models & Mechanisms. 8 (1), 1-16 (2015).
- Correa, M. A., Matusovsky, B., Brackney, D. E., Steven, B. Generation of axenic Aedes aegypti demonstrate live bacteria are not required for mosquito development. Nature Communications. 9 (1), 4464 (2018).
- Trinder, M., Daisley, B. A., Dube, J. S., Reid, G. Drosophila melanogaster as a High-Throughput Model for Host–Microbiota Interactions. Frontiers in Microbiology. 8, 751 (2017).
- Zheng, H., Steele, M. I., Leonard, S. P., Motta, E. V. S., Moran, N. A. Honey bees as models for gut microbiota research. Lab animal. 47 (11), 317-325 (2018).
- Engel, P., Moran, N. A. The gut microbiota of insects - diversity in structure and function. FeMS Microbiology Reviews. 37 (5), 699-735 (2013).
- Tinker, K. A., Ottesen, E. A. The Core Gut Microbiome of the American Cockroach, Periplaneta americana, Is Stable and Resilient to Dietary Shifts. Applied and Environmental Microbiology. 82 (22), 6603-6610 (2016).
- Zurek, L., Keddie, B. A. Contribution of the colon and colonic bacterial flora to metabolism and development of the american cockroach Periplaneta americana L. Journal of Insect Physiology. 42 (8), 743-748 (1996).
- Cruden, D. L., Markovetz, A. J. Microbial aspects of the cockroach hindgut. Archives of Microbiology. 138, 131-139 (1984).
- Pietri, J. E., Tiffany, C., Liang, D. Disruption of the microbiota affects physiological and evolutionary aspects of insecticide resistance in the German cockroach, an important urban pest. PLoS ONE. 13 (12), 0207985 (2018).
- Benschoter, C., Wrenn, R. Germfree techniques for establishment and maintenance of a colony of aseptic German cockroaches. Annals of the Entomological Society of America. 65 (3), 641-644 (1972).
- Tegtmeier, D., Thompson, C. L., Schauer, C., Brune, A. Oxygen Affects Gut Bacterial Colonization and Metabolic Activities in a Gnotobiotic Cockroach Model. Applied and Environmental Microbiology. 82 (4), 1080-1089 (2016).
- Clayton, R. A simplified method for the culture of Blattella germanica under aseptic conditions. Nature. 184 (4693), 1166-1167 (1959).
- Doll, J. P., Trexler, P. C., Reynolds, L. I., Bernard, G. R. The Use of Peracetic Acid to Obtain Germfree Invertebrate Eggs for Gnotobiotic Studies. American Midland Naturalist. 69 (1), 231 (1963).
- Wada-Katsumata, A., et al. Gut bacteria mediate aggregation in the German cockroach. Proceedings of the National Academy of Science. 112, 15678-15683 (2015).
- Jahnes, B. C., Herrmann, M., Sabree, Z. L. Conspecific coprophagy stimulates normal development in a germ-free model invertebrate. PeerJ. 7, 6914 (2019).
- Mikaelyan, A., Thompson, C. L., Hofer, M. J., Brune, A. Deterministic Assembly of Complex Bacterial Communities in Guts of Germ-Free Cockroaches. Applied Environmental Microbiology. 82 (4), 1256-1263 (2016).
- Katoh, K., et al. Group-housed females promote production of asexual ootheca in American cockroaches. Zoological Letters. 3, 3 (2017).
- Greenspan, L. Humidity fixed points of binary saturated aqueous solutions. Journal of Research of the National Bureau of Standards. 81 (1), 89-96 (1976).
- Bressan-Nascimento, S., Oliveira, D. M. P., Fox, E. G. P. Thermal requirements for the embryonic development of Periplaneta americana (L.) (Dictyoptera: Blattidae) with potential application in mass-rearing of egg parasitoids. Biological Control. 47 (3), 268-272 (2008).
- Nation, J. L. . Insect Physiology and Biochemistry, Second Edition. , (2008).
- House, H. L. Nutritional studies with Blattella germanica (L.) reared under aseptic conditions I. Equipment and technique. The Canadian Entomologist. 81 (5), 94-100 (1949).
- Stinson, L. F., Keelan, J. A., Payne, M. S. Identification and removal of contaminating microbial DNA from PCR reagents: impact on low-biomass microbiome analyses. Letters in Applied Microbiology. 68 (1), 2-8 (2018).
- Kircher, M., Sawyer, S., Meyer, M. Double indexing overcomes inaccuracies in multiplex sequencing on the Illumina platform. Nucleic Acids Research. 40, 3 (2011).
- Sabree, Z. L., Kambhampati, S., Moran, N. A. Nitrogen recycling and nutritional provisioning by Blattabacterium, the cockroach endosymbiont. Proceedings of the National Academy of Sciences of the United States of the America. 106 (46), 19521-19526 (2009).
- Ayayee, P. A., Ondrejech, A., Keeney, G., Muñoz-Garcia, A. The role of gut microbiota in the regulation of standard metabolic rate in female Periplaneta americana. PeerJ. 6, 4717 (2018).
- Krajmalnik-Brown, R., Ilhan, Z. E., Kang, D. W., DiBaise, J. K. Effects of gut microbes on nutrient absorption and energy regulation. Nutrition in clinical practice : official publication of the American Society for Parenteral and Enteral Nutrition. 27 (2), 201-214 (2012).
- Rowland, I., et al. Gut microbiota functions: metabolism of nutrients and other food components. European Journal of Nutrition. 57 (1), 1-24 (2018).
- Gier, H. T. Growth rate in the cockroach Periplaneta americana (Linn). Annals of the Entomological Society of America. 40, 303-317 (1947).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon