Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Immunology and Infection
تحليل Hypermutation الجسدية في intron JH4 من الخلايا B مركز الجرثومية من بقع باير ماوس
هنا هو المقايسة لتحديد التبدل الجسدي داخل الغلوبولين المناعي الثقيلة سلسلة جراد الجينات باستخدام الخلايا B مركز الجرثومية من بقع باير الماوس.
داخل المراكز الجرثومية للأعضاء اللمفاوية ، تغير الخلايا B الناضجة الغلوبولين المناعي المعبر عنه (Ig) من خلال إدخال طفرات غير مطلية في exons الترميز المتغير للسلسلة الجينية الثقيلة والخفيفة Ig loci. تتطلب عملية التبدل الجسدي هذه (SHM) أنزيم السيتيدين المستحث بالتنشيط deaminase (AID) ، والذي يحول deoxycytidines (C) ، إلى ديوكسيوريدينات (U). معالجة U:G الناتجة عن الإيدز عدم التطابق في الطفرات عن طريق مسارات إصلاح استئصال قاعدة وعدم التطابق يدخل تسلسل الترميز Ig الجديدة التي قد تنتج تقارب أعلى Ig. يمكن أن تمنع الطفرات في جينات إصلاح الإيدز أو الحمض النووي أو تغير بشكل كبير أنواع الطفرات التي لوحظت في Ig loci. نحن نصف بروتوكولا لقياس طفرات JH4 intron التي تستخدم فرز الخلايا المنشطة الفلورية (FACS) وPCR وتسلسل سانجر. على الرغم من أن هذا المقايسة لا تقيس بشكل مباشر نضوج تقارب Ig ، إلا أنها تشير إلى الطفرات في تسلسل الترميز المتغير Ig. بالإضافة إلى ذلك، تستخدم هذه الطرق تقنيات البيولوجيا الجزيئية الشائعة التي تحلل الطفرات في تسلسل Ig لاستنساخ خلايا B متعددة. وبالتالي، فإن هذا المقايسة هي أداة لا تقدر بثمن في دراسة تنويع SHM وIg.
الخلايا B, أعضاء الجهاز المناعي التكيفي, التعرف على والقضاء على المستضدات عن طريق إنتاج الأجسام المضادة, المعروف أيضا باسم الغلوبولين المناعي (Ig). ويتكون كل Ig من اثنين من الثقيلة (IgH) واثنين من الضوء (IgL) سلسلة polypeptides, التي عقدت معا من قبل السندات ثنائي الكبريتيد لتشكيل بنية الشكل المميز "Y" من Ig1. وN-termini من IgH وIgL تشمل منطقة متغير (V) من كل بوليبتيد ومعا أنها تشكل موقع ملزم مستضد من Ig، في حين أن المنطقة المستمرة من IgH يضفي وظيفة التأثير من Ig. تطوير الخلايا B في نخاع العظام إعادة ترتيب exons الترميز الخامس من IgH وIgL في عملية تعرف باسم V (D)Jإعادةالتركيب 2،3،4. النسخ من exons V المؤتلفة، إلى جانب exons المنطقة الثابتة المعنية، يشكل ميرنا التي تترجم إلى Ig.
الخلايا الناضجة B التي تعبر عن غشاء ملزم Ig ، المعروف أيضا باسم مستقبلات الخلايا B (BCR) ، تدور على الأعضاء اللمفاوية الثانوية ، مثل الطحال أو العقدة الليمفاوية أو بقع باير ، حيث تقوم بمسح البيئة للمستضدات والتفاعل مع الخلايا الأخرى في الجهاز المناعي1. داخل المراكز الجرثومية (GC) من الأعضاء اللمفاوية الثانوية ، تصبح الخلايا B التي تتعرف على المستضد من خلال BCR نشطة. بمساعدة الخلايا التشعبية الجريبية والخلايا التائية الجريبية المساعد ، يمكن للخلايا B المنشطة أن تتكاثر وتفرق إلى خلايا البلازما والذاكرة ، والتي هي من التأثيرات الهامة للاستجابة المناعية القوية5و6و7و8و9. بالإضافة إلى ذلك ، يمكن أن تخضع هذه الخلايا B المنشطة لعمليات تنويع الجينات الثانوية Ig - إعادة دمج تبديل الفئة (CSR) والتبدل الجسدي (SHM). أثناء المسؤولية الاجتماعية للشركات، تبادل الخلايا B المنطقة الافتراضية μ ثابت من البوليبتيد IgH مع منطقة ثابتة أخرى (γ، α، ε) من خلال رد فعل حذف الحمض النووي إعادة التركيب(الشكل 1). وهذا يسمح للتعبير عن exon ثابت مختلفة وترجمة Ig جديدة. سوف تتحول الخلية B من التعبير عن IgM إلى نوع متساوي آخر (IgG، IgA، IgE). المسؤولية الاجتماعية للشركات يغير وظيفة التأثير من Ig دون تغيير خصوصية مستضدلها 10،11،12. ومع ذلك ، خلال SHM ، تحور الخلايا B مناطق الترميز V من IgH و IgL لتمكين إنتاج واختيار Igs تقارب أعلى ، والتي يمكن أن تقضي بشكل أكثر فعالية على مستضد13،14،15 ( الشكل1). الأهم من ذلك، كل من المسؤولية الاجتماعية للشركات وSHM تعتمد على وظيفة إنزيم واحد: تنشيط الناجم عن السيتيدين deaminase (الإيدز)16،17،18. البشر والفئران ناقصة في الإيدز لا يمكن إكمال المسؤولية الاجتماعية للشركات أو SHM والحاضر مع ارتفاع الثدي مصل IgM أو Hyper-IgM17,19.
في المسؤولية الاجتماعية للشركات، AID deaminates deoxycytidines (C) في مناطق التبديل المتكررة التي تسبق كل exons الترميز المستمر، وتحويلها إلى deoxyuridines (U)20،21،مما يخلق الاقتران قاعدة غير متطابقة بين deoxyuridines وdoxyguanosines (U:G). يتم تحويل هذه عدم التطابق U:G إلى فواصل الحمض النووي مزدوجة الذين تقطعت بهم السبل، وهي مطلوبة لإعادة دمج الحمض النووي، إما عن طريق إصلاح الختان الأساسي (BER) أو إصلاح عدم التطابق (MMR) المسار22،23،24،25،26،27،28،29. في SHM، المعونة deaminates C داخل exons الترميز الخامس. النسخ المتماثل عبر عدم التطابق U:G يولد C:G إلى T:A الطفرات الانتقالية, في حين أن إزالة قاعدة uracil من قبل بروتين BER, uracil الحمض النووي جليكوسيلاز (UNG), قبل تكرار الحمض النووي تنتج كل من الانتقال والتحول الطفرات16. طفرات فارغة في UNG زيادة كبيرة C:G إلى T:A الطفرات الانتقالية21,22. وعلى غرار المسؤولية الاجتماعية للشركات، تتطلب SHM الأدوار التكميلية ل MMR و BER. خلال SHM، يولد MMR الطفرات في أزواج قاعدة A:T. تعطيل الطفرات في MutS homology 2 (MSH2) أو بوليمرات الحمض النووي η (Polη) يقلل بشكل كبير من الطفرات في قواعد A:T والطفرات المركبة في MSH2 وبوله يلغي تقريبا الطفرات في قواعد A:T21,30,31. بما يتفق مع الدور الحاسم ل BER وMMR في تحويل U الناتج عن الإيدز إلى طفرات انتقالية أو متحولة ، تعرض الفئران الناقصة لكل من MSH2 و UNG(MSH2-/-UNG-/-) فقط C:G إلى T:A الطفرات الانتقالية الناتجة عن النسخ المتماثل عبر عدم تطابق U:G21.
تحليل SHM في مناطق الترميز الخامس لا يزال معقدا لأن تطوير الخلايا B يمكن إعادة دمج أي من V (D)J الترميز exons في IgH وIgL loci1،2،4. تحليل دقيق لهذه المناطق V recombined فريدة من نوعها وتحور جسديا يتطلب تحديد وعزل استنساخ الخلايا B أو الجيش الملكي النيبالي Ig11،13. وJH4 intron، الذي هو 3 'من exon الترميز J الماضي في مكان IgH، يؤوي الطفرات الجسدية بسبب انتشار الطفرات 3' من V المروج32،33،34، وبالتالي يستخدم في كثير من الأحيان كعلامة بديلة لSHM في المناطق V31،35 ( الشكل1). لتوضيح تجريبيا كيف جينات محددة أو الطفرات الوراثية تغيير أنماط SHM أو معدلات, يمكن تسلسل intron JH4 من بقع باير (PP) الخلايا B المركز الجرثومي (GCBCs), التي تخضع لمعدلات عالية من SHM36,37,38. يمكن التعرف على GCBCs بسهولة وعزلها مع الأجسام المضادة المقترنة فلوريا ضد علامات سطح الخلية (B220+PNAHI)17،39.
يتم تقديم بروتوكول مفصل لتوصيف الطفرات intron JH4 في PP GCBCs من الفئران باستخدام مزيج من FACS (تفلورسينس تنشيط فرز الخلايا)، PCR، وتسلسل سانجر(الشكل 2).
تم الحفاظ على جميع الفئران المتحولة على خلفية C57BL/6. تم استخدام الفئران الذكور والإناث المطابقة للعمر (2-5 أشهر) لجميع التجارب. تم إجراء تربية الفئران وتجاربها وفقا للبروتوكولات التي وافقت عليها كلية مدينة نيويورك المؤسسية لرعاية الحيوانات واستخدامها.
1. تشريح بقع باير
- القتل الرحيم الماوس مع 100٪ CO2 في 3 لتر / دقيقة لمدة 5 دقائق تليها خلع عنق الرحم لتأكيد الوفاة. تعقيم أدوات تشريح (مقص، ملقط، ملقط ناعم) واليدين قفاز مع الإيثانول 70٪.
- وضع الماوس على لوحة تشريح مع البطن المكشوفة. رش بسخاء جسم الماوس مع الإيثانول 70٪ قبل إجراء أي شقوق لتعقيم منطقة تشريح.
- إجراء شق في الجلد عبر البطن وإزالة الجلد من البطن عن طريق سحب في وقت واحد على كلا الجانبين من شق نحو الرأس والذيل باستخدام ملقط (أو معقمة, قفاز اليدين).
- دبوس أسفل الأطراف الأمامية والهندية من الماوس.
- قطع تجويف الصفاق مع مقص لفضح الأعضاء الداخلية.
- تحديد موقع الأمعاء الدقيقة بين المعدة وcaecum ("J" على شكل هيكل بالقرب من القولون). إزالة الأمعاء الدقيقة عن طريق قطع تحت المعدة وفوق caecum.
- إزالة أي النسيج الضام والدهون ربط طيات الأمعاء الدقيقة معا.
ملاحظة: سيكون للدهون لون أبيض مميز، على عكس اللون الوردي للأمعاء الدقيقة. - فحص السطح الخارجي للأمعاء الدقيقة لبقع باير (PPs) ، وهي صغيرة (~ 1 ملم) ، على شكل بيضاوي الهياكل التي تظهر بيضاء تحت طبقة رقيقة من الخلايا الظهارية الشفافة.
- استئصال بعناية جميع PP مرئية مع مقص.
ملاحظة: ماوس واحد C57BL/6 البرية نوع (WT) يمكن أن تسفر عن PPs 4-8، في حين أن الماوس AID-/- سيكون 6-10 PPs. - جمع PPs في أنبوب الطرد المركزي 1.5 مل الدقيقة التي تحتوي على 1 مل من العازلة FACS على الجليد.
ملاحظة: يجب أن تغرق PP، في حين أن الدهون سوف تطفو على السطح ويمكن إزالتها.
2. عزل الخلية ل FACS
- ضع فلتر 40 ميكرومتر في طبق من 6 آبار مع 1 مل من العازلة الباردة (4 درجة مئوية) FACS.
- صب PPs من أنبوب 1.5 مل على مرشح.
- غسل أجهزة الكمبيوتر مع 1 مل من العازلة FACS الباردة، والتأكد من أنها دائما في السائل وعلى الجليد.
- استخدم الطرف المسطح من المكبس من حقنة 1 مل كحشرات لسحق PPs على الفلتر حتى يبقى النسيج الضام فقط على الفلتر.
- غسل مرشح ومغطاس مع 1 مل من العازلة FACS الباردة للافراج عن الخلايا في طبق البئر 6.
- جمع ~ 4 مل من الخلايا في العازلة FACS الباردة وتصفيتها من خلال أنبوب FACS غطاء مصفاة 40 ميكرومتر.
- غسل غطاء مصفاة مع 1 مل من العازلة FACS الباردة.
- بيليه الخلايا في 600 × ز في 4 درجة مئوية لمدة 5 دقائق في جهاز طرد مركزي دلو يتأرجح.
- (ديكانت) العملاق.
- Resuspend الخلايا في 0.4 مل من العازلة FACS الباردة.
- إزالة 10 ميكرولتر لحساب الخلية للتحقق من العائد (نتوقع ~ 5 × 106 خلايا / الماوس، انظر الشكل 3A)
- تصفية الخلايا المتبقية من خلال غطاء مصفاة 40 ميكرومتر في أنبوب FACS والمضي قدما في تلطيخ لFACS.
3. تلطيخ GCBCs ل FACS
- إضافة كتلة Fc 1 ميكرولتر (CD16/CD32 غير موسم المضادة للفأرة) إلى تعليق الخلية 400 ميكرولتر ووضع الخلايا على الجليد لمدة 15 دقيقة.
- إضافة 2 مل من العازلة FACS الباردة لغسل الخلايا.
- خلايا بيليه في 600 × ز في 4 درجة مئوية لمدة 5 دقائق والتخلص من supernatant.
- Resuspend الخلايا في 80 ميكرولتر من العازلة FACS الباردة.
- قم بإزالة 10 ميكرولتر من الخلايا من WT PP لكل عنصر تحكم في التلطيخ (4 في المجموع، بما في ذلك 3 عناصر تحكم واحدة للبقع وتحكم واحد غير ملطخ). اترك 40 ميكرولتر من WT PP للخطوة التالية. بدلا من ذلك، استخدم حبات التعويض لعناصر التحكم في التلطيخ.
- وصمة عار كل من العينات التجريبية (على سبيل المثال، WT و AID-/-) في 500 ميكرولتر من العازلة FACS الباردة مع 2.5 ميكرولتر من الفول السوداني agglutinin (PNA) البيوتين لمدة 15 دقيقة على الجليد.
- إضافة 2 مل من العازلة FACS الباردة لغسل الخلايا.
- خلايا بيليه في 600 × ز في 4 درجة مئوية لمدة 5 دقائق والتخلص من supernatant.
- وصمة عار كل عينة تجريبية مع 500 ميكرولتر من الكوكتيل في الظلام، على الجليد، لمدة 15 دقيقة (الجدول 1). تأكد من إعادة إنفاق الخلايا بالكامل في كوكتيل التلطيخ.
- إعداد ضوابط وصمة عار واحدة لمصفوفة التعويض.
- وصمة عار الخلايا في 500 ميكرولتر من العازلة FACS الباردة باستخدام التخفيفات المحددة في الجدول 2.
- احتضان ضوابط تلطيخ في الظلام، على الجليد، لمدة 15 دقيقة.
- إضافة 2 مل العازلة FACS الباردة لجميع الأنابيب في الخطوتين 3.7 و 3.8، بيليه الخلايا، وتجاهل supernatant لغسل الأجسام المضادة غير المنضمة أو DAPI.
- Resuspend الخلايا في 500 ميكرولتر من العازلة FACS الباردة ومكان على الجليد.
- باستخدام فرز الخلية، وجمع B220+السلطةالوطنية الفلسطينية مرحبا من كل عينة تجريبية ملطخة. ويبين الشكل 3 باء النسب المئوية النموذجية ل B220+ السلطةالوطنية الفلسطينية HI التي تم الحصول عليها من WT و AID-/- PPs. يعرض الشكل 3C استراتيجية gating FACS.
4. استخراج الحمض النووي من GCBCs
- بيليه فرز الخلايا في 600 × ز في 4 درجة مئوية لمدة 5 دقائق والتخلص من supernatant.
- إعادة تشغيل الخلايا في 1 مل من العازلة FACS الباردة ونقل الخلايا إلى أنبوب الطرد المركزي الدقيق 1.5 مل.
- بيليه الخلايا في 600 × ز في 4 درجة مئوية لمدة 5 دقائق والتخلص من supernatant.
- Resuspend الخلايا في 500 ميكرولتر من الحمض النووي استخراج العازلة و 5 ميكرولتر من 20 ملغ / مل بروتيناز K.
- حضانة عند 56 درجة مئوية بين عشية وضحاها.
- الحمض النووي الراسب مع 500 ميكرولتر ايزوبروبانول و 1 ميكرولتر من 20 ملغ / مل الجليكوجين. خلط أنبوب جيدا عن طريق عكس 5-6x.
- احتضان في درجة حرارة الغرفة لمدة 10 دقيقة.
- جهاز طرد مركزي في جهاز طرد مركزي صغير لمدة 15 دقيقة عند 25 درجة مئوية عند 21,000 x g.
- تجاهل supernatant والاحتفاظ بيليه، الذي يحتوي على الحمض النووي عجلت والجليكوجين.
- غسل بيليه الحمض النووي مع 1 مل من الإيثانول 70٪.
- بيليه الحمض النووي في جهاز الطرد المركزي الدقيق لمدة 10 دقائق في 25 درجة مئوية في 21،000 × ز.
- إزالة الإيثانول 70٪ والهواء الجاف بيليه الحمض النووي لمدة 5-10 دقيقة.
ملاحظة: تجنب الإفراط في التجفيف لأن الحمض النووي قد لا يتجدد تماما.
- Resuspend الحمض النووي في 30 ميكرولتر TE العازلة واحتضان بين عشية وضحاها في 56 درجة مئوية.
5. JH4 التضخيم تسلسل intron وتحليل
- قياس الحمض النووي عن طريق قياس الامتصاص على طول موجي يبلغ 260 نانومتر (A260).
ملاحظة: التركيز النموذجي للحمض النووي المسترد من B220 مفروز+PNAHI GCBCs من الماوس C57BL/6 هو 20-40 نانوغرام / ميكرولتر. - تنفيذ PCR المتداخلة للإنترون JH4 (الجدول 3، الجدول 4). تطبيع الكمية الإجمالية للحمض النووي الجينومي المستخدم في أول PCR إلى العينة الأقل تركيزا. (على سبيل المثال، إذا كانت العينة الأقل تركيزا هي 5 نانوغرام/ميكرولتر، استخدم 58.75 نانوغرام من الحمض النووي لجميع العينات في الحجم الأقصى للمياه (11.75 ميكرولتر) في #1 PCR).
- حل المنتج PCR على هلام agarose 1.5٪ في 200 V لمدة 20 دقيقة. حجم amplicon المتوقع هو 580 نقطة أساس.
- استئصال أمبليكون من هلام واستخراج الحمض النووي باستخدام عدة استخراج هلام وفقا لتعليمات الشركة المصنعة (انظر الشكل التكميلي 1).
- Elute الحمض النووي مع 30 ميكرولتر من الماء وتحديد كمية الحمض النووي عن طريق قياس A260.
ملاحظة: التركيز النموذجي للمنتج PCR المنقى هو 3-10 نانوغرام / ميكرولتر.
- Elute الحمض النووي مع 30 ميكرولتر من الماء وتحديد كمية الحمض النووي عن طريق قياس A260.
- Ligate المنتج PCR المنقى في البلازميد مع نهايات حادة. توحيد المبلغ الإجمالي لمنتج PCR المستخدم في كل تفاعل ربط(الجدول 5).
- احتضان رد فعل الربط في درجة حرارة الغرفة لمدة 5 دقائق أو بين عشية وضحاها عند 16 درجة مئوية.
- تحويل الخلايا البكتيرية الكهربائية المنافسة مع 2 ميكرولتر من رد فعل الربط.
- الكتروبورات عند 1.65 كيلو فولت.
- الإنقاذ في 600 ميكرولتر من وسائل الإعلام SOC لمدة 1 ساعة في 37 درجة مئوية في حاضنة تهتز في 225 دورة في الدقيقة.
- لوحة 100 ميكرولتر من البكتيريا المحولة على LB تكملها لوحات أجار ampicillin (100 ميكروغرام / مل) واحتضان بين عشية وضحاها في 37 درجة مئوية.
- تقديم لوحة من المستعمرات البكتيرية لتسلسل سانجر باستخدام التمهيدي T7 إلى الأمام. بدلا من ذلك، تنمو الثقافات بين عشية وضحاها من كل مستعمرة بكتيرية وأداء تنقية البلازميد.
- إذا لزم الأمر، كرر PCR، ربط، و / أو التحول لتحسين غلة المستعمرات البكتيرية
ملاحظة: يجب اختيار ما لا يقل عن 30 مستعمرة من كل لوحة.
- إذا لزم الأمر، كرر PCR، ربط، و / أو التحول لتحسين غلة المستعمرات البكتيرية
- توحيد بيانات التسلسل في ملفات .txt
- حذف تسلسل البلازميد.
- تأكد من أن كل تسلسل موجه من 5' إلى 3 ' وفقا للتسلسل المرجعي ل JH4 intron (NG_005838). توليد تكملة عكسية من أي تسلسل، حسب الضرورة.
- قم بمحاذاة التسلسلات التي تم الحصول عليها لكل PCR مقابل التسلسل المرجعي ل JH4 intron (NG_005838) باستخدام برنامج Clustal Omega (الشكل 4A).
- تحديد الاختلافات من التسلسل المرجعي كطفرات
- تحقق من أن جميع الطفرات هي طفرات نقطة حقيقية من خلال فحص electropherogram من تسلسل سانجر. تكرار التسلسل إذا لزم الأمر. (الشكل 4B, C).
- جدولة وقياس الطفرات الفريدة في intron JH4 لكل نوع جيني (الشكل 5).
- تسلسل العد مع الطفرات متطابقة مرة واحدة فقط
ملاحظة: من غير الممكن تحديد ما إذا كانت التسلسلات متطابقة تم إنشاؤها أثناء PCR أو أحداث SHM متطابقة في خلايا B مختلفة. - عد كل حالة من WT الجرثومية JH4 تسلسل intron (أي تلك التي لا توجد طفرات) لتسلسل فريد من نوعه.
- تسلسل العد مع الطفرات متطابقة مرة واحدة فقط
قياس التدفق الخلوي
الخلايا الناضجة B تعمم على المراكز الجرثومية حيث أنها تخضع لنضوج تقارب، والتوسع اللاستنساخي، والتمايز في خلايا البلازما أو الذاكرة40،41،42،43،44. ويمكن تحديد هذه GCBCs من قبل العديد من علامات سطح الخلية, بما في ذلك التعبير العالي عن مستقبلات CD45R/B220 وملزمة من agglutinin الفول السوداني (PNA)45,46. لعزل GCBCs المنشطة، كانت خلايا PP ملطخة بالأجسام المضادة المضادة B220 المرتبطة بالفيكوريثرين (PE) والبيوتينيلات-PNA، تليها ستريبتافيدين المقترنة APC-eFluor780. تم القضاء على الخلايا الميتة باستخدام الفلورسنت 4',6-Diamidino-2-Phenylindole (DAPI) صبغة, الذي يلطخ الحمض النووي من الخلايا المحتضرة أوالميتة 47,48. تم تحليل الخلايا الملطخة في وقت لاحق وفرزها عن طريق قياس التدفق الخلوي. تألفت PPs من ~ 80٪ B220+ خلايا49،50. WT PPs تحتوي على متوسط 4 × 106 خلايا لكل فأرة (الشكل 3A). وكان ما يقرب من 8٪ من خلايا WT PP B220+السلطة الوطنيةالفلسطينية HI، وهو نصف العدد الملاحظ في الإيدز-/ - ( الشكل3B). وهكذا، تم الحصول على 0.3-0.6 ×10 6 B220+PNAHI GCBCs بعد الفرز، والتي كانت كافية لتحليل الطفرات في intron JH4.
تحليل تسلسل JH4
تم تضخيم intron JH4 بواسطة PCR متداخلة باستخدام التمهيديات الأسرة VHJ558 المشتركة (J558FR3Fw وVHJ558.2) تليها JH4 intron تمتد التمهيديات VHJ558.3 وVHJ558.435،37. ومن بين 105 متواليات فريدة تم الحصول عليها من مركبات الكربون الكلورية فلورية WT GCBCs، تم العثور على ما مجموعه 226 طفرة(الشكل 5A). أظهر تحليل طيف طفرة GCBC في فئران WT مجموعة من التحولات والتحولات بمعدل 4 × 10-3 طفرات / bp ، والتي تم حسابها عن طريق قسمة العدد الإجمالي للقواعد المتحولة على العدد الإجمالي للقواعد التي تم تسلسلها32و36و37و38. بالإضافة إلى ذلك، كل JH4 PCR المنتج من WT GCBCs تحتوي على 1-25 الطفرات (الشكل 5B)، حيث تم العثور على طفرات متعددة في كثير من الأحيان على تسلسل واحد33،36. تم تحديد اثنين فقط من الطفرات في 113 AID-/- تسلسل (الشكل 5A). الإيدز-/- أظهرت خلايا B 1.66 × 10-5 طفرات / bp ، والتي كانت أقل بكثير من خلايا WT B (p < 0.05)36 وتقارن بمعدل خطأ البوليميراز عالي الدقة (5.3 × 10-7 sub/base/doubling)51،52. وهكذا، عملت الخلايا AID-/- B كتحكم سلبي مفيد لهذا المقايسة.
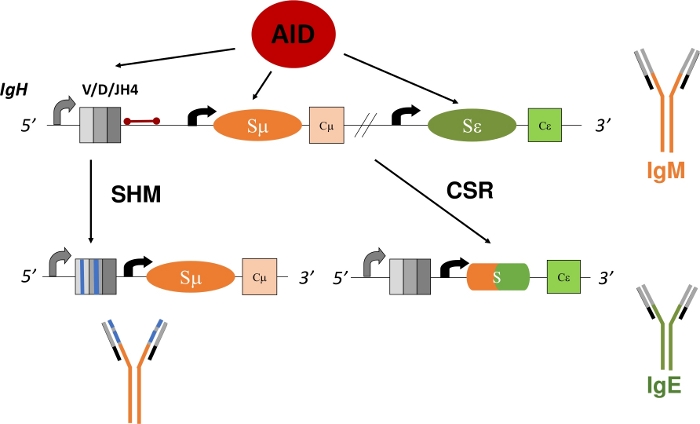
الشكل 1: تخطيطي لجراد الجينات IgH والمناطق التي تستهدفها المعونة خلال المسؤولية الاجتماعية للشركات وSHM. يشير الشريط الأحمر إلى intron JH4 580 bp الذي هو 3 ' من إعادة ترتيب VDJH4 ويتم تحليلها في هذا البروتوكول. في المسؤولية الاجتماعية للشركات، تشجع إزالة المخدرات المعتمدة على الإيدز في مناطق التبديل الإلكتروني (Sμ و Sε) على تشكيل DSB الذي يسمح بإعادة التركيب المحذوف والتعبير عن نوع جديد من الأجسام المضادة (IgM to IgE). خلال SHM، تتراكم مناطق V (الصناديق الرمادية) الطفرات (الخطوط الزرقاء) التي قد تؤدي إلى تقارب أعلى Ig. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
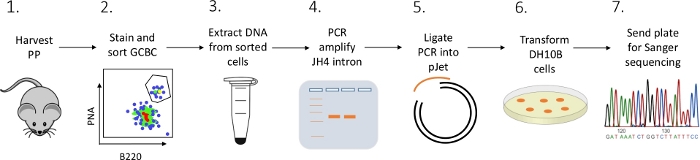
الشكل 2: سير العمل لتحليل SHM من intron JH4 في GCBCs معزولة عن PPs. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
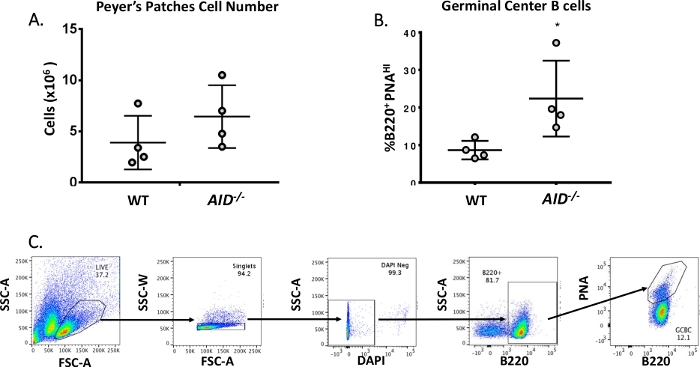
الشكل 3: توصيف المركبات الكيميائية العالمية PP. (أ)العدد الإجمالي لخلايا PP من WT و AID-/- الفئران (n = 4 لكل نمط جيني). تمثل أشرطة الخطأ الانحراف المعياري عن الوسط. (ب) النسبة المئوية ل B220+PNAHI GCBCs التي تم الحصول عليها من PPs من WT و AID-/- الفئران (n = 4 لكل نمط جيني)36. تمثل أشرطة الخطأ الانحراف المعياري عن المتوسط، *p<0.05 باستخدام اختبار t للطالب. (ج) مخططات FACS التمثيلية لفرز B220+PNAHI GCBCs من أجهزة الكمبيوتر. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
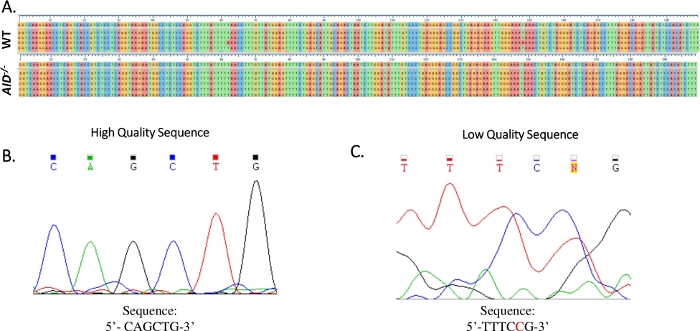
الشكل 4: تحليل بيانات تسلسل JH4 سانجر. (أ)نماذج من محاذاة تسلسل بيانات تسلسل سانجر لمنتج JH4 PCR من WT (أعلى) و AID-/- (أسفل) GCBCs إلى التسلسل الجينومي المرجعي (NG_005838) ، وهو التسلسل مباشرة تحت علامات التجزئة المرقم. تم إنشاء التحالفات باستخدام أوميغا كلوستال. (ب)Electropherogram من بيانات تسلسل سانجر عالية الجودة، والتي عرضت قمم متميزة لكل قاعدة. (ج)الكتروفيروغرام لبيانات التسلسل منخفضة الجودة، والتي أظهرت قمم غامضة وقواعد غير محددة (N). يجب أن يكون النيوكليوتيدات الموضحة باللون الأحمر مشروحة يدويا في الملف النصي التسلسلي. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
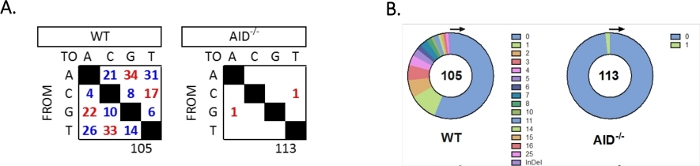
الشكل 5: تحليل الطفرات في إنترون JH4 في WT و AID-/- GCBCs. (أ)يتم تلخيص العدد الإجمالي للانتقال (الأحمر) والتحول (الأزرق) الطفرات في A، C، G، و T القواعد لكل النمط الجيني في الجداول. يشار إلى العدد الإجمالي للتسلسلات التي تم تحليلها أسفل الجدول. (ب)يتم تصوير عدد الطفرات لكل amplicon PCR لكل النمط الجيني في المخططات الدائرية. تم تعديل هذا الرقم من Choi et al.36 حقوق الطبع والنشر 2020. الرابطة الأمريكية لعلماء المناعة ، وشركة الرجاء الضغط هنا لعرض نسخة أكبر من هذا الرقم.
| كوكتيل تلطيخ لGCBCs | الحجم: 500 ميكرولتر | ||
| الأجسام المضادة أو صبغ | فلوروفور | التخفيف | ميكرولتر |
| B220 | PE | 1000 | 0.5 |
| ستريبتافيدين | APC-eفلور780 | 500 | 1 |
| DAPI | N/A | 500 | 1 |
الجدول 1: تلطيخ الكوكتيلات لGCBCs. تم استخدام مزيج من الأجسام المضادة المشار إليها أو الصبغة (المشار إليها بالخط المائل) في التخفيفات المحددة لتلطيخ خلايا PP في 500 ميكرولتر لقياس التدفق الخلوي.
| بقع واحدة للتعويض | الحجم: 500 ميكرولتر | ||
| الأجسام المضادة أو صبغ | فلوروفور | التخفيف | ميكرولتر |
| B220 | PE | 1000 | 0.5 |
| B220 | APC-eفلور780 | 750 | 0.67 |
| DAPI | N/A | 500 | 1 |
الجدول 2: ضوابط بقعة واحدة للتعويض. واستخدمت الأجسام المضادة B220 المترافقة مع الفلوروفوريس المشار إليها لضوابط وصمة عار واحدة للتعويض عن التداخل الطيفي.
| #1 PCR | ||||
| الكاشف | حجم | ظروف دورة الحرارة | ||
| 5x المخزن المؤقت | 4 ميكرولتر | 1 | 95 درجة مئوية | 3 دقائق |
| 10 mM dNTP | 2 ميكرولتر | 2 | 94 درجة مئوية | 30 ثانية |
| 10 ميكرومتر J558FR3Fw | 1 ميكرولتر | 3 | 55 درجة مئوية | 30 ثانية |
| 10 ميكرومتر VHJ558.2 | 1 ميكرولتر | 4 | 72 درجة مئوية | 1:30 دقيقة |
| بوليميراز الحمض النووي عالي الدقة | 0.25 ميكرولتر | دورة 2-4 9x | ||
| دنا | x (توحيد العينة الأقل تركيزا) | |||
| H2O | إلى 20 ميكرولتر | 5 | 72 درجة مئوية | 5 دقائق |
| تمييع PCR المنتج 1:5 في H2O قبل الشروع في PCR #2 | ||||
الجدول 3: PCR المتداخلة من intron JH4. مكونات PCR وظروف الترموسيكلر لأول تفاعل تضخيم. تمييع أول منتج PCR 1:5 بالماء واستخدام 1 ميكرولتر من هذا التخفيف لPCR الثاني.
| #2 PCR | ||||
| الكاشف | حجم | ظروف دورة الحرارة #2 | ||
| 5x المخزن المؤقت | 4 ميكرولتر | 1 | 94 درجة مئوية | 3 دقائق |
| 10 mM dNTP | 2 ميكرولتر | 2 | 94 درجة مئوية | 30 ثانية |
| 10 ميكرومتر VHJ558.3 | 1 ميكرولتر | 3 | 55 درجة مئوية | 30 ثانية |
| 10 ميكرومتر VHJ558.4 | 1 ميكرولتر | 4 | 72 درجة مئوية | 30 ثانية |
| بوليميراز الحمض النووي عالي الدقة | 0.25 ميكرولتر | دورة 2-4 21x | ||
| المخفف PCR # 1 | 1 ميكرولتر | |||
| H2O | إلى 20 ميكرولتر | 5 | 72 درجة مئوية | 5 دقائق |
الجدول 4: مكونات PCR وظروف دورة الحرارة ل PCR الثاني.
| الكاشف | حجم |
| 2x المخزن المؤقت | 10 ميكرولتر |
| جهاز PCR منقى | x (توحيد العينة الأقل تركيزا) |
| بلازميد مع نهايات حادة | 1 ميكرولتر |
| T4 الحمض النووي ليغاز | 1 ميكرولتر |
| H2O | إلى 20 ميكرولتر |
| حضانة في درجة حرارة الغرفة لمدة 5 دقائق أو بين عشية وضحاها في 16ºC | |
الجدول 5: رد فعل الربط. مكونات ربط من تنقية JH4 intron PCR المنتج في البلازميد.
| المخزن المؤقت ل FACS |
| الحرارة تعطيل FBS في 56 درجة مئوية لمدة ساعة واحدة قبل الاستخدام. ملحق برنامج تلفزيوني، درجة الحموضة 7.4 (جيبكو، #10010049) مع 2.5٪ (v/v) من FBS المعطل حراريا. يخزن عند درجة حرارة 4°C. |
| مخزن استخراج الحمض النووي (100 mM Tris pH 8.0, 0.1 M EDTA, 0.5٪ (ث/v) SDS) |
| أضف 50 مل من 1 M Tris pH 8.0 و 100mL من 0.5 M EDTA و 12.5 مل من 20٪ SDS. أضف الماء المقطر إلى 500 مل. تخزين في درجة حرارة الغرفة. |
| TE المخزن المؤقت (10 mM تريس pH 8.0، 1 mM EDTA) |
| أضف 2.5 مل من 1 M Tris pH 8.0 و 500 مل من 0.5 M EDTA. أضف الماء المقطر إلى 250 مل. تخزين في درجة حرارة الغرفة. |
الجدول 6: وصفات العازلة.
| قائمة أوليغونوكليوتيدات | ||
| J558FR3Fw | 5'-GCCTGACATCTGAGGACTCTGC-3' | |
| VHJ558.2 | 5'-CTGGACTTTCGGTGGTGGTG-3' | |
| VHJ558.3 | 5'-GGTCAAGGAACCTCAGTCA-3' | |
| VHJ558.4 | 5'-تكتاغاكاجاكاكتاك-3' | |
الجدول 7: أوليغونوكليوتيدات المستخدمة في المقايسة.
الشكل التكميلي 1: صورة هلام الآغاروز التمثيلية بعد الانتهاء من الخطوة 5.4. تم حل المنتج JH4 إينترون PCR المتداخلة على هلام agarose 1.5٪ وتم استئصال amplicon 580 bp. WT PP يشير إلى أن WT PP GCBC الحمض النووي الجينومي كان يستخدم كنموذج لأول PCR والإيدز PP يشير إلى أن AID-/- PP GCBC الحمض النووي الجينومي تم استخدامه كنموذج لأول PCR. ɸ يشير إلى عدم وجود عنصر تحكم PCR قالب و - يشير إلى أنه لم يتم تحميل أي شيء في بئر هلام agarose. الممر الأخير يظهر سلم الحمض النووي 100 نقطة أساس. يرجى الضغط هنا لتحميل هذا الرقم.
إن توصيف SHM داخل تسلسل ترميز IgH و IgL V لمحتوى الخلية B غير المتجانس يمثل تحديا ، نظرا لأن كل خلية B تعيد تنظيم شرائح ترميز V بشكل فريد أثناء إعادة دمج V(D)J34. في هذه الورقة، نصف طريقة لتحديد الطفرات في إنترون JH4 من GCBCs. وJH4 intron، الذي يقع 3 'من الجزء الأخير J الترميز في مكان IgH، ويستخدم كبديل لSHM من المناطق V (الشكل 1)31،33،34،35. لفهرسة هذه الطفرات intron JH4 وتقييم كيفية الجينات محددة تؤثر على إنتاج أو نمط الطفرات، يتم تحليل PP GCBCs على وجه التحديد. هذه الخلايا تتراكم JH4 intron الطفرات نتيجة للتحفيز المزمن عن طريق الكائنات الحية المجهرية المعوية53. وعلاوة على ذلك، فإن B220+PNAHI GCBCs من أجهزة الكمبيوتر من الفئران غير المحصنة لديها أطياف الطفرة التي تقارن مع GCBCs splenic من الحيوانات المحصنة54،55. ومع ذلك، لا يمكن ربط الطفرات في intron JH4 إلى نضوج تقارب Ig لأن هذه الطفرات هي غير الترميز.
لتحديد ما إذا كان SHM يغير تقارب Ig ، يجب تحصين الفئران intraperitoneally مع مستضد ، مثل NP (4-hydroxy-3-nitrophenylacetyl) المقترنة CGG (الدجاج غاما الجلوبيولين) أو KLH (ثقب المفتاح limpet hemocyanin)56. في وقت لاحق، يمكن تنقية مرنا من B220 splenic+السلطة الوطنيةالفلسطينية مرحبا GCBCs لفحص SHM داخل VH186.2، V الترميز exon أن يعترف في معظم الأحيان NP وتحور بعد NP-CGG أو NP-KLH التحصين31،57،58،59،60. وقد تميزت طفرة من التربتوفان-33 إلى اليوسين في VH186.2 لزيادة تقارب Ig تصل إلى 10 أضعاف59,60، وبالتالي, مؤشر واحد أن SHM واختيار كلون قد ولدت تقارب عالية Ig. قياس NP7- و NP20 محددة مصل Ig titers بواسطة ELISA وحساب نسبة NP7/NP20 محددة Ig أثناء التطعيم وثائق أيضا Ig تقارب النضج الناتج عن SHM من المناطق V17,21,36. يمكن استخدام كل من هذه المقايسات لربط SHM داخل تسلسل الترميز VH186.2 مع التغييرات في نضج تقارب Ig الخاص ب NP.
وسواء استخدمت الحيوانات المحصنة أو غير المحصنة لتحليل SHM من VH186.2 أو إنترون JH4، يجب تحديد GCBCs بدقة. نحن نقدم نهجا قائما على FACS لعزل B220+PNAHI GCBCs. بدلا من ذلك، Fas وغير كبريتات α2-6-sialyl-LacNAc مستضد، والتي يتم التعرف عليها من قبل الأجسام المضادة GL761،62،63،64، ويمكن أيضا أن تستخدم لعزل GCBCs، والتي يتم تحديدها على أنها B220 + Fas+GL7+65 أو CD19 + Fas+GL7+37. GL7 التعبير يعكس عن كثب السلطة الوطنية الفلسطينية في GCBCs تنشيط الغدد الليمفاوية64،65،66. بالإضافة إلى استخدام علامات الأجسام المضادة الخاصة ب GCBCs ، يجب أن تزيد كوكتيلات التلطيخ من إثارة الفلوروفور والكشف عن علامة بيولوجية مع تقليل التداخل الطيفي لانبعاثات الفلورسينس. وينبغي الكشف عن المستضدات التي أعرب عنها في مستويات منخفضة مع الأجسام المضادة التي يتم اقترانها إلى fluorophore مع مضان الانبعاثات قوية67. تم تحسين بروتوكول التلطيخ الموصى به للتحليل على فرز الخلايا المجهز بأربعة أشعة ليزر (405nm و 488nm و 561nm و 633nm) و 12 مرشحات؛ ومع ذلك، تختلف تكوينات التصفية وتوافر الليزر بين مقاييس الخلايا. لتعديل البروتوكول وفقا للكواشف وتوافر المعدات ، يشار القارئ إلى موارد إضافية ، مشاهدي الطيف على الإنترنت ونشر الأدب67،68،69،70،71،72،73. يتطلب بروتوكول التلطيخ متعدد الألوان الموصوف هنا تعويضا عن التداخل الطيفي لضمان أن مجموعات الخلايا المفرزة هي GCBCs بدلا من الكشف غير الدقيق عن انبعاثات الفلورسينس. B220 بمثابة عنصر تحكم تلطيخ مفيدة ل FACS وصفها (الجدول 1B) لأن PPs سيكون لها مجموعات مميزة B220 السلبية والإيجابية (الشكل 3C)، والذي يسمح بالتعويض المناسب من التداخل الطيفي. وينبغي استخدام استراتيجية الصياغة الواردة في الشكل 3C كمبدأ توجيهي. قد تختلف مؤامرات قياس التدفق الخلوي اعتمادا على ظروف التلطيخ وإعدادات قياس الخلايا. ومع ذلك، ينبغي أن يكون 4-10٪ من الخلايا الحية B220+السلطةالوطنية الفلسطينية HI 35، 52.
يجب التحقق من صحة جميع الطفرات داخل intron JH4 من PP GCBCs لضمان أن الطفرات الملاحظة تعكس حقا SHM وليس قطعة أثرية من PCR أو التسلسل. AID-/- يمكن أن تكون الخلايا B بمثابة عنصر تحكم سلبي مفيد عند فحص النمط الظاهري SHM في نماذج الماوس المتحولة الأخرى لأن هذه الخلايا لا يمكن إكمال SHM17،19. معدل طفرة intron JH4 في الإيدز-/- GCBCs (1.66x10-5 الطفرات / bp)20،21،36،37،38،5 0،74 هو مماثل لمعدل الخطأ من البوليميراز عالية الدقة (5.3x10-7 الفرعية / قاعدة / مضاعفة)51،52 التي تستخدم لتضخيم الحمض النووي في PCR المتداخلة. إذا لم تتوفر أجهزة AID-/- الفئران، فقارن نمط الطفرات الملحوظة وتكرارها بالأدبيات المنشورة. تتراكم مناطق Ig V 10-3 -10-4 طفرات لكل قسم ثنائي أساسي ، وهو ما يزيد بنحو 106أضعاف عن معدل طفرة اللوتشي الجيني الآخر73،75. قد تختلف النتائج مع عمر الحيوان76. بدلا من ذلك، B220+PNALO الخلايا، الذي يمثل غير GCBCs، يمكن استخدامها كسيطرة سلبية في غياب الإيدز-/- الفئران52. إذا كان تردد الطفرة في WT GCBCs أقل من المتوقع، قد يتم تمثيل تسلسل الجراثيم WT JH4 intronic بشكل غير متناسب. في هذه الحالة، تأكد من أن GCBCs كانت ملطخة وفرزها بشكل مناسب ومركبات ثنائي الفينيل متعدد الكلور خالية من التلوث بالجراثيم WT JH4 intron. بالإضافة إلى ذلك، ينبغي تحليل بيانات التسلسل الخام في الكتروفيروغرام بدقة للتأكد من أن الطفرات في بيانات نص التسلسل ليست قطعا أثرية من أخطاء التسلسل. على سبيل المثال، قد تقلل نتائج تسلسل Sanger الرديئة من موثوقية بيانات التسلسل(الشكل 4). هذا التحكم في جودة بيانات تسلسل سانجر سيزيد من دقة والاستنساخ لتحليل طفرة intron JH4.
وليس لدى صاحبي البلاغ ما يكشفان عنه.
نشكر تاسوكو هونجو على الإيدز-/- الفئران. وقد دعم هذا العمل المعهد الوطني المعني بصحة الأقليات والتفاوتات الصحية (5G12MD007603)، والمعهد الوطني للسرطان (2U54CA132378)، والمعهد الوطني للعلوم الطبية العامة (1SC1GM132035-01).
| Name | Company | Catalog Number | Comments |
| 0.2 ml PCR 8-tube FLEX-FREE strip, attached clear flat caps, mixed | USA Scientific | 1402-4708 | |
| Ampicillin sodium salt | Fisher | BP1760-5 | |
| APC-eFluor780 anti-CD45R/B220 | eBioscience | 47-0452-80 | clone RA3-6B2 |
| BD FACSAria II | BD | 643186 | four lasers (405nm, 488nm, 561nm, 633nm) and 12 filters (PacBlue (450/50), AmCyan (502LP; 530/30), SSC (488/10), FITC (502LP; 530/30), PerCP-Cy5.5 (655LP; 695/40), PE (585/15), PE-Texas Red (600LP; 610/20), PE-Cy5 (630LP; 670/14), PE-Cy7 (735LP; 780/60), APC (660/20), Alexa700 (710LP; 730/45), APC-Cy7 (755LP; 780/60)) |
| BD slip tip 1mL syringe | Fisher | 14-823-434 | sterile |
| Biotinylated peanut agglutinin (PNA) | Vector Labs | B-1075-5 | |
| C57BL/6J mice | Jackson Laboratories | 664 | |
| Corning Falcon test tube with cell strainer snap cap | Fisher | 08-771-23 | |
| DAPI (4',6-Diamidino-2-Phenylindole, dihydrochloride) | Fisher | D1306 | 0.5 mg/ml |
| dNTP | NEB | N0447L | 10 mM |
| ElectroMAX DH10B competent cells | Fisher | 18-290-015 | |
| Falcon cell strainer 40mm | Fisher | 08-771-1 | |
| Falcon round-bottom polystyrene tubes (FACS tubes) | Fisher | 14-959-5 | |
| Falcon round-bottom polystyrene tubes (capped) | Fisher | 149591A | |
| Fetal bovine serum | R&D Systems (Atlanta Biologicals) | S11150 | |
| Gibco phosphate buffered saline PBS pH 7.4 | Fisher | 10-010-049 | |
| Glycogen | Sigma | 10901393001 | |
| Lasergene Molecular Biology (MegAlign Pro) | DNA Star | version 15 | |
| PE anti-CD45R/B220 | BD | 553090 | clone RA3-6B2 |
| Proteinase K | Fisher | BP1700-100 | |
| Q5 High-Fidelity DNA Polymerase | NEB | M0491L | |
| QIAquick Gel Extraction Kit | Qiagen | 28706 | |
| Seal-Rite 1.5mL microcentrifuge tubes | USA Scientific | 1615-5500 | |
| Streptavidin APC-eFluor 780 Conjugate | eBioscience | 47-4317-82 | |
| T4 DNA ligase | NEB | M020L | |
| Thermo Scientific CloneJET PCR Cloning Kit | ThermoFisher | FERK1231 | |
| Tissue culture plate 6 well | Fisher | 08-772-1B | sterile |
| Unlabeled anti-mouse CD16/CD32 (Fc block), BD | Fisher | BDB553142 | Clone 2.4G2 |
- Murphy, K., Weaver, C. . Janeyway's Immunobiology. , (2016).
- Alt, F. W., et al. VDJ recombination. Immunology Today. 13 (8), 306-314 (1992).
- Schatz, D. G., Ji, Y. Recombination centres and the orchestration of V (D) J recombination. Nature Reviews Immunology. 11 (4), 251-263 (2011).
- Oettinger, M. A., Schatz, D. G., Gorka, C., Baltimore, D. RAG-1 and RAG-2, adjacent genes that synergistically activate V (D) J recombination. Science. 248 (4962), 1517-1523 (1990).
- Berek, C., Berger, A., Apel, M. Maturation of the immune response in germinal centers. Cell. 67 (6), 1121-1129 (1991).
- Linterman, M. A., et al. Foxp3+ follicular regulatory T cells control the germinal center response. Nature Medicine. 17 (8), 975 (2011).
- Shulman, Z., et al. T follicular helper cell dynamics in germinal centers. Science. 341 (6146), 673-677 (2013).
- Good-Jacobson, K. L., et al. PD-1 regulates germinal center B cell survival and the formation and affinity of long-lived plasma cells. Nature Immunology. 11 (6), 535 (2010).
- Kerfoot, S. M., et al. Germinal center B cell and T follicular helper cell development initiates in the interfollicular zone. Immunity. 34 (6), 947-960 (2011).
- Chaudhuri, J., Alt, F. W. Class-switch recombination: interplay of transcription, DNA deamination and DNA repair. Nature Reviews Immunology. 4 (7), 541-552 (2004).
- Alt, F. W., Zhang, Y., Meng, F. L., Guo, C., Schwer, B. Mechanisms of programmed DNA lesions and genomic instability in the immune system. Cell. 152 (3), 417-429 (2013).
- Xu, Z., Zan, H., Pone, E. J., Mai, T., Casali, P. Immunoglobulin class-switch DNA recombination: induction, targeting and beyond. Nature Reviews Immunology. 12 (7), 517-531 (2012).
- Di Noia, J. M., Neuberger, M. S. Molecular mechanisms of antibody somatic hypermutation. Annual Reviews of Biochemistry. 76, 1-22 (2007).
- Peled, J. U., et al. The biochemistry of somatic hypermutation. Annual Review of Immunology. 26, 481-511 (2008).
- Liu, M., Schatz, D. G. Balancing AID and DNA repair during somatic hypermutation. Trends in Immunology. 30 (4), 173-181 (2009).
- Methot, S., Di Noia, J. Molecular Mechanisms of Somatic Hypermutation and Class Switch Recombination. Advances in Immunology. 133, 37-87 (2017).
- Muramatsu, M., et al. Class switch recombination and hypermutation require activation-induced cytidine deaminase (AID), a potential RNA editing enzyme. Cell. 102 (5), 553-563 (2000).
- Petersen-Mahrt, S. K., Harris, R. S., Neuberger, M. S. AID mutates E. coli suggesting a DNA deamination mechanism for antibody diversification. Nature. 418 (6893), 99 (2002).
- Revy, P., et al. Activation-induced cytidine deaminase (AID) deficiency causes the autosomal recessive form of the Hyper-IgM syndrome (HIGM2). Cell. 102 (5), 565-575 (2000).
- Petersen-Mahrt, S. DNA deamination in immunity. Immunological Reviews. 203 (1), 80-97 (2005).
- Rada, C., Di Noia, J. M., Neuberger, M. S. Mismatch recognition and uracil excision provide complementary paths to both Ig switching and the A/T-focused phase of somatic mutation. Molecular Cell. 16 (2), 163-171 (2004).
- Rada, C., et al. Immunoglobulin isotype switching is inhibited and somatic hypermutation perturbed in UNG-deficient mice. Current Biology. 12 (20), 1748-1755 (2002).
- Schrader, C. E., Vardo, J., Stavnezer, J. Role for mismatch repair proteins Msh2, Mlh1, and Pms2 in immunoglobulin class switching shown by sequence analysis of recombination junctions. The Journal of Experimental Medicine. 195 (3), 367-373 (2002).
- Martin, A., et al. Msh2 ATPase activity is essential for somatic hypermutation at AT basepairs and for efficient class switch recombination. The Journal of Experimental Medicine. 198 (8), 1171-1178 (2003).
- Imai, K., et al. Human uracil-DNA glycosylase deficiency associated with profoundly impaired immunoglobulin class-switch recombination. Nature Immunology. 4 (10), 1023-1028 (2003).
- Masani, S., Han, L., Yu, K. Apurinic/apyrimidinic endonuclease 1 is the essential nuclease during immunoglobulin class switch recombination. Molecular and Cellular Biology. 33 (7), 1468-1473 (2013).
- Guikema, J. E., et al. APE1-and APE2-dependent DNA breaks in immunoglobulin class switch recombination. The Journal of Experimental Medicine. 204 (12), 3017-3026 (2007).
- Schrader, C. E., Guikema, J. E., Wu, X., Stavnezer, J. The roles of APE1, APE2, DNA polymerase β and mismatch repair in creating S region DNA breaks during antibody class switch. Philosophical Transactions of the Royal Society B: Biological Sciences. 364 (1517), 645-652 (2009).
- Roa, S., et al. MSH2/MSH6 complex promotes error-free repair of AID-induced dU: G mispairs as well as error-prone hypermutation of A: T sites. PLoS One. 5 (6), 11182 (2010).
- Delbos, F., Aoufouchi, S., Faili, A., Weill, J. C., Reynaud, C. A. DNA polymerase η is the sole contributor of A/T modifications during immunoglobulin gene hypermutation in the mouse. The Journal of Experimental Medicine. 204 (1), 17-23 (2007).
- Maul, R. W., Gearhart, P. J. AID and somatic hypermutation. Advances in Immunology. 105, 159-191 (2010).
- Shen, H. M., Tanaka, A., Bozek, G., Nicolae, D., Storb, U. Somatic hypermutation and class switch recombination in Msh6-/- Ung-/- double-knockout mice. The Journal of Immunology. 177 (8), 5386-5392 (2006).
- Cheng, H. L., et al. Integrity of the AID serine-38 phosphorylation site is critical for class switch recombination and somatic hypermutation in mice. Proceedings of the National Academy of Sciences. 106 (8), 2717-2722 (2009).
- Lebecque, S. G., Gearhart, P. J. Boundaries of somatic mutation in rearranged immunoglobulin genes: 5'boundary is near the promoter, and 3'boundary is approximately 1 kb from V (D) J gene. The Journal of Experimental Medicine. 172 (6), 1717-1727 (1990).
- Jolly, C. J., Klix, N., Neuberger, M. S. Rapid methods for the analysis of immunoglobulin gene hypermutation: application to transgenic and gene targeted mice. Nucleic Acids Research. 25 (10), 1913-1919 (1997).
- Choi, J. E., Matthews, A. J., Michel, G., Vuong, B. Q. AID Phosphorylation Regulates Mismatch Repair-Dependent Class Switch Recombination and Affinity Maturation. The Journal of Immunology. 204 (1), 13-22 (2020).
- McBride, K. M., et al. Regulation of class switch recombination and somatic mutation by AID phosphorylation. The Journal of Experimental Medicine. 205 (11), 2585-2594 (2008).
- Liu, M., et al. Two levels of protection for the B cell genome during somatic hypermutation. Nature. 451 (7180), 841-845 (2008).
- Ross, M., Birbeck, M., Wills, V., Forrester, J., Davis, A. Peanut lectin binding properties of germinal centers of mouse lymphoid tissues. Nature. 284, 364-366 (1980).
- Zhang, J., MacLennan, I. C., Liu, Y. J., Lane, P. J. Is rapid proliferation in B centroblasts linked to somatic mutation in memory B cell clones. Immunology Letters. 18 (4), 297-299 (1988).
- Nieuwenhuis, P., Opstelten, D. Functional anatomy of germinal centers. American Journal of Anatomy. 170 (3), 421-435 (1984).
- Lau, A. W., Brink, R. Selection in the germinal center. Current Opinion in Immunology. 63, 29-34 (2020).
- Victora, G. D., Nussenzweig, M. C. Germinal centers. Annual Review of Immunology. 30, 429-457 (2012).
- Mesin, L., Ersching, J., Victora, G. D. Germinal center B cell dynamics. Immunity. 45 (3), 471-482 (2016).
- Reichert, R. A., Gallatin, W. M., Weissman, I. L., Butcher, E. C. Germinal center B cells lack homing receptors necessary for normal lymphocyte recirculation. The Journal of Experimental Medicine. 157 (3), 813-827 (1983).
- Rose, M., Birbeck, M., Wills, V., Forrester, J., Davis, A. Peanut lectin binding properties of germinal centers of mouse lymphoid tissues. Nature. 284, 364-366 (1980).
- Hamada, S., Fujita, S. DAPI staining improved for quantitative cytofluorometry. Histochemistry. 79 (2), 219-226 (1983).
- Otto, F. DAPI staining of fixed cells for high-resolution flow cytometry of nuclear DNA. Methods in Cell Biology. 33, 105-110 (1990).
- Butcher, E., et al. Surface phenotype of Peyer's patch germinal center cells: implications for the role of germinal centers in B cell differentiation. The Journal of Immunology. 129 (6), 2698-2707 (1982).
- Rogerson, B. J., Harris, D. P., Swain, S. L., Burgess, D. O. Germinal center B cells in Peyer's patches of aged mice exhibit a normal activation phenotype and highly mutated IgM genes. Mechanisms of Ageing and Development. 124 (2), 155-165 (2003).
- Potapov, V., Ong, J. L. Examining sources of error in PCR by single-molecule sequencing. PloS One. 12 (1), 0169774 (2017).
- Gonzalez-Fernandez, A., Milstein, C. Analysis of somatic hypermutation in mouse Peyer's patches using immunoglobulin kappa light-chain transgenes. Proceedings of the National Academy of Sciences. 90 (21), 9862-9866 (1993).
- Reboldi, A., Cyster, J. G. Peyer's patches: organizing B-cell responses at the intestinal frontier. Immunological Reviews. 271 (1), 230-245 (2016).
- Betz, A. G., Rada, C., Pannell, R., Milstein, C., Neuberger, M. S. Passenger transgenes reveal intrinsic specificity of the antibody hypermutation mechanism: clustering, polarity, and specific hot spots. Proceedings of the National Academy of Sciences. 90 (6), 2385-2388 (1993).
- Rada, C., Gupta, S. K., Gherardi, E., Milstein, C. Mutation and selection during the secondary response to 2-phenyloxazolone. Proceedings of the National Academy of Sciences. 88 (13), 5508-5512 (1991).
- Heise, N., Klein, U. Somatic Hypermutation and Affinity Maturation Analysis Using the 4-Hydroxy-3-Nitrophenyl-Acetyl (NP) System. Methods in Molecular Biology. 1623, 191-208 (2017).
- Smith, F., Cumano, A., Licht, A., Pecht, I., Rajewsky, K. Low affinity of kappa chain bearing (4-hydroxy-3-nitrophenyl) acetyl (NP)-specific antibodies in the primary antibody repertoire of C57BL/6 mice may explain lambda chain dominance in primary anti-NP responses. Molecular Immunology. 22 (10), 1209-1216 (1985).
- Takahashi, Y., Dutta, P. R., Cerasoli, D. M., Kelsoe, G. In situ studies of the primary immune response to (4-hydroxy-3-nitrophenyl) acetyl. V. Affinity maturation develops in two stages of clonal selection. The Journal of Experimental Medicine. 187 (6), 885-895 (1998).
- Allen, D., Simon, T., Sablitzky, F., Rajewsky, K., Cumano, A. Antibody engineering for the analysis of affinity maturation of an anti-hapten response. The EMBO Journal. 7 (7), 1995-2001 (1988).
- Cumano, A., Rajewsky, K. Clonal recruitment and somatic mutation in the generation of immunological memory to the hapten NP. The EMBO Journal. 5 (10), 2459-2468 (1986).
- Smith, K., Nossal, G., Tarlinton, D. M. FAS is highly expressed in the germinal center but is not required for regulation of the B-cell response to antigen. Proceedings of the National Academy of Sciences. 92 (25), 11628-11632 (1995).
- Hao, Z., et al. Fas receptor expression in germinal-center B cells is essential for T and B lymphocyte homeostasis. Immunity. 29 (4), 615-627 (2008).
- Cervenak, L., Magyar, A., Boja, R., László, G. Differential expression of GL7 activation antigen on bone marrow B cell subpopulations and peripheral B cells. Immunology Letters. 78 (2), 89-96 (2001).
- Naito, Y., et al. Germinal center marker GL7 probes activation-dependent repression of N-glycolylneuraminic acid, a sialic acid species involved in the negative modulation of B-cell activation. Molecular and Cellular Biology. 27 (8), 3008-3022 (2007).
- Olson, W. J., et al. Orphan Nuclear Receptor NR2F6 Suppresses T Follicular Helper Cell Accumulation through Regulation of IL-21. Cell Reports. 28 (11), 2878-2891 (2019).
- Dorsett, Y., et al. MicroRNA-155 suppresses activation-induced cytidine deaminase-mediated Myc-Igh translocation. Immunity. 28 (5), 630-638 (2008).
- Goetz, C., Hammerbeck, C., Bonnevier, J. . Flow Cytometry Basics for the Non-Expert. , (2018).
- Hawley, T. S., Herbert, D. J., Eaker, S. S., Hawley, R. G. . Flow Cytometry Protocols. , (2004).
- Costa, E., et al. A new automated flow cytometry data analysis approach for the diagnostic screening of neoplastic B-cell disorders in peripheral blood samples with absolute lymphocytosis. Leukemia. 20 (7), 1221-1230 (2006).
- McKinnon, K. M. Flow cytometry: An overview. Current Protocols in Immunology. 120 (1), 1-11 (2018).
- McKinnon, K. M. Multiparameter Conventional Flow Cytometry. Methods in Molecular Biology. , 139-150 (2018).
- Lucchesi, S., et al. Computational Analysis of Multiparametric Flow Cytometric Data to Dissect B Cell Subsets in Vaccine Studies. Cytometry Part A. 97, 259-267 (2019).
- Longerich, S., Tanaka, A., Bozek, G., Nicolae, D., Storb, U. The very 5' end and the constant region of Ig genes are spared from somatic mutation because AID does not access these regions. The Journal of Experimental Medicine. 202 (10), 1443-1454 (2005).
- Retter, I., et al. Sequence and characterization of the Ig heavy chain constant and partial variable region of the mouse strain 129S1. The Journal of Immunology. 179 (4), 2419-2427 (2007).
- Shen, H. M., Peters, A., Baron, B., Zhu, X., Storb, U. Mutation of BCL-6 gene in normal B cells by the process of somatic hypermutation of Ig genes. Science. 280 (5370), 1750-1752 (1998).
- Richter, K., et al. Altered pattern of immunoglobulin hypermutation in mice deficient in Slip-GC protein. Journal of Biological Chemistry. 287 (38), 31856-31865 (2012).
Tags
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved