Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Immunology and Infection
从小鼠佩耶的补丁中对Germinal中心B细胞JH4因特龙的体细胞突变分析
这里介绍的是一个检测,以量化免疫球蛋白重链基因轨迹内的体细胞突变使用细菌中心B细胞从小鼠Peyer的补丁。
在淋巴器官的生殖中心内,成熟的B细胞通过将未平板的突变引入Ig重链基因的可变编码外显子来改变其表达的免疫球蛋白(Ig)。这种体质超突变(SHM)过程需要酶激活引起的环氨酸二胺酶(AID),将脱氧细胞丁(C)转化为脱氧尿素(U)。通过基础切除和不匹配修复途径将 AID 生成的 U:G 错配处理成突变,引入新的 Ig 编码序列,这些序列可能会产生更高的亲和力 Ig。 AID 或DNA修复基因的突变可以阻止或显著改变在Ig loci中观察到的突变类型。我们描述了一个使用荧光激活细胞分拣 (FACS)、PCR 和 Sanger 测序来量化 JH4 直流突变的协议。虽然此测定不直接测量 Ig 亲和力成熟度,但它表示 Ig 可变编码序列中的突变。此外,这些方法还利用常见的分子生物学技术分析多个B细胞克隆Ig序列中的突变。因此,这种测定是研究SHM和Ig多样化的宝贵工具。
B细胞是适应性免疫系统的成员,通过产生抗体(也称为免疫球蛋白(Ig)来识别和消除抗原。每个Ig由两个重(IgH)和两个轻(IgL)链聚肽组成,它们由硫化物键粘在一起,形成Ig1的特征"Y"形结构。IgH 和 IgL 的 N-termini 包括每个聚肽的可变 (V) 区域,它们共同构成了 Ig 的抗原结合位点,而 IgH 的恒定区域则传授 Ig 的效应器函数。在骨髓中培养B细胞,在称为V(D)J重组2、3、4的过程中重新排列IgH和IgL的V编码外子。重新组合的 V exons 的转录,加上各自的恒定区域外因,形成被转换为 Ig 的 mRNA。
表示膜绑定Ig(也称为B细胞受体)的成熟B细胞循环到继发淋巴器官,如脾脏、淋巴结或Peyer的斑块,在那里它们测量抗原的环境,并与免疫系统的其他细胞1相互作用。在二级淋巴器官的生殖中心(GC)内,通过BCR识别抗原的B细胞被激活。在卵泡树突状细胞和卵泡辅助T细胞的帮助下,激活的B细胞随后可以增殖并分化成血浆和记忆细胞,它们是强大的免疫反应5、6、7、8、9的重要影响因素。此外,这些激活的B细胞可以经历继发性Ig基因多样化过程 - 类开关重组(CSR)和体细胞突变(SHM)。在CSR期间,B细胞通过DNA删除重组反应(图1)将IgH多肽的默认μ恒定区域与另一个恒定区域(γ、α、ε)交换。这允许表达一个不同的恒定的exon和翻译一个新的Ig。B 细胞将从表达 IgM 切换到另一个等型(IgG、IgA、IgE)。CSR在不改变其抗原特异性10、11、12的情况下,改变Ig的效应器功能。然而,在SHM期间,B细胞会变异IgH和IgL的V编码区域,从而能够产生和选择更高的亲和力IG,从而更有效地消除抗原13、14、15(图1)。重要的是,CSR和SHM都依赖于一种酶的功能:激活引起的环氨酸酶(AID)16,17,18。缺乏AID的人类和小鼠不能完成CSR或SHM,并存在高升IgM血清滴度或超IgM17,19。
在 CSR 中,AID 在每个恒定编码前体之前的重复开关区域脱氧细胞丁 (C), 将其转换为脱氧尿素 (U)20,21, 这在脱氧尿素和脱氧瓜诺辛 (U:G) 之间创建不匹配的基础配对。 这些 U:G 错配通过基础切除修复 (BER) 或不匹配修复 (MMR) 路径22、23、24、25、26、27、28、29将转换为脱氧核糖核酸重组所需的双链脱氧核糖核酸断裂。在 SHM 中,AID 在 V 编码前体中除名 C。在整个U:G不匹配的复制产生C:G到T:A过渡突变,而去除尿素碱基的BER蛋白,尿素DNA糖酶(UNG),在DNA复制之前产生过渡和变异突变16。UNG中的空突变显著增加C:G到T:A过渡突变21,22。与 CSR 类似,SHM 需要 MMR 和 BER 的互补角色。在 SHM 期间,MMR 会在 A:T 碱基对中生成突变。在MutS同源性2(MSH2)或DNA聚合酶η(Polη)中停用突变显著减少A:T碱基的突变和MSH2中的复合突变,Polη实际上消除了A:T碱基21、30、31的突变。与 BER 和 MMR 在将 AID 生成的 U 转换为过渡或反转突变方面的关键作用一致,MSH2 和UNG(MSH2-/-UNG-)的鼠标仅显示 C:G 到 T:U:G 不匹配21中复制产生的过渡突变。
V编码区域对SHM的分析仍然很复杂,因为开发B细胞可以重新组合IgH和IgL loci1、2、4中的任何V(D)J编码外显子。 准确分析这些独特的重组和体细胞变异的V区域需要识别和隔离克隆的B细胞或Ig mRNA11,13。JH4 intron 是 IgH locus 中最后一个 J 编码 exon 的 3' ,由于 V 发起器32、33、34的突变 3' 的扩散而具有体细胞突变,因此在 V 区域31、35(图1)中经常用作 SHM 的代理标记。为了在实验中阐明特定基因或基因突变如何改变SHM模式或速率,JH4因特龙可以从Peyer的贴片(PP)基因中心B细胞(GCBCs)进行测序,这些细胞的SHM36、37、38的速率很高。GCBC可以很容易地识别和隔离与荧光结合抗体对细胞表面标记 (B220+PNAHI)17,39.
提出了一个详细的协议,使用FACS(荧光激活细胞分拣)、PCR和桑格测序(图2)的组合来描述来自小鼠的PP GCBC中的JH4直流突变。
所有突变小鼠均以C57BL/6为背景进行维护。年龄匹配(2-5个月大)的雄性小鼠和雌性小鼠用于所有实验。对小鼠进行饲养和实验是根据纽约城市学院机构动物护理和使用委员会批准的协议进行的。
1. 对佩耶的补丁进行解剖
- 用100%CO2 在3L/min安乐死小鼠5分钟,然后子宫颈脱位,以确认死亡。用70%乙醇消毒解剖工具(剪刀、钳子、细钳子)和戴手套的手。
- 将鼠标放在解剖垫上,腹部暴露。慷慨地喷洒70%乙醇小鼠的身体之前,作出任何切口消毒解剖区域。
- 用钳子(或消毒的戴手套的手)同时将切口的两侧拉向头部和尾部,切入腹部的皮肤,从腹部取出皮肤。
- 固定鼠标的前肢和后肢。
- 用剪刀切开腹腔,露出内脏。
- 定位胃和胃之间的小肠(结肠附近的"J"形结构)。通过切开胃下面和上方的小肠。
- 去除连接小肠褶皱的任何结缔组织和脂肪。
注意:脂肪将有一个独特的白色,不像小肠的粉红色。 - 检查小肠的外部表面,寻找Peyer的斑块(PPs),这些斑块很小(+1毫米),椭圆形结构在一层半透明上皮细胞下呈白色。
- 用剪刀小心地切除所有可见的PP。
注:一个 C57BL/6 野生型 (WT) 鼠标可以产生 4-8 PPs,而AID-/-鼠标将产生 6-10 PPs。 - 将 PPs 收集到 1.5 mL 微中福格管中,其中含有 1 mL 的 FACS 缓冲器在冰上。
注意:PP应该下沉,而脂肪会浮到表面,可以去除。
2. FACS 的细胞隔离
- 将 40μm 过滤器放在 6 井盘中,配有 1 mL 的冷 (4 °C) FACS 缓冲器。
- 将 1.5 mL 管中的 PP 倒入过滤器。
- 使用 1 mL 的冷 FACS 缓冲器清洗 PP,确保它们始终处于液体和冰层中。
- 使用 1 mL 注射器的柱塞平端作为害虫,粉碎过滤器上的 PPs,直到过滤器上仅保留结缔组织。
- 用 1 mL 的冷 FACS 缓冲器清洗过滤器和柱塞,将细胞释放到 6 井盘中。
- 在冷 FACS 缓冲区中收集约 4 mL 的细胞,并通过 40μm 过滤器盖 FACS 管过滤它们。
- 用 1 mL 的冷 FACS 缓冲器清洗滤网盖。
- 在摆动桶离心机中,在 4 °C 下以 600 x g 的速度将细胞颗粒化 5 分钟。
- 去除超自然人。
- 在 0.4 mL 的冷 FACS 缓冲区中恢复细胞。
- 删除 10 μL 进行细胞计数以验证产量(预计 +5 x 106 细胞/鼠标,参见 图 3A)
- 将剩余的细胞通过 40μm 过滤器盖过滤到 FACS 管中,然后继续染色 FACS。
3. 为 FACS 染色 GCC
- 在 400 μL 细胞悬架中加入 1 μL Fc 块(未标记的反鼠标 CD16/CD32),并将细胞放在冰上 15 分钟。
- 添加2mL的冷FACS缓冲器来清洗细胞。
- 颗粒细胞在 600 x g 在 4 °C 5 分钟,并丢弃超自然。
- 在 80 μL 的冷 FACS 缓冲区中恢复细胞。
- 为每个染色控制从 WT PP 中去除 10 μL 的细胞(总共 4 个,包括 3 个单个污渍控制和 1 个未染色控制)。为下一步保留 WT PP 的 40 μL。或者,使用补偿珠进行染色控制。
- 在 500 μL 的冷 FACS 缓冲器中染色每个实验样本(例如 WT 和 AID--),在冰上用 2.5μL 的花生胶蛋白 (PNA) - 生物素 15 分钟。
- 添加2mL的冷FACS缓冲器来清洗细胞。
- 颗粒细胞在 600 x g 在 4 °C 5 分钟,并丢弃超自然。
- 用500微升的鸡尾酒在黑暗中,在冰上染色每个实验样本15分钟 (表1)。 确保细胞在染色鸡尾酒中完全恢复。
- 为补偿矩阵准备单个污渍控制。
- 使用 表 2中指定的稀释剂在 500μL 的冷 FACS 缓冲区中染色细胞。
- 在黑暗中,在冰上孵化染色控制器15分钟。
- 在步骤 3.7 和 3.8 中将 2 mL 冷 FACS 缓冲器添加到所有管中,颗粒细胞,并丢弃超自然体以洗掉未绑定的抗体或 DAPI。
- 将细胞在 500 μL 的冷 FACS 缓冲区中恢复并放置在冰上。
- 使用细胞分拣机,从每个染色实验样本中收集 B220+PNAHI。图3B显示了从WT和AID-/-PPs获得的B220+PNA HI的典型百分比。图3C显示FACS门控策略。
4. 从GCBC提取的DNA
- Pellet 在 4 °C 时将细胞分拣为 600 x g 5 分钟,然后丢弃超自然体。
- 将细胞重新注入1mL的冷FACS缓冲器中,并将细胞转移到1.5mL微中微管中。
- 在 4 °C 下以 600 x g 的速度将细胞颗粒化 5 分钟,然后丢弃超自然体。
- 在 500 μL 的 DNA 提取缓冲器和 5 μL 的 20 毫克/mL 蛋白酶 K 中补充细胞。
- 在56°C的夜间孵化。
- 用500μL异丙酚和1μL的20毫克/mL糖原沉淀DNA。通过倒置 5-6 倍彻底混合管。
- 在室温下孵化10分钟。
- 离心机在微中心中15分钟,在25°C在21,000 x g。
- 丢弃超自然物并保留含有沉淀DNA和糖原的颗粒。
- 用70%乙醇的1mL清洗DNA颗粒。
- 在 25 °C 的 21,000 x g下,将 DNA 在微中枢中颗粒 10 分钟。
- 取出70%的乙醇,将DNA颗粒空气干燥5-10分钟。
注意:避免过度干燥,因为DNA可能不会完全补充水分。
- 在 30 μL TE 缓冲器中补充 DNA,并在 56 °C 的夜间孵化。
5. JH4 直子序列放大和分析
- 通过测量波长为 260 nm (A260) 的吸收量来量化 DNA。
注:从 C57BL/6 小鼠的分拣 B220+PNAHI GCBC 中回收的 DNA 典型浓度为 20-40 ng/μL。 - 执行JH4直子的嵌套PCR(表3,表4)。将第一个 PCR 中使用的基因组脱氧核糖核酸总量标准化为最不集中的样本。(例如,如果最不集中的样本为 5 ng/μL,则使用 58.75 ng 的 DNA 作为 PCR #1中水的最大体积(11.75 μL)中的所有样本。
- 在 200 V 的 1.5% agarose 凝胶上解决 PCR 产品 20 分钟。预计放大幅度为580个基点。
- 从凝胶中提取放大器,并根据制造商的说明使用凝胶提取套件提取DNA(见补充图1)。
- 用 30μL 的水将 DNA 稀释,并通过测量 A260 来量化 DNA 的量。
注:纯化 PCR 产品的典型浓度为 3-10 ng/μL。
- 用 30μL 的水将 DNA 稀释,并通过测量 A260 来量化 DNA 的量。
- 将纯化的 PCR 产品放入具有钝端的质粒中。标准化每次套合反应中使用的 PCR 产品总量(表5)。
- 在室温下孵化 5 分钟或在 16 °C 过夜的连带反应。
- 使用 2μL 的配对反应转换电能力细菌细胞。
- 电极速在1.65千伏。
- 在 225 rpm 的摇晃孵化器中,在 600 μL 的 SOC 介质中以 37 °C 的速度进行 1 小时的救援。
- 板 100 μL 的转化细菌到 LB 补充安培林 (100μg/mL) agar 板和孵化过夜在 37 °C.
- 使用 T7 前引物提交用于桑格测序的细菌菌落板。或者,生长每个细菌群落的隔夜培养物,并进行质粒净化。
- 如有必要,重复PCR、结对和/或转化,以优化细菌菌落的产量
注:应从每个盘子中至少挑选 30 个殖民地。
- 如有必要,重复PCR、结对和/或转化,以优化细菌菌落的产量
- 标准化.txt文件中的序列数据
- 删除质粒序列。
- 确保每个序列根据 JH4 intron 参考序列 (NG_005838) 定向 5' 到 3' 。根据需要生成任何序列的反向补充。
- 使用 Clustal 欧米茄软件 (图 4A)将每个 PCR 获得的序列与 JH4 直子参考序列 (NG_005838) 对齐。
- 将参考序列中的差异识别为突变
- 通过检查桑格测序的电球图,验证所有突变都是真点突变。如有必要,重复排序。(图 4B,C) 。
- 为每个基因型(图 5)在 JH4 直子中表布和量化独特的突变。
- 仅对具有相同突变的序列进行计数一次
注:无法确定相同的序列是在 PCR 期间生成的还是在不同的 B 单元中生成的相同 SHM 事件。 - 将WT生殖系JH4直子序列(即那些没有突变的)的每一个实例计算为一个独特的序列。
- 仅对具有相同突变的序列进行计数一次
流动细胞测量
成熟的B细胞循环到生殖中心,在那里它们经历亲和力成熟,克隆扩张,并分化成血浆或记忆细胞40,41,42,43,44。这些GCBC可以通过许多细胞表面标记来识别,包括CD45R/B220受体的高表达和花生凝胶素(PNA)45,46的结合。为了分离激活的 GCBC,PP 细胞被与植物红素 (PE) 和生物基化 PNA 结合的抗 B220 抗体染色,随后与 APC-eFluor780 结合的链球菌素。死细胞被消除使用荧光4',6-迪亚米迪诺-2-菲尼林多尔(DAPI)染料,污渍死亡或死细胞的核酸47,48。随后通过流动细胞测量对染色细胞进行分析和排序。PP由+80%B220+细胞49,50组成。WT PP平均包含每只小鼠4×10 6个细胞(图3A)。大约 8% 的 WT PP 细胞是 B220+PNAHI,是AID-/ - (图3B)中观察到的一半。因此,在分拣后获得 0.3-0.6 x10 6 B220+PNAHI GCBC,这足以分析 JH4 直子中的突变。
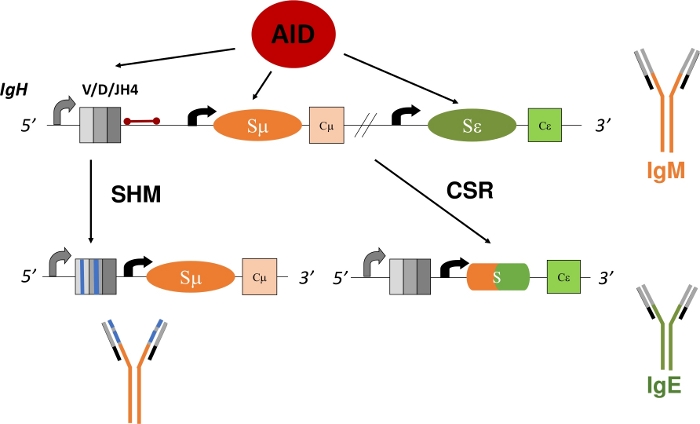
图 1:IgH 基因轨迹的原理图,以及艾滋病在CSR和SHM期间所针对的区域。红色条表示 VDJH4 重新排列的 3' 的 580 bp JH4 直子,并在本协议中进行分析。在CSR中,内向开关区域(Sμ 和Sε)的 AID 依赖性除污可促进 DSB 的形成,从而允许进行删除重组和表达新的抗体同位素 (IgM 到 IgE)。在 SHM 期间,V 区域(灰色框)会累积突变(蓝线),从而可能导致更高的亲和力 Ig。 请单击此处查看此图的更大版本。
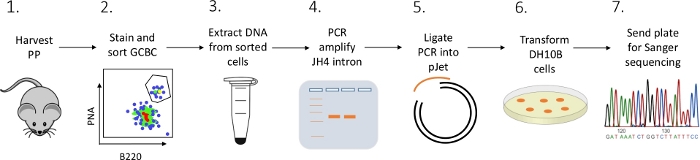
图2:工作流程,分析与PP分离的GCBC中JH4直流的SHM。请单击此处查看此图的更大版本。
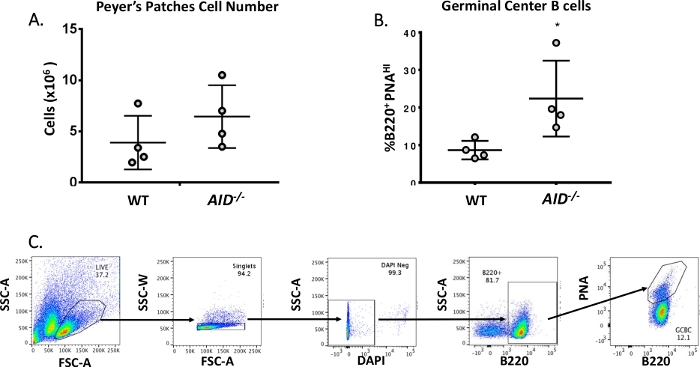
图3:PP GCBC的特征。(A) 来自 WT 和AID-/-小鼠的 PP 细胞总数(n = 每个基因型 4 个)。错误条表示标准偏离均值。(B) 从WT和AID-小鼠的PP中获得的B220+PNAHI GCBC的百分比(n = 4每基因型)36。错误条表示使用学生 t 测试的标准偏离平均值 *p<0.05。(C) 代表 Facs 阴谋从 Pps 中排序 B220+PnaHi Gcbcs 。请点击这里查看此图的更大版本。
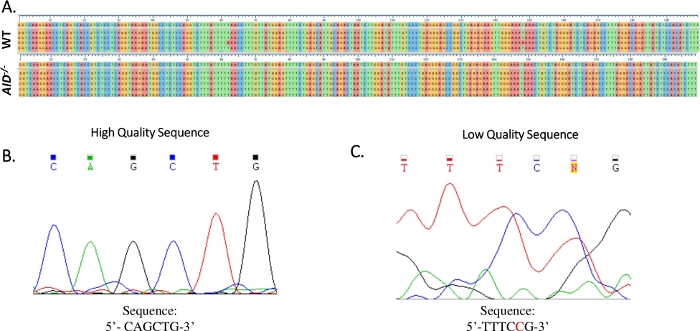
图4:JH4桑格序列数据分析。(A) 从WT(顶部)和AID-/-(底部)GCBC到参考基因组序列(NG_005838)的JH4 PCR产品的桑格序列数据的样本序列对齐,该序列紧随编号滴答声标记的正下方。 使用粘结欧米茄生成对齐。(B) 高质量的桑格序列数据的电子信息图,显示每个基座有明显的峰值。(C) 低质量序列数据的电球图,显示模糊的峰值和未指定的基数 (N)。以红色显示的核苷酸必须在序列文本文件中手动注释。 请单击此处查看此图的更大版本。
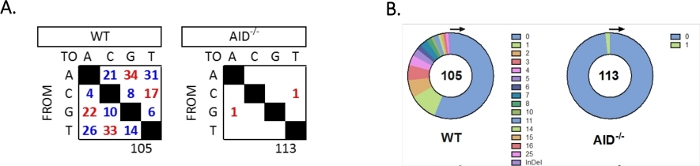
图5:WT和AID-GCBC中JH4直子突变的分析。(A) 每个基因型的 A、C、G 和 T 基的过渡(红色)和反转(蓝色)突变总数在表中进行汇总。分析的序列总数在表下方指示。(B) 每个基因型每个 PCR 放大器的突变数在饼图中描述。此数字已从 Choi 等人36版权 2020 中修改。美国免疫学家协会,公司请点击这里查看这个数字的更大版本。
| GCBC 的染色鸡尾酒 | 音量: 500 μL | ||
| 抗体或染料 | 氟磷 | 稀释 | μL |
| B220 | 体育 | 1000 | 0.5 |
| 斯特雷普塔维丁 | APC-e弗卢尔780 | 500 | 1 |
| 达皮 | 不适用 | 500 | 1 |
表1:为GCC提供染色鸡尾酒。 指定稀释处指示的抗体或染料(在白化病中表示)的鸡尾酒用于在 500 μL 中染色 PP 细胞以进行流动细胞测量。
| 单一的污渍补偿 | 音量: 500 μL | ||
| 抗体或染料 | 氟磷 | 稀释 | μL |
| B220 | 体育 | 1000 | 0.5 |
| B220 | APC-e弗卢尔780 | 750 | 0.67 |
| 达皮 | 不适用 | 500 | 1 |
表2:单一污渍控制进行补偿。 与指示的氟酚结合的 B220 抗体用于单个污渍控制,以补偿光谱重叠。
| PCR #1 | ||||
| 试剂 | 卷 | 恒温器条件 | ||
| 5x 缓冲区 | 4μL | 1 | 95°C | 3 分钟 |
| 10毫米dNTP | 2μL | 2 | 94°C | 30 秒 |
| 10μM J558FR3Fw | 1μL | 3 | 55°C | 30 秒 |
| 10μM VHJ558.2 | 1μL | 4 | 72°C | 1:30分钟 |
| 高保真度DNA聚合酶 | 0.25 微升 | 周期 2-4 9 倍 | ||
| 脱氧核糖核酸 | x(标准化到最不集中的样本) | |||
| H2O | 至20μL | 5 | 72°C | 5 分钟 |
| 在进入 PCR #2之前,在 H 2 O 中稀释 PCR 产品1:5 | ||||
表3:JH4直子的嵌套PCR。 PCR 组件和恒温器条件为第一次放大反应。用水稀释第一个 PCR 产品 1:5,并在第二个 PCR 中使用 1 μL 的稀释。
| PCR #2 | ||||
| 试剂 | 卷 | 恒温器条件#2 | ||
| 5x 缓冲区 | 4μL | 1 | 94°C | 3 分钟 |
| 10毫米dNTP | 2μL | 2 | 94°C | 30 秒 |
| 10μM VHJ558.3 | 1μL | 3 | 55°C | 30 秒 |
| 10μM VHJ558.4 | 1μL | 4 | 72°C | 30 秒 |
| 高保真度DNA聚合酶 | 0.25 微升 | 周期 2-4 21x | ||
| 稀释的 PCR#1 | 1μL | |||
| H2O | 至20μL | 5 | 72°C | 5 分钟 |
表4:第二个 PCR 的 PCR 组件和恒温器条件。
| 试剂 | 卷 |
| 2x 缓冲区 | 10 微升 |
| 纯化五氯苯酚 | x(标准化到最不集中的样本) |
| 有钝端的普拉斯米德 | 1μL |
| T4 脱氧核糖核酸连气 | 1μL |
| H2O | 至20μL |
| 在室温下孵化5分钟或在16oC过夜 | |
表5:留置反应。 将纯化的 JH4 直子 PCR 产品与质粒成一体的组件。
| 法克斯缓冲区 |
| 使用前一小时在 56 °C 处加热 FBS。补充 PBS, pH 7.4 (吉布科, #10010049) 与 2.5% (v/v) 的热灭活 FBS.存放在 4°C。 |
| 脱氧核糖核酸提取缓冲区 (100 mM 特里斯 pH 8.0, 0.1 M EDTA, 0.5% (w/v) SDS) |
| 添加 50 mL 的 1 M 特里斯 pH 8.0, 100mL 的 0.5 M EDTA, 和 12.5 mL 的 20% SDS.将蒸馏水加入 500 mL。在室温下存放。 |
| 特缓冲区 (10 米特里斯 pH 8.0, 1 米 EDTA) |
| 添加 2.5 mL 的 1 M 特里斯 pH 8.0 和 500 mL 的 0.5 M EDTA。将蒸馏水加入 250 mL。在室温下存放。 |
表6:缓冲区食谱。
| 寡头核苷酸列表 | ||
| J558FR3福 | 5'-GCCT加特加克特克-3' | |
| VHJ558.2 | 5'-克特克-3' | |
| VHJ558.3 | 5'-格特卡加克特卡格卡-3' | |
| VHJ558.4 | 5'-特克塔加卡塔克-3' | |
表7:用于检测的寡核苷酸。
补充图1:第5.4步完成后,代表阿加罗斯凝胶图像。JH4 intron 嵌套 PCR 产品在 1.5% 的蔗糖凝胶上得到解决,580 bp 安培被切除。WT PP 表示 WT PP GCBC 基因组脱氧核糖核酸用作第一个 PCR 的模板,AID PP 表示AID-/-PP GCBC 基因组脱氧核糖核酸用作第一个 PCR 的模板。ɸ表示没有模板 PCR 控制 - 指示没有加载到 agarose 凝胶的井中。最后一条车道显示了一个100 bp的DNA梯子。请单击此处下载此图。
鉴于每个 B 细胞在 V(D)J 重组34期间唯一重组 V 编码段,在异质 B 细胞群的IgH和IgL V 编码序列中对 SHM 进行定性是一个挑战。在本文中,我们描述了一种识别 GCBC JH4 intron 突变的方法。JH4 intron 位于IgH轨迹中最后一个 J 编码段的 3' 中,用作 V 区域 (图 1) 31、 33 、34、35的 SHM 的代理。为了编目这些JH4直肠突变并评估特定基因如何影响突变的产生或模式,PP GCBC 进行了专门分析。这些细胞积累JH4因肠道微生物群长期刺激而突变。此外,来自未免疫小鼠PP的B220+PNAHI GCBC具有突变光谱,与免疫动物54、55的脾脏GCC相比。然而,JH4因特龙的突变不能与Ig亲和力成熟相关,因为这些突变是非编码的。
为了确定SHM是否改变Ig亲和力,小鼠应在腹腔内用抗原进行免疫接种,如NP(4-羟基-3-硝基甲基)与CGG(鸡伽马球蛋白)或KLH(钥匙孔跛行血红素)56。随后,mRNA 可以从脾气 B220+PNAHI GCBCs 中纯化,以检查 VH186.2 中的 SHM,即最常识别 NP 的 V 编码外号,并在 NP-CGG 或 NP-KLH 免疫 31、57、58、59、60 后发生变异。色氨酸-33在VH186.2中的黄氨酸突变的特点是将Ig亲和力提高到10倍59,60,因此,SHM和克隆选择产生了高亲和力Ig的一个指标。通过 ELISA 测量 NP7 和 NP20 特异性血清 Ig 滴定器,并在免疫过程中计算 Ig 特异性 NP7/NP20 比率,还记录了 V 区17、21、36的 SHM 产生的 Ig 亲和力成熟。这两种测定可用于将 VH186.2 编码序列中的 SHM 与 NP 特定 Ig 亲和力成熟度的变化关联。
无论是免疫动物还是未免疫动物,无论是用于分析 VH186.2 的 SHM 还是 JH4 intron,都必须准确识别 GCBC。我们提出了基于FACS的方法来隔离B220+PNAHI洲际弹道导弹。 或者,Fas 和非硫化 β2-6-锡利亚利-拉克纳克抗原,由 GL7 抗体 61、62、63、64 识别,也可用于隔离 GCBC,这些 PAC 被识别为 B220+Fas=GL7+65或 CD19+Fas=GL7+37。GL7表达紧密地反映了淋巴结64、65、66等活性GC中的PNA。除了使用特定于 GCBC 的抗体标记外,染色鸡尾酒还应最大限度地激发荧光和检测生物标志物,同时最大限度地减少荧光排放的光谱重叠。在低水平表达的抗原应检测与抗体,是结合到荧光与强大的发射荧光67。建议的染色方案进行了优化,用于对配备四个激光(405nm、488nm、561nm、633nm)和12个过滤器的细胞分拣机进行分析:但是,滤光片配置和激光可用性因细胞仪而异。为了根据试剂和设备的可用性修改协议,读者将参考额外的资源、在线频谱观看者以及出版的文献67、68、69、70、71、72、73。此处描述的多色染色协议要求对光谱重叠进行补偿,以确保分拣的细胞群是 GCBC,而不是对荧光发射的不准确检测。B220 是描述的 FACS (表 1B)的有用染色控制,因为 PP 将具有独特的 B220 负和正人群 (图 3C),从而允许对光谱重叠进行适当补偿。图 3C中提出的门控策略应用作准则。流细胞图可能因染色条件和细胞计设置而异。然而,4-10%的活细胞应该是B220+PNAHI 35,52。
必须验证 PP GCBC JH4 内的所有突变,以确保观察到的突变真正反映 SHM,而不是 PCR 或测序的人工制品。AID-/-B细胞可以作为一个有用的负控制,当检查SHM表型在其他突变小鼠模型,因为这些细胞不能完成SHM17,19。 AID-/-GCBCs中的JH4直流突变率(1.66x10-5突变/bp)20、21、36、37、38、50、74可与用于放大嵌套 PCR 中的 DNA 的高保真聚合酶 (5.3x10-7子/基/倍)51,52的错误率相媲美。如果没有AID-/-小鼠,将观察到的突变模式和频率与已发表的文献进行比较。Ig V区域每个碱基对分裂累积10-3-10-4个突变,比其他基因位点73,75的突变率高约106倍。结果可能因动物的年龄而异。或者,B220+PNALO细胞,标记为非 GCBC,在没有AID-/-小鼠52的情况下,可用作负控制。如果 WT GCBC 中的突变频率低于预期,则 WT 生殖系 JH4 内向序列可能不成比例地表示。在这种情况下,请确保 GCBC 得到适当的染色和分类,并且 PCR 不受 WT 细菌线 JH4 因特龙污染。此外,应彻底分析电图中的原始测序数据,以确保序列文本数据中的突变不会成为测序错误的人工制品。例如,桑格测序结果不佳可能会降低序列数据的可靠性(图 4)。这种对桑格序列数据的质量控制将提高 JH4 直子突变分析的准确性和可重复性。
作者没有什么可透露的。
我们感谢佐佐木的AID-/-老鼠。这项工作得到了国家少数民族健康与健康差异研究所(5G12MD007603)、国家癌症研究所(2U54CA132378)和国家普通医学科学研究所(1SC1GM132035-01)的支持。
| Name | Company | Catalog Number | Comments |
| 0.2 ml PCR 8-tube FLEX-FREE strip, attached clear flat caps, mixed | USA Scientific | 1402-4708 | |
| Ampicillin sodium salt | Fisher | BP1760-5 | |
| APC-eFluor780 anti-CD45R/B220 | eBioscience | 47-0452-80 | clone RA3-6B2 |
| BD FACSAria II | BD | 643186 | four lasers (405nm, 488nm, 561nm, 633nm) and 12 filters (PacBlue (450/50), AmCyan (502LP; 530/30), SSC (488/10), FITC (502LP; 530/30), PerCP-Cy5.5 (655LP; 695/40), PE (585/15), PE-Texas Red (600LP; 610/20), PE-Cy5 (630LP; 670/14), PE-Cy7 (735LP; 780/60), APC (660/20), Alexa700 (710LP; 730/45), APC-Cy7 (755LP; 780/60)) |
| BD slip tip 1mL syringe | Fisher | 14-823-434 | sterile |
| Biotinylated peanut agglutinin (PNA) | Vector Labs | B-1075-5 | |
| C57BL/6J mice | Jackson Laboratories | 664 | |
| Corning Falcon test tube with cell strainer snap cap | Fisher | 08-771-23 | |
| DAPI (4',6-Diamidino-2-Phenylindole, dihydrochloride) | Fisher | D1306 | 0.5 mg/ml |
| dNTP | NEB | N0447L | 10 mM |
| ElectroMAX DH10B competent cells | Fisher | 18-290-015 | |
| Falcon cell strainer 40mm | Fisher | 08-771-1 | |
| Falcon round-bottom polystyrene tubes (FACS tubes) | Fisher | 14-959-5 | |
| Falcon round-bottom polystyrene tubes (capped) | Fisher | 149591A | |
| Fetal bovine serum | R&D Systems (Atlanta Biologicals) | S11150 | |
| Gibco phosphate buffered saline PBS pH 7.4 | Fisher | 10-010-049 | |
| Glycogen | Sigma | 10901393001 | |
| Lasergene Molecular Biology (MegAlign Pro) | DNA Star | version 15 | |
| PE anti-CD45R/B220 | BD | 553090 | clone RA3-6B2 |
| Proteinase K | Fisher | BP1700-100 | |
| Q5 High-Fidelity DNA Polymerase | NEB | M0491L | |
| QIAquick Gel Extraction Kit | Qiagen | 28706 | |
| Seal-Rite 1.5mL microcentrifuge tubes | USA Scientific | 1615-5500 | |
| Streptavidin APC-eFluor 780 Conjugate | eBioscience | 47-4317-82 | |
| T4 DNA ligase | NEB | M020L | |
| Thermo Scientific CloneJET PCR Cloning Kit | ThermoFisher | FERK1231 | |
| Tissue culture plate 6 well | Fisher | 08-772-1B | sterile |
| Unlabeled anti-mouse CD16/CD32 (Fc block), BD | Fisher | BDB553142 | Clone 2.4G2 |
- Murphy, K., Weaver, C. . Janeyway's Immunobiology. , (2016).
- Alt, F. W., et al. VDJ recombination. Immunology Today. 13 (8), 306-314 (1992).
- Schatz, D. G., Ji, Y. Recombination centres and the orchestration of V (D) J recombination. Nature Reviews Immunology. 11 (4), 251-263 (2011).
- Oettinger, M. A., Schatz, D. G., Gorka, C., Baltimore, D. RAG-1 and RAG-2, adjacent genes that synergistically activate V (D) J recombination. Science. 248 (4962), 1517-1523 (1990).
- Berek, C., Berger, A., Apel, M. Maturation of the immune response in germinal centers. Cell. 67 (6), 1121-1129 (1991).
- Linterman, M. A., et al. Foxp3+ follicular regulatory T cells control the germinal center response. Nature Medicine. 17 (8), 975 (2011).
- Shulman, Z., et al. T follicular helper cell dynamics in germinal centers. Science. 341 (6146), 673-677 (2013).
- Good-Jacobson, K. L., et al. PD-1 regulates germinal center B cell survival and the formation and affinity of long-lived plasma cells. Nature Immunology. 11 (6), 535 (2010).
- Kerfoot, S. M., et al. Germinal center B cell and T follicular helper cell development initiates in the interfollicular zone. Immunity. 34 (6), 947-960 (2011).
- Chaudhuri, J., Alt, F. W. Class-switch recombination: interplay of transcription, DNA deamination and DNA repair. Nature Reviews Immunology. 4 (7), 541-552 (2004).
- Alt, F. W., Zhang, Y., Meng, F. L., Guo, C., Schwer, B. Mechanisms of programmed DNA lesions and genomic instability in the immune system. Cell. 152 (3), 417-429 (2013).
- Xu, Z., Zan, H., Pone, E. J., Mai, T., Casali, P. Immunoglobulin class-switch DNA recombination: induction, targeting and beyond. Nature Reviews Immunology. 12 (7), 517-531 (2012).
- Di Noia, J. M., Neuberger, M. S. Molecular mechanisms of antibody somatic hypermutation. Annual Reviews of Biochemistry. 76, 1-22 (2007).
- Peled, J. U., et al. The biochemistry of somatic hypermutation. Annual Review of Immunology. 26, 481-511 (2008).
- Liu, M., Schatz, D. G. Balancing AID and DNA repair during somatic hypermutation. Trends in Immunology. 30 (4), 173-181 (2009).
- Methot, S., Di Noia, J. Molecular Mechanisms of Somatic Hypermutation and Class Switch Recombination. Advances in Immunology. 133, 37-87 (2017).
- Muramatsu, M., et al. Class switch recombination and hypermutation require activation-induced cytidine deaminase (AID), a potential RNA editing enzyme. Cell. 102 (5), 553-563 (2000).
- Petersen-Mahrt, S. K., Harris, R. S., Neuberger, M. S. AID mutates E. coli suggesting a DNA deamination mechanism for antibody diversification. Nature. 418 (6893), 99 (2002).
- Revy, P., et al. Activation-induced cytidine deaminase (AID) deficiency causes the autosomal recessive form of the Hyper-IgM syndrome (HIGM2). Cell. 102 (5), 565-575 (2000).
- Petersen-Mahrt, S. DNA deamination in immunity. Immunological Reviews. 203 (1), 80-97 (2005).
- Rada, C., Di Noia, J. M., Neuberger, M. S. Mismatch recognition and uracil excision provide complementary paths to both Ig switching and the A/T-focused phase of somatic mutation. Molecular Cell. 16 (2), 163-171 (2004).
- Rada, C., et al. Immunoglobulin isotype switching is inhibited and somatic hypermutation perturbed in UNG-deficient mice. Current Biology. 12 (20), 1748-1755 (2002).
- Schrader, C. E., Vardo, J., Stavnezer, J. Role for mismatch repair proteins Msh2, Mlh1, and Pms2 in immunoglobulin class switching shown by sequence analysis of recombination junctions. The Journal of Experimental Medicine. 195 (3), 367-373 (2002).
- Martin, A., et al. Msh2 ATPase activity is essential for somatic hypermutation at AT basepairs and for efficient class switch recombination. The Journal of Experimental Medicine. 198 (8), 1171-1178 (2003).
- Imai, K., et al. Human uracil-DNA glycosylase deficiency associated with profoundly impaired immunoglobulin class-switch recombination. Nature Immunology. 4 (10), 1023-1028 (2003).
- Masani, S., Han, L., Yu, K. Apurinic/apyrimidinic endonuclease 1 is the essential nuclease during immunoglobulin class switch recombination. Molecular and Cellular Biology. 33 (7), 1468-1473 (2013).
- Guikema, J. E., et al. APE1-and APE2-dependent DNA breaks in immunoglobulin class switch recombination. The Journal of Experimental Medicine. 204 (12), 3017-3026 (2007).
- Schrader, C. E., Guikema, J. E., Wu, X., Stavnezer, J. The roles of APE1, APE2, DNA polymerase β and mismatch repair in creating S region DNA breaks during antibody class switch. Philosophical Transactions of the Royal Society B: Biological Sciences. 364 (1517), 645-652 (2009).
- Roa, S., et al. MSH2/MSH6 complex promotes error-free repair of AID-induced dU: G mispairs as well as error-prone hypermutation of A: T sites. PLoS One. 5 (6), 11182 (2010).
- Delbos, F., Aoufouchi, S., Faili, A., Weill, J. C., Reynaud, C. A. DNA polymerase η is the sole contributor of A/T modifications during immunoglobulin gene hypermutation in the mouse. The Journal of Experimental Medicine. 204 (1), 17-23 (2007).
- Maul, R. W., Gearhart, P. J. AID and somatic hypermutation. Advances in Immunology. 105, 159-191 (2010).
- Shen, H. M., Tanaka, A., Bozek, G., Nicolae, D., Storb, U. Somatic hypermutation and class switch recombination in Msh6-/- Ung-/- double-knockout mice. The Journal of Immunology. 177 (8), 5386-5392 (2006).
- Cheng, H. L., et al. Integrity of the AID serine-38 phosphorylation site is critical for class switch recombination and somatic hypermutation in mice. Proceedings of the National Academy of Sciences. 106 (8), 2717-2722 (2009).
- Lebecque, S. G., Gearhart, P. J. Boundaries of somatic mutation in rearranged immunoglobulin genes: 5'boundary is near the promoter, and 3'boundary is approximately 1 kb from V (D) J gene. The Journal of Experimental Medicine. 172 (6), 1717-1727 (1990).
- Jolly, C. J., Klix, N., Neuberger, M. S. Rapid methods for the analysis of immunoglobulin gene hypermutation: application to transgenic and gene targeted mice. Nucleic Acids Research. 25 (10), 1913-1919 (1997).
- Choi, J. E., Matthews, A. J., Michel, G., Vuong, B. Q. AID Phosphorylation Regulates Mismatch Repair-Dependent Class Switch Recombination and Affinity Maturation. The Journal of Immunology. 204 (1), 13-22 (2020).
- McBride, K. M., et al. Regulation of class switch recombination and somatic mutation by AID phosphorylation. The Journal of Experimental Medicine. 205 (11), 2585-2594 (2008).
- Liu, M., et al. Two levels of protection for the B cell genome during somatic hypermutation. Nature. 451 (7180), 841-845 (2008).
- Ross, M., Birbeck, M., Wills, V., Forrester, J., Davis, A. Peanut lectin binding properties of germinal centers of mouse lymphoid tissues. Nature. 284, 364-366 (1980).
- Zhang, J., MacLennan, I. C., Liu, Y. J., Lane, P. J. Is rapid proliferation in B centroblasts linked to somatic mutation in memory B cell clones. Immunology Letters. 18 (4), 297-299 (1988).
- Nieuwenhuis, P., Opstelten, D. Functional anatomy of germinal centers. American Journal of Anatomy. 170 (3), 421-435 (1984).
- Lau, A. W., Brink, R. Selection in the germinal center. Current Opinion in Immunology. 63, 29-34 (2020).
- Victora, G. D., Nussenzweig, M. C. Germinal centers. Annual Review of Immunology. 30, 429-457 (2012).
- Mesin, L., Ersching, J., Victora, G. D. Germinal center B cell dynamics. Immunity. 45 (3), 471-482 (2016).
- Reichert, R. A., Gallatin, W. M., Weissman, I. L., Butcher, E. C. Germinal center B cells lack homing receptors necessary for normal lymphocyte recirculation. The Journal of Experimental Medicine. 157 (3), 813-827 (1983).
- Rose, M., Birbeck, M., Wills, V., Forrester, J., Davis, A. Peanut lectin binding properties of germinal centers of mouse lymphoid tissues. Nature. 284, 364-366 (1980).
- Hamada, S., Fujita, S. DAPI staining improved for quantitative cytofluorometry. Histochemistry. 79 (2), 219-226 (1983).
- Otto, F. DAPI staining of fixed cells for high-resolution flow cytometry of nuclear DNA. Methods in Cell Biology. 33, 105-110 (1990).
- Butcher, E., et al. Surface phenotype of Peyer's patch germinal center cells: implications for the role of germinal centers in B cell differentiation. The Journal of Immunology. 129 (6), 2698-2707 (1982).
- Rogerson, B. J., Harris, D. P., Swain, S. L., Burgess, D. O. Germinal center B cells in Peyer's patches of aged mice exhibit a normal activation phenotype and highly mutated IgM genes. Mechanisms of Ageing and Development. 124 (2), 155-165 (2003).
- Potapov, V., Ong, J. L. Examining sources of error in PCR by single-molecule sequencing. PloS One. 12 (1), 0169774 (2017).
- Gonzalez-Fernandez, A., Milstein, C. Analysis of somatic hypermutation in mouse Peyer's patches using immunoglobulin kappa light-chain transgenes. Proceedings of the National Academy of Sciences. 90 (21), 9862-9866 (1993).
- Reboldi, A., Cyster, J. G. Peyer's patches: organizing B-cell responses at the intestinal frontier. Immunological Reviews. 271 (1), 230-245 (2016).
- Betz, A. G., Rada, C., Pannell, R., Milstein, C., Neuberger, M. S. Passenger transgenes reveal intrinsic specificity of the antibody hypermutation mechanism: clustering, polarity, and specific hot spots. Proceedings of the National Academy of Sciences. 90 (6), 2385-2388 (1993).
- Rada, C., Gupta, S. K., Gherardi, E., Milstein, C. Mutation and selection during the secondary response to 2-phenyloxazolone. Proceedings of the National Academy of Sciences. 88 (13), 5508-5512 (1991).
- Heise, N., Klein, U. Somatic Hypermutation and Affinity Maturation Analysis Using the 4-Hydroxy-3-Nitrophenyl-Acetyl (NP) System. Methods in Molecular Biology. 1623, 191-208 (2017).
- Smith, F., Cumano, A., Licht, A., Pecht, I., Rajewsky, K. Low affinity of kappa chain bearing (4-hydroxy-3-nitrophenyl) acetyl (NP)-specific antibodies in the primary antibody repertoire of C57BL/6 mice may explain lambda chain dominance in primary anti-NP responses. Molecular Immunology. 22 (10), 1209-1216 (1985).
- Takahashi, Y., Dutta, P. R., Cerasoli, D. M., Kelsoe, G. In situ studies of the primary immune response to (4-hydroxy-3-nitrophenyl) acetyl. V. Affinity maturation develops in two stages of clonal selection. The Journal of Experimental Medicine. 187 (6), 885-895 (1998).
- Allen, D., Simon, T., Sablitzky, F., Rajewsky, K., Cumano, A. Antibody engineering for the analysis of affinity maturation of an anti-hapten response. The EMBO Journal. 7 (7), 1995-2001 (1988).
- Cumano, A., Rajewsky, K. Clonal recruitment and somatic mutation in the generation of immunological memory to the hapten NP. The EMBO Journal. 5 (10), 2459-2468 (1986).
- Smith, K., Nossal, G., Tarlinton, D. M. FAS is highly expressed in the germinal center but is not required for regulation of the B-cell response to antigen. Proceedings of the National Academy of Sciences. 92 (25), 11628-11632 (1995).
- Hao, Z., et al. Fas receptor expression in germinal-center B cells is essential for T and B lymphocyte homeostasis. Immunity. 29 (4), 615-627 (2008).
- Cervenak, L., Magyar, A., Boja, R., László, G. Differential expression of GL7 activation antigen on bone marrow B cell subpopulations and peripheral B cells. Immunology Letters. 78 (2), 89-96 (2001).
- Naito, Y., et al. Germinal center marker GL7 probes activation-dependent repression of N-glycolylneuraminic acid, a sialic acid species involved in the negative modulation of B-cell activation. Molecular and Cellular Biology. 27 (8), 3008-3022 (2007).
- Olson, W. J., et al. Orphan Nuclear Receptor NR2F6 Suppresses T Follicular Helper Cell Accumulation through Regulation of IL-21. Cell Reports. 28 (11), 2878-2891 (2019).
- Dorsett, Y., et al. MicroRNA-155 suppresses activation-induced cytidine deaminase-mediated Myc-Igh translocation. Immunity. 28 (5), 630-638 (2008).
- Goetz, C., Hammerbeck, C., Bonnevier, J. . Flow Cytometry Basics for the Non-Expert. , (2018).
- Hawley, T. S., Herbert, D. J., Eaker, S. S., Hawley, R. G. . Flow Cytometry Protocols. , (2004).
- Costa, E., et al. A new automated flow cytometry data analysis approach for the diagnostic screening of neoplastic B-cell disorders in peripheral blood samples with absolute lymphocytosis. Leukemia. 20 (7), 1221-1230 (2006).
- McKinnon, K. M. Flow cytometry: An overview. Current Protocols in Immunology. 120 (1), 1-11 (2018).
- McKinnon, K. M. Multiparameter Conventional Flow Cytometry. Methods in Molecular Biology. , 139-150 (2018).
- Lucchesi, S., et al. Computational Analysis of Multiparametric Flow Cytometric Data to Dissect B Cell Subsets in Vaccine Studies. Cytometry Part A. 97, 259-267 (2019).
- Longerich, S., Tanaka, A., Bozek, G., Nicolae, D., Storb, U. The very 5' end and the constant region of Ig genes are spared from somatic mutation because AID does not access these regions. The Journal of Experimental Medicine. 202 (10), 1443-1454 (2005).
- Retter, I., et al. Sequence and characterization of the Ig heavy chain constant and partial variable region of the mouse strain 129S1. The Journal of Immunology. 179 (4), 2419-2427 (2007).
- Shen, H. M., Peters, A., Baron, B., Zhu, X., Storb, U. Mutation of BCL-6 gene in normal B cells by the process of somatic hypermutation of Ig genes. Science. 280 (5370), 1750-1752 (1998).
- Richter, K., et al. Altered pattern of immunoglobulin hypermutation in mice deficient in Slip-GC protein. Journal of Biological Chemistry. 287 (38), 31856-31865 (2012).
Tags
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved