Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Immunology and Infection
ניתוח של היפרמוטציה סומטית באינטרון JH4 של תאי מרכז נגרינל B מן המדבקות של עכבר פייר
מוצג כאן הוא מבחנה לכמת היפרמוטציה סומטית בתוך לוקוז גנים שרשרת כבד אימונוגלובולין באמצעות תאי מרכז B נביטה מן המדבקות של העכבר פייר.
בתוך המרכזים הנבטיים של איברי הלימפה, תאי B בוגרים משנים את האימונוגלובולין המובע שלהם (Ig) על ידי החדרת מוטציות לא מופצות לתוך האקסונים המשתנים של איג כבד ושרשרת אור גן loci. תהליך זה של היפרמוטציה סומטית (SHM) דורש דימינאז ציטידין הנגרמת על ידי הפעלת אנזים (AID), הממיר deoxycytidines (C), לתוך deoxyuridines (U). עיבוד אי-התאמות U:G שנוצרו על-ידי איידס למוטציות על-ידי נתיבי תיקון כריתה ואי-התאמה בסיסיים מציג רצפי קידוד איג חדשים שעשויים לייצר איג זיקה גבוהה יותר. מוטציות בגנים לתיקון איידס או דנ"א יכולות לחסום או לשנות באופן משמעותי את סוגי המוטציות שנצפו ב- Ig loci. אנו מתארים פרוטוקול לכימות מוטציות אינטרון JH4 המשתמשת מיון תאים המופעלים פלואורסצנטיות (FACS), PCR, ו רצף סנגר. למרות שבדיקת זיקה זו אינה מודדת ישירות את התבגרות הזיקה של Ig, היא מעידה על מוטציות ברצפי קידוד משתנים של Ig. בנוסף, שיטות אלה משתמשות בטכניקות ביולוגיה מולקולרית נפוצות המנתחות מוטציות ברצפי Ig של שיבוטים מרובים של תאי B. לפיכך, מבחנה זו היא כלי רב ערך בחקר גיוון SHM ו- Ig.
תאי B, חברי מערכת החיסון האדפטיבית, מזהים ומבטלים אנטיגנים על ידי ייצור נוגדנים, הידועים גם בשם אימונוגלובולין (Ig). כל Ig מורכב משני כבד (IgH) ושני פוליפפטידים שרשרת אור (IgL), אשר מוחזקים יחד על ידי קשרים דיסולפידים כדי ליצור את מבנה הצורה האופייני "Y" של Ig1. N-termini של IgH ו- IgL מהווים את האזור המשתנה (V) של כל פוליפפטיד ויחד הם יוצרים את האתר מחייב אנטיגן של Ig, ואילו האזור הקבוע של IgH מקנה את פונקציית המשפיע של Ig. פיתוח תאי B במח העצם לסדר מחדש את exons קידוד V של IgH ו IgL בתהליך המכונה V(D)J רקומביניזציה2,3,4. שעתוק של exons V recombined, יחד עם exons אזור קבוע בהתאמה, יוצר את mRNA המתורגם Ig.
תאי B בוגרים המבטאים איג הקשור לקרום, הידוע גם בשם קולטן תא B (BCR), מסתובבים לאיברים לימפואידיים משניים, כגון הטחול, בלוטות הלימפה או המדבקות של פייר, שם הם סוקרים את הסביבה עבור אנטיגנים ומתקשרים עם תאים אחרים של המערכת החיסונית1. בתוך המרכזים הנבטיים (GC) של איברי הלימפה המשניים, תאי B המזהים אנטיגן באמצעות BCR הופכים מופעלים. בעזרת תאים דנדריטיים זקיקיים ותאי T עוזר זקיקיים, תאי B מופעלים יכולים להתרבות ולהבדיל לתאי פלזמה וזיכרון, שהם משפיעים חשובים שלתגובה חיסוניתחזקה 5,6,7,8,9. בנוסף, תאי B מופעלים אלה יכולים לעבור תהליכי גיוון משניים של גנים מסוג Ig - רקומבינציה של מתג מחלקה (CSR) והיפרמוטציה סומטית (SHM). במהלך CSR, תאי B מחליפים את האזור הקבוע μ המוגדר כברירת מחדל בפוליפפטיד IgH עם אזור קבוע אחר (γ, α, ε) באמצעות תגובת מחיקה-רקומבינציה של DNA (איור 1). זה מאפשר ביטוי של אקסון קבוע שונה ותרגום של Ig חדש. התא B יעבור מהבעת IgM לאיזוטיפ אחר (IgG, IgA, IgE). CSR משנה את פונקציית האפקט של Ig מבלי לשנות את הספציפיות האנטיגן שלה10,11,12. עם זאת, במהלך SHM, תאי B משנים את אזורי הקידוד V של IgH ו- IgL כדי לאפשר ייצור ובחירה של Igs זיקה גבוהה יותר, אשר יכול לחסל ביעילות רבה יותר אנטיגן13,14,15 ( איור1). חשוב לציין, הן CSR והן SHM תלויים בתפקוד של אנזים אחד: deaminase ציטידין הנגרמת על ידי הפעלה (AID)16,17,18. בני אדם ועכברים לקויים ב- AID לא יכולים להשלים CSR או SHM ולהציג עם titers סרום IgM מוגבה או Hyper-IgM17,19.
ב- CSR, AID deaminates deoxycytidines (C) באזורי המתג החוזרים על עצמם הקודמים לכל אקסונים מקודדים קבועים, ממירים אותם לדיאוקסיורידינים (U)20,21, מה שיוצר זיווג בסיס לא תואם בין deoxyuridines ו deoxyguanosines (U:G). אשר נדרשים עבור שילוב מחדש של ה- DNA, על ידי תיקון כריתת הבסיס (BER) או תיקון אי התאמה (MMR) מסלול22,23,24,25,26,27,28,29. ב SHM, סיוע deaminates C בתוך exons קידוד V. שכפול על פני חוסר התאמה U:G מייצר מוטציות מעבר C:G כדי T:A, ואילו הסרת בסיס uracil על ידי חלבון BER, uracil DNA גליקוסילאז (UNG), לפני שכפול DNA מייצרת מוטציות מעבר והן טרנספרציה16. מוטציות ריקות ב- UNG מגדילות באופן משמעותי את מוטציות המעבר C:G ל- T:A21,22. בדומה ל- CSR, SHM דורש את התפקידים המשלימים של MMR ו- BER. במהלך SHM, MMR יוצר מוטציות בזוגות בסיס A:T. השבתת מוטציות ב- MutS homology 2 (MSH2) או η פולימראז DNA (Polη) מפחיתה באופן משמעותי מוטציות בבסיסי A:T ומוטציות מורכבות ב- MSH2 ופולהו מבטלת למעשה מוטציות בבסיסי A:T21,30,31. בהתאם לתפקיד הקריטי עבור BER ו- MMR בהמרת U שנוצר על-ידי AID למוטציות מעבר או טרנזיום, עכברים לקויים הן עבור MSH2 והן עבור UNG (MSH2-/-UNG-/-) מציגים רק את C:G ל- T:A מוטציות מעבר הנובעות משכפול ברחבי U:G אי התאמה21.
הניתוח של SHM באזורי קידוד V נשאר מסובך מכיוון שפיתוח תאי B יכול לשלב מחדש כל אחד מאקסוני הקידוד V(D)J ב- IgH ו- IgL loci1,2,4. ניתוח מדויק של אזורי V אלה שעברו שילוב מחדש באופן ייחודי ומשותם באופן סומטי דורש זיהוי ובידוד של שיבוטים של תאי B או של Ig mRNA11,13. אינטרון JH4, שהוא 3 ' של האקסון האחרון J קידוד ב לוקוס IgH, מטפח מוטציות סומטיות עקב התפשטות מוטציות 3 ' של מקדם V32,33,34 ולכן משמש לעתים קרובות כסמן פונדקאי עבור SHM באזורים V31,35 ( איור1). כדי להבהיר באופן ניסיוני כיצד גנים ספציפיים או מוטציות גנטיות לשנות דפוסים או שיעורים SHM, intron JH4 ניתן לרצף מן טלאים של פייר (PP) תאי מרכז נביטה B (GCBCs), אשר עוברים שיעורים גבוהים של SHM36,37,38. GCBCs ניתן לזהות בקלות ומבודד עם נוגדנים מצומדים פלואורסצנטי נגד סמני משטח התא (B220+PNAHI)17,39.
פרוטוקול מפורט מוצג כדי לאפיין מוטציות אינטרון JH4 ב- PP GCBCs מעכברים באמצעות שילוב של FACS (מיון תאים המופעל על ידי פלואורסצנטיות), PCR, רצף סנגר (איור 2).
כל העכברים המוטנטים נשמרו על רקע C57BL/6. עכברים זכריים ונקביים תואמי גיל (2-5 חודשים) שימשו לכל הניסויים. גידול וניסויים בעכברים נערכו על פי פרוטוקולים שאושרו על ידי ועדת הטיפול והשימוש בבעלי חיים של סיטי קולג' בניו יורק.
1. ניתוח של המדבקות של פייר
- המתת חסד לעכבר עם 100% CO2 ב 3 L / min במשך 5 דקות ואחריו נקע בצוואר הרחם כדי לאשר את המוות. לעקר כלי ניתוח (מספריים, מלקחיים, מלקחיים עדינים) וכפפות ידיים עם 70% אתנול.
- הניחו את העכבר על משטח הניתוח כאשר הבטן חשופה. בנדיבות לרסס את הגוף של העכבר עם 70% אתנול לפני ביצוע חתכים כדי לעקר את אזור הניתוח.
- בצע חתך לתוך העור על פני הבטן ולהסיר את העור מהבטן על ידי משיכת בו זמנית משני צידי החתך לכיוון הראש והזנב באמצעות מלקחיים (או מעוקר, ידיים כפפה).
- הצמד את הגפיים המבהילות והיעכבות של העכבר.
- חותכים את חלל הצפק עם מספריים כדי לחשוף את האיברים הפנימיים.
- אתר את המעי הדק בין הקיבה לבין caecum ("J" מבנה בצורת ליד המעי הגס). הסר את המעי הדק על ידי חיתוך מתחת לקיבה ומעל caecum.
- הסר כל רקמת חיבור ושומן המקשרים את קפלי המעי הדק יחד.
הערה: שומן יהיה צבע לבן ייחודי, בניגוד לצבע הוורוד של המעי הדק. - בדוק את המשטח החיצוני של המעי הדק עבור כתמי Peyer (PPs), שהם קטנים (~ 1 מ"מ), מבנים בצורת אליפסה המופיעים לבנים מתחת לשכבה דקה של תאי אפיתל שקופים.
- בזהירות excise כל PP גלוי עם מספריים.
הערה: עכבר C57BL/6 מסוג פראי אחד (WT) יכול להניב 4-8 PPs, ואילו עכבר AID-/- יהיה 6-10 PPs. - לאסוף את PPs לתוך צינור מיקרוצנטריפוגה 1.5 מ"ל המכיל 1 מ"ל של חיץ FACS על הקרח.
הערה: PP צריך לשקוע, ואילו שומן יצוף על פני השטח וניתן להסירו.
2. בידוד תאים עבור FACS
- מניחים מסנן 40 מיקרומטר בצלחת 6 באר עם 1 מ"ל של קר (4 מעלות צלזיוס) מאגר FACS.
- יוצקים את PPs מצינור 1.5 מ"ל על המסנן.
- לשטוף PPs עם 1 מ"ל של מאגר FACS קר, לוודא כי הם תמיד בנוזל על הקרח.
- השתמש בקצה השטוח של הוכנה ממזרק 1 מ"ל כמו עלה כדי למחוץ את PPs על המסנן עד רקמת חיבור בלבד נשאר על המסנן.
- לשטוף את המסנן ואת הוכנה עם 1 מ"ל של מאגר FACS קר לשחרר את התאים לתוך צלחת 6 גם.
- לאסוף את ~ 4 מ"ל של תאים במאגר FACS קר ולסנן אותם דרך צינור 40 μm מסננת כובע FACS.
- לשטוף את מכסה מסננת עם 1 מ"ל של מאגר FACS קר.
- גלולה התאים ב 600 x g ב 4 מעלות צלזיוס במשך 5 דקות בצנטריפוגה דלי מתנדנד.
- תכריז על העל-טבעי.
- התעבשים מחדש את התאים ב- 0.4 מ"ל של מאגר FACS קר.
- הסר 10 μL כדי שספירת תאים תאים תאים תוודא את התפוקה (צפו ~ 5 x 106 תאים/עכבר, ראו איור 3A)
- סנן את התאים הנותרים באמצעות מכסה מסננת של 40 מיקרומטר לתוך צינור FACS והמשך להכתים עבור FACS.
3. מכתים GCBCs עבור FACS
- הוסף בלוק Fc μL 1 (ללא תווית נגד עכבר CD16/CD32) להשעיית תא 400 μL ומניחים את התאים על קרח במשך 15 דקות.
- הוסף 2 מ"ל של מאגר FACS קר כדי לשטוף את התאים.
- כדורי תאים ב 600 x g ב 4 מעלות צלזיוס במשך 5 דקות ולהשליך את supernatant.
- התעבשים מחדש את התאים ב- 80 μL של מאגר FACS קר.
- הסר 10 μL של תאים מן WT PP עבור כל פקד כתמים (4 בסך הכל, כולל 3 פקדי כתם יחיד 1 שליטה מוכתמת). השאירו 40 μL של WT PP לשלב הבא. לחלופין, השתמש בקרוזי פיצוי עבור פקדי הכתמים.
- הכתים כל אחת מהדגימות הניסיוניות (למשל, WT ו- AID-/-) ב-500 μL של מאגר FACS קר עם 2.5 μL של אגלוטינין בוטנים (PNA) -ביוטין במשך 15 דקות על קרח.
- הוסף 2 מ"ל של מאגר FACS קר כדי לשטוף את התאים.
- כדורי תאים ב 600 x g ב 4 מעלות צלזיוס במשך 5 דקות ולהשליך את supernatant.
- הכתים כל דגימה ניסיונית עם 500 μL של הקוקטייל בחושך, על הקרח, במשך 15 דקות (שולחן 1). ודאו שהתאים מחוברים במלואם לקוקטייל הכתים.
- הכן פקדי כתם בודדים עבור מטריצת הפיצוי.
- הכתים את התאים ב 500 μL של מאגר FACS קר באמצעות דילול שצוין בטבלה 2.
- דגירה פקדי הכתמים בחושך, על הקרח, במשך 15 דקות.
- הוסף 2 מ"ל מאגר FACS קר לכל הצינורות בשלבים 3.7 ו 3.8, גלולה התאים, ולהשליך את supernatant לשטוף נוגדנים מאוגדים או DAPI.
- מניחים מחדש את התאים ב 500 μL של חיץ FACS קר ומניחים על קרח.
- באמצעות סדרן תאים, לאסוף B220+PNAHI מכל מדגם ניסיוני מוכתם. איור 3B מציג את האחוזים האופייניים של B220+ PNAHI המתקבלים מ- WT ו- AID-/- PPs. איור 3C מציג את אסטרטגיית הגירן של FACS.
4. מיצוי DNA מ- GCBCs
- גלולה ממוינת תאים ב 600 x g ב 4 מעלות צלזיוס במשך 5 דקות ולהשליך את supernatant.
- השהה מחדש את התאים ב- 1 מ"ל של מאגר FACS קר והעבר את התאים לצינור מיקרוצנטריפוגה של 1.5 מ"ל.
- גלולה התאים ב 600 x g ב 4 מעלות צלזיוס במשך 5 דקות ולהשליך את supernatant.
- resuspend התאים ב 500 μL של מאגר מיצוי DNA ו 5 μL של 20 מ"ג / מ"ל Proteinase K.
- דגירה ב 56 מעלות צלזיוס לילה.
- לזרז DNA עם 500 μL איזופרופנול ו 1 μL של 20 מ"ג / מ"ל גליקוגן. מערבבים את הצינור ביסודיות על ידי היפוך 5-6x.
- דגירה בטמפרטורת החדר במשך 10 דקות.
- צנטריפוגה במיקרוצנטריפוגה למשך 15 דקות ב-25 מעלות צלזיוס ב-21,000 x גרם.
- להשליך את supernatant ולשמור את גלולה, אשר מכיל את ה-DNA מזרז וגליקוגן.
- לשטוף את גלולת ה-DNA עם 1 מ"ל של 70% אתנול.
- גלולה ה-DNA במיקרוצנטריפוגה במשך 10 דקות ב 25 מעלות צלזיוס ב 21,000 x גרם.
- הסר את 70% אתנול ואוויר לייבש את גלולת ה-DNA במשך 5-10 דקות.
הערה: הימנע ייבוש יתר כמו ה-DNA לא יכול rehydrate לחלוטין.
- התחדשו בדנ"א במאגר TE של 30 μL ותדגרו במשך הלילה ב-56 מעלות צלזיוס.
5. הגברה וניתוח של רצף אינטרון JH4
- לכמת דנ"א על ידי מדידת הספיגה באורך גל של 260 ננומטר (A260).
הערה: הריכוז האופייני של DNA התאושש B220ממוין +PNAHI GCBCs של עכבר C57BL/6 הוא 20-40 ng/μL. - בצע את ה- PCR המקונן עבור intron JH4 (טבלה 3, טבלה 4). לנרמל את הכמות הכוללת של DNA גנומי בשימוש PCR הראשון לדגימה מרוכזת לפחות. (למשל, אם המדגם הכי פחות מרוכז הוא 5 ng/μL, השתמש 58.75 ng של DNA עבור כל הדגימות בנפח המרבי של מים (11.75 μL) ב PCR #1).
- פתור את מוצר PCR על ג'ל agarose 1.5% ב 200 V במשך 20 דקות. גודל האמפליקון הצפוי הוא 580 bp.
- מוציאים את האמפליקון מהג'ל ומוציאים את הדנ"א באמצעות ערכת מיצוי ג'ל בהתאם להוראות היצרן (ראו איור משלים 1).
- לטבול את ה-DNA עם 30 μL של מים לכמת את כמות ה-DNA על ידי מדידת A260.
הערה: הריכוז האופייני של מוצר PCR מטוהר הוא 3-10 ng/μL.
- לטבול את ה-DNA עם 30 μL של מים לכמת את כמות ה-DNA על ידי מדידת A260.
- תכניס את מוצר ה-PCR המטוהר לפלסמיד עם קצוות קהים. תקנן את הכמות הכוללת של מוצר PCR המשמש בכל תגובת קשירה (טבלה 5).
- דגירה תגובת קשירה בטמפרטורת החדר במשך 5 דקות או לילה ב 16 מעלות צלזיוס.
- להפוך תאים חיידקיים אלקטרו-תחרותיים עם 2 μL של תגובת הקשירה.
- אלקטרופורט ב-1.65 קילו-ואט.
- הצלה ב 600 μL של מדיה SOC עבור 1 שעה ב 37 °C (69 °F) באינקובטור רועד ב 225 סל"ד.
- צלחת 100 μL של חיידקים שהשתנו על LB בתוספת אמפילין (100 מיקרוגרם / מ"ל) צלחות אגר דגירה לילה ב 37 °C (69 °F).
- שלח את הצלחת של מושבות חיידקים לריצוף סנגר באמצעות פריימר T7 קדימה. לחלופין, לגדל תרבויות לילה של כל מושבת חיידקים ולבצע טיהור פלסמיד.
- במידת הצורך, חזור על PCR, קשירה, ו /או טרנספורמציה כדי לייעל את התשואה של מושבות חיידקים
הערה: יש לקטוף לפחות 30 מושבות מכל צלחת.
- במידת הצורך, חזור על PCR, קשירה, ו /או טרנספורמציה כדי לייעל את התשואה של מושבות חיידקים
- סטנדרטיזציה של נתוני הרצף בקבצי .txt
- מחק את רצף הפלסמיד.
- ודא שכל רצף מכוון בין 5' ל- 3' בהתאם לרצף ההפניות לאינטרון JH4 (NG_005838). צור את המשלים ההפוך של כל רצף, לפי הצורך.
- יישר את הרצפים המתקבלים עבור כל PCR מול רצף ההפניות לאנתרון JH4 (NG_005838) באמצעות תוכנת אומגה קלוסטלית (איור 4A).
- זיהוי הבדלים מרצף ההפניות כמוטציות
- ודא שכל המוטציות הן מוטציות נקודתיות אמיתיות על-ידי בחינת האלקטרופרוגרמה של רצף הסנגר. יש לחזור על הרצף במידת הצורך. (איור4ב', ג).
- יש לחשב ולכמת מוטציות ייחודיות באינטורן JH4 עבור כל גנוטיפ (איור 5).
- ספירת רצפים עם מוטציות זהות רק פעם אחת
הערה: לא ניתן לקבוע אם הרצפים הזהים נוצרו במהלך PCR או אירועי SHM זהים בתאי B שונים. - ספור כל מופע של רצפי אינטרון WT germline JH4 (כלומר, אלה ללא מוטציות) כרצף ייחודי.
- ספירת רצפים עם מוטציות זהות רק פעם אחת
ציטומטריית זרימה
תאי B בוגרים מסתובבים במרכזים נביטיים שבהם הם עוברים התבגרות זיקה, התרחבות שיבוט, ובידול לתאי פלזמה או זיכרון40,41,42,43,44. GCBCs אלה יכולים להיות מזוהים על ידי סמני משטח תאים רבים, כולל ביטוי גבוה של קולטן CD45R/B220 ו מחייב של אגלוטינין בוטנים (PNA)45,46. כדי לבודד GCBCs מופעל, תאי PP היו מוכתמים בנוגדנים נגד B220 הקשורים לפיקוריתרין (PE) וביוטינילציה-PNA, ואחריו סטרפטבידין מצומד ל- APC-eFluor780. תאים מתים בוטלו באמצעות פלואורסצנט 4',6-Diamidino-2-פנילינדול (DAPI) צבע, אשר מכתים את חומצת הגרעין של תאים גוססים או מתים47,48. התאים המוכתמים נותחו ומוינו לאחר מכן באמצעות ציטומטריית זרימה. PPs כלל ~ 80% B220+ תאים49,50. עמודי WT מכילים בממוצע 4 x 106 תאים לעכבר (איור 3A). כ-8% מתאי WT PP היו B220+PNAHI, שהוא מחצית מהמספר שנצפה ב-AID-/ - ( איור3B). לכן, 0.3-0.6 x 106 B220+PNAHI GCBCs הושגו לאחר מיון, אשר היו מספיקים כדי לנתח מוטציות intron JH4.
ניתוח רצף JH4
אינטרון JH4 הוגבר על ידי PCR מקונן באמצעות פריימרים משפחתיים נפוצים VHJ558 (J558FR3Fw ו- VHJ558.2) ואחריו JH4 intron פורש פריימרים VHJ558.3 ו VHJ558.435,37. מתוך 105 הרצפים הייחודיים שהתקבלו מ-WT GCBCs, נמצאו בסך הכל 226 מוטציות (איור 5A). ניתוח ספקטרום המוטציות של GCBC בעכברי WT הראה מגוון של מעברים והתמרות בקצב של 4 x 10-3 מוטציות / bp, אשר חושב על ידי חלוקת המספר הכולל של בסיסים שעברו מוטציה על ידי המספר הכולל של בסיסים שהיו ברצף32,36,37,38. בנוסף, כל מוצר JH4 PCR מ- WT GCBCs הכיל 1-25 מוטציות (איור 5B), שבהן מוטציות מרובות נמצאו לעתים קרובות ברצף אחד33,36. רק שתי מוטציות זוהו ב-113 רצפי AID-/-( איור 5A). AID-/- תאי B הציגו 1.66 x10 -5 מוטציות /bp, שהיה נמוך משמעותית מתאי WT B (p <0.05)36 ומשווה לשיעור השגיאה של פולימראז נאמנות גבוהה (5.3 x 10-7 sub /base/הכפלה)51,52. לכן, תאי AID-/- B שימשו כבקרה שלילית שימושית לבדיקה זו.
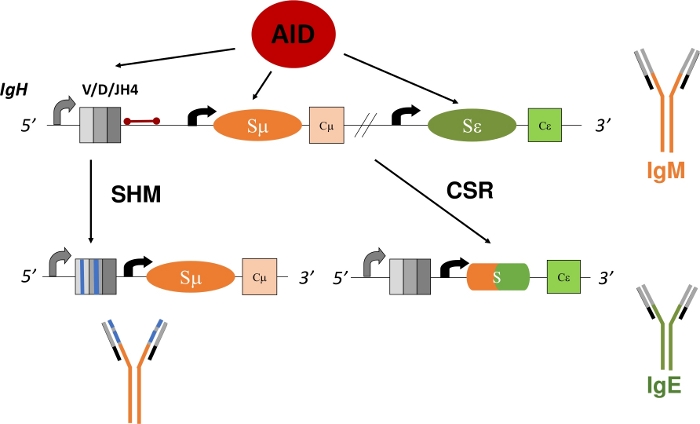
איור 1: סכמטי של לוקוס הגן IgH והאזורים הממוקדים על ידי סיוע במהלך CSR ו- SHM. הסרגל האדום מציין את 580 bp JH4 intron כי הוא 3 ' של סידורים מחדש VDJH4 והוא מנותח בפרוטוקול זה. ב- CSR, deamination תלויי איידס של אזורי מתג פנים (Sμ ו- Sε) מקדם היווצרות DSB המאפשרת מחיקה-רקומבינציה וביטוי של איזוטיפ נוגדן חדש (IgM ל- IgE). במהלך SHM, אזורי V (קופסאות אפורות) לצבור מוטציות (קווים כחולים) שעלולים להוביל Ig זיקה גבוהה יותר. לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
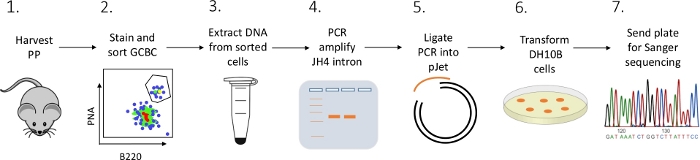
איור 2: זרימת עבודה לניתוח SHM של intron JH4 ב- GCBCs מבודד ממחשבים אישיים. לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
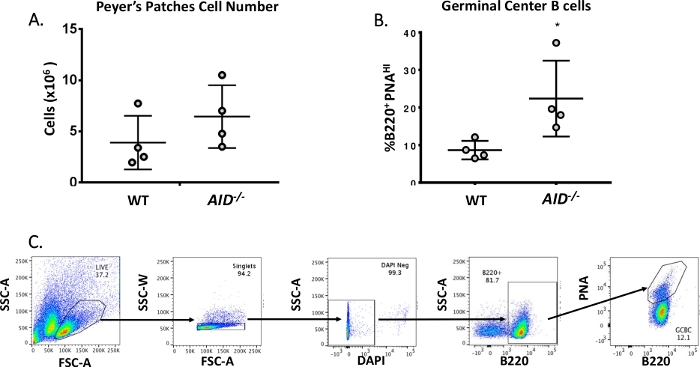
איור 3: אפיון של PP GCBCs. (A) המספר הכולל של תאי PP מעכברי WT ו- AID-/- (n = 4 לכל גנוטיפ). קווי שגיאה מייצגים סטיית תקן מהתו הממוצע. (B)אחוז B220+PNAHI GCBCs המתקבלים ממחשבים אישיים של עכברי WT וסיוע-/- (n = 4 לכל גנוטיפ)36. קווי שגיאה מייצגים סטיית תקן מהתו הממוצע* p<0.05 באמצעות מבחן t של התלמיד. (ג)התוויות FACS מייצגות למיון B220+PNAHI GCBCs ממחשבים אישיים.
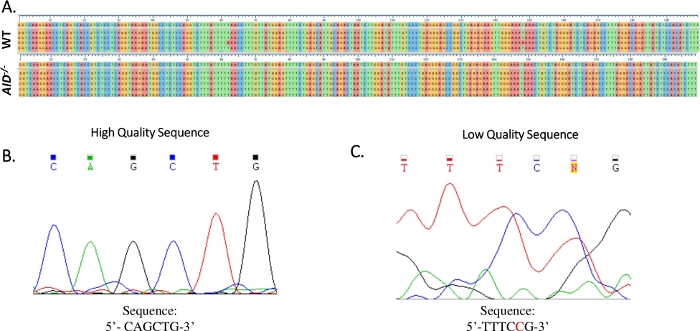
איור 4: ניתוח נתוני רצף JH4 Sanger. (A) יישורי רצף לדוגמה של נתוני רצף Sanger של מוצר JH4 PCR מ- WT (למעלה) ו- AID-/- (למטה) GCBCs לרצף הגנומי של ההפניה (NG_005838), שהוא הרצף ממש מתחת לסימוני השנתות הממוספרים. היישורים נוצרו באמצעות אומגה קלוסטלית. (B) אלקטרופרוגרמה של נתוני רצף סנגר באיכות גבוהה, אשר הציגו פסגות נפרדות עבור כל בסיס. (C)אלקטרופרוגרמה של נתוני רצף באיכות נמוכה, שהראו פסגות מעורפלות ובסיסים לא מוגדרים (N). יש להוסיף ביאור ידני של הנוקלאוטידים המוצגים באדום בקובץ הטקסט של הרצף. לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
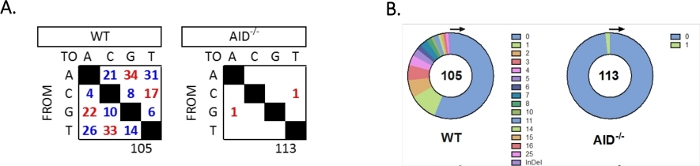
איור 5: ניתוח מוטציות באינרון JH4 ב- WT וב- AID-/- GCBCs. (A) המספר הכולל של מוטציות מעבר (אדום) והעברה (כחול) בבסיסי A, C, G ו- T עבור כל גנוטיפ מסוכם בטבלאות. המספר הכולל של הרצפים שנותחו מצוין מתחת לטבלה. (B) מספר המוטציות לכל אמפליקון PCR עבור כל גנוטיפ מתואר בתרשימי העוגה. נתון זה שונה מ- Choi et al.36 Copyright 2020. האגודה האמריקאית לאימונולוגים בע"מ אנא לחץ כאן כדי להציג גרסה גדולה יותר של נתון זה.
| קוקטייל מכתים עבור GCBCs | נפח: 500 μL | ||
| נוגדן או צבע | פלואורופור | דילול | μL (μL) |
| B220 | Pe | 1000 | 0.5 |
| סטרפטבידין | APC-eFluor780 | 500 | 1 |
| DAPI | מספר N/A | 500 | 1 |
שולחן 1: מכתים קוקטיילים עבור GCBCs. קוקטייל של הנוגדנים המצוינים או צבע (המצוין בכתב נטוי) בדילול שצוין שימשו להכתמת תאי PP ב 500 μL עבור cytometry זרימה.
| כתמים בודדים לפיצוי | נפח: 500 μL | ||
| נוגדן או צבע | פלואורופור | דילול | μL (μL) |
| B220 | Pe | 1000 | 0.5 |
| B220 | APC-eFluor780 | 750 | 0.67 |
| DAPI | מספר N/A | 500 | 1 |
טבלה 2: פקדי כתם יחיד לפיצוי. נוגדני B220 המוטלים על הפלואורופורים המצוינים שימשו לבקרות כתם יחיד כדי לפצות על חפיפה ספקטרלית.
| #1 PCR | ||||
| מגיב | אמצעי אחסון | תנאי התרמוציקלר | ||
| מאגר 5x | 4 μL | 1 | 95 °C (69 °F) | 3 דקות |
| 10 מ"מ dNTP | 2 מיקרומטר | 2 | 94 °C (69 °F) | 30 שניות |
| 10 מיקרומטר J558FR3Fw | μL אחד | 3 | 55 °C (69 °F) | 30 שניות |
| 10 מיקרומטר VHJ558.2 | μL אחד | 4 | 72 °C (69 °F) | 1:30 דק' |
| פולימראז DNA נאמנות גבוהה | 0.25 מיקרו-ל | מחזור 2-4 9x | ||
| דנ א | x (סטנדרטיזציה לדגימה הכי פחות מרוכזת) | |||
| H2O | עד 20 μL | 5 | 72 °C (69 °F) | 5 דקות |
| לדלל את מוצר PCR 1:5 ב H2O לפני שתמשיך PCR #2 | ||||
טבלה 3: PCR מקונן של אינטרון JH4. רכיבי PCR ותנאי תרמוציקלר לתגובת ההגברה הראשונה. לדלל את המוצר PCR הראשון 1:5 עם מים ולהשתמש 1 μL של דילול זה עבור PCR השני.
| #2 PCR | ||||
| מגיב | אמצעי אחסון | תנאי התרמוציקלר #2 | ||
| מאגר 5x | 4 μL | 1 | 94 °C (69 °F) | 3 דקות |
| 10 מ"מ dNTP | 2 מיקרומטר | 2 | 94 °C (69 °F) | 30 שניות |
| 10 מיקרומטר VHJ558.3 | μL אחד | 3 | 55 °C (69 °F) | 30 שניות |
| 10 מיקרומטר VHJ558.4 | μL אחד | 4 | 72 °C (69 °F) | 30 שניות |
| פולימראז DNA נאמנות גבוהה | 0.25 מיקרו-ל | מחזור 2-4 21x | ||
| PCR מדולל #1 | μL אחד | |||
| H2O | עד 20 μL | 5 | 72 °C (69 °F) | 5 דקות |
טבלה 4: רכיבי PCR ותנאי התרמוציקלר עבור PCR השני.
| מגיב | אמצעי אחסון |
| מאגר 2x | 10 μL |
| PCR מטוהר | x (סטנדרטיזציה לדגימה הכי פחות מרוכזת) |
| פלסמיד עם קצוות קהים | μL אחד |
| T4 DNA ליגאז | μL אחד |
| H2O | עד 20 μL |
| דגירה בטמפרטורת החדר במשך 5 דקות או לילה ב 16 מעלות צלזיוס | |
טבלה 5: תגובת קשירה. רכיבים עבור קשירה של מוצר PCR intron JH4 מטוהר לתוך פלסמיד.
| מאגר FACS |
| חום להשבית FBS ב 56 °C (66 °F) למשך שעה אחת לפני השימוש. תוספת PBS, pH 7.4 (Gibco, #10010049) עם 2.5% (v /v) של FBS מומת חום. יש לאחסן ב-4 מעלות צלזיוס. |
| מאגר מיצוי DNA (100 mM Tris pH 8.0, 0.1 M EDTA, 0.5% (w/v) SDS) |
| הוסף 50 מ"ל של 1 M Tris pH 8.0, 100mL של 0.5 M EDTA, ו 12.5 מ"ל של 20% SDS. מוסיפים מים מזוקקים ל-500 מ"ל. יש לאחסן בטמפרטורת החדר. |
| מאגר TE (10 mM Tris pH 8.0, EDTA של 1 מ"מ) |
| הוסף 2.5 מ"ל של 1 M Tris pH 8.0, ו 500 מ"ל של 0.5 M EDTA. מוסיפים מים מזוקקים ל-250 מ"ל. יש לאחסן בטמפרטורת החדר. |
טבלה 6: מתכוני חיץ.
| רשימת אוליגונוקלאוטידים | ||
| J558FR3Fw | 5'-GCCTGACATCTGGACTCTGC-3' | |
| VHJ558.2 | 5'-CTGGACTTTCGGTTTGGTG-3' | |
| VHJ558.3 | 5'-GGTCAAGGAACCTCAGTCA-3' | |
| VHJ558.4 | 5'-TCTCTAGACAGACTAC-3' | |
טבלה 7: אוליגונוקלאוטידים המשמשים במהלך ההסתעפות.
איור משלים 1: תמונת ג'ל אגרוז מייצגת לאחר השלמת שלב 5.4. מוצר PCR מקונן Intron JH4 נפתרה על ג'ל agarose 1.5% ואת 580 bp amplicon נכרת. WT PP מציין כי WT PP GCBC DNA גנומי שימש כתבנית עבור PCR הראשון ו- AID PP מציין כי סיוע-/- PP GCBC DNA גנומי שימש כתבנית עבור PCR הראשון. ɸ מציין את אין פקד PCR תבנית - מציין שום דבר לא נטען לתוך הבאר של ג'ל agarose. הנתיב האחרון מראה סולם דנ"א של 100 bp. אנא לחץ כאן כדי להוריד נתון זה.
אפיון SHM בתוך רצפי קידוד IgH ו- IgL V של אוכלוסיית תא B הטרוגנית מהווה אתגר, בהתחשב בכך שכל תא B ארגן מחדש באופן ייחודי מקטעי קידוד V במהלך V(D)J recombination34. במאמר זה, אנו מתארים שיטה לזיהוי מוטציות באינרון JH4 של GCBCs. אינטרון JH4, אשר ממוקם 3 ' של קטע קידוד J האחרון בוקוס IgH, משמש פונדקאית עבור SHM של אזורי V (איור 1)31,33,34,35. כדי לקטלג מוטציות אינטרון JH4 אלה ולהעריך כיצד גנים ספציפיים משפיעים על הייצור או דפוס של מוטציות, PP GCBCs מנותחים במיוחד. תאים אלה צוברים מוטציות אינטרון JH4 כתוצאה מגירוי כרוני על ידי microbiota מעיים53. יתר על כן, B220+PNAHI GCBCs מן PPs של עכברים לא ממוננים יש ספקטרום מוטציה המשווה GCBCs טחול מבעלי חיים מחוסנים54,55. עם זאת, מוטציות באינרון JH4 לא ניתן לתאם התבגרות איג זיקה כי מוטציות אלה אינן קידוד.
כדי לקבוע אם SHM משנה את זיקה Ig, עכברים צריכים להיות מחוסנים תוך-פירוטונית עם אנטיגן, כגון NP (4-הידרוקסי-3-nitrophenylacetyl) מצומד CGG (עוף גמא גלובולין) או KLH (חור מנעול לימפה hemocyanin)56. לאחר מכן, mRNA ניתן לטהר מן הטחול B220+PNAHI GCBCs לבחון SHM בתוך VH186.2, exon קידוד V כי לעתים קרובות ביותר מזהה NP והוא מוטציה בעקבות NP-CGG או NP-KLHחיסון 31,57,58,59,60. מוטציה של טריפטופן-33 כדי לאוצין ב VH186.2 אופיינה כדי להגדיל את זיקה Ig עד 10-פי59,60 ולכן, אינדיקטור אחד כי SHM ובחירה שיבוט יצרה איג זיקה גבוהה. מדידת NP7- ו NP20 ספציפי סרום Ig titers על ידי ELISA וחישוב יחס Ig ספציפי NP7/NP20 במהלך החיסון גם מתעד Ig זיקה התבגרות הנובעת SHM של V אזורים17,21,36. שני מבחנים אלה יכולים לשמש כדי לתאם SHM בתוך VH186.2 רצפי קידוד עם שינויים IG ספציפי NP זיקה התבגרות.
בין אם בעלי חיים מחוסנים או לא מחוסנים משמשים לניתוח SHM של VH186.2 או intron JH4, GCBCs חייב להיות מזוהה במדויק. אנו מציגים גישה מבוססת FACS לבידוד B220+PNAHI GCBCs. לחלופין, פאס ולא גופרית α2-6-sialyl-LacNAc אנטיגן, אשר מוכר על ידי נוגדן GL761,62,63,64, יכול לשמש גם כדי לבודד GCBCs, אשר מזוהים כמו B220+Fas+GL7+65 או CD19+Fas+GL7+37. ביטוי GL7 משקף מקרוב PNA ב GCBCs מופעל של בלוטות הלימפה64,65,66. בנוסף לשימוש בסמני נוגדנים ספציפיים ל- GCBCs, קוקטיילים מכתימים צריכים למקסם את העירור של פלואורופור וגילוי של סמן ביולוגי תוך מזעור חפיפה ספקטרלית של פליטת פלואורסצנטיות. אנטיגנים לידי ביטוי ברמות נמוכות צריך להיות מזוהה עם נוגדן כי הוא מצומד פלואורופור עם פלואורסצנטיות פליטה חזקה67. פרוטוקול הכתם המומלץ היה מותאם לניתוח על סדרן תאים מצויד בארבעה לייזרים (405nm, 488nm, 561nm, 633nm) ו 12 מסננים; עם זאת, תצורות המסנן וזמינות הלייזר משתנות בין ציטומטרים. כדי לתקן את הפרוטוקול על פי ריאגנט וזמינות ציוד, הקורא מופנה למשאבים נוספים, צופי ספקטרום מקוון וספרות שפורסמה67,68,69,70,71,72,73. פרוטוקול הכתם הרב-צבעי המתואר בזאת דורש פיצוי של חפיפה ספקטרלית כדי להבטיח שאוכלוסיות התאים הממוינות הן GCBCs במקום זיהוי לא מדויק של פליטת פלואורסצנטיות. B220 משמש כבקרת כתמים שימושית עבור FACS המתואר (טבלה 1B) מכיוון שלמחשבים יהיו אוכלוסיות שליליות וחיוביות B220 ייחודיות (איור 3C), המאפשרות פיצוי הולם של חפיפה ספקטרלית. יש להשתמש באסטרטגיית הג'ינג המוצגת באיור 3C כקו מנחה. החלקות cytometry זרימה עשוי להשתנות בהתאם לתנאי הכתמים והגדרות ציטומטר. עם זאת, 4-10% מהתאים החיים צריכים להיות B220+PNAHI 35, 52.
כל המוטציות בתוך intron JH4 של PP GCBCs חייב להיות מאומת כדי להבטיח כי המוטציות שנצפו הם באמת משקף של SHM ולא החפץ של PCR או רצף. AID-/- תאי B יכולים לשמש כפקד שלילי שימושי בעת בדיקת פנוטיפ SHM במודלים אחרים של עכבר מוטנטים מכיוון שתאים אלה אינם יכולים להשלים את SHM17,19. שיעור מוטציית האינטרון JH4 ב- AID-/- GCBCs (1.66x10-5 מוטציות/bp)20,21,36,37,38,50,74 דומה לשיעור השגיאה של פולימראז נאמנות גבוהה (5.3x10-7 sub/base/הכפלה)51,52 המשמש להגברת ה- DNA PCR המקונן. אם עכברי AID-/- אינם זמינים, השווה את דפוס המוטציה הנצפות ואת התדירות לספרות שפורסמה. אזורי Ig V לצבור 10-3-10-4 מוטציות לכל חטיבת זוג בסיס, שהוא כ 106-פי 6גבוה יותר מאשר שיעור המוטציה של לוקוסים גנים אחרים73,75. התוצאות עשויות להשתנות עם גיל החיה76. לחלופין, B220+תאי PNALO, המסמנים שאינם GCBCs, עשויים לשמש כפקד שלילי בהיעדר סיוע-/- עכברים52. אם תדירות המוטציה ב- WT GCBCs נמוכה מהצפוי, ייתכן שהרצף המופנם של נבט WT JH4 מיוצג באופן לא פרופורציונלי. במקרה זה, ודא כי GCBCs היו מוכתמים וממוינים כראוי PCRs חופשיים זיהום נבט WT JH4 intron. בנוסף, יש לנתח ביסודיות נתוני רצף גולמי באלקטרופרוגרמות כדי להבטיח שמוטציות בנתוני הטקסט של הרצף אינן חפצים של שגיאות רצף. לדוגמה, תוצאות רצף סנגר גרועות עשויות להפחית את המהימנות של נתוני הרצף (איור 4). בקרת איכות זו של נתוני רצף סנגר תגדיל את הדיוק והשחזור של ניתוח מוטציית אינטרון JH4.
למחברים אין מה לחשוף.
אנו מודים לטסוקו הונג'ו על הסיוע- / - עכברים. עבודה זו נתמכה על ידי המכון הלאומי על פערי בריאות ובריאות מיעוטים (5G12MD007603), המכון הלאומי לסרטן (2U54CA132378), והמכון הלאומי למדעי הרפואה הכללית (1SC1GM132035-01).
| Name | Company | Catalog Number | Comments |
| 0.2 ml PCR 8-tube FLEX-FREE strip, attached clear flat caps, mixed | USA Scientific | 1402-4708 | |
| Ampicillin sodium salt | Fisher | BP1760-5 | |
| APC-eFluor780 anti-CD45R/B220 | eBioscience | 47-0452-80 | clone RA3-6B2 |
| BD FACSAria II | BD | 643186 | four lasers (405nm, 488nm, 561nm, 633nm) and 12 filters (PacBlue (450/50), AmCyan (502LP; 530/30), SSC (488/10), FITC (502LP; 530/30), PerCP-Cy5.5 (655LP; 695/40), PE (585/15), PE-Texas Red (600LP; 610/20), PE-Cy5 (630LP; 670/14), PE-Cy7 (735LP; 780/60), APC (660/20), Alexa700 (710LP; 730/45), APC-Cy7 (755LP; 780/60)) |
| BD slip tip 1mL syringe | Fisher | 14-823-434 | sterile |
| Biotinylated peanut agglutinin (PNA) | Vector Labs | B-1075-5 | |
| C57BL/6J mice | Jackson Laboratories | 664 | |
| Corning Falcon test tube with cell strainer snap cap | Fisher | 08-771-23 | |
| DAPI (4',6-Diamidino-2-Phenylindole, dihydrochloride) | Fisher | D1306 | 0.5 mg/ml |
| dNTP | NEB | N0447L | 10 mM |
| ElectroMAX DH10B competent cells | Fisher | 18-290-015 | |
| Falcon cell strainer 40mm | Fisher | 08-771-1 | |
| Falcon round-bottom polystyrene tubes (FACS tubes) | Fisher | 14-959-5 | |
| Falcon round-bottom polystyrene tubes (capped) | Fisher | 149591A | |
| Fetal bovine serum | R&D Systems (Atlanta Biologicals) | S11150 | |
| Gibco phosphate buffered saline PBS pH 7.4 | Fisher | 10-010-049 | |
| Glycogen | Sigma | 10901393001 | |
| Lasergene Molecular Biology (MegAlign Pro) | DNA Star | version 15 | |
| PE anti-CD45R/B220 | BD | 553090 | clone RA3-6B2 |
| Proteinase K | Fisher | BP1700-100 | |
| Q5 High-Fidelity DNA Polymerase | NEB | M0491L | |
| QIAquick Gel Extraction Kit | Qiagen | 28706 | |
| Seal-Rite 1.5mL microcentrifuge tubes | USA Scientific | 1615-5500 | |
| Streptavidin APC-eFluor 780 Conjugate | eBioscience | 47-4317-82 | |
| T4 DNA ligase | NEB | M020L | |
| Thermo Scientific CloneJET PCR Cloning Kit | ThermoFisher | FERK1231 | |
| Tissue culture plate 6 well | Fisher | 08-772-1B | sterile |
| Unlabeled anti-mouse CD16/CD32 (Fc block), BD | Fisher | BDB553142 | Clone 2.4G2 |
- Murphy, K., Weaver, C. . Janeyway's Immunobiology. , (2016).
- Alt, F. W., et al. VDJ recombination. Immunology Today. 13 (8), 306-314 (1992).
- Schatz, D. G., Ji, Y. Recombination centres and the orchestration of V (D) J recombination. Nature Reviews Immunology. 11 (4), 251-263 (2011).
- Oettinger, M. A., Schatz, D. G., Gorka, C., Baltimore, D. RAG-1 and RAG-2, adjacent genes that synergistically activate V (D) J recombination. Science. 248 (4962), 1517-1523 (1990).
- Berek, C., Berger, A., Apel, M. Maturation of the immune response in germinal centers. Cell. 67 (6), 1121-1129 (1991).
- Linterman, M. A., et al. Foxp3+ follicular regulatory T cells control the germinal center response. Nature Medicine. 17 (8), 975 (2011).
- Shulman, Z., et al. T follicular helper cell dynamics in germinal centers. Science. 341 (6146), 673-677 (2013).
- Good-Jacobson, K. L., et al. PD-1 regulates germinal center B cell survival and the formation and affinity of long-lived plasma cells. Nature Immunology. 11 (6), 535 (2010).
- Kerfoot, S. M., et al. Germinal center B cell and T follicular helper cell development initiates in the interfollicular zone. Immunity. 34 (6), 947-960 (2011).
- Chaudhuri, J., Alt, F. W. Class-switch recombination: interplay of transcription, DNA deamination and DNA repair. Nature Reviews Immunology. 4 (7), 541-552 (2004).
- Alt, F. W., Zhang, Y., Meng, F. L., Guo, C., Schwer, B. Mechanisms of programmed DNA lesions and genomic instability in the immune system. Cell. 152 (3), 417-429 (2013).
- Xu, Z., Zan, H., Pone, E. J., Mai, T., Casali, P. Immunoglobulin class-switch DNA recombination: induction, targeting and beyond. Nature Reviews Immunology. 12 (7), 517-531 (2012).
- Di Noia, J. M., Neuberger, M. S. Molecular mechanisms of antibody somatic hypermutation. Annual Reviews of Biochemistry. 76, 1-22 (2007).
- Peled, J. U., et al. The biochemistry of somatic hypermutation. Annual Review of Immunology. 26, 481-511 (2008).
- Liu, M., Schatz, D. G. Balancing AID and DNA repair during somatic hypermutation. Trends in Immunology. 30 (4), 173-181 (2009).
- Methot, S., Di Noia, J. Molecular Mechanisms of Somatic Hypermutation and Class Switch Recombination. Advances in Immunology. 133, 37-87 (2017).
- Muramatsu, M., et al. Class switch recombination and hypermutation require activation-induced cytidine deaminase (AID), a potential RNA editing enzyme. Cell. 102 (5), 553-563 (2000).
- Petersen-Mahrt, S. K., Harris, R. S., Neuberger, M. S. AID mutates E. coli suggesting a DNA deamination mechanism for antibody diversification. Nature. 418 (6893), 99 (2002).
- Revy, P., et al. Activation-induced cytidine deaminase (AID) deficiency causes the autosomal recessive form of the Hyper-IgM syndrome (HIGM2). Cell. 102 (5), 565-575 (2000).
- Petersen-Mahrt, S. DNA deamination in immunity. Immunological Reviews. 203 (1), 80-97 (2005).
- Rada, C., Di Noia, J. M., Neuberger, M. S. Mismatch recognition and uracil excision provide complementary paths to both Ig switching and the A/T-focused phase of somatic mutation. Molecular Cell. 16 (2), 163-171 (2004).
- Rada, C., et al. Immunoglobulin isotype switching is inhibited and somatic hypermutation perturbed in UNG-deficient mice. Current Biology. 12 (20), 1748-1755 (2002).
- Schrader, C. E., Vardo, J., Stavnezer, J. Role for mismatch repair proteins Msh2, Mlh1, and Pms2 in immunoglobulin class switching shown by sequence analysis of recombination junctions. The Journal of Experimental Medicine. 195 (3), 367-373 (2002).
- Martin, A., et al. Msh2 ATPase activity is essential for somatic hypermutation at AT basepairs and for efficient class switch recombination. The Journal of Experimental Medicine. 198 (8), 1171-1178 (2003).
- Imai, K., et al. Human uracil-DNA glycosylase deficiency associated with profoundly impaired immunoglobulin class-switch recombination. Nature Immunology. 4 (10), 1023-1028 (2003).
- Masani, S., Han, L., Yu, K. Apurinic/apyrimidinic endonuclease 1 is the essential nuclease during immunoglobulin class switch recombination. Molecular and Cellular Biology. 33 (7), 1468-1473 (2013).
- Guikema, J. E., et al. APE1-and APE2-dependent DNA breaks in immunoglobulin class switch recombination. The Journal of Experimental Medicine. 204 (12), 3017-3026 (2007).
- Schrader, C. E., Guikema, J. E., Wu, X., Stavnezer, J. The roles of APE1, APE2, DNA polymerase β and mismatch repair in creating S region DNA breaks during antibody class switch. Philosophical Transactions of the Royal Society B: Biological Sciences. 364 (1517), 645-652 (2009).
- Roa, S., et al. MSH2/MSH6 complex promotes error-free repair of AID-induced dU: G mispairs as well as error-prone hypermutation of A: T sites. PLoS One. 5 (6), 11182 (2010).
- Delbos, F., Aoufouchi, S., Faili, A., Weill, J. C., Reynaud, C. A. DNA polymerase η is the sole contributor of A/T modifications during immunoglobulin gene hypermutation in the mouse. The Journal of Experimental Medicine. 204 (1), 17-23 (2007).
- Maul, R. W., Gearhart, P. J. AID and somatic hypermutation. Advances in Immunology. 105, 159-191 (2010).
- Shen, H. M., Tanaka, A., Bozek, G., Nicolae, D., Storb, U. Somatic hypermutation and class switch recombination in Msh6-/- Ung-/- double-knockout mice. The Journal of Immunology. 177 (8), 5386-5392 (2006).
- Cheng, H. L., et al. Integrity of the AID serine-38 phosphorylation site is critical for class switch recombination and somatic hypermutation in mice. Proceedings of the National Academy of Sciences. 106 (8), 2717-2722 (2009).
- Lebecque, S. G., Gearhart, P. J. Boundaries of somatic mutation in rearranged immunoglobulin genes: 5'boundary is near the promoter, and 3'boundary is approximately 1 kb from V (D) J gene. The Journal of Experimental Medicine. 172 (6), 1717-1727 (1990).
- Jolly, C. J., Klix, N., Neuberger, M. S. Rapid methods for the analysis of immunoglobulin gene hypermutation: application to transgenic and gene targeted mice. Nucleic Acids Research. 25 (10), 1913-1919 (1997).
- Choi, J. E., Matthews, A. J., Michel, G., Vuong, B. Q. AID Phosphorylation Regulates Mismatch Repair-Dependent Class Switch Recombination and Affinity Maturation. The Journal of Immunology. 204 (1), 13-22 (2020).
- McBride, K. M., et al. Regulation of class switch recombination and somatic mutation by AID phosphorylation. The Journal of Experimental Medicine. 205 (11), 2585-2594 (2008).
- Liu, M., et al. Two levels of protection for the B cell genome during somatic hypermutation. Nature. 451 (7180), 841-845 (2008).
- Ross, M., Birbeck, M., Wills, V., Forrester, J., Davis, A. Peanut lectin binding properties of germinal centers of mouse lymphoid tissues. Nature. 284, 364-366 (1980).
- Zhang, J., MacLennan, I. C., Liu, Y. J., Lane, P. J. Is rapid proliferation in B centroblasts linked to somatic mutation in memory B cell clones. Immunology Letters. 18 (4), 297-299 (1988).
- Nieuwenhuis, P., Opstelten, D. Functional anatomy of germinal centers. American Journal of Anatomy. 170 (3), 421-435 (1984).
- Lau, A. W., Brink, R. Selection in the germinal center. Current Opinion in Immunology. 63, 29-34 (2020).
- Victora, G. D., Nussenzweig, M. C. Germinal centers. Annual Review of Immunology. 30, 429-457 (2012).
- Mesin, L., Ersching, J., Victora, G. D. Germinal center B cell dynamics. Immunity. 45 (3), 471-482 (2016).
- Reichert, R. A., Gallatin, W. M., Weissman, I. L., Butcher, E. C. Germinal center B cells lack homing receptors necessary for normal lymphocyte recirculation. The Journal of Experimental Medicine. 157 (3), 813-827 (1983).
- Rose, M., Birbeck, M., Wills, V., Forrester, J., Davis, A. Peanut lectin binding properties of germinal centers of mouse lymphoid tissues. Nature. 284, 364-366 (1980).
- Hamada, S., Fujita, S. DAPI staining improved for quantitative cytofluorometry. Histochemistry. 79 (2), 219-226 (1983).
- Otto, F. DAPI staining of fixed cells for high-resolution flow cytometry of nuclear DNA. Methods in Cell Biology. 33, 105-110 (1990).
- Butcher, E., et al. Surface phenotype of Peyer's patch germinal center cells: implications for the role of germinal centers in B cell differentiation. The Journal of Immunology. 129 (6), 2698-2707 (1982).
- Rogerson, B. J., Harris, D. P., Swain, S. L., Burgess, D. O. Germinal center B cells in Peyer's patches of aged mice exhibit a normal activation phenotype and highly mutated IgM genes. Mechanisms of Ageing and Development. 124 (2), 155-165 (2003).
- Potapov, V., Ong, J. L. Examining sources of error in PCR by single-molecule sequencing. PloS One. 12 (1), 0169774 (2017).
- Gonzalez-Fernandez, A., Milstein, C. Analysis of somatic hypermutation in mouse Peyer's patches using immunoglobulin kappa light-chain transgenes. Proceedings of the National Academy of Sciences. 90 (21), 9862-9866 (1993).
- Reboldi, A., Cyster, J. G. Peyer's patches: organizing B-cell responses at the intestinal frontier. Immunological Reviews. 271 (1), 230-245 (2016).
- Betz, A. G., Rada, C., Pannell, R., Milstein, C., Neuberger, M. S. Passenger transgenes reveal intrinsic specificity of the antibody hypermutation mechanism: clustering, polarity, and specific hot spots. Proceedings of the National Academy of Sciences. 90 (6), 2385-2388 (1993).
- Rada, C., Gupta, S. K., Gherardi, E., Milstein, C. Mutation and selection during the secondary response to 2-phenyloxazolone. Proceedings of the National Academy of Sciences. 88 (13), 5508-5512 (1991).
- Heise, N., Klein, U. Somatic Hypermutation and Affinity Maturation Analysis Using the 4-Hydroxy-3-Nitrophenyl-Acetyl (NP) System. Methods in Molecular Biology. 1623, 191-208 (2017).
- Smith, F., Cumano, A., Licht, A., Pecht, I., Rajewsky, K. Low affinity of kappa chain bearing (4-hydroxy-3-nitrophenyl) acetyl (NP)-specific antibodies in the primary antibody repertoire of C57BL/6 mice may explain lambda chain dominance in primary anti-NP responses. Molecular Immunology. 22 (10), 1209-1216 (1985).
- Takahashi, Y., Dutta, P. R., Cerasoli, D. M., Kelsoe, G. In situ studies of the primary immune response to (4-hydroxy-3-nitrophenyl) acetyl. V. Affinity maturation develops in two stages of clonal selection. The Journal of Experimental Medicine. 187 (6), 885-895 (1998).
- Allen, D., Simon, T., Sablitzky, F., Rajewsky, K., Cumano, A. Antibody engineering for the analysis of affinity maturation of an anti-hapten response. The EMBO Journal. 7 (7), 1995-2001 (1988).
- Cumano, A., Rajewsky, K. Clonal recruitment and somatic mutation in the generation of immunological memory to the hapten NP. The EMBO Journal. 5 (10), 2459-2468 (1986).
- Smith, K., Nossal, G., Tarlinton, D. M. FAS is highly expressed in the germinal center but is not required for regulation of the B-cell response to antigen. Proceedings of the National Academy of Sciences. 92 (25), 11628-11632 (1995).
- Hao, Z., et al. Fas receptor expression in germinal-center B cells is essential for T and B lymphocyte homeostasis. Immunity. 29 (4), 615-627 (2008).
- Cervenak, L., Magyar, A., Boja, R., László, G. Differential expression of GL7 activation antigen on bone marrow B cell subpopulations and peripheral B cells. Immunology Letters. 78 (2), 89-96 (2001).
- Naito, Y., et al. Germinal center marker GL7 probes activation-dependent repression of N-glycolylneuraminic acid, a sialic acid species involved in the negative modulation of B-cell activation. Molecular and Cellular Biology. 27 (8), 3008-3022 (2007).
- Olson, W. J., et al. Orphan Nuclear Receptor NR2F6 Suppresses T Follicular Helper Cell Accumulation through Regulation of IL-21. Cell Reports. 28 (11), 2878-2891 (2019).
- Dorsett, Y., et al. MicroRNA-155 suppresses activation-induced cytidine deaminase-mediated Myc-Igh translocation. Immunity. 28 (5), 630-638 (2008).
- Goetz, C., Hammerbeck, C., Bonnevier, J. . Flow Cytometry Basics for the Non-Expert. , (2018).
- Hawley, T. S., Herbert, D. J., Eaker, S. S., Hawley, R. G. . Flow Cytometry Protocols. , (2004).
- Costa, E., et al. A new automated flow cytometry data analysis approach for the diagnostic screening of neoplastic B-cell disorders in peripheral blood samples with absolute lymphocytosis. Leukemia. 20 (7), 1221-1230 (2006).
- McKinnon, K. M. Flow cytometry: An overview. Current Protocols in Immunology. 120 (1), 1-11 (2018).
- McKinnon, K. M. Multiparameter Conventional Flow Cytometry. Methods in Molecular Biology. , 139-150 (2018).
- Lucchesi, S., et al. Computational Analysis of Multiparametric Flow Cytometric Data to Dissect B Cell Subsets in Vaccine Studies. Cytometry Part A. 97, 259-267 (2019).
- Longerich, S., Tanaka, A., Bozek, G., Nicolae, D., Storb, U. The very 5' end and the constant region of Ig genes are spared from somatic mutation because AID does not access these regions. The Journal of Experimental Medicine. 202 (10), 1443-1454 (2005).
- Retter, I., et al. Sequence and characterization of the Ig heavy chain constant and partial variable region of the mouse strain 129S1. The Journal of Immunology. 179 (4), 2419-2427 (2007).
- Shen, H. M., Peters, A., Baron, B., Zhu, X., Storb, U. Mutation of BCL-6 gene in normal B cells by the process of somatic hypermutation of Ig genes. Science. 280 (5370), 1750-1752 (1998).
- Richter, K., et al. Altered pattern of immunoglobulin hypermutation in mice deficient in Slip-GC protein. Journal of Biological Chemistry. 287 (38), 31856-31865 (2012).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved