Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Immunology and Infection
Анализ соматической гипермутации в интроне JH4 герминального центра B-клеток из патчей мыши Пейера
Представлено здесь является анализ для количественной соматической гипермутации в иммуноглобулин тяжелых цепных генов локус с использованием зародышевых клеток центра В из патчей мыши Пейер.
В зародышевых центрах лимфоидных органов, зрелые В-клетки изменяют их выраженный иммуноглобулин (Ig), вводя неоплатенные мутации в переменное кодирование экзонов ig тяжелых и легких цепных генных локусов. Этот процесс соматической гипермутации (SHM) требует фермента активации индуцированной цитидина деаминазы (AID), который преобразует дезоксицитидины (C), в дезоксиуридины (U). Обработка НЕСОВМЕСТИМЫХ несоответствий в мутации базовым иссечением и несоответствующей ремонтной дорожкой вводит новые последовательности кодирования Ig, которые могут привести к более высокому сродству Ig. Мутации в генах AID или ДНК могут блокировать или значительно изменять типы мутаций, наблюдаемых в локусах Ig. Мы описываем протокол количественной оценки интрон мутаций JH4, который использует флуоресценцию активированной сортировки клеток (FACS), ПЦР и секвенирования Sanger. Хотя этот анализ непосредственно не измеряет созревание сродства Ig, это свидетельствует о мутациях в переменных последовательностях кодирования Ig. Кроме того, эти методы используют общие методы молекулярной биологии, которые анализируют мутации в последовательностях Ig нескольких клонов В-клеток. Таким образом, этот анализ является бесценным инструментом в изучении SHM и Ig диверсификации.
В-клетки, члены адаптивной иммунной системы, распознают и устраняют антигены, вырабатывая антитела, также известные как иммуноглобулины (Ig). Каждый Ig состоит из двух тяжелых (IgH) и двух легких (IgL) цепных полипептидов, которые проводятся вместе дисульфидными связями, чтобы сформировать характерную структуру формы "Y" Ig1. N-termini IgH и IgL составляют переменную (V) область каждого полипептида и вместе они образуют антиген связывания сайта Ig, в то время как постоянная область IgH придает эффектор функции Ig. Развитие B-клеток в костном мозге переставить V кодирования экзонов IgH и IgL в процессе, известном как V (D)J рекомбинации2,3,4. Транскрипция рекомбинированного V exons, в сочетании с соответствующими постоянными экзонами региона, образует мРНК, которая переводится в Ig.
Зрелые В-клетки, выражаюющие мембрану связаны Ig, также известный как рецептор В-клеток (BCR), циркулируют во вторичные лимфоидные органы, такие как селезенка, лимфатический узел, или патчи Пейера, где они обследуют среду для антигенов и взаимодействуют с другими клетками иммуннойсистемы 1. В зародышевых центрах (GC) вторичных лимфоидных органов, B клетки, которые признают антиген через BCR становятся активированными. С помощью фолликулярных дендритных клеток и фолликулярных помощников Т-клеток, активированные В-клетки могут размножаться и дифференцироваться в плазменные клетки и клетки памяти, которые являются важными эффекторами надежного иммунного ответа5,6,7,8,9. Кроме того, эти активированные В-клетки могут проходить вторичные процессы диверсификации генов Ig - рекомбинацию коммутатора класса (CSR) и соматическую гипермутацию (SHM). Во время КСО В-клетки обмениваются по умолчанию μ постоянной областью полипептида IgH с другой постоянной областью (γ, α, ε) через реакциюудаления ДНК-рекомбинации (рисунок 1). Это позволяет выражение различных постоянных exon и перевод нового Ig. Ячейка B перейдет от выражения IgM к другому изотипу (IgG, IgA, IgE). КСО изменяет функцию эффектора Ig, не изменяя его антигеннуюспецифичность 10,11,12. Тем не менее, во время SHM, B-клетки мутируют V кодирования регионов IgH иIgL,чтобы производство и выбор более высокого сродства Igs, которые могут более эффективно устранить антиген13,14,15 (Рисунок 1). Важно отметить, что и КСО, и SHM зависят от функции одного фермента: активация индуцированной цитидин деаминазы (AID)16,17,18. Люди и мыши, не хватает AID не может завершить КСО или SHM и настоящее время с повышенным IgM сыворотки титеры или Hyper-IgM17,19.
В КСО, AID deaminates дезоксицитидин (C) в повторяющихся регионах коммутатора, которые предшествуют каждой постоянной кодирования экзонов, превращая их в дезоксиуридины (U)20,21, что создает несовместимые базы сопряжения между дезоксиуридинов и дезоксигуанозинов (U:G). Эти U:G несоответствия преобразуются в двойной ДНК перерывов, которые необходимы для рекомбинации ДНК, либо путем ремонта иссечения базы (BER) или несоответствия ремонта (MMR)путь 22,23,24,25,26,27,28,29. В SHM AID deaminates C в эксонах кодирования V. Репликация через несоответствие U:G генерирует C:G к T: Переходные мутации, в то время как удаление базы uracil белком BER, гликозилаза ДНК uracil (UNG), до репликации ДНК производит как переход, так и трансверсиимутаций 16. Нулевые мутации в UNG значительно увеличивают C:G до T:A переходныхмутаций 21,22. Как и КСО, SHM требует дополнительных функций MMR и BER. Во время SHM MMR генерирует мутации в базовых парах A:T. Инактивирующие мутации в гомологии MutS 2 (MSH2)или полимеразе ДНК η (Pol) значительно уменьшают мутации на базах A:T и сложные мутации в MSH2 и Polе практически отменяет мутации на базах A:T21,30,31. В соответствии с критической ролью BER и MMR в преобразовании САИР-генерируемых U в переходные или трансверсионные мутации, мыши испытывают дефицит как для MSH2, так и для UNG (MSH2-/-UNG-/-)отображают только C:G к T:Переходные мутации в результате репликации через несоответствие U:G21.
Анализ SHM в регионах V кодирования остается сложным, потому что развивающиеся B-клетки могут рекомбинировать любой из экзонов кодирования V(D)J в локусе IgH и IgL1,2,4. Точный анализ этих уникально рекомбинированных и соматически мутировавших V областей требует идентификации и изоляции клонов В-клеток или Ig mRNA11,13. JH4 интрон, который является 3' из последних J кодирования экзон в локусе IgH, гавани соматических мутаций из-за распространения мутаций 3' из V промоутер32,33,34 и, следовательно, часто используется в качестве суррогатного маркера для SHM в V регионах31,35 (Рисунок 1). Чтобы экспериментально выяснить, как конкретные гены или генетические мутации изменить SHM моделей или ставок, JH4 интрон может быть секвенирован из патчей Пейера (PP) герминального центра B клеток (GCBCs), которые проходят высокие показатели SHM36,37,38. GCBCs можно легко определить и изолировать с флуоресцентно спряженными антителамипротив маркеров поверхности клетки (B220 и PNAHI)17,39.
Представлен подробный протокол для характеристики интронных мутаций JH4 в PP GCBCs у мышей с использованием комбинации FACS (сортировка активированных клеток флуоресценции), ПЦР и секвенированияСэнгера (рисунок 2).
Все мыши-мутанты были сохранены на фоне C57BL/6. Для всех экспериментов использовались возрастные (2-5 месяцев) мыши мужского и женского пола. Мужство и эксперименты с мышами проводились в соответствии с протоколами, утвержденными Городским колледжем Нью-йоркского институционального комитета по уходу за животными и использованию.
1. Вскрытие патчей Пейера
- Euthanize мыши со 100% CO2 на 3 л / мин в течение 5 минут с последующим вывихом шейки матки, чтобы подтвердить смерть. Стерилизовать инструменты для вскрытия (ножницы, типсы, тонкие типсы) и руки в перчатках с 70% этанола.
- Положите мышь на вскрытии площадку с животом подвергаются. Обильно распылить тело мыши с 70% этанола до принятия каких-либо разрезов для стерилизации области вскрытия.
- Сделайте разрез на коже живота и удалить кожу из живота, потянув одновременно по обе стороны от разреза к голове и хвосту с помощью миппов (или стерилизованных, в перчатках руки).
- Прикрепите передовую и задние конечности мыши.
- Вырезать брюшной полости ножницами, чтобы разоблачить внутренние органы.
- Найдите тонкий кишечник между желудком и caecum ("J" формы структуры вблизи толстой кишки). Удалите тонкой кишки путем резки ниже желудка и выше caecum.
- Удалите любые соединительной ткани и жира, связывающие складки тонкой кишки вместе.
ПРИМЕЧАНИЕ: жир будет иметь отличительный белый цвет, в отличие от розового цвета тонкой кишки. - Изучите внешнюю поверхность тонкой кишки на участки Пейера (PPs), которые являются небольшими (1 мм), овальной формы структур, которые появляются белые ниже тонкого слоя полупрозрачных эпителиальных клеток.
- Тщательно акциз все видимые PP с ножницами.
ПРИМЕЧАНИЕ: Одна мышь дикого типа C57BL/6 (WT) может дать 4-8 PPs, в то время как AID-/- мышь будет иметь 6-10 PPs. - Соберите PPs в 1,5 мл микроцентрифуг трубки, содержащей 1 мл буфера FACS на льду.
ПРИМЕЧАНИЕ: PP должен утонуть, в то время как жир будет плавать на поверхность и могут быть удалены.
2. Изоляция клеток для FACS
- Поместите 40 мкм фильтр в 6-хорошо блюдо с 1 мл холодного (4 кк) FACS буфера.
- Налейте PPs из 1,5 мл трубки на фильтр.
- Вымойте PPs с 1 мл холодного буфера FACS, убедившись, что они всегда находятся в жидкости и на льду.
- Используйте плоский конец поршеня из шприца 1 мл в качестве пестика, чтобы раздавить PPs на фильтре, пока только соединительная ткань остается на фильтре.
- Вымойте фильтр и поршень с 1 мл холодного буфера FACS, чтобы освободить клетки в 6 хорошо блюдо.
- Соберите 4 мл ячеек в холодном буфере FACS и отфильтруйте их через 40 мкм ситечко крышка FACS трубки.
- Вымойте крышку ситечком с 1 мл холодного буфера FACS.
- Пеллет клетки при 600 х г при 4 градусов по Цельсию в течение 5 минут в размахивая центрифуг ведро.
- Декант супернатант.
- Повторное приостановление ячеек в 0,4 мл холодного буфера FACS.
- Удалите 10 МКЛ для подсчета ячеек для проверки урожайности (ожидайте 5 х 106 ячеек/мышей, см. Рисунок 3A)
- Фильтр остальные клетки через 40 мкм ситечко крышка в трубку FACS и приступить к окрашивания для FACS.
3. Окрашивание ГКБК для FACS
- Добавьте блок 1 йл Fc (неоцеличные антимошки CD16/CD32) к 400 йл клеточной подвески и поместите клетки на лед в течение 15 минут.
- Добавьте 2 мл холодного буфера FACS для мытья клеток.
- Пеллетные клетки при 600 x g при 4 градусах Цельсия в течение 5 минут и отбрасывайте супернатант.
- Переусердуйтесь с клетками в 80 МКЛ холодного буфера FACS.
- Удалите 10 МКЛ клеток из WT PP для каждого контроля окрашивания (4 в общей сложности, в том числе 3 одного контроля пятна и 1 неоплеканный контроль). Оставьте 40 МКЛ WT PP для следующего шага. Кроме того, используйте компенсационные бусинки для контроля окрашивания.
- Пятно каждого из экспериментальных образцов (например, WT и AID-/-) в 500 МКЛ холодного буфера FACS с 2,5 мл арахисового агглютинина (PNA)-биотина в течение 15 минут на льду.
- Добавьте 2 мл холодного буфера FACS для мытья клеток.
- Пеллетные клетки при 600 x g при 4 градусах Цельсия в течение 5 минут и отбрасывайте супернатант.
- Пятно каждого экспериментального образца с 500 йл коктейля в темноте, на льду, в течение 15 минут (таблица 1). Убедитесь, что клетки полностью повторно в окрашивание коктейль.
- Подготовь одиночные элементы управления пятнами для матрицы компенсации.
- Пятно клеток в 500 МКЛ холодного буфера FACS с помощью разбавления, указанные в таблице 2.
- Инкубировать окрашивание элементов управления в темноте, на льду, в течение 15 минут.
- Добавьте 2 мл холодного буфера FACS ко всем трубам в шагах 3.7 и 3.8, гранулы клетки, и отбросить супернатант, чтобы смыть несъебленные антитела или DAPI.
- Переусердуйтесь с клетками в 500 МКЛ холодного буфера FACS и поместите на лед.
- Используя сортер клеток, соберите B220иPNAHI с каждого окрашенного экспериментального образца. Рисунок 3B показывает типичные проценты B220и PNAHI, полученные от WT и AID-/- PPs. Рисунок 3C отображает стратегию FACS gating.
4. Извлечение ДНК из ГХФУ
- Пеллет отсортированы клетки при 600 х г при 4 градусов по Цельсию в течение 5 мин и отказаться от супернатанта.
- Перепробовать клетки в 1 мл холодного буфера FACS и передать клетки в 1,5 мл микроцентрифуг трубки.
- Пеллет клетки на 600 х г при 4 градусов по Цельсию в течение 5 минут и отказаться от супернатанта.
- Повторное потребление клеток в 500 МКЛ буфера извлечения ДНК и 5 МКЛ 20 мг/мл протеиназы К.
- Инкубировать при 56 градусов по Цельсию на ночь.
- Осадок ДНК с 500 мкл изопропанола и 1 йл 20 мг/мл гликогена. Смешайте трубку тщательно, инвертирование 5-6x.
- Инкубировать при комнатной температуре в течение 10 минут.
- Центрифуга в микроцентрифуге в течение 15 мин при 25 градусов по Цельсию при 21 000 х г.
- Откажитесь от супернатанта и сохраните гранулы, которые содержат осажденную ДНК и гликоген.
- Вымойте гранулы ДНК с 1 мл 70% этанола.
- Пеллет ДНК в микроцентрифуге в течение 10 мин при 25 градусов по Цельсию при 21 000 х г.
- Удалите 70% этанола и высушите гранулы ДНК в течение 5-10 мин.
ПРИМЕЧАНИЕ: Избегайте чрезмерной сушки, как ДНК не может регидратировать полностью.
- Переподход ДНК в буфере TE 30 хл и инкубировать на ночь при 56 градусов по Цельсию.
5. JH4 интрон последовательность усиления и анализа
- Количественная оценка ДНК путем измерения поглощения на длине волны 260 нм (A260).
ПРИМЕЧАНИЕ: Типичная концентрация ДНК, извлеченной изотсортированного B220 и PNAHI GCBCs мыши C57BL/6, составляет 20-40 нг/мл. - Выполните вложенный ПЦР для интрона JH4(таблица 3, таблица 4). Нормализует общее количество геномной ДНК, используемой в первом ПЦР, до наименее концентрированного образца. (например, если наименее концентрированная выборка составляет 5 нг/мл, используйте 58,75 нг ДНК для всех образцов в максимальном объеме воды (11,75 МЛ) в ПЦР #1).
- Решите pcR продукт на 1,5% агарозный гель при 200 V в течение 20 мин. Ожидаемый размер ампликона составляет 580 б.п.
- Акциз amplicon из геля и извлечь ДНК с помощью комплекта извлечения геля в соответствии с инструкциями производителя (см. Дополнительная цифра 1).
- Elute ДНК с 30 йл воды и количественно количество ДНК путем измерения A260.
ПРИМЕЧАНИЕ: Типичная концентрация очищенного продукта ПЦР составляет 3-10 нг/мл.
- Elute ДНК с 30 йл воды и количественно количество ДНК путем измерения A260.
- Ligate очищенный продукт ПЦР в плазмиду с тупыми концами. Стандартизация общего количества продукта ПЦР, используемого в каждой реакции перевязки(таблица 5).
- Инкубировать реакцию перевязки при комнатной температуре в течение 5 минут или на ночь при температуре 16 градусов по Цельсию.
- Преобразование электрокомпетентных бактериальных клеток с 2 йл реакции перевязки.
- Электропорат при 1,65 кВ.
- Спасение в 600 МКЛ soC средств массовой информации для 1 ч при 37 градусов по Цельсию в трясущимся инкубаторе при 225 об/мин.
- Плита 100 Л преобразованных бактерий на LB дополняется ампициллином (100 мкг/мл) агар пластин и инкубировать на ночь при 37 градусов по Цельсию.
- Отправить пластины бактериальных колоний для Сэнгера секвенирования с помощью T7 вперед грунтовки. Кроме того, расти ночные культуры каждой бактериальной колонии и выполнять плазмидной очистки.
- При необходимости повторите ПЦР, перевязку и/или трансформацию для оптимизации урожайности бактериальных колоний
ПРИМЕЧАНИЕ: Минимум 30 колоний должны быть собраны из каждой пластины.
- При необходимости повторите ПЦР, перевязку и/или трансформацию для оптимизации урожайности бактериальных колоний
- Стандартизация данных последовательности в .txt файлов
- Удалите плазмидную последовательность.
- Убедитесь, что каждая последовательность ориентирована от 5' до 3' в соответствии с интронной последовательностью JH4 (NG_005838). Создать обратный комплект любой последовательности, по мере необходимости.
- Выровнять последовательности, полученные для каждого ПЦР против JH4 интрон эталонной последовательности (NG_005838) с помощью программного обеспечения Clustal Omega (Рисунок 4A).
- Определить отличия от эталонной последовательности как мутации
- Убедитесь, что все мутации являются истинными точечными мутациями, изучая электроферограмму секвенирования Сэнгера. Повторите секвенирование, если это необходимо. (Рисунок 4B,C).
- Табулировать и количественно уникальные мутации в JH4 интрон для каждого генотипа (Рисунок 5).
- Подсчитайте последовательности с идентичными мутациями только один раз
ПРИМЕЧАНИЕ: Невозможно определить, были ли идентичные последовательности созданы во время ПЦР или идентичных событий SHM в разных клетках группы В. - Подсчитайте каждый экземпляр интронных последовательностей WT germline JH4 (т.е. тех, у кого нет мутаций) как уникальную последовательность.
- Подсчитайте последовательности с идентичными мутациями только один раз
Цитометрия потока
Зрелые В-клетки циркулируют в зародышевые центры, где они проходят сродство созревания, клонального расширения, идифференциации в плазме или клеткипамяти 40,41,42,43,44. Эти GCBCs могут быть определены многочисленные маркеры поверхности клеток, в том числе высокое выражение рецептора CD45R/B220 и связывание арахисового агглютинина (PNA)45,46. Чтобы изолировать активированные ГХК, PP-клетки были окрашены антителами против В220, конъюгированными с фикоэритроном (PE) и биотинилированным ПНА, а затем стрептавидином, спряженным с APC-eFluor780. Мертвые клетки были ликвидированы с помощью флуоресцентных 4',6-Diamidino-2-фенилиндол (DAPI) красителя, который окрашивает нуклеиновую кислоту умирающих илимертвых клеток 47,48. Окрашенные клетки были впоследствии проанализированы и отсортированы с помощью цитометрии потока. PPs состоял из 80% B220и ячеек 49,50. WT PPs содержат в среднем 4 х 106 ячеек на мышь(рисунок 3A). Приблизительно 8% клеток WT PP были B220иPNAHI, что в два раза меньше, наблюдаемого в AID-/ - ( Рисунок 3B). Таким образом, после сортировки было получено 0,3-0,6х 10 6 B220 и PNAHI GCBCs, которых было достаточно для анализа мутаций в интроне JH4.
Анализ последовательности JH4
JH4 интрон был усилен вложенных ПЦР с использованием общих VHJ558 семьи грунтовки (J558FR3Fw и VHJ558.2), а затем JH4 интронохватывающихгрунтовки VHJ558.3 и VHJ558.435,37. Из 105 уникальных последовательностей, полученных из WT GCBCs, в общей сложности было обнаружено 226 мутаций(рисунок 5A). Анализ спектра мутации GCBC у мышей WT показал диапазон переходов и трансверсий со скоростью 4 х 10-3 мутаций/bp, который был рассчитан путем деления общего числа мутировавших баз на общее количествооснований,которыебыли секвенированы 32,36,37,38. Кроме того, каждый продукт JH4 PCR от WT GCBCs содержал 1-25 мутаций(рисунок 5B), где несколько мутаций часто находились на однойпоследовательности 33,36. Только две мутации были выявлены в 113 AID-/- последовательностях(рисунок 5A). AID-/- B-клетки продемонстрировали 1,66 х 10-5 мутаций/bp, что было значительно ниже, чем WT B клеток (p lt;0.05)36 и сравнивает с погрешностью высокой точности полимеразы (5,3 х 10-7 sub/base/doubling)51,52. Таким образом, AID-/- B-клетки служили полезным негативным контролем для этого анализа.
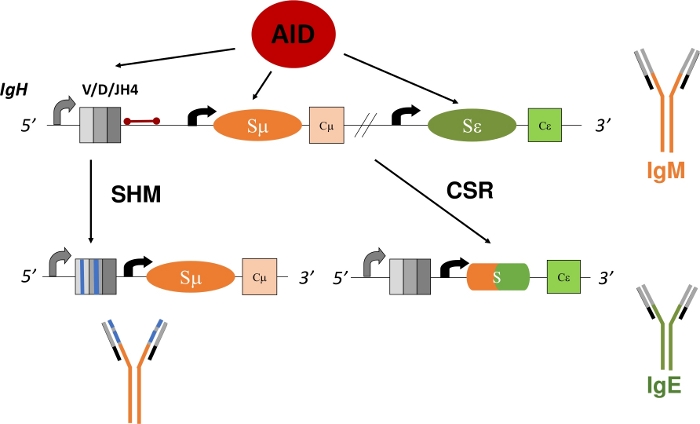
Рисунок 1: Схема локуса гена IgH и регионов, на которые нацелена AID во время КСО и ШМ. Красная планка указывает на интрон 580 bp JH4, который является 3' перестановки VDJH4 и анализируется в этом протоколе. В КСО деаминация интронных регионов коммутаторов, зависящих от AID, способствует образованию DSB, что позволяет удаление рекомбинации и экспрессию нового изотипа антител (IgM to IgE). Во время SHM, V регионов (серые ящики) накапливаются мутации (синие линии), которые могут привести к более высокой близости Ig. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
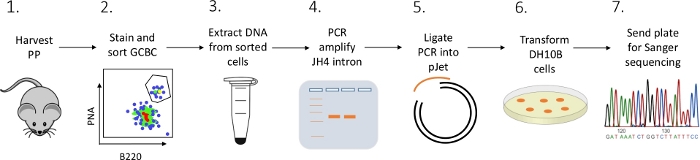
Рисунок 2: Рабочий процесс для анализа SHM интрона JH4 в GCBCs изолированы от PPs. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
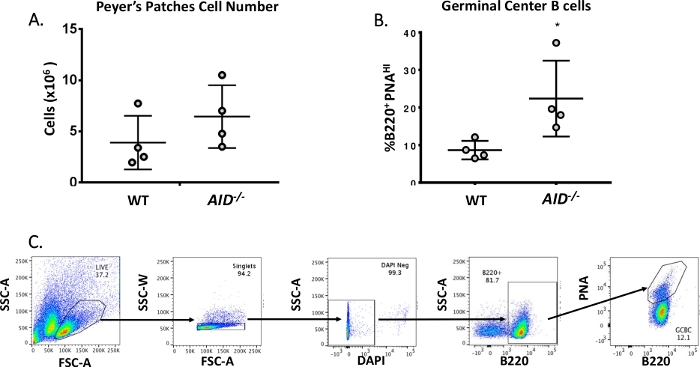
Рисунок 3: Характеристика ГКБК ПП. (A)Общее количество pp клеток от WT и AID-/- мышей (n q 4 в генотип). Бары ошибок представляют собой стандартное отклонение от среднего. (B) Процент B220иPNAHI GCBCs, полученных от PPs WT и AID-/- мышей (n No 4 на генотип)36. Бары ошибок представляют собой стандартное отклонение от среднего, «p'lt;0.05» с помощью тестов студента. (C) Представитель FACS участков для сортировки B220иPNAHI GCBCs от ПК. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
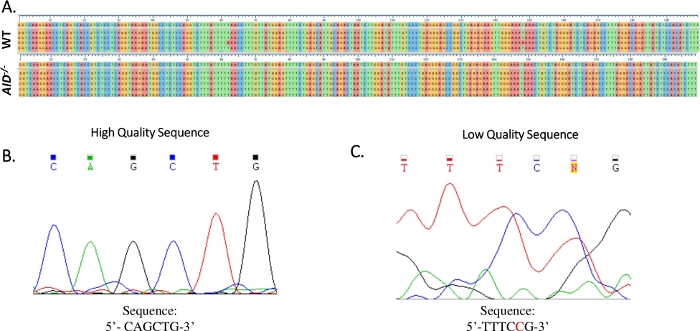
Рисунок 4: Анализ данных последовательности JH4 Sanger. (A) Пример последовательности выравнивания данных последовательности Sanger продукта JH4 PCR от WT (вверху) и AID-/- (внизу) GCBCs к последовательности справки геномной (NG_005838), которая последовательность сразу под пронумероваваемые метки тика. Выравнивания были созданы с использованием Clustal Omega. (B)Электроферограмма высококачественных данных последовательности Sanger, которые отображали различные пики для каждой базы. (C)Электроферограмма низкого качества данных последовательности, которые показали неоднозначные пики и неопределенные основания (N). Нуклеотид, показанный красным цветом, должен быть вручную аннотирован в текстовом файле последовательности. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
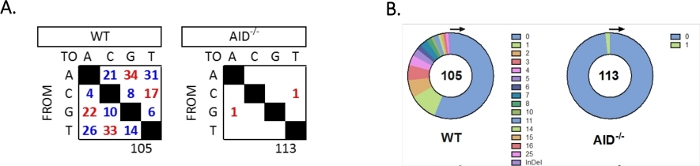
Рисунок 5: Анализ мутаций в интроне JH4 в WT и AID-/- GCBCs. (A)Общее количество переходных (красных) и трансверсийных (голубых) мутаций в базах A, C, G и T для каждого генотипа обобщено в таблицах. Общее количество анализируемых последовательностей указано ниже таблицы. (B)Количество мутаций на ПЦР ампликона для каждого генотипа изображено на кругообразной диаграмме. Эта цифра была изменена с Чой и др.36 Авторское право 2020. Американская ассоциация иммунологов, Inc Пожалуйста, нажмите здесь, чтобы просмотреть более широкую версию этой цифры.
| Окрашивание Коктейль для GCBCs | Объем: 500 мкл | ||
| Антитела или краситель | Флюорофор | разбавление | КЛ |
| B220 | PE | 1000 | 0.5 |
| Стрептавидин | БТР-эФлюор780 | 500 | 1 |
| ДАПИ | N/A | 500 | 1 |
Таблица 1: Окрашивание коктейлей для GCBCs. Коктейль из указанных антител или красителя (указанный в литий)в указанных разбавлениях были использованы для окрашивания клеток PP в 500 йл для цитометрии потока.
| Одиночные пятна для компенсации | Объем: 500 мкл | ||
| Антитела или краситель | Флюорофор | разбавление | КЛ |
| B220 | PE | 1000 | 0.5 |
| B220 | БТР-эФлюор780 | 750 | 0.67 |
| ДАПИ | N/A | 500 | 1 |
Таблица 2: Одиночные элементы управления пятнами для компенсации. Антитела B220, конъюгированные с указанными флюорофорами, использовались для одного контроля пятен для компенсации спектрального перекрытия.
| ПЦР #1 | ||||
| реагент | том | Условия термоциклера | ||
| 5x Буфер | 4 йл | 1 | 95 КК | 3 мин. |
| 10 мМ дНТП | 2 МЛ | 2 | 94 КК | 30 сек |
| 10 МКМ J558FR3Fw | 1 йл | 3 | 55 КК | 30 сек |
| 10 МКМ VHJ558.2 | 1 йл | 4 | 72 КК | 1:30 мин |
| Полимераза ДНК высокой верности | 0,25 МЛ | Цикл 2-4 9x | ||
| ДНК | x (стандартизация наименее концентрированной выборки) | |||
| H2O | до 20 мкл | 5 | 72 КК | 5 мин. |
| Разбавить ПЦР продукт 1:5 в H2O, прежде чем переступить к ПЦР #2 | ||||
Таблица 3: Вложенный ПЦР интрона JH4. Компоненты ПЦР и условия термоциклера для первой реакции усиления. Разбавить первый продукт ПЦР 1:5 водой и использовать 1 МКЛ этого разбавления для второго ПЦР.
| ПЦР #2 | ||||
| реагент | том | Термоциклер Условия #2 | ||
| 5x Буфер | 4 йл | 1 | 94 КК | 3 мин. |
| 10 мМ дНТП | 2 МЛ | 2 | 94 КК | 30 сек |
| 10 МКМ VHJ558.3 | 1 йл | 3 | 55 КК | 30 сек |
| 10 МКМ VHJ558.4 | 1 йл | 4 | 72 КК | 30 сек |
| Полимераза ДНК высокой верности | 0,25 МЛ | Цикл 2-4 21x | ||
| Разбавленный ПЦР-1 | 1 йл | |||
| H2O | до 20 мкл | 5 | 72 КК | 5 мин. |
Таблица 4: Компоненты ПЦР и термоциклерные условия для второго ПЦР.
| реагент | том |
| 2x Буфер | 10 йл |
| Очищенный ПЦР | x (стандартизация наименее концентрированной выборки) |
| Плазмид с тупыми концами | 1 йл |
| T4 Лигас ДНК | 1 йл |
| H2O | до 20 мкл |
| Инкубационный при температуре комнаты в течение 5 минут или на ночь при температуре 16oC | |
Таблица 5: Реакция лигации. Компоненты для перевязки очищенного продукта JH4 intron PCR в плазмиду.
| Буфер FACS |
| Тепло инактивировать FBS при температуре 56 градусов по Цельсию в течение одного часа до использования. Дополнение PBS, рН 7.4 (Gibco, #10010049) с 2,5% (v/v) тепловой инактивированной FBS. Хранить при 4 градусах Цельсия. |
| Буфер извлечения ДНК (100 мМ Трис рН 8,0, 0,1 М ЭДТА, 0,5% (ж/в) SDS) |
| Добавьте 50 мл 1 M Tris pH 8.0, 100mL 0.5 M EDTA, и 12.5 mL 20% SDS. Добавьте дистиллированную воду до 500 мл. Хранить при комнатной температуре. |
| TE Буфер (10 мМ Трис рН 8,0, 1 мМ ЭДТА) |
| Добавьте 2,5 мл 1 M Tris pH 8.0 и 500 мл 0.5 M EDTA. Добавьте дистиллированную воду до 250 мл. Хранить при комнатной температуре. |
Таблица 6: Буферные рецепты.
| Список олигонуклеотидов | ||
| J558FR3Fw | 5'-GCCTGACATCTGAGGACTCTGC-3' | |
| VHJ558.2 | 5'-CTGGACTTCGGTTTGGTG-3' | |
| VHJ558.3 | 5'-GGTCAAGGAACCTCAGTCA-3' | |
| VHJ558.4 | 5'-TCTCTAGACCAACTAC-3' | |
Таблица 7: Олигонуклеотиды, используемые в анализе.
Дополнительная цифра 1: Представитель агарозы гель изображение после завершения шага 5.4. JH4 интрон вложенных ПЦР продукт был решен на 1,5% агарозный гель и 580 bp amplicon был вырезан. WT PP указывает, что геномная ДНК WT PP GCBC использовалась в качестве шаблона для первого ПЦР и AID PP указывает на то, что геномнаяДНК AID-/- PP GCBC использовалась в качестве шаблона для первого ПЦР. ɸ указывает на отсутствие шаблона управления ПЦР и - указывает на то, что ничего не было загружено в колодец агарозного геля. Последняя полоса показывает 100 bp ДНК лестницы. Пожалуйста, нажмите здесь, чтобы загрузить эту цифру.
Характеристика SHM в igH и IgL V кодирования последовательностей неоднородной популяции клеток B представляет собой проблему, учитывая, что каждая клетка B однозначно реорганизует V сегментов кодирования во время рекомбинации V(D)J34. В этой статье мы описываем метод выявления мутаций в интроне JH4 ГХК. JH4 интрон, который расположен 3' из последнего сегмента кодирования J в локусе IgH, используется в качестве суррогата для SHM регионов V(рисунок 1)31,33,34,35. Чтобы каталогизировать эти интрон мутации JH4 и оценить, как конкретные гены влияют на производство или структуру мутаций, PP GCBCs специально анализируются. Эти клетки накапливают интрональные мутации JH4 в результате хронической стимуляции кишечной микробиотой53. Кроме того, B220иPNAHI GCBCs от PPs неиммунизированных мышей имеют спектр мутации, который сравнивается с splenic GCBCs от иммунизированныхживотных 54,55. Тем не менее, мутации в интроне JH4 не могут быть связаны с созреванием сродства Ig, потому что эти мутации не кодируются.
Чтобы определить, изменяет ли SHM сродство Ig, мыши должны быть иммунизированы intraperitoneally с антигеном, таких как NP (4-гидрокси-3-нитрофенилацетил) конъюгированных cGG (куриный гамма-глобулин) или KLH (ключ отверстие хрома hemocyanin)56. Впоследствии, мРНК может быть очищена отsplenic B220 и PNAHI GCBCs для изучения SHM в VH186.2, V кодирования экзон, который чаще всего распознает NP и мутировал после NP-CGG или NP-KLHиммунизации 31,57,58,59,60. Мутация триптофан-33 на лейцин в VH186.2 была охарактеризована для увеличения сродства Ig до 10 раз59,60 и,следовательно, один показатель того, что SHM и клональный отбор вызвал высокое сродство Ig. Измерение NP7- и NP20-специфических сывороток Ig титеры ELISA и расчета Ig-специфических NP7/NP20 соотношение в ходе иммунизации также документы Ig сродства созревания в результате SHM Vрегионов 17,21,36. Оба эти анализа могут быть использованы для корреляции SHM в VH186.2 кодирования последовательностей с изменениями в NP-специфических Ig сродства созревания.
Используются ли иммунизированные или неимунизированные животные для анализа SHM VH186.2 или интрона JH4, GCBCs должны быть точно идентифицированы. Мы представляем подход, основанный на FACS, чтобы изолировать B220 и PNAHI GCBCs. В качестве альтернативы, Фас и не сульфатных No 2-6-sialyl-LacNAc антиген, который признается антителом GL761,62,63,64,также могут быть использованы для изоляции GCBCs, которые определены как B220иFasNO GL7No 65 илиCD19 Выражение GL7 близко отражает PNA в активированных GCBCs лимфатических узлов64,65,66. В дополнение к использованию маркеров антител, характерных для ГХДК, окрашивание коктейлей должно максимизировать возбуждение флюорофора и обнаружение биомаркера при минимизации спектрального перекрытия флуоресцентного излучения. Антигены, выраженные на низких уровнях, должны быть обнаружены с антителом, которое спрягается с флюорофором с надежной флуоресценциейвыбросов 67. Рекомендуемый протокол окрашивания был оптимизирован для анализа на сортаторе клеток, оснащенном четырьмя лазерами (405 нм, 488 нм, 561 нм, 633 нм) и 12 фильтрами; однако конфигурации фильтров и доступность лазеров различаются между цитометрами. Для внесения изменений в протокол в соответствии с реагентом и наличием оборудования, читателю направляются дополнительные ресурсы, онлайн-зрители спектра и опубликованная литература67,68, 69,70,71,72,73. Многоцветный протокол окрашивания, описанный в настоящем, требует компенсации спектрального перекрытия для обеспечения того, чтобы отсортированная популяция клеток была ГХОК, а не неточного обнаружения флуоресцентного излучения. B220 служит полезным контролем окрашивания для описанного FACS(таблица 1B), потому что PPs будет иметь отличительные B220 отрицательных и положительных популяций (Рисунок 3C), что позволяет для соответствующей компенсации спектрального перекрытия. Стратегия гатинга, представленная на рисунке 3C, должна использоваться в качестве ориентира. Участки цитометрии потока могут варьироваться в зависимости от условий окрашивания и параметров цитометра. Тем не менее, 4-10% живых клеток должны быть B220иPNAHI 35, 52.
Все мутации в JH4 intron PP GCBCs должны быть проверены, чтобы убедиться, что наблюдаемые мутации действительно отражают SHM, а не артефакт ПЦР или секвенирования. AID-/- B-клетки могут служить полезным негативным контролем при изучении фенотипа SHM в других моделях мышей-мутантов, потому что эти клетки не могут завершить SHM17,19. Скорость мутации JH4 интрона в AID-/- GCBCs (1.66x10-5 мутаций/bp)20,21,36,37,38,50,74 сопоставима с погрешностью полимеразы высокой точности (5.3x10-7 sub/base/doubling)51,52, которая используется для усиления ДНК в вложенном ПЦР. Если AID-/- мыши недоступны, сравните наблюдаемую модель мутации и частоту с опубликованной литературой. Ig V регионов накапливаются 10-3-10-4 мутаций на базовую пару деления, что примерно в 106раз выше, чем скорость мутации других генныхлокусов 73,75. Результаты могут варьироваться в зависимости от возраста животного76. Кроме того, B220иPNALO клетки, которые марки не-GCBCs, могут быть использованы в качестве отрицательного контроля в отсутствие AID-/- мышей 52. Если частота мутаций в WT GCBCs ниже, чем ожидалось, ВТ зародышевой JH4 intronic последовательность может быть непропорционально представлены. В этом случае убедитесь, что ГХДК были окрашены и отсортированы надлежащим образом, а ПЦР свободны от загрязнения интроном WT germline JH4. Кроме того, необработанные данные секвенирования в электроферограммах должны быть тщательно проанализированы, чтобы убедиться, что мутации в текстовых данных последовательности не являются артефактами ошибок секвенирования. Например, плохие результаты секвенирования Sanger могут снизить надежность данных последовательности(рисунок 4). Такой контроль качества данных последовательности Sanger повысит точность и воспроизводимость анализа интрон мутаций JH4.
Авторов нечего раскрывать.
Мы благодарим Тасуку Хонджо за ПОМОЩЬ-/- мышей. Эта работа была поддержана Национальным институтом по вопросам здоровья меньшинств и неравенства в области здравоохранения (5G12MD007603), Национальным институтом рака (2U54CA132378) и Национальным институтом общих медицинских наук (1SC1GM132035-01).
| Name | Company | Catalog Number | Comments |
| 0.2 ml PCR 8-tube FLEX-FREE strip, attached clear flat caps, mixed | USA Scientific | 1402-4708 | |
| Ampicillin sodium salt | Fisher | BP1760-5 | |
| APC-eFluor780 anti-CD45R/B220 | eBioscience | 47-0452-80 | clone RA3-6B2 |
| BD FACSAria II | BD | 643186 | four lasers (405nm, 488nm, 561nm, 633nm) and 12 filters (PacBlue (450/50), AmCyan (502LP; 530/30), SSC (488/10), FITC (502LP; 530/30), PerCP-Cy5.5 (655LP; 695/40), PE (585/15), PE-Texas Red (600LP; 610/20), PE-Cy5 (630LP; 670/14), PE-Cy7 (735LP; 780/60), APC (660/20), Alexa700 (710LP; 730/45), APC-Cy7 (755LP; 780/60)) |
| BD slip tip 1mL syringe | Fisher | 14-823-434 | sterile |
| Biotinylated peanut agglutinin (PNA) | Vector Labs | B-1075-5 | |
| C57BL/6J mice | Jackson Laboratories | 664 | |
| Corning Falcon test tube with cell strainer snap cap | Fisher | 08-771-23 | |
| DAPI (4',6-Diamidino-2-Phenylindole, dihydrochloride) | Fisher | D1306 | 0.5 mg/ml |
| dNTP | NEB | N0447L | 10 mM |
| ElectroMAX DH10B competent cells | Fisher | 18-290-015 | |
| Falcon cell strainer 40mm | Fisher | 08-771-1 | |
| Falcon round-bottom polystyrene tubes (FACS tubes) | Fisher | 14-959-5 | |
| Falcon round-bottom polystyrene tubes (capped) | Fisher | 149591A | |
| Fetal bovine serum | R&D Systems (Atlanta Biologicals) | S11150 | |
| Gibco phosphate buffered saline PBS pH 7.4 | Fisher | 10-010-049 | |
| Glycogen | Sigma | 10901393001 | |
| Lasergene Molecular Biology (MegAlign Pro) | DNA Star | version 15 | |
| PE anti-CD45R/B220 | BD | 553090 | clone RA3-6B2 |
| Proteinase K | Fisher | BP1700-100 | |
| Q5 High-Fidelity DNA Polymerase | NEB | M0491L | |
| QIAquick Gel Extraction Kit | Qiagen | 28706 | |
| Seal-Rite 1.5mL microcentrifuge tubes | USA Scientific | 1615-5500 | |
| Streptavidin APC-eFluor 780 Conjugate | eBioscience | 47-4317-82 | |
| T4 DNA ligase | NEB | M020L | |
| Thermo Scientific CloneJET PCR Cloning Kit | ThermoFisher | FERK1231 | |
| Tissue culture plate 6 well | Fisher | 08-772-1B | sterile |
| Unlabeled anti-mouse CD16/CD32 (Fc block), BD | Fisher | BDB553142 | Clone 2.4G2 |
- Murphy, K., Weaver, C. . Janeyway's Immunobiology. , (2016).
- Alt, F. W., et al. VDJ recombination. Immunology Today. 13 (8), 306-314 (1992).
- Schatz, D. G., Ji, Y. Recombination centres and the orchestration of V (D) J recombination. Nature Reviews Immunology. 11 (4), 251-263 (2011).
- Oettinger, M. A., Schatz, D. G., Gorka, C., Baltimore, D. RAG-1 and RAG-2, adjacent genes that synergistically activate V (D) J recombination. Science. 248 (4962), 1517-1523 (1990).
- Berek, C., Berger, A., Apel, M. Maturation of the immune response in germinal centers. Cell. 67 (6), 1121-1129 (1991).
- Linterman, M. A., et al. Foxp3+ follicular regulatory T cells control the germinal center response. Nature Medicine. 17 (8), 975 (2011).
- Shulman, Z., et al. T follicular helper cell dynamics in germinal centers. Science. 341 (6146), 673-677 (2013).
- Good-Jacobson, K. L., et al. PD-1 regulates germinal center B cell survival and the formation and affinity of long-lived plasma cells. Nature Immunology. 11 (6), 535 (2010).
- Kerfoot, S. M., et al. Germinal center B cell and T follicular helper cell development initiates in the interfollicular zone. Immunity. 34 (6), 947-960 (2011).
- Chaudhuri, J., Alt, F. W. Class-switch recombination: interplay of transcription, DNA deamination and DNA repair. Nature Reviews Immunology. 4 (7), 541-552 (2004).
- Alt, F. W., Zhang, Y., Meng, F. L., Guo, C., Schwer, B. Mechanisms of programmed DNA lesions and genomic instability in the immune system. Cell. 152 (3), 417-429 (2013).
- Xu, Z., Zan, H., Pone, E. J., Mai, T., Casali, P. Immunoglobulin class-switch DNA recombination: induction, targeting and beyond. Nature Reviews Immunology. 12 (7), 517-531 (2012).
- Di Noia, J. M., Neuberger, M. S. Molecular mechanisms of antibody somatic hypermutation. Annual Reviews of Biochemistry. 76, 1-22 (2007).
- Peled, J. U., et al. The biochemistry of somatic hypermutation. Annual Review of Immunology. 26, 481-511 (2008).
- Liu, M., Schatz, D. G. Balancing AID and DNA repair during somatic hypermutation. Trends in Immunology. 30 (4), 173-181 (2009).
- Methot, S., Di Noia, J. Molecular Mechanisms of Somatic Hypermutation and Class Switch Recombination. Advances in Immunology. 133, 37-87 (2017).
- Muramatsu, M., et al. Class switch recombination and hypermutation require activation-induced cytidine deaminase (AID), a potential RNA editing enzyme. Cell. 102 (5), 553-563 (2000).
- Petersen-Mahrt, S. K., Harris, R. S., Neuberger, M. S. AID mutates E. coli suggesting a DNA deamination mechanism for antibody diversification. Nature. 418 (6893), 99 (2002).
- Revy, P., et al. Activation-induced cytidine deaminase (AID) deficiency causes the autosomal recessive form of the Hyper-IgM syndrome (HIGM2). Cell. 102 (5), 565-575 (2000).
- Petersen-Mahrt, S. DNA deamination in immunity. Immunological Reviews. 203 (1), 80-97 (2005).
- Rada, C., Di Noia, J. M., Neuberger, M. S. Mismatch recognition and uracil excision provide complementary paths to both Ig switching and the A/T-focused phase of somatic mutation. Molecular Cell. 16 (2), 163-171 (2004).
- Rada, C., et al. Immunoglobulin isotype switching is inhibited and somatic hypermutation perturbed in UNG-deficient mice. Current Biology. 12 (20), 1748-1755 (2002).
- Schrader, C. E., Vardo, J., Stavnezer, J. Role for mismatch repair proteins Msh2, Mlh1, and Pms2 in immunoglobulin class switching shown by sequence analysis of recombination junctions. The Journal of Experimental Medicine. 195 (3), 367-373 (2002).
- Martin, A., et al. Msh2 ATPase activity is essential for somatic hypermutation at AT basepairs and for efficient class switch recombination. The Journal of Experimental Medicine. 198 (8), 1171-1178 (2003).
- Imai, K., et al. Human uracil-DNA glycosylase deficiency associated with profoundly impaired immunoglobulin class-switch recombination. Nature Immunology. 4 (10), 1023-1028 (2003).
- Masani, S., Han, L., Yu, K. Apurinic/apyrimidinic endonuclease 1 is the essential nuclease during immunoglobulin class switch recombination. Molecular and Cellular Biology. 33 (7), 1468-1473 (2013).
- Guikema, J. E., et al. APE1-and APE2-dependent DNA breaks in immunoglobulin class switch recombination. The Journal of Experimental Medicine. 204 (12), 3017-3026 (2007).
- Schrader, C. E., Guikema, J. E., Wu, X., Stavnezer, J. The roles of APE1, APE2, DNA polymerase β and mismatch repair in creating S region DNA breaks during antibody class switch. Philosophical Transactions of the Royal Society B: Biological Sciences. 364 (1517), 645-652 (2009).
- Roa, S., et al. MSH2/MSH6 complex promotes error-free repair of AID-induced dU: G mispairs as well as error-prone hypermutation of A: T sites. PLoS One. 5 (6), 11182 (2010).
- Delbos, F., Aoufouchi, S., Faili, A., Weill, J. C., Reynaud, C. A. DNA polymerase η is the sole contributor of A/T modifications during immunoglobulin gene hypermutation in the mouse. The Journal of Experimental Medicine. 204 (1), 17-23 (2007).
- Maul, R. W., Gearhart, P. J. AID and somatic hypermutation. Advances in Immunology. 105, 159-191 (2010).
- Shen, H. M., Tanaka, A., Bozek, G., Nicolae, D., Storb, U. Somatic hypermutation and class switch recombination in Msh6-/- Ung-/- double-knockout mice. The Journal of Immunology. 177 (8), 5386-5392 (2006).
- Cheng, H. L., et al. Integrity of the AID serine-38 phosphorylation site is critical for class switch recombination and somatic hypermutation in mice. Proceedings of the National Academy of Sciences. 106 (8), 2717-2722 (2009).
- Lebecque, S. G., Gearhart, P. J. Boundaries of somatic mutation in rearranged immunoglobulin genes: 5'boundary is near the promoter, and 3'boundary is approximately 1 kb from V (D) J gene. The Journal of Experimental Medicine. 172 (6), 1717-1727 (1990).
- Jolly, C. J., Klix, N., Neuberger, M. S. Rapid methods for the analysis of immunoglobulin gene hypermutation: application to transgenic and gene targeted mice. Nucleic Acids Research. 25 (10), 1913-1919 (1997).
- Choi, J. E., Matthews, A. J., Michel, G., Vuong, B. Q. AID Phosphorylation Regulates Mismatch Repair-Dependent Class Switch Recombination and Affinity Maturation. The Journal of Immunology. 204 (1), 13-22 (2020).
- McBride, K. M., et al. Regulation of class switch recombination and somatic mutation by AID phosphorylation. The Journal of Experimental Medicine. 205 (11), 2585-2594 (2008).
- Liu, M., et al. Two levels of protection for the B cell genome during somatic hypermutation. Nature. 451 (7180), 841-845 (2008).
- Ross, M., Birbeck, M., Wills, V., Forrester, J., Davis, A. Peanut lectin binding properties of germinal centers of mouse lymphoid tissues. Nature. 284, 364-366 (1980).
- Zhang, J., MacLennan, I. C., Liu, Y. J., Lane, P. J. Is rapid proliferation in B centroblasts linked to somatic mutation in memory B cell clones. Immunology Letters. 18 (4), 297-299 (1988).
- Nieuwenhuis, P., Opstelten, D. Functional anatomy of germinal centers. American Journal of Anatomy. 170 (3), 421-435 (1984).
- Lau, A. W., Brink, R. Selection in the germinal center. Current Opinion in Immunology. 63, 29-34 (2020).
- Victora, G. D., Nussenzweig, M. C. Germinal centers. Annual Review of Immunology. 30, 429-457 (2012).
- Mesin, L., Ersching, J., Victora, G. D. Germinal center B cell dynamics. Immunity. 45 (3), 471-482 (2016).
- Reichert, R. A., Gallatin, W. M., Weissman, I. L., Butcher, E. C. Germinal center B cells lack homing receptors necessary for normal lymphocyte recirculation. The Journal of Experimental Medicine. 157 (3), 813-827 (1983).
- Rose, M., Birbeck, M., Wills, V., Forrester, J., Davis, A. Peanut lectin binding properties of germinal centers of mouse lymphoid tissues. Nature. 284, 364-366 (1980).
- Hamada, S., Fujita, S. DAPI staining improved for quantitative cytofluorometry. Histochemistry. 79 (2), 219-226 (1983).
- Otto, F. DAPI staining of fixed cells for high-resolution flow cytometry of nuclear DNA. Methods in Cell Biology. 33, 105-110 (1990).
- Butcher, E., et al. Surface phenotype of Peyer's patch germinal center cells: implications for the role of germinal centers in B cell differentiation. The Journal of Immunology. 129 (6), 2698-2707 (1982).
- Rogerson, B. J., Harris, D. P., Swain, S. L., Burgess, D. O. Germinal center B cells in Peyer's patches of aged mice exhibit a normal activation phenotype and highly mutated IgM genes. Mechanisms of Ageing and Development. 124 (2), 155-165 (2003).
- Potapov, V., Ong, J. L. Examining sources of error in PCR by single-molecule sequencing. PloS One. 12 (1), 0169774 (2017).
- Gonzalez-Fernandez, A., Milstein, C. Analysis of somatic hypermutation in mouse Peyer's patches using immunoglobulin kappa light-chain transgenes. Proceedings of the National Academy of Sciences. 90 (21), 9862-9866 (1993).
- Reboldi, A., Cyster, J. G. Peyer's patches: organizing B-cell responses at the intestinal frontier. Immunological Reviews. 271 (1), 230-245 (2016).
- Betz, A. G., Rada, C., Pannell, R., Milstein, C., Neuberger, M. S. Passenger transgenes reveal intrinsic specificity of the antibody hypermutation mechanism: clustering, polarity, and specific hot spots. Proceedings of the National Academy of Sciences. 90 (6), 2385-2388 (1993).
- Rada, C., Gupta, S. K., Gherardi, E., Milstein, C. Mutation and selection during the secondary response to 2-phenyloxazolone. Proceedings of the National Academy of Sciences. 88 (13), 5508-5512 (1991).
- Heise, N., Klein, U. Somatic Hypermutation and Affinity Maturation Analysis Using the 4-Hydroxy-3-Nitrophenyl-Acetyl (NP) System. Methods in Molecular Biology. 1623, 191-208 (2017).
- Smith, F., Cumano, A., Licht, A., Pecht, I., Rajewsky, K. Low affinity of kappa chain bearing (4-hydroxy-3-nitrophenyl) acetyl (NP)-specific antibodies in the primary antibody repertoire of C57BL/6 mice may explain lambda chain dominance in primary anti-NP responses. Molecular Immunology. 22 (10), 1209-1216 (1985).
- Takahashi, Y., Dutta, P. R., Cerasoli, D. M., Kelsoe, G. In situ studies of the primary immune response to (4-hydroxy-3-nitrophenyl) acetyl. V. Affinity maturation develops in two stages of clonal selection. The Journal of Experimental Medicine. 187 (6), 885-895 (1998).
- Allen, D., Simon, T., Sablitzky, F., Rajewsky, K., Cumano, A. Antibody engineering for the analysis of affinity maturation of an anti-hapten response. The EMBO Journal. 7 (7), 1995-2001 (1988).
- Cumano, A., Rajewsky, K. Clonal recruitment and somatic mutation in the generation of immunological memory to the hapten NP. The EMBO Journal. 5 (10), 2459-2468 (1986).
- Smith, K., Nossal, G., Tarlinton, D. M. FAS is highly expressed in the germinal center but is not required for regulation of the B-cell response to antigen. Proceedings of the National Academy of Sciences. 92 (25), 11628-11632 (1995).
- Hao, Z., et al. Fas receptor expression in germinal-center B cells is essential for T and B lymphocyte homeostasis. Immunity. 29 (4), 615-627 (2008).
- Cervenak, L., Magyar, A., Boja, R., László, G. Differential expression of GL7 activation antigen on bone marrow B cell subpopulations and peripheral B cells. Immunology Letters. 78 (2), 89-96 (2001).
- Naito, Y., et al. Germinal center marker GL7 probes activation-dependent repression of N-glycolylneuraminic acid, a sialic acid species involved in the negative modulation of B-cell activation. Molecular and Cellular Biology. 27 (8), 3008-3022 (2007).
- Olson, W. J., et al. Orphan Nuclear Receptor NR2F6 Suppresses T Follicular Helper Cell Accumulation through Regulation of IL-21. Cell Reports. 28 (11), 2878-2891 (2019).
- Dorsett, Y., et al. MicroRNA-155 suppresses activation-induced cytidine deaminase-mediated Myc-Igh translocation. Immunity. 28 (5), 630-638 (2008).
- Goetz, C., Hammerbeck, C., Bonnevier, J. . Flow Cytometry Basics for the Non-Expert. , (2018).
- Hawley, T. S., Herbert, D. J., Eaker, S. S., Hawley, R. G. . Flow Cytometry Protocols. , (2004).
- Costa, E., et al. A new automated flow cytometry data analysis approach for the diagnostic screening of neoplastic B-cell disorders in peripheral blood samples with absolute lymphocytosis. Leukemia. 20 (7), 1221-1230 (2006).
- McKinnon, K. M. Flow cytometry: An overview. Current Protocols in Immunology. 120 (1), 1-11 (2018).
- McKinnon, K. M. Multiparameter Conventional Flow Cytometry. Methods in Molecular Biology. , 139-150 (2018).
- Lucchesi, S., et al. Computational Analysis of Multiparametric Flow Cytometric Data to Dissect B Cell Subsets in Vaccine Studies. Cytometry Part A. 97, 259-267 (2019).
- Longerich, S., Tanaka, A., Bozek, G., Nicolae, D., Storb, U. The very 5' end and the constant region of Ig genes are spared from somatic mutation because AID does not access these regions. The Journal of Experimental Medicine. 202 (10), 1443-1454 (2005).
- Retter, I., et al. Sequence and characterization of the Ig heavy chain constant and partial variable region of the mouse strain 129S1. The Journal of Immunology. 179 (4), 2419-2427 (2007).
- Shen, H. M., Peters, A., Baron, B., Zhu, X., Storb, U. Mutation of BCL-6 gene in normal B cells by the process of somatic hypermutation of Ig genes. Science. 280 (5370), 1750-1752 (1998).
- Richter, K., et al. Altered pattern of immunoglobulin hypermutation in mice deficient in Slip-GC protein. Journal of Biological Chemistry. 287 (38), 31856-31865 (2012).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved