Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Immunology and Infection
Analys av somatisk hypermutation i JH4-intronen i Germinal Center B-celler från Mouse Peyer's Patches
Presenteras här är en analys för att kvantifiera somatisk hypermutation inom immunglobulin tunga kedjan gen locus med germinal centrum B celler från mus Peyers fläckar.
Inom germinal centers av lymfoida organ, mogna B celler ändra deras uttryckt immunglobulin (Ig) genom att införa otemplat mutationer i variabel kodning exons av Ig tunga och lätta kedjan gen lokus. Denna process av somatisk hypermutation (SHM) kräver enzym aktivering-inducerad cytidindeaminas (AID), som omvandlar deoxycytidiner (C), till deoxyuridiner (U). Bearbetning av AID-genererade U:G-missmatchningar i mutationer av basen excision och missmatchning reparation vägar introducerar nya Ig kodning sekvenser som kan producera en högre affinitet Ig. Mutationer i AID- eller DNA-reparationsgener kan blockera eller väsentligt förändra de typer av mutationer som observerats i Ig lokus. Vi beskriver ett protokoll för att kvantifiera JH4 intron mutationer som använder fluorescens aktiverad cell sortering (FACS), PCR och Sanger sekvensering. Även om denna analys inte direkt mäter Ig affinitet mognad, det är vägledande för mutationer i Ig variabel kodning sekvenser. Dessutom använder dessa metoder vanliga molekylärbiologiska tekniker som analyserar mutationer i Ig-sekvenser av flera B-cellkloner. Således är denna analys ett ovärderligt verktyg i studien av SHM och Ig diversifiering.
B-celler, medlemmar av det adaptiva immunsystemet, känner igen och eliminerar antigener genom att producera antikroppar, även kända som immunglobuliner (Ig). Varje Ig består av två tunga (IgH) och två lätta (IgL) kedjepolypeptider, som hålls samman av disulfidbindningar för att bilda den karakteristiska "Y" formstrukturen i Ig1. N-termini av IgH och IgL omfattar variabel (V) regionen för varje polypeptid och tillsammans bildar de antigen bindande platsen för Ig, medan den konstanta regionen IgH ger effektor funktionen av Ig. Utveckla B-celler i benmärgen omorganisera V-kodningsexonerna av IgH och IgL i en process som kallas V(D)J rekombination2,3,4. Transkription av de rekombinerade V-exonerna, i kombination med respektive konstanta region exoner, bildar mRNA som översätts till Ig.
Mogna B-celler som uttrycker en membranbunden Ig, även känd som en B-cellsreceptor (BCR), cirkulerar till sekundära lymfoida organ, såsom mjälte, lymfkörtel eller Peyers fläckar, där de undersöker miljön för antigener och interagerar med andra celler i immunsystemet1. Inom germinala centra (GC) av sekundära lymfoida organ aktiveras B-celler som känner igen antigen genom BCR. Med hjälp av follikulära dendritiska celler och follikulära hjälpare T-celler kan aktiverade B-celler sedan föröka sig och differentiera till plasma- och minnesceller, som är viktiga effektorer av ett robustimmunsvar 5,6,7,8,9. Dessutom kan dessa aktiverade B-celler genomgå sekundära Ig-gendiversifieringsprocesser - klassomkopplarrekombination (CSR) och somatisk hypermutation (SHM). Under CSR utbyter B-celler standard μ konstant region i IgH-polypeptiden med en annan konstant region (γ, α, ε) genom en DNA-deletional-rekombinationsreaktion (Figur 1). Detta möjliggör uttryck av en annan konstant exon och översättning av en ny Ig. B-cellen växlar från att uttrycka IgM till en annan isotyp (IgG, IgA, IgE). CSR ändrar Ig:s effektorfunktion utan att ändra dess antigenspecifikitet10,11,12. Under SHM muterar dock B-cellerna V-kodningsregionerna IgH och IgL för att möjliggöra produktion och val av högre affinitetSgs, vilket mer effektivt kan eliminera ett antigen13,14,15 ( figur1). Viktigt är att både CSR och SHM är beroende av ett enzyms funktion: aktiveringsinducerad cytidindeaminas (AID)16,17,18. Människor och möss som har brist på AID kan inte slutföra CSR eller SHM och presentera med förhöjda IgM serum titers eller Hyper-IgM17,19.
I CSR deaminerar AID deoxycytidiner (C) i de repetitiva switchregionerna som föregår varje konstant kodning exoner, omvandlar dem till deoxyuridiner (U)20,21, vilket skapar omaka basparning mellan deoxyuridin och deoxyguanosiner (U:G). Dessa U:G-missmatchningar omvandlas till de dubbelsträngade DNA-pauserna, som krävs för DNA-rekombination, antingen genom reparation av basexcision (BER) eller mmr-väg22, 23,24,25,26,27,28,29. I SHM deaminerar AID C inom V-kodningsexonerna. Replikering över U:G-missmatchning genererar C:G till T:A övergångsmutationer, medan avlägsnande av uracilbasen av BER-proteinet, uracil DNA glykosylas (UNG), före DNA-replikation ger både övergångs- och transversionsmutationer16. Null mutationer i UNG ökar avsevärt C:G till T:A övergångsmutationer21,22. I likhet med CSR kräver SHM de kompletterande rollerna mmr och ber. Under SHM genererar MMR mutationer vid A:T-baspar. Inaktivera mutationer i MutS homology 2 (MSH2) eller DNA-polymeras η (Polη) minskar signifikant mutationer vid A:T-baser och sammansatta mutationer i MSH2 och Polη avskaffar praktiskt taget mutationer vid A:Tbaser 21,30,31. I överensstämmelse med den kritiska rollen för BER och MMR vid konvertering av AID-genererade U till övergångs- eller transversionsmutationer visar möss som saknar både MSH2 och UNG(MSH2-/-UNG-/-) endast C:G till T:A övergångsmutationer som härrör från replikering över U:G-missmatchningen21.
Analysen av SHM i V-kodningsregioner är fortfarande komplicerad eftersom utveckling av B-celler kan rekombinera någon av V(D)J-kodningsexonerna i IgH och IgL lokus1,2,4. Noggrann analys av dessa unikt rekombinerade och somatiskt muterade V-regioner kräver identifiering och isolering av kloner av B-celler eller Ig mRNA11,13. JH4-intronen, som är 3' av den sista J-kodningsexonen i IgH-locus, hyser somatiska mutationer på grund av spridning av mutationer 3' av V-promotorn32,33,34 och används därför ofta som surrogatmarkör för SHM i V-regionerna31,35 ( Figur1). För att experimentellt klargöra hur specifika gener eller genetiska mutationer förändrar SHM-mönster eller hastigheter kan JH4-intronen sekvenseras från Peyers fläckar (PP) germinala B-celler (GCBCs), som genomgår höga nivåer av SHM36,37,38. GCBC kan lätt identifieras och isoleras med fluorescerande konjugerade antikroppar mot cellytans markörer (B220+PNAHI)17,39.
Ett detaljerat protokoll presenteras för att karakterisera JH4 intronmutationer i PP GCBCs från möss med hjälp av en kombination av FACS (fluorescensaktiverad cellsortering), PCR och Sanger sekvensering (Figur 2).
Alla mutanta möss bibehölls på en C57BL/6 bakgrund. Åldersmatchade (2-5 månader gamla) han- och honmöss användes för alla experiment. Djurhållning och experiment med möss utfördes enligt protokoll som godkänts av The City College of New York Institutional Animal Care and Use Committee.
1. Dissekering av Peyers plåster
- Avliva musen med 100% CO2 vid 3 L/min i 5 min följt av livmoderhalsförskjutning för att bekräfta döden. Sterilisera dissekeringsverktyg (sax, tång, fina tångar) och handskehänder med 70% etanol.
- Lägg musen på dissektionsdynan med buken exponerad. Spraya generöst musens kropp med 70% etanol innan du gör några snitt för att sterilisera dissekeringsområdet.
- Gör ett snitt i huden över buken och ta bort huden från buken genom att dra samtidigt på båda sidor av snittet mot huvudet och svansen med hjälp av tång (eller steriliserade, handske händer).
- Fäst musens för- och bakben.
- Skär den peritoneala håligheten med sax för att exponera de inre organen.
- Lokalisera tunntarmen mellan magen och caecum ("J" formad struktur nära tjocktarmen). Ta bort tunntarmen genom att skära under magen och ovanför caecum.
- Ta bort eventuell bindväv och fett som länkar ihop tunntarmens veck.
OBS: Fett kommer att ha en distinkt vit färg, till skillnad från tunntarmens rosa färg. - Undersök tunntarmens yttre yta för Peyers fläckar (PPs), som är små (~ 1 mm), ovala strukturer som verkar vita under ett tunt lager genomskinliga epitelceller.
- Punktskatt försiktigt alla synliga PP med sax.
OBS: En C57BL/6 WT-mus (wild-type) kan ge 4-8 PPs, medan en AID-/- mus kommer att ha 6-10 PPs. - Samla PPs i ett 1,5 mL mikrocentrifugrör som innehåller 1 ml FACS-buffert på is.
OBS: PP bör sjunka, medan fett kommer att flyta till ytan och kan avlägsnas.
2. Cellisolering för FACS
- Placera ett 40 μm filter i en 6-brunns skål med 1 ml kall (4 °C) FACS-buffert.
- Häll PPs från 1,5 ml-röret på filtret.
- Tvätta PPs med 1 ml kall FACS-buffert, se till att de alltid är i vätska och på is.
- Använd kolvens plana ände från en 1 ml spruta som mortel för att krossa PPs på filtret tills endast bindväv finns kvar på filtret.
- Tvätta filtret och kolven med 1 ml kall FACS-buffert för att frigöra cellerna i 6-brunnsskålen.
- Samla upp ~4 ml celler i kall FACS-buffert och filtrera dem genom ett FACS-rör på 40 μm sillock.
- Tvätta sillocket med 1 ml kall FACS-buffert.
- Pellet cellerna vid 600 x g vid 4 °C i 5 min i en svängande hink centrifug.
- Dekanta supernaten.
- Återanvänd cellerna i 0,4 ml kall FACS-buffert.
- Ta bort 10 μL för cellräkning för att verifiera utbyte (förvänta dig ~5 x 106 celler/mus, se figur 3A)
- Filtrera de återstående cellerna genom ett 40 μm sillock i ett FACS-rör och fortsätt till färgning för FACS.
3. Färgning av GCBCs för FACS
- Tillsätt 1 μL Fc-block (omärkt antimus-CD16/CD32) till 400 μL-cellupphängningen och placera cellerna på is i 15 minuter.
- Tillsätt 2 ml kall FACS-buffert för att tvätta cellerna.
- Pelletsceller vid 600 x g vid 4 °C i 5 min och kassera supernatanten.
- Återanvänd cellerna i 80 μL kall FACS-buffert.
- Ta bort 10 μL celler från WT PP för varje färgningskontroll (4 totalt, inklusive 3 enfläckskontroller och 1 obefläckad kontroll). Lämna 40 μL WT PP i nästa steg. Alternativt kan du använda kompensationspärlor för färgningsreglagen.
- Färga var och en av de experimentella proverna (t.ex. WT och AID-/-) i 500 μL kall FACS-buffert med 2,5 μL jordnötsagglutinin (PNA)-biotin i 15 minuter på is.
- Tillsätt 2 ml kall FACS-buffert för att tvätta cellerna.
- Pelletsceller vid 600 x g vid 4 °C i 5 min och kassera supernatanten.
- Färga varje experimentellt prov med 500 μL av cocktailen i mörker, på is, i 15 minuter (tabell 1). Se till att cellerna är helt återanvända i färgcocktailen.
- Förbered kontroller med en fläck för kompensationsmatrisen.
- Färga cellerna i 500 μL kall FACS-buffert med de utspädningar som anges i tabell 2.
- Inkubera färgkontrollerna i mörkret, på isen, i 15 minuter.
- Tillsätt 2 ml kall FACS-buffert till alla rör i steg 3.7 och 3.8, pelleta cellerna och kassera supernatanten för att tvätta bort obundna antikroppar eller DAPI.
- Återanvänd cellerna i 500 μL kall FACS-buffert och lägg på is.
- Använd en cellsortering och samla in B220+PNAHI från varje färgat experimentellt prov. Figur 3B visar de typiska procentsatserna för B220+ PNAHI som erhållits från WT och AID-/- PPs. Figur 3C visar FACS-gating-strategin.
4. DNA-extraktion från GCBCs
- Pelletssorterade celler vid 600 x g vid 4 °C i 5 min och kassera supernatanten.
- Återanvänd cellerna i 1 ml kall FACS-buffert och överför cellerna till ett 1,5 ml mikrocentrifugrör.
- Pellet cellerna vid 600 x g vid 4 °C i 5 min och kassera supernaten.
- Återanvänd cellerna i 500 μL DNA-extraktionsbuffert och 5 μL 20 mg/ml proteinas K.
- Inkubera vid 56 °C över natten.
- Fäll ut DNA med 500 μL isopropanol och 1 μL 20 mg/mL glykogen. Blanda röret noggrant genom att invertera 5-6x.
- Inkubera i rumstemperatur i 10 min.
- Centrifug i mikrocentrifug i 15 min vid 25 °C vid 21 000 x g.
- Kassera supernatanten och behåll pelleten, som innehåller utfällt DNA och glykogen.
- Tvätta DNA-pelleten med 1 ml 70% etanol.
- Pellet DNA i en mikrocentrifug i 10 min vid 25 °C vid 21 000 x g.
- Ta bort 70% etanol och lufttorka DNA-pelleten i 5-10 min.
OBS: Undvik övertorkning eftersom DNA:t kanske inte återfuktas helt.
- Återanvänd DNA i 30 μL TE-buffert och inkubera över natten vid 56 °C.
5. JH4 intronsekvensförstärkning och analys
- Kvantifiera DNA genom att mäta absorbansen vid en våglängd på 260 nm (A260).
OBS: Den typiska koncentrationen av DNA som återvinns från sorterade B220+PNAHI GCBCs av en C57BL/6-mus är 20-40 ng/μL. - Utför den kapslade PCR:n för JH4-intronen(tabell 3, tabell 4). Normalisera den totala mängden genomiskt DNA som används i det första PCR till det minst koncentrerade provet. (t.ex. om det minst koncentrerade provet är 5 ng/μL, använd 58,75 ng DNA för alla prover i den maximala vattenvolymen (11,75 μL) i PCR-#1).
- Lös PCR-produkten på en 1,5% agarose gel vid 200 V i 20 min. Den förväntade ampliconstorleken är 580 bp.
- Ta bort ampliconen från gelén och extrahera DNA:t med hjälp av ett gelextraktionskit enligt tillverkarens instruktioner (se kompletterande figur 1).
- Eluera DNA:t med 30 μL vatten och kvantifiera mängden DNA genom att mäta A260.
OBS: Den typiska koncentrationen av den renade PCR-produkten är 3-10 ng/μL.
- Eluera DNA:t med 30 μL vatten och kvantifiera mängden DNA genom att mäta A260.
- Ligate den renade PCR-produkten till en plasmid med trubbiga ändar. Standardisera den totala mängden PCR-produkt som används vid varje ligaturreaktion (tabell 5).
- Inkubera ligaturreaktionen vid rumstemperatur i 5 min eller över natten vid 16 °C.
- Omvandla elektrokompetenta bakterieceller med 2 μL av ligationsreaktionen.
- Elektroporat vid 1,65 kV.
- Räddning i 600 μL SOC-media i 1 timme vid 37 °C i en skakande inkubator vid 225 varv/min.
- Plåt 100 μL omvandlade bakterier till LB kompletterad med ampicillin (100 μg/ml) agarplattor och inkubera över natten vid 37 °C.
- Skicka in plattan av bakteriekolonier för Sanger-sekvensering med T7 framåt primer. Alternativt odla över natten kulturer av varje bakteriell koloni och utföra en plasmid rening.
- Upprepa vid behov PCR, ligatur och/eller omvandling för att optimera utbytet av bakteriekolonier
OBS: Minst 30 kolonier bör plockas från varje tallrik.
- Upprepa vid behov PCR, ligatur och/eller omvandling för att optimera utbytet av bakteriekolonier
- Standardisera sekvensdata i .txt filer
- Ta bort plasmidsekvensen.
- Se till att varje sekvens är orienterad 5' till 3' enligt JH4 intron referenssekvensen (NG_005838). Generera det omvända komplementet av alla sekvenser vid behov.
- Justera de sekvenser som erhålls för varje PCR mot JH4-referenssekvensen (NG_005838) med hjälp av en Clustal Omega-programvara (Figur 4A).
- Identifiera skillnader från referenssekvensen som mutationer
- Kontrollera att alla mutationer är sanna punktmutationer genom att undersöka elektrosfärogrammet i Sanger-sekvenseringen. Upprepa sekvenseringen om det behövs. (Figur 4B,C).
- Tabulera och kvantifiera unika mutationer i JH4-intronen för varje genotyp (figur 5).
- Räkna sekvenser med identiska mutationer endast en gång
OBS: Det är inte möjligt att avgöra om de identiska sekvenserna genererades under PCR- eller identiska SHM-händelser i olika B-celler. - Räkna varje instans av WT-könsceller JH4 intron sekvenser (dvs. de utan mutationer) som en unik sekvens.
- Räkna sekvenser med identiska mutationer endast en gång
Flödescytometri
Mogna B-celler cirkulerar till germinala centra där de genomgår affinitetsmognad, klonurexpansion och differentiering i plasma- ellerminnesceller 40,41,42,43,44. Dessa GCBCs kan identifieras av många cell ytmarkörer, inklusive högt uttryck för CD45R/B220 receptorn och bindning av jordnöts agglutinin (PNA)45,46. För att isolera aktiverade GCBCs var PP-celler färgade med anti-B220 antikroppar konjugerade till phycoerythrin (PE) och biotinylated-PNA, följt av streptavidin konjugerade till APC-eFluor780. Döda celler eliminerades med fluorescerande 4',6-Diamidino-2-Phenylindole (DAPI) färgämne, som fläckar nukleinsyran av döende eller döda celler47,48. De färgade cellerna analyserades och sorterades därefter via flöde cytometri. PPs bestod av ~80% B220+ celler49,50. WT PPs innehåller i genomsnitt 4 x 106 celler per mus (Figur 3A). Ungefär 8% av WT PP-cellerna var B220+PNAHI, vilket är hälften av det antal som observerats i AID-/ - ( Figur3B). Således erhölls 0,3-0,6 x 106 B220+PNAHI GCBCs efter sortering, som var tillräckliga för att analysera mutationer i JH4 intron.
JH4-sekvensanalys
JH4-intronen förstärktes av en kapslad PCR med vanliga VHJ558-familjens primers (J558FR3Fw och VHJ558.2) följt av JH4 intron som spänner över primers VHJ558.3 och VHJ558.435,37. Av de 105 unika sekvenser som erhållits från WT GCBCs hittades totalt 226 mutationer (figur 5A). Analys av GCBC mutationsspektrum i WT möss visade en rad övergångar och omvandlingar med en hastighet av 4 x 10-3 mutationer/bp, som beräknades genom att dividera det totala antalet muterade baser med det totala antalet baser som varsekvenserade 32,36,37,38. Dessutom innehöll varje JH4 PCR-produkt från WT GCBCs 1-25 mutationer (Figur 5B), där flera mutationer ofta hittades på ensekvens 33,36. Endast två mutationer identifierades i 113 AID-/- sekvenser ( Figur5A). AID-/- B-celler uppvisade 1,66 x 10-5 mutationer/bp, vilket var betydligt lägre än WT B-celler (p <0,05)36 och kan jämföras med felfrekvensen för polymeras med hög återgivning (5,3 x 10-7 sub/bas/fördubbling)51,52. Således fungerade AID-/- B-celler som en användbar negativ kontroll för denna analys.
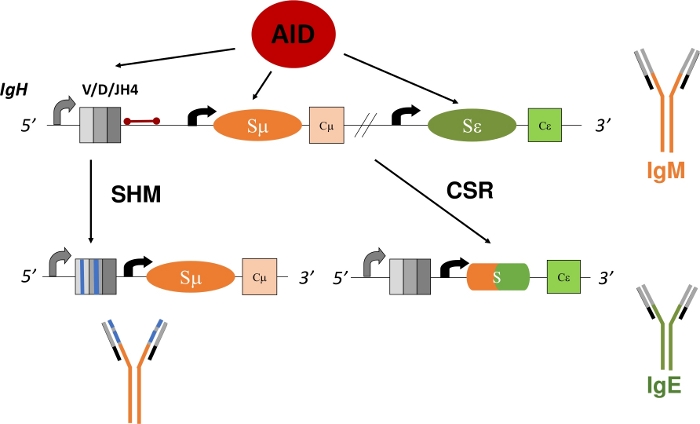
Figur 1: Schematisk för genloket IgH och de regioner som AID riktar in sig på under CSR och SHM. Den röda stapeln anger den 580 bp JH4 intron som är 3' av VDJH4 omorganiseringar och analyseras i detta protokoll. I CSR främjar AID-beroende deamination av intronic switch-regioner (Sμ och Sε) DSB-bildandet som möjliggör deletional-rekombination och uttryck för en ny antikroppsisottyp (IgM till IgE). Under SHM ackumulerar V-regioner (grå lådor) mutationer (blå linjer) som kan leda till högre affinitet Ig. Klicka här om du vill visa en större version av den här figuren.
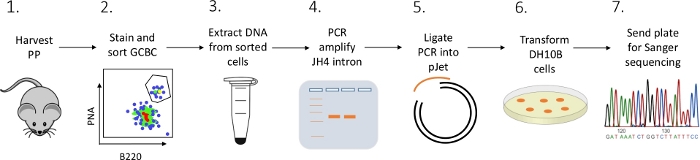
Bild 2: Arbetsflöde för att analysera SHM för JH4-intronen i GCBCs som isolerats från PPs. Klicka här om du vill visa en större version av den här figuren.
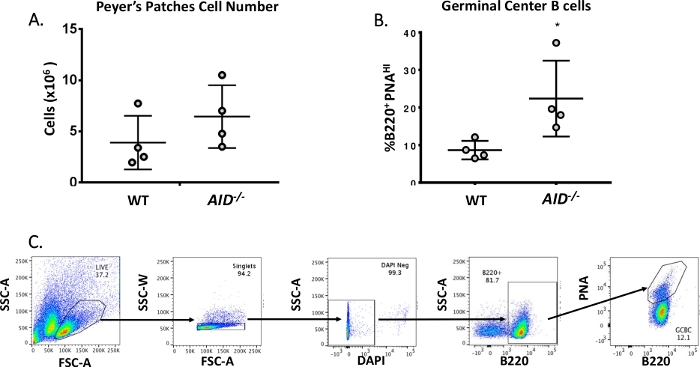
Figur 3: Karakterisering av PP GCBCs. (A) Totalt antal PP-celler från WT och AID-/- möss (n = 4 per genotyp). Felstaplar representerar standardavvikelse från medelvärdet. B)Procentandel B220+PNAHI GCBCs erhållna från PPs av WT och AID-/- möss (n = 4 per genotyp)36. Felstaplar representerar standardavvikelse från medelvärdet , * p<0.05 med hjälp av deltagarens t-test. (C) Representativa FACS-tomter för att sortera B220+PNAHI GCBCs från datorer. Klicka här för att se en större version av denna siffra.
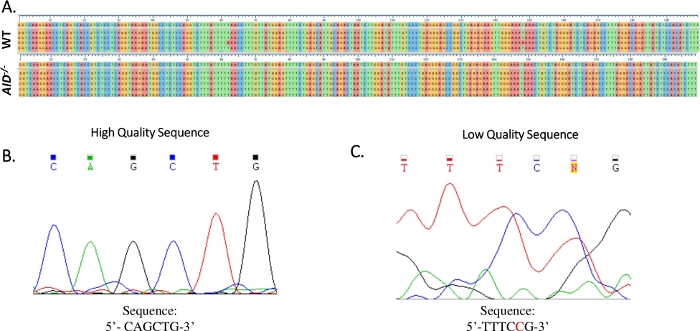
Figur 4: Analys av JH4 Sanger-sekvensdata. (A) Provsekvensjusteringar av Sanger-sekvensdata för JH4 PCR-produkten från WT (överst) och AID-/- (nedre) GCBCs till referensgenomsekvensen (NG_005838), som är sekvensen omedelbart under de numrerade skalstrecken. Inriktningar genererades med hjälp av Clustal Omega. (B) Elektrosfärogram av högkvalitativa Sanger-sekvensdata, som visade distinkta toppar för varje bas. (C) Elektrosfärogram av lågkvalitativa sekvensdata, som visade tvetydiga toppar och ospecificerade baser (N). Nukleotid som visas i rött måste kommenteras manuellt i sekvenstextfilen. Klicka här om du vill visa en större version av den här figuren.
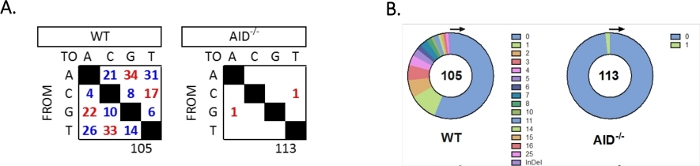
Figur 5: Analys av mutationer i JH4-intronen i WT och AID-/- GCBCs. (A) Det totala antalet övergångsmutationer (röda) och transversionsmutationer (blå) vid A-, C-, G- och T-baser för varje genotyp sammanfattas i tabellerna. Det totala antalet analyserade sekvenser anges under tabellen. (B) Antalet mutationer per PCR-amplicon för varje genotyp visas i cirkeldiagrammen. Denna siffra har ändrats från Choi et al.36 Copyright 2020. American Association of Immunologists, Inc. Klicka här för att se en större version av denna siffra.
| Färgningscocktail för GCBCs | Volym: 500 μL | ||
| Antikropp eller färgämne | Fluorofor | Utspädning | Μl |
| B220 (B220) | Pe | 1000 | 0.5 |
| Streptavidin (streptavidin) | APC-eFluor780 | 500 | 1 |
| DAPI (dapi) | Ej tillämpligt | 500 | 1 |
Bord 1: Färgning av cocktails för GCBCs. Cocktail av de angivna antikropparna eller färgämnet (indikerat i klystik) vid de angivna utspädningarna användes för att färga PP-celler i 500 μL för flödescytometri.
| Enstaka fläckar för ersättning | Volym: 500 μL | ||
| Antikropp eller färgämne | Fluorofor | Utspädning | Μl |
| B220 (B220) | Pe | 1000 | 0.5 |
| B220 (B220) | APC-eFluor780 | 750 | 0.67 |
| DAPI (dapi) | Ej tillämpligt | 500 | 1 |
Tabell 2: Kontroller med en fläck mot ersättning. B220 antikroppar konjugerade till de angivna fluorforerna användes för enfärgade kontroller för att kompensera för spektral överlappning.
| PCR-#1 | ||||
| Reagens | Volym | Termocyklistförhållanden | ||
| 5x buffert | 4 μL | 1 | 95 °C | 3 min |
| 10 mM dNTP | 2 μL | 2 | 94 °C | 30 sek |
| 10 μM J558FR3Fw | 1 μL | 3 | 55 °C | 30 sek |
| 10 μM VHJ558,2 | 1 μL | 4 | 72 °C | 1:30 min |
| DNA-polymeras med hög trohet | 0,25 μL | Cykel 2-4 9x | ||
| Dna | x (standardisera till minst koncentrerat prov) | |||
| H2O | till 20 μL | 5 | 72 °C | 5 min |
| Späd PCR-produkt 1:5 i H2O innan du fortsätter till PCR-#2 | ||||
Tabell 3: Kapslad PCR för JH4-intronen. PCR-komponenter och termocyklistförhållanden för den första förstärkningsreaktionen. Späd ut den första PCR-produkten 1:5 med vatten och använd 1 μL av denna utspädning för den andra PCR.
| PCR-#2 | ||||
| Reagens | Volym | Termocyklistförhållanden #2 | ||
| 5x buffert | 4 μL | 1 | 94 °C | 3 min |
| 10 mM dNTP | 2 μL | 2 | 94 °C | 30 sek |
| 10 μM VHJ558,3 | 1 μL | 3 | 55 °C | 30 sek |
| 10 μM VHJ558,4 | 1 μL | 4 | 72 °C | 30 sek |
| DNA-polymeras med hög trohet | 0,25 μL | Cykel 2-4 21x | ||
| Utspädd PCR #1 | 1 μL | |||
| H2O | till 20 μL | 5 | 72 °C | 5 min |
Tabell 4: PCR-komponenter och termocyklistförhållanden för den andra PCR.Table 4: PCR components and thermocycler conditions for the second PCR.
| Reagens | Volym |
| 2x buffert | 10 μL |
| Renad PCR | x (standardisera till minst koncentrerat prov) |
| Plasmid med trubbiga ändar | 1 μL |
| T4 DNA-liga | 1 μL |
| H2O | till 20 μL |
| Inkubera vid rumstemperatur i 5 min eller över natten vid 16ºC | |
Tabell 5: Ligationsreaktion. Komponenter för ligatur av den renade JH4 intron PCR-produkten i plasmiden.
| FACS-buffert |
| Värm inaktivera FBS vid 56 °C i en timme före användning. Tillägg PBS, pH 7,4 (Gibco, #10010049) med 2,5% (v/v) värmeinaktiverade FBS. Förvara vid 4°C. |
| DNA-extraktionsbuffert (100 mM Tris pH 8,0, 0,1 M EDTA, 0,5% (w/v) SDS) |
| Tillsätt 50 ml 1 M Tris pH 8,0, 100 mL 0,5 M EDTA och 12,5 ml 20% SDS. Tillsätt destillerat vatten till 500 ml. Förvara i rumstemperatur. |
| TE-buffert (10 mM Tris pH 8,0, 1 mM EDTA) |
| Tillsätt 2,5 ml 1 M Tris pH 8,0 och 500 ml 0,5 M EDTA. Tillsätt destillerat vatten till 250 ml. Förvara i rumstemperatur. |
Tabell 6: Buffertrecept.
| Oligonukleotider Lista | ||
| J558FR3Fw | 5'-GCCTGACATCTGAGGACTCTGC-3' | |
| VHJ558.2 | 5'-CTGGACTTTCGGTTTGGTG-3' | |
| VHJ558.3 | 5'-GGTCAAGGAACCTCAGTCA-3' | |
| VHJ558,4 | 5'-TCTCTAGACAGCAACTAC-3' | |
Tabell 7: Oligonukleotider som används i analysen.
Kompletterande figur 1: Representativ agarosgelbild efter avslutad steg 5.4. JH4 intron kapslade PCR produkt löstes på en 1,5% agarose gel och 580 bp amplicon var strukits. WT PP indikerar att WT PP GCBC genomiskt DNA användes som mall för den första PCR och AID PP indikerar att AID-/- PP GCBC genomiskt DNA användes som mall för den första PCR. ɸ indikerar ingen mall PCR-kontroll och - indikerar att ingenting laddades i agarosegelens brunn. Det sista körfältet visar en DNA-stege på 100 bp. Klicka här för att ladda ner den här siffran.
Karakterisering av SHM inom IgH- och IgL V-kodningssekvenserna för en heterogen B-cellpopulation utgör en utmaning, med tanke på att varje B-cell unikt omorganiserar V-kodningssegment under V(D)J-rekombination34. I detta dokument beskriver vi en metod för att identifiera mutationer i JH4 intron av GCBCs. JH4-intronen, som ligger 3' av det sista J-kodningssegmentet i IgH-locus, används som surrogat för SHM i V-regioner(figur 1)31,33,34,35. För att katalogisera dessa JH4 intronmutationer och bedöma hur specifika gener påverkar produktionen eller mönstret av mutationer analyseras PP GCBCs specifikt. Dessa celler ackumulerar JH4 intronmutationer som ett resultat av kronisk stimulering av intestinala mikrobiota53. Dessutom har B220+PNAHI GCBCs från PPs av oimmuniserade möss ett mutationsspektra som jämförs med splenic GCBCs från immuniserade djur54,55. Mutationer i JH4 intron kan dock inte korreleras till Ig affinity mognad eftersom dessa mutationer är icke-kodning.
För att avgöra om SHM förändrar Ig-affiniteten bör möss immuniseras intraperitoneally med ett antigen, såsom NP (4-hydroxy-3-nitrophenylacetyl) konjugerat till CGG (kyckling gamma globulin) eller KLH (nyckelhål limpet hemocyanin)56. Därefter kan mRNA renas från mjält B220+PNAHI GCBCs för att undersöka SHM inom VH186.2, V-kodningsexon som oftast känner igen NP och muteras efter NP-CGG eller NP-KLH immunisering31,57,58,59,60. Mutation av tryptofan-33 till en leucin i VH186.2 har karakteriserats för att öka Ig affinitet upp till 10-faldiga59,60 och är därför en indikator på att SHM och klonurvalet har genererat hög affinitet Ig. Mätning av NP7- och NP20-specifika serum Ig-titrar av ELISA och beräkning av det Ig-specifika NP7/NP20-förhållandet under immuniseringens gång dokumenterar också Ig affinitetsmognad till följd av SHM iV-regionerna 17,21,36. Båda dessa analyser kan användas för att korrelera SHM inom VH186.2 kodningssekvenser med förändringar i NP-specifik Ig affinity mognad.
Oavsett om immuniserade eller oimmuniserade djur används för att analysera SHM av VH186.2 eller JH4 intron, måste GCBCs identifieras noggrant. Vi presenterar en FACS-baserad metod för att isolera B220+PNAHI GCBCs. Alternativt kan fas och icke-sulfaterad α2-6-sialyl-LacNAc-antigen, som känns igen av GL7-antikroppen61,62,63,64, också användas för att isolera GCBCs, som identifieras som B220+Fas+GL7+65 eller CD19+Fas+GL7+37. GL7 uttryck speglar nära PNA i aktiverade GCBCs av lymfkörtlarna64,65,66. Förutom att använda antikroppsmarkörer som är specifika för GCBCs, bör färgcocktails maximera excitationen av en fluorofor och detektion av en biomarkör samtidigt som spektral överlappning av fluorescensutsläpp minimeras. Antigener uttryckta vid låga nivåer bör detekteras med en antikropp som konjugeras till en fluorfor med en robust emissionsfluorescens67. Det rekommenderade färgningsprotokollet optimerades för analys på en cellsorterare utrustad med fyra lasrar (405nm, 488nm, 561nm, 633nm) och 12 filter; Filterkonfigurationer och lasertillgänglighet varierar dock mellan cytometrar. För att ändra protokollet enligt reagens och utrustningstillgänglighet hänvisas läsaren till ytterligare resurser, onlinespektrumvisare och publiceradlitteratur 67,68,69,70,71,72,73. Det flerfärgsfärgningsprotokoll som beskrivs häri kräver ersättning för spektral överlappning för att säkerställa att de sorterade cellpopulationerna är GCBC snarare än felaktig upptäckt av fluorescensutsläpp. B220 fungerar som en användbar färgningskontroll för de beskrivna FACS (tabell 1B) eftersom PPs kommer att ha distinkta B220 negativa och positiva populationer (figur 3C), vilket möjliggör lämplig ersättning av spektralöverlappning. Den gatingstrategi som presenteras i figur 3C bör användas som riktlinje. Flödescytometridiagrammen kan variera beroende på färgningsförhållandena och cytometerinställningarna. Ändå bör 4-10% av levande celler vara B220+PNAHI 35, 52.
Alla mutationer inom JH4 intron av PP GCBCs måste valideras för att säkerställa att de observerade mutationerna verkligen återspeglar SHM och inte en artefakt av PCR eller sekvensering. AID-/- B-celler kan fungera som en användbar negativ kontroll när man undersöker SHM fenotyp i andra mutanta musmodeller eftersom dessa celler inte kan slutföra SHM17,19. JH4 intron mutationshastighet i AID-/- GCBCs (1.66x10-5 mutationer/bp)20,21,36,37,38,50är74 jämförbar med felfrekvensen för polymeras med hög återgivning (5,3x10-7 sub/base/doubling)51,52 som används för att förstärka DNA i det kapslade PCR. Om AID-/- möss inte är tillgängliga, jämför det observerade mutationsmönstret och frekvensen med den publicerade litteraturen. Ig V-regioner ackumulerar 10-3 -10-4 mutationer per baspardelning, vilket är ungefär 106gånger högre än mutationshastigheten hos andra gen lokus73,75. Resultaten kan variera med djurets ålder76. Alternativt kan B220+PNALO-celler, som markerar icke-GCBCs, användas som en negativ kontroll i avsaknad av AID-/- möss52. Om mutationsfrekvensen i WT GCBCs är lägre än förväntat kan WT-bakterien JH4 intronic sekvensen vara oproportionerligt representerad. I detta fall, se till att GCBCs färgades och sorteras på lämpligt sätt och PCR är fria från WT-bakterien JH4 intron kontaminering. Dessutom bör råsekvenseringsdata i elektrosfärogram analyseras noggrant för att säkerställa att mutationer i sekvenstextdata inte är artefakter av sekvenseringsfel. Till exempel kan dåliga Sanger-sekvenseringsresultat minska tillförlitligheten hos sekvensdata (figur 4). Denna kvalitetskontroll av Sanger-sekvensdata kommer att öka noggrannheten och reproducerbarheten av JH4-intronmutationsanalysen.
Författarna har inget att avslöja.
Vi tackar Tasuku Honjo för AID-/- möss. Detta arbete stöddes av National Institute on Minority Health and Health Differences (5G12MD007603), National Cancer Institute (2U54CA132378) och National Institute of General Medical Sciences (1SC1GM132035-01).
| Name | Company | Catalog Number | Comments |
| 0.2 ml PCR 8-tube FLEX-FREE strip, attached clear flat caps, mixed | USA Scientific | 1402-4708 | |
| Ampicillin sodium salt | Fisher | BP1760-5 | |
| APC-eFluor780 anti-CD45R/B220 | eBioscience | 47-0452-80 | clone RA3-6B2 |
| BD FACSAria II | BD | 643186 | four lasers (405nm, 488nm, 561nm, 633nm) and 12 filters (PacBlue (450/50), AmCyan (502LP; 530/30), SSC (488/10), FITC (502LP; 530/30), PerCP-Cy5.5 (655LP; 695/40), PE (585/15), PE-Texas Red (600LP; 610/20), PE-Cy5 (630LP; 670/14), PE-Cy7 (735LP; 780/60), APC (660/20), Alexa700 (710LP; 730/45), APC-Cy7 (755LP; 780/60)) |
| BD slip tip 1mL syringe | Fisher | 14-823-434 | sterile |
| Biotinylated peanut agglutinin (PNA) | Vector Labs | B-1075-5 | |
| C57BL/6J mice | Jackson Laboratories | 664 | |
| Corning Falcon test tube with cell strainer snap cap | Fisher | 08-771-23 | |
| DAPI (4',6-Diamidino-2-Phenylindole, dihydrochloride) | Fisher | D1306 | 0.5 mg/ml |
| dNTP | NEB | N0447L | 10 mM |
| ElectroMAX DH10B competent cells | Fisher | 18-290-015 | |
| Falcon cell strainer 40mm | Fisher | 08-771-1 | |
| Falcon round-bottom polystyrene tubes (FACS tubes) | Fisher | 14-959-5 | |
| Falcon round-bottom polystyrene tubes (capped) | Fisher | 149591A | |
| Fetal bovine serum | R&D Systems (Atlanta Biologicals) | S11150 | |
| Gibco phosphate buffered saline PBS pH 7.4 | Fisher | 10-010-049 | |
| Glycogen | Sigma | 10901393001 | |
| Lasergene Molecular Biology (MegAlign Pro) | DNA Star | version 15 | |
| PE anti-CD45R/B220 | BD | 553090 | clone RA3-6B2 |
| Proteinase K | Fisher | BP1700-100 | |
| Q5 High-Fidelity DNA Polymerase | NEB | M0491L | |
| QIAquick Gel Extraction Kit | Qiagen | 28706 | |
| Seal-Rite 1.5mL microcentrifuge tubes | USA Scientific | 1615-5500 | |
| Streptavidin APC-eFluor 780 Conjugate | eBioscience | 47-4317-82 | |
| T4 DNA ligase | NEB | M020L | |
| Thermo Scientific CloneJET PCR Cloning Kit | ThermoFisher | FERK1231 | |
| Tissue culture plate 6 well | Fisher | 08-772-1B | sterile |
| Unlabeled anti-mouse CD16/CD32 (Fc block), BD | Fisher | BDB553142 | Clone 2.4G2 |
- Murphy, K., Weaver, C. . Janeyway's Immunobiology. , (2016).
- Alt, F. W., et al. VDJ recombination. Immunology Today. 13 (8), 306-314 (1992).
- Schatz, D. G., Ji, Y. Recombination centres and the orchestration of V (D) J recombination. Nature Reviews Immunology. 11 (4), 251-263 (2011).
- Oettinger, M. A., Schatz, D. G., Gorka, C., Baltimore, D. RAG-1 and RAG-2, adjacent genes that synergistically activate V (D) J recombination. Science. 248 (4962), 1517-1523 (1990).
- Berek, C., Berger, A., Apel, M. Maturation of the immune response in germinal centers. Cell. 67 (6), 1121-1129 (1991).
- Linterman, M. A., et al. Foxp3+ follicular regulatory T cells control the germinal center response. Nature Medicine. 17 (8), 975 (2011).
- Shulman, Z., et al. T follicular helper cell dynamics in germinal centers. Science. 341 (6146), 673-677 (2013).
- Good-Jacobson, K. L., et al. PD-1 regulates germinal center B cell survival and the formation and affinity of long-lived plasma cells. Nature Immunology. 11 (6), 535 (2010).
- Kerfoot, S. M., et al. Germinal center B cell and T follicular helper cell development initiates in the interfollicular zone. Immunity. 34 (6), 947-960 (2011).
- Chaudhuri, J., Alt, F. W. Class-switch recombination: interplay of transcription, DNA deamination and DNA repair. Nature Reviews Immunology. 4 (7), 541-552 (2004).
- Alt, F. W., Zhang, Y., Meng, F. L., Guo, C., Schwer, B. Mechanisms of programmed DNA lesions and genomic instability in the immune system. Cell. 152 (3), 417-429 (2013).
- Xu, Z., Zan, H., Pone, E. J., Mai, T., Casali, P. Immunoglobulin class-switch DNA recombination: induction, targeting and beyond. Nature Reviews Immunology. 12 (7), 517-531 (2012).
- Di Noia, J. M., Neuberger, M. S. Molecular mechanisms of antibody somatic hypermutation. Annual Reviews of Biochemistry. 76, 1-22 (2007).
- Peled, J. U., et al. The biochemistry of somatic hypermutation. Annual Review of Immunology. 26, 481-511 (2008).
- Liu, M., Schatz, D. G. Balancing AID and DNA repair during somatic hypermutation. Trends in Immunology. 30 (4), 173-181 (2009).
- Methot, S., Di Noia, J. Molecular Mechanisms of Somatic Hypermutation and Class Switch Recombination. Advances in Immunology. 133, 37-87 (2017).
- Muramatsu, M., et al. Class switch recombination and hypermutation require activation-induced cytidine deaminase (AID), a potential RNA editing enzyme. Cell. 102 (5), 553-563 (2000).
- Petersen-Mahrt, S. K., Harris, R. S., Neuberger, M. S. AID mutates E. coli suggesting a DNA deamination mechanism for antibody diversification. Nature. 418 (6893), 99 (2002).
- Revy, P., et al. Activation-induced cytidine deaminase (AID) deficiency causes the autosomal recessive form of the Hyper-IgM syndrome (HIGM2). Cell. 102 (5), 565-575 (2000).
- Petersen-Mahrt, S. DNA deamination in immunity. Immunological Reviews. 203 (1), 80-97 (2005).
- Rada, C., Di Noia, J. M., Neuberger, M. S. Mismatch recognition and uracil excision provide complementary paths to both Ig switching and the A/T-focused phase of somatic mutation. Molecular Cell. 16 (2), 163-171 (2004).
- Rada, C., et al. Immunoglobulin isotype switching is inhibited and somatic hypermutation perturbed in UNG-deficient mice. Current Biology. 12 (20), 1748-1755 (2002).
- Schrader, C. E., Vardo, J., Stavnezer, J. Role for mismatch repair proteins Msh2, Mlh1, and Pms2 in immunoglobulin class switching shown by sequence analysis of recombination junctions. The Journal of Experimental Medicine. 195 (3), 367-373 (2002).
- Martin, A., et al. Msh2 ATPase activity is essential for somatic hypermutation at AT basepairs and for efficient class switch recombination. The Journal of Experimental Medicine. 198 (8), 1171-1178 (2003).
- Imai, K., et al. Human uracil-DNA glycosylase deficiency associated with profoundly impaired immunoglobulin class-switch recombination. Nature Immunology. 4 (10), 1023-1028 (2003).
- Masani, S., Han, L., Yu, K. Apurinic/apyrimidinic endonuclease 1 is the essential nuclease during immunoglobulin class switch recombination. Molecular and Cellular Biology. 33 (7), 1468-1473 (2013).
- Guikema, J. E., et al. APE1-and APE2-dependent DNA breaks in immunoglobulin class switch recombination. The Journal of Experimental Medicine. 204 (12), 3017-3026 (2007).
- Schrader, C. E., Guikema, J. E., Wu, X., Stavnezer, J. The roles of APE1, APE2, DNA polymerase β and mismatch repair in creating S region DNA breaks during antibody class switch. Philosophical Transactions of the Royal Society B: Biological Sciences. 364 (1517), 645-652 (2009).
- Roa, S., et al. MSH2/MSH6 complex promotes error-free repair of AID-induced dU: G mispairs as well as error-prone hypermutation of A: T sites. PLoS One. 5 (6), 11182 (2010).
- Delbos, F., Aoufouchi, S., Faili, A., Weill, J. C., Reynaud, C. A. DNA polymerase η is the sole contributor of A/T modifications during immunoglobulin gene hypermutation in the mouse. The Journal of Experimental Medicine. 204 (1), 17-23 (2007).
- Maul, R. W., Gearhart, P. J. AID and somatic hypermutation. Advances in Immunology. 105, 159-191 (2010).
- Shen, H. M., Tanaka, A., Bozek, G., Nicolae, D., Storb, U. Somatic hypermutation and class switch recombination in Msh6-/- Ung-/- double-knockout mice. The Journal of Immunology. 177 (8), 5386-5392 (2006).
- Cheng, H. L., et al. Integrity of the AID serine-38 phosphorylation site is critical for class switch recombination and somatic hypermutation in mice. Proceedings of the National Academy of Sciences. 106 (8), 2717-2722 (2009).
- Lebecque, S. G., Gearhart, P. J. Boundaries of somatic mutation in rearranged immunoglobulin genes: 5'boundary is near the promoter, and 3'boundary is approximately 1 kb from V (D) J gene. The Journal of Experimental Medicine. 172 (6), 1717-1727 (1990).
- Jolly, C. J., Klix, N., Neuberger, M. S. Rapid methods for the analysis of immunoglobulin gene hypermutation: application to transgenic and gene targeted mice. Nucleic Acids Research. 25 (10), 1913-1919 (1997).
- Choi, J. E., Matthews, A. J., Michel, G., Vuong, B. Q. AID Phosphorylation Regulates Mismatch Repair-Dependent Class Switch Recombination and Affinity Maturation. The Journal of Immunology. 204 (1), 13-22 (2020).
- McBride, K. M., et al. Regulation of class switch recombination and somatic mutation by AID phosphorylation. The Journal of Experimental Medicine. 205 (11), 2585-2594 (2008).
- Liu, M., et al. Two levels of protection for the B cell genome during somatic hypermutation. Nature. 451 (7180), 841-845 (2008).
- Ross, M., Birbeck, M., Wills, V., Forrester, J., Davis, A. Peanut lectin binding properties of germinal centers of mouse lymphoid tissues. Nature. 284, 364-366 (1980).
- Zhang, J., MacLennan, I. C., Liu, Y. J., Lane, P. J. Is rapid proliferation in B centroblasts linked to somatic mutation in memory B cell clones. Immunology Letters. 18 (4), 297-299 (1988).
- Nieuwenhuis, P., Opstelten, D. Functional anatomy of germinal centers. American Journal of Anatomy. 170 (3), 421-435 (1984).
- Lau, A. W., Brink, R. Selection in the germinal center. Current Opinion in Immunology. 63, 29-34 (2020).
- Victora, G. D., Nussenzweig, M. C. Germinal centers. Annual Review of Immunology. 30, 429-457 (2012).
- Mesin, L., Ersching, J., Victora, G. D. Germinal center B cell dynamics. Immunity. 45 (3), 471-482 (2016).
- Reichert, R. A., Gallatin, W. M., Weissman, I. L., Butcher, E. C. Germinal center B cells lack homing receptors necessary for normal lymphocyte recirculation. The Journal of Experimental Medicine. 157 (3), 813-827 (1983).
- Rose, M., Birbeck, M., Wills, V., Forrester, J., Davis, A. Peanut lectin binding properties of germinal centers of mouse lymphoid tissues. Nature. 284, 364-366 (1980).
- Hamada, S., Fujita, S. DAPI staining improved for quantitative cytofluorometry. Histochemistry. 79 (2), 219-226 (1983).
- Otto, F. DAPI staining of fixed cells for high-resolution flow cytometry of nuclear DNA. Methods in Cell Biology. 33, 105-110 (1990).
- Butcher, E., et al. Surface phenotype of Peyer's patch germinal center cells: implications for the role of germinal centers in B cell differentiation. The Journal of Immunology. 129 (6), 2698-2707 (1982).
- Rogerson, B. J., Harris, D. P., Swain, S. L., Burgess, D. O. Germinal center B cells in Peyer's patches of aged mice exhibit a normal activation phenotype and highly mutated IgM genes. Mechanisms of Ageing and Development. 124 (2), 155-165 (2003).
- Potapov, V., Ong, J. L. Examining sources of error in PCR by single-molecule sequencing. PloS One. 12 (1), 0169774 (2017).
- Gonzalez-Fernandez, A., Milstein, C. Analysis of somatic hypermutation in mouse Peyer's patches using immunoglobulin kappa light-chain transgenes. Proceedings of the National Academy of Sciences. 90 (21), 9862-9866 (1993).
- Reboldi, A., Cyster, J. G. Peyer's patches: organizing B-cell responses at the intestinal frontier. Immunological Reviews. 271 (1), 230-245 (2016).
- Betz, A. G., Rada, C., Pannell, R., Milstein, C., Neuberger, M. S. Passenger transgenes reveal intrinsic specificity of the antibody hypermutation mechanism: clustering, polarity, and specific hot spots. Proceedings of the National Academy of Sciences. 90 (6), 2385-2388 (1993).
- Rada, C., Gupta, S. K., Gherardi, E., Milstein, C. Mutation and selection during the secondary response to 2-phenyloxazolone. Proceedings of the National Academy of Sciences. 88 (13), 5508-5512 (1991).
- Heise, N., Klein, U. Somatic Hypermutation and Affinity Maturation Analysis Using the 4-Hydroxy-3-Nitrophenyl-Acetyl (NP) System. Methods in Molecular Biology. 1623, 191-208 (2017).
- Smith, F., Cumano, A., Licht, A., Pecht, I., Rajewsky, K. Low affinity of kappa chain bearing (4-hydroxy-3-nitrophenyl) acetyl (NP)-specific antibodies in the primary antibody repertoire of C57BL/6 mice may explain lambda chain dominance in primary anti-NP responses. Molecular Immunology. 22 (10), 1209-1216 (1985).
- Takahashi, Y., Dutta, P. R., Cerasoli, D. M., Kelsoe, G. In situ studies of the primary immune response to (4-hydroxy-3-nitrophenyl) acetyl. V. Affinity maturation develops in two stages of clonal selection. The Journal of Experimental Medicine. 187 (6), 885-895 (1998).
- Allen, D., Simon, T., Sablitzky, F., Rajewsky, K., Cumano, A. Antibody engineering for the analysis of affinity maturation of an anti-hapten response. The EMBO Journal. 7 (7), 1995-2001 (1988).
- Cumano, A., Rajewsky, K. Clonal recruitment and somatic mutation in the generation of immunological memory to the hapten NP. The EMBO Journal. 5 (10), 2459-2468 (1986).
- Smith, K., Nossal, G., Tarlinton, D. M. FAS is highly expressed in the germinal center but is not required for regulation of the B-cell response to antigen. Proceedings of the National Academy of Sciences. 92 (25), 11628-11632 (1995).
- Hao, Z., et al. Fas receptor expression in germinal-center B cells is essential for T and B lymphocyte homeostasis. Immunity. 29 (4), 615-627 (2008).
- Cervenak, L., Magyar, A., Boja, R., László, G. Differential expression of GL7 activation antigen on bone marrow B cell subpopulations and peripheral B cells. Immunology Letters. 78 (2), 89-96 (2001).
- Naito, Y., et al. Germinal center marker GL7 probes activation-dependent repression of N-glycolylneuraminic acid, a sialic acid species involved in the negative modulation of B-cell activation. Molecular and Cellular Biology. 27 (8), 3008-3022 (2007).
- Olson, W. J., et al. Orphan Nuclear Receptor NR2F6 Suppresses T Follicular Helper Cell Accumulation through Regulation of IL-21. Cell Reports. 28 (11), 2878-2891 (2019).
- Dorsett, Y., et al. MicroRNA-155 suppresses activation-induced cytidine deaminase-mediated Myc-Igh translocation. Immunity. 28 (5), 630-638 (2008).
- Goetz, C., Hammerbeck, C., Bonnevier, J. . Flow Cytometry Basics for the Non-Expert. , (2018).
- Hawley, T. S., Herbert, D. J., Eaker, S. S., Hawley, R. G. . Flow Cytometry Protocols. , (2004).
- Costa, E., et al. A new automated flow cytometry data analysis approach for the diagnostic screening of neoplastic B-cell disorders in peripheral blood samples with absolute lymphocytosis. Leukemia. 20 (7), 1221-1230 (2006).
- McKinnon, K. M. Flow cytometry: An overview. Current Protocols in Immunology. 120 (1), 1-11 (2018).
- McKinnon, K. M. Multiparameter Conventional Flow Cytometry. Methods in Molecular Biology. , 139-150 (2018).
- Lucchesi, S., et al. Computational Analysis of Multiparametric Flow Cytometric Data to Dissect B Cell Subsets in Vaccine Studies. Cytometry Part A. 97, 259-267 (2019).
- Longerich, S., Tanaka, A., Bozek, G., Nicolae, D., Storb, U. The very 5' end and the constant region of Ig genes are spared from somatic mutation because AID does not access these regions. The Journal of Experimental Medicine. 202 (10), 1443-1454 (2005).
- Retter, I., et al. Sequence and characterization of the Ig heavy chain constant and partial variable region of the mouse strain 129S1. The Journal of Immunology. 179 (4), 2419-2427 (2007).
- Shen, H. M., Peters, A., Baron, B., Zhu, X., Storb, U. Mutation of BCL-6 gene in normal B cells by the process of somatic hypermutation of Ig genes. Science. 280 (5370), 1750-1752 (1998).
- Richter, K., et al. Altered pattern of immunoglobulin hypermutation in mice deficient in Slip-GC protein. Journal of Biological Chemistry. 287 (38), 31856-31865 (2012).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved