Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Cancer Research
Flödescytometrisk analys av apoptotiska biomarkörer i aktinomycin D-behandlade SiHa livmoderhalscancerceller
Apoptos kan karakteriseras genom flödescytometrisk analys av tidiga och sena apoptotiska biomarkörer. Livmoderhalscancercellinjen, SiHa, analyserades för biomarkörer för apoptos efter behandling med Actinomycin D med hjälp av en benchtop flödescytometer.
Apoptos biomarkörer undersöktes i aktinomycin D-behandlade SiHa livmoderhalscancerceller med användning av en bänkflödescytometer. Tidiga biomarkörer (Annexin V och mitokondriell membranpotential) och sena biomarkörer (kaspaser 3 och 7 och DNA-skador) av apoptos mättes i experimentella och kontrollkulturer. Odlingarna inkuberades i 24 timmar i en fuktad inkubator vid 37 °C med 5 % CO2. Cellerna lossades sedan med trypsin och räknades upp med hjälp av en flödescytometrisk cellräkningsanalys. Celler analyserades vidare för apoptos med hjälp av en Annexin V-analys, en mitokondriell elektrokemisk transmembranpotentialanalys, en kaspase 3/7-analys och en DNA-skadeanalys. Denna artikel ger en översikt över apoptos och traditionell flödescytometri och utarbetar flödescytometriska protokoll för bearbetning och analys av SiHa-celler. Resultaten beskriver positiva, negativa och suboptimala experimentella data. Dessutom diskuteras tolkning och varningar vid utförande av flödescytometrisk analys av apoptos med hjälp av denna analytiska plattform. Flödescytometrisk analys ger en noggrann mätning av tidiga och sena biomarkörer för apoptos.
Apoptos, klassificerad som typ 1 programmerad celldöd1, säkerställer en jämvikt mellan cellproliferation och celldöd2. Apoptos är viktigt under mänsklig utveckling, efter skada och för att förebygga sjukdomar som cancer3. Inneboende och extrinsiska apoptotiska celldödssignalvägar4 orsakar sekventiella biokemiska och morfologiska intracellulära förändringar 2,5,6. Morfologiska apoptotiska egenskaper kan identifieras genom mikroskopi, och den biokemiska störningen kan analyseras med biokemiska analyser, inklusive flödescytometri (FC) 7.
Flödescytometrisk analys för att identifiera apoptos och förstå de associerade intracellulära mekanismerna har vuxit under de senaste två decennierna8. FC är en vetenskaplig metod som analyserar celler i en vätska som passerar genom en- eller flerkanalslasrar (figur 1)9,10,11. Cellerna i vätskan fokuseras i en enda fil av flödescytometerns fluidiksystem med hydrodynamisk fokusering. När celler passerar genom lasern sprids eller emitteras ljus från cellerna. Det spridda ljuset kan vara i riktning framåt (framåtspridning) eller mot sidan (sidospridning) och ger information om cellstorlek respektive cellgranularitet eller interna strukturer.
Dessutom detekterar fluorescerande reagens, såsom fluorescerande färgämnen eller antikroppar märkta med fluoroforer, specifika yt- eller intracellulära strukturer eller molekyler. När lasern exciterar fluoroforerna avges ljus vid en specifik våglängd. Detektorer - vanligtvis fotomultiplikatorrör - kvantifierar det spridda och utsända ljuset från cellprover. Detektorerna producerar en kvantifierbar ström som är proportionell mot ljusspridningen och fluorescensemissionen. Den elektroniska utgången omvandlas till digitala signaler genom datorprogramvara för att identifiera cellpopulationer baserat på cellstorlek, cellgranularitet och den relativa cellfluorescensen hos fluoroformärkta molekyler 9,12,13.
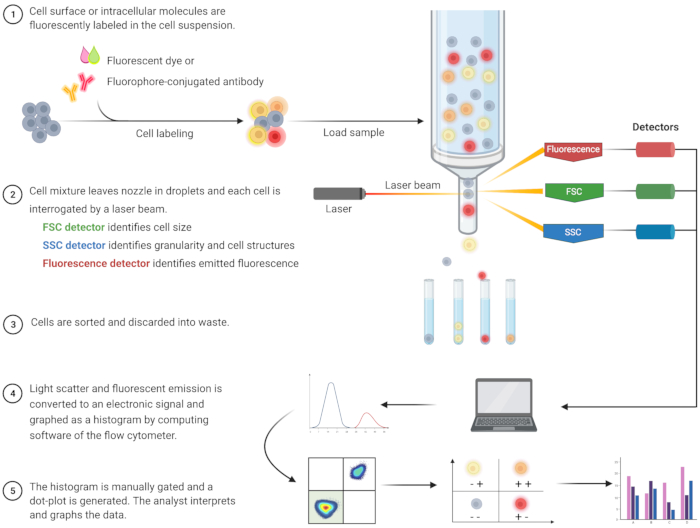
Figur 1: Schematisk beskrivning av den tekniska driften och arbetsflödet för traditionell flödescytometri. Cellerna färgas med fluorescerande reagens och sonderas med en laser. De fluorescenssignaler som genereras detekteras och omvandlas till en elektronisk utgång, som vidaredigitaliseras och analyseras av datorprogram och statistiska program. Förkortningar: FSC = forward scatter; SSC = sidospridning. Klicka här för att se en större version av denna figur.
FC används inom både forskning och hälsodiagnostik. De två målen för FC i nekrobiologi är klarläggandet av molekylära och funktionella egenskaper hos celldöd och diskrimineringen av olika former av celldöd 14,15,16,17,18. FC-tillämpningar inkluderar cellräkning, sortering av cellpopulationer, immunofenotypning, biomarkördetektion (t.ex. apoptosbiomarkörer), toxicitetsstudier och proteinteknik12. Dessutom används FC ofta för hälsodiagnostik för att hjälpa till med diagnos och övervakning av patienter med hematologiska maligniteter. Framsteg inom instrumentering, fluorofordetektering och detektorsystem utökar FC-applikationer till att omfatta bildcytometri, masscytometri och spektralcytometri med bredare forskningsapplikationer12.
Flödescytometrisk analys av apoptos ger fördelar jämfört med traditionella tekniker som används för att bedöma cellhälsa. FC kan analysera många enskilda celler i ett heterogent prov snabbt och reproducerbart för att uppskatta apoptos 3,5. FC: s förmåga att tillhandahålla kvantitativ information om cellfenotyper på individuell cellbasis och undvika bulkanalys erbjuder överlägsen känslighet för Western blotting, enzymkopplade immunosorbentanalyser (ELISA), fluorometri och spektrofotometritekniker som används vid analys av apoptos 8,19. Dessutom är den relativt enkla FC-analysen i motsats till de besvärliga och dåligt reproducerbara manuella stegen i Western blots och ELISAs fördelaktig. Den reproducerbara, exakta och höga genomströmningsanalysen av FC är därför fördelaktig i cancerforskning20.
FC tillåter också samtidig analys av cellcykelparametrar för friska och onormala apoptotiska cellpopulationer21. Eftersom apoptos är en dynamisk process kan olika metoder ge varierande resultat och är beroende av den tidpunkt då cellerna skördas22. Den samtidiga kvantitativa bedömningen av flera parametrar av cellfenotyp möjliggör detektion av mindre subpopulationer med hög noggrannhet, t.ex. kan sällsynta cellundergrupper med en låg frekvens på 0,01% detekteras23. Multiparametrisk FC-analys är särskilt användbar eftersom apoptotisk död inträffar längs ett spektrum av tidiga och sena biokemiska förändringar med celler vid olika punkter längs det apoptotiska kontinuumet. Till exempel möjliggör användningen av dubbelfärgning med användning av Annexin V och propidiumjodid i FC-analys av apoptotiska celler kategorisering av tidiga apoptotiska celler, sena apoptotiska celler och döda celler24. Den exakta detekteringen av apoptos i flera steg undviker felklassificering och falskt negativa resultat. Således förbättrar multiparametrisk analys av FC den övergripande specificiteten för detektering av cellfenotyper och undviker felklassificering av mindre populationer. Dessutom möjliggör cellsortering med FC isolering av cellpopulationer med hög renhet för efterföljande analys7.
Nackdelen med FC inkluderar användningen av celler i suspension, vilket kan vara utmanande vid vävnadsanalys, eftersom uppdelning av vävnad i celler kan förändra cellulär funktion19. Dessutom kan bristen på standardisering av FC-instrumentinställningar, dataanalys och analysrapporter orsaka variation i resultat19, vilket betonar behovet av optimal utbildning av FC-operatörer för att utföra och analysera och rapportera data. Till exempel kräver FC: s förmåga att diskriminera äkta apoptotiska skräp från apoptotiska kärnor i) korrekta förvärvsinställningar, ii) användning av kalibreringspärlor för att identifiera en diploid DNA-topp och iii) negativa och positiva cellkontroller som är cellspecifika3. Dessutom begränsas multiparametrisk analys av antalet detektorer, och optimal kompensation måste utföras för att undvika ospecifika resultat och spridning av fluorescerande emission vid användning av flera fluorescerande reagens25. Framsteg inom instrument- och fluoroforteknik har förbättrat parameterdetekteringen till 30 parametrar12.
Identifieringen av apoptotisk celldöd är inte alltid enkel7, och känsliga och specifika biomarkörer bör övervägas. Nomenklaturkommittén för celldöd (NCCD) rekommenderar att mer än en analys används för att studera och kvantifiera processen för apoptos26. Mikroskopianalys för klassiska apoptotiska egenskaper26 rekommenderas också för att bekräfta apoptos och undvika falskt positiva resultat7. Fyra kardinala biokemiska egenskaper som spänner över tidiga och sena apoptotiska händelser är (1) förlust av cellmembranasymmetri; (2) mitokondriell membranpotential för avledning (ΔΨm); (3) aktivering av kaspas; och (4) DNA-skador26.
Under tidig apoptos externaliseras fosfatidylserin till det yttre cellmembranet 27 och kan detekteras genom Annexin V fluorescerande märkt med fykoerytrin27,28,29. Vidare skiljer dubbelfärgning med det fluorescerande DNA-bindande färgämnet, 7-aminoaktinomycin D (7-AAD), levande, sen-apoptotiska och döda celler. Därför färgar tidigt apoptotiska celler positivt för Annexin V och negativt för 7-AAD, i motsats till sena apoptotiska celler, som färgar positivt för båda färgämnena24.
Inneboende apoptotiska signaler inducerar spridning av mitokondriell membranpotential (ΔΨm). Den störda ΔΨm orsakar frisättning av tidiga pro-apoptotiska proteiner från mitokondriellt intermembranutrymme till cytosolen27,29,30. Förändring av ΔΨm kan bedömas genom dubbelfärgning med det positivt laddade, lipofila färgämnet, tetrametylrhodaminetylester, TMRE och 7-AAD. TMRE-färgämnet ackumuleras i det inre membranet i intakta mitokondrier när membranpotentialen är hög. Depolariserade mitokondrier visar minskad fluorescens. Levande celler med polariserade mitokondrier (intakt mitokondriellt membran) färgar positivt för TMRE och negativt för 7-AAD. Döda celler med depolariserade mitokondrier färgar negativt för TMRE och positivt för 7-AAD31.
Kaspaserna är en familj av intracellulära proteaser som, när de aktiveras, signalerar och utför apoptos26,27. Den terminala bödeln caspases (3,6,7) effekt sen apoptos 29,32,33. Caspase-3 och -7 aktiviteter kan mätas med ett fluorescerande märkt substrat, som, när det klyvs, binder till DNA och avger en fluorescerande signal. Dessutom kan varje kompromiss med cellmembranintegriteten bedömas genom färgning med 7-AAD. Apoptotiska celler färgar positivt för det DNA-bindande färgämnet men negativt för 7-AAD. Senapoptotiska och döda celler färgar positivt för båda färgämnena34.
Sen apoptos kännetecknas av DNA-skada27,29,35, som kan utvärderas genom fosforylerat ataxiatelangiectasia-muterat kinas (ATM) och histon H2A.X. Dubbelsträngade DNA-brott (DSB) orsakar fosforylering av H2A.X. Fluorescerande märkta antikroppar mot ATM och H2A. X kan bestämma DNA-skador. Negativ detektering av både ATM och H2A. X indikerar ingen DNA-skada, medan detektion av båda färgämnena indikerar närvaron av dubbelsträngbrott i DNA36.
Actinomycin D är en potent inducerare av apoptos och verkar genom att binda till DNA för att blockera transkriptions- och översättningshändelser37. Denna studie syftade till att bedöma biokemisk apoptos inducerad av aktinomycin D i SiHa-cellinjen genom att analysera tidiga och sena biomarkörer för apoptos. Fyra biokemiska biomarkörer för apoptos utvärderade de sekventiella stegen i den apoptotiska kaskaden som inkluderade förlust av cellmembranasymmetri, förändring i mitokondriell membranpotential, aktivering av terminala kaspaser och DNA-skador.
OBS: Detta protokoll beskriver steg i cellberedningen, cellräkning, cellfärgning och analys av aktinomycin D-behandlade SiHa-celler med hjälp av flödescytometriska kommersiella analyser uppmätta och analyserade på en benchtop flödescytometer (figur 2).
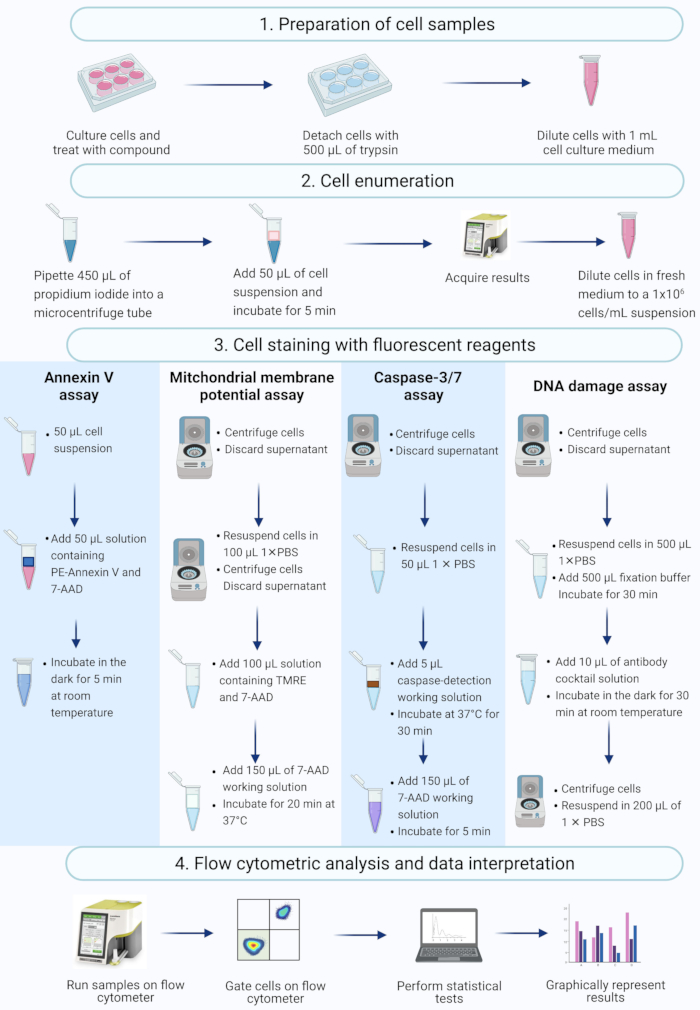
Figur 2: Arbetsflöde för detektion av biokemiska apoptotiska biomarkörer genom flödescytometri. Celler odlas och behandlas enligt beskrivningen i protokollsteg 1.1. (1) Cellerna odlas, (2) räknas upp och (3) färgas med fluorescerande reagens och (4) analyseras med en benchtop flödescytometer. Data gated ytterligare och analyseras statistiskt. Förkortningar: 7-AAD = 7-aminoaktinomycin D; PBS = fosfatbuffrad saltlösning; PE = Phycoerythrin; TMRE = tetrametylrhodaminetylester. Klicka här för att se en större version av denna figur.
1. Beredning av cellodling och behandlingar för flödescytometri
OBS: Se till att aseptisk teknik följs vid hantering av cellkulturer.
- Odla cellkulturer i en fuktad CO 2-miljö vid 37 ° C med 5% CO2. Se till att cellodlingen är ungefär 70 % sammanflytande i moderkolven innan cellerna passeras för experiment.
- Ta bort mediet från kolven, tvätta cellerna med 1x fosfatbuffrad saltlösning (PBS) och tillsätt 500 μL trypsin för att lossa cellerna. När cellerna börjar runda och lossna från kolven, knacka kolvens botten kraftigt på bänken för att lossa cellerna. Neutralisera sedan trypsinet genom att tillsätta cirka 5 ml färskt odlingsmedium kompletterat med 10% fosterkalvserum innan cellerna räknas.
- Fröceller vid 15 000 celler/ml i 3 ml cellodlingsmedium i en cellodlingsplatta med 6 brunnar. Inkubera odlingsplattorna över natten vid 37 °C med 5 %CO2 så att cellerna kan fästas i botten av brunnen.
- Behandla experimentkulturerna med 100 ng/ml aktinomycin D och medie- och lösningsmedelskontrollerna med färskt odlingsmedium respektive dimetylsulfoxid (DMSO) i 24 timmar. Samla det använda mediet i ett 15 ml rör och tvätta celler med 1x PBS. Tillsätt därefter 1x PBS-tvätten till röret och tillsätt sedan 500 μL trypsin till brunnen. Därefter neutralisera trypsinet genom att tillsätta 5 ml färskt odlingsmedium.
OBS: (1) Långvarig trypsinkubation eller ofullständig neutralisering kan smälta cellerna och äventyra deras cellmembran, vilket kan snedvrida resultaten. Dessutom kan det också förändra cellmembranasymmetri och därmed tillgängligheten till fosfatidylserin. (2) Celler som har lossnat och flytit upp till ytan kan inkluderas i den efterföljande analysen genom centrifugering av det borttagna mediet vid 300 × g i 5 minuter och resuspendering av cellerna i färskt odlingsmedium.
2. Uppräkning av celler med hjälp av viabilitetsanalysen
- Pipettera 450 μL propidiumjodid i ett mikrocentrifugrör. Tillsätt 50 μl av cellsuspensionen till mikrocentrifugröret. Inkubera röret vid rumstemperatur i 5 minuter. Räkna upp cellerna med flödescytometri (se avsnitt 4).
- Späd alla prover till en koncentration av 1 × 106 celler/ml med cellodlingsmedium innan du går vidare till apoptostesterna.
3. Färgning av celler för flödescytometri
OBS: Sterila förhållanden krävs inte för denna del av protokollet.
- Detektion av fosfatidylserin externalisering med användning av Annexin V
- Tillsätt 100 μl cellsuspension i ett mikrocentrifugrör. Tillsätt 100 μl av en 1:1-blandning av fluorescerande konjugerat annexin V och 7-AAD-reagens. Inkubera vid rumstemperatur i 20 minuter, skyddad från ljus.
- Analys av mitokondriell membrandepolarisering
- Centrifugera 100 μl av cellsuspensionen vid 300 × g i 5 minuter och kassera supernatanten.
- Superera upp cellerna igen i 1 ml 1x PBS, tillsätt 100 μl TMRE-färgningslösning till varje prov och blanda suspensionen genom försiktig backpipettering.
- Inkubera cellerna i 20 minuter i en fuktad CO2-miljö vid 37 °C. Slå in proverna i ren aluminiumfolie för att skydda mot ljus.
OBS: Mitokondriell membranpotential är en funktionell markör som är känslig för mindre förändringar i cellmiljön. Därför bör proverna inkuberas och mätas under identiska förhållanden (temperatur, pH och tid som förflutit mellan inkubationens början och fluorescerande mätning) för att bibehålla reproducerbarheten). Observera också att otillräckligt skydd av prover från ljus orsakar fotoblekning av fluoroforer vilket resulterar i falskt låg emitterad fluorescens. - Efter inkubation tillsätts 5 μL 7-AAD-färgningslösning till varje prov och blandas. Inkubera i 5 minuter vid rumstemperatur, skyddad från ljus.
- Detektion av aktiverad terminal caspase-3 och -7 med användning av kaspassubstrat DEVD
Följande lösningar bereds innan denna analys utförs.- Späd den DEVD-bundna DNA-bindande peptiden i DMSO till ett förhållande av 1: 8 med steril 1x PBS för att få kaspasdetekteringslösningen att fungera. Förvara lösningen på is eller vid 2-8 °C, skyddad från ljus.
OBS: Varje prov kräver 5 μL av denna lösning. - Tillsätt 2 μL av en 7-AAD-stamlösning till 148 μL 1x PBS för att göra 7-AAD-arbetslösningen. Förvara lösningen på is eller vid 2-8 °C, skyddad från ljus.
OBS: Varje prov kräver 150 μL av denna lösning. - Centrifugera 50 μl av cellsuspensionen i 5 min vid 300 × g. Kassera supernatanten. Återsuspendera cellerna i 50 μL 1x PBS, följt av 5 μL av arbetslösningen för kaspasdetektion. Blanda noggrant.
- Lossa locket på rören och inkubera i 30 minuter i en fuktad CO2-miljö vid 37 °C, skyddad från ljus. Tillsätt 150 μL av 7-AAD-arbetslösningen till varje prov och blanda. Inkubera i 5 minuter vid rumstemperatur, skyddad från ljus.
- Späd den DEVD-bundna DNA-bindande peptiden i DMSO till ett förhållande av 1: 8 med steril 1x PBS för att få kaspasdetekteringslösningen att fungera. Förvara lösningen på is eller vid 2-8 °C, skyddad från ljus.
- Detektion av dubbelsträngade DNA-brott och total DNA-skada
- Centrifugera 50 μl av cellsuspensionen i 5 min vid 300 × g. Kassera supernatanten.
- Resuspendera cellerna i 500 μL 1x PBS. Tillsätt 500 μl av en formaldehydbaserad fixeringsbuffert och blanda. Inkubera proverna på is i 10 minuter.
- Centrifugera i 5 minuter vid 300 × g och kassera supernatanten. Återsuspendera cellerna i 90 μL 1x PBS i ett mikrocentrifugrör. Tillsätt 10 μl antikroppslösning till mikrocentrifugröret. Inkubera vid rumstemperatur i 30 minuter i mörker.
- Tillsätt 100 μL 1x PBS och centrifugera i 5 min vid 300 × g. Kassera supernatanten. Resuspendera cellerna i 200 μL 1x PBS.
4. Kör prover på flödescytometern.
- Kontrollera flödescytometerns analytiska prestanda genom att köra instrumentets systemkontrollkit. Fortsätt inte med löpande prover förrän alla kontroller är klara och godkända.
- Leta reda på önskad analys genom att bläddra igenom katalogen med förprogrammerade analyser på instrumentet och välj Kör analys.
- Blanda provet genom att försiktigt backpipettera innan provet laddas på flödescytometern.
OBS: Tillräcklig blandning säkerställer att cellerna förblir i suspension och förhindrar lågt cellantal. - Läs först in ett negativt kontrollprov på flödescytometern och välj Kör (justera inställningar) så att instrumentet börjar aspirera provet och ger en förhandsgranskning i realtid av upptäckta händelser. Se materialtabellen för instrumentnamn och detaljer.
- Använd liveförhandsvisningen för att justera tröskelvärdena för fluorescens och cellstorlek och rita en rektangulär grind runt cellpopulationen. Dra tröskelmarkören för att utesluta cellulärt skräp. Välj Nästa (Ange hälsoprofil) för att fortsätta.
OBS: Det är viktigt att veta storleken på cellerna. Dra skjutreglagen och observera förändringar i hur upptäckta händelser ritas i förhandsgranskningen i realtid, eftersom detta kommer att informera ett korrekt val av tröskelvärden. Om cellulärt skräp inte utesluts i detta skede kan det inte tas bort i analyser efter förvärvet. - Tryck och dra kvadrantmarkörerna för att separera cellpopulationerna och så att instrumentet ritar upptäckta händelser i realtid. Använd dessa diagram för att vägleda slutanvändaren om lämplig placering av kvadrantmarkörerna. Välj Nästa (Verifiera exempel) för att fortsätta så att instrumentet visar en sammanfattning av inställningarna. När du har granskat inställningarna väljer du Nästa (verifiera inställningar) för att tillämpa dessa inställningar för alla exempel i experimentet.
OBS: Instrumentet ger en 2-minuters liveförhandsvisning av celler som används för att justera instrumentets inställningar. Om denna tidsgräns löper ut kommer instrumentet att släppa provet och steg 4.2.2-4.2.4 måste upprepas. Ta bort provet och blanda väl innan du laddar om och fortsätter. - Grinda en population av celler genom att rita en region runt cellpopulationen. Justera tröskelvärdena för fluorescens och cellstorlek med skjutreglagen på x- och y-axeln i direktförhandsvisningen. Använd de här inställningarna för alla exempel i experimentet.
- Blanda det första provet genom att försiktigt backpipettera och ladda det första provet på flödescytometern och välj Nästa. Namnge exemplet och välj Kör så att systemet börjar köra exemplet.
OBS: Instrumentet kan bara köra ett prov i taget. - När alla prover har körts sparar du experimentet genom att ge det en lämplig titel. Spara inställningarna för det aktuella experimentet för hämtning i framtida körningar (valfritt).
- Blanda provet genom att försiktigt backpipettera innan provet laddas på flödescytometern.
5. Analys efter förvärvet
- Vid behov utför du finjustering av grindar eller kvadrantmarkörer efter förvärvet.
- Leta reda på experimentet som behöver justeras genom att navigera i systemets filbläddrare och öppna experimentet.
- Tryck på miniatyrförhandsgranskningen av tomten för att förstora den. Tryck på de övre vänstra eller nedre högra hörnen av cellporten för att justera portens dimensioner. För att justera kvadrantmarkörerna, tryck på skärningspunkten mellan de vertikala och horisontella linjerna för att flytta markörerna som de är. För att justera vinkeln på endera linjen, tryck på linjen och dra handtaget.
- Justera markörerna (som tidigare beskrivits i steg 4.1.3-4.1.4) efter behov och tillämpa dessa inställningar på alla prover i experimentet genom att välja bockmarkeringsikonen , markera alla prover och välja Acceptera.
6. Statistisk analys
- Kör tester i tre exemplar och kör en variansanalys (ANOVA) med ett post-hoc-Bonferroni-test för att bedöma signifikanta skillnader mellan de behandlade proverna och kontrollerna.
OBS: Det valda statistiska testet är beroende av utredaren och de variabler som analyseras.
Resultaten av cellantal och livskraft (figur 3) visade att 95,2% av cellerna i provet var levande och 4,8% var döda. Den totala cellkoncentrationen i det ursprungliga provet var 6,20 x 106 celler/ml.
Annexin V och celldödsanalysen (figur 4) visade en signifikant ökning (p < 0,0001) av apoptotiska celler i SiHa-celler behandlade med 100 ng/ml aktinomycin D jämfört med kontrollerna. Eftersom Annexin V-färgning ökar i celler under apoptos i tidigt stadium, tyder detta fynd på att 100 ng / ml aktinomycin D inducerade apoptos i SiHa-celler.
Den mitokondriella elektrokemiska transmembranpotentialanalysen (figur 5) visade en signifikant minskning (p < 0,0001) i cellhälsoprofiler (levande, depolariserade och levande, depolariserade och döda, döda) mellan aktinomycin D, medelkontroll och lösningsmedelskontroll. Dessa data tyder på att 100 ng/ml aktinomycin D inducerade mitokondriell depolarisering i SiHa-celler.
Caspase 3/7-testet (figur 6) visade signifikant (p < 0,0001) aktivering av kaspaser 3 och 7 i SiHa-celler behandlade med 100 ng/ml aktinomycin D jämfört med kontrollerna. Dessa fynd visar att 100 ng / ml aktinomycin D inducerad apoptos i SiHa-celler.
DNA-skadeanalysen (figur 7) visade att 100 ng/ml aktinomycin D signifikant (p < 0,0001) inducerade DNA-skademarkörer, ATM och H2A. X, i SiHa-celler. Detta fynd tyder på signifikant ökning av DNA-skador i SiHa-celler behandlade med aktinomycin D.
Resultaten av suboptimala experiment (figur 8) visar analytiska överväganden över alla analyser. Cellkoncentrationen påverkar noggrannheten i data. I figur 8A är cellantalet oacceptabelt lågt. De gated cellpopulationerna i alla 4 kvadranter i punktdiagrammet har låg signalintensitet. Tillverkaren optimerar analysen för 300-700 celler/μl i den slutliga provvolymen. Detta exempel illustrerar vikten av att använda rätt provkoncentration som föreskrivs av tillverkaren.
Dessutom orsakade höga cellkoncentrationer också felaktiga resultat (figur 8B). Medium och experimentella kulturer visade 99,95% respektive 100% levande celler. Flödeshastigheten för båda analyserna överskred tillverkarens optimerade koncentration på 100-500 celler/μl och krävde utspädning med 1x analysbuffert för att undvika felaktig analys.
Klumpbildning av celler bör undvikas vid beredning av experimentella kulturer, eftersom det ger felaktiga resultat på grund av ökade cellstorleksindex, vilket illustreras i Annexin V-testet. Figur 8C visar ett dubbelt problem med hög cellkoncentration som överstiger tillverkarens instruktioner och cellklumpning, vilket framgår av cellstorleksindex som överstiger 4 i SiHa-mediekontrollen. Den höga cellkoncentrationen illustreras av arkning av celler som bildar ett ljusrött plan av celler i medelkulturer, vilket visar diskordant höga apoptotiska cellpopulationer.
Långvarig färgning av kulturer kan resultera i ospecifik bindning av proteiner och resultera i falska resultat, vilket framgår av Annexin V-testet. Figur 8D visar liknande resultat för medelstora och experimentella kulturer på grund av långvarig färgning.
Dålig provhantering, förlängd trypsinisering av vidhäftande celler, kraftig pipettering under tvättsteg och höghastighets- och långvariga centrifugeringssteg orsakar celllys och stora mängder cellskräp. I figur 8E visar kulturer analyserade med caspase 3/7-analysen ökat cellskräp som framgår av ett litet cellstorleksindex (<2.2 cellstorleksindex). Försiktighet bör därför iakttas när prover förbereds för datainsamling.
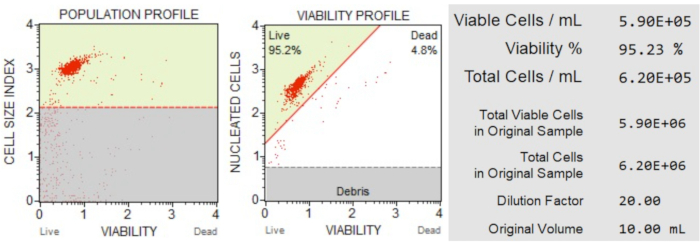
Figur 3: Cellräkning och viabilitetsanalys. Befolkningsprofilen separerar skräp från levande och döda celler. Det tvådimensionella punktdiagrammet är gated och delar levande och döda cellpopulationer. Informationspanelen ger kvantitativa data om cellantal, procentandel av totalt viabla celler och det totala antalet viabla celler i provet. Dessa data kan användas för att standardisera cellantalet i alla prover för efterföljande apoptosanalyser. Klicka här för att se en större version av denna figur.
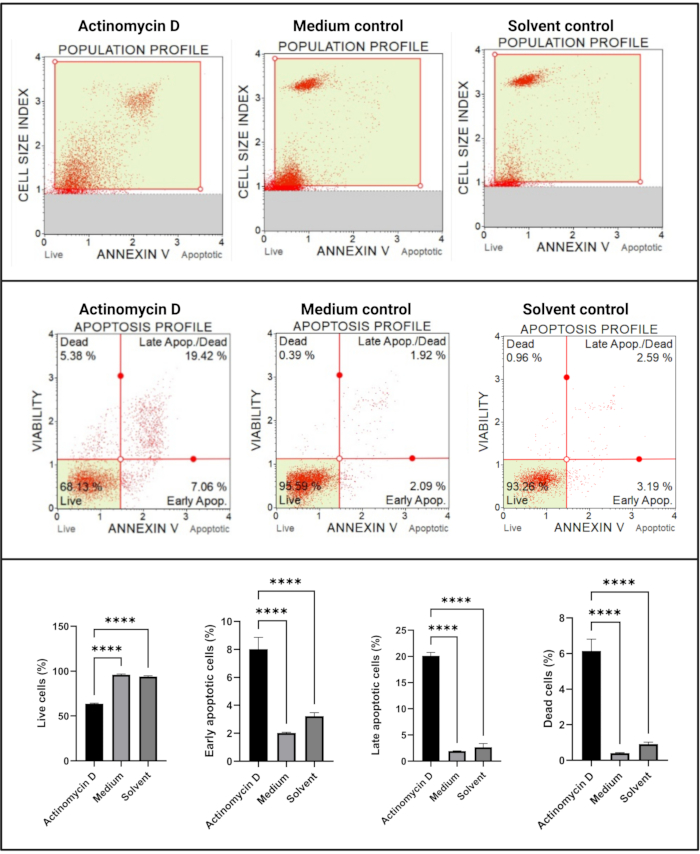
Figur 4: Annexin V-test. Alla prover visar identiska grindparametrar, och statistisk analys av varje subpopulation avslöjar en signifikant ökning av apoptos i celler behandlade med aktinomycin D. Alla analyser utfördes som tre oberoende experiment, och varje experiment analyserades i tre exemplar. Data presenteras som medelvärde ± SD, och p < 0,05 ansågs vara statistiskt signifikant. p < 0,0001. Klicka här för att se en större version av denna figur.
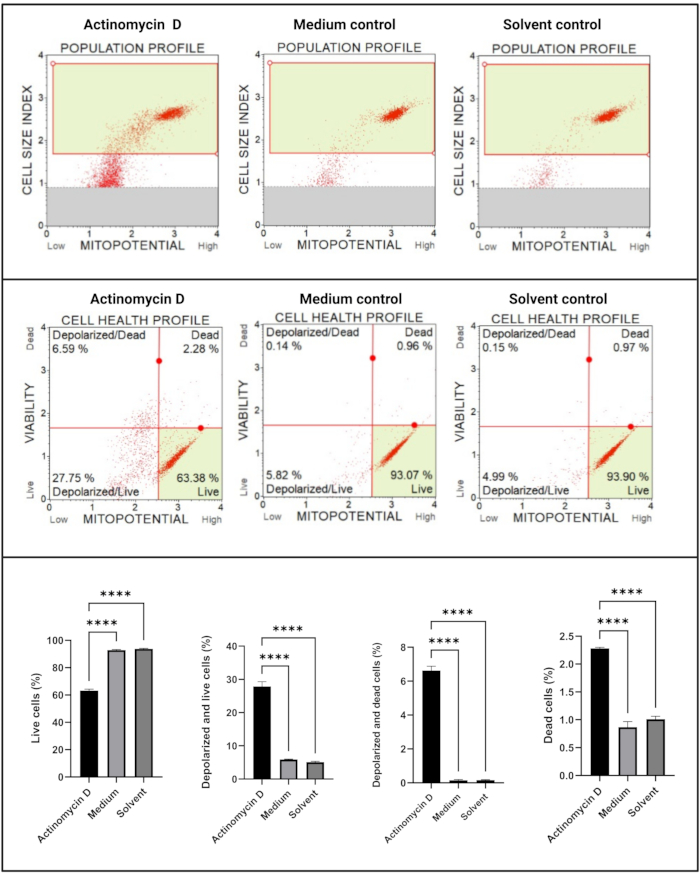
Figur 5: Mitokondriell elektrokemisk transmembranpotentialanalys. Alla prover visar identiska grindparametrar, och statistisk analys av varje subpopulation avslöjar signifikant störning av mitokondriell membranpotential i celler behandlade med aktinomycin D. Alla analyser utfördes som tre oberoende experiment, och varje experiment analyserades i tre exemplar. Data presenteras som medelvärde ± SD, och p < 0,05 ansågs vara statistiskt signifikant. p < 0,0001. Klicka här för att se en större version av denna figur.
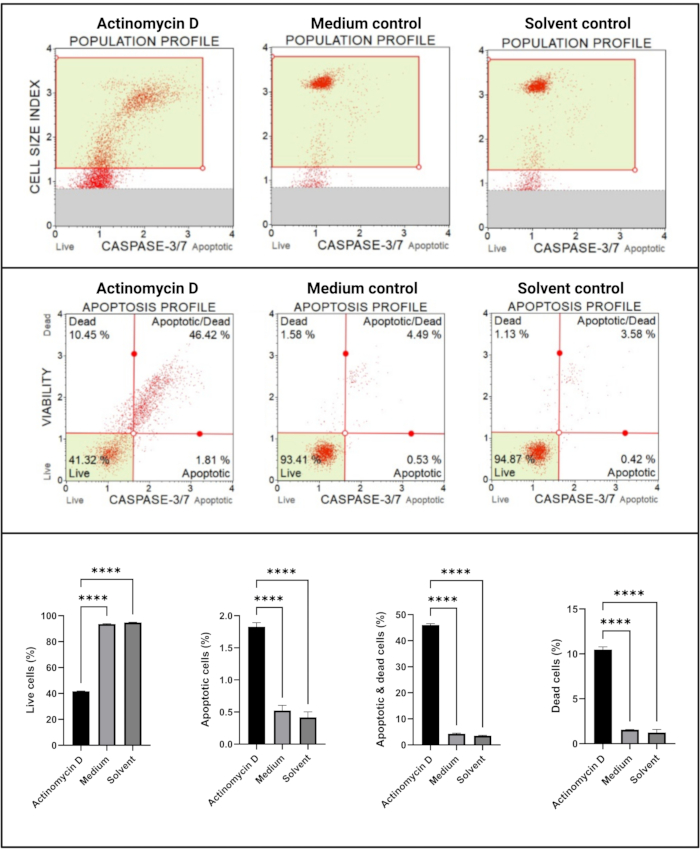
Figur 6: Detektionstest för kaspas 3/7. Alla prover visar identiska grindparametrar, och statistisk analys av varje subpopulation avslöjar en signifikant ökning av kaspas 3/7 aktivitet i celler behandlade med aktinomycin D. Alla analyser utfördes som tre oberoende experiment, och varje experiment analyserades i tre exemplar. Data presenteras som medelvärde ± SD, och p < 0,05 ansågs vara statistiskt signifikant. p < 0,0001. Klicka här för att se en större version av denna figur.
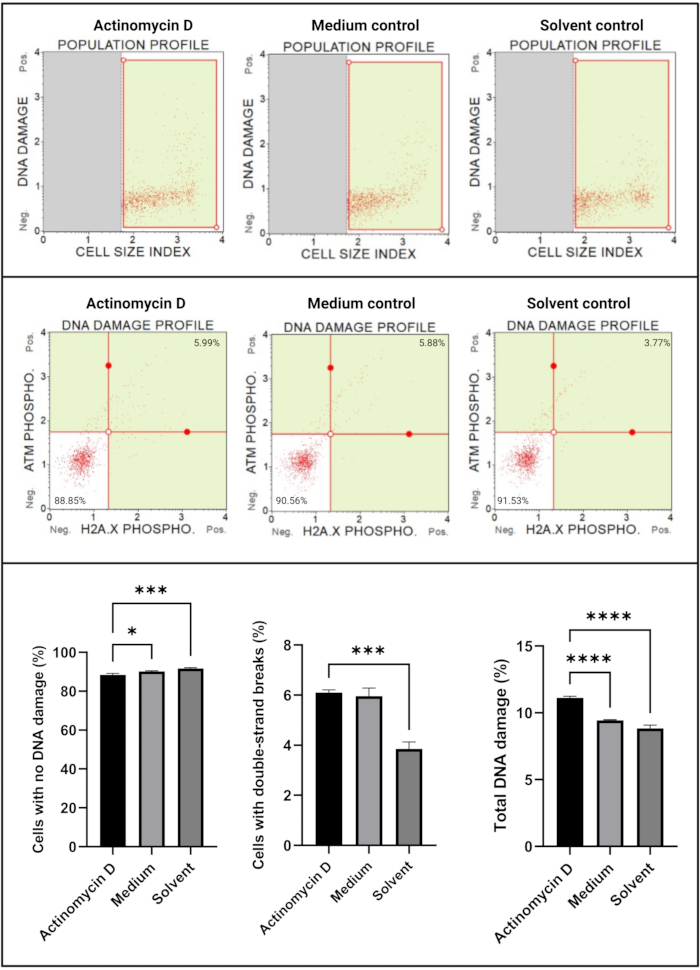
Figur 7: DNA-skadeanalys. Alla prover visar identiska grindparametrar, och statistisk analys av varje subpopulation avslöjar en signifikant ökning av dubbelsträngad DNA-skada och total DNA-skada i celler behandlade med aktinomycin D. Alla analyser utfördes på tre oberoende experiment, och varje experiment analyserades i tre exemplar. Data presenteras som medelvärde ± SD, och p < 0,05 ansågs vara statistiskt signifikant. * p < 0,05; p < 0,001; p < 0,0001. Klicka här för att se en större version av denna figur.
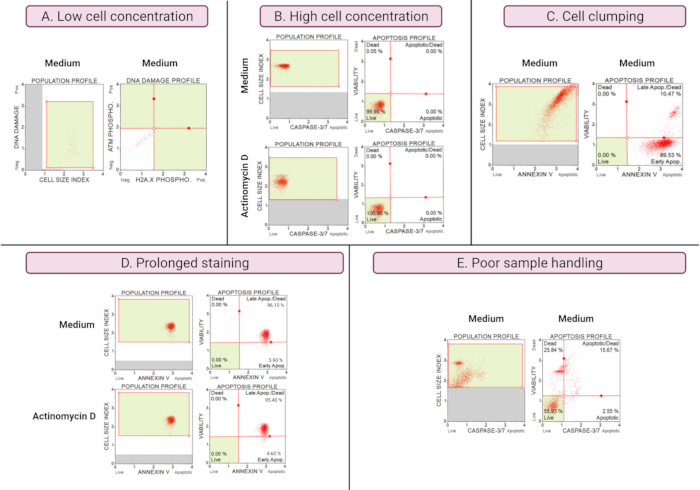
Figur 8: Suboptimala experimentella förhållanden ger dåliga resultat . (A) låg koncentration av celler, (B) hög koncentration av celler, (C) cellklumpning och aggregering uppenbar av högt cellstorleksindex, (D) långvarig färgning av cellprover uppenbar genom ökad positiv färgning i båda proverna, och (E) dålig provhantering uppenbar genom ökat cellulärt skräp (cellstorleksindex < 2.2). Klicka här för att se en större version av denna figur.
I denna studie avslöjade aktinomycin D-behandlade SiHa-celler analyserade av FC signifikanta tidiga och sena biomarkörer för apoptos. Suboptimala förhållanden för cellberedning, uppräkning och färgning identifierade felaktiga resultat, vilket betonar behovet av noggrann efterlevnad av tillverkarens instruktioner vid utförande av FC.
Denna studie av apoptos genom tidig och sen biomarköridentifiering överensstämmer med NCCD-riktlinjerna1 för undersökning av apoptos. Actinomycin D-behandlade SiHa-kulturer visade positiva biomarkörer för tidiga och sena apoptotiska stadier. Annexin V/PI-analysen och mitokondriell permeabilitetsanalys visade att aktinomycin D inducerade ett PS-flip-mönster respektive försvinnande av mitokondriell membranövergång. När apoptotiska celler når punkten utan återvändo inducerad av mitokondriell störning aktiveras de terminala kaspaserna 3,7. Aktiveringen av de terminala kaspaserna 3 och 7 som observerats i denna studie indikerar apoptos i sen fas. Vidare orsakar terminal kaspasaktivering internukleosomal DNA-klyvning och omfattande DNA-fragmentering, vilket klassiskt har rapporterats som ett stegstegemönster observerat av gelelektrofores28,38.
Kärnskadorna med ATM och H2A. X FC DNA-skadeanalys visade dubbelsträngsbrott i DNA och total DNA-skada. Dessa resultat bekräftade klassisk nedströms kaspasinducerad apoptotisk kärnskada (karyorrhexis och karyorrlys) i experimentella kulturer. Användningen av cytometriska biomarkörer med flera flöden detekterade således de sekventiella flerstegshändelserna vid apoptos och identifierade noggrant och reproducerbart cellpopulationer i tidiga och sena apoptotiska stadier. Dessa fynd överensstämmer med de kända pro-apoptotiska egenskaperna hos aktinomycin D vid cancerbehandling hos människa 37,39,40,41 och stöder vidare användningen av aktinomycin D som en positiv kontroll i FC-cellodlingsexperiment som undersöker apoptos.
Gating av cellpopulationer i denna studie informerades av negativa medium- och lösningsmedelskontroller, som separerade apoptotiska från friska celler. Alternativt kan en blandning av populationer av positiva och negativa kontroller också användas för att definiera levande och apoptotiska cellpopulationer för att ställa in cellpopulationsgrindar 7,9. När sjuka och friska cellulära tillstånd har definierats och gated kan mallinställningarna tillämpas på alla efterföljande experimentella och kontrollkulturer.
Strikt efterlevnad av FC-protokollet är viktigt för att undvika falska resultat. Under optimeringen av protokollet observerades följande problem: (1) låg cellkoncentration, (2) hög cellkoncentration, (3) cellklumpning, (4) långvarig färgning och (5) dålig provhantering. Dessa problem kan förhindras genom strikt efterlevnad av optimerade protokollkrav. Detta betonar den avgörande karaktären av föranalytiska och analytiska steg för FC för att få korrekta data. Under cellberedning måste trypsinisering, pipettering, centrifugering och utspädning utföras med försiktighet. Övertrypsinisering och kraftig pipettering kan resultera i kemisk respektive mekanisk skjuvning av celler. Långvarig och höghastighetscentrifugering kan resultera i cellnedbrytning och högt cellulärt skräpantal. Optimal cellkoncentration krävs för att minimera felaktig förvärv av cellhändelser. Därför bör primära cellsuspensioner spädas för att uppnå optimal cellkoncentration.
Vid hantering av prover måste man dessutom se till att förhindra cellklumpning och cellfragmentering och se till att cellerna förblir suspenderade under analysen. Provhantering för att förhindra cellklumpning möjliggör enstaka laminärt cellflöde, förhindrar mekanisk blockering av instrumentets kapillärrör och begränsar falska stora cellstorleksindex. En annan varning är att skydda kulturer mot ljus för att undvika fotooxidation och släckning av fluoroforerna i analyserna för att förhindra falskt negativa resultat. Försiktighet måste vidtas för att säkerställa minimal ljusexponering vid färgningssteget i cellerna och efterföljande bearbetningssteg. Dessutom kan förlängda immunfärgningstider resultera i falskt positiva resultat eftersom proteiner är icke-specifikt färgade. Därför är det viktigt att följa tillverkarens föreskrivna inkubationsfärgningsperioder.
Sammanfattningsvis kan FC exakt detektera apoptos och diskriminera mellan tidiga och sena apoptosbiomarkörer i cellodling. Dessutom har tekniska framsteg lett till tillverkning av benchtopflödescytometrar för icke-expertforskare för att studera cellhälsa och komplexa intracellulära signalvägar.
Luminex® Corporation tillhandahöll vänligen avgifter för artikelbehandling.
Studien stöddes ekonomiskt av National Research Foundation (NRF) och South African Medical Research Council (SAMRC). Vi vill tacka National Health Laboratory Service (NHLS) för inköp av Guava Muse Cell Analyzer. Alla siffror i denna publikation skapades med Biorender.com.
| Name | Company | Catalog Number | Comments |
| 6-well plates | Lasec | P1PLA044C-000006 | |
| Dimethyl Sulfoxide | Sigma-Aldrich | D8418 | |
| DMEM | ThermoFisher | 41966052 | |
| Glutamine | Sigma-Aldrich | P10-040500 | |
| Guava Muse Cell Analyzer | Luminex | 0500-3115 | |
| Microcentrifuge tubes/Eppendorf | Merck | EP0030122208-200EA | |
| Muse Annexin V kit | Merck | MCH100105 | |
| Muse Caspase-3/7 kit | Merck | MCH100108 | |
| Muse Count and Viability kit | Merck | MCH600103 | |
| Muse DNA Damage kit | Merck | MCH200107 | |
| Muse MitoPotential kit | Merck | MCH100110 | |
| PBS Buffer | ThermoFisher | 70013065 | |
| Pen-strep | Sigma-Aldrich | P4333 | |
| SiHa cells | ATCC | CRL-1550 | |
| T25 culture flasks | Sigma-Aldrich | C6231 | |
| Trypsin | Pan Biotech | P10-040500 |
- Galluzzi, L., et al. Molecular mechanisms of cell death: Recommendations of the Nomenclature Committee on Cell Death 2018. Cell Death and Differentiation. 25 (3), 486-541 (2018).
- Kerr, J. F., Wyllie, A. H., Currie, A. R. Apoptosis: a basic biological phenomenon with wide-ranging implications in tissue kinetics. British journal of cancer. 26 (4), 239-257 (1972).
- Riccardi, C., Nicoletti, I. Analysis of apoptosis by propidium iodide staining and flow cytometry. Nature Protocols. 1 (3), 1458-1461 (2006).
- Edinger, A. L., Thompson, C. B. Death by design: apoptosis, necrosis and autophagy. Current Opinion in Cell Biology. 16 (6), 663-669 (2004).
- Arends, M. J., Morris, R. G., Wyllie, A. H. Apoptosis. The role of the endonuclease. The American journal of pathology. 136 (3), 593-608 (1990).
- Majno, G., Joris, I. Apoptosis, oncosis, and necrosis. An overview of cell death. Am J Pathol. 146 (1), 3-15 (1995).
- Darzynkiewicz, Z., Traganos, F., Al-Rubeai, M. . Apoptosis. , 33-73 (1998).
- Wlodkowic, D., Skommer, J., Darzynkiewicz, Z. Flow cytometry-based apoptosis detection. Methods in molecular biology. 559, 19-32 (2009).
- . Introduction to Flow Cytometry Basics Available from: https://www.bio-rad-antibodies.com/introduction-to-flow-cytometry.html (2021)
- Telford, W. G., Komoriya, A., Packard, B. Z. Detection of localized caspase activity in early apoptotic cells by laser scanning cytometry. Cytometry. 47 (2), 81-88 (2002).
- Castedo, M., et al. Quantitation of mitochondrial alterations associated with apoptosis. J Immunol Methods. 265 (1-2), 39-47 (2002).
- McKinnon, K. M. Flow Cytometry: An Overview. Current protocols in immunology. 120, 1-11 (2018).
- Macey, M. G. Flow cytometry: principles and clinical applications. Med Lab Sci. 45 (2), 165-173 (1988).
- Darzynkiewicz, Z., et al. Features of apoptotic cells measured by flow cytometry. Cytometry. 13 (8), 795-808 (1992).
- Darzynkiewicz, Z., et al. Cytometry in cell necrobiology: Analysis of apoptosis and accidental cell death (necrosis). Cytometry. 27 (1), 1-20 (1997).
- Ormerod, M. G. The study of apoptotic cells by flow cytometry. Leukemia. 12 (7), 1013-1025 (1998).
- van Engeland, M., Nieland, L. J., Ramaekers, F. C., Schutte, B., Reutelingsperger, C. P. Annexin V-affinity assay: a review on an apoptosis detection system based on phosphatidylserine exposure. Cytometry. 31 (1), 1-9 (1998).
- Vermes, I., Haanen, C., Reutelingsperger, C. Flow cytometry of apoptotic cell death. Journal of Immunological Methods. 243 (1), 167-190 (2000).
- Jahan-Tigh, R. R., Ryan, C., Obermoser, G., Schwarzenberger, K. Flow cytometry. J Invest Dermatol. 132 (10), 1-6 (2012).
- Lövborg, H., Gullbo, J., Larsson, R. Screening for apoptosis-classical and emerging techniques. Anti-cancer drugs. 16 (6), 593-599 (2005).
- Vorobjev, I. A., Barteneva, N. S. Multi-parametric imaging of cell heterogeneity in apoptosis analysis. Methods. 112, 105-123 (2017).
- Telford, W. G., Komoriya, A., Packard, B. Z. Multiparametric analysis of apoptosis by flow and image cytometry. Methods in molecular biology. 263, 141-160 (2004).
- Kagami, S., Rizzo, H. L., Lee, J. J., Koguchi, Y., Blauvelt, A. Circulating Th17, Th22, and Th1 cells are increased in psoriasis. J Invest Dermatol. 130 (5), 1373-1383 (2010).
- . Muse® Annexin V & Dead Cell Kit Available from: https://www.luminexcorp.com/muse-annexin-v-dead-cell-kit/ (2019)
- Roederer, M. Spectral compensation for flow cytometry: visualization artifacts, limitations, and caveats. Cytometry. 45 (3), 194-205 (2001).
- Kroemer, G., et al. Classification of cell death: recommendations of the Nomenclature Committee on Cell Death. Cell Death and Differentiation. 12 (2), 1463-1467 (2005).
- Apoptosis assays and markers guide. Abcam Available from: https://www.abcam.com/kits/apoptosis-assays (2021)
- Vermes, I., Haanen, C., Steffens-Nakken, H., Reutelingsperger, C. A novel assay for apoptosis. Flow cytometric detection of phosphatidylserine expression on early apoptotic cells using fluorescein labelled Annexin V. Journal of Immunological Methods. 184 (1), 39-51 (1995).
- Elmore, S. Apoptosis: A Review of Programmed Cell Death. Toxicologic Pathology. 35 (4), 495-516 (2007).
- Saelens, X., et al. Toxic proteins released from mitochondria in cell death. Oncogene. 23 (16), 2861-2874 (2004).
- Muse™ MitoPotential Kit User's Guide. Luminex Corporation Available from: https://www.luminexcorp.com/muse-mitopotential-kit (2013)
- McIlwain, D. R., Berger, T., Mak, T. W. Caspase functions in cell death and disease. Cold Spring Harbor Perspectives in Biology. 5 (4), 008656 (2013).
- Wigdal, S. S., Kirkland, R. A., Franklin, J. L., Haak-Frendscho, M. Cytochrome c release precedes mitochondrial membrane potential loss in cerebellar granule neuron apoptosis: lack of mitochondrial swelling. Journal of Neurochemistry. 82 (5), 1029-1038 (2002).
- Muse® Caspase-3/7 Kit. Luminex Corporation Available from: https://www.luminexcorp.com/muse-caspase-3-7-kit/#overview (2019)
- Häcker, G. The morphology of apoptosis. Cell and Tissue Research. 301 (1), 5-17 (2000).
- Muse® Multi-Color DNA Damage Kit User's Guide. Luminex Corporation Available from: https://www.luminexcorp.com/muse-multi-color-dna-damage-kit/#overview (2020)
- Kleeff, J., Kornmann, M., Sawhney, H., Korc, M. Actinomycin D induces apoptosis and inhibits growth of pancreatic cancer cells. International journal of cancer. 86 (3), 399-407 (2000).
- Wlodkowic, D., Skommer, J., Darzynkiewicz, Z. Cytometry of apoptosis. Historical perspective and new advances. Experimental oncology. 34 (3), 255-262 (2012).
- Szeberenyi, J. The effect of actinomycin D on RNA metabolism in human cells. Biochem Mol Biol Educ. 34 (1), 50-51 (2006).
- Ginell, S., Lessinger, L., Berman, H. M. The crystal and molecular structure of the anticancer drug actinomycin D--some explanations for its unusual properties. Biopolymers. 27 (5), 843-864 (1988).
- Hou, M. H., Robinson, H., Gao, Y. G., Wang, A. H. Crystal structure of actinomycin D bound to the CTG triplet repeat sequences linked to neurological diseases. Nucleic Acids Res. 30 (22), 4910-4917 (2002).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved