Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Biochemistry
Självmontering av mikrotubulitaptoider
Denna artikel presenterar ett protokoll för bildandet av mikrotubuliaggregat i form av taktoider med MAP65, en växtbaserad mikrotubulär tvärbindare och PEG som trängselmedel.
Cytoskeletten ansvarar för större intern organisation och omorganisation inom cellen, allt utan en chef som styr förändringarna. Detta är särskilt fallet under mitos eller meios, där mikrotubuli bildar spindeln under celldelning. Spindeln är det maskineri som används för att separera genetiskt material under celldelning. För att skapa självorganiserade spindlar in vitro utvecklade vi nyligen en teknik för att rekonstruera mikrotubuli till spindelliknande enheter med en minimal uppsättning mikrotubuliassocierade proteiner och trängselmedel. Specifikt användes MAP65, som är en antiparallell mikrotubulär tvärbindare från växter, en homolog av Ase1 från jäst och PRC1 från däggdjursorganismer. Denna tvärbindare organiserar själv mikrotubuli i långa, tunna, spindelliknande mikrotubuli självorganiserade sammansättningar. Dessa sammansättningar liknar också flytande kristalltaptoider, och mikrotubuli kan användas som mesoskala mesogener. Här presenteras protokoll för att skapa dessa mikrotubuli-taktoider, liksom för att karakterisera formen på enheterna med användning av fluorescensmikroskopi och rörligheten hos beståndsdelarna med användning av fluorescensåtervinning efter fotoblekning.
Celldelning via mitos är en av de viktigaste biologiska processerna för att upprätthålla livet. Mikrotubulifilamenten, som består av tubulindimerer, är väsentliga strukturella element i denna process. Det övergående maskineriet som skapas i metafas när kromosomerna är i linje i cellcentret kallas den mitotiska spindeln på grund av dess form, som är som en spindel av en vävstol täckt av trådar (figur 1A). Det är väletablerat i många organismer att mikrotubuli används i metafas för att trycka och dra kondenserade kromosomer in i mitten av cellen, anpassa dem och ansluta dem till mikrotubuli som kommer att dra dem isär i anafas (Figur 1B, C). Spindeln bildas i både meios (figur 1B) och mitos (figur 1C), skapad av många överlappande mikrotubuli som inte lindas runt den centrala axeln som tråd utan löper parallellt med gränssnittet. Att skapa dessa mikrotubulibaserade strukturer kräver associerade proteiner som tvärbinder och associerade enzymer som kan fungera som motorer för att hjälpa till att trycka och dra kromosomerna1.
Studier av meiotiska spindlar har visat att mikrotubuli är korta, dynamiska och överlappande i tvärbundna arrayer 2,3,4,5,6 (figur 1Di). På grund av den fysiska organisationen av dessa korta mikrotubuli liknar den meiotiska spindeln en flytande kristall taktoid (Figur 1E). Faktum är att spindlar har visat sig samlas och smälta samman, som man kan förvänta sig av flytande kristalltaptoider5.
Många studier som går tillbaka till 1960-talet har använt fixering, seriella sektioner och elektronmikroskopi för att bestämma att det finns två typer av mikrotubuli inuti den mitotiska spindeln 7,8,9,10. Den första typen kallas kinetochore mikrotubuli, som förbinder spindelpolen med kinetokore. Den andra typen kallas interpolära eller polära mikrotubuli, som växer förbi kromosomerna och överlappar varandra vid mittzonen (Figur 1Dii)8,9,10. En tredje typ kallas de astrala mikrotubuli, som ligger utanför spindeln och förbinder polerna med cellkanten; dessa mikrotubuliorganisationer ligger utanför ramen för den aktuella diskussionen. Det har nyligen gjorts studier om interaktionen mellan augmin6 och gamma-tubulinringkomplex som påverkar kärnbildningscentra för mikrotubuli, vilket resulterar i en mitotisk spindel med kortare mikrotubuli som i figur 1D.
Eftersom mikrotubuli är längre än de är breda, med ett högt bildförhållande och hög styvhet, är de som uppskalade versioner av flytande kristallmolekyler. Inom mjukämnesfysik har atomer och molekyler approximerats med hjälp av minimala interaktioner för att härleda de fysikaliska mekanismerna för fasövergångar, inklusive kärnbildning och smältning av kristaller11. På samma sätt är mikrotubuli mesoskalaobjekt som är uppskalade versioner av flytande kristallmolekyler, vilket ger insikter i fysiken för flytande kristalldynamik, inklusive kärnbildning och tillväxt av de nematiska faserna från isotropa. Vidare, som diskuterats ovan, visar den meiotiska spindeln egenskaper som de hos en flytande kristall taktoid, ett nematiskt tillstånd som kärnar och växer från det isotropa tillståndet hos flytande kristallmolekyler 3,4,5. För taktoider är kärnbildning och tillväxt som för andra kristaller (dvs kräver en relativt hög koncentration av mesogener [molekylerna som bildar flytande kristaller]). Den unika "spindel" -formen på taktoiden kommer från den lokala inriktningen av de flytande kristallmesogenerna som anpassar sig till den nematiska fasen (figur 1E). De kan inte bilda en rundad kristall eftersom molekylerna är mycket asymmetriska. Med tanke på mikrotubulis natur är det kanske inte förvånande att det mitotiska spindelmaskineriet tillverkat av en hög lokal koncentration av mikrotubuli också har samma form, oavsett om det kallas en taktoid eller spindel. Tactoider kan vara bipolära, med poler vid de avsmalnande ändarna (figur 1Ei), eller homogena, med poler effektivt vid oändligheten (figur 1Eii).
Med tanke på vikten av spindelbildning har ansträngningar pågått mot självorganiserad spindelbildning in vitro genom att demonstrera mikrotubulär kondensation i buntar via joniska arter12,13, trängselmedel som skapar utarmningsinteraktioner 14,15 och specifika mikrotubuli tvärbindande proteiner 13,16,17,18,19, 21. Överraskande, även om dessa medel alla arbetar för att öka den lokala koncentrationen av mikrotubuli, resulterar de ofta i långa mikrotubulibuntar men inte taktoider. En anledning till att dessa buntar är långa kan vara att mikrotubuli som utgör dem också är långa. Nyligen utfört arbete med kortare mikrotubuli rapporterade också längre buntar som inte är avsmalnande i slutetav 15; i detta fall hålls buntarna ihop med motorproteiner som orsakar förlängning av buntarna och därigenom gör dem längre. Korta mikrotubuli med icke-extensila tvärbindare behövs för avsmalnande, spindelliknande enheter, som beskrivs här.
Nyligen har vi utvecklat en teknik för att möjliggöra skapandet av mikrotubulära takttoider med hjälp av den antiparallella tvärbindaren, MAP65, i närvaro av kärnbildande stabila mikrotubuli22. Mikrotubuli behövde vara korta, men få kända regulatorer av mikrotubulilängd kan täcka mikrotubuli mot dynamisk instabilitet eller glödgning från ände till ände. Istället användes GMPCPP för att kärnbilda och stabilisera filamenten efter tillväxt. Detta möjliggjorde skapandet av en hög densitet av korta mikrotubuli som kunde självorganisera sig i taktoider. Dessa taktoider var homogena när de betraktades under birefringence. Förutom korta mikrotubuli användes en specifik antiparallell tvärbindare, MAP65, för att bilda taktoiderna (figur 2). MAP65 är ett växtmikrotubuliassocierat protein i PRC1/Ase1-familjen av mitotiska tvärbindare23. MAP65 existerar som en dimer, med en stark affinitet att binda till sig själv såväl som mikrotubuli24. Till skillnad från den meiotiska spindeln och taktoiderna som observerats med aktinfilament 25,26,27, som är bipolära och har de vätskeliknande egenskaperna hos flytande kristaller, har mikrotubuli taktoider observerats vara fastliknande22,28.
Här presenteras protokoll för att skapa mikrotubuli-takttoider och karakterisera formen på sammansättningarna och rörligheten hos beståndsdelarna med hjälp av fluorescensbaserade tekniker.
OBS: Om inget annat anges kan delar av experimentet utföras på en labbbänk medan du bär lämplig skyddsutrustning (handskar).
1. Täckglas silanisering
OBS: Täckglas måste silaniseras för att kunna användas med polymerborstbeläggningen som används i dessa experiment. Detta är en hydrofob silaniseringsbehandling som gör att en blocksampolymer med ett hydrofobt centralt block kan binda och skapa en polymerborste. Följande steg bör utföras i en dragskåp för att förhindra exponering för giftiga ångor när du bär handskar. Dimetyldiklorsilan är mycket giftigt och måste hanteras med största försiktighet.
- Skölj täckglassen med ddH2O, 70% etanol och ddH2O i ordning. Torka dem med luddfria laboratorieservetter mellan varje sköljning. Detta tar bort damm och vattenlösliga eller organiska partiklar från ytan före behandling.
- Placera täckglasen i ett metallöverdragsställ och överför racket till en UV-ozonmaskin (UVO). Bestråla täckglasen med UVO i 20 minuter för att ta bort eventuell bakgrundsfluorescens. En plasmakammare kan användas istället för UVO.
- Använd pincett och överför täckglasen från metallstället som används för UVO-behandling till ett annat metallställ som används för silanisering. Använd inte samma rack för båda, eftersom det kommer att orsaka höga oxidationsnivåer när UVO appliceras. Förrensa racken med vatten och etanol så att inga restkemikalier finns kvar från tidigare användningar.
- Sänk ner stället med täckglassen i en behållare med 100% aceton i 1 timme. Skölj behållaren 3x med kranvatten och sedan 3x med ddH2O för att ta bort all aceton.
- Sänk ner racket med täckglasen i 100% etanol i 10 min. Skölj behållaren 3x med kranvatten och sedan 3x med ddH2Oför att ta bort all etanol.
- Sänk ner racket med täckglasen 3x i ddH2O i 5 min vardera.
- Sänk ner racket med täckglasen i 0,1 M KOH (50 ml 1 M KOH i 450 ml ddH2O) i 15 minuter. Skölj behållaren 3x med kranvatten och sedan 3x med ddH2O för att ta bort all KOH.
- Sänk ner racket med täckglas 3x i ddH2O i 5 min vardera.
- Lufttorka stället med täckglasögonen över natten i en dragskåpa eller laminär flödeshuv.
- Efter att ha torkat racket och täckglasen helt, sänk ner dem i 5 minuter i 2% dimetyldiklorsilan (DDS) som tas i en annan behållare som används speciellt för silan. Låt inte något som inte är torrt komma i kontakt med silan.
- Sänk ner stället och täckglasen 2x i en behållare med 100% etanol i 5 min. Skölj behållaren 3x med kranvatten och sedan 3x med ddH2O.
- Sänk ner racket och täckglasen 3x i ddH2O i 5 minuter vardera.
- Lufttorka stället med täckglasögonen över natten i en dragskåpa eller laminär flödeshuv.
- Efter detta sista torkningssteg överför du täckglasen tillbaka till täckglas med pincett. Dessa täckglas kan användas under de närmaste 1-2 månaderna. Gamla täckglas börjar förlora sin beläggning och bör kasseras.
2. Tubulin beredning
OBS: Det köpta tubulinet kommer som ett frystorkat pulver som antingen är omärkt eller märkt med fluoroforer. Frystorkat tubulin förvaras i en frys på −80 °C. Följande procedur används för att blanda omärkt tubulin med märkt tubulin i ett förhållande som är bra för visualisering.
- Avlägsna en alikvot av omärkt tubulin innehållande 1 mg fryskrofiliserat tubulin från frysen vid −80 °C och förvara den på is. Tillsätt 200 μl kall PEM-80 till röret för att få tubulinkoncentrationen till 5 mg / ml. Håll den på is i 10 minuter för att lösa upp allt frystorkat.
- Ta bort en alikvot rhodaminmärkt tubulin som innehåller 20 μg frystorkat tubulin från −80 °C frys och förvara den på is. Tillsätt 4 μl kall PEM-80 till röret för att få tubulinkoncentrationen till 5 mg / ml. Håll den på is i 10 minuter för att helt lösa upp frystorkat.
- När den är upplöst, tillsätt 100 μL omärkt resuspenderad tubulinlösning till 4 μL-lösningen av rhodaminmärkt tubulin. Pipettera 6x-7x mycket långsamt för att blanda. Om aggregat är synliga, centrifugera det solubiliserade tubulinet i 10 minuter vid 90 000 x g för att avlägsna aggregat genom att kassera pelleten och behålla supernatanten. Denna tubulinblandning kommer att resultera i ~ 4% märkt tubulin.
- Droppfrys de återstående 100 μl omärkta tubulinerna till flytande kväve (LN2) och förvara det vid −80 °C för att användas för ytterligare tubulinblandningar.
- Ta den märkta tubulinblandningen och alikvotera i sju rör med 15 μl vardera. Varje alikvot kan användas för en enda experimentkammare. Droppfrys de återstående alikvoterna och förvara dem vid −80 °C för framtida experiment.
3. MAP65-rening
OBS: MAP65 är inte kommersiellt tillgänglig och måste därför renas för detta arbete. Protokollet har tidigare utvecklats i flera publikationer23,29.
- Omvandla MAP65-plasmiden och GFP-MAP65-plasmiden till BL21-bakteriestammen för proteinuttryck.
- Odla BL21-bakterier till en optisk densitet på 0,6-1 vid 600 nm. Inducera proteinproduktion med hjälp av lac-operatören och odla bakterierna över natten.
- Pelletera kulturerna och lysera bakterierna.
- Samla lysaten efter centrifugering och inkubera den med pärlor som har en nickeljon tillgänglig för att binda 6x-histidintaggen.
- Elue proteinet med imidazol och avsalta det.
- Droppfrys proteinet med flytande kväve och förvara det vid −80 °C för användning inom 1 år.
4. Montering av flödeskamrar
OBS: Experiment utförs i flödeskammare gjorda av en glasskiva och silaniserat täckglas (figur 3).
- Ta en glasskiva och rengör den medddH2O, etanol och ddH2Oi ordning. Torka med en luddfri laboratorietork mellan varje sköljning.
- Använd en bit dubbelhäftande tejp för att skapa en flödesbana. Skär tejpen med handskar till ~ 25-30 mm i längd. Dela tejpen på längden för att skapa två tunnare remsor. Placera de två tejpremsorna på bilden med ca 5-8 mm mellan dem.
OBS: Eftersom tejpens tjocklek är standardiserad till cirka 80-100 μm, kommer bredden på vägen mellan tejpbitarna att bestämma volymen i kammaren. - Placera de silaniserade täckglasen ovanpå flödesbanan. Försegla bilden och täckglaset till de dubbelsidiga tejpremsorna genom att försiktigt trycka på tejpområdet med baksidan av en penna. Se till att få en bra tätning över hela området; tejpen ska vända sig från genomskinlig till klar när tätningen görs bra.
- Ta bort den extra tejpen på kanterna och lämna endast 1 mm från flödeskammarens ingång genom att klippa tejpen med ett rakblad.
- Märk kammaren med information om de experimentella parametrarna, efter behov.
5. Tactoid experiment
OBS: När alla reagenser och förnödenheter har genererats kan de användas för att nukleera och polymerisera mikrotubulära takttoider i flödeskammaren.
- Samla alla reagenser som ska användas. Tina dem på is och förvara dem på is medan du arbetar. Gör flera flödeskamrar för experimenten.
- Använd en flödeskammare för varje experiment. Täck flödeskammarytorna med en polymerborste genom att flöda i 20 μL 5% icke-joniskt block-sampolymertensider (materialtabell) upplöst i PEM-80, med små droppar i båda ändarna av kammaren för att förhindra bildandet av luftbubblor inuti. Förvara detta i en fuktig kammare (dvs. petriskål med en våt luddfri laboratorieservett) tills den är klar att användas (minst 5-7 min).
- Blanda följande i ett sterilt rör för att skapa Tubulin-MAP-blandningen: 9,5 μl PEM-80; 4 μl 10 mM GMPCPP; 4 μL 5% Pluronic-F127; 1 μl 1M DTT; 1 μl glukos; 2 μl polyetylenglykol (PEG); 12 μl 5 mg/ml tubulinblandning (13,6 μM slutlig koncentration) från steg 2.5. och 5,5 μl arbetslager av MAP65 där 10% är GFP-MAP65 för visualisering. Håll på is medan du blandar.
OBS: Det rekommenderas att använda en positiv förskjutningspipett för hantering av den viskösa PEG-lösningen. Vanliga pipetter kan användas efter skärning av spetsen för att göra öppningen större; denna metod är dock mindre exakt. - Blanda 5x-6x genom pipettering.
- Strax innan du lägger till kammaren, tillsätt 1 μL av en förblandad lösning av glukosoxidas (0,5 mg / ml) och katalas (0,15 mg / ml) (Deoxi) i Tubulin-MAP-blandningen och blanda 7x-8x. Dela den totala volymen av lösningen (40 μL) i två delar som ska användas i separata kamrar.
- Flöda Tubulin-MAP-blandningen i kamrar. Eftersom kamrarna redan har icke-joniskt block-sampolymertensider i sig, kan mer vätska inte tillsättas utan att ta bort den gamla vätskan. För att göra detta, använd en bit filterpapper eller en luddfri laboratorietork i andra änden av kammaren för att ta bort vätska via kapillärverkan.
- När provet är helt inne i kammaren, försegla kammarens två ändar med 5-minuters epoxi och håll det vid 37 ° C i ~ 30 minuter för att kärna och odla mikrotubuli taktoider.
6. Fluorescensmikroskopi
- Använd ett fluorescensmikroskop för att avbilda takttoider.
OBS: Total intern reflektion fluorescensmikroskopi eller snurrande skivkonfokalmikroskopi är bra för att ta bort bakgrundsfluorescens från fritt tubulin, men taktoider är också synliga genom regelbunden epi-fluorescens och till och med överförd ljusmikroskopi när de har bildats, vilket gör denna procedur tillgänglig utan specialutrustning. - Använd ett numeriskt bländarmål (NA) på 1,2 NA eller högre med en förstoring på 60x eller högre för att samla tillräckligt med ljus i fluorescens. Dessa mål kräver ofta nedsänkning i antingenddH2Oeller olja.
- Spela in bilder med CMOS- eller CCD-kamera. Använd en effektiv pixelstorlek på kameran på 108 nm.
OBS: Pixelstorleken beror på kameran och förstoringen som användes, som i detta fall var 60x eller 100x med en hög numerisk bländare (1,2 eller 1,49 NA). Ytterligare bildutvidgare kan användas före kameran för att uppnå den nödvändiga pixelstorleken. - Förvara provet vid 37 °C med hjälp av en miljökammare inställd på denna temperatur. Alternativt kan du använda andra stegvärmare inklusive varmluftsvärmare och objektiva temperaturkontrollerade krage med cirkulerande varmt vatten.
- Använd excitationskällor som är korrekta för den fluorescens som behövs. För rhodamin tubulin, använd en 561 nm laser med minst 1 mW effekt vid provet, och för GFP-MAP65, använd en 488 nm laser med minst 1 mW effekt vid provet.
OBS: Om du använder epi-fluorescensmikroskopi med brett fält, använd en rhodaminfilterkub med excitation: 540 ± 12,5 nm, dikroisk: 545 nm ± 12,5 nm avstängning och utsläpp: 575 nm långt pass och en GFP-filterkub med excitation: 480 ± 15 nm, dikroisk: 505 nm ± 15 nm avstängning och utsläpp: 515 nm långt pass. - Ta minst 10 bilder av olika områden för att avbilda över 100 taktoider. Ta bilder i både de röda och gröna kanalerna och spara dem som 16-bitars tiff-bilder för analys. Se till att belysningseffekten och exponeringstiderna är sådana att intensitetsskalan för kameran inte är mättad.
7. Fluorescensåtervinning efter fotoblekning (FRAP)
OBS: För att studera rörligheten hos de inre beståndsdelarna i tactoider användes FRAP. FRAP fungerar genom att fotoblekta en utvald del av rhodaminmärkt tubulin och GFP-märkt MAP65 tactoid och sedan observera återhämtningen av fluorescensen med tiden i den regionen. Återhämtningshastigheten beror på omsättningen av arten som fotoblekas. Denna omsättningshastighet kan bero på diffusion och bindande reaktioner. För MAP65-bindning till tactoider kan bindande växelkurser uppskattas. FRAP utförs med hjälp av ytterligare ett 405 nm lasersystem som kan skanna lasern i vilken form som helst. Det finns många möjligheter att utföra FRAP, inklusive att använda den överförda lampan och bländaren för att fotoblecka ett lokalt område14.
- Välj en isolerad taktoid i kammaren för att skapa en intressant region (ROI) som täcker delar av takttoider och den omgivande lösningen.
- Använd ett mikroskop med ytterligare 405 nm laser för FRAP för att fotoblechera både tubulin och MAP65 samtidigt. Alternativt kan en ljus lampa användas genom fältstoppet på iris14. Justera den specifika intensiteten hos fotoblekningssystemen empiriskt för att undvika att skada proteinerna under blekning.
- Spela in tactoid som en tidsseriefilm i 30-60 s innan du fotoblecherar för att få information om intensiteten före blekmedlet. Spela in både de röda och gröna kanalerna.
- Fotoblechera takten genom att exponera ROI med antingen lasrarna eller lampan så länge som behövs för att fotoblechera utan att skada takten. Bestäm intensiteten och tiden empiriskt.
- Fortsätt att spela in filmen i båda färgkanalerna i 5-10 minuter efter fotografering eller tills återhämtningen verkar ha nått jämvikt.
- Inspektera GFP-MAP65-kanalen visuellt för återställning.
8. Analys av data
OBS: Kvantitativ analys av bilderna av tactoider utfördes för att lära sig om effekterna av miljöförändringar som infördes via olika trängselmedel, joniska förhållanden och tillägg av andra faktorer.
- Karakterisering av taktform
- Kvantifiera längden och bredden på taktoiderna från de röda och gröna bilderna tagna med konfokalmikroskopi.
- Öppna bilderna med FIJI/ImageJ.
- Om rådata tas i 16-bitars, justera ljusstyrkan och kontrasten om det behövs. Välj Bild > Justera > Ljusstyrka och Kontrast för att justera bilden för att kunna se takttoformen tydligt. Justera ljusstyrkan och kontrasten utan att använda inställningen för att inte oavsiktligt ändra intensitetsdata.
- När taktoiderna är tydligt synliga, välj bra taktoider att mäta (figur 4Bi). Se till att taktoiderna är tydligt synliga utan överlappning med andra taktoider eller aggregat och inte är böjda eller böjda för att kunna använda linjära mätverktyg.
- Kontrollera sedan att rätt pixelstorlek är inställd för bilderna. Mikroskopbilderna kommer med metadata om pixelstorleken. När du använder en annan kamera som inte har metadata eller externa bildexpansionssystem som kan ändra den förväntade effektiva pixelstorleken justerar du pixelstorleken manuellt. I FIJI/ImageJ går du till Analysera > Ställ in skala för att ställa in rätt pixelkonvertering.
- Använd verktyget Straight Line från verktygsfältet i FIJI/ImageJ, klicka på ena änden av takttoida och dra markören till den andra änden av takttoida (figur 4Bii). När linjen ROI har valts väljer du Analysera > Mått för att mäta längden. Om längden inte mäts som standard måste du ange att måttet ska inkludera längd i dialogrutan Analysera > Ange mått .
OBS: Vanligtvis, när du mäter med straight line-verktyget , kommer det att ge längden och vinkeln på den ritade linjen. Som ett exempel visar figur 4Bii en rak linje dragen till sidan av takttolen för att göra den senare synlig men gör mätningen direkt på takten. - När du har gjort mätningen använder du textverktyget i verktygsfältet för att märka takten. Skapa en textruta, lägg till en sifferetikett och välj Redigera > Rita för att åtgärda etiketten i bilden. Spara bilden som en separat ROI-fil.
OBS: Märkning och sparande av den här filen gör det möjligt för utredaren att veta vilken mätning som motsvarar vilken taktoid från rådata. Se till att mäta varje taktoid en gång. - När taktoiderna för hela bilden har mätts sparar du data i fönstret Resultat i en komma- eller tabbavgränsad textfil (med Fil > Spara som) och öppnar data i ett kalkylprogram för att parsa data i siffror. Samla alla data tillsammans (råbilddata, ROI-bild och textfil med resultat) i en mapp med en lämplig namngivningskonvention för att hålla allt organiserat.
OBS: Även om tactoidlängdsmätningar utförs för hand, med tanke på att takttobredderna är smala, är det bättre att använda en annan metod för att mäta takttodbredd (se nedan) för att minska mätfelet. - Använd ImageJ/FIJI och rita ett linjeområde med verktyget Rak linje . Rita linjen som en vinkelrät bisektorer till den taktoida långa axeln (figur 4Bii).
- Välj Analysera > plottprofil för att skapa intensitetsprofilen för den linjära bisektorn (bild 4Biii). En tomt kommer att visas. För att hämta och spara data från diagrammet, välj knappen Lista längst ner till vänster; Detta genererar textfillistan över intensitetsdata längs längden på den ritade linjen. Spara textfilen som en .csv- eller .txt fil.
- Öppna textfilen i ett passande program som MatLab, Python (sciPy) eller andra program. Anpassa intensitetsdata med en gaussisk funktion av formen:
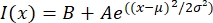 , där I(x) är gråskalevärdet längs längden, x; B är bakgrundsnivån; A är gaussens amplitud; μ är gaussernas medelvärde eller centrum; och σ är gaussens standardavvikelse.
, där I(x) är gråskalevärdet längs längden, x; B är bakgrundsnivån; A är gaussens amplitud; μ är gaussernas medelvärde eller centrum; och σ är gaussens standardavvikelse. - Rapport 2σ som bredden på takttoida. Uppskatta intensiteten hos mikrotubuli i taktoiden genom att beräkna området under Gaussian (exklusive bakgrunden).
OBS: Om bilderna ligger inom kamerans linjära intensitetsområde och tas med samma exponeringstid och excitationsintensitet, kan integrerade intensiteter jämföras för att uppskatta det relativa antalet mikrotubuli i takttoider.
- FRAP-analys
OBS: Experiment för att testa rörligheten hos mikrotubuli och MAP65 använde FRAP för att registrera den specifika fotoblekningen och återhämtningen av intensitet på grund av molekylär rörelse (figur 5A). Data kvantifierades från bildtidsseriedata med hjälp av ImageJ/FIJI.- Använd ImageJ/FIJI för att öppna filmdata.
- Registrera stackarna (tidsseriedata) över tid för att ta bort avdrift. Använd StackReg-plugin tillsammans med tillhörande TurboReg-plugin ; För instruktioner om hur du använder plugins, se webblänkarna i materialförteckningen. Välj översättning för att flytta ramarnas position och därmed registrera bilderna.
- När bilderna har registrerats för att ta bort avdrift roterar du bilden så att takten är antingen lodrät eller vågrät i ramen genom att välja Bild > Transformera > Rotera. Välj vinkeln som ska roteras och använd Förhandsvisning för att avgöra om takten roteras tillräckligt. När förhandsgranskningen visar att takten är antingen lodrät eller vågrät väljer du OK för att rotera alla bilder i filmen.
- Använd rektangelmarkeringsverktyget i verktygsfältet för att skapa ett rektangulärt avsnitt över det fotoblekta området i tactoiden. Registrera den integrerade intensiteten för ROI-området för varje bildruta med hjälp av Image > Stacks > Measure Stack. Ställ in måtttypen på Integrerad densitet med hjälp av Analysera > Ställ in mätningar. Spara de analyserade intensitetsdata som visas i fönstret Resultat som en textfil i .csv- eller .txt format genom att välja Arkiv > Spara som.
OBS: Figur 5B visar ett exempel på de råa 16-bitars intensitetsdata som uppmätts för mikrotubuli- och GFP-MAP65-kanalerna i blekmedelsområdet. - Eftersom bildernas totala intensitet kommer att blekna med tiden globalt på grund av fotoblekning orsakad av avbildning, måste denna globala fotoblekning korrigeras. Det gör du genom att använda samma ROI-storlek (steg 8.2.4.) och flytta den till ett område i bildens bakgrund där inga mikrotubuli eller MAP65 är synliga. Mät stackens integrerade intensitet enligt beskrivningen i steg 8.2.4. Spara resultatet som en andra textfil.
Obs: Figur 5B visar ett exempel på råa 16-bitars intensitetsdata uppmätta för mikrotubuli och GFP-MAP65-kanaler i bakgrundsområdet. - För att korrigera bakgrundsblekningen, dela signalintensiteten på tactoiden med bakgrundsintensiteten för samma tidpunkt. Beräkna Ikorrigerad (t) som:
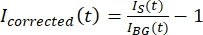 , där IS (t) (signalen) är mätningen som gjorts på det blekta området och IBG (t) (bruset) är mätningen som gjorts på bakgrundsområdet (figur 5C). Detta beräknar signal-brusförhållandet för varje ram och subtraherar också bruset.
, där IS (t) (signalen) är mätningen som gjorts på det blekta området och IBG (t) (bruset) är mätningen som gjorts på bakgrundsområdet (figur 5C). Detta beräknar signal-brusförhållandet för varje ram och subtraherar också bruset. - Skala sedan om data så att de sträcker sig mellan noll och en med ,
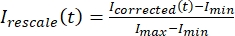 där Imin och Imax anger det globala minimumet respektive maximumet av I-korrigerade data under hela tiden (Figur 5C).
där Imin och Imax anger det globala minimumet respektive maximumet av I-korrigerade data under hela tiden (Figur 5C). - Anpassa dessa data till en sönderfallande exponentiell form:
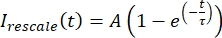 , där A är amplituden för återhämtningen och τ är tidsskalan för återhämtningen (figur 5C).
, där A är amplituden för återhämtningen och τ är tidsskalan för återhämtningen (figur 5C).
Med endast ett litet antal komponenter, tubulindimerer och mikrotubulära tvärbindare kan mikrotubuli-takttoider bildas (figur 2A). Även om detta protokoll beskriver inkubation för att kärna och odla mikrotubuli i en inkubator, kan kärnbildning och tillväxt observeras direkt under mikroskopet (som är fullständiga inom 30 min) (Figur 2B). Koncentrationen av tubulin hålls konstant vid 13,6 μm och MAP65-MT-bindning vid 10%.
Bild 4 representerar lyckade data. Takttoider ska vara synliga med både en 561 nm laser i tubulinkanalen och 488 nm i MAP65-kanalen, som perfekt överlappar varandra (figur 4A). Ett mysterium med systemet har varit att bredden på takttoider inte verkar variera under en mängd olika experimentella förändringar, inklusive ändring av mikrotubulilängderna, MAP65-koncentrationen och trängselmedlen (figur 4B)22,28. Längden är mycket mer variabel och beror på både mikrotubulilängderna och MAP65-koncentrationen (figur 4B)22,28.
Vid utförande av FRAP har det observerats att MAP65-signalen återhämtar sig, men mikrotubulisignalen återhämtar sig inte (figur 5). Återhämtningen i FRAP beror på rörligheten och rörelsen hos de märkta och fotoblekta föremålen. När det gäller MAP65 dissocierar de mörka molekylerna och rör sig bort från mikrotubuli och nya flyttar in i regionen (figur 5). MAP65-bindningen är i jämvikt, så bindningshastigheten och avbindningshastigheten är lika (mätt i molekyler per sekund). För mikrotubuli sågs ingen återhämtning som innebär att mikrotubuli inte kan lämna takten (figur 5A, Bi, C). Vidare sågs ingen spridning av den mörkare regionen, vilket tyder på att mikrotubuli är lokalt orörliga och inte en vätska inom taktoidformen.
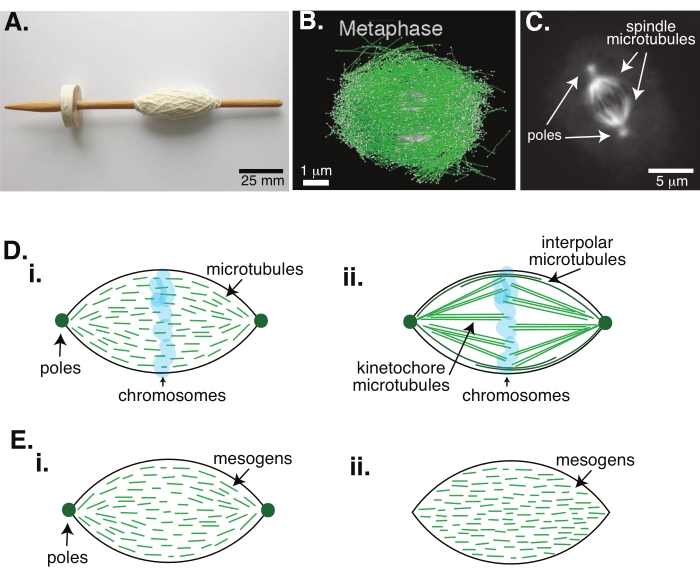
Figur 1: Olika modeller av spindelbildning. En mitotisk spindel är en maskin gjord av mikrotubuli och deras associerade proteiner och enzymer som justerar och separerar kromosomerna i de två nya dottercellerna under celldelning. (A) Bild av en tidig medeltida droppspindelreplika med fint garn från Holland. Denna figur har modifierats från en Wikimedia-bild av Peter van der Sluijs30. (B) Tredimensionell rekonstruktion av mikrotubuli i olika stadier av vildtyp meios II. Mikrotubuli visas i grönt och kromosomer visas i grått. Skalstreck = 1 μm. Denna siffra har modifierats från Lantzsch et al.31. (C) Mikroskopibild av mikrotubuli i en mitotisk spindel av en delande Sf9-cell. Spindelpolerna och spindelns mikrotubuli är märkta med ett grönt fluorescerande protein. Skalstreck = 5 μm. Denna siffra har modifierats från Advani et al.32. (D) Olika modeller av hur mitotiska och meiotiska spindelmikrotubuli är organiserade. (i) Tidigare observerats för meiotiska spindlar skapade från Xenopus äggextrakt, mikrotubuli (grön) härleddes för att vara korta och dynamiska i hela spindeln. Detta liknar en bipolär taktoid organisation inuti en flytande kristall. (ii) Den kanoniska modellen för mikrotubuliorganisation inuti en mitotisk spindel har två typer av mikrotubuli: interpolära eller polära mikrotubuli (mörkgröna) som tvärbinder vid mittzonen runt kromosomerna och kinetokoremikrotubuli (ljusgröna) som buntas och sträcker sig från polen till kinetokore för att trycka och dra kromosomerna. I alla bilder visas kromosomer i transparent blått och spindelpoler representeras i mörkgrön. (E) Scheman för mesogener (gröna linjer) i en flytande kristall taktoid för (i) bipolär och (ii) homogena taktoider. Bipolära taktoider har två poler i slutet av taktoiden, och mesogenerna omorienterar för att peka på dessa poler. Homogena taktoider har poler i oändlighet, och mesogenerna ändrar inte orientering längs taktoidens längd. Klicka här för att se en större version av denna siffra.
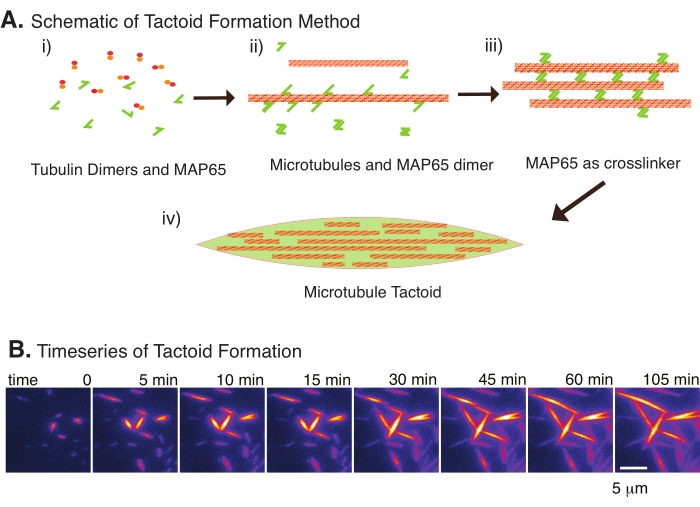
(A) Mikrotubuli kan buntas och tvärbindas med en mängd olika metoder inklusive joniska arter, utarmningskrafter orsakade av trängselmedel och specifika mikrotubulära tvärbindare, såsom MAP65. (i) Tubulindimerer och MAP65-proteiner blandas för att kärna och odla mikrotubuli. (ii) Mikrotubuli kärnar och växer från tubulinet, och MAP65 binder omedelbart till mikrotubuli, en annan MAP65-monomer, eller båda och orsakar buntning. (iii) Mikrotubuli i de tvärbundna buntarna kärnar och växer. (iv) Den slutliga konfigurationen är en mikrotubulär taktoid som liknar en spindel. (B) Tidsserier av mikrotubuli takttoider som kärnar och växer över 105 minuter. Skalstreck = 5 μm. Figur anpassad från Edozie et al.22. Klicka här för att se en större version av denna siffra.
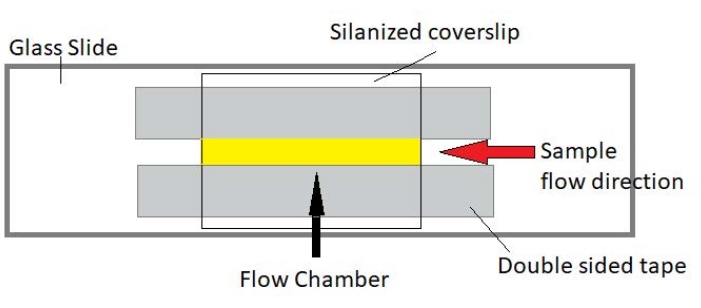
Figur 3: Flödeskammarenhet. Flödeskammaren är gjord med hjälp av en glasskiva, silaniserat täckglas och permanent dubbelsidig tejp. Det gula markerade området är flödesvägen där provet flödas och observeras. Flödeskammarens volym är ~ 20 μL. Epoxi användes för att täta kammarens ändar för att förhindra att provet avdunstar under långvarig avbildning under flera timmar. Klicka här för att se en större version av denna siffra.
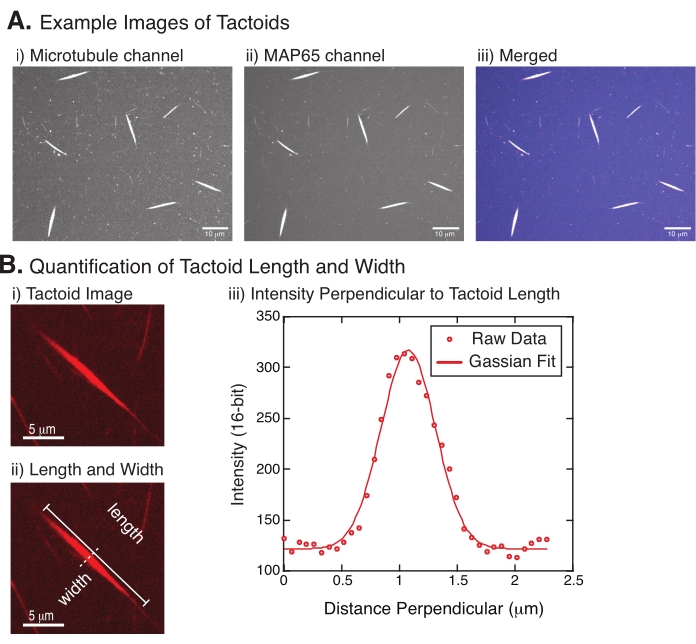
Figur 4: Tactoidbilder och längd- och breddanalys. (A) Exempeldata för taktoider bildade enligt beskrivningen och bilden med hjälp av snurrande skivkonfokal som visar (i) mikrotubulikanalavbildning av rhodaminmärkt tubulin med hjälp av en 561 nm laser, (ii) GFP-MAP65-kanal som avbildar GFP med en 488 nm laser och (iii) sammanfogad överlagringsbild från mikrotubulikanalen (magenta) och GFP-MAP65-kanalen (cyan). Överlappningsregioner visas som vita och visar att mikrotubuli och MAP65 samlokaliseras exakt. Skalstreck = 10 μm för alla bilder i (A). (B) Kvantifiering av taktoidlängd och bredd. (i) Bild av en tactoid som ska analyseras utan etiketter. Skalstreck = 5 μm. (ii) Samma bild som i (i), där måtten längd (heldragen linje med linjekapsyler) och bredd (streckad linje) betecknas. Skalstreck = 5 μm. (iii) Bredden mättes genom att ta intensitetsprofilen över takttoden vid den vinkelräta bisektorn (streckad linje) betecknad i (ii). Intensitetsprofilen passade till en gaussisk funktion för att avslöja takttoformens amplitud och bredd. Klicka här för att se en större version av denna siffra.
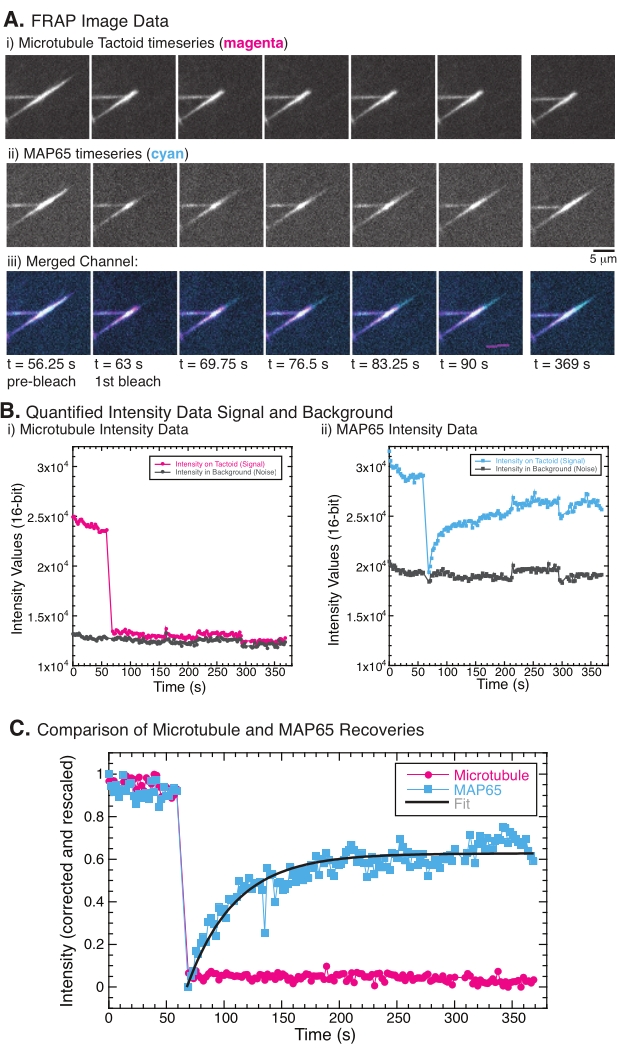
(A) Mikroskopitidsseriedata för (i) mikrotubuli taktoid och (ii) GFP-MAP65, och (iii) överlagringsbild av båda kanalerna med mikrotubuli i magenta och GFP-MAP65 i cyan som fotoblekades vid tiden 63 s och observerades i ytterligare 5 minuter (B) Kvantifierad intensitet av (i) ) mikrotubulikanal i det blekta området (magenta cirklar) och bakgrunden (mörkgrå ringar) och (ii) GFP-MAP65-kanalen i det blekta området (cyanrutor) och bakgrunden (mörkgrå rutor). (C) Uppgifterna korrigerades för bakgrundsbruset och skalades om för mikrotubulikanalen (magentacirklarna) och GFP-MAP65-kanalen (cyanrutor). Mikrotubuli återhämtar sig inte, men GFP-MAP65 gör det och kan passas (mörkgrå linje) till ett stigande exponentiellt sönderfall för att hitta amplituden och tidsskalan för återhämtning. Klicka här för att se en större version av denna siffra.
Metoderna som beskrivs här har använts i flera artiklar för att skapa mikrotubuli takttoider (Figur 2)22,28. Dessa experiment är biologiskt relevanta för att hjälpa till att avslöja de organisatoriska principerna som styr formen och stabiliteten hos den mitotiska eller meiotiska spindeln i de flesta celltyper. Dessutom är mikrotubuli modell flytande kristallmesogener som kan hjälpa till att lära sig mer om hur flytande kristaller kärnar och växer nematiska faser från isotropa faser.
Förfarandet som beskrivs här har flera fördelar för att utforska mikrotubuli självorganisation. För det första är det mycket reproducerbart, efter att ha utförts i labbet av många studenter, inklusive gymnasieelever, med liten förkunskap eller träning innan de börjar i labbet. Taktoiderna är birefringenta22, vilket gör att de kan ses i överfört ljus förutom fluorescensmikroskopi, vilket gör denna metod tillgänglig för många laboratorier och detta experimentella förfarande anpassningsbart till utbildningsändamål, förutom avancerad forskning. Slutligen öppnar denna process vägar för att fortsätta förstå och undersöka biologiska system i ett avskalat, reduktionistiskt tillvägagångssätt, så att man kan förstå hur varje ytterligare tillstånd, protein eller tillsats kan förändra självorganisationen av takttoider och kanske i slutändan spindeln. Mål för bättre biomimik inkluderar sortering av aktivitet, fluiditet och filamentpolaritet.
Det kan finnas flera faktorer som påverkar experimentet som ger oväntade resultat. Till exempel, om takttoider inte bildas (figur 2) men fläktliknande mönster observeras, är MAP65 sannolikt inte närvarande eller inte bindande för mikrotubuli22,28. Detta borde också vara uppenbart i MAP65-fluorescenskanalen eftersom GFP-MAP65 inte kommer att vara bunden till mikrotubuli.
Om taktoiderna inte bildas och bakgrunden visas som fläckar på glaset kan det bero på ytbeläggningen. När silaniseringen har utförts varar den bara 1 månad på täckglas. När det slits av kommer tubulinet att kunna binda till den exponerade ytan icke-specifikt. Denna bindning kommer att ske i udda mönster.
Om taktoiderna inte bildas och tubulinet observeras i aggregat av olika former och storlekar, kan detta bero på tubulin av dålig kvalitet. Tubulin kan centrifugeras för att avlägsna initiala aggregat som kan driva denna off-pathway-aggregering istället för mikrotubulipolymerisation. Om ytan är bindande för tubulinet kan den också tömma tubulinet i lösningen. Låga koncentrationer av tubulin, under den kritiska koncentrationen för polymerisering av mikrotubuli, kan resultera i aggregat.
I FRAP-experiment, om MAP65-kanalen inte visar någon återhämtning (figur 5), är det möjligt att fotoblekningen skadade mikrotubuli. Fotoskador orsakar lokal förstöring av filamenten. Detta kan kontrolleras genom undersökning i den överförda kanalen. Mikrotubuli taktoider är synliga i den överförda kanalen genom ett högt brytningsindex som inte överensstämmer med det omgivande vattnet. Ljusinducerad fotoskada kommer att visas som ett brännmärke eller förlust av kontrast vid överföring av ljusavbildning på platsen för ROI som utsätts för fotoblekning. Om detta inträffar måste lasern eller ljuseffekten minskas för att hämma proteinernas fotoskador.
Det fanns flera utmaningar som uppstod i detta förfarande och tillvägagångssätt. Ett problem är att längdmåtten för närvarande utförs för hand genom att klicka på bilden. Även om denna metod är enkel kan den leda till stor osäkerhet. Breddmätningen som använder tvärsnittet och monteringen till en Gaussian är en bättre metod för att kvantifiera storleken. En liknande metod skulle kunna användas för längden. En andra fråga är att ibland kan takttoider, eftersom de är så långa och tunna, böjas. Detta gör det svårare att kvantifiera längden. Konturlängden kan kvantifieras med hjälp av en segmenterad linje, men det finns en extra osäkerhet varje gång ett segment läggs till.
Ur ett vetenskapligt perspektiv har detta tillvägagångssätt några andra utmaningar för dess användning som modell för flytande kristaller eller spindlar. Den första utmaningen har varit den långa, tunna formen på de taktoider som mikrotubuli skapar (figur 3 och figur 4). Som noterats i tidigare publikationer22 är mikrotubulära takttoider homogena taktoider, inte bipolära. Detta innebär att mikrotubuli som utgör formen inte omorienterar för att peka mot strukturens spetsar. Istället är alla mikrotubuli parallella med den långa axeln och "polerna" ligger i oändligheten. Detta skiljer sig mycket från de taktoider som observerats för molekylära flytande kristaller eller till och med för aktin eller DNA som också kan fungera som flytande kristallmesogener. I dessa andra system är takttoider bipolära och när de ses i korsade polarisatorer visar de de tydliga tecknen på omorientering av stavarna.
En andra stor utmaning i detta system är att mikrotubuli är orörliga inuti takten. Detta framgår tydligt av FRAP-experiment och analyser eftersom återhämtningen av mikrotubuli är mycket låg. Deras fasta natur gör mikrotubuli tactoider mindre värdefulla som storskaliga flytande kristallanaloger. Den nematiska fasen av en flytande kristall bör ha både flytande (flytande) och kristall (organiserade) egenskaper. Även om formen verkar rätt för spindeln, gör orörligheten systemet mindre spännande som en modell mitotisk spindel. Å andra sidan ger denna fråga möjligheter att undersöka hur man kan modifiera experimenten för att skapa mer flyt i systemet.
Dessa vetenskapliga utmaningar erbjuder spännande möjligheter som möjliggör ny kunskap om systemet. För att göra mikrotubuli-takttoider mer bipolära kan man använda kortare mikrotubuli. Det finns dock en extra utmaning, eftersom mikrotubuli inte har många väl karakteriserade kapslingsproteiner för att kontrollera längden som aktin gör. Användningen av kärnbildning och tillväxt kräver användning av mycket höga koncentrationer av tubulin och GMPCPP för att göra korta mikrotubuli. Den höga tubulinkoncentrationen resulterar i ett större antal filament i systemet, vilket gör det svårare att separera takttoider från varandra. Tillägget av nya mikrotubulikapslar, såsom DARPin33, kan hjälpa till med denna situation. Den andra frågan om att mikrotubuli är orörliga kan mildras genom tillsats av motorproteiner, såsom kinesin-534, som är tetramerer av motorer som används vid mitos. Alternativt kan konstgjorda dimerer av dimerisk kinesin-1 användas15.
Ett annat sätt att lägga till mer flyt skulle vara att låta mikrotubuli utföra sin dynamiska instabilitet, växande och krympande mikrotubuli. För närvarande är mikrotubuli som är sådda med stabila GMPCPP-filament och sedan genomgår dynamisk instabilitet mycket längre än önskat för att bilda en spindel eller taktoid, vilket skulle resultera i mycket långa organisationer som fläktar eller buntar. Så att lägga till mikrotubuli dynamisk instabilitet skulle behöva göras noggrant för att bevara taktformen. Tillsatsen av associerade proteiner och enzymer som kan kontrollera längden kan mildra problemet. Till exempel skulle depolymeriserande kinesiner, såsom kinesin-1335, eller avskiljande enzymer, som katanin36, sannolikt behövas. Dessa experiment är komplexa och svåra, även om de skulle vara mycket insiktsfulla oavsett vad resultaten avslöjar. Oavsett vilken riktning framtida experiment tar, kan plattformen som utvecklats här för att skapa mikrotubuli-takttoider exponera ny information på den fysiska grunden för mikrotubuliorganisation.
Författarna förklarar att de inte har några konkurrerande ekonomiska intressen.
Författarna vill tacka alla rosslabbmedlemmar sommaren 2021, särskilt K. Alice Lindsay, för deras hjälp. Detta arbete stöddes av ett bidrag från NSF BIO-2134215 som stödde S. Sahu, N. Goodbee, H.B. Lee och J.L. Ross. Ett bidrag från KECK Foundation (Rae Anderson, USD, lead PI) stödde delvis R. Branch och P. Chauhan
| Name | Company | Catalog Number | Comments |
| 2% Dichlorodimethylsilane | GE Healthcare | 118945 | A hydrophobic silane surface treatment. This can be resused upto three times and kept at room temperature for one year. |
| 5-minute epoxy | Bob Smith Industries | For sealing experimental chambers | |
| Acetone | Fisher | 32900HPLC | 100% |
| BL21 cells | Bio Labs | C2527I | Competent bacterial cells used to express MAP65 |
| Catalase | Sigma | C30-500MG | Part of the oxygen scavenging system. A 300 mg/ml stock is made in ddH2O and stored in 10 μl aliquots in -20°C for upto one year. |
| Coverslips (22 mm x 22 mm or 22 mm x 30 mm) | Fisher | 12544-AP | For experimental chambers |
| Dithiothreitol | Sigma | 43815-5G | A small molecule that is used to break disulfide bonds and scavenge oxygen. A 1 M stock is made from powder (Sigma) in ddH2O. The solution is aliquoted and stored at -20C for upto one year. The aliquots are used 7-8 times then discarded. |
| EGTA | Sigma | E3889-10G | Tubulin buffer base ingredient |
| Eppendorf 0.5 ml tubes | Eppendorf | 05 402 18 | For holding experimental solutions |
| Ethanol | Fisher | 111000200 | 200 proof |
| Filter paper | Whatman | 1004-110 | For cleaning and for pulling solutions through experimental chambers |
| Fluorescence microscope with high NA objectives | Nikon | Ti-E, W2 Confocal | For imaging experiments |
| Freezer -20°C | Fisherbrand | 13986148 | For storing reagents |
| Freezer -80°C | Thermo scientific | 328223H01-C | For storing proteins. |
| Glass containers for silanization | Michaels | For preparing experimental chambers - treating cover glasses | |
| Glass slides | Fisher | 12544-4 | For experimental chambers |
| Glucose | Sigma | G7528-250G | Part of the oxygen scavenging system. A 300 mg/ml stock is made in ddH2O and stored in 10 μl aliquots in -20°C. |
| Glucose oxidase | Sigma | G2133-250KU | Part of the oxygen scavenging system. This is stored at 4°C for upto one year. |
| GMPCPP | Jenna Bioscience | NU-4055 | Slowly hydrolyzable analog of GTP used to polymerize and stabilize the microtubules by reducing the dynamic instability and spontaneous critical concentration for microtubule nucleation to get a consistent length. We purchase a 10 mM stock from Jena Biosciences and store it at -20°C for upto one year. |
| Heating element for microscope | Okolab stage top incubator | For imaging experiments | |
| Imidizole | Sigma | I2399 | Used to elute MAP65 protein from Nickel beads to purify MAP65 |
| Kimwipes | Fisher | 34155 | For cleaning and for pulling solutions through experimental chambers. |
| KOH | Sigma | P250-500 | 1 M in ddH2O, made fresh to prevent acidification over time. |
| Liquid Nitrogen | Airgas | NI 230LT22 | To drop freeze aliquots. This can also be used for storage (not recommended) |
| MAP65 protein | Ram Dixit | A microtubule-associated protein (MAP) with a molecular weight of 65 kD that is an antiparallel microtubule crosslinker. We have purified an unlabeled and GFP-labeled version of MAP65-1 from Arabidopsis thaliana. We mix the GFP-MAP65 with the unlabeled MAP65 such that 10% of the protein is labeled. The working stock is a 10.8 μM solution. This working solution is stored at 4°C and remade fresh every week. The protocol for purifying the MAP65 and GFP-MAP65 is given in our prior methods chapter (26). | |
| MgSO4 | Sigma | MKCJ940 | Tubulin buffer ingredient |
| NTA-Nickel beads | Qiagen | 30210 | Beads required to purify 6xHis tagged MAP65 proteins |
| Optomicroscan | Nikon | 405 nm laser system which can focus the laser in any desired shape of region of interest | |
| PEM80 | Neutral tubulin polymerizing base buffer for solution made from 80 mM K-PIPES, pH 6.8, 1 mM MgSO4, 1 mM EGTA, stored at 4°C for upto one year. | ||
| Permanent double-sided tape | 3M - Scotch | 34-8724-5691-7 | For experimental chambers |
| Petri dish | Fisher | FB0875713 | For humid chamber |
| PIPES | Sigma | P7643-100G | Tubulin buffer base ingredient |
| Pluronic-F127 | Sigma | P2443-250G | A block-copolymer with two hydrophilic polyethylene oxide (PEO) blocks on the ends and a hydrophobic center block of polyphenylene oxide (PPO) hydrophobic surface coating we use to prevent protein binding to the surface. Pluronic-F127 is purchased as a powder (Sigma) and dissolved to a 5% (w/v) solution in ddH2O overnight. Once dissolved, the solution can be stored at room temperature for upto one year. |
| Polyethylene Glycol | Affymetrix Inc | 19966 500 GM | A crowding agent used to create depletion forces to bring tactoids to the surface and help to organize microtubules. We create a 5% (w/v) solution of 100 kDa PEG in PEM80. The solution is stored in 4°C for upto one year and placed on the rocker before use. It is viscous, so we recommend using a positive displacement pipette to work with it. |
| Positive displacement pipette | Eppendorf | For pipetting viscous liquids | |
| Racks for coverslips | Electron Microscopy Sciences | 72240 | For preparing experimental chambers - treating cover glasses |
| Refrigerator 4°C | Fisherbrand | For storing reagents | |
| Tubulin Labeled | Cytoskeleton | TL590M | lyophilized rhodamine-labeled tubulin from pig brain is purchased (Cytoskeleton) and stored in -80°C until hydrated in PEM80 and used for upto one year. |
| Tubulin protein | Cytoskeleton | T240 | lyophilized tubulin 99% pure unlabeled from pig brain is purchased (Cytoskeleton) and stored in -80°C until hydrated in PEM80 and used for upto one year. |
| UV-Ozone | Jelight | Model 342 | For preparing experimental chambers - treating cover glasses |
| Stackreg | Biomedical Imaging Group | http://bigwww.epfl.ch/thevenaz/stackreg/ | plugin for registering time series data to remove drift |
| Turboreg | Biomedical Imaging Group | http://bigwww.epfl.ch/thevenaz/turboreg/ | plugin for registering time series data to remove drift |
- Bodakuntla, S., Jijumon, A. S., Villablanca, C., Gonzalez-Billault, C., Janke, C. Microtubule-associated proteins: structuring the cytoskeleton. Trends in Cell Biology. 29 (10), 804-819 (2019).
- Severson, A. F., von Dassow, G., Bowerman, B. Oocyte meiotic spindle assembly and function. Current Topics in Developmental Biology. 116, 65-98 (2016).
- Brugués, J., Needleman, D. Physical basis of spindle self-organization. Proceedings of the National Academy of Sciences of the United States of America. 111 (52), 18496-18500 (2014).
- Brugués, J., Nuzzo, V., Mazur, E., Needleman, D. J. Nucleation and transport organize microtubules in metaphase spindles. Cell. 149 (3), 554-564 (2012).
- Gatlin, J. C., et al. Spindle fusion requires dynein-mediated sliding of oppositely oriented microtubules. Current Biology. 19 (4), 287-296 (2009).
- Goshima, G., Mayer, M., Zhang, N., Stuurman, N., Vale, R. D. Augmin: A protein complex required for centrosome-independent microtubule generation within the spindle. Journal of Cell Biology. 181 (3), 421-429 (2008).
- Inoue, S., Sato, H. Cell motility by labile association of the nature of mitotic spindle fibers and their role in chromosome movement molecules. Journal of General Physiology. 50 (6), 259-292 (1967).
- Allenspach, A. L., Roth, L. E. Structural variations during mitosis in the chick embryo. Journal of Cell Biology. 33 (1), 179-196 (1967).
- Theg, D. E. Cytoplasmic microtubules in different animal cells. Journal of Cell Biology. 23 (2), 265-275 (1964).
- Mcdonald, K., Pickett-Heaps, J. D., Mcintosh, J. R., Tippit, D. H. On the mechanism of anaphase spindle elongation in Diatoma vulgare. Journal of Cell Biology. 9, 377-388 (1977).
- Chaikin, P. M., Lubensky, T. C. . Principles of Condensed Matter Physics. , (1995).
- Hamon, L., Savarin, P., Curmi, P. A., Pastré, D. Rapid assembly and collective behavior of microtubule bundles in the presence of polyamines. Biophysical Journal. 101 (1), 205 (2011).
- Needleman, D. J., et al. Higher-order assembly of microtubules by counterions: From hexagonal bundles to living necklaces. Proceedings of the National Academy of Sciences. 101 (46), 16099-16103 (2004).
- Ross, J. L., Fygenson, D. K. Mobility of taxol in microtubule bundles. Biophysical Journal. 84, 3959-3967 (2003).
- Sanchez, T., Welch, D., Nicastro, D., Dogic, Z. Cilia-like beating of active microtubule bundles. Science. 333 (6041), 456-459 (2011).
- Brandt, R., Lee, G. Functional organization of microtubule-associated protein tau. Identification of regions which affect microtubule growth, nucleation, and bundle formation in vitro. Journal of Biological Chemistry. 268 (5), 3414-3419 (1993).
- Hirokawa, N. Microtubule organization and dynamics dependent on microtubule-associated proteins. Current Opinion in Cell Biology. 6 (1), 74-81 (1994).
- Kanai, Y., et al. Expression of multiple tau isoforms and microtubule bundle formation in fibroblasts transfected with a single tau cDNA. The Journal of Cell Biology. 109 (3), 1173 (1989).
- MacRae, T. H. Microtubule organization by cross-linking and bundling proteins. Biochimica et Biophysica Acta (BBA). Protein Structure and Molecular Enzymology. 1160 (2), 145-155 (1992).
- She, Z. Y., Wei, Y. L., Lin, Y., Li, Y. L., Lu, M. H. Mechanisms of the Ase1/PRC1/MAP65 family in central spindle assembly. Biological Reviews. 94 (6), 2033-2048 (2019).
- Walczak, C. E., Shaw, S. L. A MAP for Bundling Microtubules. Cell. 142 (3), 364-367 (2010).
- Edozie, B., et al. Self-organization of spindle-like microtubule structures. Soft Matter. 15 (24), 4797-4807 (2019).
- Tulin, A., McClerklin, S., Huang, Y., Dixit, R. Single-molecule analysis of the microtubule cross-linking protein MAP65-1 reveals a molecular mechanism for contact-angle-dependent microtubule bundling. Biophysical Journal. 102 (4), 802-809 (2012).
- Chan, J., Jensen, C. G., Jensen, L. C. W., Bush, M., Lloyd, C. W. The 65-kDa carrot microtubule-associated protein forms regularly arranged filamentous cross-bridges between microtubules. Proceedings of the National Academy of Sciences of the United States of America. 96 (26), 14931-14936 (1999).
- Scheff, D. R., et al. Tuning shape and internal structure of protein droplets via biopolymer filaments. Soft Matter. 16 (24), 5659-5668 (2020).
- Weirich, K. L., et al. Liquid behavior of cross-linked actin bundles. Proceedings of the National Academy of Sciences of the United States of America. 114 (9), 2131-2136 (2017).
- Weirich, K. L., Dasbiswas, K., Witten, T. A., Vaikuntanathan, S., Gardel, M. L. Self-organizing motors divide active liquid droplets. Proceedings of the National Academy of Sciences of the United States of America. 166 (23), 11125-11130 (2019).
- Sahu, S., Herbst, L., Quinn, R., Ross, J. L. Crowder and surface effects on self-organization of microtubules. Physical Review E. 103 (6), 062408 (2021).
- Stanhope, K. T., Ross, J. L. Microtubules, MAPs, and motor patterns. Methods in Cell Biology. 128, 23-38 (2015).
- Early Middle Ages drop single.jpg. Wikimedia Commons Available from: https://commons.wikimedia.org/wiki/File:Early_middle_ages_drop_spingle.jpg (2022)
- Lantzsch, I., et al. Microtubule reorganization during female meiosis in c. Elegans. eLife. 10, 58903 (2021).
- Advani, S., Maresca, T. J., Ross, J. L. Creation and testing of a new, local microtubule-disruption tool based on the microtubule-severing enzyme, katanin p60. Cytoskeleton. 75 (12), 531-544 (2018).
- Pecqueur, L., et al. A designed ankyrin repeat protein selected to bind to tubulin caps the microtubule plus end. Proceedings of the National Academy of Sciences of the United States of America. 109 (30), 12011-12016 (2012).
- Valentine, M. T., Fordyce, P. M., Krzysiak, T. C., Gilbert, S. P., Block, S. M. Individual dimers of the mitotic kinesin motor Eg5 step processively and support substantial loads in vitro. Nature Cell Biology. 8 (5), 470-476 (2006).
- Wagenbach, M., Domnitz, S., Wordeman, L., Cooper, J. A kinesin-13 mutant catalytically depolymerizes microtubules in ADP. Journal of Cell Biology. 183 (4), 617-623 (2008).
- McNally, F. J., Vale, R. D. Identification of katanin, an ATPase that severs and disassembles stable microtubules. Cell. 75 (3), 419-429 (1993).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved