Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Biology
調整可能なモーター駆動ダイナミクスとメカニクスによるアクチン-微小管複合材料の再構成と特性評価
ERRATUM NOTICE
Important: There has been an erratum issued for this article. Read more …この論文では、共絡アクチンフィラメントと微小管の調整可能な3次元複合ネットワークをエンジニアリングおよび特性評価するためのプロトコルを紹介します。複合材料は、ミオシンIIおよびキネシンモーターによって駆動される能動的再構成および弾道運動を受け、アクチン、微小管、モータータンパク質、および受動架橋剤の相対濃度によって調整される。
半柔軟なアクチンフィラメントと硬い微小管の相互作用ネットワークで構成される複合細胞骨格は、ミオシンIIやキネシンなどのモータータンパク質を使用して再構築および力を生成し、遊走、細胞質分裂、接着、メカノセンスなどの重要なプロセスを推進します。アクチン-微小管相互作用は細胞骨格の多様性と適応性の鍵ですが、ミオシンおよびキネシン活性との相互作用の理解はまだ初期段階です。この研究では、ミオシンIIおよびキネシンモーターによって駆動され、アクチン、微小管、モータータンパク質、およびパッシブ架橋剤の相対濃度によって調整される、能動的再構築と弾道運動を受ける共絡アクチンフィラメントと微小管の調整可能な3次元複合ネットワークを設計する方法について説明します。マルチスペクトル共焦点イメージングを使用して複合材料の再構築と動きを最も効果的に視覚化するための微小管とアクチンフィラメントの蛍光標識のプロトコルも詳しく説明されています。最後に、非平衡構造、ダイナミクス、および力学を定量的に特徴付けるために使用できるデータ解析手法の結果が提示されます。この調整可能な生体模倣プラットフォームを再現して調査することで、運動活動、複合力学、フィラメントダイナミクスの結合が、有糸分裂から分極、メカノ感覚までの無数の細胞プロセスにどのようにつながるかについての貴重な洞察が得られます。
細胞骨格は、相互作用する生体高分子の動的な複合ネットワークであり、細胞に構造的および機械的サポートを提供します。関連する分子モーターと結合タンパク質は、細胞骨格を再構築および適応させて、細胞の成長、形状の変化、硬化、移動、さらには自己修復を可能にし、遊走や分裂からメカノセンシングに至るまでの無数の細胞プロセスを可能にします1,2。細胞生物物理学におけるその重要性を超えて、細胞骨格は、創傷治癒や薬物送達からろ過やソフトロボティクスに至るまでの潜在的な材料用途を備えた活性物質の典型的な例でもあります1,3,4,5,6,7,8,9。
細胞骨格にその独特の構造的および機械的多様性および多機能性を与える2つの重要な特徴は、1)半可撓性アクチンフィラメントおよび剛直微小管などの複数の相互作用タンパク質フィラメント、ならびにそれらに関連する結合および架橋タンパク質を含むその複合的性質である3,5,10;2)ミオシンやキネシンなどのエネルギーを消費するモーターを介して連続的に再構築、移動、粗大化、および作業を実行し、糸状タンパク質を押したり引いたりする能力1,7,11,12,13。この優雅な複雑さにより、細胞骨格は細胞運動性、細胞質分裂、創傷治癒などの多様なプロセスを媒介することができますが3、6、7、11、再構成されたin vitroシステムで細胞骨格の特徴的なin vivo特性を再現する研究者の能力を妨げます。
現在のフロンティア再構成の取り組みは、絡み合って架橋されたアクチンフィラメントと微小管の複合材料に焦点を当てています3,10,14,15,16,17、力を発生させるアクトミオシンネットワーク2,8,18,19,20,21、およびキネシン-微小管によって駆動される活性ネマティクス相互作用22,23,24,25,26。定常状態のアクチン-微小管複合材料は、単一成分系と比較して、フィラメントの移動度の向上や剛性の増加など、創発的な機械的特性15,16,27を示すことが示されています27。in vitroアクトミオシン系に関する研究は、アクチン、ミオシン、および架橋剤の濃度に依存する広範囲の構造的および動的特性を報告している28,29,30,31。例えば、十分な架橋があると、アクトミオシンネットワークは大規模な収縮と粗大化を起こしますが2,28,30,32,33,34,35,36、架橋剤がない場合、ネットワークは急速で不安定な流れと破裂を示します19,29.キネシンモーターのクラスターを使用して微小管束を架橋および引っ張る再構成された微小管ベースの活性ネマティクスは、長期にわたる乱流、伸展、座屈、破砕、および治癒を示すことが報告されています12、22、23、24、25、37、38、39、40、41、 42,43,44,45,46,47。
最近では、ミオシンIIミニフィラメントによって駆動されるアクチン-微小管複合材料は、架橋剤のないアクトミオシンネットワークが示す無秩序な流れおよびネットワーク破裂と比較して、より秩序ある収縮およびネットワーク完全性をもたらすことが示されている17,26,48。さらに、複合ロバスト性と力発生の組み合わせは、アクチンと微小管が同等の濃度で存在する場合に最適化されます。製剤空間のこの領域における主要な創発的特徴には、強化された機械的強度26、アクチンと微小管の協調運動26、安定した持続的収縮、およびメソスケールの再構築17が含まれる。
ここでは、アクチンフィラメントと微小管に作用するミオシンIIミニフィラメントとキネシンクラスターによって平衡から押し出される微小管とアクチンフィラメントの共絡および架橋複合材料を設計および調整するためのプロトコルについて説明します(図1)。このクラスの複合材料のダイナミクス、構造、および力学は、フィラメント、モーター、および架橋剤の相対濃度によって調整でき、移流および乱流、等方性収縮、加速、減速、デミキシング、硬化、緩和、および破裂の豊富な位相空間を示します。この研究の焦点は、このクラスの活性細胞骨格複合材料の調製および調整にある。ただし、研究者が記載されたアクティブ複合材料のベンチマークと特性評価を支援するために、マルチスペクトル共焦点顕微鏡を使用した効果的なイメージング方法も詳しく説明されています。最後に、複合材料のダイナミクス、構造、および力学を測定するために使用できる主要な計算分析方法の結果が提示されます。研究者は、複合材料の複雑なダイナミクスと構造多様性を特徴付けるために最適化されているため、示差動的顕微鏡(DDM)、空間画像自己相関(SIA)、粒子画像速度測定(PIV)を含むこれらの方法を採用することをお勧めします17,26,49。
以下に説明する手順は、複合材料の調製と共焦点顕微鏡を使用したイメージングに焦点を当てています。取得後のデータ分析および光ピンセット測定を記述するプロトコルは、以前の研究17、26、48、50に見出すことができ、要求に応じて提供される。すべての材料は、提供された材料の表に記載されています。
1.チャンバー表面へのタンパク質の吸着を防ぐために、シラン化カバーガラスと顕微鏡スライドを準備します
注:これは2日間のプロセスです。シラン化されたスライドは、使用の1か月前までに準備できます。
- 1番のカバーガラス(24 mm x 24 mm)と顕微鏡スライド(1インチx 3インチ)を、プラズマクリーナーに収まる指定されたラックに入れます。ラックをプラズマクリーナーに入れ、20分間実行します。
- カバーガラスとスライドをシラン専用に指定された新しいラックに移し、ラックをガラス容器に入れて、以下に説明するようにガラスを清掃します。
- カバーガラスとスライドを100%アセトンに1時間浸します。カバーガラスとスライドを100%エタノールに10分間浸します。
- カバーガラスとスライドを脱イオン水(DI)に5分間浸します。クリーニング手順をさらに2回繰り返します。
- カバーガラスとスライドを、作りたての0.1 M KOHに15分間浸します。カバーガラスとスライドを新鮮なDIに5分間浸します。この手順をさらに 2 回繰り返します。
- カバーガラスとスライドを10分間風乾します。洗浄したカバーガラスとスライドをシランで処理して、以下に説明するように疎水性の表面を生成します。
注意: ドラフトで次の手順を実行します。- 乾燥したカバーガラスとスライドを2%シラン(トルエンに溶解)に5分間浸します。漏斗を使用してシランを指定されたボトルに戻し、最大5回再利用します。
- カバーガラスとスライドを100%エタノールに5分間浸します。エタノールを新鮮なエタノールに置き換えます。カバーガラスとスライドを5分間浸します。
- カバーガラスとスライドを新鮮なDIに5分間浸します。毎回新鮮なエタノールとDIを使用して、エタノールとDIの洗浄ステップをさらに2回繰り返します。カバーガラスとスライドを10分間風乾します。
2. ミオシンミニフィラメントによる活性アクチン-微小管複合体の調製
- アクチンフィラメント結合を介して不活性ミオシンを除去し、以下に説明するように超遠心を介してプルダウンを実行します。
- アクチンをフィラメントに重合します。精密マイクロピペットと滅菌ピペットチップを使用して、1.87 μLのDI、1.3 μLの10x Gバッファー、1.3 μLの10x Fバッファー、1.63 μLの4 M KCl、4.53 μLのアクチン(47.6 μM)、および1.08 μLの100 μMファロイジンをマイクロ遠心チューブで組み合わせます。
注:十分な重合を確保するには、アクチン濃度とアクチン:ファロイジンのモル比をそれぞれ18.4μMと2:1にする必要があります。 - 溶液をゆっくりと上下にピペッティングして混合し、暗所で氷の上に≥1時間置きます。超遠心分離機を4°Cに冷却します。 -80°Cからミオシンアリコートを除去し、氷上に置きます。
注:アクチンが重合している間に、この時点でステップ2.2を完了します。 - アクチン重合≥1時間後、重合したアクチンに1.3 μLの10 mM ATPおよび2 μLの19 μMミオシンを加えます。
注:アクチン:ミオシンのモル比は、不活性ミオシンモーター(つまり、デッドヘッド)を十分に除去するために>5である必要があります。. - 溶液をゆっくりと上下にピペッティングして混合します。超遠心グレードのチューブに移します。
4°C、121,968 x g で30分間遠心分離します。
- アクチンをフィラメントに重合します。精密マイクロピペットと滅菌ピペットチップを使用して、1.87 μLのDI、1.3 μLの10x Gバッファー、1.3 μLの10x Fバッファー、1.63 μLの4 M KCl、4.53 μLのアクチン(47.6 μM)、および1.08 μLの100 μMファロイジンをマイクロ遠心チューブで組み合わせます。
- 以下に説明するように、アクチンフィラメントと微小管の共絡複合ネットワークを調製します。
注意: ミオシンスピンダウンの30分前に開始します(ステップ2.1.4)。- ヒートブロックを37°Cに設定します。 精密マイクロピペットと滅菌ピペットチップを使用して、マイクロ遠心チューブに以下を追加します:13.9 μLのPEM、3 μLの1%Tween20、1.55 μLの47.6 μMアクチン、0.36 μLの34.8 μM R-アクチン、0.3 μLの250 mM ATP、0.87 μLの100 μMファロイジン、1.91 μLの5-488-チューブリン、0.3 μLの100 mM GTP、 200 μMタキソールを0.75 μL、総容量23 μLにします。
注:記載されているアクチンとチューブリンの濃度は、2.9μMアクチンと2.9μMチューブリンとの複合体の場合です。総タンパク質濃度はc = cA + c T = 5.8μMであり、モルアクチン画分はc A /(cA + cT)=ΦA = 0.5である。これらの値を調整するには、手順 2.5 を参照してください。 - 溶液をゆっくりと上下にピペッティングして混合し、光から保護された37°Cのヒートブロックに1時間置きます。
- ヒートブロックを37°Cに設定します。 精密マイクロピペットと滅菌ピペットチップを使用して、マイクロ遠心チューブに以下を追加します:13.9 μLのPEM、3 μLの1%Tween20、1.55 μLの47.6 μMアクチン、0.36 μLの34.8 μM R-アクチン、0.3 μLの250 mM ATP、0.87 μLの100 μMファロイジン、1.91 μLの5-488-チューブリン、0.3 μLの100 mM GTP、 200 μMタキソールを0.75 μL、総容量23 μLにします。
- 共焦点イメージング実験用の試料室を以下のように調製する。
メモ: 待機期間中に手順 2.1.4 および 2.2.2 を実行します。- 2つのシラン化スライドをホットプレート(オフ)に並べて置き、スライド全体に熱可塑性シーリングフィルムの2つのストリップを~3 mm離して置き、2つのシラン化カバーガラスを熱可塑性シーリングフィルムの上に置き、サンプルチャンバーを形成します。
- カバースリップが溶けた熱可塑性シーリングフィルムでスライドにしっかりと結合するまで、ホットプレートを低設定にします(~1〜2分)。均等な圧力で押し下げて、2つの表面間の間隔を~100μmに保ちながら接着を確保します。
- チャンバーを取り外し、ホットプレートをオフにします。チャンバーに(+)と(-)のラベルを付けます。(+)チャンバーは活性サンプル(ミオシンを含む)用であり、(-)チャンバーはコントロール用(ミオシンなし)になります。各チャンバーが≤10μLの液体を収容できることを確認してください。
- 以下のように画像化するサンプルを準備します。
メモ: 手順 2.1 および 2.2 を完了した直後に、この手順を完了することが重要です。- ミオシン-アクチンサンプルを超遠心分離機から慎重に取り出し(ステップ2.1.4)、すぐに上清の上部7.5 μLをピペットで固め、新しいマイクロ遠心チューブに移します。
- アクチン微小管サンプルをヒートブロックから取り出し、1.5 μLの10x D-グルコース、1.5 μLの10x GOC、および1.5 μLの1 mMブレビスタチンを穏やかに混合します。溶液を2つの13.7 μLアリコートに分け、(+)および(-)のラベルを付けます。
- ステップ2.4.1の上清1.28 μLを(+)アリコートに混合します。1.28 μLのDIを(-)アリコートに混合します。毛細管現象 を介して 、各溶液を対応するチャンバーにゆっくりと流します(ステップ2.3)。チャネルに気泡を入れないように注意してください。
- 各チャンネルの2つの開放端を速乾性のエポキシまたはUV接着剤でシールします。顕微鏡に置く前に、接着剤が完全に乾いていることを確認してください。手順 3 の説明に従ってすぐにイメージします。
注:UV接着剤は、UVにさらされるとほぼ瞬時に硬化するため、有利です。ただし、ブレビスタチンはUV感受性であるため、ブレビスタチンの不活性化を避けるために、小さなUVワンドを使用して接着剤(サンプルチャンバーの端)のみを局所的に照らすことが重要です。
- オプション:タンパク質濃度を変化させて、複合材料のダイナミクスと構造を調整します。
注:次の手順は、必要に応じてアクチン、微小管、およびミオシンの濃度を変更するために、上記の手順を変更することをお勧めします。- 手順 2.2.1 および 2.4.3 での次の変更を除き、上記の手順に従います。
- アクチンおよび微小管の濃度を変化させ、それによってcおよびΦAを調整し、所望に応じて、ステップ2.2.1で使用されるアクチン、R−アクチン、および5−488−チューブリンの体積を増減する26。アクチン濃度を変化させる場合は、アクチンと同じモル比を維持するために、R-アクチンとファロイジンのモル濃度を比例的に調整してください。混合物の最終容量が23μLのままになるようにPEMの容量を調整します。他のすべての成分の量と濃度は同じままです。
- ミオシン濃度を変化させるには、必要に応じてステップ2.4.3で(+)アリコートに添加するミオシンの量を調整します。それに応じて、(-)アリコートに追加されたDIボリュームを調整します。ステップ2.2.1でPEM容量を調整して、ミオシン(+)およびDI(-)ボリュームの増減を考慮し、各サンプル(+)および(-))の最終容量が14.98μLであることを確認します。
3. 共焦点顕微鏡を用いた活性複合材料のイメージングとキャラクタリゼーション
- ステップ2で調製したアクトミオシン-微小管複合材料を画像化するには、60x 1.4 NAの油浸対物レンズを備えたレーザー走査型共焦点顕微鏡(LSCM)または同様の顕微鏡を使用します。アクチンフィラメントと微小管を別々の蛍光チャンネルで同時に可視化するには、565/591 nm励起/発光フィルターを備えた561 nmレーザーと、488/525 nm励起/発光フィルターを備えた488 nmレーザーを使用します。
- コントロールチャンネルが対物レンズの真上に位置するように、サンプルチャンバーを顕微鏡上に置きます。対物レンズとカバーガラスの間にオイルインターフェースがあることを確認してください。
- ステージコントロールを使用してコントロールコンポジットに焦点を合わせ、サンプルチャンバーの両面を見つけます。z位置をサンプルチャンバーの中央に移動します。 図2に示すように、明確な糸状ネットワークの存在を確認します。
- コントロールチャンバーを視覚化しながら、各レーザーの強度を調整して、アクチンフィラメントと微小管を同時に視覚化できるようにします。光退色(アクチンチャネルでより一般的)とブリードスルー(通常は微小管からアクチンチャネルへの)を防ぐために、可能な限り低いレーザー強度を維持します。
- 非アクティブな制御サンプルの特性評価には、2.65 fpsで256 x 256平方ピクセル(213 μm x 213 μm)の3つの時系列(ビデオ)を収集し、合計≥1000フレームを収集します。各時系列を≥500 μm離れたサンプルチャンバーの異なる領域に収集します。検出可能な動きが最小限であり、流れや再構築がないことを確認してください。
- 488 nmレーザーをシャッターオフし、ステージコントロールを使用して(+)チャンバーに移動します。
- 568 nmレーザーを使用して、(+)チャネル内の微小管を視覚化して適切なネットワーク形成を確保し(図2)、サンプルチャンバーの軸方向の中心を特定します(制御チャンバーの中心z位置とは異なる場合があります)。
- 488 nmレーザーをオンにし、次の変更を加えて上記の手順3.5を繰り返します。最大45分間時系列を収集し、サンプルが視野外に移動したり、破裂したり、光退色したりすると取得を停止します。5〜10個の時系列を記録し、最初の時系列の開始を基準にして各時系列が開始される時間を追跡します。
- 図 3、図 4、図 5、および前述の17、48、50、51 で説明したように、DDM、SIA、および PIV を使用してデータを分析します。
注:488 nmレーザーは、ブレビスタチンを不活性化することによりミオシンATPase活性を局所的に活性化するため、t = 0が時系列の開始時になるように、データ取得の開始時にのみオンにする必要があります。これらの取得パラメータは、以前に行われたように、示差動的顕微鏡(DDM)分析用に最適化されています26。
4. キネシンモーターで駆動する活性アクチン-微小管複合材料の作製
注:次の手順では、キネシンモーターまたはキネシンとミオシン50の組み合わせによって平衡から外れて駆動されるアクチン-微小管複合材料を作成します。
- 以下に説明するようにキネシンおよびミオシンモーターを準備します。
- ミオシンを組み込む場合は、ステップ2.1に従ってください。
- 微小管のペア間で結合して力を加えるキネシンモータークラスターを形成するには、マイクロピペットと滅菌ピペットチップを使用して、滅菌1.5 mLマイクロ遠心チューブに以下を追加します:1.16 μL PEM、2.74 μL 8.87 μMキネシンダイマー、7.29 μL 83.3 μMニュートラアビジン、0.81 μL 2mM DTT。溶液を上下にピペッティングして穏やかに混合し、光から保護された状態(黒色の微量遠心チューブを使用するか、ホイルで包む)を4°Cで30分間インキュベートします。
注:NAに対するキネシン二量体のモル比は1:25です。
- ステップ2.3に従ってサンプルチャンバーを準備し、2つではなく3つのチャンバーを作成します。キネシンインキュベーション(ステップ4.1.2)およびミオシン超遠心分離(ステップ4.1.1)の間にこのステップを実行します。
- アクチンフィラメントと微小管の共絡複合ネットワークを準備します。
- ヒートブロックを37°Cに設定します。 マイクロピペットと滅菌ピペットチップを使用して、滅菌1.5 mLマイクロ遠心チューブに以下を追加します:3.21 μL PEM、4.5 μLの1%Tween20、2.18 μLの47.6 μMアクチン、3.46 μLの5-R-チューブリン、4.5 μLの100 mM ATP、4.5 μLの10 mM GTP、1.13 μLの200 μM タキソール、および1.57 μLの20 μM 488-ファロイジン。総容量が25μLであることを確認してください。
- 溶液をゆっくりと上下にピペッティングして混合し、光から保護された37°Cのヒートブロックに1時間置きます。ヒートブロックからチューブを取り外し、マイクロピペットを使用して0.84 μLの100 μMファロイジンを穏やかに混合します。光から保護された室温で5〜10分間インキュベートします。
注:ステップ4.3.1ではなくこのステップでファロイジンを追加すると、488-ファロイジンがアクチン結合部位で非標識ファロイジンと競合する必要がないため、アクチンフィラメントの蛍光標識が改善されます。
- 共焦点イメージング用のアクティブコンポジットを準備します。
- ステップ4.3.2の溶液に1.13 μLの200 μMブレビスタチン、1.35 μLの10x Glu、および1.35 μLの10x GOCを加え、上下にピペッティングして穏やかに混合します。溶液を3つの10 μLアリコートに分け、(K)、(K+M)、および(-)とラベル付けします。
- ステップ2.1.4のミオシン2.54 μLを(K + M)アリコートに混合します。2.54 μL PEMを(K)および(-)アリコートに混合します。
- マイクロピペットと滅菌ピペットチップを使用して、ステップ4.1.2のキネシンクラスター2.5 μLを(K)および(K+M)アリコートに追加します。ピペットを上下に混ぜます。同じ手法を使用して、2.5 μL PEMを(-)に混合します。
注:記載されているアクチンとチューブリンの濃度は、2.32μMアクチンと3.48μMチューブリンとの複合体の場合です。総タンパク質濃度はc = cA + c T = 5.8μMであり、モルアクチン分画はc A /(cA + cT)=ΦA = 0.4である。キネシンおよびミオシン濃度はそれぞれ0.35μMおよび0.47μMである。c A、cT、c、および ΦA を調整するための一般的なガイドラインについては、ステップ 2.5 を参照してください。 - マイクロピペットを使用して、毛細管現象 を介して 、調製したサンプルチャンバーの対応するチャネルに各溶液をゆっくりと流します(ステップ4.2)。チャネルに気泡を導入しないように、ピペットを非常にゆっくりと穏やかに押し下げます。
- 各チャンネルの2つの開放端を速乾性エポキシまたはUV硬化型接着剤でシールします。顕微鏡に置く前に、接着剤が完全に乾いていることを確認してください。
注:キネシンが監視されずに作用する時間を最小限に抑えるために、この手順を迅速に実行することが重要です。このため、(5分や10分ではなく)1分で硬化するエポキシをお勧めします。UV硬化型接着剤は、UV曝露時にほぼ瞬時に硬化するため、この点で有利です。
- サンプルの画像は直ちに、以下の重要な変更を除き、工程3に続く。キネシンは光活性化によって制御されないため、ステップ4.4.3の直後に働き始めるので、この時間をt=0としてマークします。コンポジットを初期非アクティブ状態(t = 0)にできるだけ近づけて画像化するには、最初に(K)および(K+M)チャンネルを画像化し、ステップ4.4.3からデータ集録の開始までの経過時間(ステップ3.8)を記録します。実際には、この経過時間は~5分です。
5. アクティブコンポジットへのパッシブ架橋剤の組み込み
注:これらの手順では、ビオチン化アクチンとチューブリンサブユニット、およびニュートラアビジン(NA)を使用して、ステップ4で説明されているアクティブコンポジットでアクチンをアクチン(A-A)または微小管から微小管(M-M)に受動的に架橋する方法について説明します。
- ビオチン-アクチン/チューブリン:ビオチン:NAの比率で、ビオチン化タンパク質(ビオチン-アクチンまたはビオチン-チューブリン)、NA、およびビオチンとのA-AまたはM-M架橋剤複合体を調製します。ステップ 4 の前にこのプロセスを開始してください。
- A-A架橋剤の場合は、マイクロピペットと滅菌ピペットチップを使用して、2 μLの11.6 μMビオチン-アクチン、1.39 μLの8.33 μM NA、2.27 μLの1.02 μMビオチン、および4.34 μLのPEMをマイクロ遠心チューブに追加します。上下にピペッティングして穏やかに混ぜます。
- M-M架橋剤の場合は、マイクロピペットと滅菌ピペットチップを使用して、1.86 μLの4.55 μMビオチンチューブリン、1.11 μLの8.33 μM NA、1.82 μLの1.02 μMビオチン、および5.21 μLのPEMをマイクロ遠心チューブに追加します。上下にピペッティングして穏やかに混ぜます。
- 手順5.1.1および/または5.1.2のチューブを熱可塑性シーリングフィルムで包み、水密シールを作成します。4°Cに設定された温度制御された超音波処理器浴の浮選いかだに入れます。
- 4°Cで90分間超音波処理します。 実際には、低温を維持するために超音波処理器を冷蔵室に置き、超音波処理浴にアイスパックを追加するのが最善です。
- 架橋剤複合体をイメージング用のサンプルに組み込むには、ステップ4.3に従い、A−A架橋(ステップ5.2.1)またはM−M架橋(ステップ5.2.2)について以下に説明するようにステップ4.3.1を修飾する。
- A-A架橋の場合、微小遠心チューブで以下を組み合わせます:1.94 μLのPEM、4.50 μLの1%Tween20、2.18 μLの47.6 μMアクチン、3.46 μLの45.5 μM 5-R-チューブリン、1.13 μLのA-A架橋剤(ステップ5.1.1)、4.50 μLの100 mM ATP、4.50 μLの10 mM GTP、1.13 μLの200 μMタキソール、 1.57 μLの20 μM 488-ファロイジン。総容量が25μLであることを確認してください。
- M-M架橋の場合、微小遠心チューブで以下を組み合わせます:1.97 μLのPEM、4.50 μLの1%Tween20、2.18 μLの47.6 μMアクチン、3.76 μLの45.5 μM 5-R-チューブリン、1.13 μLのM-M架橋剤の1:4希釈(ステップ5.1.2)、4.50 μLの100 mM ATP、4.50 μLの10 mM GTP、1.13 μLの200 μMタキソール、 1.57 μLの20 μM 488-ファロイジン。総容量が25μLであることを確認してください。
- 手順4.3.2〜4.5に従い、架橋剤:アクチンモル比がRA = 0.02、架橋剤:チューブリンモル比がRT = 0.005の特定の濃度を使用します。これらのRA値およびRT値は、アクチンフィラメントおよび微小管に沿った架橋剤間の同様の長さ(dA
 60 nmおよびd MT 67 nm)をもたらし、dA = Iモノマー/2RA(ここでIモノマーはアクチンモノマーの長さ)、およびdMT
60 nmおよびd MT 67 nm)をもたらし、dA = Iモノマー/2RA(ここでIモノマーはアクチンモノマーの長さ)、およびdMT  = I環/26RT(I環は13個のチューブリン15の環の長さ)を用いて推定される。17.
= I環/26RT(I環は13個のチューブリン15の環の長さ)を用いて推定される。17.
活性複合材料の調製の成功を決定し(図1)、それらのダイナミクスと構造を特徴付けるために、少なくとも2つの蛍光チャネルを備えたレーザー走査型蛍光顕微鏡を使用して、アクチンフィラメントと微小管を同時に視覚化します(図2および図6)。複合材料中のすべてのアクチンフィラメントと微小管は、in vitro研究でよく行われるように、トレーサーの明るいフィラメントにドーピングするのではなく、まばらに標識されています。この方法により、測定されたダイナミクスと構造が、複合材料とは異なる条件下で形成されるトレーサーではなく、複合材料自体を代表するものになります。このため、個々のアクチンフィラメントと微小管は通常分解できず、画像はメソスケールのネットワーク構造を描写します(図2および図6)。
このラベリングアプローチは、空間画像自己相関(SIA)および逆フーリエ空間のダイナミクスと構造を調べる示差動的顕微鏡(DDM)分析に最適化されました(図4、図5、および図8)52、53、54、55。粒子画像速度測定(PIV)は、ダイナミクスと流れ場の描写と特性評価にも使用できますが(図3および図7)、高密度で低信号の画像のノイズから生じる誤ったベクトルを排除するには、SIAやDDMよりもピクセルビニング(空間分解能が低い)と大きなラグタイム増分(時間分解能が低い)が必要です。それにもかかわらず、PIVは流れ場の定性的検査とDDM結果の裏付けに推奨されます(図4および図8)26,50。
これらの分析(すなわち、DDM、SIA、PIV)を使用した記述されたネットワークのサンプル特性評価は、研究者がサンプルをベンチマークおよび特性評価するために同様の分析を採用するのを支援するために提供されます。ただし、これらの手法の詳細な説明は、この作業の範囲外です。ユーザーフレンドリーなPythonコードを含む、これらおよび他の同様のシステムでDDMを実行する方法の詳細な説明については、以前の作業17、26、49、50とその中の参照を参照してください。ここで説明するシステムでSIAとPIVを実行する方法の詳細については、読者は以前の作品17,50に誘導されます。
以下で説明するいくつかの制御は、コンポジットが期待どおりに機能していることを確認するために実行する必要があります。ミオシンまたはキネシンを含まない複合材料は、熱変動またはドリフトを最小限に抑えて本質的に静的に見えるはずです。アクチンフィラメントと微小管は、~200 μm x 200 μmの視野全体にわたってアクチンと微小管の束ね、凝集、または相分離を最小限に抑えて、共絡し、均一に分布しているように見える必要があります(図2、左端)17。ミオシンを含むが488nmの光にさらされていない複合材料についても同様の結果が期待できます(ブレビスタチンを不活性化するため)。
ミオシンを取り込んで488 nmの光に曝露すると、ミオシン活性の前後に撮影された顕微鏡画像(図2)、および活性中のさまざまな時間に対応するPIVフローフィールド(図3)に見られるように、複合材料はアクチンと微小管でほぼ等方性で類似した収縮を受けます。運動が弾道、拡散、亜拡散などであるかどうかを判断するために、DDMから決定された特性非相関時間τ(q)を波動ベクトル(すなわち逆数空間)の関数として評価します。17、26、49で詳細に説明したとおりに参照のこと。 図4は、DDMを使用してこれらの複合材料の特性評価を行う方法も示しています。べき乗則スケーリングτ(q)~1/vq β、β = 1 の場合、速度 v の弾道運動を示します。参考までに、β = 2は拡散ダイナミクスを表し、vは拡散係数です。すべての活性複合材料は、アクチンとミオシンの濃度によって調整された速度で弾道スケーリング(図4A)を示し(図4B)、活動中に加速または減速のいずれかで時間的に変化する可能性があります(図4C、D)。
ネットワーク再構築およびクラスタリングは、図2に見られ、より高いアクチンおよびミオシン濃度についてより明白であり、図5に描かれているようにSIAを用いて特徴付けることができ、17、48、50と前述した。簡単に言えば、画像内の特徴の特性サイズの尺度である相関長ξは、各空間強度自己相関曲線g(r)をピクセル間の距離rの指数関数に適合させることによって決定できます。より長い距離にわたって持続するより大きなg(r)ピークは、より大きな構造的特徴(すなわち、個々のフィラメントの束ね、クラスタリング)を示す。図5に示すように、より高いアクチン画分およびミオシン濃度の場合、有意な再構築および凝集が時間の経過に伴うξの増加に反映される。
活性複合材料の粘弾性特性および非線形機械的応答は、光ピンセットマイクロレオロジー(OTM)を用いて測定することもできる。ただし、これらの実験のプロトコルと代表的な結果は、この作業の範囲外です。興味のある読者は、OTM測定の実行方法と期待される結果を徹底的に説明している以前の作品48,56を参照します。
次のセクションでは、上記の実験ツールと分析ツールの同じプログラムを使用して、キネシンモーターとビオチン-NA架橋剤を複合材料に組み込むと、ダイナミクスと構造がどのように変化するかについて説明します(図6、図 7、 および図8)。 図6 は、アクチンフィラメントまたは微小管の受動架橋(XL)の有無にかかわらず、キネシンのみ(K)またはキネシンとミオシン(K + M)のいずれかによって駆動される複合材料の代表的な共焦点画像を示しています。
キネシンを複合材料に組み込むと、図7(クラス1)の一番上の行に見られるように、ミオシン駆動複合材料と同様のダイナミクスと再構築が最初にもたらされます。ただし、ダイナミクスは通常、大規模な異方性流れ(図7中段、クラス2)、加速、および減速(図7下段、クラス3)に移行します。これらの特性は、5〜30分後にメソスケールのクラスタリングと集約と結合します(図6および図8B)。図7に示すPIV生成流れ場と時間カラーマップは、等方性再構築(クラス1、上部パネル)、有向流れ(クラス2、中央パネル)、および双方向加速度(クラス3、下部パネル)の例を示しています。
活動中のさまざまな時点でのアクチンと微小管の速度は、τ(q)曲線への適合によって決定され、架橋に依存する加速とそれに続く減速を示しています(図8)。図8にも示すように、両方のモータータンパク質が組み込まれている場合、実際にはキネシンのみの複合材料よりもダイナミクスが遅く、メソスケールの流れの開始が遅れます。ミオシンはまた、活性期間中のアクチンおよび微小管ネットワークのより均質な相互浸透、ならびにより少ない凝集および再構築をサポートする。これらの影響は図6の画像で確認でき、SIAを介して計算された時間変化する相関長によって定量化され、ミオシンの存在下では一般的に小さくなります(図8B)。
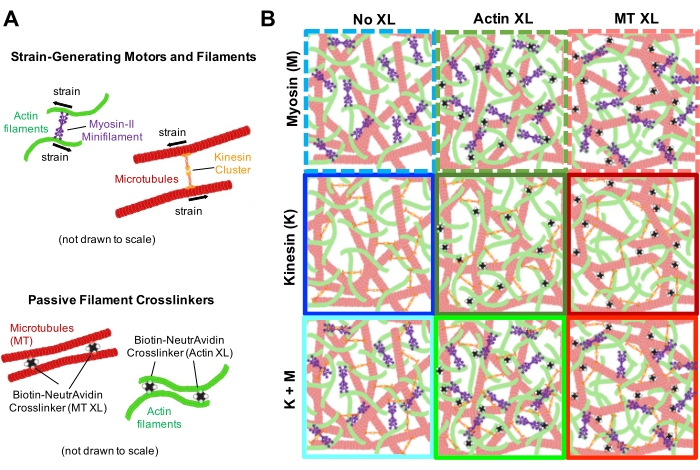
図 1.複数の力を発生させるモーターとパッシブ架橋剤を備えたアクティブアクチン-微小管複合材料の設計と特性評価。(A)アクチンモノマーとチューブリン二量体は、0.73〜11.6μMのモル濃度CAおよびCTで共重合され、アクチンΦA=cA/(c A+ cT)=0、0.25、0.5、0.75、および1のモル分画で、アクチンフィラメント(緑)と微小管(赤)の共絡ネットワークを形成します。受動架橋は、NAを使用してビオチン化アクチンフィラメント(アクチンXL)または微小管(MT XL)を架橋剤:アクチンおよび微小管のそれぞれRA = 0.01-0.08およびRMT= 0.001-0.01のタンパク質モル比で結合するために達成されます。ミオシンIIミニフィラメント(紫色)およびキネシンクラスター(オレンジ色)は、c M = 0.12 - 0.48 μMおよびcK = 0.2 - 0.7 μMの濃度で、フィラメントを押したり引いたりして、複合材料を定常状態から追い出します。(B)製剤空間の概略図。ミオシンIIミニフィラメント(M)、キネシンクラスター(K)、または両方のモーター(K + M)は、パッシブ架橋剤なし(XLなし)、アクチン-アクチン架橋(アクチンXL)、および微小管-微小管架橋(MT XL)を備えた複合材料に組み込まれています。すべての漫画が縮尺通りに描かれているわけではありません。この図の拡大版を表示するには、ここをクリックしてください。
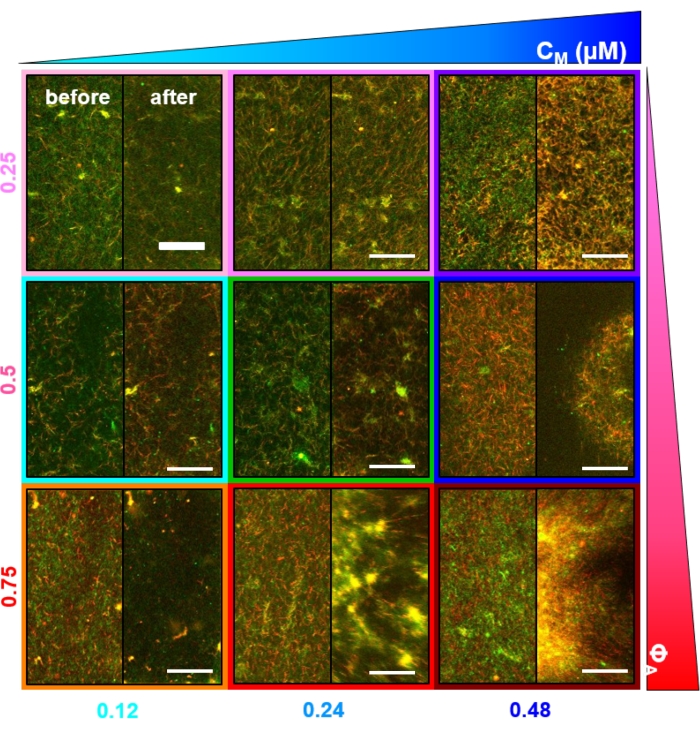
図 2.ミオシン濃度cmおよびモルアクチン画分ΦAを変化させたミオシン駆動細胞骨格複合材料の2色共焦点イメージング。(A)256 x 128平方ピクセル(212 x 106 μm 2)の2色共焦点顕微鏡画像は、アクチンフィラメント(緑)と微小管(赤)の複合材料がミオシン運動活動を介してどのように再配列されるかを示しています。キネシンモーターやパッシブ架橋剤は存在しません。各パネルでは、45分間のミオシン活性化の開始(左、前)および終了(右、後)で撮影された画像(ブレビスタチンを不活性化するための488nm光による照明を介して)が示されている。パネルは、ミオシンのモル濃度(cm)を左から右に増加させ、アクチンのモル分率(ΦA)を上から下に向かって増加させることによって順序付けられる。各パネルの輪郭を描く色は、図 4 および図 5 で使用されている色分けと一致しています。スケールバーは50μMです。分析のためにダイナミクスと構造を最適にキャプチャするために、収縮と再配置の速度に応じて、1〜5 fpsのフレームレート、50〜250 μmの側面のROI、および5〜45分の時系列期間を使用します。変更前と変更後の画像が似ているパネルは、ピンク、マゼンタ、シアンのパネルに見られるように、最小限の再構築を示します。不均一性の増加と明るい点状特徴の存在によって証明される小規模なクラスタリングは、オレンジ、緑、および赤のパネルで見ることができます。一様に縮小するネットワークとして見られる大規模な収縮は、青と紫のパネルで明らかです。この図は参考文献17から修正されています。この図の拡大版を表示するには、ここをクリックしてください。
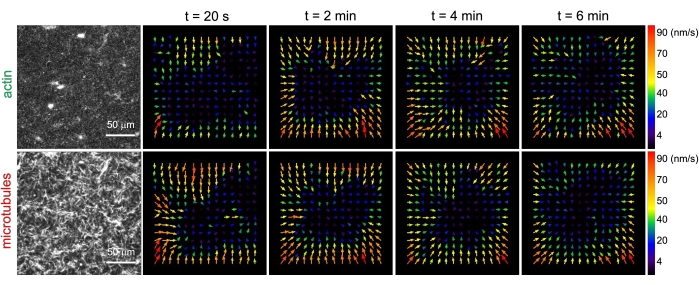
図 3.粒子画像速度測定(PIV)は、アクトミオシン活性が共絡複合材中のアクチンと微小管の協調収縮ダイナミクスを引き起こすことを示しています。ミオシン駆動複合材料におけるアクチン(上段)と微小管(下段)のPIVフロー場は、(ΦA, CM) = (0.5, 0.24)で、6分間の時系列で増加する時間で。フローフィールドは、Fiji/ImageJ PIVプラグインを使用して、ラグタイムが20秒、2ピクセルx2ピクセルのビニングで生成されました。アクチンと微小管はどちらも、映画の継続時間を通して視野の中心領域に向けられた一貫した動きを示します。すべての画像のスケールバーは50μmです。異なる矢印の色は、ベクトルフィールドの右側のカラースケールに示されているように、異なる速度に対応します。この図は参考文献26から修正されています。この図の拡大版を表示するには、ここをクリックしてください。
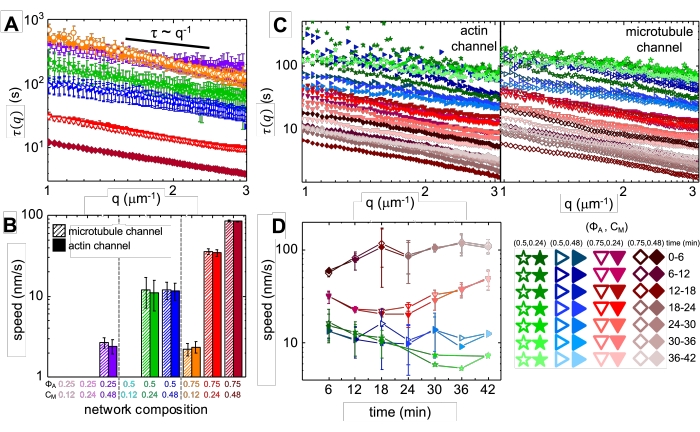
図 4.時間分解示差動的顕微鏡(DDM)は、活性複合材料中のアクチンと微小管の運動の速度とタイプを測定します。(A)DDMは、前述のように、アクチン(塗りつぶされたシンボル)と微小管(開いたシンボル)の両方の特徴的な減衰時間τ対波数qを決定するために、時系列の微小管(上、開いたシンボル)とアクチン(下の、塗りつぶされたシンボル)チャネルに対して実行されます17,26。すべての曲線はτ~q-1スケーリングに従い、弾道運動を示し、速度vはτ(q)=(vq)-1へのフィットによって決定されます。速度が速いほど、任意のqに対してτ(q)値が小さくなります。記号の色と形状は、Bに示す(ΦA、cm)の組み合わせに対応します。 (B)収縮速度vは、Aに示すτ(q)曲線への適合によって決定され、各45分の時系列の期間のすべてのラグタイムにわたって平均化されます。(C)時間分解DDM(trDDM)は、45分の活性化時間中に連続した6分間隔(同じ色の異なる色合いで示される)のアクチン(塗りつぶされたシンボル、左)と微小管(開いたシンボル、右)のτ(q)を評価することにより、ダイナミクスが時間とともにどのように変化するかを定量化します。trDDMは、右下の凡例に記載されているように、(ΦA、cm)の組み合わせ(異なる記号と色で示される)ごとに実行されます。 Cで示されているτ(q)曲線は、Aと同様のスケーリングと傾向に従いますが、特定の(ΦA、cM)組成、特にΦA = 0.75の時間依存性も示します。(D)アクチンフィラメント(閉じたシンボル)と微小管(開いたシンボル)の収縮速度は、対応するτ(q)曲線へのフィットから決定されます。すべてのプロットのエラーバーは、3〜5回の反復にわたる値の標準誤差を表します。この図は参考文献17から修正されています。この図の拡大版を表示するには、ここをクリックしてください。
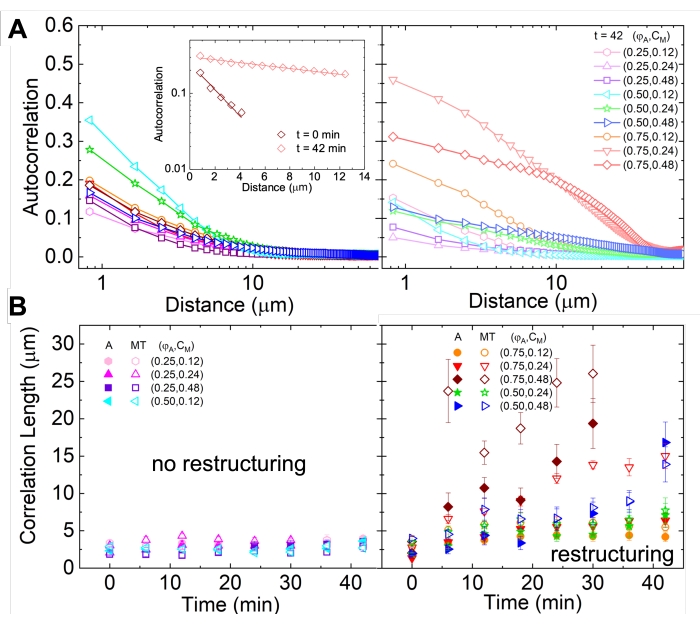
図 5.空間画像自己相関(SIA)解析は、活性な細胞骨格複合材料のモーター駆動の再構築を定量化します。(A)凡例に記載されている(ΦA、cM)製剤の実験の開始時(左、t = 0分、暗い色合い)と終了(右、t = 42分、明るい色合い)の微小管の自己相関g(r)。挿入図: (ΦA, cM) = (0.75, 0.12) に対する初期および最終時間におけるデータの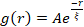 適合例。(B)アクチン(閉記号)と微小管(白接点)のそれぞれの平均相関長ξ(ΦA、cm)は、Aの挿入図に示すように、各g(r)曲線の指数関数的適合によって決定されます。 データは、最小(左)と実質的(右)の再構築を示すものに分けられます。 AとBのエラーバーは、3回から5回の反復における標準誤差を表します。この図は参考文献17から修正されています。この図の拡大版を表示するには、ここをクリックしてください。
適合例。(B)アクチン(閉記号)と微小管(白接点)のそれぞれの平均相関長ξ(ΦA、cm)は、Aの挿入図に示すように、各g(r)曲線の指数関数的適合によって決定されます。 データは、最小(左)と実質的(右)の再構築を示すものに分けられます。 AとBのエラーバーは、3回から5回の反復における標準誤差を表します。この図は参考文献17から修正されています。この図の拡大版を表示するには、ここをクリックしてください。
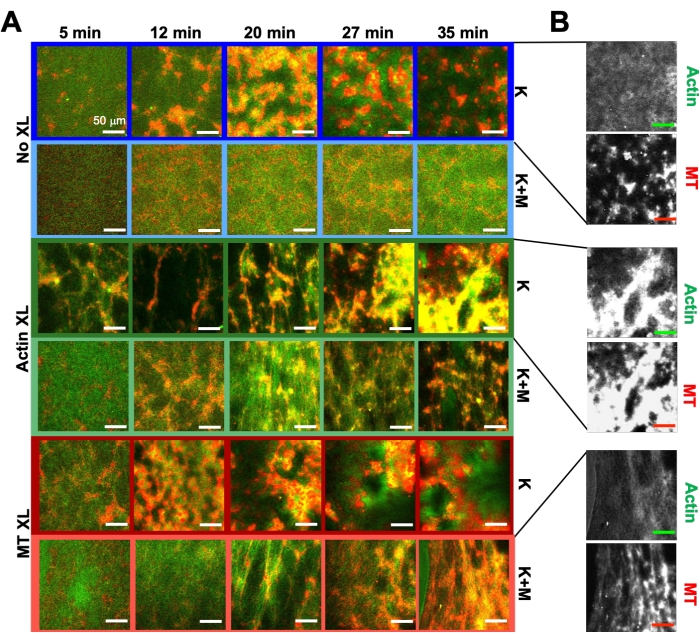
図 6.キネシンモーターとパッシブ架橋剤をアクティブコンポジットに組み込んで、プログラマビリティを高め、ダイナミクスと構造の位相空間を拡大します。(A)活性複合材料中のアクチン(緑)と微小管(赤)の2色共焦点画像は、時間の経過とともに複雑な製剤依存的な再構築を示しています(分でリストされています)。各行の5つの画像は、キネシン(K、行1、3、5)またはキネシンとミオシン(K+M、行2、4、6)によって駆動される複合材料について取得された2000フレーム時系列の5フレームに対応し、パッシブ架橋剤なし(XLなし、行1、2)、アクチン-アクチン架橋(アクチンXL、行3、4)、または微小管-微小管架橋(MT XL、 行 5、6)。スケールバーはすべて50μmです。アウトラインの色は、図 8 の配色と一致します。(B)キネシンのみの複合材料用の別々のアクチンおよび微小管蛍光チャネルは、アクチン-MT共局在とミクロ相分離の両方でさまざまな構造を示します。示されている画像は、c A = 2.32 μM、c T = 3.48 μM、c K = 0.35 μM、cM = 0.47 μM(行2、4、6)、RA = 0.02(行3、4)、およびRMT = 0.005(行5、6)の複合材料の場合です。すべての複合材料は、アクチンと微小管の均一に分布した相互侵入ネットワークから始まります(カラム1)。架橋剤を含まないキネシン駆動複合材料(行1)は、MTリッチな緩結合アモルファスクラスターを形成します。アクチンは、最初はこれらの凝集体の中心で共局在しますが、その後、収縮して互いに切断し続けるMTリッチ領域から絞り出されます。アクチン-アクチン架橋(行3)は、このマイクロスケールのアクチン-MT分離を妨げ、代わりにMTリッチ凝集体はアクチンの長い鎖を介して結合されます。アクチン架橋はまた、MTリッチ領域へのアクチンのゆっくりとした取り込みを可能にし、その結果、複合体は共局在アクチンとMTクラスターの接続ネットワークになります。微小管架橋(行5)は、時間の経過とともに合体するMTのアモルファスクラスタリングをもたらし、アクチンとMTの大規模な相分離をもたらします。 ミオシンを添加すると(行2、4、6)、キネシンによる脱混合と再構築が減少します。架橋剤がない場合(2列目)、複合材料は数時間にわたってほとんど再配列を示しません。架橋は、アクチンと微小管の再構築と共局在を増加させます(行4、6)。具体的には、微小管が架橋されると(列6)、線維のウェブ状ネットワークへの有意な相互浸透および再編成がある。この図は参考文献50から修正されています。この図の拡大版を表示するには、ここをクリックしてください。
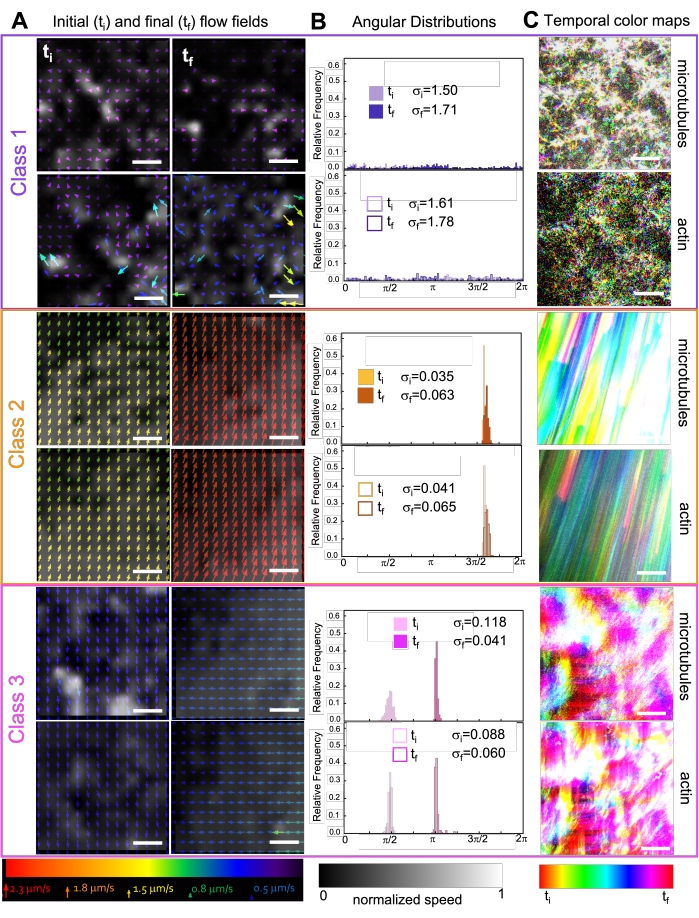
図 7.PIVは、アクティブ複合材料が時空間的に異なる流れ場の3つのクラスを示すことを示しています。(a)3つの代表的な時系列の最初の(ti)フレームと最後の(tf)フレームに対するPIVフローフィールドは、図6に示す複合材が示す異なる動的クラスを示す。クラス1(上、紫)、クラス2(中央、オレンジ)、クラス3(下、マゼンタ)のサンプルビデオの微小管(上)とアクチン(下)のPIVフローフィールド、下部にユニバーサルスピードスケールに対応する矢印の色、および空間速度分布を示すグレースケールカラーマップは、下部に示すスケールに従ってフローフィールドごとに個別に正規化されています。スケールバーはすべて50μMです。(B)Aからの速度ベクトルの角度分布(ラジアン単位)で、初期 および最終標準偏差σ iおよびσfがリストされています。(C)AとBで分析されたビデオの時間カラーマップは、その開始点に対する各ピクセルのフレーム間位置を示しています。クラス1マップは、小規模なランダムモーションを示します。クラス2マップは、空間的または時間的変動を最小限に抑えた高速の一方向の動きを示しています。クラス3マップは、クラス1とクラス2の両方の機能を示します。この図は参考文献50から修正されています。この図の拡大版を表示するには、ここをクリックしてください。
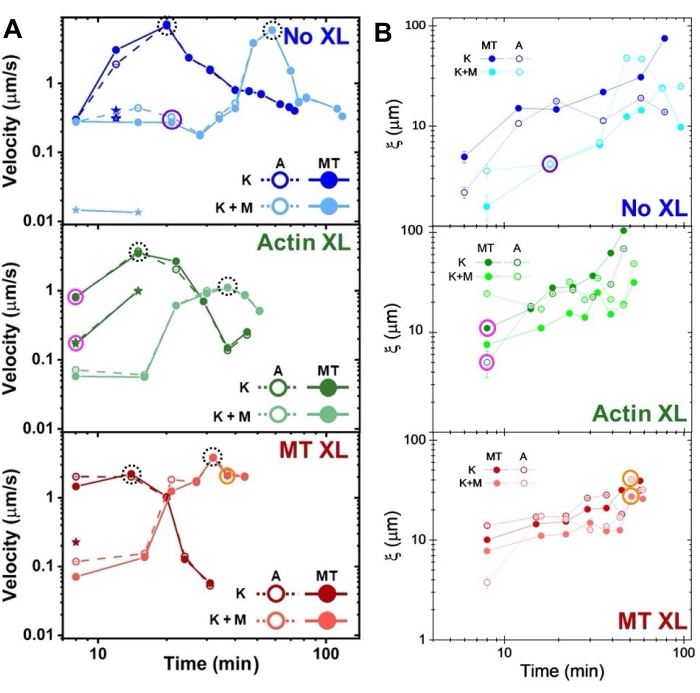
図 8.DDMとSIAは、2モーターアクチン-微小管複合材料の時間変化するダイナミクスと構造を測定します。(A)DDMを介して測定された図6および図7に記載されている複合材料の速度は、架橋およびミオシン活性によってプログラムされた複合材料の加速および減速を示す。微小管(MT、閉じた円)とアクチン(A、白丸)の速度は、架橋なし(上、青)、アクチン架橋(中央、緑)、微小管架橋(下、赤)、ミオシンなし(K、暗い色合い)、およびミオシン(K + M、明るい色合い)の複合材料の活性時間の関数としてプロットされます。速度が 2 つのクラス 3 の場合、低速は星印で示されます。黒い破線の円で囲まれたデータポイントは、各定式化の最高速度vmaxに対応します。エラーバー(ほとんどが小さすぎて見えない)は、対応するτ(q)のべき乗則適合に対する標準誤差です。(B)Aで評価された同じ時系列のセットについて、SIAを介して決定された構造相関の長さξと活動時間。各データポイントは、対応する時系列の最初と最後のフレームに対して決定された相関長の平均です。一般に、ξはすべての複合材料系においてアクチンと微小管の両方で時間的に増加し、キネシンのみによって駆動される複合材料は、ミオシンも存在する複合材料よりも相関長が大きくなります。図 7 で分析された 3 つの時系列に対応する A と B のデータ ポイントは、対応するクラスの色 (1 = 紫、2 = オレンジ、3 = マゼンタ) で囲まれています。この図は参考文献50から修正されています。この図の拡大版を表示するには、ここをクリックしてください。
上記の再構成システムの主な進歩は、そのモジュール性と調整可能性であるため、ユーザーは、特定の細胞プロセスをエミュレートしたり、特定の機能や機械的特性を持つ材料を設計したりするなど、目的の結果に合わせてタンパク質、モーター、架橋剤などの濃度を変更することをお勧めします。アクチンおよびチューブリンの濃度範囲の制限は、アクチン(~0.2 μM)57,58,59およびチューブリン(~3 - 4 μM)60の重合に必要な臨界濃度によって下限に設定され、アクチンフィラメント(~90 μM)61,62または微小管(~35 μM)63のネマチックアライメントへの移行によって上限に設定されます。.アクチンモノマーとチューブリン二量体は、互いに相乗的に支持する均質に相互侵入するパーコレートネットワークを形成するために、重合後に一緒に混合するのではなく、一緒にフィラメントに重合する必要があります。複合材料が示す新しいダイナミクスは、この相互作用に依存しています。一般に、示されている結果を正常に再現するには、プロトコルで概説されているすべての手順に従うことが重要ですが、より厳密な手順もあれば、特定のニーズと利用可能なリソースに合わせて変更および調整する余地がある手順もあります。
たとえば、再現性のある結果を確保するための重要なステップの1つは、材料表に記載されているガイドラインに従って試薬を適切に調製および保管することです。細胞骨格タンパク質(アクチン、チューブリン、ミオシン、キネシン)は不安定であるため、分注し、液体窒素で瞬間凍結し、使い捨てアリコートで-80°Cで保存する必要があります。-80°Cから除去したら、アリコートを氷上に保持する必要があります。細胞骨格タンパク質は、追加の凍結融解サイクル後に機能を確実に保持しません。
微小管は、アクチンよりも解重合および変性に対してより敏感である。チューブリンを-80°Cから取り出したら、重合前に氷上に保持し、12時間以内に使用する必要があります。重合したら、微小管は室温に保つ必要があります。また、解重合を防ぐために微小管をタキソールで安定化させることも重要です。アクチンフィラメントのファロイジン安定化は、ミオシンおよびキネシン活性と競合するATP消費アクチントレッドミルを抑制するために同様に重要である。
ミオシンモーターの超遠心分離は、不活性なミオシンデッドヘッドを除去するため、別の重要なステップです。酵素的に不活性なモノマーを除去しないと、アクチンネットワークの受動架橋および活性の喪失が生じる。モーターのATPアーゼ活性を延長するために、クレアチンリン酸およびクレアチンホスホキナーゼ64 などのATP再生システムを組み込むことができる。
最後に、複合活性を維持するには、サンプルチャンバーの壁へのフィラメントとモーターの吸着を抑制する必要があり、これは顕微鏡のカバーガラスとスライドの不動態化によって達成できます。モータータンパク質は特に吸着しやすく、その結果、複合材料がサンプルチャンバーの表面に引っ張られ、視野から外れ、2Dに崩壊し、活性がなくなります。カバーガラスとスライドをシラン化することは、表面を不動態化し、吸着を防ぐ効果的な方法です(手順1を参照)。 インビトロ 細胞骨格実験において効果的に使用される代替のパッシベーション方法は、細胞膜18と同様に、脂質二重層で表面をコーティングすることである。この方法は、タンパク質を表面につなぎ留めたり、他の特定のタンパク質-表面相互作用を導入したりする場合に、二重層を機能化できるため有利です。光ピンセット実験では、ミクロスフェアの不動態化も重要であり、カルボジイミド架橋剤化学 を介して カルボキシル化ミクロスフェアをBSAまたはPEGでコーティングすることによって達成することができる48。
提示されたプロトコルには、研究者がニーズに合わせて変更することを検討する可能性のあるいくつかの側面があります。第一に、研究者は、非天然のビオチン-NA架橋剤を、アクチンおよび微小管をそれぞれ架橋するα-アクチニンまたはMAP65などの生物学的架橋剤に置き換えることを選択することができる28,65,66。ここで説明する複合材料における非天然架橋剤の使用は、天然架橋剤と比較して再現性、安定性、および同調性が向上していることが動機となっています。強力なビオチン-NA結合のため、架橋剤は、広範囲の回転率で一過性に結合するほとんどの天然架橋剤ではなく、永続的であると見なすことができます。過渡架橋のダイナミクスは、架橋剤とモーターからダイナミクスへの寄与の解析を複雑にします。さらに、ビオチン-NAリンカーは、アクチンと微小管の両方を架橋するために、またアクチンを微小管に架橋するために多目的に使用できます。このようにして、他のすべての変数(例えば、架橋剤サイズ、結合親和性、化学量論など)を固定したまま、架橋モチーフ間の明確な比較を行うことができます。最後に、ビオチン-NAリンカーを組み込むために必要な試薬は、広く市販されており、十分に特徴付けられており、多くの生物物理学研究室で一般的に使用されています。ただし、ここで説明するin vitroプラットフォームの主要な強みの1つはモジュール性であるため、研究者は必要に応じてビオチン-NAリンカーをネイティブリンカーにシームレスに置き換えることができるはずです。
第二に、現在のプロトコルでは、アクチンモノマーとチューブリン二量体は、サンプルチャンバーに追加する前に、遠沈管内で一緒にフィラメントに重合されます。絡み合った糸状タンパク質の溶液をサンプルチャンバーに流すと、特に微小管の流れが整列し、複合材料の望ましい等方性と均質性が損なわれる可能性があります。実際、定常状態のアクチン-微小管複合材料に関する以前の研究における大きな進歩は、アクチンと微小管をin situ(サンプルチャンバー内)で共重合して、アクチンと微小管の等方性相互侵入ネットワークの形成を確実にする能力でした15,16,27。ただし、このアプローチを活性複合材料に拡張するには、アクチンとチューブリンの重合前にモーターをサンプルに追加し、実験前にサンプル全体を37°Cで一緒にインキュベートする必要があります。プロトコルに対するこの変動のテストでは、おそらく競合するATPase活性とモーターの長時間の37°Cインキュベーションが原因で、アクチン重合が減少し、識別可能な運動活性が見られませんでした。幸いなことに、図2、図3、および図6に示すように、現在のプロトコルに従うと、複合材料の識別可能なフローアライメントはありません。それにもかかわらず、研究者は、活性複合材料のin situ形成を可能にするプロトコルを設計することが奨励されています。
別の考慮事項は、ネットワーク内のすべてのアクチンフィラメントと微小管をまばらに標識することを伴う蛍光標識スキームです。このラベリングアプローチは、トレーサーフィラメントやミクロスフェア を介して 構造とダイナミクスを推測するのではなく、ネットワークの構造を直接視覚化するように最適化されました。ただし、トレードオフは、個々のフィラメントが明るくラベル付けされて解決できないことです。研究者が単一のフィラメントの分離とネットワーク構造の視覚化の両方に採用できるアプローチの1つは、別の蛍光色素で標識された事前に形成されたフィラメントにドープして、周囲のネットワークと個々のフィラメントの両方を同時にイメージングできるようにすることです。ただし、2つ以上の蛍光色素と励起/発光チャンネルを使用する場合、チャンネル間のブリードスルーを排除するのは難しいことが多いため、蛍光色素、フィルター、レーザー強度の選択には注意が必要です。
関連する制限は、複合材料中のミオシンまたはキネシンモーターを視覚化できないことです。使用される蛍光標識アクチンモノマーおよびチューブリン二量体は市販されているが、複合材料中のミオシンまたはキネシンの可視化には社内標識が必要である。研究者は、以前に行われたように、モーターにラベルを付けるための次のステップを踏むことが奨励されています18,67、運動活動と結合を私たちの複合材料が示すダイナミクスと構造に明確に結び付けることができるようにするためです。
最後に、現在のプロトコルでは、キネシン活性の開始および持続時間は制御されていないことに注意することが重要です。ミオシン活性はブレビスタチンの光失活を用いて制御されるので、上述のように、キネシンの同様の光活性化を組み込むために、光活性化ATPを組み込むことができる。
ここで説明する設計の複雑さを構築し、細胞条件をよりよく模倣し、動的構造関数パラメータ空間を広げるために、将来の作業では、ビメンチン68,69などの中間フィラメントや、ダイニン13,70などの他のモーターを組み込むことに焦点を当てます。ゲルソリンはまた、アクチン長14を制御するために異なる濃度で組み込まれ、微小管の剛性を制御するためにタウタンパク質も組み込まれます。
要約すると、提示されたプロトコルは、単一のシステム内の異なる基質に作用する2つの別々の活性力発生コンポーネントを含む、細胞骨格に触発された活性物質システムのダイナミクス、構造、およびメカニズムを設計、作成、および特性評価する方法を説明しています。このチューナブルでモジュール式のプラットフォームは、再構成の取り組みを細胞の細胞骨格の模倣に一歩近づけ、さまざまなコンポーネントを独立して組み込む、除去する、調整することにより、広いフェーズスペースにわたってその特性をプログラムする独自の機能を提供します。さらに、この汎用性の高いシステムの全ての成分は、前述のようにロスラボで精製され50、要求に応じて入手可能なキネシン二量体を除いて、市販されている(材料の表を参照)。最後に、すべての分析コードはGitHub49 から無料で入手でき、無料のプログラミング言語とソフトウェア(Pythonとフィジー)に基づいています。これらのシステムを設計するためのプロトコルの透過的な普及により、さまざまな専門知識、背景、所属機関、および研究目標を持つ多様なユーザーグループがこのプラットフォームにアクセスしやすくなることを願っています。
著者は開示するものは何もありません
我々は、データ分析の支援をしてくれたマヤ・ヘンディヤ博士とジョナサン・ミシェル博士、有益な議論と指導をしてくれたジャネット・シュン博士、モウミタ・ダス博士、マイケル・ラスト博士に感謝する。この研究は、RMRAとJLRに授与されたウィリアムM.ケック財団研究助成金とNSF DMREF賞(DMR 2119663)、およびRMR-AとRJMに授与された国立衛生研究所R15助成金(R15GM123420、2R15GM123420-02)によってサポートされました。
| Name | Company | Catalog Number | Comments |
| (-)-Blebbistatin Abbreviation used in paper: blebbistatin | Sigma Aldrich | B0560 | Stock Concentration: 200 μM in DMSO Storage: dessicated, in DMSO, -20ºC Stock and Experiment Recipes: dissolve 1 mg of powder to 200 μM in DMSO Storage, Handling, Troubleshooting Notes: limited shelf-life, typically stops functioning reliably after 3-4 months. purchase and prepare new solution every 3 months. |
| 1:20 488-tubulin:tubulin mixture Abbreviation used in paper: 5-488-tubulin | NA | NA | Stock Concentration: 5 mg/ml in PEM Storage: single use aliquots, -80ºC, avoid freeze-thaw cycles Stock and Experiment Recipes: mix tubulin and 488-tubulin at a 20:1 ratio, flash freeze with LN2 Storage, Handling, Troubleshooting Notes: each aliquot can be used for up to 12 hrs stored on ice at 4ºC, protect from light |
| 1:20 R-tubulin:tubulin mixture Abbreviation used in paper: 5-R-tubulin | NA | NA | Stock Concentration: 5 mg/ml in PEM Storage: single use aliquots, -80ºC, avoid freeze-thaw cycles Stock and Experiment Recipes: mix tubulin and rhodamine tubulin at a 20:1 ratio, flash freeze with LN2 Storage, Handling, Troubleshooting Notes: each aliquot can be used for up to 12 hrs stored on ice at 4ºC, protect from light |
| actin (biotin): skeletal muscle Abbreviation used in paper: biotin-actin | Cytoskeleton | AB07 | Stock Concentration: 1 mg/ml in G-buffer Storage: single use aliquots, -80ºC, avoid freeze-thaw cycles Stock and Experiment Recipes: reconstitute to 1 mg/ml in G-buffer, flash freeze with LN2 Storage, Handling, Troubleshooting Notes: (1) immediately prior to use dilute to 0.5 mg/ml in PEM, (2) once removed from -80ºC, store aliquot on ice at 4ºC for up to 1 week |
| actin (rhodamine): rabbit skeletal muscle Abbreviation used in paper: R-actin | Cytoskeleton | AR05 | Stock Concentration: 1.5 mg/ml in G-buffer Storage: single use aliquots, -80ºC, avoid freeze-thaw cycles Stock and Experiment Recipes: reconstitute to 1.5 mg/ml in G-buffer, flash freeze with LN2 Storage, Handling, Troubleshooting Notes: once removed from -80ºC, store aliquot on ice at 4ºC, can be used for up to 1 week |
| adenosine triphosphate Abbreviation used in paper: ATP | Thermo Fisher Scientific | A1048 | Stock Concentration: 100 mM Storage: in solution (pH 7), -20ºC Stock and Experiment Recipes: reconsitute in DI H20, bring pH to 7 with NaOH Storage, Handling, Troubleshooting Notes: routinely check pH and adjust as needed, hydrolyzes over time, replace every ~6-12 months |
| AlexaFluor488 Phalloidin Abbreviation used in paper: 488-phalloidin | Thermo Fisher Scientific | A12379 | Stock Concentration: 100 μM DMSO Storage: protected from light, dessicated, -20ºC Stock and Experiment Recipes: reconstitute to 100 μM with DMSO Storage, Handling, Troubleshooting Notes: immediately prior to use dilute to 20 μM in PEM (1 μL in 4 μL PEM) |
| AlexaFluor488–labeled actin Abbreviation used in paper: 488-actin | Thermo Fisher Scientific | A12373 | Stock Concentration: 1.5 mg/ml in G-buffer Storage: single use aliquots, -80ºC, avoid freeze-thaw cycles Stock and Experiment Recipes: reconstitute to 1.5 mg/ml in G-buffer, flash freeze with LN2 Storage, Handling, Troubleshooting Notes: this item has been discontinued |
| Basic Plasma Cleaner Abbreviation used in paper: plasma cleaner | Harrick Plasma | PDC-32G | |
| Bemis Parafilm M Laboratory Wrapping Film Abbreviation used in paper: transparent film | Thermo Fisher Scientific | 13-374-5 | |
| D-(+)-Glucose Abbreviation used in paper: | Thermo Fisher Scientific | A1682836 | Stock Concentration: 100x Storage: store at stock concentration (100x) or 10x concentration, dessicated, at -20ºC Stock and Experiment Recipes: reconstitute powder to 4.5 mg/ml in DI H20 Storage, Handling, Troubleshooting Notes: final concentration in solution should 45 μg/mL |
| D-Biotin Abbreviation used in paper: biotin | Fisher Scientific | BP232-1 | Stock Concentration: 1.02 mM in PEM Storage: dessicated, 4ºC |
| deionized nanopure water Abbreviation used in paper: DI | |||
| Dimethyldichlorosilane Abbreviation used in paper: silane | Thermo Fisher Scientific | D/3820/PB05 | Stock Concentration: 2% dissolved in Toulene |
| Dithiothreitol Abbreviation used in paper: DTT | Thermo Fisher Scientific | R0861 | Stock Concentration: 1 M in DMSO Storage: dessicated, -20ºC Stock and Experiment Recipes: dilute to 2 mM in PEM immediately before each experiment |
| DMSO Anhydrous Abbreviation used in paper: DMSO | Thermo Fisher Scientific | D12345 | |
| F-Buffer Abbreviation used in paper: F-buffer | NA | NA | Stock Concentration: 10x Storage: dessicated, -20ºC Stock and Experiment Recipes: 10 mM Imidazole (pH 7.0), 50 mM KCl, 1 mM MgCl2, 1 mM EGTA, 0.2 mM ATP |
| G-Buffer Abbreviation used in paper: G-buffer | NA | NA | Stock Concentration: 10x Storage: dessicated, -20ºC Stock and Experiment Recipes: 2.0 mM Tris (pH 8), 0.2 mM ATP, 0.5 mM DTT, 0.1 mM CaCl2. Store at -20°C. |
| glass microscope slide Abbreviation used in paper: slide | Thermo Fisher Scientific | 22-310397 | |
| Glucose oxidase + catalase + β-mercaptoethanol Abbreviation used in paper: GOC | Sigma Aldrich | G2133-250KU, C1345, 63689 | Stock Concentration: 100x Storage: store at stock concentration (100x) or 10x concentration, dessicated, at -20ºC Stock and Experiment Recipes: For 100x: 4.3 mg/ml glucose oxidase, 0.7 mg/ml catalase, 0.5% v/v β-mercaptoethanol in DI H20 Storage, Handling, Troubleshooting Notes: final concentration in solution should be: 0.005% β-mercaptoethanol, 43 μg/mL glucose oxidase, 7 μg/mL catalase |
| glu-GOC oxygen scavenging system Abbreviation used in paper: glu-GOC | NA | NA | Stock Concentration: 100x Storage: prepare fresh each time Stock and Experiment Recipes: mix equal parts Glu and GOC and add at 1/100 final sample volume immediately before imaging Storage, Handling, Troubleshooting Notes: prepare from Glu and GOC immediately before imaging |
| Guanosine triphosphate Abbreviation used in paper: GTP | Thermo Fisher Scientific | R0461 | Stock Concentration: 100 mM Storage: 100 μL aliquots at -20ºC |
| Instant Mix 1-minute epoxy Abbreviation used in paper: epoxy | Loctite | 1366072 | |
| Kinesin-1 401 BIO 6x HIS Abbreviation used in paper: kinesin | Prepared in JL Ross Lab at Syracuse University | NA | Stock Concentration: 8.87 μM in PEM Storage: single use aliquots, -80ºC, avoid freeze-thaw cycles Storage, Handling, Troubleshooting Notes: biotinylated dimers form kinesin clusters, each aliquot can be used for up to 12 hrs stored on ice at 4ºC |
| NeutrAvidin Abbreviation used in paper: NA | Thermo Fisher Scientific | 31000 | Stock Concentration: 5 mg/ml in PEM Storage: dessicated, -20ºC Stock and Experiment Recipes: reconstitute powder to 5 mg/ml in PEM |
| No 1. glass coverslips (24 mm x 24 mm) Abbreviation used in paper: coverslip | Thermo Fisher Scientific | 12-548-CP | |
| Paclitaxel Abbreviation used in paper: Taxol | Thermo Fisher Scientific | P3456 | Stock Concentration: 2 mM in DMSO Storage: protected from light, dessicated, -20ºC Stock and Experiment Recipes: reconstitute to 2 mM with DMSO Storage, Handling, Troubleshooting Notes: immediately prior to use dilute to 200 μM in DMSO (0.4 μL in 3.6 μL DMSO) |
| PEM-100 Abbreviation used in paper: PEM | NA | NA | Stock Concentration: 1x Storage: room temperature (RT) Stock and Experiment Recipes: 100 mM K-PIPES (pH 6.8), 2 mM EGTA, 2 mM MgCl2 Storage, Handling, Troubleshooting Notes: use KOH to adjust pH to 6.8, recheck pH often and adjust accordingly |
| phalloidin Abbreviation used in paper: phalloidin | Thermo Fisher Scientific | P3457 | Stock Concentration: 100 μM in DMSO Storage: protected from light, dessicated, -20ºC, adhere closely to storage/handling conditions Stock and Experiment Recipes: reconstitute to 100 μM with DMSO Storage, Handling, Troubleshooting Notes: susceptible to impurities in its preparation and denaturing, identifiable as large amorphous aggregates of actin in samples |
| porcine brain tubulin Abbreviation used in paper: tubulin | Cytoskeleton | T240 | Stock Concentration: 5 mg/ml in PEM Storage: single use aliquots, -80ºC, avoid freeze-thaw cycles Stock and Experiment Recipes: reconstitute powder to 5 mg/ml in PEM, flash freeze with LN2 Storage, Handling, Troubleshooting Notes: each aliquot can be used for up to 12 hrs stored on ice at 4ºC |
| Potassium Chloride Abbreviation used in paper: KCl | Thermo Fisher Scientific | AM9640G | Stock Concentration: 4 M Storage: RT |
| Rabbit skeletal actin Abbreviation used in paper: actin | Cytoskeleton | AKL99 | Stock Concentration: 2 mg/ml in G-buffer Storage: single use aliquots, -80ºC, avoid freeze-thaw cycles Stock and Experiment Recipes: reconstitute to 2 mg/ml in G-buffer, flash freeze with LN2 Storage, Handling, Troubleshooting Notes: once removed from -80ºC, store aliquot on ice at 4ºC, can be used for up to 1 week |
| Rabbit skeletal myosin II Abbreviation used in paper: myosin | Cytoskeleton | MY02 | Stock Concentration: 10 mg/ml in PEM Storage: single use aliquots, -80ºC, avoid freeze-thaw cycles Stock and Experiment Recipes: reconstitute powder to 10 mg/ml in PEM, flash freeze with LN2 Storage, Handling, Troubleshooting Notes: monomers form minifilaments at low KCl, each aliquot can be used for up to 12 hrs stored on ice at 4ºC |
| Tubulin (biotin): porcine brain Abbreviation used in paper: biotin-tubulin | Cytoskeleton | T333P | Stock Concentration: 5 mg/ml in PEM Storage: single use aliquots, -80ºC, avoid freeze-thaw cycles Stock and Experiment Recipes: reconstitute powder to 5 mg/ml in PEM, flash freeze with LN2 Storage, Handling, Troubleshooting Notes: immediately prior to use dilute to 0.5 mg/ml in PEM |
| Tubulin (fluorescent HiLyte 488): porcine brain Abbreviation used in paper: 488-tubulin | Cytoskeleton | TL488M | Stock Concentration: 5 mg/ml in PEM Storage: single use aliquots, -80ºC, avoid freeze-thaw cycles Stock and Experiment Recipes: reconstitute powder to 5 mg/ml in PEM, flash freeze with LN2 Storage, Handling, Troubleshooting Notes: each aliquot can be used for up to 12 hrs stored on ice at 4ºC, protect from light |
| tubulin (rhodamine): porcine brain Abbreviation used in paper: R-tubulin | Cytoskeleton | TL590M | Stock Concentration: 5 mg/ml in PEM Storage: single use aliquots, -80ºC, avoid freeze-thaw cycles Stock and Experiment Recipes: reconstitute powder to 5 mg/ml in PEM, flash freeze with LN2 Storage, Handling, Troubleshooting Notes: each aliquot can be used for up to 12 hrs stored on ice at 4ºC, protect from light |
| Tween 20 Abbreviation used in paper: Tween20 | Thermo Fisher Scientific | J20605.AP | Stock Concentration: 1% v/v in DI H20 Storage: RT |
| ultracentrifuge grade microtubes Abbreviation used in paper: Beckman-Coulter Optima Max XP | Beckman Coultier | 343776 | Storage, Handling, Troubleshooting Notes: 8x34 mm PC |
| UV light curing glue Abbreviation used in paper: UV glue | Pharda | SKG-2869 |
- Fletcher, D. A., Mullins, R. D. Cell mechanics and the cytoskeleton. Nature. 463 (7280), 485-492 (2010).
- Koenderink, G. H., Paluch, E. K. Architecture shapes contractility in actomyosin networks. Current Opinion in Cell Biology. 50, 79-85 (2018).
- Dogterom, M., Koenderink, G. H. Actin-microtubule crosstalk in cell biology. Nature Reviews Molecular Cell Biology. 20 (1), 38-54 (2019).
- Burla, F., Mulla, Y., Vos, B. E., Aufderhorst-Roberts, A., Koenderink, G. H. From mechanical resilience to active material properties in biopolymer networks. Nature Reviews Physics. 1 (4), 249-263 (2019).
- Wen, Q., Janmey, P. A. Polymer physics of the cytoskeleton. Current Opinion in Solid State and Materials Science. 15 (5), 177-182 (2011).
- Xiao, Q., Hu, X., Wei, Z., Tam, K. Y. Cytoskeleton molecular motors: structures and their functions in neuron. International Journal of Biological Sciences. 12 (9), 1083-1092 (2016).
- Ajeti, V. et al. Wound healing coordinates actin architectures to regulate mechanical work. Nature Physics. 15 (7), 696-705 (2019).
- Jung, W. et al. Dynamic motions of molecular motors in the actin cytoskeleton. Cytoskeleton. 76 (11-12), 517-531 (2019).
- Pollard, T. D., O'Shaughnessy, B. Molecular mechanism of cytokinesis. Annual Review of Biochemistry. 88 (1), 661-689 (2019).
- Huber, F., Boire, A., López, M. P., Koenderink, G. H. Cytoskeletal crosstalk: when three different personalities team up. Current Opinion in Cell Biology. 32, 39-47 (2015).
- Rivero, F. et al. The role of the cortical cytoskeleton: F-actin crosslinking proteins protect against osmotic stress, ensure cell size, cell shape and motility, and contribute to phagocytosis and development. Journal of Cell Science. 109 (11), 2679-2691 (1996).
- Duclos, G. et al. Topological structure and dynamics of three-dimensional active nematics. Science. 367 (6482), 1120-1124 (2020).
- Baclayon, M. et al. Optical tweezers-based measurements of forces and dynamics at microtubule ends. Optical Tweezers. 1486, 411-435 (2017).
- Gurmessa, B., Fitzpatrick, R., Falzone, T. T., Robertson-Anderson, R. M. Entanglement density tunes microscale nonlinear response of entangled actin. Macromolecules. 49 (10), 3948-3955 (2016).
- Francis, M. L. et al. Non-monotonic dependence of stiffness on actin crosslinking in cytoskeleton composites. Soft Matter. 15 (44), 9056-9065 (2019).
- Ricketts, S. N. et al. Varying crosslinking motifs drive the mesoscale mechanics of actin-microtubule composites. Scientific Reports. 9 (1), 12831 (2019).
- Lee, G. et al. Active cytoskeletal composites display emergent tunable contractility and restructuring. Soft Matter. 17 (47), 10765-10776 (2021).
- Murrell, M. P., Gardel, M. L. F-actin buckling coordinates contractility and severing in a biomimetic actomyosin cortex. Proceedings of the National Academy of Sciences. 109 (51), 20820-20825 (2012).
- Soares e Silva, M. et al. Active multistage coarsening of actin networks driven by myosin motors. Proceedings of the National Academy of Sciences. 108 (23), 9408-9413 (2011).
- Sonn-Segev, A., Bernheim-Groswasser, A., Roichman, Y. Dynamics in steady state in vitro acto-myosin networks. Journal of Physics: Condensed Matter. 29 (16), 163002 (2017).
- Ideses, Y., Sonn-Segev, A., Roichman, Y., Bernheim-Groswasser, A. Myosin II does it all: assembly, remodeling, and disassembly of actin networks are governed by myosin II activity. Soft Matter. 9 (29), 7127 (2013).
- Fürthauer, S. et al. Self-straining of actively crosslinked microtubule networks. Nature Physics. 15 (12), 1295-1300 (2019).
- Lemma, L. M. et al. Multiscale microtubule dynamics in active nematics. Physical Review Letters. 127 (14), 148001 (2021).
- Fan, Y., Wu, K.-T., Aghvami, S. A., Fraden, S., Breuer, K. S. Effects of confinement on the dynamics and correlation scales in kinesin-microtubule active fluids. Physical Review E. 104 (3), 034601 (2021).
- Triclin, S. et al. Self-repair protects microtubules from destruction by molecular motors. Nature Materials. 20 (6), 883-891 (2021).
- Lee, G. et al. Myosin-driven actin-microtubule networks exhibit self-organized contractile dynamics. Science Advances. 7 (6), eabe4334 (2021).
- Ricketts, S. N., Ross, J. L., Robertson-Anderson, R. M. Co-entangled actin-microtubule composites exhibit tunable stiffness and power-law stress relaxation. Biophysical Journal. 115 (6), 1055-1067 (2018).
- Bendix, P. M. et al. A quantitative analysis of contractility in active cytoskeletal protein networks. Biophysical Journal. 94 (8), 3126-3136 (2008).
- Linsmeier, I. et al. Disordered actomyosin networks are sufficient to produce cooperative and telescopic contractility. Nature Communications. 7 (1), 12615 (2016).
- Stam, S. et al. Filament rigidity and connectivity tune the deformation modes of active biopolymer networks. Proceedings of the National Academy of Sciences. 114 (47), E10037-E10045 (2017).
- Yadav, V. et al. Filament nucleation tunes mechanical memory in active polymer networks. Advanced Functional Materials. 29 (49), 1905243 (2019).
- Ennomani, H. et al. Architecture and connectivity govern actin network contractility. Current Biology. 26 (5), 616-626 (2016).
- Alvarado, J., Sheinman, M., Sharma, A., MacKintosh, F. C., Koenderink, G. H. Molecular motors robustly drive active gels to a critically connected state. Nature Physics. 9 (9), 591-597 (2013).
- Alvarado, J., Cipelletti, L., Koenderink, G. H. Uncovering the dynamic precursors to motor-driven contraction of active gels. Soft Matter. 15 (42), 8552-8565 (2019).
- Jung, W., Murrell, M. P., Kim, T. F-actin cross-linking enhances the stability of force generation in disordered actomyosin networks. Computational Particle Mechanics. 2 (4), 317-327 (2015).
- Lenz, M., Thoresen, T., Gardel, M. L., Dinner, A. R. Contractile units in disordered actomyosin bundles arise from f-actin buckling. Physical Review Letters. 108 (23), 238107 (2012).
- Memarian, F.L. et al. Active nematic order and dynamic lane formation of microtubules driven by membrane-bound diffusing motors. Proceedings of the National Academy of Sciences. 118 (52), e2117107118 (2021).
- Needleman, D., Dogic, Z. Active matter at the interface between materials science and cell biology. Nature Reviews Materials. 2 (9), 17048 (2017).
- Foster, P. J., Fürthauer, S., Shelley, M. J., Needleman, D. J. Active contraction of microtubule networks. eLife. 4, e10837 (2015).
- Thijssen, K. et al. Submersed micropatterned structures control active nematic flow, topology, and concentration. Proceedings of the National Academy of Sciences. 118 (38), e2106038118 (2021).
- Sanchez, T., Chen, D. T. N., DeCamp, S. J., Heymann, M., Dogic, Z. Spontaneous motion in hierarchically assembled active matter. Nature. 491 (7424), 431-434 (2012).
- Colen, J. et al. Machine learning active-nematic hydrodynamics. Proceedings of the National Academy of Sciences. 118 (10), e2016708118 (2021).
- Mitchell, K. A., Tan, A. J., Arteaga, J., Hirst, L. S. Fractal generation in a two-dimensional active-nematic fluid. Chaos: An Interdisciplinary Journal of Nonlinear Science. 31 (7), 073125 (2021).
- Pandolfi, R. J., Edwards, L., Johnston, D., Becich, P., Hirst, L. S. Designing highly tunable semiflexible filament networks. Physical Review E. 89 (6), 062602 (2014).
- Tan, A. J. et al. Topological chaos in active nematics. Nature Physics. 15 (10), 1033-1039 (2019).
- Roostalu, J., Rickman, J., Thomas, C., Nédélec, F., Surrey, T. Determinants of polar versus nematic organization in networks of dynamic microtubules and mitotic motors. Cell. 175 (3), 796-808.e14 (2018).
- Ndlec, F. J., Surrey, T., Maggs, A. C., Leibler, S. Self-organization of microtubules and motors. Nature. 389 (6648), 305-308 (1997).
- Sheung, J. Y. et al. Motor-driven restructuring of cytoskeleton composites leads to tunable time-varying elasticity. ACS Macro Letters. 10 (9), 1151-1158 (2021).
- McGorty, R. PyDDM v0.2.0. Zenodo. (2022).
- Achiriloaie, D. H. et al. Kinesin and myosin motors compete to drive rich multi-phase dynamics in programmable cytoskeletal composites. arXiv. (2021).
- Wulstein, D. M., Regan, K. E., Garamella, J., McGorty, R. J., Robertson-Anderson, R. M. Topology-dependent anomalous dynamics of ring and linear DNA are sensitive to cytoskeleton crosslinking. Science Advances. 5 (12), eaay5912 (2019).
- McGorty, R. Image-Correlation. at <https://github.com/rmcgorty/Image-Correlation>. (2020).
- Robertson, C. Theory and practical recommendations for autocorrelation-based image correlation spectroscopy. Journal of Biomedical Optics. 17 (8), 080801 (2012).
- McGorty, R. Differential Dynamic Microscopy - Python. at <https://github.com/rmcgorty/Differential-Dynamic-Microscopy---Python>. (2021).
- Cerbino, R., Trappe, V. Differential dynamic microscopy: probing wave vector dependent dynamics with a microscope. Physical Review Letters. 100 (18), 188102 (2008).
- Robertson-Anderson, R. M. Optical tweezers microrheology: from the basics to advanced techniques and applications. ACS Macro Letters. 7 (8), 968-975 (2018).
- Pollard, T. D. Polymerization of ADP-actin. Journal of Cell Biology. 99 (3), 769-777 (1984).
- Coué, M., Brenner, S. L., Spector, I., Korn, E. D. Inhibition of actin polymerization by latrunculin A. FEBS Letters. 213 (2), 316-318 (1987).
- Pollard, T. D. Actin and actin-binding proteins. Cold Spring Harbor Perspectives in Biology. 8 (8), a018226 (2016).
- Kumar, N. Taxol-induced polymerization of purified tubulin. Mechanism of action. Journal of Biological Chemistry. 256 (20), 10435-10441 (1981).
- Käs, J. et al. F-actin, a model polymer for semiflexible chains in dilute, semidilute, and liquid crystalline solutions. Biophysical Journal. 70 (2), 609-625 (1996).
- Viamontes, J., Narayanan, S., Sandy, A. R., Tang, J. X. Orientational order parameter of the nematic liquid crystalline phase of F -actin. Physical Review E. 73 (6), 061901 (2006).
- Hitt, A. L., Cross, A. R., Williams, R. C. Microtubule solutions display nematic liquid crystalline structure. Journal of Biological Chemistry. 265 (3), 1639-1647 (1990).
- Andexer, J. N., Richter, M. Emerging enzymes for ATP regeneration in biocatalytic processes. ChemBioChem. 16 (3), 380-386 (2015).
- Farhadi, L. et al. Actin and microtubule crosslinkers tune mobility and control co-localization in a composite cytoskeletal network. Soft Matter. 16 (31), 7191-7201 (2020).
- Falzone, T. T., Lenz, M., Kovar, D. R., Gardel, M. L. Assembly kinetics determine the architecture of α-actinin crosslinked F-actin networks. Nature Communications. 3 (1), 861 (2012).
- Thoresen, T., Lenz, M., Gardel, M. L. Reconstitution of contractile actomyosin bundles. Biophysical Journal. 100 (11), 2698-2705 (2011).
- Sanghvi-Shah, R., Weber, G. F. Intermediate filaments at the junction of mechanotransduction, migration, and development. Frontiers in Cell and Developmental Biology. 5, 81 (2017).
- Shen, Y. et al. Effects of vimentin intermediate filaments on the structure and dynamics of in vitro multicomponent interpenetrating cytoskeletal networks. Physical Review Letters. 127 (10), 108101 (2021).
- Laan, L., Roth, S., Dogterom, M. End-on microtubule-dynein interactions and pulling-based positioning of microtubule organizing centers. Cell Cycle. 11 (20), 3750-3757 (2012).
Erratum
Erratum: Reconstituting and Characterizing Actin-Microtubule Composites with Tunable Motor-Driven Dynamics and MechanicsAn erratum was issued for: Reconstituting and Characterizing Actin-Microtubule Composites with Tunable Motor-Driven Dynamics and Mechanics. The Authors section was updated.
Mehrzad Sasanpour1
Daisy H. Achiriloaie1,2
Gloria Lee1
Gregor Leech1
Christopher Currie1
K. Alice Lindsay3
Jennifer L. Ross3
Ryan J. McGorty1
Rae M. Robertson-Anderson1
1Department of Physics and Biophysics, University of San Diego
2W. M. Keck Science Department, Scripps College, Pitzer College, and Claremont McKenna College
3Department of Physics, Syracuse University
to:
Mehrzad Sasanpour1
Daisy H. Achiriloaie1,2
Gloria Lee1
Gregor Leech1
Maya Hendija1
K. Alice Lindsay3
Jennifer L. Ross3
Ryan J. McGorty1
Rae M. Robertson-Anderson1
1Department of Physics and Biophysics, University of San Diego
2W. M. Keck Science Department, Scripps College, Pitzer College, and Claremont McKenna College
3Department of Physics, Syracuse University
Tags
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved