Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Cancer Research
Antikor Bağımlı Hücresel Sitotoksisiteyi Modifiye Eden Bileşiklerin Tanımlanması için Yüksek İçerikli Tarama Testi
Bu protokol, terapötik bir anti-HER-2 antikoru varlığında doğal öldürücü hücre aracılı meme kanseri hücresi öldürmeyi modüle eden bileşikleri tanımlamak için otomatik, görüntü tabanlı yüksek verimli bir teknik sunar.
Antijene özgü antikorlar veya immün kontrol noktası inhibitörleri ile immünoterapi, meme kanseri tedavisinde devrim yaratmıştır. Epidermal büyüme faktörü reseptörü HER2'yi eksprese eden meme kanseri hücreleri, anti-HER-2 antikoru trastuzumab tarafından hedeflenebilir. Antikora bağımlı hücresel sitotoksisite (ADCC), HER-2'nin antitümör etkisinde rol oynayan önemli bir mekanizmadır. Kanser hücrelerine bağlı trastuzumab, ADCC efektör hücrelerinin (örneğin, doğal öldürücü (NK) hücreler, makrofajlar ve granülositler) Fc reseptörleri tarafından tanınabilir ve bu bağışıklık hücrelerinin sitotoksik aktivitesini tetikleyerek kanser hücresi ölümüne yol açar. Yüksek içerikli tarama ile yeni ADCC modülatör bileşiklerini tanımlamak için ADCC'nin nicelleştirilmesi için görüntü tabanlı bir tahlil geliştirmek üzere yola çıktık. Tahlilde, JIMT-1 meme kanseri hücrelerini aşırı eksprese eden HER2, trastuzumab varlığında NK-92 hücreleri ile birlikte kültürlenir ve hedef hücre ölümü otomatik mikroskopi ve kantitatif görüntü analizi ile ölçülür. Hedef hücreler, EGFP floresanlarına göre efektör hücrelerden ayırt edilir. ADCC modülatör ilaçlarını tanımlamak için bileşik kütüphanelerin tahlilde nasıl test edilebileceğini gösteriyoruz. Bu amaçla, laboratuvar rafından rastgele seçilmiş ince kimyasallar kullanılarak bir bileşik kütüphane test plakası kuruldu. NK hücre göçü ve degranülasyonuna müdahale etmesi beklenen üç mikrotübül destabilize edici bileşik (kolşisin, vinkristin, podofillotoksin) de test kütüphanesine dahil edildi. Test ekranı, üç pozitif kontrol bileşiğinin hepsini, kimyasal bir kütüphanede ADCC modifiye edici ilaçları tanımlamak için yöntemin uygunluğunu kanıtlayan isabetler olarak tanımladı. Bu tahlil ile, antikanser immünoterapileri alan hastaların tedavisinde adjuvan terapötik ajanlar olarak kullanılabilecek ADCC arttırıcı bileşikleri tanımlamak için bileşik kütüphane ekranları yapılabilir. Ek olarak, yöntem, kanser hastaları tarafından farklı endikasyonlar için alınan terapötik ilaçların istenmeyen ADCC inhibe edici yan etkilerini tanımlamak için de kullanılabilir.
Antikanser antikorları, immün kontrol noktası inhibitörleri veya kimerik antijen reseptörü eksprese eden T (CAR-T) hücreleri ile immünoterapi, kanser tedavisine güçlü bir yaklaşımı temsil eder 1,2,3. Trastuzumab, HER-2 pozitif erken evre veya metastatik meme kanserinin yanı sıra HER-2 pozitif metastatik mide kanseri 4,5,6 tedavisinde kullanılan insanlaştırılmış bir monoklonal anti-HER-2 (insan epidermal büyüme faktörü reseptörü 2) antikorudur. Öncelikle epidermal büyüme faktörü
NOT: Tahlil iş akışının temel adımları Şekil 2'de sunulmuştur.
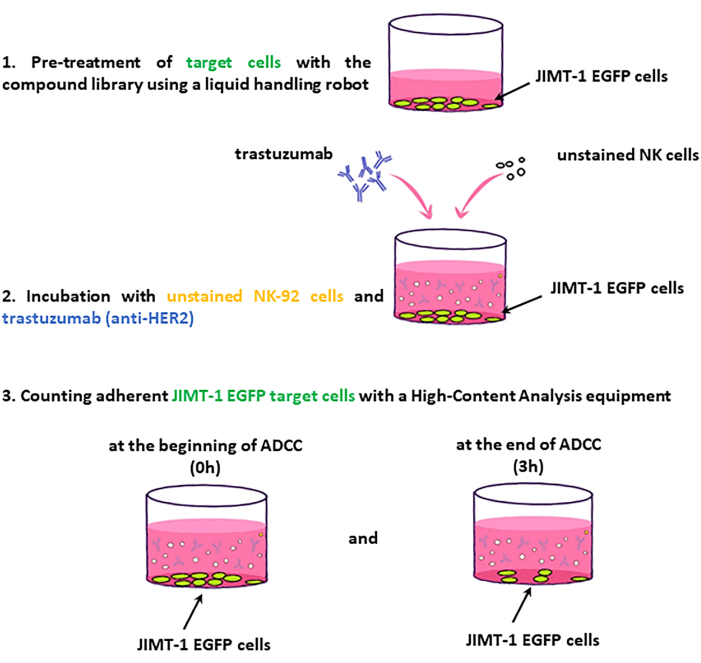
Şekil 2: ADCC ekranının iş akışı. 96 kuyucuklu HCS plakasına tohumlanan JIMT-1-EGFP hedef hücreleri, bileşik kütüphanesinin ilaçlarıyla muamele edilir. Buna karşılık, lekesiz NK (efektör) hücreleri ve t.......
Tahlilin gerçek hayatta nasıl çalıştığını göstermek için, laboratuvar raflarından rastgele seçilen 16 bileşikten oluşan bir test kütüphanesi oluşturduk (Şekil 3). Ek olarak, DMSO ayrıca negatif kontrol olarak ve pozitif kontroller olarak üç mikrotübül polimerizasyon inhibitörü bileşiği (kolşisin, vinkristin ve podofillotoksin) dahil edildi. İkincisinin, kanser hücrelerine NK hücre göçüne ve NK hücre degranülasyonuna müdahale ederek ADCC'yi inhibe etmesi .......
ADCC reaksiyonu nispeten uzun zaman önce tanımlanmıştır. Sürecin anahtar moleküler olayları da tanımlanmıştır19. ADCC'yi ölçme yöntemleri, altın standart radyoaktif krom salınım testinden, sitoplazmik enzim salınım testlerinden birkaç floresan bazlı akış sitometrisine veya mikroplaka tahlillerinekadar uzanır 20. Bununla birlikte, bu testlerin ortak bir sınırlaması, yüksek verimli uygulamalara uygun olmamalarıdır. Daha önce, ADCC modifiye edic.......
LV, Ulusal Araştırma, Geliştirme ve İnovasyon Ofisi'nden GINOP-2.3.2-15-2016-00010 TUMORDNS", GINOP-2.3.2-15-2016-00048-STAYALIVE ve OTKA K132193, K147482 hibelerinden fon aldı. CD16.176V.NK-92 hücreleri Dr. Kerry S. Campbell'den (Fox Chase Center, Philapedlphia, PA, Brink Biologics, lnc. San Diego, CA), dünya çapında patentlerle korunmaktadır ve Nantkwest, lnc tarafından lisanslanmıştır. Yazarlar, NK-92 hücre hattının kullanımı ve teknik tavsiyeler için György Vereb ve Árpád Szöőr'e teşekkür eder.
....| Name | Company | Catalog Number | Comments |
| 5-fluorouracil | Applichem | A7686 | in compound library |
| 96-well Cell Carrier Ultra plate | PerkinElmer | LLC 6055302 | |
| Betulin | Sigma | B9757 | in compound library |
| CD16.176V.NK92 cells | Nankwest Inc. | ||
| Cerulenin | ChemCruz | sc-396822 | in compound library |
| Cisplatin | Santa Cruz Biotechnology | sc-200896 | in compound library |
| Colchicine | Sigma | C9754 | in compound library |
| Concanavalin-A | Calbiochem | 234567 | in compound library |
| Dexamethasone | Sigma | D4902 | in compound library |
| DMEM/F-12 medium | Sigma | D8437 | in JIMT-1 EGFP medium |
| DMSO | Sigma | D2650 | in compound library |
| Etoposide | Sigma | E1383 | E1383 |
| Fetal bovine serum (FBS) | Biosera | FB-1090/500 | JIMT-1 EGFP and NK medium |
| Fisetin | Sigma | F4043 | in compound library |
| Freedom EVO liquid handling robot | TECAN | ||
| Gallotannin | Fluka Chemical Corp. | 16201 | in compound library |
| Glutamine | Gibco | 35,050–061 | in NK medium |
| Harmony software | PerkinElmer | ||
| Humanized anti-HER2 monoclonal antibody (Herzuma) | EGIS Pharmaceuticals, Budapest Hungary | N/A | |
| Humulin R (insulin) | Eli Lilly | HI0219 | JIMT-1 EGFP medium |
| IL-2 | Novartis Hungária Kft. | PHC0026 | in NK medium |
| Isatin | Sigma | 114618 | in compound library |
| MEM Non-essential Amino Acids (MEM-NEAA) | Gibco | 11,140–050 | in NK medium |
| Na-pyruvate | Lonza | BE13-115E | in NK medium |
| Naringenin | Sigma | N5893 | in compound library |
| NQDI-1 | Sigma | SML0185 | in compound library |
| Opera Phenix High-Content Analysis equipment | PerkinElmer | ||
| Penicillin–streptomycin | Biosera | LM-A4118 | JIMT-1 EGFP and NK medium |
| Pentoxyfilline | Sigma | P1784 | in compound library |
| Phosphate buffered saline (PBS) | Lonza | BE17-517Q | to wash the cells |
| Podophyllotoxin | Sigma | P4405 | in compound library |
| Quercetin | Sigma | Q4951 | in compound library |
| Tannic acid | Sigma | T8406 | in compound library |
| Temozolomide | Sigma | T2577 | in compound library |
| Trypan blue 0.4% solution | Sigma | T8154 | for cell counting |
| Vincristine sulfate | Sigma | V0400000 | in compound library |
| α-MEM | Sigma | M8042 | in NK medium |
- Gupta, S. L., Basu, S., Soni, V., Jaiswal, R. K. Immunotherapy: an alternative promising therapeutic approach against cancers. Molecular Biology Reports. 49 (10), 9903-9913 (2022).
- Moretti, A., et al. The past, present, and future of non-viral CAR T cells. Frontiers in Immunology. 13, 867013 (2022).
- June, C. H., O'Connor, R. S., Kawalekar, O. U., Ghassemi, S., Milone, M. C. CAR T cell immunotherapy for human cancer. Science. 359 (6382), 1361-1365 (2018).
- Ross, J. S., et al. The HER-2 receptor and breast cancer: ten years of targeted anti-HER-2 therapy and personalized medicine. Oncologist. 14 (4), 320-368 (2009).
- Shitara, K., et al. Discovery and development of trastuzumab deruxtecan and safety management for patients with HER2-positive gastric cancer. Gastric Cancer. 24 (4), 780-789 (2021).
- Gianni, L., et al. Efficacy and safety of neoadjuvant pertuzumab and trastuzumab in women with locally advanced, inflammatory, or early HER2-positive breast cancer (NeoSphere): a randomised multicentre, open-label, phase 2 trial. Lancet Oncology. 13 (1), 25-32 (2012).
- Barok, M., et al. Trastuzumab causes antibody-dependent cellular cytotoxicity-mediated growth inhibition of submacroscopic JIMT-1 breast cancer xenografts despite intrinsic drug resistance. Molecular and Cancer Therapy. 6 (7), 2065-2072 (2007).
- Gauthier, M., Laroye, C., Bensoussan, D., Boura, C., Decot, V. Natural Killer cells and monoclonal antibodies: Two partners for successful antibody dependent cytotoxicity against tumor cells. Crit Rev Oncol Hematol. 160, 103261 (2021).
- Gruijs, M., Sewnath, C. A. N., van Egmond, M. Therapeutic exploitation of neutrophils to fight cancer. Semin Immunol. 57, 101581 (2021).
- Mando, P., Rivero, S. G., Rizzo, M. M., Pinkasz, M., Levy, E. M. Targeting ADCC: A different approach to HER2 breast cancer in the immunotherapy era. Breast. 60, 15-25 (2021).
- van der Haar Avila, I., Marmol, P., Kiessling, R., Pico de Coana, Y. Evaluating antibody-dependent cell-mediated cytotoxicity by chromium release assay. Methods in Molecular Biology. 1913, 167-179 (2019).
- Broussas, M., Broyer, L., Goetsch, L. Evaluation of antibody-dependent cell cytotoxicity using lactate dehydrogenase (LDH) measurement. Methods in Molecular Biology. 988, 305-317 (2013).
- Toth, G., Szollosi, J., Vereb, G. Quantitating ADCC against adherent cells: Impedance-based detection is superior to release, membrane permeability, or caspase activation assays in resolving antibody dose response. Cytometry A. 91 (10), 1021-1029 (2017).
- Chung, S., Nguyen, V., Lin, Y. L., Kamen, L., Song, A. Thaw-and-use target cells pre-labeled with calcein AM for antibody-dependent cell-mediated cytotoxicity assays. Journal of Immunological Methods. 447, 37-46 (2017).
- Lee-MacAry, A. E., et al. Development of a novel flow cytometric cell-mediated cytotoxicity assay using the fluorophores PKH-26 and TO-PRO-3 iodide. Journal of Immunological Methods. 252 (1-2), 83-92 (2001).
- Tanito, K., et al. Comparative evaluation of natural killer cell-mediated cell killing assay based on the leakage of an endogenous enzyme or a pre-loaded fluorophore. Analytical Science. 37 (11), 1571-1575 (2021).
- Lin, S., Schorpp, K., Rothenaigner, I., Hadian, K. Image-based high-content screening in drug discovery. Drug Discovery Today. 25 (8), 1348-1361 (2020).
- Guti, E., et al. The multitargeted receptor tyrosine kinase inhibitor sunitinib induces resistance of HER2 positive breast cancer cells to trastuzumab-mediated ADCC. Cancer Immunology, Immunotherapy. 71 (9), 2151-2168 (2022).
- Li, F., Liu, S. Focusing on NK cells and ADCC: A promising immunotherapy approach in targeted therapy for HER2-positive breast cancer. Frontiers in Immunology. 13, 1083462 (2022).
- Perussia, B., Loza, M. J. Assays for antibody-dependent cell-mediated cytotoxicity (ADCC) and reverse ADCC (redirected cytotoxicity) in human natural killer cells. Methods in Molecular Biology. 121, 179-192 (2000).
- Garcia-Alonso, S., Ocana, A., Pandiella, A. Trastuzumab emtansine: Mechanisms of action and resistance, clinical progress, and beyond. Trends in Cancer. 6 (2), 130-146 (2020).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved