Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Neuroscience
التجزئة تحت الخلوية لعزل المكونات المتشابكة من دماغ الفئران
يقدم هذا البروتوكول طريقة قوية ومفصلة للحصول على تشابك عصبي عالي النقاء ، وحويصلات متشابكة ، وكسور متشابكة أخرى من دماغ الفأر. تتيح هذه الطريقة تقييم العمليات المشبكية ، بما في ذلك التحليل الكيميائي الحيوي لتوطين البروتين ووظيفته بدقة مجزأة.
المحطات المشبكية هي المواقع الرئيسية للاتصال العصبي. الخلل الوظيفي المشبكي هو السمة المميزة للعديد من الاضطرابات العصبية والنفسية والعصبية. وبالتالي ، فإن توصيف الأجزاء الفرعية المشبكية عن طريق العزل الكيميائي الحيوي هو طريقة قوية لتوضيح القواعد الجزيئية للعمليات المشبكية ، سواء في الصحة أو المرض. يصف هذا البروتوكول عزل المحطات المشبكية والمقصورات الفرعية المشبكية من أدمغة الفئران عن طريق التجزئة تحت الخلوية. أولا ، يتم عزل الهياكل الطرفية المشبكية المختومة ، والمعروفة باسم المشابك العصبية ، بعد تجانس أنسجة المخ. المشبك العصبي عبارة عن مقصورات عصبية قبل وبعد مشبكي مع أغشية مقروصة ومختومة. تحتفظ هذه الهياكل بحالة نشطة أيضيا وهي ذات قيمة لدراسة التركيب والوظيفة المشبكية. ثم تخضع الجيبتوسومات لتحلل منخفض التوتر وطرد مركزي فائق للحصول على مقصورات فرعية متشابكة غنية للحويصلات المشبكية ، والعصارة الخلوية المشبكية ، وغشاء البلازما المشبكي. يتم تأكيد نقاء الكسر عن طريق الفحص المجهري الإلكتروني وتحليل التخصيب الكيميائي الحيوي للبروتينات الخاصة بالمقصورات شبه المشبكية. الطريقة المقدمة هي أداة مباشرة وقيمة لدراسة الخصائص الهيكلية والوظيفية للمشابك والمسببات الجزيئية لاضطرابات الدماغ المختلفة.
نقاط الاشتباك العصبي هي الوحدات الحسابية الأساسية للدماغ التي تتواصل من خلالها الخلايا العصبية وتمارس وظائف متنوعة ومعقدة بشكل رائع. وبالتالي ، فإن نقاط الاشتباك العصبي أساسية لصحة الدماغ1 ؛ الخلل الوظيفي المشبكي متورط كمصدر أو نتيجة للعديد من الاضطرابات2. تتكون نقاط الاشتباك العصبي من أطراف قبل وبعد المشبكي ، وهي امتدادات لخليتين عصبيتين مختلفتين يتم وضعهما بشكل وثيق وفصلهما عن طريق شق متشابك تجتازه جزيئات الالتصاق المشبكية. تتدفق المعلومات من حجرة ما قبل المشبكي إلى ما بعده في شكل رسل كيميائي يسمى الناقلات العصبية1. العمليات الجزيئية المشاركة في النقل العصبي هي مجالات نشطة للبحث3،4،5. يعد فهم العمليات المسببة للأمراض داخل المحطات المشبكية واستجابة نقاط الاشتباك العصبي للأمراض في المقصورات الفرعية العصبية الأخرى خطوات حاسمة لمعالجة اضطرابات الدماغ 1,2. العديد من التطورات المنهجية ، المطبقة في الغالب على نماذج الفئران ، قد عززت هذا السعي6. إن عزل الكسور المشبكية عن طريق الطرد المركزي التفاضلي هو أحد طرق تغيير النموذج التي مكنت من التقييم التفصيلي للعمليات المشبكية في الصحة والمرض.
يتكون الدماغ البشري البالغ من 80-90 مليار خلية عصبية 7,8. من بين أنواع الفئران ، يحتوي دماغ الفئران على ما يقرب من ~ 200 مليون خلية عصبية ، بينما تحتوي الفئران على ~ 70 مليون 9,10. تشكل كل خلية عصبية الآلاف من الوصلات المشبكية المحددة مع شبكة من الخلايا العصبية شديدة الاستقطاب المخلوطة بالخلايا الدبقية والأوعية الدموية الكثيفة. في مثل هذه الأنسجة المعقدة وغير المتجانسة ، كان من غير المعقول عزل ودراسة نقاط الاشتباك العصبي كنظام مستقل. في 1960s ، جعل فيكتور ويتاكر ، كاثرين هيب ، وآخرون هذا ممكنا عن طريق عزل المحطات المشبكية السليمة باستخدام التجزئة تحت الخلوية11،12،13،14. في محاولة لعزل الحويصلات المشبكية (SVs) ، قاموا بتجانس الأدمغة من خلال قوة القص السائل في السكروز متساوي التناضح (0.32 M) متبوعا بالطرد المركزي الفائق. لقد حصلوا على أطراف عصبية أو دوالي مقروصة أو مغلقة بغشاء البلازما ، والتي أطلقوا عليها اسم الجسيمات العصبية (NEPs)11,13. نظرا للحفاظ على الخصائص الهيكلية والوظيفية للمشبك في هذه الهياكل ، فقد أطلق على NEPs لاحقا اسم "synaptosomes" للتطابق مع العضيات تحت الخلوية الأخرى13,15. تجدر الإشارة إلى أن عمل إدواردو دي روبرتيس وزملائه ، الذين صاغوا مصطلح "الحويصلة المشبكية" ، تداخل مع عمل ويتاكر وزملائه وساهم في التحقق من صحة عزل وتوصيف "المشبك"16،17،18.
Synaptosomes هي هياكل نشطة من الناحية الفسيولوجية تحتوي على جميع الخصائص الخلوية والجزيئية اللازمة لتخزين وإطلاق وإعادة امتصاص الناقلات العصبية13,18. يساهم الحفاظ على الخصائص المشبكية الرئيسية في المختبر والتحرر من المكونات غير المشبكية أيضا في فائدة طريقة العزل هذه. ساهمت السينابتوسومات بشكل كبير في فهم الخصائص الكيميائية والفسيولوجية للنقل العصبي ويتم استخدامها الآن لدراسة العمليات الجزيئية المشبكية وتغييراتها في المرض19،20،21،22،23. Synaptosomes هي أيضا مادة المصدر الأولية لعزل المكونات المشبكية مثل SVs ، والحويصلات المغلفة بالكلثرين (CCVs) ، والعصارة الخلوية المشبكية ، وغشاء البلازما المشبكي ، والميتوكوندريا المشبكية ، وجزيئات الالتصاق المشبكي ، والمكونات الأخرى ذات الأهمية ، والتي يمكن أن تسهل فهم الآليات الجزيئية للوظيفة المشبكية18،19،20،24،25،26 ، 27,28. يمكن الحصول على هذه المكونات شبه المشبكية عن طريق التحلل التناضحي للتشابك العصبي والطرد المركزي الفائق المتدرجلكثافة السكروز 15,29. على الرغم من أن طريقة التجزئة تحت الخلوية الأصلية من قبل مجموعة أبحاث ويتاكر معروفة بأنها فعالة في عزل المشبك العصبي عالي الجودة و SVs13،30 ، إلا أن التحسينات الحديثة تعزز نقاء الكسور تحت الخلوية 22،23،31،32. توفر هذه المقالة نسخة مفصلة للغاية ويمكن الوصول إليها من بروتوكول كلاسيكي للتجزئة تحت الخلوية لأنسجة دماغ الفئران لعزل التشابك العصبي و SVs والمكونات شبه المشبكية الأخرى.
تمت الموافقة على جميع التجارب على الفئران من قبل اللجنة المؤسسية لرعاية واستخدام الحيوان (IACUC) في جامعة ييل (بروتوكول 2021-11117) وتم إجراؤها في منشأة معتمدة من قبل جمعية تقييم واعتماد المنظمة الدولية لرعاية المختبر (AAALAC). امتثلت رعاية الحيوانات والإسكان لدليل رعاية واستخدام المختبر33 وتم توفيرها من قبل مركز موارد الحيوانات بجامعة ييل (YARC). تم الحفاظ على الحيوانات في دورة الضوء / الظلام لمدة 12 ساعة مع وصول مخصص إلى الطعام والماء. مطلوب خمسة إلى ثمانية فئران أو اثنين إلى أربعة فئران لكل نمط وراثي أو حالة للبروتوكول التالي. عدد أقل من الفئران ضروري بسبب أحجام الدماغ الأكبر. وبالمثل ، قد يؤثر عمر التجارب على محصول الكسور. قد تكون هناك حاجة الفئران إضافية للأعمار أقل من 2 أشهر. خلاف ذلك ، تنطبق الإجراءات المحددة على كل من أنواع الفئران والحيوانات البالغة السليمة من أي عمر. استخدمت البيانات التمثيلية المقدمة في هذه الدراسة الفئران من النوع البري (C57BL / 6J) (العمر = 2 أشهر ؛ أربعة ذكور وأربع إناث لكل نسخة متماثلة) تم الحصول عليها من مصدر تجاري (انظر جدول المواد).
1. التحضير التجريبي
ملاحظة: يتطلب هذا البروتوكول ~ 11 ساعة لباحث واحد لإكماله. يوصى بشدة بإكمال إعداد الطاولة (الشكل 1) ، وإعداد المخزن المؤقت (الجدول 1) ، والتبريد المسبق لأجهزة الطرد المركزي والدوارات إلى 4 درجات مئوية ، وجمع المواد والمعدات اللازمة ووضع العلامات عليها (انظر جدول المواد) في اليوم السابق لتنفيذ البروتوكول ، عند الاقتضاء.
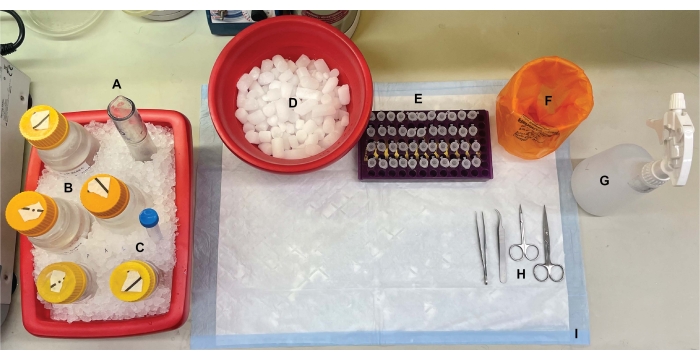
الشكل 1: إعداد الطاولة قبل تشريح الدماغ ، (أ) المجانسات الزجاجية Dounce و (ب) تم تبريد جميع المخازن المؤقتة على الجليد. (ج) إذابة محاليل مخزون مثبطات الأنزيم البروتيني على الجليد. تم الحصول على حاوية ثانية من الثلج الرطب لأنابيب الطرد المركزي ، وديوار من النيتروجين السائل (غير معروض) ، و (د) حاوية من الثلج الجاف للتخزين قصير الأجل للعينات المجمدة في النيتروجين السائل. (ه) تم وضع علامات مسبقة على أنابيب الطرد المركزي الدقيقة لجميع العينات ، حيث تم جمع أربعة حصص من كل عينة جزء تحت خلوي لكل نمط وراثي أو حالة أثناء هذا الإجراء (نصيحة موفرة للوقت: قم بتسمية جميع الأنابيب بدقة في اليوم السابق لإجراء التجربة). (و) حاوية نفايات بيولوجية مناسبة ، (ز) 70٪ إيثانول ، (ح) أدوات جراحية ، و (ط) وسادة سطحية ماصة. تم وضع أنابيب الطرد المركزي والمستهلكات المطلوبة جانبا للوصول الفعال أثناء تنفيذ البروتوكول (غير معروض). الرجاء الضغط هنا لعرض نسخة أكبر من هذا الشكل.
- جهز سطح الطاولة للجراحة واجمع المقص والملقط اللازمين لاستئصال الدماغ (انظر جدول المواد). أنابيب الطرد المركزي الدقيقة 1.5 مل قبل التسمية لخزعات ذيل الفأر وأربعة أنابيب لكل جزء تم جمعه ، كما هو موضح في الشكل 2.
- احصل على حاويتين من الثلج الرطب ، وحاوية واحدة من الثلج الجاف ، وقارورة ديوار النيتروجين السائل الموضوعة على الطاولة.
- إذابة فلوريد فينيل ميثيل سلفونيل (PMSF) ، وبيبستاتين أ ، وأبروتينين ، ومحلول مخزون الليوببتين على الجليد (انظر جدول المواد). قم بإعداد المخازن المؤقتة اللازمة (الجدول 1).
ملاحظة: يمكن تحضير محاليل السكروز مسبقا وتخزينها عند 4 درجات مئوية. ومع ذلك ، يجب إضافة مثبطات الأنزيم البروتيني (المخزونات والأقراص المذابة) طازجة إلى جميع المخازن المؤقتة في بداية التجربة بسبب عدم استقرار هذه الكواشف في المحاليل المائية. علاوة على ذلك ، يجب تحضير جميع المخازن المؤقتة بأواني زجاجية خالية من المنظفات ومياه خالية من المنظفات لتمكين جمع التشابك السليم. - قم بتبريد جميع المخازن المؤقتة والزجاج خالطات Dounce (انظر جدول المواد) على الثلج. اضبط أجهزة الطرد المركزي على 4 درجات مئوية وقم بتبريد الدوارات إلى 4 درجات مئوية.
- أضف 14 مل من المخزن المؤقت A (الجدول 1) إلى خالط Dounce على الجليد.
الجدول 1: تكوين مخازن التجزئة تحت الخلوية. الرجاء الضغط هنا لتحميل هذا الجدول.
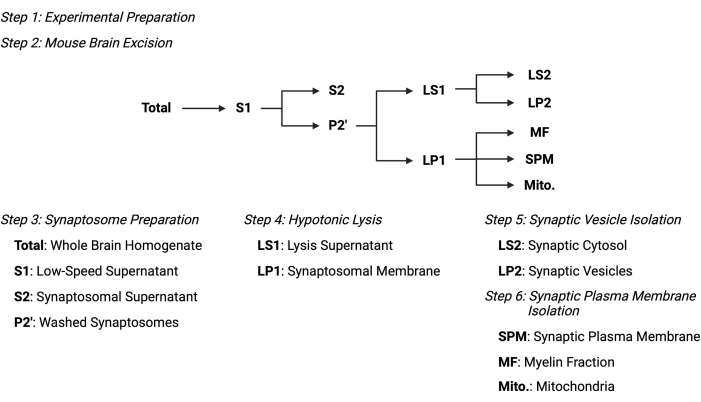
الشكل 2: نظرة عامة على بروتوكول التجزئة تحت الخلوية. ملخص تخطيطي لخطوات التجزئة تحت الخلوية والعينات التي تم جمعها. الرجاء الضغط هنا لعرض نسخة أكبر من هذا الشكل.
2. استئصال دماغ الفأر
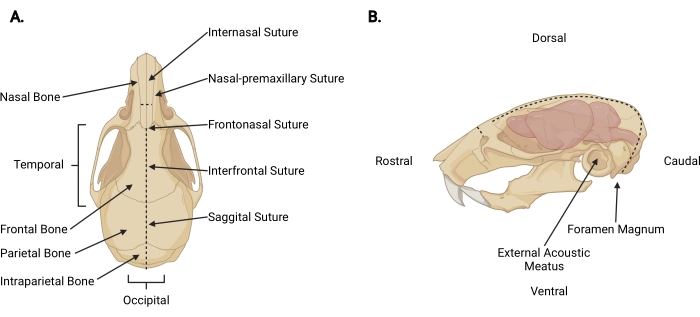
الشكل 3: التشريح القحفي الوجهي . (أ) منظر ظهري لجمجمة فأر مع الإشارة إلى التراكيب القحفية ذات الصلة. (ب) منظر جانبي يسار لجمجمة فأر ودماغه مع الإشارة إلى التراكيب القحفية ذات الصلة والاتجاهات التشريحية. تمثل الخطوط المتقطعة المواقع التي يجب إجراء الشقوق فيها. الرجاء الضغط هنا لعرض نسخة أكبر من هذا الشكل.
- تخدير عميق لكل فأر بنسبة 100٪ إيزوفلوران في غرفة التخدير الموجودة في غطاء الدخان أو خزانة السلامة الحيوية باستخدام طريقة الإسقاط المفتوح34. التضحية بكل فأر عن طريق خلع العمود الفقري العنقي تليها بسرعة قطع الرأس. قم بالتناوب بين الأنماط الجينية أو المجموعات التجريبية لكل ذبيحة وتشريح12. الحصول على خزعات الذيل بعد القتل الرحيم عن طريق استئصال 2 مم من طرف الذيل البعيد بمقص دقيق. تخزين الأنسجة للتنميط الجيني.
- رش الرأس مقطوع الرأس بنسبة 70٪ من الإيثانول لمنع الشعر من الالتصاق بالأنسجة والأدوات الجراحية أثناء التشريح.
- أدخل مقصا دقيقا تحت الجلد عند شق قطع الرأس إلى عمق حول الجمجمة وقم بعمل شق منتصف السهمي حتى الخيط الأنفي (الشكل 3 أ) لسحب فروة الرأس من الجمجمة.
- من خلال العمل من المنطقة القذالية باتجاه كل جانب صدغي ، قم بقص اللفافة والعضلات لكشف السطح الخارجي للجمجمة خارج كل صماخ صوتي خارجي (الشكل 3 ب).
- تأمين فروة الرأس والجانب المنبر من الجمجمة مع اليد غير المهيمنة. مع الآخر ، أدخل مقصا ناعما 2 مم في الجانب الذيلي من الثقبة العظمى ، حيث يمكن رؤية الحبل الشوكي للخروج. قم بعمل شق في خط الوسط حتى يصل المقص إلى السطح الداخلي للعظم داخل الجداري (الشكل 3 ؛ خطوط متقطعة).
ملاحظة: أثناء الشق الأولي ، يجب أن يكون المقص موازيا للحبل الشوكي مع الضغط على السطح الداخلي للجمجمة لمنع تلف جذع الدماغ والمخيخ. - قم بتغيير زاوية المقص بحيث تعمل الشفرات بالتوازي مع السطح الظهري للجمجمة. استمر في تقدم شق منتصف السهمي بشكل دائري عبر العظام الجدارية والأمامية ، باستخدام الغرز السهمية والجبهية كدليل. استخدم ضغطا تصاعديا ثابتا لتجنب تلف القشرة. قم بإنهاء الشق خارج الخيط الأنفي مباشرة (الشكل 3 أ).
- قم بعمل شق عمودي صغير (~ 3 مم) على عظم الأنف ، منبر على الخيط الأنفي ، عن طريق وضع المقص بشكل عمودي على الجمجمة مع وضع كل شفرة في خياطة الأنف قبل الفك العلوي وجعل واحدة حتى قطع (الشكل 3 ؛ خطوط متقطعة).
ملاحظة: ستزيد هذه الخطوة من سهولة سحب الجمجمة وستكون حاسمة لجمع البصلة الشمية إذا كانت هذه المنطقة ذات أهمية. - أثناء تأمين الجانب المنقاري ، استخدم جانبا واحدا من زوج من الملقط المحكم لرفع الجمجمة برفق من الدماغ ، ثم أفقيا وبطنيا. كرر على طول خط الوسط حسب الحاجة ، ثم لنصف الكرة الآخر حتى ينكشف سطح الدماغ بالكامل.
- باستخدام ملقط منحني أو ملعقة دقيقة ، ارفع الجانب المنبر من الدماغ برفق. قطع الأعصاب البصرية والقحفية لإكمال الاستئصال من الجمجمة.
- لكل حالة ، اجمع خمسة إلى ثمانية أدمغة فأر معا في خالط Dounce الزجاجي المبرد الذي يحتوي على 14 مل من المخزن المؤقت A (الجدول 1).
3. إعداد المشبك
ملاحظة: يتم عرض مخططات هذا الإجراء في الشكل 4.
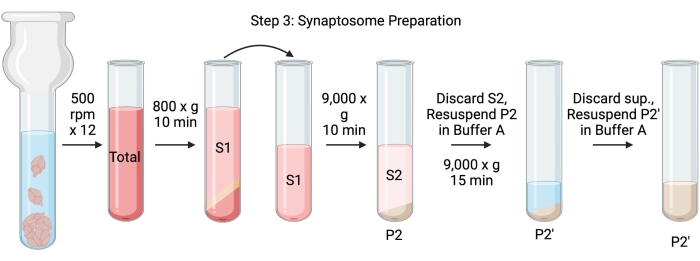
الشكل 4: تحضير التشابك العصبي. رسم تخطيطي للخطوة 3 ، توليد المشابك العصبية (P2 '). الرجاء الضغط هنا لعرض نسخة أكبر من هذا الشكل.
- تجانس العقول باستخدام خالط Dounce الزجاجي في 12 تمريرة من أعلى إلى أسفل عند 500 دورة في الدقيقة (إجمالي). توقف لفترة وجيزة عند كل ضربة لأسفل لضمان التجانس الشامل للأنسجة. تجانس بشكل تفضيلي في حمام جليدي لتجنب الاحترار وتمسخ البروتين. خذ 5 ميكرولتر من القسمة لتحديد تركيز البروتين عن طريق مقايسة حمض البيسينتشونينيك (BCA ، انظر جدول المواد). خذ 100 ميكرولتر من حصص المحللة للدماغ بالكامل لللطخة الغربية (WB). لهذه العينة وجميع العينات اللاحقة (الشكل 2) ، خذ قسمتين ل BCA واثنين من القسمة ل WB. قم بتجميد جميع الحصص المجمعة في النيتروجين السائل وتخزينها عند -80 درجة مئوية.
- قم بتدوير تجانس الدماغ الكلي في أنبوب طرد مركزي دائري القاع عالي السرعة (14 مل) (انظر جدول المواد) عند 800 × جم لمدة 10 دقائق عند 4 درجات مئوية للحصول على المادة الطافية (S1). انقل S1 إلى أنبوب طرد مركزي جديد ، تاركا الحبيبات وراءه (P1) ، والتي تحتوي على خلايا ونوى سليمة. تجنب سحب الحبيبات الرقيقة والبيضاء والسائبة والسطحية. خذ 2 × 5 ميكرولتر من S1 ل BCA و 2 × 100 ميكرولتر من S1 ل WB.
- قم بتدوير S1 عند 9000 × جم لمدة 15 دقيقة عند 4 درجات مئوية للحصول على الطاف المشبكي (S2) وحبيبات المشبكي الخام (P2). خذ 2 × 10 ميكرولتر من S2 ل BCA و 2 × 500 ميكرولتر من S2 ل WB. تخلص من المادة الطافية بعد الحصول على القسمة وانتقل إلى الخطوة التالية مع الحبيبات.
- أعد تعليق P2 في 3 مل من المخزن المؤقت A المثلج البارد مع مثبطات الأنزيم البروتيني وأجهزة الطرد المركزي عند 9000 × جم لمدة 15 دقيقة عند 4 درجات مئوية للحصول على المادة الطافية (S2 ') والمشابك المغسولة (P2'). تخلص من المادة الطافية واحتفظ بالحبيبات.
- أعد تعليق P2 'في 3 مل من المخزن المؤقت A. تجنب إعادة تعليق الجزء الأحمر الداكن في الجزء السفلي من الحبيبات ، والذي يحتوي بشكل أساسي على الميتوكوندريا. خذ 2 × 20 ميكرولتر من P2 'ل BCA و 2 × 100 ميكرولتر من P2 'ل WB.
ملاحظة: يمكن تحقيق ذلك عن طريق خلط حواف وسطح الحبيبات برفق لإعادة تعليق المشابك البيضاء المغسولة أثناء توجيه طرف الماصة بعيدا عن المركز الأحمر للحبيبة.
4. تحلل منخفض التوتر
ملاحظة: تظهر مخططات هذا الإجراء في الشكل 5.
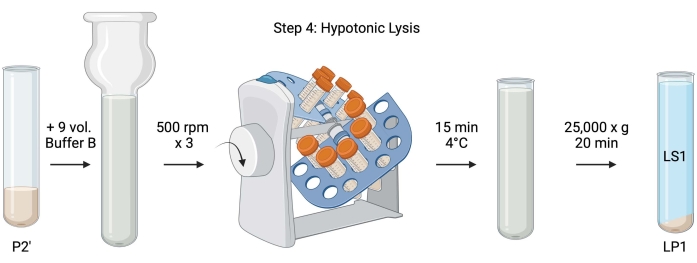
الشكل 5: تحلل منخفض القدر. رسم تخطيطي للخطوة 4 ، التحلل منخفض التوتر للسينابتوسومات لتوليد طاف التحلل (LS1) وكسور الغشاء المشبكي (LP1). الرجاء الضغط هنا لعرض نسخة أكبر من هذا الشكل.
- بالنسبة للتحلل منخفض التوتر للجينات المشبكة المغسولة ، أضف 9 مجلدات من المخزن المؤقت B المبرد (الجدول 1) لإعادة تعليق P2 '(~ 27 مل). تجانس المشابك في خالط Dounce زجاجي (ثلاثة ممرات من أعلى إلى أسفل عند 500 دورة في الدقيقة).
- نقل العينات إلى أنابيب الطرد المركزي المخروطية المغطاة 50 مل. قم بتدويرها على مسدس أنبوبي في غرفة باردة بدرجة حرارة 4 درجات مئوية لمدة 15 دقيقة.
- تحلل جهاز الطرد المركزي P2 'عند 25000 × جم لمدة 20 دقيقة عند 4 درجات مئوية للحصول على طاف التحلل (LS1) وحبيبات التحلل التي تحتوي على أغشية متشابكة (LP1). خذ 2 × 50 ميكرولتر من LS1 ل BCA و 2 × 400 ميكرولتر من LS1 ل WB. انقل LS1 إلى أنبوب طرد مركزي مغطى للطرد المركزي الفائق (انظر جدول المواد).
5. عزل الحويصلة المشبكية
ملاحظة: يتم عرض مخططات هذا الإجراء في الشكل 6.
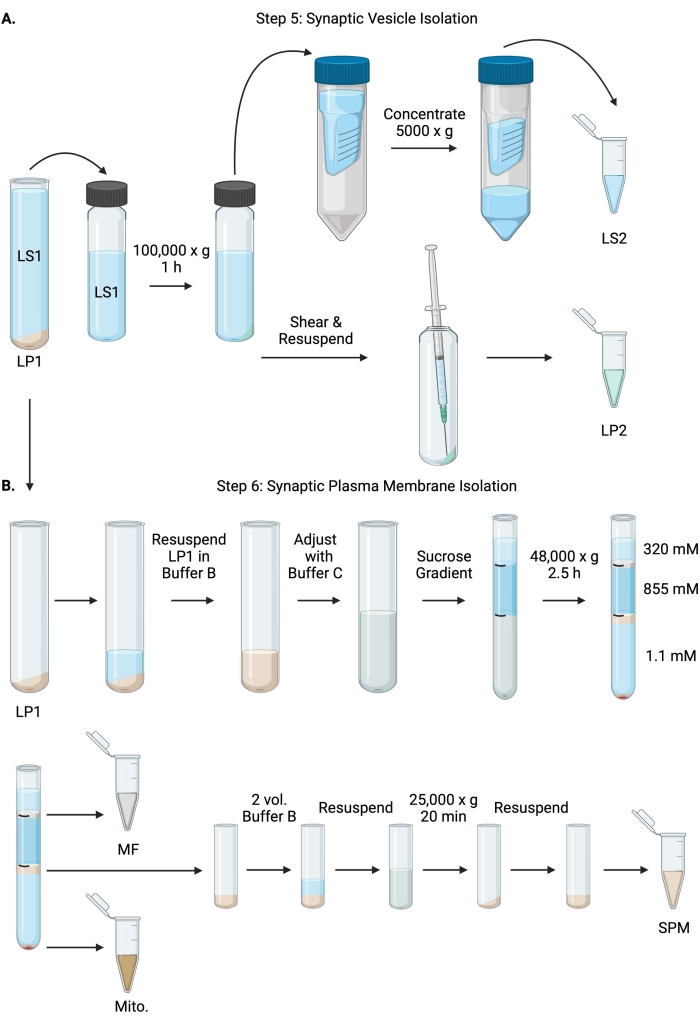
الشكل 6: عزل الحويصلة المشبكية وعزل غشاء البلازما المشبكي. (أ) رسم تخطيطي للخطوة 5، عزل السيتوسول المشبكي (LS2) وكسور الحويصلة المشبكية (LP2)، و(ب) الخطوة 6، توليد المايلين (MF)، وغشاء البلازما المشبكي (SPM)، وكسور الميتوكوندريا (ميتو) بعد الطرد المركزي الفائق لتدرجات السكروز. الرجاء الضغط هنا لعرض نسخة أكبر من هذا الشكل.
- جهاز طرد مركزي LS1 في دوار طرد مركزي فائق الزاوية ثابت (انظر جدول المواد) عند 100000 × جم لمدة 60 دقيقة عند 4 درجات مئوية للحصول على طاف السيتوسول المشبكي (LS2) وحبيبات الحويصلة المشبكية (LP2). سيكون LP2 صغيرا وشفافا ويلتصق بقوة بجانب أنبوب الطرد المركزي.
- أعد تعليق LP2 في 500 ميكرولتر من المخزن المؤقت A. باستخدام إبرة 23 جم وحقنة 1 مل ، قص LP2 مع تثليث لطيف. خذ 2 × 10 ميكرولتر من LP2 ل BCA و 2 × 250 ميكرولتر من LP2 ل WB.
- نقل LS2 (~ 30 مل) إلى وحدات تصفية الطرد المركزي مع قطع 10 كيلو دالتون (انظر جدول المواد).
ملاحظة: إذا كانت البروتينات الأصغر من 10 كيلو دالتون ذات أهمية ، تتوفر وحدات مرشح طرد مركزي مقطوعة 4 كيلو دالتون ولكنها ستؤدي إلى أوقات دوران أطول. - ركز LS2 على حوالي 0.5 مل عن طريق الدوران عند 5000 × جم لمدة تصل إلى 1 ساعة عند 4 درجات مئوية. خذ 2 × 10 ميكرولتر من LS2 المركز ل BCA و 2 × 250 ميكرولتر من LS2 المركز ل WB. بعد بدء الدوران ، انتقل مباشرة إلى الخطوة 6.1.
6. عزل غشاء البلازما المشبكي
- أعد تعليق LP1 (الخطوة 4.3) في 1 مل من المخزن المؤقت B (الجدول 1). خذ 2 × 10 ميكرولتر من LP1 ل BCA و 2 × 50 ميكرولتر من LP1 ل WB. اضبط LP1 المتبقي على حجم نهائي يبلغ 7.5 مل وتركيز سكروز نهائي يبلغ 1.1 M مع المخزن المؤقت B والمخزن المؤقت C (الجدول 1).
- انقل 7.5 مل من LP1 المعاد تعليقه إلى أنبوب طرد مركزي فائق سعة 14 مل (انظر جدول المواد). تراكب LP1 بعناية مع 3.75 مل من المخزن المؤقت D (الجدول 1) ، ثم تراكب مع 1.25 مل من المخزن المؤقت A (أو حجم أكبر لملء أسفل الجزء العلوي مباشرة من أنبوب الطرد المركزي). تجنب السحب على جانب الأنبوب ، مما يؤدي إلى تعطيل واجهات تدرج السكروز. بعد تراكب كل جزء من السكروز ، ضع علامة على الجزء العلوي من المحلول بقلم. قم بموازنة أنابيب الطرد المركزي الفائق بالوزن وليس الحجم ، مع إضافة Buffer A بالتنقيط إلى حدود 10 مجم. جهاز طرد مركزي عند 48000 × جم لمدة 2.5 ساعة عند 4 درجات مئوية في دلو متأرجح دوار فائق الطرد المركزي (انظر جدول المواد).
- الحصول على صور للتدرجات السليمة بعد الطرد المركزي الفائق لتوثيق تميز كل واجهة سكروز ونجاح التجزئة.
- قم بإزالة الطبقة السطحية من السكروز 320 ملي مول بعناية (المخزن المؤقت أ). استرجع جزء المايلين (MF) عند واجهة السكروز 320 mM / 855 mM في حجم 800 ميكرولتر. استرجع جزء غشاء البلازما المشبكي (SPM) عند واجهة السكروز 855 mM / 1.1 M في حجم 1000 ميكرولتر. ماصة كل جزء لأعلى من جدار الأنبوب بطريقة دائرية لضمان جمع الكسر الكامل. استنشاق بعناية من السكروز المتبقي واستعادة حبيبات الميتوكوندريا (ميتو.) عن طريق تعليق 200 ميكرولتر من المخزن المؤقت ب. خذ 2 × 100 ميكرولتر من MF ل BCA و 2 × 10 ميكرولتر من Mito. ل BCA ؛ قسم ما تبقى من MF وميتو. عينات في النصف ل WB.
- قم بتخفيف جزء SPM بمجلدين من المخزن المؤقت B (~ 2 مل) ، ثم قم بالطرد المركزي في دوار بزاوية ثابتة في أنبوب طرد مركزي سعة 3.5 مل (انظر جدول المواد) عند 25000 × جم لمدة 20 دقيقة عند 4 درجات مئوية. تخلص من المادة الطافية وأعد تعليق حبيبات SPM في المخزن المؤقت A للحصول على حجم نهائي يبلغ 250 ميكرولتر. خذ 2 × 5 ميكرولتر من SPM ل BCA وقسم SPM المتبقي إلى نصفين ل WB.
- قم بإجراء BCA لتحديد تركيز البروتين لكل عينة ، مع مراعاة حجم القسمة المتغير.
ملاحظة: بالنسبة لتحليل WB ، فإن تركيز البروتين العامل المقترح لجميع الكسور تحت الخلوية هو 2 ميكروغرام / ميكرولتر (أو أعلى ما يمكن تحقيقه ل LS1 و MF).
ينتج عن الطريقة المقدمة 11 كسرا تحت خلوي في الدماغ يمكن إخضاعها لمزيد من التنقية وأشكال مختلفة من التحليل النهائي35,36. الطريقة القياسية الذهبية لتقييم جودة التشابك العصبي ، SVs23 ، والمكونات الأخرى هي المجهر الإلكتروني (EM) (الشكل 7). يمكن أيضا إجراء النشاف المناعي الكمي للبروتينات الموجودة في كسور تحت خلوية محددة لتقييم علامات نقاء الكسر (الشكل 8). على سبيل المثال ، يكشف تحليل اللطخة المناعية للكسور عن إثراء N-cadherin (CDH2 ، اسم UniProt) في جزء غشاء البلازما المشبكي (SPM) ، α-synuclein (SYUA) في السيتوسول المشبكي (LS2) ، المشبك العصبي (SYPH) في جزء الحويصلة المشبكية (LP2) ، وبروتين المايلين الأساسي (MBP) في جزء المايلين (MF) عند مقارنته بمستويات البروتين في تجانس الدماغ الكامل الأولي (الإجمالي) (الشكل 8 ). بمجرد تحديد نقاء الكسر (على سبيل المثال ، لاحظ عدم وجود CDH2 في جزء LS2 أو الزيادة متعددة الأضعاف في SYPH في جزء LP2) ، يمكن استخدام النشاف المناعي الكمي لتحديد توطين البروتينات ذات الأهمية أو اختلافات الاستعلام في توزيع البروتين بين الأنماط الجينية أو العلاجات. يمكن أن يؤدي فهم التوطين تحت الخلوي للبروتينات المشبكية إلى تمكين تشريح وظائف البروتين غير الموصوفة سابقا. علاوة على ذلك ، قد توضح هذه الطريقة عيوب الاتجار أو الخلل الوظيفي المشبكي في حالات المرض ، خاصة عند إقرانها بالمقايسات الوظيفية. على سبيل المثال ، استخدم فريقنا هذه الطريقة لتحديد مجموعة من بروتين بالميتويل النشط إنزيميا ثيوستيراز 1 المخصب في السيتوسول19 المشبكي.
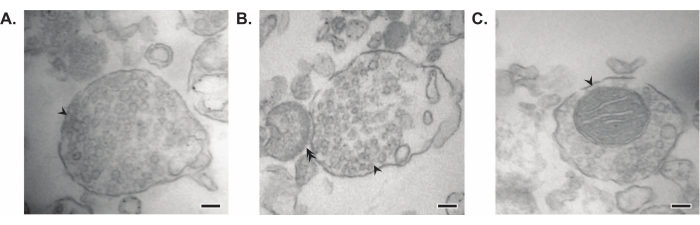
الشكل 7: المجهر الإلكتروني (EM) للتشابك العصبي. (أ) صورة EM تمثيلية لإنزيم متشابك يحتوي على حويصلات متشابكة (سهم). (ب) صورة EM تمثيلية لمتشابك مع كل من مكونات ما قبل (السهم) وما بعد المشبكي (السهم المزدوج). (ج) صورة EM تمثيلية لمركب يحتوي على حويصلات متشابكة وميتوكوندريون (سهم) (قضبان المقياس = 100 نانومتر). الرجاء الضغط هنا لعرض نسخة أكبر من هذا الشكل.
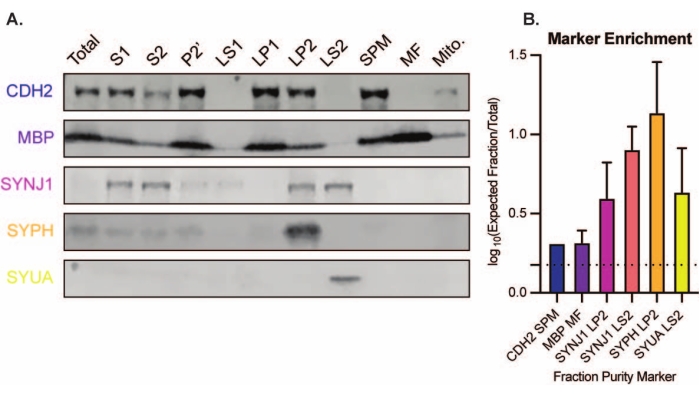
الشكل 8: تحليل اللطخة المناعية للكسور تحت الخلوية. (أ) علامات نقاء الكسر تحت الخلوي (المشار إليها بتسمية UniProt) موضعية بشكل مناسب مقارنة بتجانس الدماغ بالكامل (الإجمالي): N-cadherin (CDH2) في جزء غشاء البلازما المشبكي (SPM) ، synaptophysin 1 (SYPH) و synaptojanin 1 (SYNJ1) في الجزء المخصب للحويصلة المشبكية (LP2) ، α-synuclein (SYUA) في السيتوسول المشبكي (LS2) ، وبروتين المايلين الأساسي (MBP) في جزء المايلين (MF). (ب) يكشف التحليل الكمي للبقع المناعية عن إثراء (تغيير الطي من الكلي) لعلامات نقاء الكسر. يتم تمثيل البيانات كمتوسط ± الانحراف المعياري على مقياس log10. يشير الخط المنقط إلى تغيير بمقدار 1.5 ضعف (y = 0.176) (n = 3 تجارب مكررة مع 8 فئران من النوع البري ؛ العمر = شهرين ؛ n = 4-5 بقع ل SYPH ، SYUA ، MBP ، مع n = 3 قيم مرسومة تم نشرها مسبقا بواسطة Gorenberg et al.19 ؛ n = 5 ل SYNJ1 ؛ n = 1 ل CDH2). الرجاء الضغط هنا لعرض نسخة أكبر من هذا الشكل.
في دراساتهم الأساسية ، استخدم ويتاكر وزملاؤه أربعة معايير مورفولوجية لتحديد المشابك العصبية: (1) الهياكل لها غشاء بلازما مختوم. (2) تحتوي الهياكل على SVs تشبه تلك الموجودة في النهايات العصبية والدوالي في الموقع من حيث الحجم والعدد ؛ (3) تحتوي الهياكل على واحد أو أكثر من الميتوكوندريا الصغيرة ؛ و (4) غالبا ما يتم الالتزام بالغشاء قبل المشبكي بمكون ما بعد المشبكي11،12،13. على الرغم من أن المعيارين الأولين ينطبقان بشكل عام على كل طريقة عزل ، في أحدث البروتوكولات الموضحة في هذه المقالة ، لن تحتوي جميع التفاعلات الناتجة على الميتوكوندريا ومحطات ما بعد المشبكية المرفقة. ما يقرب من 60 ٪ من المشابك سيكون لها الميتوكوندريا ، ويقدر أن ما يصل إلى 15 ٪ فقط قد تعلق محطات ما بعد المشبكي37. إذا كانت مكونات ما بعد المشبكي ذات أهمية خاصة ، فمن المعروف أن استخدام مخزن التجانس الشبيه ب Krebs متساوي التوتر وترشيح الضغط للتخصيب ينتج تركيزات عالية من synaptosomes مع أطراف ما بعد المشبكي (تسمى أيضا synaptoneurosomes)22،38.
يمكن أن تؤثر طريقة التضحية بالحيوان على جودة التشابك العصبي والجزئيات المشبكية. الحيوانات البالغة التي يتم التضحية بها باستخدام طريقة القتل الرحيم التي لا تتطلب التخدير ستؤدي إلى أفضل جودة للكسر. علاوة على ذلك ، يجب تشريح الأدمغة حديثا ، وليس تجميدها ، وتجانسها باستخدام نسبة 1:10 من مخزن التجانس (الوزن / الحجم) للكسور المشبكية الأكثر قابلية للحياة22. يحتوي الدماغ على مجموعة غير متجانسة من نقاط الاشتباك العصبي التي يمكن تمييزها حسب نوع الناقلات العصبية التي تحملها. لا يتأثر تكوين المشبك بشكل عام بنوع المشبك العصبي أو محتوى الناقل العصبي13. الاستثناء هو الألياف المطحونة في المخيخ ، والتي من المعروف أنها تتعطل في الظروف المثلى للحصول على المشابك العصبية من بقية الدماغ39,40. وبالتالي ، يوصى بإزالة المخيخ قبل تجانس الدماغ إذا كان استبعاد هذه المنطقة لا يؤثر على الهدف التجريبي. إذا كنت مهتما بعزل التشابك العصبي لشخصية ناقل عصبي معين ، فيمكن أولا عزل مناطق الدماغ المخصب للخلايا العصبية التي تحتوي على الناقل العصبي محل الاهتمام. ومع ذلك ، فإن هذا النهج سيفرض قيودا على عائد الكسر النهائي ، اعتمادا على حجم المنطقة محل الاهتمام (وبالتالي ، فإن عمر الحيوانات هو أيضا اعتبار). هناك طرق مناعية لعزل المشابك العصبية الخاصة بالناقل العصبي ، ولكن سيتم اختراق الجدوى والعائد بشكل كبير22. إذا كان تقييم الجدوى الأيضية للمتشابكة أمرا مهما ، فيمكن استخدام قياس إطلاق الناقل العصبي 41,42 أو بعض المقايسات الأنزيمية43.
تشمل الملوثات الشائعة في مستحضرات المشبك الميكروسومات والميتوكوندريا الحرة و SVs والأغشية العصبية والدبقية. يمكن تقليل التلوث عن طريق زيادة عدد عمليات الغسيل في الكسور P1 و P222 وتجنب إعادة تعليق حبيبات الميتوكوندريا الحمراء في الخطوات اللاحقة. في التجارب التي تكون فيها قابلية التمثيل الغذائي والوقت أمرا بالغ الأهمية ، فإن تقليل عدد عمليات الغسل واستخدام تدرجات Ficoll أو Percoll على تدرجات السكروز سيكون مفيدا44،45،46. هذه الطرق أيضا تقلل التلوث بشكل كبير. أسفر بروتوكول ويتاكر الأصلي عن SVs عالية الجودة. مزيد من التحسين بواسطة Nagy et al.23 ، المتضمن في هذه الطريقة ، ينتج SVs بتجانس ونقاء ملحوظين دون المساومة بشكل كبير على المحصول36. إذا كانت أنواع فرعية معينة من SV ذات أهمية ، مثل الجلوتاماترجيك (المحتوي على VGLUT-1) أو GABAergic (المحتوية على VGAT-1) SVs ، فيمكن إجراء العزل المناعي باستخدام أجسام مضادة محددة47,48. تتوفر أيضا طرق بديلة لعزل CCVs عن التشابك العصبي ، والتي ، بسبب الكثافة التفاضلية ، قد لا تكون موجودة في نفس الواجهة مثل SVs التي تم الحصول عليها بهذه الطريقة20،49،50.
بشكل عام ، يمكن تحسين البروتوكول الحالي لعزل المكونات المشبكية للحصول على كسور ذات تجانس وقابلية أفضل بناء على جودة وكمية أنسجة المخ المصدر والأهداف التجريبية. لمزيد من تفاصيل استكشاف الأخطاء وإصلاحها ، ينبغي للمرء الرجوع إلى فصول كتاب Dunkley و Robinson22 و Ganzella et al.36.
ليس لدى المؤلفين ما يكشفون عنه.
نود أن نشكر P. Colosi على إعداد صورة EM. تم دعم هذا العمل من قبل المعاهد الوطنية للصحة (R01 NS064963, SSC; R01 NS110354 ، SSC ؛ R01 NS083846 ، SSC ؛ R21 NS094971 ، SSC ؛ T32 NS007224 ، SMT ؛ T32 NS041228, SMT)، وزارة الدفاع الأمريكية (W81XWH-17-1-0564, SSC; W81XWH-19-1-0264 ، VDJ) ، مواءمة العلوم عبر شبكة الأبحاث التعاونية لمرض باركنسون (ASAP) ، وبرنامج النهوض بالهدف لمؤسسة مايكل جيه فوكس (MJFF-020160 ، SSC و VDJ). أنشأنا رسوما توضيحية رسومية باستخدام BioRender.com.
| Name | Company | Catalog Number | Comments |
| 1 mL TB Syringe | BD | 309649 | |
| 1.5 mL Eppendorf Tubes | USA Scientific | 1415-2500 | |
| 14 mL, Open-Top Thinwall Ultra-Clear Tube | Beckman Coulter | 344060 | Compatible with SW 40 Ti |
| 23 Gauge Precision Glide Hypodermic Needle | BD | 305145 | |
| 26.3 mL, Polycarbonate Bottle with Cap Assembly | Beckman Coulter | 355618 | Compatible with Ti70 |
| 3.5 mL, Open-Top Thickwall Polypropylene Tube | Beckman Coulter | 349623 | Compatible with TLA-100.3 |
| 50 mL Falcon Tubes | Fisher Scientific | 14-432-22 | |
| Amicon Ultra-15 Centrifugal Filter Unit | Millipore Sigma | UFC901024 | |
| Aprotinin | Sigma-Aldrich | A6279 | 1 mg/mL in diH2O |
| Avanti J-26 XP Centrifuge | Beckman Coulter | B22984 | <26,000 rpm |
| Benchtop HDPE Dewar Flask | Thermo Scientific | 5028U19 | |
| C57BL/6J Mice | The Jackson Labs | 000664 | |
| Centrifuge 5810R | Eppendorf | EP022628168 | <14,000 rpm |
| complete, Mini, EDTA-free Protease Inhibitor Cocktail Tablets | Roche | 11873580001 | Add 1 tablet per 50 mL of solution |
| Curved Forceps | Fine Science Tools | 11273-20 | |
| Fine Surgical Scissors | Fine Science Tools | 8r | |
| Glas-Col Tissue Homogenizing System | Cole-Parmer | UX-04369-15 | |
| Graefe Forceps | Fine Science Tools | 11650-10 | |
| High-Speed Polycarbonate Round Bottom Centrifuge Tubes | ThermoFisher | 3117-0500 | Compatible with JA20 |
| Isofluorane | Henry Schein Animal Health | NDC 11695-6776-2 | |
| JA-20 Rotor | Beckman Coulter | 334831 | |
| Leupeptin | American Bio | AB01108 | 1 mg/mL in diH2O |
| N-[2-Hydroxyethyl] piperazine-N’-[2-ethanesulfonic acid] (HEPES) | American Bio | AB00892 | |
| Optima L-80 XP Ultracentrifuge | Beckman Coulter | <100,000 rpm | |
| Optima TLX Ultracentrifuge | Beckman Coulter | <120,000 rpm | |
| Pepstatin A | Thermo Scientific | 78436 | 1 mg/mL in DMSO |
| Phenylmethylsulfonyl fluoride (PMSF) | American Bio | AB01620 | |
| Pierce BCA Protein Assay Kit | Thermo Scientific | 23335 | For determination of protein concentration |
| Pipette Tips | |||
| Serological Pipettes | |||
| Sucrose | Sigma-Aldrich | S0389 | |
| Surgical Scissors | Fine Science Tools | 14002-12 | |
| SW 40 Ti Swinging-Bucket Rotor | Beckman Coulter | 331301 | |
| Teflon-Coated Pestle and Mortar Tissue Grinder | Thomas Scientific | 3431D94 | |
| Ti70 Rotor | Beckman Coulter | 337922 | |
| TLA-100.3 Rotor | Beckman Coulter | 349490 | |
| Tube Revolver | Dot Scientific | DTR-02VS |
- Kandel, E. R., Schwartz, J. H., Jessell, T. M., Siegelbaum, S. A., Hudspeth, A. J., Education, A. J. Synaptic Transmission. Principles of Neural Science, Fifth Edition. , (2014).
- Lepeta, K., et al. Synaptopathies: synaptic dysfunction in neurological disorders - A review from students to students. Journal of Neurochemistry. 138 (6), 785-805 (2016).
- Südhof, T. C., Malenka, R. C. Understanding synapses: Past, present, and future. Neuron. 60 (3), 469-476 (2008).
- Südhof, T. C. The molecular machinery of neurotransmitter release (Nobel lecture). Angewandte Chemie International Edition. 53 (47), 12696-12717 (2014).
- Jahn, R., Boyken, J., Pfaff, D. W. Molecular Regulation of Synaptic Release. Neuroscience in the 21st Century: From Basic to Clinical. , 351-401 (2013).
- Xiong, H., Gendelman, H. E. . Current Laboratory Methods in Neuroscience Research. , (2014).
- Azevedo, F. A., et al. Equal numbers of neuronal and nonneuronal cells make the human brain an isometrically scaled-up primate brain. Journal of Comparative Neurology. 513 (5), 532-541 (2009).
- Herculano-Houzel, S. The remarkable, yet not extraordinary, human brain as a scaled-up primate brain and its associated cost. Proceedings of the National Academy of Sciences of the United States of America. 109, 10661-10668 (2012).
- Herculano-Houzel, S., Lent, R. Isotropic fractionator: A simple, rapid method for the quantification of total cell and neuron numbers in the brain. Journal of Neuroscience. 25 (10), 2518-2521 (2005).
- Herculano-Houzel, S., Mota, B., Lent, R. Cellular scaling rules for rodent brains. Proceedings of the National Academy of Sciences of the United States of America. 103 (32), 12138-12143 (2006).
- Gray, E. G., Whittaker, V. P. The isolation of nerve endings from brain: An electron-microscopic study of cell fragments derived by homogenization and centrifugation. Journal of Anatomy. 96, 79-88 (1962).
- Gray, E. G., Whittaker, V. P. The isolation of synaptic vesicles from the central nervous system. Journal of Physiology. 153, 35-37 (1960).
- Whittaker, V. P. Thirty years of synaptosome research. Journal of Neurocytology. 22 (9), 735-742 (1993).
- Jahn, R., Fasshauer, D. Molecular machines governing exocytosis of synaptic vesicles. Nature. 490, 201-207 (2012).
- Whittaker, V. P., Michaelson, I. A., Kirkland, R. J. The separation of synaptic vesicles from nerve-ending particles ('synaptosomes). Biochemical Journal. 90 (2), 293-303 (1964).
- De Robertis, E., Rodriguez De Lores Arnaiz, G., Pellegrino De Iraldi, A. Isolation of synaptic vesicles from nerve endings of the rat brain. Nature. 194, 794-795 (1962).
- De Robertis, E., Pellegrino De Iraldi, A., Rodriguez, G., Gomez, C. J. On the isolation of nerve endings and synaptic vesicles. The Journal of Biophysical and Biochemical Cytology. 9 (1), 229-235 (1961).
- Zimmermann, H., Whittaker, V. P., Murphy, K. M. The Discovery of the Synaptosome and Its Implications. Synaptosomes. , 9-26 (2018).
- Gorenberg, E. L., et al. Identification of substrates of palmitoyl protein thioesterase 1 highlights roles of depalmitoylation in disulfide bond formation and synaptic function. PLoS Biology. 20 (3), 3001590 (2022).
- Vidyadhara, D. J., et al. Dopamine transporter and synaptic vesicle sorting defects initiate auxilin-linked Parkinson's disease. bioRxiv. , (2022).
- Schrimpf, S. P., et al. Proteomic analysis of synaptosomes using isotope-coded affinity tags and mass spectrometry. Proteomics. 5 (10), 2531-2541 (2005).
- Dunkley, P. R., Robinson, P. J., Murphy, K. M. Synaptosome Preparations: Which Procedure Should I Use. Synaptosomes. , 27-53 (2018).
- Nagy, A., Baker, R. R., Morris, S. J., Whittaker, V. P. The preparation and characterization of synaptic vesicles of high purity. Brain Research. 109 (2), 285-309 (1976).
- Takamori, S., et al. Molecular anatomy of a trafficking organelle. Cell. 127 (4), 831-846 (2006).
- Wagner, J. A., Kelly, R. B. Topological organization of proteins in an intracellular secretory organelle: the synaptic vesicle. Proceedings of the National Academy of Sciences of the United States of America. 76 (8), 4126-4130 (1979).
- Jahn, R., Schiebler, W., Ouimet, C., Greengard, P. A 38,000-dalton membrane protein (p38) present in synaptic vesicles. Proceedings of the National Academy of Sciences of the United States of America. 82 (12), 4137-4141 (1985).
- Binotti, B., Jahn, R., Pérez-Lara, &. #. 1. 9. 3. ;. An overview of the synaptic vesicle lipid composition. Archives of Biochemistry and Biophysics. 709, 108966 (2021).
- Siegel, D. P., Ware, B. R. Electrokinetic properties of synaptic vesicles and synaptosomal membranes. Biophysical Journal. 30 (1), 159-172 (1980).
- Whittaker, V. P., Michaelson, I. A., Kirkland, R. J. The separation of synaptic vesicles from disrupted nervending particles. Biochemical Pharmacology. 12 (3), 300-302 (1963).
- Clementi, F., Whittaker, V. P., Sheridan, M. N. The yield of synaptosomes from the cerebral cortex of guinea pigs estimated by a polystyrene bead "tagging" procedure. Zeitschrift für Zellforschung und Mikroskopische Anatomie. 72, 126-138 (1966).
- Carlson, S. S., Wagner, J. A., Kelly, R. B. Purification of synaptic vesicles from elasmobranch electric organ and the use of biophysical criteria to demonstrate purity. Biochemistry. 17 (7), 1188-1199 (1978).
- Huttner, W. B., Schiebler, W., Greengard, P., De Camilli, P. Synapsin I (protein I), a nerve terminal-specific phosphoprotein. III. Its association with synaptic vesicles studied in a highly purified synaptic vesicle preparation. Journal of Cell Biology. 96 (5), 1374-1388 (1983).
- Hawkins, P., et al. A guide to defining and implementing protocols for the welfare assessment of laboratory animals: eleventh report of the BVAAWF/FRAME/RSPCA/UFAW Joint Working Group on Refinement. Laboratory Animals. 45 (1), 1-13 (2011).
- Risling, T. E., Caulkett, N. A., Florence, D. Open-drop anesthesia for small laboratory animals. Canadian Veterinary Journal. 53 (3), 299-302 (2012).
- Deutsch, C., Drown, C., Rafalowska, U., Silver, I. A. Synaptosomes from rat brain: Morphology, compartmentation, and transmembrane pH and electrical gradients. Journal of Neurochemistry. 36 (6), 2063-2072 (1981).
- Ganzella, M., Ninov, M., Riedel, D., Jahn, R. Isolation of synaptic vesicles from mammalian brain. Methods in Molecular Biology. 2417, 131-145 (2022).
- Dunkley, P. R., et al. A rapid Percoll gradient procedure for isolation of synaptosomes directly from an S1 fraction: homogeneity and morphology of subcellular fractions. Brain Research. 441 (1-2), 59-71 (1988).
- Schwartz, R. D., Skolnick, P., Hollingsworth, E. B., Paul, S. M. Barbiturate and picrotoxin-sensitive chloride efflux in rat cerebral cortical synaptoneurosomes. FEBS Letters. 175 (1), 193-196 (1984).
- Pittaluga, A., Thellung, S., Maura, G., Raiteri, M. Characterization of two central AMPA-preferring receptors having distinct location, function and pharmacology. Naunyn-Schmiedeberg's Archives of Pharmacology. 349 (6), 555-558 (1994).
- Israël, M., Whittaker, V. P. The isolation of mossy fibre endings from the granular layer of the cerebellar cortex. Experientia. 21 (6), 325-326 (1965).
- Khvotchev, M., Lonart, G., Südhof, T. C. Role of calcium in neurotransmitter release evoked by alpha-latrotoxin or hypertonic sucrose. Neuroscience. 101 (3), 793-802 (2000).
- Lonart, G., Janz, R., Johnson, K. M., Südhof, T. C. Mechanism of action of rab3A in mossy fiber LTP. Neuron. 21 (5), 1141-1150 (1998).
- Nicholls, D. G., Sihra, T. S. Synaptosomes possess an exocytotic pool of glutamate. Nature. 321 (6072), 772-773 (1986).
- Dunkley, P. R., Jarvie, P. E., Robinson, P. J. A rapid Percoll gradient procedure for preparation of synaptosomes. Nature Protocols. 3 (11), 1718-1728 (2008).
- Cotman, C. W., Matthews, D. A. Synaptic plasma membranes from rat brain synaptosomes: Isolation and partial characterization. Biochimica et Biophysica Acta. 249 (2), 380-394 (1971).
- Booth, R. F., Clark, J. B. A rapid method for the preparation of relatively pure metabolically competent synaptosomes from rat brain. Biochemical Journal. 176 (2), 365-370 (1978).
- Takamori, S., Riedel, D., Jahn, R. Immunoisolation of GABA-specific synaptic vesicles defines a functionally distinct subset of synaptic vesicles. Journal of Neuroscience. 20 (3), 4904-4911 (2000).
- Burger, P. M., et al. Synaptic vesicles immunoisolated from rat cerebral cortex contain high levels of glutamate. Neuron. 3 (6), 715-720 (1989).
- Blondeau, F., et al. Tandem MS analysis of brain clathrin-coated vesicles reveals their critical involvement in synaptic vesicle recycling. Proceedings of the National Academy of Sciences of the United States of America. 101 (11), 3833-3838 (2004).
- Maycox, P. R., Link, E., Reetz, A., Morris, S. A., Jahn, R. Clathrin-coated vesicles in nervous tissue are involved primarily in synaptic vesicle recycling. Journal of Cell Biology. 118 (6), 1379-1388 (1992).
Tags
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved