Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Neuroscience
Subcellulær fraktionering til isolering af synaptiske komponenter fra Murine-hjernen
Denne protokol præsenterer en robust, detaljeret metode til at opnå meget rene synaptosomer, synaptiske vesikler og andre synaptiske fraktioner fra musehjernen. Denne metode muliggør evaluering af synaptiske processer, herunder biokemisk analyse af proteinlokalisering og funktion med rumopløsning.
Synaptiske terminaler er de primære steder for neuronal kommunikation. Synaptisk dysfunktion er et kendetegn for mange neuropsykiatriske og neurologiske lidelser. Karakteriseringen af synaptiske underrum ved biokemisk isolering er derfor en kraftfuld metode til at belyse de molekylære baser af synaptiske processer, både i sundhed og sygdom. Denne protokol beskriver isoleringen af synaptiske terminaler og synaptiske underrum fra musehjerner ved subcellulær fraktionering. For det første isoleres forseglede synaptiske terminalstrukturer, kendt som synaptosomer, efter homogenisering af hjernevæv. Synaptosomer er neuronale præ- og postsynaptiske rum med klemte og forseglede membraner. Disse strukturer bevarer en metabolisk aktiv tilstand og er værdifulde til at studere synaptisk struktur og funktion. Synaptosomerne udsættes derefter for hypotonisk lysis og ultracentrifugering for at opnå synaptiske underrum beriget til synaptiske vesikler, synaptisk cytosol og synaptisk plasmamembran. Brøkrenhed bekræftes ved elektronmikroskopi og biokemisk berigelsesanalyse for proteiner, der er specifikke for subsynaptiske rum. Den præsenterede metode er et ligetil og værdifuldt værktøj til at studere synapsens strukturelle og funktionelle egenskaber og molekylære ætiologi af forskellige hjernesygdomme.
Synapser er de grundlæggende beregningsenheder i hjernen, hvorigennem neuroner kommunikerer og udøver forskellige og udsøgt komplekse funktioner. Synapser er således grundlæggende for hjernens sundhed1; Synaptisk dysfunktion er impliceret som kilde eller resultat af mange lidelser2. Synapser udgøres af præ- og postsynaptiske terminaler, forlængelser af to forskellige neuroner, der er tæt apposed og adskilt af en synaptisk kløft krydset af synaptiske adhæsionsmolekyler. Information strømmer fra det præ- til postsynaptiske rum i form af kemiske budbringere kaldet neurotransmittere1. De molekylære processer, der er involveret i neurotransmission, er aktive forskningsområder 3,4,5. Forståelse af de patogene processer inden for synaptiske terminaler og synapsernes respons på patologi i andre neuronale underrum er afgørende skridt til at løse forstyrrelser i hjernen 1,2. Flere metodiske fremskridt, overvejende anvendt på murinemodeller, har fremmet denne forfølgelse6. Isolering af synaptiske fraktioner ved differentiel centrifugering er en sådan paradigmeskiftende metode, der har muliggjort detaljeret evaluering af synaptiske processer inden for sundhed og sygdom.
Den voksne menneskelige hjerne består af 80-90 milliarder neuroner 7,8. Blandt murinearter indeholder rottehjernen ca. ~ 200 millioner neuroner, mens mus har ~ 70 millioner 9,10. Hver neuron danner tusindvis af specifikke synaptiske forbindelser med et netværk af stærkt polariserede neuroner blandet med gliaceller og tæt vaskulatur. I et så komplekst og heterogent væv var det engang utænkeligt at isolere og studere synapser som et uafhængigt system. I 1960'erne gjorde Victor Whittaker, Catherine Hebb og andre dette muligt ved at isolere intakte synaptiske terminaler ved hjælp af subcellulær fraktionering11,12,13,14. I et forsøg på at isolere synaptiske vesikler (SV'er) homogeniserede de hjerner gennem flydende forskydningskraft i iso-osmotisk (0,32 M) saccharose efterfulgt af ultracentrifugering. De opnåede afbrudte, plasmamembranlukkede, intakte nerveterminaler eller varicositeter, som de kaldte nerveendende partikler (NEP'er)11,13. Da synapsens strukturelle og funktionelle egenskaber blev bevaret i disse strukturer, blev NEP'er senere betegnet "synaptosomer" for kongruens med andre subcellulære organeller13,15. Det er værd at bemærke, at Eduardo de Robertis og kollegers arbejde, der opfandt udtrykket "synaptisk vesikel", overlappede med Whittaker og kolleger og bidrog til valideringen af "synaptosom" isolation og karakterisering16,17,18.
Synaptosomer er fysiologisk aktive strukturer, der indeholder alle de cellulære og molekylære egenskaber, der kræves til opbevaring, frigivelse og genoptagelse af neurotransmittere13,18. Bevarelsen af vigtige synaptiske egenskaber in vitro og frihed fra ikke-synaptiske komponenter bidrager også til nytten af denne isolationsmetode. Synaptosomer har bidraget enormt til forståelsen af de kemiske og fysiologiske egenskaber ved neurotransmission og bruges nu til at studere synaptiske molekylære processer og deres ændringer i sygdom 19,20,21,22,23. Synaptosomer er også det oprindelige kildemateriale til isolering af synaptiske komponenter såsom SV'er, clathrinbelagte vesikler (CCV'er), synaptisk cytosol, synaptisk plasmamembran, synaptiske mitokondrier, synaptiske adhæsionsmolekyler og andre komponenter af interesse, som kan lette forståelsen af de molekylære mekanismer for synaptisk funktion 18,19,20,24,25,26, 27,28. Disse subsynaptiske komponenter kan opnås ved osmotisk lysis af synaptosomer og saccharosedensitetsgradient ultracentrifugering15,29. Selvom den oprindelige subcellulære fraktioneringsmetode fra Whittakers forskningsgruppe er kendt for at være effektiv til at isolere kvalitetssynaptosomer og SV'er 13,30, forbedrer nylige optimeringer renheden af de subcellulære fraktioner 22,23,31,32. Denne artikel giver en meget detaljeret og tilgængelig version af en klassisk protokol til subcellulær fraktionering af murinhjernevæv til isolering af synaptosomer, SV'er og andre subsynaptiske komponenter.
Alle forsøg med mus blev godkendt af Institutional Animal Care and Use Committee (IACUC) ved Yale University (protokol 2021-11117) og udført i en facilitet akkrediteret af Association for the Assessment and Accreditation of Laboratory Animal Care International (AAALAC). Dyrepleje og opstaldning overholdt vejledningen til pleje og brug af forsøgsdyr33 og blev leveret af Yale Animal Resource Center (YARC). Dyrene blev opretholdt i en 12 timers lys/mørk cyklus med ad libitum adgang til mad og vand. Fem til otte mus eller to til fire rotter pr. genotype eller tilstand er påkrævet for følgende protokol. Færre rotter er nødvendige på grund af deres større hjernevolumener. På samme måde kan forsøgsdyrenes alder påvirke brøkudbyttet; Yderligere mus kan være påkrævet i aldre mindre end 2 måneder. Ellers gælder de skitserede procedurer for både murinearter og sunde voksne dyr i alle aldre. De repræsentative data, der blev præsenteret i denne undersøgelse, anvendte vildtype (C57BL / 6J) mus (alder = 2 måneder; fire hanner og fire hunner pr. replikat) opnået fra en kommerciel kilde (se Materialetabel).
1. Eksperimentelt præparat
BEMÆRK: Denne protokol kræver ~ 11 timer for en enkelt forsker at gennemføre. Det anbefales på det kraftigste at gennemføre benchtop-opsætning (figur 1), bufferforberedelse (tabel 1), forkøling af centrifuger og rotorer til 4 °C og indsamling og mærkning af nødvendige materialer og udstyr (se Materialetabel) dagen før protokoludførelse, hvor det er relevant.
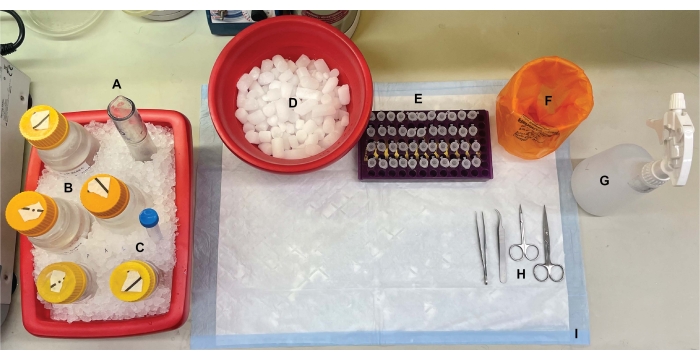
Figur 1: Opsætning af bordplade. Før hjernedissektioner blev (A) Dounce glas homogenisatorer og (B) alle buffere kølet på is. (C) Proteasehæmmerstamopløsninger blev optøet på is. Der blev opnået en anden beholder med våd is til centrifugerør, en Dewar med flydende nitrogen (ikke vist) og (D) en beholder med tøris til kortvarig opbevaring af prøverne lynfrosset i flydende nitrogen. (E) Mikrocentrifugerør blev forudmærket til alle prøver, da fire alikvoter af hver subcellulær fraktionsprøve pr. genotype eller tilstand blev indsamlet under denne procedure (tidsbesparende tip: grundigt mærket alle rørene dagen før eksperimentet udføres). (F) En passende beholder til biofarligt affald, (G) 70% ethanol, (H) kirurgiske værktøjer og (I) en absorberende overfladepude. De nødvendige centrifugerør og engangsartikler blev afsat til effektiv adgang under protokolimplementering (ikke vist). Klik her for at se en større version af denne figur.
- Forbered bordpladen til operation og saml saks og tang, der kræves til hjerneudskæring (se Materialetabel). Formærket 1,5 ml mikrocentrifugerør til musehalebiopsier og fire rør pr. opsamlet fraktion, som beskrevet i figur 2.
- Få to beholdere med våd is, en beholder med tøris og en bordplade flydende nitrogen Dewar kolbe.
- Optøning af phenylmethylsulfonylfluorid (PMSF), pepstatin A, aprotinin og leupeptinstamopløsninger på is (se materialetabel). Forbered de nødvendige buffere (tabel 1).
BEMÆRK: Saccharoseopløsninger kan fremstilles på forhånd og opbevares ved 4 °C. Proteasehæmmere (optøede lagre og tabletter) skal dog tilsættes friske til alle buffere ved forsøgets begyndelse på grund af ustabiliteten af disse reagenser i vandige opløsninger. Desuden skal alle buffere fremstilles med vaskemiddelfri glasvarer og vaskemiddelfrit vand for at muliggøre opsamling af intakte synaptosomer. - Chill alle buffere og glas Dounce homogenisatorer (se Tabel over materialer) på is. Centrifugerne indstilles til 4 °C, og rotorerne afkøles til 4 °C.
- Der tilsættes 14 ml buffer A (tabel 1) til en Dounce-homogenisator på is.
Tabel 1: Sammensætning af de subcellulære fraktioneringsbuffere. Klik her for at downloade denne tabel.
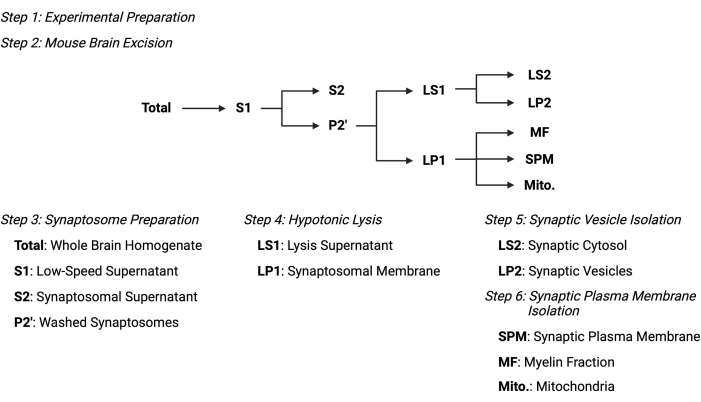
Figur 2: Oversigt over den subcellulære fraktioneringsprotokol. Resuméskematisk af de subcellulære fraktioneringstrin og indsamlede prøver. Klik her for at se en større version af denne figur.
2. Musehjerne excision
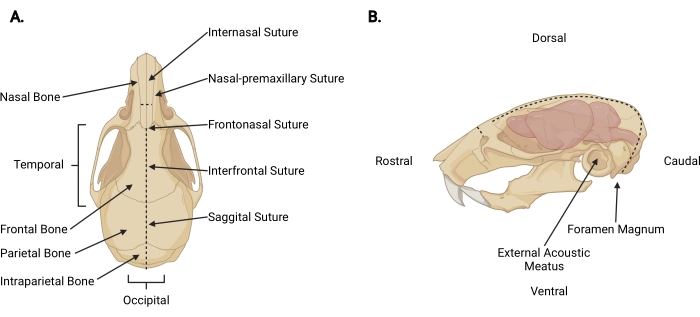
Figur 3: Kraniofacial anatomi . (A) Dorsal visning af et musekranium med relevante kraniestrukturer angivet. (B) Venstre lateral visning af et musekranium og hjerne med relevante kraniestrukturer og anatomiske retninger angivet. De stiplede linjer repræsenterer de steder, hvor snit skal foretages. Klik her for at se en større version af denne figur.
- Bedøve hver mus dybt med 100% isofluoran i et anæstesikammer placeret i en røghætte eller biosikkerhedsskab ved hjælp af en åben dråbemetode34. Ofr hver mus ved cervikal rygsøjleforskydning efterfulgt hurtigt af halshugning. Skift mellem genotyper eller eksperimentelle grupper for hvert offer og dissektion12. Få halebiopsier efter aktiv dødshjælp ved at fjerne 2 mm af den distale halespids med en fin saks. Opbevar vævet til genotypning.
- Spray det afhuggede hoved med 70% ethanol for at forhindre hår i at klæbe til vævet og kirurgiske instrumenter under dissektion.
- Indsæt fin saks under huden ved halshugningssnittet til en pericranial dybde og lav et midsagittalt snit op til den internasale sutur (figur 3A) for at trække hovedbunden ud af kraniet.
- Arbejd fra det occipitale område mod hvert tidsmæssigt aspekt, trim fascia og muskel for at udsætte kraniets ydre overflade ud over hver ekstern akustisk meatus (figur 3B).
- Fastgør hovedbunden og rostralaspektet af kraniet med den ikke-dominerende hånd. Med den anden indsættes en fin saks 2 mm i den kaudale side af foramen magnum, hvor rygmarven er synlig ud. Lav et midterlinjesnit, indtil saksen når den indre overflade af den intraparietale knogle (figur 3; stiplede linjer).
BEMÆRK: Under det indledende snit skal saksen være parallel med rygmarven med tryk påført mod kraniets indre overflade for at forhindre skade på hjernestammen og lillehjernen. - Skift saksens vinkel, så knivene løber parallelt med kraniets dorsale overflade. Fortsæt med at fremme det midsagittale snit rostralt gennem parietal- og frontknoglerne ved hjælp af sagittale og interfrontale suturer som vejledning. Brug konstant opadgående tryk for at undgå beskadigelse af cortex. Afslut snittet lige ud over den internasale sutur (figur 3A).
- Lav et lille vinkelret snit (~ 3 mm) til næsebenet, rostral til den internasale sutur, ved at placere saksen vinkelret på kraniet med hvert blad placeret ved en nasal-premaxillær sutur og gøre en jævn skåret (figur 3; stiplede linjer).
BEMÆRK: Dette trin vil øge letheden ved at trække kraniet tilbage og vil være afgørende for indsamling af den olfaktoriske pære, hvis dette område er af interesse. - Mens du sikrer rostralaspektet, skal du bruge den ene side af et par teksturerede tang til forsigtigt at løfte kraniet op fra hjernen, derefter lateralt og ventralt. Gentag langs midterlinjen efter behov, derefter for den anden halvkugle, indtil hele hjerneoverfladen er udsat.
- Brug buede tang eller en fin spatel til forsigtigt at løfte den rostrale side af hjernen. Skær de optiske og kraniale nerver for at fuldføre udskæringen fra kraniet.
- For hver tilstand samles fem til otte musehjerner sammen i den kølede glas Dounce homogenisator indeholdende 14 ml buffer A (tabel 1).
3. Synaptosom forberedelse
BEMÆRK: Skemaerne for denne procedure er vist i figur 4.
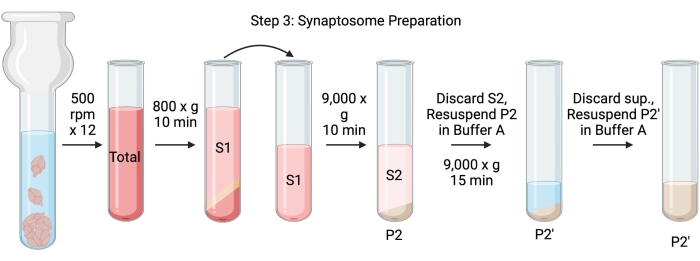
Figur 4: Synaptosom forberedelse. Skematisk af trin 3, generering af synaptosomer (P2'). Klik her for at se en større version af denne figur.
- Homogeniser hjernerne ved hjælp af en glas Dounce homogenisator i 12 op-ned passerer ved 500 o / min (i alt). Hold en kort pause ved hvert nedslag for at sikre grundig homogenisering af vævet. Homogeniser fortrinsvis i et isbad for at undgå opvarmning og proteindenaturering. Tag 5 μL alikvoter til bestemmelse af proteinkoncentration ved bicinchoninsyreassay (BCA, se Materialetabel). Tag 100 μL hele hjernen lysat aliquots for western blot (WB). For denne og alle efterfølgende prøver (figur 2) udtages to alikvoter for BCA og to aliquoter for WB. Flash-frys alle de opsamlede alikvoter i flydende nitrogen og opbevar dem ved -80 °C.
- Spin den totale hjernehomogenat i et højhastigheds rundt bundcentrifugerør (14 ml) (se materialetabel) ved 800 x g i 10 minutter ved 4 °C for at opnå supernatanten (S1). Overfør S1 til et nyt centrifugerør, og efterlad pelleten (P1), som indeholder intakte celler og kerner. Undgå at pipettere den luftige, hvide, løse, overfladiske pille op. Tag 2 x 5 μL S1 til BCA og 2 x 100 μL S1 til WB.
- Spin S1 ved 9.000 x g i 15 minutter ved 4 °C for at opnå synaptosomal supernatant (S2) og rå synaptosompellet (P2). Tag 2 x 10 μL S2 til BCA og 2 x 500 μL S2 til WB. Kassér supernatanten efter opnåelse af aliquots og fortsæt til næste trin med pelleten.
- P2 resuspenderes i 3 ml iskold buffer A med proteasehæmmere og centrifuge ved 9.000 x g i 15 minutter ved 4 °C for at opnå supernatanten (S2') og vaskede synaptosomer (P2'). Kassér supernatanten og behold pelleten.
- Resuspend P2' i 3 ml buffer A. Undgå at genbruge den mørkerøde del i bunden af pelleten, som hovedsageligt indeholder mitokondrier. Tag 2 x 20 μL P2' for BCA og 2 x 100 μL P2' for WB.
BEMÆRK: Dette kan opnås ved forsigtigt pipetteblanding af pillens kanter og overflade for at resuspendere de hvidvaskede synaptosomer, mens pipettespidsen ledes væk fra pellets røde centrum.
4. Hypotonisk lysis
BEMÆRK: Skemaerne for denne procedure er vist i figur 5.
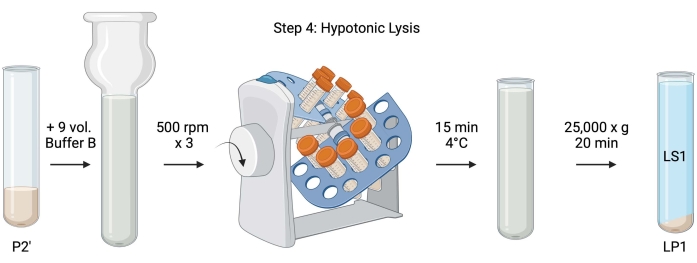
Figur 5: Hypotonisk lyse. Skematisk af trin 4, den hypotoniske lysis af synaptosomer til at generere lysis supernatant (LS1) og synaptosomale membranfraktioner (LP1). Klik her for at se en større version af denne figur.
- Til hypotonisk lysis af vaskede synaptosomer tilsættes 9 volumener kølet buffer B (tabel 1) til resuspenderet P2' (~27 ml). Homogeniser synaptosomerne i en glas Dounce homogenisator (tre op-ned passerer ved 500 o / min).
- Prøverne overføres til 50 ml koniske centrifugerør med låg. Drej dem på en rørrevolver i et 4 °C kølerum i 15 min.
- Centrifuge lysed P2' ved 25.000 x g i 20 minutter ved 4 °C for at opnå lysis supernatant (LS1) og lysis pellet indeholdende synaptosomale membraner (LP1). Tag 2 x 50 μL LS1 til BCA og 2 x 400 μL LS1 til WB. Overfør LS1 til et centrifugerør med låg til ultracentrifugering (se Materialetabel).
5. Synaptisk vesikel isolering
BEMÆRK: Skemaerne for denne procedure er vist i figur 6.
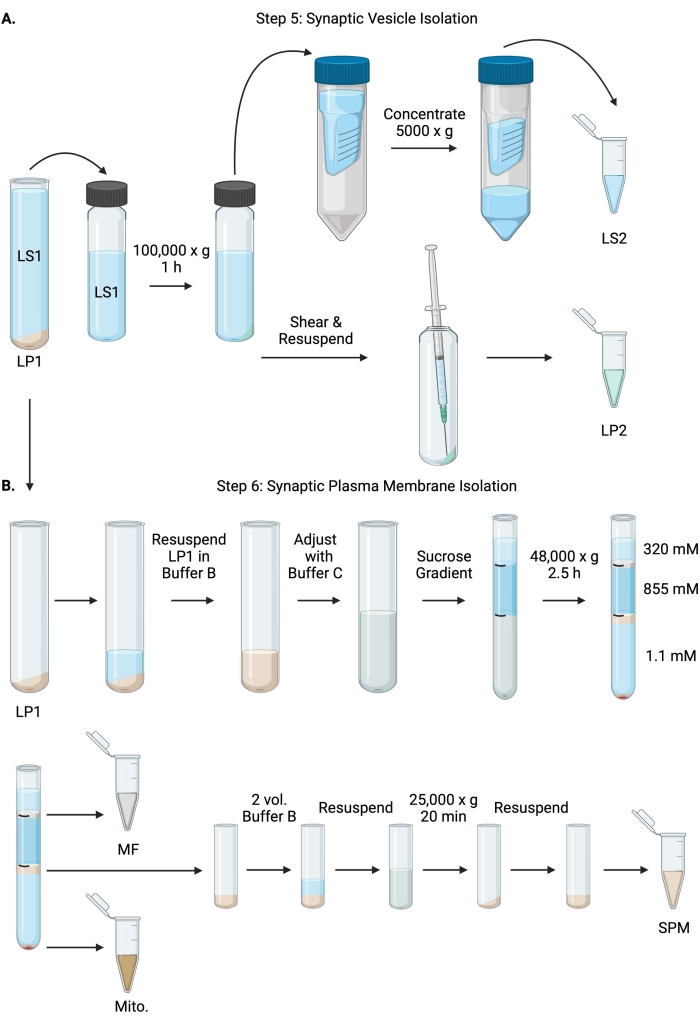
Figur 6: Synaptisk vesikelisolering og synaptisk plasmamembranisolering. (A) Skematisk af trin 5, isolering af synaptisk cytosol (LS2) og synaptisk vesikel (LP2) fraktioner og (B) trin 6, generering af myelin (MF), synaptisk plasmamembran (SPM) og mitokondrie (Mito.) fraktioner efter ultracentrifugering af saccharosegradienter. Klik her for at se en større version af denne figur.
- Centrifuge LS1 i en ultracentrifugerotor med fast vinkel (se Materialetabel) ved 100.000 x g i 60 minutter ved 4 °C for at opnå synaptisk cytosolsupernatant (LS2) og synaptisk vesikelpellet (LP2). LP2 vil være lille, gennemskinnelig og stærkt klæbet til siden af centrifugerøret.
- Resuspender LP2 i 500 μL buffer A. Brug en 23 G nål og en 1 ml sprøjte, forskydning LP2 med blid trituration. Tag 2 x 10 μL LP2 til BCA og 2 x 250 μL LP2 til WB.
- Overfør LS2 (~30 ml) til centrifugalfilterenheder med en 10 kDa afskæring (se Materialetabel).
BEMÆRK: Hvis proteiner mindre end 10 kDa er af interesse, er 4 kDa afskæringscentrifugalfilterenheder tilgængelige, men vil resultere i længere omdrejningstider. - LS2 koncentreres til ca. 0,5 ml ved at dreje ved 5000 x g i op til 1 time ved 4 °C. Tag 2 x 10 μL koncentreret LS2 til BCA og 2 x 250 μL koncentreret LS2 til WB. Når du har startet spin, skal du fortsætte direkte til trin 6.1.
6. Synaptisk plasmamembranisolering
- Resuspender LP1 (trin 4.3) i 1 ml buffer B (tabel 1). Tag 2 x 10 μL LP1 til BCA og 2 x 50 μL LP1 til WB. Den resterende LP1 justeres til et slutvolumen på 7,5 ml og en endelig saccharosekoncentration på 1,1 M med buffer B og buffer C (tabel 1).
- Overfør 7,5 ml resuspenderet LP1 til et 14 ml ultracentrifugerør (se Materialetabel). Overlejr forsigtigt LP1 med 3,75 ml buffer D (tabel 1), og overlejr derefter med 1,25 ml buffer A (eller et større volumen til at fylde lige under toppen af centrifugerøret). Undgå pipettering ned ad siden af røret, hvilket vil forstyrre saccharosegradientgrænsefladerne. Efter overlejring af hver saccharosefraktion skal du markere toppen af opløsningen med en pen. Rør til ultracentrifugering afbalanceres efter vægt, ikke volumen, med dråbevis tilsætning af buffer A til inden for 10 mg. Centrifuge ved 48.000 x g i 2,5 timer ved 4 °C i en svingende spand ultracentrifugerotor (se Materialetabel).
- Få billeder af de intakte gradienter efter ultracentrifugering for at dokumentere særpræget af hver saccharosegrænseflade og succesen med fraktionering.
- Fjern forsigtigt det overfladiske lag af 320 mM saccharose (buffer A). Gendan myelinfraktionen (MF) ved 320 mM/855 mM saccharosegrænsefladen i et volumen på 800 μL. Gendan den synaptiske plasmamembranfraktion (SPM) ved 855 mM/1,1 M saccharosegrænsefladen i et volumen på 1.000 μL. Pipeter hver fraktion op fra rørets væg på en cirkulær måde for at sikre, at den komplette fraktion opsamles. Opsug forsigtigt den resterende saccharose og genfind mitokondriepellet (Mito.) ved at resuere i 200 μL buffer B. Tag 2 x 100 μL MF til BCA og 2 x 10 μL Mito. for BCA; dele resten af MF og Mito. prøver i halvdelen til WB.
- Fortynd SPM-fraktionen med 2 volumener buffer B (~2 ml), og centrifuger derefter i en rotor med fast vinkel i et 3,5 ml centrifugerør (se Materialetabel) ved 25.000 x g i 20 minutter ved 4 °C. Supernatanten kasseres, og SPM-pelleten i buffer A gensuspenderes i et slutvolumen på 250 μL. Tag 2 x 5 μL SPM til BCA og del den resterende SPM i to for WB.
- Udfør en BCA for at bestemme proteinkoncentrationen i hver prøve, der tegner sig for variabelt aliquotvolumen.
BEMÆRK: For WB-analyse er den foreslåede arbejdsproteinkoncentration for alle subcellulære fraktioner 2 μg / μL (eller så høj som muligt for LS1 og MF).
Den præsenterede metode resulterer i 11 hjerne subcellulære fraktioner, der kan udsættes for yderligere oprensning og forskellige former for downstream analyse35,36. Guldstandardmetoden til vurdering af kvaliteten af synaptosomer, SV'er23 og andre komponenter er elektronmikroskopi (EM) (figur 7). Kvantitativ immunoblotting for proteiner, der er til stede i specifikke subcellulære fraktioner, kan også udføres for at vurdere markører for fraktionsrenhed (figur 8). For eksempel afslører immunoblotanalyse af fraktioner berigelsen af N-cadherin (CDH2, UniProt-navn) i den synaptiske plasmamembranfraktion (SPM), α-synuclein (SYUA) i den synaptiske cytosol (LS2), synaptophysin (SYPH) i den synaptiske vesikelfraktion (LP2) og myelinbasisk protein (MBP) i myelinfraktionen (MF) sammenlignet med proteinniveauer i det oprindelige hele hjernehomogenat (total) (figur 8) (figur 8 ). Når fraktionsrenhed er blevet fastslået (bemærk for eksempel fraværet af CDH2 i LS2-fraktionen eller den mange gange stigning i SYPH i LP2-fraktionen), kan kvantitativ immunoblotting bruges til at bestemme lokaliseringen af proteiner af interesse eller forespørge forskelle i proteinfordeling mellem genotyper eller behandlinger. Forståelse af den subcellulære lokalisering af synaptiske proteiner kan muliggøre dissektion af tidligere ubeskrevne proteinfunktioner. Desuden kan denne metode belyse defekter eller synaptisk dysfunktion i sygdomstilstande, især når den er parret med funktionelle assays. For eksempel har vores team brugt denne metode til at identificere en pulje af enzymatisk aktivt palmitoylprotein thioesterase 1, der er beriget i den synaptiske cytosol19.
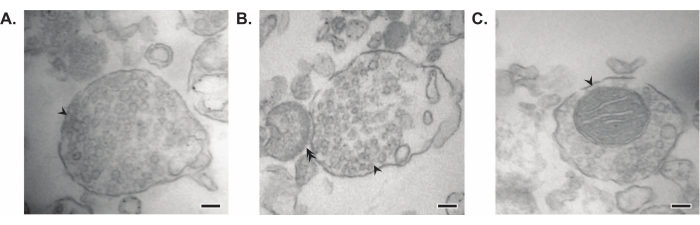
Figur 7: Elektronmikroskopi (EM) af synaptosomer. (A) Repræsentativt EM-billede af et synaptosom, der indeholder synaptiske vesikler (pil). (B) Repræsentativt EM-billede af et synaptosom med både præ- (pil) og postsynaptiske komponenter (dobbeltpil). (C) Repræsentativt EM-billede af et synaptosom, der indeholder synaptiske vesikler og en mitokondrion (pil) (skalabjælker = 100 nm). Klik her for at se en større version af denne figur.
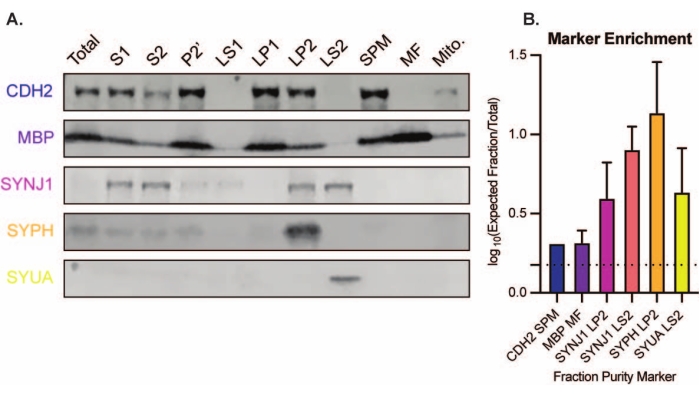
Figur 8: Immunoblotanalyse af subcellulære fraktioner. (A) Markører for subcellulær fraktionsrenhed (angivet med UniProt-nomenklatur) er passende lokaliseret sammenlignet med hele hjernehomogenatet (total): N-cadherin (CDH2) i den synaptiske plasmamembranfraktion (SPM), synaptophysin 1 (SYPH) og synaptojanin 1 (SYNJ1) i den synaptiske vesikel berigede fraktion (LP2), α-synuclein (SYUA) i den synaptiske cytosol (LS2), og myelin basisk protein (MBP) i myelinfraktionen (MF). (B) Immunoblot-kvantificeringsanalyse afslører berigelsen (foldændring fra total) af fraktionsrenhedsmarkører. Data repræsenteres som middel ± standardafvigelse på log10-skala. Den stiplede linje angiver en 1,5 gange ændring (y = 0,176) (n = 3 replikate eksperimenter med 8 vildtypemus; alder = 2 måneder; n = 4-5 blots for SYPH, SYUA, MBP, med n = 3 afbildede værdier, der tidligere er offentliggjort af Gorenberg et al.19; n = 5 for SYNJ1; n = 1 for CDH2). Klik her for at se en større version af denne figur.
I deres skelsættende undersøgelser brugte Whittaker og kolleger fire morfologiske kriterier til at identificere synaptosomer: (1) strukturerne har en forseglet plasmamembran; (2) strukturerne indeholder SV'er, der ligner dem i nerveterminaler og varicositeter in situ i størrelse og antal; 3) strukturerne har en eller flere små mitokondrier og (4) den præsynaptiske membran klæbes ofte til en postsynaptisk komponent11,12,13. Selvom de to første kriterier generelt gælder for enhver isolationsmetode, vil ikke alle resulterende synaptosomer i de seneste protokoller, der er beskrevet i denne artikel, have mitokondrier og vedhæftede postsynaptiske terminaler. Ca. 60% af synaptosomerne vil have mitokondrier, og kun op til 15% anslås at have vedhæftede postsynaptiske terminaler37. Hvis postsynaptiske komponenter er af særlig interesse, er brugen af en isotonisk Krebs-lignende homogeniseringsbuffer og trykfiltrering til berigelse kendt for at give høje koncentrationer af synaptosomer med postsynaptiske terminaler (også kaldet synaptoneurosomer)22,38.
Metoden til at ofre dyret kan påvirke kvaliteten af synaptosomer og synaptiske subfraktioner. Voksne dyr, der ofres ved hjælp af en eutanasi-metode, der ikke kræver anæstesi, vil resultere i den bedste fraktionskvalitet. Endvidere skal hjernerne være frisk dissekeret, ikke frosset og homogeniseret ved hjælp af et 1:10-forhold mellem homogeniseringsbuffer (vægt / volumen) for de mest levedygtige synaptiske fraktioner22. Hjernen har en heterogen population af synapser, der kan differentieres efter den type neurotransmittere, de bærer. Synaptosomdannelse påvirkes generelt ikke af synapsetype eller neurotransmitterindhold13. En undtagelse er mosbegroede fibre i lillehjernen, som vides at blive forstyrret under optimale forhold for at opnå synaptosomer fra resten af hjernen39,40. Således anbefales fjernelse af cerebellum før hjernehomogenisering, hvis udelukkelsen af denne region ikke påvirker det eksperimentelle mål. Hvis interesseret i at isolere synaptosomer af en bestemt neurotransmitterkarakter, kan områder i hjernen, der er beriget for neuroner, der indeholder neurotransmitteren af interesse, først isoleres. Denne tilgang vil imidlertid medføre begrænsninger for det endelige brøkudbytte afhængigt af størrelsen af interesseområdet (dyrenes alder er derfor også en overvejelse). Der er immunokemiske metoder til isolering af neurotransmitterspecifikke synaptosomer, men levedygtigheden og udbyttet vil blive væsentligt kompromitteret22. Hvis det er vigtigt at vurdere synaptosomets metaboliske levedygtighed, kan måling af neurotransmitterfrigivelse 41,42 eller visse enzymatiske assays43 anvendes.
Almindelige forurenende stoffer i synaptosompræparater omfatter mikrosomer, frie mitokondrier, SV'er og neuronale og glialmembraner. Forurening kan reduceres ved at øge antallet af vaske ved P1- og P2-fraktionerne22 og undgå resuspension af den røde mitokondriepellet i efterfølgende trin. I eksperimenter, hvor metabolisk levedygtighed og tid er afgørende, vil det være nyttigtat reducere antallet af vaske og bruge Ficoll- eller Percoll-gradienter over saccharosegradienter 44,45,46. Disse metoder reducerer også forurening betydeligt. Whittakers oprindelige protokol gav SV'er af høj kvalitet. Yderligere optimering af Nagy et al.23, inkluderet i denne metode, producerer SV'er med bemærkelsesværdig homogenitet og renhed uden at gå væsentligt på kompromis med udbytte36. Hvis specifikke SV-undertyper er af interesse, såsom glutamatergiske (VGLUT-1-indeholdende) eller GABAergic (VGAT-1-indeholdende) SV'er, kan immunisolering ved hjælp af specifikke antistoffer udføres47,48. Der findes også alternative metoder til isolering af CCV'er fra synaptosomer, som på grund af differentialdensitet muligvis ikke er til stede ved samme grænseflade som SV'er opnået med denne metode20,49,50.
Samlet set kan den nuværende protokol til isolering af synaptiske komponenter optimeres yderligere for at opnå fraktioner med forbedret homogenitet og levedygtighed baseret på kvaliteten og kvantiteten af kildehjernevævet og de eksperimentelle mål. For yderligere fejlfindingsdetaljer skal man henvise til bogkapitler af Dunkley og Robinson22 og Ganzella et al.36.
Forfatterne har intet at afsløre.
Vi vil gerne takke P. Colosi for EM-billedforberedelse. Dette arbejde blev støttet af National Institutes of Health (R01 NS064963, SSC; R01 NS110354, SSC; R01 NS083846, SSC; R21 NS094971, SSC; T32 NS007224, SMT; T32 NS041228, SMT), det amerikanske forsvarsministerium (W81XWH-17-1-0564, SSC; W81XWH-19-1-0264, VDJ), Aligning Science Across Parkinsons (ASAP) Collaborative Research Network (SSC) og Michael J. Fox Foundation Target Advancement Program (MJFF-020160, SSC & VDJ). Vi skabte grafiske illustrationer ved hjælp af BioRender.com.
| Name | Company | Catalog Number | Comments |
| 1 mL TB Syringe | BD | 309649 | |
| 1.5 mL Eppendorf Tubes | USA Scientific | 1415-2500 | |
| 14 mL, Open-Top Thinwall Ultra-Clear Tube | Beckman Coulter | 344060 | Compatible with SW 40 Ti |
| 23 Gauge Precision Glide Hypodermic Needle | BD | 305145 | |
| 26.3 mL, Polycarbonate Bottle with Cap Assembly | Beckman Coulter | 355618 | Compatible with Ti70 |
| 3.5 mL, Open-Top Thickwall Polypropylene Tube | Beckman Coulter | 349623 | Compatible with TLA-100.3 |
| 50 mL Falcon Tubes | Fisher Scientific | 14-432-22 | |
| Amicon Ultra-15 Centrifugal Filter Unit | Millipore Sigma | UFC901024 | |
| Aprotinin | Sigma-Aldrich | A6279 | 1 mg/mL in diH2O |
| Avanti J-26 XP Centrifuge | Beckman Coulter | B22984 | <26,000 rpm |
| Benchtop HDPE Dewar Flask | Thermo Scientific | 5028U19 | |
| C57BL/6J Mice | The Jackson Labs | 000664 | |
| Centrifuge 5810R | Eppendorf | EP022628168 | <14,000 rpm |
| complete, Mini, EDTA-free Protease Inhibitor Cocktail Tablets | Roche | 11873580001 | Add 1 tablet per 50 mL of solution |
| Curved Forceps | Fine Science Tools | 11273-20 | |
| Fine Surgical Scissors | Fine Science Tools | 8r | |
| Glas-Col Tissue Homogenizing System | Cole-Parmer | UX-04369-15 | |
| Graefe Forceps | Fine Science Tools | 11650-10 | |
| High-Speed Polycarbonate Round Bottom Centrifuge Tubes | ThermoFisher | 3117-0500 | Compatible with JA20 |
| Isofluorane | Henry Schein Animal Health | NDC 11695-6776-2 | |
| JA-20 Rotor | Beckman Coulter | 334831 | |
| Leupeptin | American Bio | AB01108 | 1 mg/mL in diH2O |
| N-[2-Hydroxyethyl] piperazine-N’-[2-ethanesulfonic acid] (HEPES) | American Bio | AB00892 | |
| Optima L-80 XP Ultracentrifuge | Beckman Coulter | <100,000 rpm | |
| Optima TLX Ultracentrifuge | Beckman Coulter | <120,000 rpm | |
| Pepstatin A | Thermo Scientific | 78436 | 1 mg/mL in DMSO |
| Phenylmethylsulfonyl fluoride (PMSF) | American Bio | AB01620 | |
| Pierce BCA Protein Assay Kit | Thermo Scientific | 23335 | For determination of protein concentration |
| Pipette Tips | |||
| Serological Pipettes | |||
| Sucrose | Sigma-Aldrich | S0389 | |
| Surgical Scissors | Fine Science Tools | 14002-12 | |
| SW 40 Ti Swinging-Bucket Rotor | Beckman Coulter | 331301 | |
| Teflon-Coated Pestle and Mortar Tissue Grinder | Thomas Scientific | 3431D94 | |
| Ti70 Rotor | Beckman Coulter | 337922 | |
| TLA-100.3 Rotor | Beckman Coulter | 349490 | |
| Tube Revolver | Dot Scientific | DTR-02VS |
- Kandel, E. R., Schwartz, J. H., Jessell, T. M., Siegelbaum, S. A., Hudspeth, A. J., Education, A. J. Synaptic Transmission. Principles of Neural Science, Fifth Edition. , (2014).
- Lepeta, K., et al. Synaptopathies: synaptic dysfunction in neurological disorders - A review from students to students. Journal of Neurochemistry. 138 (6), 785-805 (2016).
- Südhof, T. C., Malenka, R. C. Understanding synapses: Past, present, and future. Neuron. 60 (3), 469-476 (2008).
- Südhof, T. C. The molecular machinery of neurotransmitter release (Nobel lecture). Angewandte Chemie International Edition. 53 (47), 12696-12717 (2014).
- Jahn, R., Boyken, J., Pfaff, D. W. Molecular Regulation of Synaptic Release. Neuroscience in the 21st Century: From Basic to Clinical. , 351-401 (2013).
- Xiong, H., Gendelman, H. E. . Current Laboratory Methods in Neuroscience Research. , (2014).
- Azevedo, F. A., et al. Equal numbers of neuronal and nonneuronal cells make the human brain an isometrically scaled-up primate brain. Journal of Comparative Neurology. 513 (5), 532-541 (2009).
- Herculano-Houzel, S. The remarkable, yet not extraordinary, human brain as a scaled-up primate brain and its associated cost. Proceedings of the National Academy of Sciences of the United States of America. 109, 10661-10668 (2012).
- Herculano-Houzel, S., Lent, R. Isotropic fractionator: A simple, rapid method for the quantification of total cell and neuron numbers in the brain. Journal of Neuroscience. 25 (10), 2518-2521 (2005).
- Herculano-Houzel, S., Mota, B., Lent, R. Cellular scaling rules for rodent brains. Proceedings of the National Academy of Sciences of the United States of America. 103 (32), 12138-12143 (2006).
- Gray, E. G., Whittaker, V. P. The isolation of nerve endings from brain: An electron-microscopic study of cell fragments derived by homogenization and centrifugation. Journal of Anatomy. 96, 79-88 (1962).
- Gray, E. G., Whittaker, V. P. The isolation of synaptic vesicles from the central nervous system. Journal of Physiology. 153, 35-37 (1960).
- Whittaker, V. P. Thirty years of synaptosome research. Journal of Neurocytology. 22 (9), 735-742 (1993).
- Jahn, R., Fasshauer, D. Molecular machines governing exocytosis of synaptic vesicles. Nature. 490, 201-207 (2012).
- Whittaker, V. P., Michaelson, I. A., Kirkland, R. J. The separation of synaptic vesicles from nerve-ending particles ('synaptosomes). Biochemical Journal. 90 (2), 293-303 (1964).
- De Robertis, E., Rodriguez De Lores Arnaiz, G., Pellegrino De Iraldi, A. Isolation of synaptic vesicles from nerve endings of the rat brain. Nature. 194, 794-795 (1962).
- De Robertis, E., Pellegrino De Iraldi, A., Rodriguez, G., Gomez, C. J. On the isolation of nerve endings and synaptic vesicles. The Journal of Biophysical and Biochemical Cytology. 9 (1), 229-235 (1961).
- Zimmermann, H., Whittaker, V. P., Murphy, K. M. The Discovery of the Synaptosome and Its Implications. Synaptosomes. , 9-26 (2018).
- Gorenberg, E. L., et al. Identification of substrates of palmitoyl protein thioesterase 1 highlights roles of depalmitoylation in disulfide bond formation and synaptic function. PLoS Biology. 20 (3), 3001590 (2022).
- Vidyadhara, D. J., et al. Dopamine transporter and synaptic vesicle sorting defects initiate auxilin-linked Parkinson's disease. bioRxiv. , (2022).
- Schrimpf, S. P., et al. Proteomic analysis of synaptosomes using isotope-coded affinity tags and mass spectrometry. Proteomics. 5 (10), 2531-2541 (2005).
- Dunkley, P. R., Robinson, P. J., Murphy, K. M. Synaptosome Preparations: Which Procedure Should I Use. Synaptosomes. , 27-53 (2018).
- Nagy, A., Baker, R. R., Morris, S. J., Whittaker, V. P. The preparation and characterization of synaptic vesicles of high purity. Brain Research. 109 (2), 285-309 (1976).
- Takamori, S., et al. Molecular anatomy of a trafficking organelle. Cell. 127 (4), 831-846 (2006).
- Wagner, J. A., Kelly, R. B. Topological organization of proteins in an intracellular secretory organelle: the synaptic vesicle. Proceedings of the National Academy of Sciences of the United States of America. 76 (8), 4126-4130 (1979).
- Jahn, R., Schiebler, W., Ouimet, C., Greengard, P. A 38,000-dalton membrane protein (p38) present in synaptic vesicles. Proceedings of the National Academy of Sciences of the United States of America. 82 (12), 4137-4141 (1985).
- Binotti, B., Jahn, R., Pérez-Lara, &. #. 1. 9. 3. ;. An overview of the synaptic vesicle lipid composition. Archives of Biochemistry and Biophysics. 709, 108966 (2021).
- Siegel, D. P., Ware, B. R. Electrokinetic properties of synaptic vesicles and synaptosomal membranes. Biophysical Journal. 30 (1), 159-172 (1980).
- Whittaker, V. P., Michaelson, I. A., Kirkland, R. J. The separation of synaptic vesicles from disrupted nervending particles. Biochemical Pharmacology. 12 (3), 300-302 (1963).
- Clementi, F., Whittaker, V. P., Sheridan, M. N. The yield of synaptosomes from the cerebral cortex of guinea pigs estimated by a polystyrene bead "tagging" procedure. Zeitschrift für Zellforschung und Mikroskopische Anatomie. 72, 126-138 (1966).
- Carlson, S. S., Wagner, J. A., Kelly, R. B. Purification of synaptic vesicles from elasmobranch electric organ and the use of biophysical criteria to demonstrate purity. Biochemistry. 17 (7), 1188-1199 (1978).
- Huttner, W. B., Schiebler, W., Greengard, P., De Camilli, P. Synapsin I (protein I), a nerve terminal-specific phosphoprotein. III. Its association with synaptic vesicles studied in a highly purified synaptic vesicle preparation. Journal of Cell Biology. 96 (5), 1374-1388 (1983).
- Hawkins, P., et al. A guide to defining and implementing protocols for the welfare assessment of laboratory animals: eleventh report of the BVAAWF/FRAME/RSPCA/UFAW Joint Working Group on Refinement. Laboratory Animals. 45 (1), 1-13 (2011).
- Risling, T. E., Caulkett, N. A., Florence, D. Open-drop anesthesia for small laboratory animals. Canadian Veterinary Journal. 53 (3), 299-302 (2012).
- Deutsch, C., Drown, C., Rafalowska, U., Silver, I. A. Synaptosomes from rat brain: Morphology, compartmentation, and transmembrane pH and electrical gradients. Journal of Neurochemistry. 36 (6), 2063-2072 (1981).
- Ganzella, M., Ninov, M., Riedel, D., Jahn, R. Isolation of synaptic vesicles from mammalian brain. Methods in Molecular Biology. 2417, 131-145 (2022).
- Dunkley, P. R., et al. A rapid Percoll gradient procedure for isolation of synaptosomes directly from an S1 fraction: homogeneity and morphology of subcellular fractions. Brain Research. 441 (1-2), 59-71 (1988).
- Schwartz, R. D., Skolnick, P., Hollingsworth, E. B., Paul, S. M. Barbiturate and picrotoxin-sensitive chloride efflux in rat cerebral cortical synaptoneurosomes. FEBS Letters. 175 (1), 193-196 (1984).
- Pittaluga, A., Thellung, S., Maura, G., Raiteri, M. Characterization of two central AMPA-preferring receptors having distinct location, function and pharmacology. Naunyn-Schmiedeberg's Archives of Pharmacology. 349 (6), 555-558 (1994).
- Israël, M., Whittaker, V. P. The isolation of mossy fibre endings from the granular layer of the cerebellar cortex. Experientia. 21 (6), 325-326 (1965).
- Khvotchev, M., Lonart, G., Südhof, T. C. Role of calcium in neurotransmitter release evoked by alpha-latrotoxin or hypertonic sucrose. Neuroscience. 101 (3), 793-802 (2000).
- Lonart, G., Janz, R., Johnson, K. M., Südhof, T. C. Mechanism of action of rab3A in mossy fiber LTP. Neuron. 21 (5), 1141-1150 (1998).
- Nicholls, D. G., Sihra, T. S. Synaptosomes possess an exocytotic pool of glutamate. Nature. 321 (6072), 772-773 (1986).
- Dunkley, P. R., Jarvie, P. E., Robinson, P. J. A rapid Percoll gradient procedure for preparation of synaptosomes. Nature Protocols. 3 (11), 1718-1728 (2008).
- Cotman, C. W., Matthews, D. A. Synaptic plasma membranes from rat brain synaptosomes: Isolation and partial characterization. Biochimica et Biophysica Acta. 249 (2), 380-394 (1971).
- Booth, R. F., Clark, J. B. A rapid method for the preparation of relatively pure metabolically competent synaptosomes from rat brain. Biochemical Journal. 176 (2), 365-370 (1978).
- Takamori, S., Riedel, D., Jahn, R. Immunoisolation of GABA-specific synaptic vesicles defines a functionally distinct subset of synaptic vesicles. Journal of Neuroscience. 20 (3), 4904-4911 (2000).
- Burger, P. M., et al. Synaptic vesicles immunoisolated from rat cerebral cortex contain high levels of glutamate. Neuron. 3 (6), 715-720 (1989).
- Blondeau, F., et al. Tandem MS analysis of brain clathrin-coated vesicles reveals their critical involvement in synaptic vesicle recycling. Proceedings of the National Academy of Sciences of the United States of America. 101 (11), 3833-3838 (2004).
- Maycox, P. R., Link, E., Reetz, A., Morris, S. A., Jahn, R. Clathrin-coated vesicles in nervous tissue are involved primarily in synaptic vesicle recycling. Journal of Cell Biology. 118 (6), 1379-1388 (1992).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved