Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Neuroscience
マウス脳からのシナプス成分の単離のための細胞内分画
このプロトコルは、マウスの脳から高純度のシナプトソーム、シナプス小胞、およびその他のシナプス画分を取得するための堅牢で詳細な方法を提供します。この方法は、タンパク質の局在と機能の生化学的分析を含むシナプスプロセスのコンパートメント分解能での評価を可能にします。
シナプス終末は、ニューロンコミュニケーションの主要な部位です。シナプス機能障害は、多くの神経精神障害および神経障害の特徴です。したがって、生化学的分離によるシナプスサブコンパートメントの特性評価は、健康と疾患の両方におけるシナプスプロセスの分子基盤を解明するための強力な方法です。このプロトコルは、細胞内分画によるマウス脳からのシナプス終末およびシナプスサブコンパートメントの単離を記載する。まず、シナプトソームとして知られる密封されたシナプス末端構造は、脳組織の均質化に続いて単離されます。シナプトソームは、挟み込まれた密封された膜を有するニューロンのシナプス前およびシナプス後のコンパートメントである。これらの構造は代謝的に活性な状態を保持しており、シナプスの構造と機能を研究するために価値があります。次に、シナプトソームを低張溶解および超遠心分離にかけ、シナプス小胞、シナプス細胞質ゾル、およびシナプス原形質膜に富むシナプスサブコンパートメントを取得します。画分の純度は、サブシナプスコンパートメントに特異的なタンパク質の電子顕微鏡および生化学的濃縮分析によって確認されます。提示された方法は、シナプスの構造的および機能的特徴ならびに様々な脳障害の分子病因を研究するための簡単で貴重なツールである。
シナプスは、ニューロンが通信し、多様で絶妙に複雑な機能を発揮するための脳の基本的な計算単位です。したがって、シナプスは脳の健康の基本です1;シナプス機能障害は、多くの障害の原因または結果として関係しています2。シナプスは、シナプス前およびシナプス後終末、シナプス接着分子が横断するシナプス間隙によって密接に関連および分離された2つの異なるニューロンの拡張によって構成される。情報は、シナプス前からシナプス後のコンパートメントから、神経伝達物質1と呼ばれる化学伝達物質の形で流れます。神経伝達に関与する分子プロセスは、研究の活発な分野です3,4,5。シナプス終末内の病原性プロセスと、他のニューロンサブコンパートメントの病理に対するシナプスの応答を理解することは、脳の障害に対処するための重要なステップです1,2。主にマウスモデルに適用されるいくつかの方法論の進歩は、この追求を進めました6。差動遠心分離によるシナプス画分の単離は、健康と疾患におけるシナプスプロセスの詳細な評価を可能にしたパラダイムシフト法の1つです。
成人の人間の脳は、80〜900億個のニューロンで構成されています7,8。マウス種の中で、ラットの脳には約~2億個のニューロンが含まれていますが、マウスには~7000万個のニューロンがあります9,10。各ニューロンは、グリア細胞と密な血管系と混ざり合った高度に分極されたニューロンのネットワークと何千もの特定のシナプス接続を形成します。このような複雑で不均一な組織では、シナプスを独立したシステムとして分離して研究することはかつて考えられませんでした。1960年代に、Victor Whittaker、Catherine Hebbらは、細胞内分画を用いて無傷のシナプス終末を単離することによってこれを可能にしました11,12,13,14。シナプス小胞(SV)を単離するために、彼らは等浸透圧(0.32 M)スクロース中の液体せん断力とそれに続く超遠心分離によって脳を均質化した。彼らは、挟み込まれた原形質膜に囲まれた無傷の神経終末または静脈瘤を取得し、それを神経終末粒子(NEP)と呼んだ11,13。シナプスの構造的および機能的特徴がこれらの構造に保存されているため、NEPは後に他の細胞内オルガネラとの合同のために「シナプトソーム」と呼ばれました13,15。「シナプス小胞」という用語を作り出したEduardo de Robertisらの研究は、Whittakerらの研究と重複し、「シナプトソーム」の単離と特性評価の検証に貢献したことは注目に値します16,17,18。
シナプトソームは、神経伝達物質の貯蔵、放出、および再取り込みに必要なすべての細胞および分子特性を含む生理活性構造である13,18。in vitroでの主要なシナプス特性の保存および非シナプス成分からの解放もまた、この単離方法の有用性に寄与する。シナプトソームは、神経伝達の化学的および生理学的特性の理解に大きく貢献しており、現在、シナプス分子プロセスおよび疾患におけるそれらの変化の研究に使用されています19,20,21,22,23。シナプトソームは、SV、クラスリン被覆小胞(CCV)、シナプス細胞質ゾル、シナプス原形質膜、シナプスミトコンドリア、シナプス接着分子、およびその他の関心のある成分などのシナプス成分を単離するための最初の供給源でもあり、シナプス機能の分子メカニズムの理解を容易にすることができます18,19,20,24,25,26、27,28。これらのサブシナプス成分は、シナプトソームの浸透圧溶解およびスクロース密度勾配超遠心15、29によって得ることができる。Whittakerの研究グループによる元の細胞内分画法は、高品質のシナプトソームとSVを単離するのに効率的であることが知られていますが13,30、最近の最適化により、細胞内画分の純度が向上しています22,23,31,32。この記事では、シナプトソーム、SV、およびその他のシナプス下コンポーネントを分離するためのマウス脳組織の細胞内分画のための従来のプロトコルの非常に詳細でアクセスしやすいバージョンを提供します。
マウスを用いたすべての実験は、イェール大学の施設動物管理および使用委員会(IACUC)によって承認され(プロトコル2021-11117)、実験動物ケア国際評価認定協会(AAALAC)によって認定された施設で実施されました。動物の世話と住居は、実験動物の世話と使用のためのガイド33 に準拠し、イェール動物リソースセンター(YARC)によって提供されました。動物は、食物と水への 自由アクセス を伴う12時間の明暗サイクルで維持されました。遺伝子型または状態ごとに5〜8匹のマウスまたは2〜4匹のラットが、以下のプロトコルに必要である。脳の容積が大きいため、必要なラットは少なくなります。同様に、実験動物の年齢は分数収量に影響を与える可能性があります。2ヶ月未満の年齢には追加のマウスが必要になる場合があります。.それ以外の場合、概説された手順は、マウス種とあらゆる年齢の健康な成体動物の両方に適用されます。この研究で提示された代表的なデータは、市販の情報源から入手した野生型(C57BL / 6J)マウス(年齢= 2か月、反復あたり4人の男性と4人の女性)を利用しました( 資料表を参照)。
1. 実験準備
注:このプロトコルは、1人の研究者が完了するのに~11時間かかります。該当する場合は、プロトコル実行の前日に、ベンチトップセットアップ(図1)、バッファーの準備(表1)、遠心分離機とローターの4°Cへの予冷、および必要な材料と機器の収集とラベル付け( 材料の表を参照)を完了することを強くお勧めします。
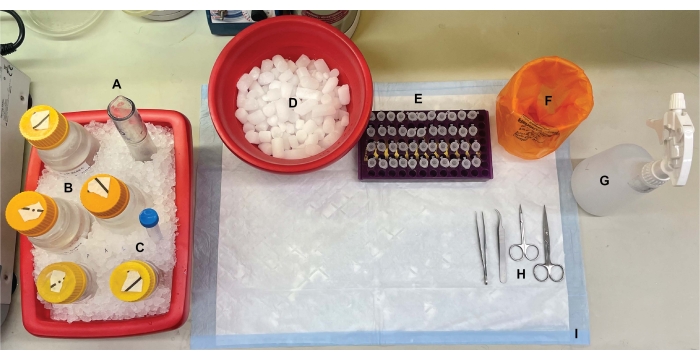
図1:ベンチトップのセットアップ。 脳解剖の前に、(A)ガラスホモジナイザーと(B)すべてのバッファーを氷上で冷やしました。(C)プロテアーゼ阻害剤原液を氷上で解凍した。遠心管用のウェットアイスの第2の容器、液体窒素のデュワー(図示せず)、および(D)液体窒素中で瞬間凍結したサンプルの短期保存用のドライアイスの容器を得た。(E)この手順中に遺伝子型または条件ごとに各細胞内画分サンプルの4つのアリコートが収集されたため、マイクロ遠心チューブはすべてのサンプルに対して事前にラベル付けされました(時間節約のヒント:実験が行われる前日にすべてのチューブに完全にラベルを付けます)。(F)適切なバイオハザード廃棄物容器、(G)70%エタノール、(H)手術器具、および(I)吸収性表面パッド。必要な遠心分離管および使い捨て品は、プロトコル実施中の効率的なアクセスのために確保された(図示せず)。 この図の拡大版を表示するには、ここをクリックしてください。
- 手術用のベンチトップを準備し、脳切除に必要なはさみと鉗子を収集します( 資料表を参照)。マウス尾部生検用の1.5 mL微量遠心チューブに事前にラベルを付け、 図2に概説されているように、採取した画分ごとに4本のチューブをラベル付けします。
- ウェットアイスの容器2つ、ドライアイスの容器1つ、およびベンチトップ液体窒素デュワーフラスコを入手します。
- フェニルメチルスルホニルフルオリド(PMSF)、ペプスタチンA、アプロチニン、およびロイペプチンストック溶液を氷上で解凍します( 材料の表を参照)。必要なバッファーを準備します (表 1)。
注:ショ糖溶液は事前に調製し、4°Cで保存することができます。 ただし、プロテアーゼ阻害剤(解凍ストックおよび錠剤)は、水溶液中でこれらの試薬が不安定であるため、実験の開始時にすべてのバッファーに新鮮に添加する必要があります。さらに、すべてのバッファーは、無傷のシナプトソームの収集を可能にするために、洗剤を含まないガラス製品と洗剤を含まない水で調製する必要があります。 - すべてのバッファーとガラスのダウンスホモジナイザー( 材料の表を参照)を氷上で冷やします。遠心分離機を4°Cに設定し、ローターを4°Cに冷却します。
- 14 mLのバッファーA(表1)を氷上のダウンスホモジナイザーに加えます。
表1:細胞内分画バッファーの組成。この表をダウンロードするには、ここをクリックしてください。
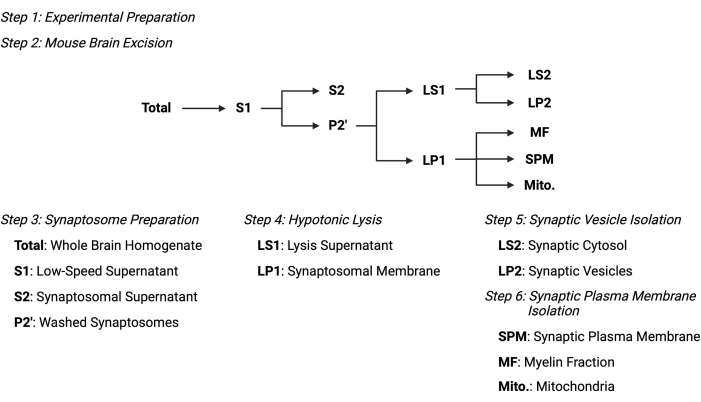
図2:細胞内分画プロトコルの概要。 細胞内分画工程および採取したサンプルの概略図。 この図の拡大版を表示するには、ここをクリックしてください。
2.マウス脳切除
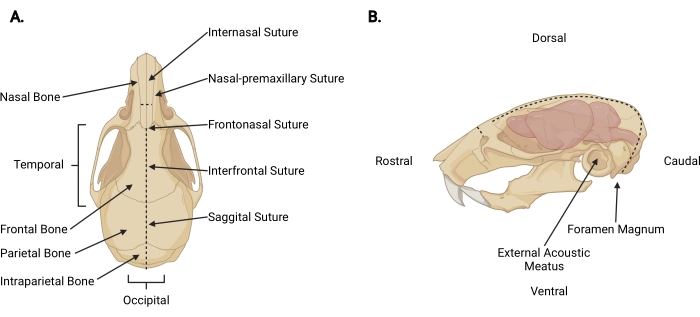
図3:頭蓋顔面解剖学 。 (A)関連する頭蓋構造が示されたマウス頭蓋骨の背側図。(B)マウスの頭蓋骨と脳の左側面図で、関連する頭蓋構造と解剖学的方向が示されています。破線は、切開を行う位置を表します。 この図の拡大版を表示するには、ここをクリックしてください。
- オープンドロップ法34を使用して、ヒュームフードまたはバイオセーフティキャビネットにある麻酔室で各マウスを100%イソフルオランで深く麻酔します。頸椎脱臼によって各マウスを犠牲にし、その後迅速に斬首します。犠牲と解剖ごとに遺伝子型または実験グループを交互に行う12.安楽死後の尾生検は、遠位尾端2 mmを細かいハサミで切除して取得します。ジェノタイピングのために組織を保管してください。
- 断頭した頭部に70%エタノールをスプレーして、解剖中に髪が組織や手術器具に付着するのを防ぎます。
- 断頭切開部で皮膚の下に細かいハサミを頭蓋周囲の深さまで挿入し、鼻間縫合糸まで矢状中切開を行い(図3A)、頭皮を頭蓋骨から引っ込めます。
- 後頭部から各側頭に向かって作業し、筋膜と筋肉をトリミングして、各外部音響口を越えて頭蓋骨の外面を露出させます(図3B)。
- 利き手ではない手で頭蓋骨の頭皮と吻側の側面を固定します。もう一方では、脊髄が出ているのが見える大孔の尾側に2 mmの細かいはさみを挿入します。はさみが頭頂内骨の内面に到達するまで正中線を切開します(図3;破線)。
注:最初の切開時には、脳幹と小脳の損傷を防ぐために、はさみが脊髄と平行で、頭蓋骨の内面に向かって圧力がかかる必要があります。 - はさみの角度を変更して、ブレードが頭蓋骨の背側表面と平行になるようにします。矢状縫合糸と前頭間縫合糸をガイドとして使用して、頭頂骨と前頭骨を通して吻側方向に矢状切開を進み続けます。皮質への損傷を避けるために一定の上向きの圧力を使用してください。鼻間縫合糸のすぐ向こうの切開を終了します(図3A)。
- 鼻骨に小さな垂直切開(~3 mm)、鼻間縫合糸に対して吻側を、はさみを頭蓋骨に垂直に配置し、各ブレードを鼻上顎前縫合に配置し、1つを均等に切断します(図3;破線)。
注:この手順により、頭蓋骨の収縮が容易になり、この領域が関心のある場合は嗅球を収集するために重要になります。 - 吻側を固定しながら、テクスチャー加工された鉗子の片側を使用して、頭蓋骨を脳からゆっくりと持ち上げ、次に横方向と腹側に持ち上げます。必要に応じて正中線に沿って繰り返し、次に脳表面全体が露出するまでもう一方の半球についても繰り返します。
- 湾曲した鉗子または細いへらを使用して、脳の吻側をそっと持ち上げます。視神経と脳神経を切断して、頭蓋骨からの切除を完了します。
- 各条件について、5〜8匹のマウスの脳を一緒に14 mLのバッファーAを含むチルドグラスDounceホモジナイザーに集めます(表1)。
3.シナプトソームの準備
メモ: この手順の回路図を 図 4 に示します。
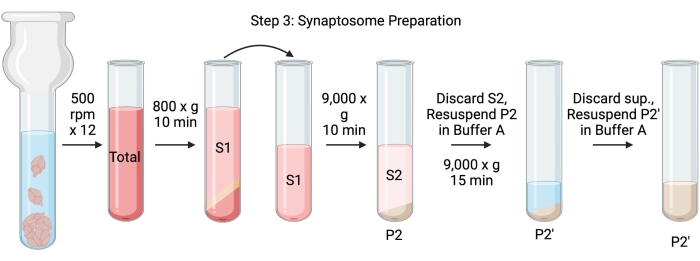
図4:シナプトソーム調製。 工程3の概略図は、シナプトソーム(P2 ́)の生成である。 この図の拡大版を表示するには、ここをクリックしてください。
- ガラスDounceホモジナイザーを使用して、500rpm(合計)で12回のアップダウンパスで脳を均質化します。各ダウンストロークで短時間一時停止して、組織の完全な均質化を確実にします。加温やタンパク質の変性を避けるために、氷浴中で優先的に均質化します。ビシンコニン酸アッセイによるタンパク質濃度測定のために5 μLのアリコートを取ります(BCA、 材料表を参照)。ウェスタンブロット(WB)のために100 μLの全脳ライセートアリコートを取ります。このサンプルとそれに続くすべてのサンプル(図2)について、BCAには2つのアリコート、WBには2つのアリコートを取ります。採取したすべてのアリコートを液体窒素でフラッシュ凍結し、-80°Cで保存します。
- 全脳ホモジネートを高速丸底遠沈管(14mL)中で800 x gで4°Cで10分間回転させ、上清(S1)を得た。S1を新しい遠心チューブに移し、無傷の細胞と核を含むペレット(P1)を残します。ふわふわの、白い、ゆるい、表面的なペレットをピペッティングすることは避けてください。BCAの場合は2 x 5 μLのS1を、WBの場合は2 x 100 μLのS1を取ります。
- S1を9,000 x g で4°Cで15分間スピンし、シナプトソーム上清(S2)および粗シナプトソームペレット(P2)を得た。BCAの場合は10 μLのS2を2 x、WBの場合はS2の500 μLを2 x 2します。アリコートを得た後、上清を捨て、ペレットで次のステップに進みます。
- P2をプロテアーゼ阻害剤を含む3 mLの氷冷バッファーAに再懸濁し、9,000 x g で4°Cで15分間遠心分離して、上清(S2')と洗浄シナプトソーム(P2')を得ました。上清を捨て、ペレットを保管してください。
- P2'を3 mLのバッファーAに再懸濁します。 主にミトコンドリアを含むペレットの底にある暗赤色の部分を再懸濁しないでください。BCAの場合は20 μLのP2'を2 x、WBの場合はP2 'を2 x 100 μL取ります。
注:これは、ペレットの端と表面を穏やかにピペット混合して、ピペットチップをペレットの赤い中心から遠ざけながら、白く洗浄されたシナプトソームを再懸濁することによって達成できます。
4.低張性溶解
メモ: この手順の回路図を 図 5 に示します。
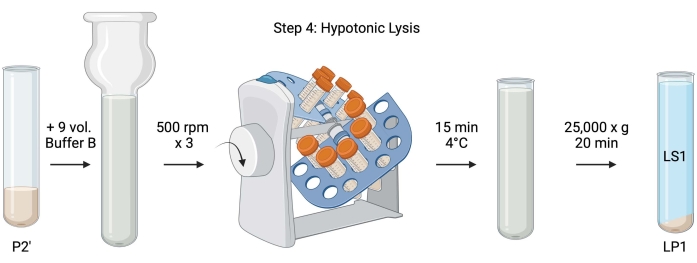
図5:低張性溶解。 工程4の概略図は、シナプトソームの低張溶解により、溶解上清(LS1)およびシナプトソーム膜画分(LP1)を生成する。 この図の拡大版を表示するには、ここをクリックしてください。
- 洗浄したシナプトソームの低張溶解のために、9容量の冷やしたバッファーB(表1)を再懸濁したP2'(~27 mL)に加えます。シナプトソームをガラス製ダウンスホモジナイザーでホモジナイズします(500 rpmで3回のアップダウンパス)。
- サンプルを50 mLキャップ付きコニカル遠心チューブに移します。4°Cの冷蔵室でチューブリボルバーで15分間回転させます。
- 遠心分離機はP2 'を25,000 x gで4°Cで20分間溶解し、溶解上清(LS1)およびシナプトソーム膜を含む溶解ペレット(LP1)を得た。BCAの場合はLS1を2 x 50 μL、WBの場合はLS1を2 x 400 μL服用します。LS1を超遠心分離用のキャップ付き遠沈管に移します(材料表を参照)。
5.シナプス小胞の分離
メモ: この手順の回路図を 図 6 に示します。
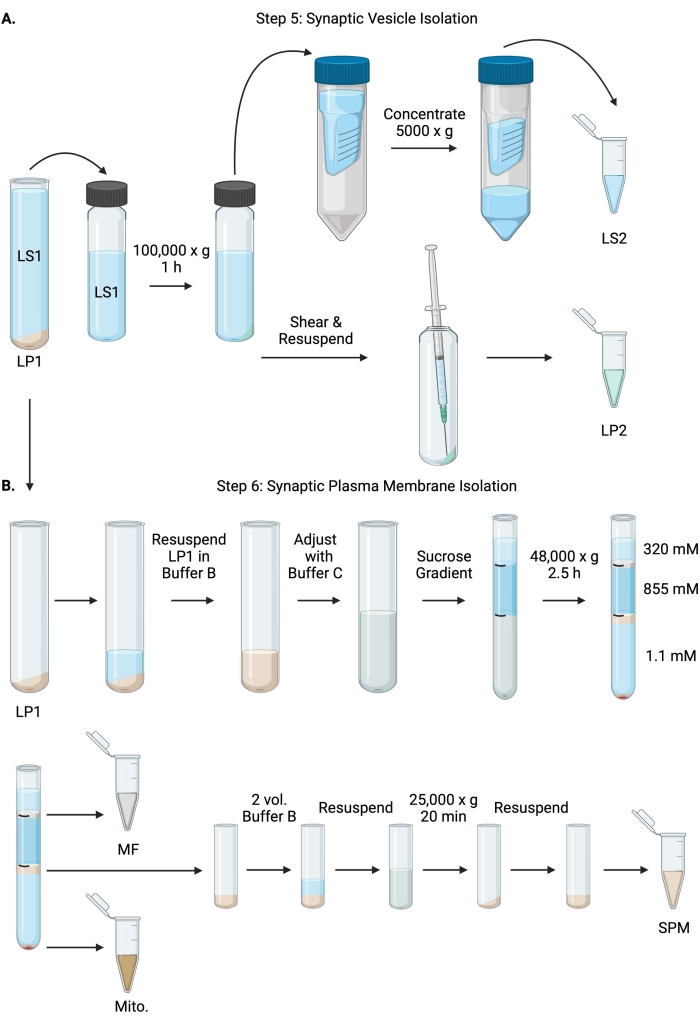
図6:シナプス小胞の単離とシナプス原形質膜の単離。 (A)工程5の概略図、シナプス細胞質ゾル(LS2)およびシナプス小胞(LP2)画分の単離、および(B)工程6、スクロース勾配の超遠心分離後のミエリン(MF)、シナプス原形質膜(SPM)、およびミトコンドリア(Mito.)画分の生成。この図の拡大版を表示するには、ここをクリックしてください。
- LS1を固定角度超遠心ローター( 材料の表を参照)で100,000 x g で4°Cで60分間遠心分離し、シナプス細胞質ゾル上清(LS2)およびシナプス小胞ペレット(LP2)を得た。LP2は小さく、半透明で、遠心管の側面に強く付着します。
- LP2を500 μLのバッファーAに再懸濁します。 23 Gの針と1 mLのシリンジを使用して、穏やかな粉砕でLP2をせん断します。BCAの場合は10 μLのLP2を2 x、WBにはLP2 x 250 μLを取ります。
- LS2(~30 mL)を10 kDaカットオフの遠心フィルターユニットに移します(材料表を参照)。
注:10 kDa未満のタンパク質が対象である場合は、4 kDaカットオフ遠心フィルターユニットを使用できますが、スピン時間が長くなります。 - LS2を5000 x g で4°Cで最大1時間回転させて、LS2を約0.5 mLまで濃縮します。 BCAには10 μLの濃縮LS2を2 x、WBには2 x 250 μLの濃縮LS2を取ります。スピンを開始したら、手順6.1に直接進みます。
6. シナプス原形質膜分離
- LP1を1 mLのバッファーBに再懸濁します(ステップ4.3)(表1)。BCAには10 μLのLP1を2 x、WBにはLP1のLP1を2 x 50 μL摂取します。残りのLP1をバッファーBとバッファーCを使用して、最終容量7.5 mL、最終スクロース濃度1.1 Mに調整します(表1)。
- 再懸濁したLP17.5 mLを14 mL超遠心チューブに移します( 材料の表を参照)。LP1を3.75 mLのバッファーD(表1)で注意深く重ね合わせ、次に1.25 mLのバッファーA(または遠心管の上部のすぐ下に充填する大容量)を重層します。チューブの側面をピペッティングすると、スクロースグラジエント界面が乱れます。各スクロース画分を重ねた後、溶液の上部にペンで印を付けます。超遠心用のチューブを容量ではなく重量でバランスを取り、バッファーAを10 mg以内に滴下します。スイングバケット超遠心ローターで4°Cで2.5時間、48,000 x g で遠心分離します( 材料の表を参照)。
- 超遠心分離後のインタクトグラジエントの画像を取得して、各スクロース界面の区別と分画の成功を文書化します。
- 320 mMスクロース(バッファーA)の表面層を慎重に除去します。320 mM/855 mMのスクロース界面のミエリン画分(MF)を800 μLの容量で回収します。855 mM/1.1 Mショ糖界面のシナプス原形質膜(SPM)画分を1,000 μLの容量で回収します。各フラクションをチューブの壁から円形にピペットで持ち上げて、完全なフラクションを確実に収集します。残ったスクロースを注意深く吸引し、200 μLのバッファーBに再懸濁してミトコンドリアペレット(水戸)を回収します。BCAの場合はMFを2 x 100 μL、水戸の場合は2 x 10 μLを取ります。BCAの場合;MFと水戸の残りを分ける。WB用に半分のサンプル。
- SPM画分を2容量のバッファーB(~2 mL)で希釈し、3.5 mL遠心チューブ( 材料表を参照)の固定角度ローターで25,000 x g で4°Cで20分間遠心分離します。 上清を廃棄し、SPMペレットをバッファーAに再懸濁して、最終容量250 μLにします。BCA用に2 x 5 μLのSPMを取り、残りのSPMをWB用に半分に分割します。
- BCAを実行して、可変アリコート量を考慮して各サンプルのタンパク質濃度を決定します。
注:WB分析の場合、すべての細胞内画分の推奨作動タンパク質濃度は2 μg/μL(またはLS1およびMFで達成可能な高さ)です。
提示された方法は、さらなる精製および様々な形態の下流分析に供することができる11の脳内細胞画分をもたらす35、36。シナプトソーム、SV23、およびその他の成分の品質を評価するためのゴールドスタンダードの方法は、電子顕微鏡(EM)です(図7)。特定の細胞内画分に存在するタンパク質の定量的イムノブロッティングも、画分純度のマーカーを評価するために実施できます(図8)。例えば、画分のイムノブロット分析では、シナプス原形質膜画分(SPM)中のN-カドヘリン(CDH2、UniProt名)、シナプス細胞質ゾル(LS2)中のα-シヌクレイン(SYUA)、シナプス小胞画分(LP2)中のシナプトフィジン(SYPH)、およびミエリン画分(MF)中のミエリン塩基性タンパク質(MBP)の富化が、初期の全脳ホモジネート(Total)のタンパク質レベルと比較すると明らかになりました(図8).画分の純度が確立されたら(例えば、LS2画分にCDH2が存在しないこと、またはLP2画分にSYPHが何倍にも増加することに注目)、定量的イムノブロッティングを使用して、目的のタンパク質の局在を決定したり、遺伝子型または処理間のタンパク質分布の違いを調べたりすることができます。シナプスタンパク質の細胞内局在を理解することで、これまで記載されていなかったタンパク質機能の解剖が可能になります。さらに、この方法は、特に機能アッセイと組み合わせた場合に、疾患状態における人身売買欠陥またはシナプス機能障害を解明し得る。たとえば、私たちのチームはこの方法を使用して、シナプス細胞質ゾル19に富む酵素的に活性なパルミトイルタンパク質チオエステラーゼ1のプールを特定しました。
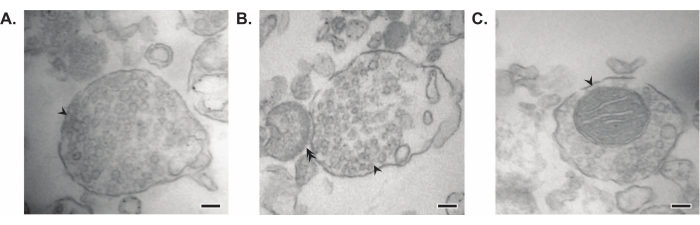
図7:シナプトソームの電子顕微鏡(EM )。 (A)シナプス小胞を含むシナプトソームの代表的なEM像(矢印)。(B)シナプス前(矢印)とシナプス後の両方を含むシナプトソームの代表的なEM画像(二重矢印)。(C)シナプス小胞とミトコンドリアを含むシナプトソームの代表的なEM像(矢印)(スケールバー=100nm)。 この図の拡大版を表示するには、ここをクリックしてください。
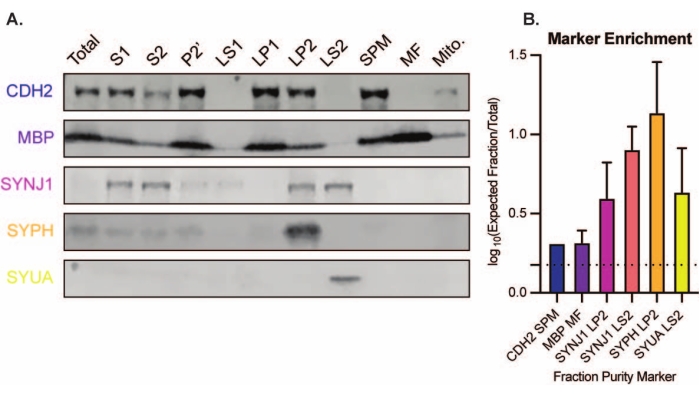
図8:細胞内画分のイムノブロット分析。 (A)細胞内画分純度のマーカー(UniProt命名法で示される)は、全脳ホモジネート(総量)と比較して適切に局在している:シナプス原形質膜画分(SPM)中のN-カドヘリン(CDH2)、シナプス小胞濃縮画分(LP2)中のシナプトフィジン1(SYPH)およびシナプトジャニン1(SYNJ1)、シナプス細胞質ゾル(LS2)中のα-シヌクレイン(SYUA)、 ミエリン画分(MF)中のミエリン塩基性タンパク質(MBP)。(B)イムノブロット定量分析により、画分純度マーカーの濃縮(合計からの倍率変化)が明らかになります。データは、log10スケールの平均値±標準偏差として表されます。点線は1.5倍の変化(y = 0.176)を示す(n = 8匹の野生型マウスを用いた3回の反復実験;齢= 2ヶ月;SYPH、SYUA、MBPについてはn = 4-5ブロット、n = 3プロット値はGorenbergらによって以前に発表された19;n = 5はSYNJ1;n = 1はCDH2)。 この図の拡大版を表示するには、ここをクリックしてください。
彼らの独創的な研究において、Whittakerと同僚はシナプトソームを特定するために4つの形態学的基準を使用しました:(1)構造は密封された原形質膜を持っています。(2)構造には、神経終末および静脈瘤のサイズと数に類似したSVが含まれています。(3)前記構造体は、1つ以上の小さなミトコンドリアを有し、(4)シナプス前膜は、シナプス後成分11、12、13に頻繁に接着される。最初の2つの基準は一般的にすべての単離方法に適用されますが、この記事で説明されている最新のプロトコルでは、結果として生じるすべてのシナプトソームがミトコンドリアとシナプス後末端を結合するわけではありません。シナプトソームの約60%がミトコンドリアを有し、シナプス後終末を付着していると推定されるのは最大15%のみである37。シナプス後成分が特に興味深い場合、濃縮のための等張クレブス様ホモジナイゼーションバッファーと圧力ろ過の使用は、シナプス後末端を有する高濃度のシナプトソーム(シナプトニューロソームとも呼ばれる)を生成することが知られています22,38。
動物を犠牲にする方法は、シナプトソームおよびシナプス亜分画の質に影響を与える可能性がある。麻酔を必要としない安楽死法を使用して犠牲にされた成体動物は、最高の画分品質をもたらします。さらに、脳は凍結ではなく新たに解剖し、最も生存可能なシナプス画分に対して1:10の比率のホモジナイズバッファー(重量/体積)を使用してホモジナイズする必要があります22。脳には、それらが運ぶ神経伝達物質の種類によって区別できるシナプスの不均一な集団があります。シナプトソーム形成は、一般に、シナプス型または神経伝達物質含量の影響を受けない13。例外は小脳の苔状線維であり、これは脳の残りの部分からシナプトソームを得るための最適な条件で破壊されることが知られている39,40。したがって、この領域の除外が実験目標に影響を及ぼさない場合は、脳の均質化の前に小脳を除去することが推奨されます。特定の神経伝達物質特性のシナプトソームを単離することに関心がある場合、関心のある神経伝達物質を含むニューロンに富む脳の領域を最初に単離することができる。ただし、このアプローチでは、関心領域のサイズに応じて、最終的な分数収量に制限が課されます(したがって、動物の年齢も考慮されます)。神経伝達物質特異的シナプトソームの単離には免疫化学的方法がありますが、生存率と収量は著しく損なわれます22。シナプトソーム代謝生存率を評価することが重要である場合、神経伝達物質放出の測定41、42またはある種の酵素アッセイ43が採用され得る。
シナプトソーム調製物中の一般的な汚染物質には、ミクロソーム、遊離ミトコンドリア、SV、ならびにニューロンおよびグリア膜が含まれる。汚染は、P1およびP2画分22での洗浄回数を増やし、後続のステップでの赤いミトコンドリアペレットの再懸濁を回避することによって減らすことができます。代謝生存率と時間が重要な実験では、洗浄回数を減らし、スクロース勾配よりもFicollまたはPercoll勾配を使用することが役立ちます44,45,46。これらの方法はまた汚染を大幅に減らします。ウィテカーの元のプロトコルは、高品質のSVを生み出しました。この方法に含まれるNagyら23によるさらなる最適化は、歩留まりを大幅に損なうことなく、驚くべき均質性と純度を持つSVを生成します36。グルタミン酸作動性(VGLUT-1含有)またはGABA作動性(VGAT-1含有)SVなどの特定のSVサブタイプが対象である場合、特異的抗体を用いた免疫単離を行うことができる47,48。CCVをシナプトソームから単離するための代替方法も利用可能であり、シナプトソームは密度が異なるため、この方法20,49,50で得られたSVと同じ界面に存在しない可能性がある。
全体として、シナプス成分を単離するための本プロトコールは、ソース脳組織の質および量および実験目標に基づいて、改善された均質性および生存率を有する画分を得るためにさらに最適化され得る。トラブルシューティングの詳細については、Dunkley and Robinson22 および Ganzella et al.36 の書籍の章を参照してください。
著者は開示するものは何もありません。
EM画像の準備をしてくれたP.コロシに感謝します。この研究は、国立衛生研究所(R01 NS064963、SSC;R01 NS110354, SSC;R01 NS083846, SSC;R21 NS094971, SSC;T32 NS007224、SMT;T32 NS041228、SMT)、米国国防総省(W81XWH-17-1-0564、SSC;W81XWH-19-1-0264, VDJ), Aligning Science Across Parkinson's (ASAP) Collaborative Research Network (SSC), and the Michael J. Fox Foundation Target Advancement Program (MJFF-020160, SSC & VDJ).BioRender.com を使用してグラフィカルなイラストを作成しました。
| Name | Company | Catalog Number | Comments |
| 1 mL TB Syringe | BD | 309649 | |
| 1.5 mL Eppendorf Tubes | USA Scientific | 1415-2500 | |
| 14 mL, Open-Top Thinwall Ultra-Clear Tube | Beckman Coulter | 344060 | Compatible with SW 40 Ti |
| 23 Gauge Precision Glide Hypodermic Needle | BD | 305145 | |
| 26.3 mL, Polycarbonate Bottle with Cap Assembly | Beckman Coulter | 355618 | Compatible with Ti70 |
| 3.5 mL, Open-Top Thickwall Polypropylene Tube | Beckman Coulter | 349623 | Compatible with TLA-100.3 |
| 50 mL Falcon Tubes | Fisher Scientific | 14-432-22 | |
| Amicon Ultra-15 Centrifugal Filter Unit | Millipore Sigma | UFC901024 | |
| Aprotinin | Sigma-Aldrich | A6279 | 1 mg/mL in diH2O |
| Avanti J-26 XP Centrifuge | Beckman Coulter | B22984 | <26,000 rpm |
| Benchtop HDPE Dewar Flask | Thermo Scientific | 5028U19 | |
| C57BL/6J Mice | The Jackson Labs | 000664 | |
| Centrifuge 5810R | Eppendorf | EP022628168 | <14,000 rpm |
| complete, Mini, EDTA-free Protease Inhibitor Cocktail Tablets | Roche | 11873580001 | Add 1 tablet per 50 mL of solution |
| Curved Forceps | Fine Science Tools | 11273-20 | |
| Fine Surgical Scissors | Fine Science Tools | 8r | |
| Glas-Col Tissue Homogenizing System | Cole-Parmer | UX-04369-15 | |
| Graefe Forceps | Fine Science Tools | 11650-10 | |
| High-Speed Polycarbonate Round Bottom Centrifuge Tubes | ThermoFisher | 3117-0500 | Compatible with JA20 |
| Isofluorane | Henry Schein Animal Health | NDC 11695-6776-2 | |
| JA-20 Rotor | Beckman Coulter | 334831 | |
| Leupeptin | American Bio | AB01108 | 1 mg/mL in diH2O |
| N-[2-Hydroxyethyl] piperazine-N’-[2-ethanesulfonic acid] (HEPES) | American Bio | AB00892 | |
| Optima L-80 XP Ultracentrifuge | Beckman Coulter | <100,000 rpm | |
| Optima TLX Ultracentrifuge | Beckman Coulter | <120,000 rpm | |
| Pepstatin A | Thermo Scientific | 78436 | 1 mg/mL in DMSO |
| Phenylmethylsulfonyl fluoride (PMSF) | American Bio | AB01620 | |
| Pierce BCA Protein Assay Kit | Thermo Scientific | 23335 | For determination of protein concentration |
| Pipette Tips | |||
| Serological Pipettes | |||
| Sucrose | Sigma-Aldrich | S0389 | |
| Surgical Scissors | Fine Science Tools | 14002-12 | |
| SW 40 Ti Swinging-Bucket Rotor | Beckman Coulter | 331301 | |
| Teflon-Coated Pestle and Mortar Tissue Grinder | Thomas Scientific | 3431D94 | |
| Ti70 Rotor | Beckman Coulter | 337922 | |
| TLA-100.3 Rotor | Beckman Coulter | 349490 | |
| Tube Revolver | Dot Scientific | DTR-02VS |
- Kandel, E. R., Schwartz, J. H., Jessell, T. M., Siegelbaum, S. A., Hudspeth, A. J., Education, A. J. Synaptic Transmission. Principles of Neural Science, Fifth Edition. , (2014).
- Lepeta, K., et al. Synaptopathies: synaptic dysfunction in neurological disorders - A review from students to students. Journal of Neurochemistry. 138 (6), 785-805 (2016).
- Südhof, T. C., Malenka, R. C. Understanding synapses: Past, present, and future. Neuron. 60 (3), 469-476 (2008).
- Südhof, T. C. The molecular machinery of neurotransmitter release (Nobel lecture). Angewandte Chemie International Edition. 53 (47), 12696-12717 (2014).
- Jahn, R., Boyken, J., Pfaff, D. W. Molecular Regulation of Synaptic Release. Neuroscience in the 21st Century: From Basic to Clinical. , 351-401 (2013).
- Xiong, H., Gendelman, H. E. . Current Laboratory Methods in Neuroscience Research. , (2014).
- Azevedo, F. A., et al. Equal numbers of neuronal and nonneuronal cells make the human brain an isometrically scaled-up primate brain. Journal of Comparative Neurology. 513 (5), 532-541 (2009).
- Herculano-Houzel, S. The remarkable, yet not extraordinary, human brain as a scaled-up primate brain and its associated cost. Proceedings of the National Academy of Sciences of the United States of America. 109, 10661-10668 (2012).
- Herculano-Houzel, S., Lent, R. Isotropic fractionator: A simple, rapid method for the quantification of total cell and neuron numbers in the brain. Journal of Neuroscience. 25 (10), 2518-2521 (2005).
- Herculano-Houzel, S., Mota, B., Lent, R. Cellular scaling rules for rodent brains. Proceedings of the National Academy of Sciences of the United States of America. 103 (32), 12138-12143 (2006).
- Gray, E. G., Whittaker, V. P. The isolation of nerve endings from brain: An electron-microscopic study of cell fragments derived by homogenization and centrifugation. Journal of Anatomy. 96, 79-88 (1962).
- Gray, E. G., Whittaker, V. P. The isolation of synaptic vesicles from the central nervous system. Journal of Physiology. 153, 35-37 (1960).
- Whittaker, V. P. Thirty years of synaptosome research. Journal of Neurocytology. 22 (9), 735-742 (1993).
- Jahn, R., Fasshauer, D. Molecular machines governing exocytosis of synaptic vesicles. Nature. 490, 201-207 (2012).
- Whittaker, V. P., Michaelson, I. A., Kirkland, R. J. The separation of synaptic vesicles from nerve-ending particles ('synaptosomes). Biochemical Journal. 90 (2), 293-303 (1964).
- De Robertis, E., Rodriguez De Lores Arnaiz, G., Pellegrino De Iraldi, A. Isolation of synaptic vesicles from nerve endings of the rat brain. Nature. 194, 794-795 (1962).
- De Robertis, E., Pellegrino De Iraldi, A., Rodriguez, G., Gomez, C. J. On the isolation of nerve endings and synaptic vesicles. The Journal of Biophysical and Biochemical Cytology. 9 (1), 229-235 (1961).
- Zimmermann, H., Whittaker, V. P., Murphy, K. M. The Discovery of the Synaptosome and Its Implications. Synaptosomes. , 9-26 (2018).
- Gorenberg, E. L., et al. Identification of substrates of palmitoyl protein thioesterase 1 highlights roles of depalmitoylation in disulfide bond formation and synaptic function. PLoS Biology. 20 (3), 3001590 (2022).
- Vidyadhara, D. J., et al. Dopamine transporter and synaptic vesicle sorting defects initiate auxilin-linked Parkinson's disease. bioRxiv. , (2022).
- Schrimpf, S. P., et al. Proteomic analysis of synaptosomes using isotope-coded affinity tags and mass spectrometry. Proteomics. 5 (10), 2531-2541 (2005).
- Dunkley, P. R., Robinson, P. J., Murphy, K. M. Synaptosome Preparations: Which Procedure Should I Use. Synaptosomes. , 27-53 (2018).
- Nagy, A., Baker, R. R., Morris, S. J., Whittaker, V. P. The preparation and characterization of synaptic vesicles of high purity. Brain Research. 109 (2), 285-309 (1976).
- Takamori, S., et al. Molecular anatomy of a trafficking organelle. Cell. 127 (4), 831-846 (2006).
- Wagner, J. A., Kelly, R. B. Topological organization of proteins in an intracellular secretory organelle: the synaptic vesicle. Proceedings of the National Academy of Sciences of the United States of America. 76 (8), 4126-4130 (1979).
- Jahn, R., Schiebler, W., Ouimet, C., Greengard, P. A 38,000-dalton membrane protein (p38) present in synaptic vesicles. Proceedings of the National Academy of Sciences of the United States of America. 82 (12), 4137-4141 (1985).
- Binotti, B., Jahn, R., Pérez-Lara, &. #. 1. 9. 3. ;. An overview of the synaptic vesicle lipid composition. Archives of Biochemistry and Biophysics. 709, 108966 (2021).
- Siegel, D. P., Ware, B. R. Electrokinetic properties of synaptic vesicles and synaptosomal membranes. Biophysical Journal. 30 (1), 159-172 (1980).
- Whittaker, V. P., Michaelson, I. A., Kirkland, R. J. The separation of synaptic vesicles from disrupted nervending particles. Biochemical Pharmacology. 12 (3), 300-302 (1963).
- Clementi, F., Whittaker, V. P., Sheridan, M. N. The yield of synaptosomes from the cerebral cortex of guinea pigs estimated by a polystyrene bead "tagging" procedure. Zeitschrift für Zellforschung und Mikroskopische Anatomie. 72, 126-138 (1966).
- Carlson, S. S., Wagner, J. A., Kelly, R. B. Purification of synaptic vesicles from elasmobranch electric organ and the use of biophysical criteria to demonstrate purity. Biochemistry. 17 (7), 1188-1199 (1978).
- Huttner, W. B., Schiebler, W., Greengard, P., De Camilli, P. Synapsin I (protein I), a nerve terminal-specific phosphoprotein. III. Its association with synaptic vesicles studied in a highly purified synaptic vesicle preparation. Journal of Cell Biology. 96 (5), 1374-1388 (1983).
- Hawkins, P., et al. A guide to defining and implementing protocols for the welfare assessment of laboratory animals: eleventh report of the BVAAWF/FRAME/RSPCA/UFAW Joint Working Group on Refinement. Laboratory Animals. 45 (1), 1-13 (2011).
- Risling, T. E., Caulkett, N. A., Florence, D. Open-drop anesthesia for small laboratory animals. Canadian Veterinary Journal. 53 (3), 299-302 (2012).
- Deutsch, C., Drown, C., Rafalowska, U., Silver, I. A. Synaptosomes from rat brain: Morphology, compartmentation, and transmembrane pH and electrical gradients. Journal of Neurochemistry. 36 (6), 2063-2072 (1981).
- Ganzella, M., Ninov, M., Riedel, D., Jahn, R. Isolation of synaptic vesicles from mammalian brain. Methods in Molecular Biology. 2417, 131-145 (2022).
- Dunkley, P. R., et al. A rapid Percoll gradient procedure for isolation of synaptosomes directly from an S1 fraction: homogeneity and morphology of subcellular fractions. Brain Research. 441 (1-2), 59-71 (1988).
- Schwartz, R. D., Skolnick, P., Hollingsworth, E. B., Paul, S. M. Barbiturate and picrotoxin-sensitive chloride efflux in rat cerebral cortical synaptoneurosomes. FEBS Letters. 175 (1), 193-196 (1984).
- Pittaluga, A., Thellung, S., Maura, G., Raiteri, M. Characterization of two central AMPA-preferring receptors having distinct location, function and pharmacology. Naunyn-Schmiedeberg's Archives of Pharmacology. 349 (6), 555-558 (1994).
- Israël, M., Whittaker, V. P. The isolation of mossy fibre endings from the granular layer of the cerebellar cortex. Experientia. 21 (6), 325-326 (1965).
- Khvotchev, M., Lonart, G., Südhof, T. C. Role of calcium in neurotransmitter release evoked by alpha-latrotoxin or hypertonic sucrose. Neuroscience. 101 (3), 793-802 (2000).
- Lonart, G., Janz, R., Johnson, K. M., Südhof, T. C. Mechanism of action of rab3A in mossy fiber LTP. Neuron. 21 (5), 1141-1150 (1998).
- Nicholls, D. G., Sihra, T. S. Synaptosomes possess an exocytotic pool of glutamate. Nature. 321 (6072), 772-773 (1986).
- Dunkley, P. R., Jarvie, P. E., Robinson, P. J. A rapid Percoll gradient procedure for preparation of synaptosomes. Nature Protocols. 3 (11), 1718-1728 (2008).
- Cotman, C. W., Matthews, D. A. Synaptic plasma membranes from rat brain synaptosomes: Isolation and partial characterization. Biochimica et Biophysica Acta. 249 (2), 380-394 (1971).
- Booth, R. F., Clark, J. B. A rapid method for the preparation of relatively pure metabolically competent synaptosomes from rat brain. Biochemical Journal. 176 (2), 365-370 (1978).
- Takamori, S., Riedel, D., Jahn, R. Immunoisolation of GABA-specific synaptic vesicles defines a functionally distinct subset of synaptic vesicles. Journal of Neuroscience. 20 (3), 4904-4911 (2000).
- Burger, P. M., et al. Synaptic vesicles immunoisolated from rat cerebral cortex contain high levels of glutamate. Neuron. 3 (6), 715-720 (1989).
- Blondeau, F., et al. Tandem MS analysis of brain clathrin-coated vesicles reveals their critical involvement in synaptic vesicle recycling. Proceedings of the National Academy of Sciences of the United States of America. 101 (11), 3833-3838 (2004).
- Maycox, P. R., Link, E., Reetz, A., Morris, S. A., Jahn, R. Clathrin-coated vesicles in nervous tissue are involved primarily in synaptic vesicle recycling. Journal of Cell Biology. 118 (6), 1379-1388 (1992).
Tags
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved