Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Neuroscience
Fraccionamiento subcelular para el aislamiento de componentes sinápticos del cerebro murino
Este protocolo presenta un método robusto y detallado para obtener sinaptosomas altamente puros, vesículas sinápticas y otras fracciones sinápticas del cerebro del ratón. Este método permite la evaluación de procesos sinápticos, incluyendo el análisis bioquímico de la localización y función de proteínas con resolución compartimental.
Los terminales sinápticos son los sitios primarios de la comunicación neuronal. La disfunción sináptica es un sello distintivo de muchos trastornos neuropsiquiátricos y neurológicos. La caracterización de subcompartimentos sinápticos mediante aislamiento bioquímico es, por tanto, un potente método para dilucidar las bases moleculares de los procesos sinápticos, tanto en la salud como en la enfermedad. Este protocolo describe el aislamiento de terminales sinápticas y subcompartimentos sinápticos de cerebros de ratones mediante fraccionamiento subcelular. Primero, las estructuras terminales sinápticas selladas, conocidas como sinaptosomas, se aíslan después de la homogeneización del tejido cerebral. Los sinaptosomas son compartimentos neuronales pre y postsinápticos con membranas pellizcadas y selladas. Estas estructuras conservan un estado metabólicamente activo y son valiosas para estudiar la estructura y función sináptica. Los sinaptosomas se someten a lisis hipotónica y ultracentrifugación para obtener subcompartimentos sinápticos enriquecidos para vesículas sinápticas, citosol sináptico y membrana plasmática sináptica. La pureza de la fracción se confirma mediante microscopía electrónica y análisis de enriquecimiento bioquímico para proteínas específicas de compartimentos subsinápticos. El método presentado es una herramienta sencilla y valiosa para estudiar las características estructurales y funcionales de la sinapsis y la etiología molecular de diversos trastornos cerebrales.
Las sinapsis son las unidades computacionales básicas del cerebro a través de las cuales las neuronas se comunican y ejercen funciones diversas y exquisitamente complejas. Las sinapsis son, por lo tanto, fundamentales para la salud del cerebro1; La disfunción sináptica está implicada como fuente o resultado de muchos trastornos2. Las sinapsis están constituidas por terminales pre y postsinápticas, extensiones de dos neuronas diferentes que están estrechamente apostadas y separadas por una hendidura sináptica atravesada por moléculas de adhesión sináptica. La información fluye desde el compartimento pre a post-sináptico en forma de mensajeros químicos llamados neurotransmisores1. Los procesos moleculares implicados en la neurotransmisión son áreas activas de investigación 3,4,5. La comprensión de los procesos patogénicos dentro de las terminales sinápticas y la respuesta de las sinapsis a la patología en otros subcompartimentos neuronales son pasos cruciales para abordar los trastornos del cerebro 1,2. Varios avances metodológicos, predominantemente aplicados a modelos murinos, han avanzado en esta búsqueda6. El aislamiento de fracciones sinápticas por centrifugación diferencial es uno de esos métodos de cambio de paradigma que ha permitido la evaluación detallada de los procesos sinápticos en la salud y la enfermedad.
El cerebro humano adulto consta de 80-90 mil millones de neuronas 7,8. Entre las especies murinas, el cerebro de la rata contiene aproximadamente ~ 200 millones de neuronas, mientras que los ratones tienen ~ 70 millones 9,10. Cada neurona forma miles de conexiones sinápticas específicas con una red de neuronas altamente polarizadas entremezcladas con células gliales y vasculatura densa. En un tejido tan complejo y heterogéneo, alguna vez fue impensable aislar y estudiar las sinapsis como un sistema independiente. En la década de 1960, Victor Whittaker, Catherine Hebb y otros hicieron esto posible aislando terminales sinápticas intactas utilizando fraccionamiento subcelular11,12,13,14. En un intento de aislar vesículas sinápticas (SV), homogeneizaron cerebros a través de fuerza de cizallamiento líquido en sacarosa iso-osmótica (0,32 M) seguida de ultracentrifugación. Obtuvieron terminales nerviosas intactas, pellizcadas, encerradas en la membrana plasmática o varicosidades, que llamaron partículas que terminan en los nervios (NEPs)11,13. Como las características estructurales y funcionales de la sinapsis se conservaron en estas estructuras, las NEP se denominaron más tarde "sinaptosomas" por congruencia con otros orgánulos subcelulares13,15. Vale la pena señalar que el trabajo de Eduardo de Robertis y colegas, quienes acuñaron el término "vesícula sináptica", se superpuso con el de Whittaker y colegas y contribuyó para la validación del aislamiento y caracterización del "sinaptosoma"16,17,18.
Los sinaptosomas son estructuras fisiológicamente activas que contienen todas las propiedades celulares y moleculares requeridas para el almacenamiento, liberación y recaptación de neurotransmisores13,18. La preservación de las características sinápticas clave in vitro y la ausencia de componentes no sinápticos también contribuyen a la utilidad de este método de aislamiento. Los sinaptosomas han contribuido enormemente a la comprensión de las propiedades químicas y fisiológicas de la neurotransmisión y ahora se están utilizando para estudiar los procesos moleculares sinápticos y sus alteraciones en la enfermedad 19,20,21,22,23. Los sinaptosomas son también el material de origen inicial para aislar componentes sinápticos como SVs, vesículas recubiertas de clatrina (CCV), citosol sináptico, membrana plasmática sináptica, mitocondrias sinápticas, moléculas de adhesión sináptica y otros componentes de interés, que pueden facilitar la comprensión de los mecanismos moleculares de la función sináptica 18,19,20,24,25,26, 27,28. Estos componentes subsinápticos pueden obtenerse por la lisis osmótica de sinaptosomas y ultracentrifugación por gradiente de densidad de sacarosa15,29. Aunque se sabe que el método original de fraccionamiento subcelular del grupo de investigación de Whittaker es eficiente para aislar sinaptosomas de calidad y SVs 13,30, las optimizaciones recientes mejoran la pureza de las fracciones subcelulares 22,23,31,32. Este artículo proporciona una versión muy detallada y accesible de un protocolo clásico para el fraccionamiento subcelular del tejido cerebral murino para aislar sinaptosomas, SV y otros componentes subsinápticos.
Todos los experimentos con ratones fueron aprobados por el Comité Institucional de Cuidado y Uso de Animales (IACUC) de la Universidad de Yale (Protocolo 2021-11117) y se realizaron en una instalación acreditada por la Asociación para la Evaluación y Acreditación de Laboratory Animal Care International (AAALAC). El cuidado y el alojamiento de los animales cumplieron con la Guía para el Cuidado y Uso de Animales de Laboratorio33 y fueron proporcionados por el Centro de Recursos para Animales de Yale (YARC). Los animales se mantuvieron en un ciclo de luz/oscuridad de 12 h con acceso ad libitum a alimentos y agua. Se requieren de cinco a ocho ratones o de dos a cuatro ratas por genotipo o condición para el siguiente protocolo. Se necesitan menos ratas debido a sus mayores volúmenes cerebrales. Del mismo modo, la edad de los animales de experimentación puede afectar el rendimiento de la fracción; Es posible que se requieran ratones adicionales para edades inferiores a 2 meses. De lo contrario, los procedimientos descritos se aplican tanto a especies murinas como a animales adultos sanos de cualquier edad. Los datos representativos presentados en este estudio utilizaron ratones de tipo salvaje (C57BL / 6J) (edad = 2 meses; cuatro machos y cuatro hembras por réplica) obtenidos de una fuente comercial (ver Tabla de materiales).
1. Preparación experimental
NOTA: Este protocolo requiere ~ 11 h para que un solo investigador lo complete. Se recomienda encarecidamente completar la configuración de sobremesa (Figura 1), la preparación del tampón (Tabla 1), el preenfriamiento de centrífugas y rotores a 4 °C, y la recolección y etiquetado de los materiales y equipos necesarios (consulte la Tabla de materiales) el día anterior a la ejecución del protocolo, cuando corresponda.
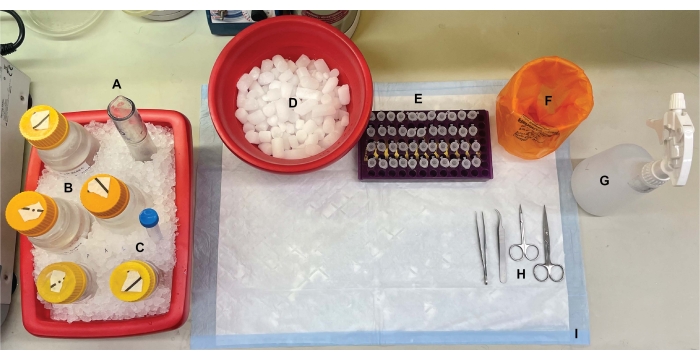
Figura 1: Configuración de sobremesa. Antes de las disecciones cerebrales, (A) los homogeneizadores de vidrio de rebote y (B) todos los tampones se enfriaron en hielo. (C) Las soluciones madre de inhibidores de la proteasa se descongelaron en hielo. Se obtuvo un segundo contenedor de hielo húmedo para tubos de centrífuga, un Dewar de nitrógeno líquido (no mostrado) y (D) un recipiente de hielo seco para el almacenamiento a corto plazo de las muestras congeladas en nitrógeno líquido. (E) Los tubos de microcentrífuga se etiquetaron previamente para todas las muestras, ya que se recolectaron cuatro alícuotas de cada muestra de fracción subcelular por genotipo o condición durante este procedimiento (consejo para ahorrar tiempo: etiquete completamente todos los tubos el día antes de que se realice el experimento). (F) Un contenedor apropiado para desechos de riesgo biológico, (G) etanol al 70%, (H) herramientas quirúrgicas e (I) una almohadilla de superficie absorbente. Los tubos de centrífuga y desechables requeridos se reservaron para un acceso eficiente durante la implementación del protocolo (no se muestra). Haga clic aquí para ver una versión más grande de esta figura.
- Prepare la mesa de trabajo para la cirugía y recoja las tijeras y fórceps necesarios para la escisión cerebral (consulte la Tabla de materiales). Pre-etiqueta tubos de microcentrífuga de 1,5 ml para biopsias de cola de ratón y cuatro tubos por fracción recolectada, como se describe en la Figura 2.
- Obtenga dos recipientes de hielo húmedo, un recipiente de hielo seco y un matraz Dewar de nitrógeno líquido de sobremesa.
- Descongele las soluciones madre de fluoruro de fenilmetilsulfonilo (PMSF), pepstatina A, aprotinina y leupeptina en hielo (consulte la Tabla de materiales). Prepare los buffers necesarios (Tabla 1).
NOTA: Las soluciones de sacarosa pueden prepararse previamente y almacenarse a 4 °C. Sin embargo, los inhibidores de la proteasa (cepas descongeladas y tabletas) deben agregarse frescos a todos los tampones al comienzo del experimento debido a la inestabilidad de estos reactivos en soluciones acuosas. Además, todos los tampones deben prepararse con cristalería sin detergente y agua sin detergente para permitir la recolección de sinaptosomas intactos. - Enfríe todos los amortiguadores y homogeneizadores de vidrio (consulte la Tabla de materiales) en hielo. Ajuste las centrífugas a 4 °C y enfríe los rotores a 4 °C.
- Agregue 14 ml de tampón A (Tabla 1) a un homogeneizador de rebote en hielo.
Tabla 1: Composición de los tampones de fraccionamiento subcelular. Haga clic aquí para descargar esta tabla.
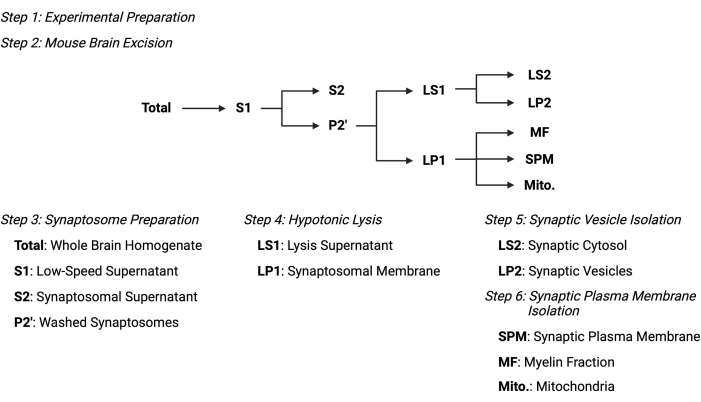
Figura 2: Descripción general del protocolo de fraccionamiento subcelular. Esquema resumido de los pasos de fraccionamiento subcelular y muestras recogidas. Haga clic aquí para ver una versión más grande de esta figura.
2. Escisión del cerebro del ratón
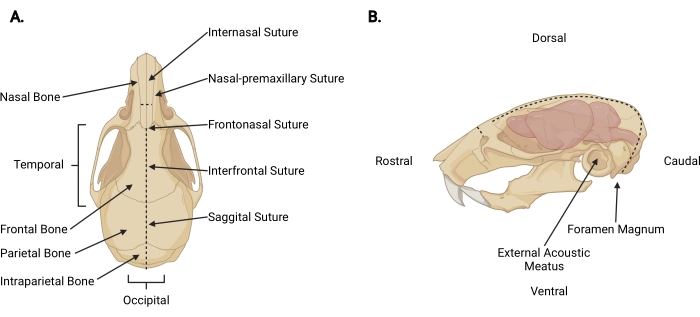
Figura 3: Anatomía craneofacial . (A) Vista dorsal de un cráneo de ratón con estructuras craneales relevantes indicadas. (B) Vista lateral izquierda de un cráneo y cerebro de ratón con estructuras craneales relevantes y direcciones anatómicas indicadas. Las líneas discontinuas representan los lugares donde se deben hacer las incisiones. Haga clic aquí para ver una versión más grande de esta figura.
- Anestesiar profundamente a cada ratón con isofluorano al 100% en una cámara de anestesia ubicada en una campana extractora o gabinete de bioseguridad utilizando un método de gota abierta34. Sacrificar cada ratón por dislocación de la columna cervical seguida rápidamente por la decapitación. Alternar entre genotipos o grupos experimentales para cada sacrificio y disección12. Obtenga biopsias de cola después de la eutanasia extirpando 2 mm de la punta distal de la cola con tijeras finas. Almacene el tejido para la genotipificación.
- Rocíe la cabeza decapitada con etanol al 70% para evitar que el cabello se adhiera al tejido y a los instrumentos quirúrgicos durante la disección.
- Inserte tijeras finas debajo de la piel en la incisión de decapitación a una profundidad pericraneal y haga una incisión sagital media hasta la sutura internasal (Figura 3A) para retraer el cuero cabelludo del cráneo.
- Trabajando desde el área occipital hacia cada aspecto temporal, recorte la fascia y el músculo para exponer la superficie externa del cráneo más allá de cada meato acústico externo (Figura 3B).
- Asegure el cuero cabelludo y la cara rostral del cráneo con la mano no dominante. Con el otro, inserte tijeras finas de 2 mm en el lado caudal del foramen magno, donde la médula espinal es visible saliendo. Haga una incisión en la línea media hasta que las tijeras lleguen a la superficie interna del hueso intraparietal (Figura 3; líneas discontinuas).
NOTA: Durante la incisión inicial, las tijeras deben estar paralelas a la médula espinal con presión aplicada hacia la superficie interna del cráneo para evitar daños en el tronco encefálico y el cerebelo. - Cambie el ángulo de las tijeras para que las cuchillas corran paralelas a la superficie dorsal del cráneo. Continuar avanzando la incisión sagital media rostralmente a través de los huesos parietal y frontal, utilizando las suturas sagital e interfrontal como guía. Use una presión constante hacia arriba para evitar daños en la corteza. Terminar la incisión justo más allá de la sutura internasal (Figura 3A).
- Haga una pequeña incisión perpendicular (~3 mm) al hueso nasal, rostral a la sutura internasal, colocando las tijeras perpendiculares al cráneo con cada cuchilla colocada en una sutura nasal-premaxilar y haciendo un corte uniforme (Figura 3; líneas discontinuas).
NOTA: Este paso aumentará la facilidad de retracción del cráneo y será crítico para recolectar el bulbo olfatorio si esta área es de interés. - Mientras asegura el aspecto rostral, use un lado de un par de pinzas texturizadas para levantar suavemente el cráneo desde el cerebro, luego lateral y ventralmente. Repita a lo largo de la línea media según sea necesario, luego para el otro hemisferio hasta que toda la superficie del cerebro esté expuesta.
- Usando fórceps curvos o una espátula fina, levante suavemente el lado rostral del cerebro. Cortar los nervios óptico y craneal para completar la escisión del cráneo.
- Para cada condición, recoja de cinco a ocho cerebros de ratón juntos en el homogeneizador de vidrio refrigerado que contiene 14 ml de tampón A (Tabla 1).
3. Preparación del sinaptosoma
NOTA: Los esquemas de este procedimiento se muestran en la figura 4.
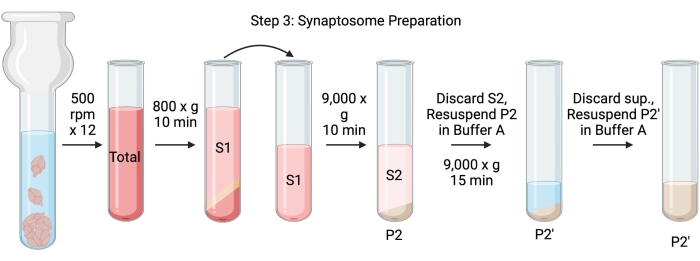
Figura 4: Preparación del sinaptosoma. Esquema del paso 3, la generación de sinaptosomas (P2'). Haga clic aquí para ver una versión más grande de esta figura.
- Homogeneice los cerebros usando un homogeneizador de vidrio Dounce en 12 pasadas arriba-abajo a 500 rpm (total). Haga una breve pausa en cada carrera descendente para asegurar una homogeneización completa del tejido. Homogeneizar preferentemente en un baño de hielo para evitar el calentamiento y la desnaturalización de proteínas. Tomar 5 μL de alícuotas para la determinación de la concentración de proteínas mediante el ensayo de ácido bicinchonínico (BCA, ver Tabla de materiales). Tome 100 μL de alícuotas de lisado cerebral completo para Western blot (WB). Para esta y todas las muestras posteriores (figura 2), tomar dos alícuotas para BCA y dos alícuotas para WB. Congelar rápidamente todas las alícuotas recogidas en nitrógeno líquido y almacenarlas a -80 °C.
- Girar el homogeneizado cerebral total en un tubo centrífugo de fondo redondo de alta velocidad (14 ml) (ver Tabla de materiales) a 800 x g durante 10 min a 4 °C para obtener el sobrenadante (S1). Transfiera S1 a un nuevo tubo de centrífuga, dejando atrás el pellet (P1), que contiene células y núcleos intactos. Evite pipetear el pellet esponjoso, blanco, suelto y superficial. Tomar 2 x 5 μL de S1 para BCA y 2 x 100 μL de S1 para WB.
- Girar S1 a 9.000 x g durante 15 min a 4 °C para obtener el sobrenadante sinaptosomal (S2) y el pellet sinaptosómico crudo (P2). Tomar 2 x 10 μL de S2 para BCA y 2 x 500 μL de S2 para WB. Deseche el sobrenadante después de obtener alícuotas y continúe con el siguiente paso con el pellet.
- Resuspender P2 en 3 ml de Tampón A helado con inhibidores de la proteasa y centrifugar a 9.000 x g durante 15 min a 4 °C para obtener el sobrenadante (S2') y los sinaptosomas lavados (P2'). Deseche el sobrenadante y guarde el pellet.
- Resuspenda P2' en 3 ml de tampón A. Evite resuspender la porción de color rojo oscuro en la parte inferior del pellet, que contiene principalmente mitocondrias. Tomar 2 x 20 μL de P2' para BCA y 2 x 100 μL de P2' para WB.
NOTA: Esto se puede lograr mezclando suavemente los bordes y la superficie del pellet para resuspender los sinaptosomas blancos lavados mientras se dirige la punta de la pipeta lejos del centro rojo del pellet.
4. Lisis hipotónica
NOTA: Los esquemas de este procedimiento se muestran en la figura 5.
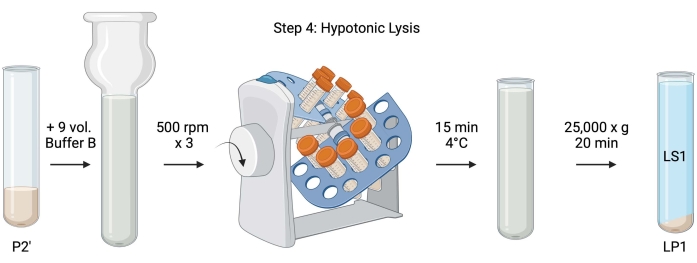
Figura 5: Lisis hipotónica. Esquema del paso 4, la lisis hipotónica de los sinaptosomas para generar el sobrenadante de lisis (LS1) y las fracciones de membrana sinaptosómica (LP1). Haga clic aquí para ver una versión más grande de esta figura.
- Para la lisis hipotónica de los sinaptosomas lavados, agregue 9 volúmenes de tampón B refrigerado (Tabla 1) a P2' resuspendido (~ 27 ml). Homogeneizar los sinaptosomas en un homogeneizador de vidrio Dounce (tres pasadas arriba-abajo a 500 rpm).
- Transfiera las muestras a tubos de centrífuga cónica tapados de 50 ml. Gíralos en un revólver tubular en una cámara frigorífica a 4 °C durante 15 min.
- Centrifugación lisada P2' a 25.000 x g durante 20 min a 4 °C para obtener el sobrenadante de lisis (LS1) y el pellet de lisis que contiene membranas sinaptosómicas (LP1). Tomar 2 x 50 μL de LS1 para BCA y 2 x 400 μL de LS1 para WB. Transfiera LS1 a un tubo de centrífuga tapado para ultracentrifugación (consulte la Tabla de materiales).
5. Aislamiento de vesículas sinápticas
NOTA: Los esquemas de este procedimiento se muestran en la figura 6.
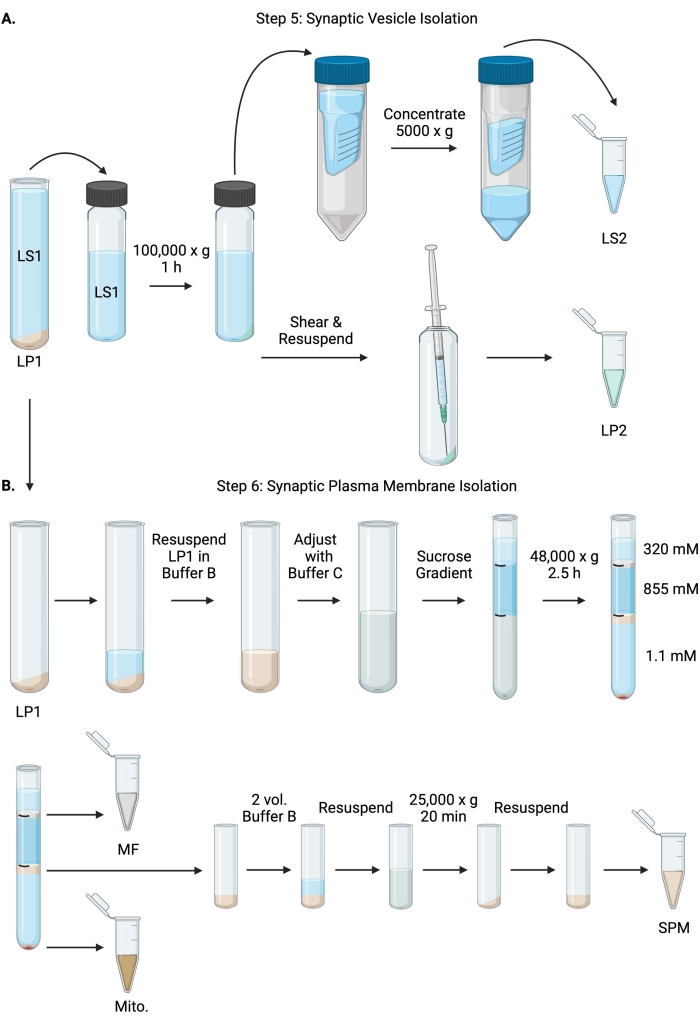
Figura 6: Aislamiento de vesículas sinápticas y aislamiento de membrana plasmática sináptica. (A) Esquema del paso 5, el aislamiento de las fracciones del citosol sináptico (LS2) y la vesícula sináptica (LP2), y (B) el paso 6, la generación de mielina (MF), la membrana plasmática sináptica (SPM) y las fracciones mitocondriales (Mito.) después de la ultracentrifugación de gradientes de sacarosa. Haga clic aquí para ver una versión más grande de esta figura.
- Centrífuga LS1 en un rotor de ultracentrífuga de ángulo fijo (ver Tabla de materiales) a 100.000 x g durante 60 min a 4 °C para obtener sobrenadante de citosol sináptico (LS2) y pellet de vesícula sináptica (LP2). LP2 será pequeño, translúcido y fuertemente adherido al lado del tubo de centrífuga.
- Resuspender LP2 en 500 μL de tampón A. Con una aguja de 23 g y una jeringa de 1 ml, cortar LP2 con una trituración suave. Tomar 2 x 10 μL de LP2 para BCA y 2 x 250 μL de LP2 para WB.
- Transfiera LS2 (~30 ml) a unidades de filtro centrífugas con un corte de 10 kDa (consulte la Tabla de materiales).
NOTA: Si las proteínas menores de 10 kDa son de interés, las unidades de filtro centrífuga de corte de 4 kDa están disponibles, pero darán como resultado tiempos de centrifugado más largos. - Concentrar LS2 a aproximadamente 0,5 ml girando a 5000 x g durante un máximo de 1 h a 4 °C. Tomar 2 x 10 μL de LS2 concentrado para BCA y 2 x 250 μL de LS2 concentrado para WB. Después de iniciar el giro, continúe directamente con el paso 6.1.
6. Aislamiento de la membrana plasmática sináptica
- Resuspender LP1 (paso 4.3) en 1 ml de tampón B (Tabla 1). Tome 2 x 10 μL de LP1 para BCA y 2 x 50 μL de LP1 para WB. Ajustar el LP1 restante a un volumen final de 7,5 ml y una concentración final de sacarosa de 1,1 M con tampón B y tampón C (Tabla 1).
- Transfiera 7,5 ml de LP1 resuspendido a un tubo de ultracentrífuga de 14 ml (consulte la Tabla de materiales). Superponga cuidadosamente LP1 con 3.75 ml de tampón D (Tabla 1) y luego superponga con 1.25 ml de tampón A (o un volumen mayor para llenar justo debajo de la parte superior del tubo de centrífuga). Evite pipetear por el costado del tubo, lo que interrumpirá las interfaces de gradiente de sacarosa. Después de superponer cada fracción de sacarosa, marque la parte superior de la solución con una pluma. Equilibre los tubos para la ultracentrifugación por peso, no por volumen, con la adición gota a gota de tampón A dentro de 10 mg. Centrífuga a 48.000 x g durante 2,5 h a 4 °C en un rotor ultracentrífugo de cangilón oscilante (ver Tabla de materiales).
- Adquiera imágenes de los gradientes intactos después de la ultracentrifugación para documentar la distinción de cada interfaz de sacarosa y el éxito del fraccionamiento.
- Retire con cuidado la capa superficial de sacarosa de 320 mM (tampón A). Recuperar la fracción de mielina (MF) en la interfaz sacarosa de 320 mM/855 mM en un volumen de 800 μL. Recuperar la fracción de membrana plasmática sináptica (MPS) en la interfaz sacarosa de 855 mM/1,1 M en un volumen de 1.000 μL. Pipete cada fracción hacia arriba desde la pared del tubo de manera circular para asegurarse de que se recoge la fracción completa. Aspirar cuidadosamente la sacarosa restante y recuperar el pellet mitocondrial (Mito.) resuspendiendo en 200 μL de tampón B. Tome 2 x 100 μL de MF para BCA y 2 x 10 μL de Mito. para BCA; dividir el resto de MF y Mito. muestras a la mitad para WB.
- Diluir la fracción SPM con 2 volúmenes de tampón B (~2 ml) y luego centrifugar en un rotor de ángulo fijo en un tubo centrífugo de 3,5 ml (consulte la tabla de materiales) a 25.000 x g durante 20 min a 4 °C. Desechar el sobrenadante y resuspender el pellet SPM en el tampón A para obtener un volumen final de 250 μL. Tome 2 x 5 μL de SPM para BCA y divida el SPM restante por la mitad para WB.
- Realizar un BCA para determinar la concentración de proteínas de cada muestra, teniendo en cuenta el volumen de alícuota variable.
NOTA: Para el análisis de WB, la concentración de proteína de trabajo sugerida para todas las fracciones subcelulares es de 2 μg / μL (o tan alta como se pueda lograr para LS1 y MF).
El método presentado da como resultado 11 fracciones subcelulares cerebrales que pueden ser sometidas a una purificación adicional y diversas formas de análisis aguas abajo35,36. El método estándar de oro para evaluar la calidad de los sinaptosomas, SV23 y otros componentes es la microscopía electrónica (EM) (Figura 7). También se puede realizar inmunotransferencia cuantitativa para proteínas que están presentes en fracciones subcelulares específicas para evaluar los marcadores de pureza de la fracción (Figura 8). Por ejemplo, el análisis inmunoblot de fracciones revela el enriquecimiento de N-cadherina (CDH2, nombre UniProt) en la fracción sináptica de la membrana plasmática (SPM), α-sinucleína (SYUA) en el citosol sináptico (LS2), sinaptofisina (SYPH) en la fracción de vesícula sináptica (LP2) y proteína básica de mielina (MBP) en la fracción de mielina (MF) en comparación con los niveles de proteína en el homogeneizado inicial de todo el cerebro (Total) (Figura 8 ). Una vez que se ha establecido la pureza de la fracción (por ejemplo, observe la ausencia de CDH2 en la fracción LS2 o el aumento de muchas veces en SYPH en la fracción LP2), se puede utilizar la inmunotransferencia cuantitativa para determinar la localización de proteínas de interés o consultar diferencias en la distribución de proteínas entre genotipos o tratamientos. Comprender la localización subcelular de las proteínas sinápticas puede permitir la disección de funciones proteicas previamente no descritas. Además, este método puede dilucidar defectos de tráfico o disfunción sináptica en estados de enfermedad, especialmente cuando se combina con ensayos funcionales. Por ejemplo, nuestro equipo ha utilizado este método para identificar un conjunto de proteína palmitoil tioesterasa 1 enzimáticamente activa que está enriquecida en el citosol sináptico19.
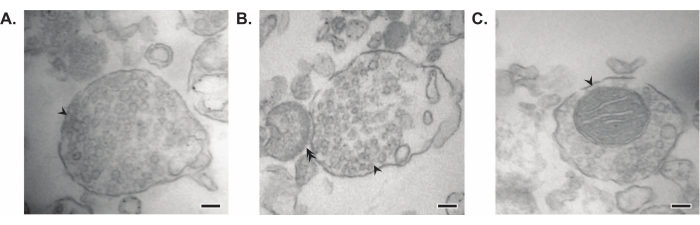
Figura 7: Microscopía electrónica (EM) de sinaptosomas. (A) Imagen EM representativa de un sinaptosoma que contiene vesículas sinápticas (flecha). (B) Imagen EM representativa de un sinaptosoma con componentes pre- (flecha) y post-sinápticos (flecha doble). (C) Imagen EM representativa de un sinaptosoma que contiene vesículas sinápticas y una mitocondria (flecha) (barras de escala = 100 nm). Haga clic aquí para ver una versión más grande de esta figura.
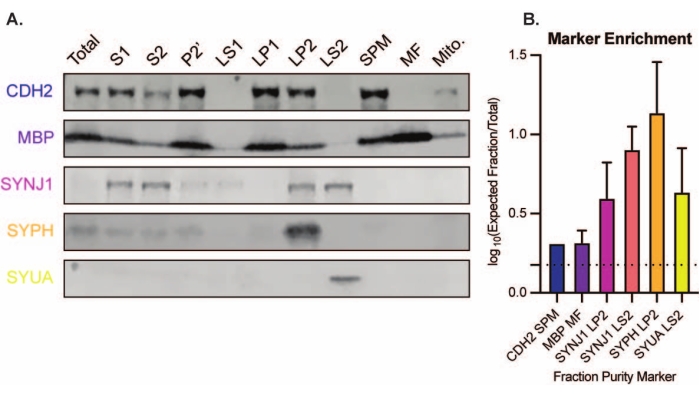
Figura 8: Análisis de inmunoblot de fracciones subcelulares. (A) Los marcadores de pureza de la fracción subcelular (indicados con la nomenclatura UniProt) están localizados adecuadamente en comparación con el homogeneizado cerebral completo (total): N-cadherina (CDH2) en la fracción de membrana plasmática sináptica (SPM), sinaptofisina 1 (SYPH) y sinaptojanina 1 (SYNJ1) en la fracción enriquecida con vesículas sinápticas (LP2), α-sinucleína (SYUA) en el citosol sináptico (LS2), y proteína básica de mielina (MBP) en la fracción de mielina (MF). (B) El análisis de cuantificación de inmunoblot revela el enriquecimiento (cambio de pliegue del total) de los marcadores de pureza de fracción. Los datos se representan como media ± desviación estándar en una escala log10. La línea punteada indica un cambio de 1,5 veces (y = 0,176) (n = 3 experimentos replicados con 8 ratones de tipo salvaje; edad = 2 meses; n = 4-5 blots para SYPH, SYUA, MBP, con n = 3 valores trazados previamente publicados por Gorenberg et al.19; n = 5 para SYNJ1; n = 1 para CDH2). Haga clic aquí para ver una versión más grande de esta figura.
En sus estudios seminales, Whittaker y sus colegas utilizaron cuatro criterios morfológicos para identificar los sinaptosomas: (1) las estructuras tienen una membrana plasmática sellada; (2) las estructuras contienen SV que se asemejan a las de las terminales nerviosas y varicosidades in situ en tamaño y número; (3) las estructuras poseen una o más mitocondrias pequeñas; y (4) la membrana presináptica está frecuentemente adherida a un componente postsináptico11,12,13. Aunque los dos primeros criterios generalmente se aplican a todos los métodos de aislamiento, en los protocolos más recientes descritos en este artículo, no todos los sinaptosomas resultantes tendrán mitocondrias y terminales postsinápticas adjuntas. Aproximadamente 60% de los sinaptosomas tendrán mitocondrias, y se estima que sólo hasta 15% tienen terminales postsinápticas unidas37. Si los componentes postsinápticos son de particular interés, se sabe que el uso de un tampón de homogeneización isotónico similar a Krebs y la filtración a presión para el enriquecimiento producen altas concentraciones de sinaptosomas con terminales postsinápticos (también denominados sinaptoneurosomas)22,38.
El método de sacrificio del animal puede afectar la calidad de los sinaptosomas y las subfracciones sinápticas. Los animales adultos sacrificados mediante un método de eutanasia que no requiere anestesia darán como resultado la mejor calidad de fracción. Además, los cerebros deben ser recién diseccionados, no congelados, y homogeneizados utilizando una relación 1:10 de tampón de homogeneización (peso/volumen) para las fracciones sinápticas más viables22. El cerebro tiene una población heterogénea de sinapsis que pueden diferenciarse por el tipo de neurotransmisores que llevan. La formación de sinaptosoma generalmente no se ve afectada por el tipo de sinapsis o el contenido de neurotransmisores13. Una excepción son las fibras musgosas en el cerebelo, que se sabe que se alteran en condiciones óptimas para obtener sinaptosomas del resto del cerebro39,40. Por lo tanto, se recomienda la extirpación del cerebelo antes de la homogeneización cerebral si la exclusión de esta región no afecta el objetivo experimental. Si está interesado en aislar sinaptosomas de un carácter neurotransmisor particular, primero se pueden aislar las áreas del cerebro que están enriquecidas para las neuronas que contienen el neurotransmisor de interés. Sin embargo, este enfoque impondrá limitaciones en el rendimiento de la fracción final, dependiendo del tamaño de la región de interés (la edad de los animales también es, por lo tanto, una consideración). Existen métodos inmunoquímicos para el aislamiento de sinaptosomas específicos de neurotransmisores, pero la viabilidad y el rendimiento se verán significativamente comprometidos22. Si la evaluación de la viabilidad metabólica del sinaptosoma es importante, se puede emplear la medición de la liberación de neurotransmisores 41,42 o ciertos ensayos enzimáticos43.
Los contaminantes comunes en las preparaciones de sinaptosoma incluyen microsomas, mitocondrias libres, SV y membranas neuronales y gliales. La contaminación puede reducirse aumentando el número de lavados en las fracciones P1 y P222 y evitando la resuspensión del pellet mitocondrial rojo en pasos posteriores. En experimentos donde la viabilidad metabólica y el tiempo son cruciales, reducir el número de lavados y usar gradientes de Ficoll o Percoll sobre gradientes de sacarosa será útil44,45,46. Estos métodos también reducen significativamente la contaminación. El protocolo original de Whittaker produjo SV de alta calidad. La optimización adicional por Nagy et al.23, incluida en este método, produce SVs con notable homogeneidad y pureza sin comprometer significativamente el rendimiento36. Si los subtipos específicos de SV son de interés, como los SV glutamatérgicos (que contienen VGLUT-1) o GABAérgicos (que contienen VGAT-1), se puede realizar inmunoaislamiento con anticuerpos específicos47,48. También se dispone de métodos alternativos para aislar los CCV de los sinaptosomas, que, debido a la densidad diferencial, pueden no estar presentes en la misma interfaz que los SV obtenidos con este método20,49,50.
En general, el protocolo actual para aislar componentes sinápticos se puede optimizar aún más para obtener fracciones con homogeneidad y viabilidad mejoradas basadas en la calidad y cantidad del tejido cerebral fuente y los objetivos experimentales. Para obtener más detalles sobre la solución de problemas, se deben consultar los capítulos del libro de Dunkley y Robinson22 y Ganzella et al.36.
Los autores no tienen nada que revelar.
Nos gustaría agradecer a P. Colosi por la preparación de imágenes EM. Este trabajo fue apoyado por los Institutos Nacionales de Salud (R01 NS064963, SSC; R01 NS110354, SSC; R01 NS083846, SSC; R21 NS094971, SSC; T32 NS007224, SMT; T32 NS041228, SMT), el Departamento de Defensa de los Estados Unidos (W81XWH-17-1-0564, SSC; W81XWH-19-1-0264, VDJ), Aligning Science Across Parkinson's (ASAP) Collaborative Research Network (SSC), y el Michael J. Fox Foundation Target Advancement Program (MJFF-020160, SSC & VDJ). Creamos ilustraciones gráficas usando BioRender.com.
| Name | Company | Catalog Number | Comments |
| 1 mL TB Syringe | BD | 309649 | |
| 1.5 mL Eppendorf Tubes | USA Scientific | 1415-2500 | |
| 14 mL, Open-Top Thinwall Ultra-Clear Tube | Beckman Coulter | 344060 | Compatible with SW 40 Ti |
| 23 Gauge Precision Glide Hypodermic Needle | BD | 305145 | |
| 26.3 mL, Polycarbonate Bottle with Cap Assembly | Beckman Coulter | 355618 | Compatible with Ti70 |
| 3.5 mL, Open-Top Thickwall Polypropylene Tube | Beckman Coulter | 349623 | Compatible with TLA-100.3 |
| 50 mL Falcon Tubes | Fisher Scientific | 14-432-22 | |
| Amicon Ultra-15 Centrifugal Filter Unit | Millipore Sigma | UFC901024 | |
| Aprotinin | Sigma-Aldrich | A6279 | 1 mg/mL in diH2O |
| Avanti J-26 XP Centrifuge | Beckman Coulter | B22984 | <26,000 rpm |
| Benchtop HDPE Dewar Flask | Thermo Scientific | 5028U19 | |
| C57BL/6J Mice | The Jackson Labs | 000664 | |
| Centrifuge 5810R | Eppendorf | EP022628168 | <14,000 rpm |
| complete, Mini, EDTA-free Protease Inhibitor Cocktail Tablets | Roche | 11873580001 | Add 1 tablet per 50 mL of solution |
| Curved Forceps | Fine Science Tools | 11273-20 | |
| Fine Surgical Scissors | Fine Science Tools | 8r | |
| Glas-Col Tissue Homogenizing System | Cole-Parmer | UX-04369-15 | |
| Graefe Forceps | Fine Science Tools | 11650-10 | |
| High-Speed Polycarbonate Round Bottom Centrifuge Tubes | ThermoFisher | 3117-0500 | Compatible with JA20 |
| Isofluorane | Henry Schein Animal Health | NDC 11695-6776-2 | |
| JA-20 Rotor | Beckman Coulter | 334831 | |
| Leupeptin | American Bio | AB01108 | 1 mg/mL in diH2O |
| N-[2-Hydroxyethyl] piperazine-N’-[2-ethanesulfonic acid] (HEPES) | American Bio | AB00892 | |
| Optima L-80 XP Ultracentrifuge | Beckman Coulter | <100,000 rpm | |
| Optima TLX Ultracentrifuge | Beckman Coulter | <120,000 rpm | |
| Pepstatin A | Thermo Scientific | 78436 | 1 mg/mL in DMSO |
| Phenylmethylsulfonyl fluoride (PMSF) | American Bio | AB01620 | |
| Pierce BCA Protein Assay Kit | Thermo Scientific | 23335 | For determination of protein concentration |
| Pipette Tips | |||
| Serological Pipettes | |||
| Sucrose | Sigma-Aldrich | S0389 | |
| Surgical Scissors | Fine Science Tools | 14002-12 | |
| SW 40 Ti Swinging-Bucket Rotor | Beckman Coulter | 331301 | |
| Teflon-Coated Pestle and Mortar Tissue Grinder | Thomas Scientific | 3431D94 | |
| Ti70 Rotor | Beckman Coulter | 337922 | |
| TLA-100.3 Rotor | Beckman Coulter | 349490 | |
| Tube Revolver | Dot Scientific | DTR-02VS |
- Kandel, E. R., Schwartz, J. H., Jessell, T. M., Siegelbaum, S. A., Hudspeth, A. J., Education, A. J. Synaptic Transmission. Principles of Neural Science, Fifth Edition. , (2014).
- Lepeta, K., et al. Synaptopathies: synaptic dysfunction in neurological disorders - A review from students to students. Journal of Neurochemistry. 138 (6), 785-805 (2016).
- Südhof, T. C., Malenka, R. C. Understanding synapses: Past, present, and future. Neuron. 60 (3), 469-476 (2008).
- Südhof, T. C. The molecular machinery of neurotransmitter release (Nobel lecture). Angewandte Chemie International Edition. 53 (47), 12696-12717 (2014).
- Jahn, R., Boyken, J., Pfaff, D. W. Molecular Regulation of Synaptic Release. Neuroscience in the 21st Century: From Basic to Clinical. , 351-401 (2013).
- Xiong, H., Gendelman, H. E. . Current Laboratory Methods in Neuroscience Research. , (2014).
- Azevedo, F. A., et al. Equal numbers of neuronal and nonneuronal cells make the human brain an isometrically scaled-up primate brain. Journal of Comparative Neurology. 513 (5), 532-541 (2009).
- Herculano-Houzel, S. The remarkable, yet not extraordinary, human brain as a scaled-up primate brain and its associated cost. Proceedings of the National Academy of Sciences of the United States of America. 109, 10661-10668 (2012).
- Herculano-Houzel, S., Lent, R. Isotropic fractionator: A simple, rapid method for the quantification of total cell and neuron numbers in the brain. Journal of Neuroscience. 25 (10), 2518-2521 (2005).
- Herculano-Houzel, S., Mota, B., Lent, R. Cellular scaling rules for rodent brains. Proceedings of the National Academy of Sciences of the United States of America. 103 (32), 12138-12143 (2006).
- Gray, E. G., Whittaker, V. P. The isolation of nerve endings from brain: An electron-microscopic study of cell fragments derived by homogenization and centrifugation. Journal of Anatomy. 96, 79-88 (1962).
- Gray, E. G., Whittaker, V. P. The isolation of synaptic vesicles from the central nervous system. Journal of Physiology. 153, 35-37 (1960).
- Whittaker, V. P. Thirty years of synaptosome research. Journal of Neurocytology. 22 (9), 735-742 (1993).
- Jahn, R., Fasshauer, D. Molecular machines governing exocytosis of synaptic vesicles. Nature. 490, 201-207 (2012).
- Whittaker, V. P., Michaelson, I. A., Kirkland, R. J. The separation of synaptic vesicles from nerve-ending particles ('synaptosomes). Biochemical Journal. 90 (2), 293-303 (1964).
- De Robertis, E., Rodriguez De Lores Arnaiz, G., Pellegrino De Iraldi, A. Isolation of synaptic vesicles from nerve endings of the rat brain. Nature. 194, 794-795 (1962).
- De Robertis, E., Pellegrino De Iraldi, A., Rodriguez, G., Gomez, C. J. On the isolation of nerve endings and synaptic vesicles. The Journal of Biophysical and Biochemical Cytology. 9 (1), 229-235 (1961).
- Zimmermann, H., Whittaker, V. P., Murphy, K. M. The Discovery of the Synaptosome and Its Implications. Synaptosomes. , 9-26 (2018).
- Gorenberg, E. L., et al. Identification of substrates of palmitoyl protein thioesterase 1 highlights roles of depalmitoylation in disulfide bond formation and synaptic function. PLoS Biology. 20 (3), 3001590 (2022).
- Vidyadhara, D. J., et al. Dopamine transporter and synaptic vesicle sorting defects initiate auxilin-linked Parkinson's disease. bioRxiv. , (2022).
- Schrimpf, S. P., et al. Proteomic analysis of synaptosomes using isotope-coded affinity tags and mass spectrometry. Proteomics. 5 (10), 2531-2541 (2005).
- Dunkley, P. R., Robinson, P. J., Murphy, K. M. Synaptosome Preparations: Which Procedure Should I Use. Synaptosomes. , 27-53 (2018).
- Nagy, A., Baker, R. R., Morris, S. J., Whittaker, V. P. The preparation and characterization of synaptic vesicles of high purity. Brain Research. 109 (2), 285-309 (1976).
- Takamori, S., et al. Molecular anatomy of a trafficking organelle. Cell. 127 (4), 831-846 (2006).
- Wagner, J. A., Kelly, R. B. Topological organization of proteins in an intracellular secretory organelle: the synaptic vesicle. Proceedings of the National Academy of Sciences of the United States of America. 76 (8), 4126-4130 (1979).
- Jahn, R., Schiebler, W., Ouimet, C., Greengard, P. A 38,000-dalton membrane protein (p38) present in synaptic vesicles. Proceedings of the National Academy of Sciences of the United States of America. 82 (12), 4137-4141 (1985).
- Binotti, B., Jahn, R., Pérez-Lara, &. #. 1. 9. 3. ;. An overview of the synaptic vesicle lipid composition. Archives of Biochemistry and Biophysics. 709, 108966 (2021).
- Siegel, D. P., Ware, B. R. Electrokinetic properties of synaptic vesicles and synaptosomal membranes. Biophysical Journal. 30 (1), 159-172 (1980).
- Whittaker, V. P., Michaelson, I. A., Kirkland, R. J. The separation of synaptic vesicles from disrupted nervending particles. Biochemical Pharmacology. 12 (3), 300-302 (1963).
- Clementi, F., Whittaker, V. P., Sheridan, M. N. The yield of synaptosomes from the cerebral cortex of guinea pigs estimated by a polystyrene bead "tagging" procedure. Zeitschrift für Zellforschung und Mikroskopische Anatomie. 72, 126-138 (1966).
- Carlson, S. S., Wagner, J. A., Kelly, R. B. Purification of synaptic vesicles from elasmobranch electric organ and the use of biophysical criteria to demonstrate purity. Biochemistry. 17 (7), 1188-1199 (1978).
- Huttner, W. B., Schiebler, W., Greengard, P., De Camilli, P. Synapsin I (protein I), a nerve terminal-specific phosphoprotein. III. Its association with synaptic vesicles studied in a highly purified synaptic vesicle preparation. Journal of Cell Biology. 96 (5), 1374-1388 (1983).
- Hawkins, P., et al. A guide to defining and implementing protocols for the welfare assessment of laboratory animals: eleventh report of the BVAAWF/FRAME/RSPCA/UFAW Joint Working Group on Refinement. Laboratory Animals. 45 (1), 1-13 (2011).
- Risling, T. E., Caulkett, N. A., Florence, D. Open-drop anesthesia for small laboratory animals. Canadian Veterinary Journal. 53 (3), 299-302 (2012).
- Deutsch, C., Drown, C., Rafalowska, U., Silver, I. A. Synaptosomes from rat brain: Morphology, compartmentation, and transmembrane pH and electrical gradients. Journal of Neurochemistry. 36 (6), 2063-2072 (1981).
- Ganzella, M., Ninov, M., Riedel, D., Jahn, R. Isolation of synaptic vesicles from mammalian brain. Methods in Molecular Biology. 2417, 131-145 (2022).
- Dunkley, P. R., et al. A rapid Percoll gradient procedure for isolation of synaptosomes directly from an S1 fraction: homogeneity and morphology of subcellular fractions. Brain Research. 441 (1-2), 59-71 (1988).
- Schwartz, R. D., Skolnick, P., Hollingsworth, E. B., Paul, S. M. Barbiturate and picrotoxin-sensitive chloride efflux in rat cerebral cortical synaptoneurosomes. FEBS Letters. 175 (1), 193-196 (1984).
- Pittaluga, A., Thellung, S., Maura, G., Raiteri, M. Characterization of two central AMPA-preferring receptors having distinct location, function and pharmacology. Naunyn-Schmiedeberg's Archives of Pharmacology. 349 (6), 555-558 (1994).
- Israël, M., Whittaker, V. P. The isolation of mossy fibre endings from the granular layer of the cerebellar cortex. Experientia. 21 (6), 325-326 (1965).
- Khvotchev, M., Lonart, G., Südhof, T. C. Role of calcium in neurotransmitter release evoked by alpha-latrotoxin or hypertonic sucrose. Neuroscience. 101 (3), 793-802 (2000).
- Lonart, G., Janz, R., Johnson, K. M., Südhof, T. C. Mechanism of action of rab3A in mossy fiber LTP. Neuron. 21 (5), 1141-1150 (1998).
- Nicholls, D. G., Sihra, T. S. Synaptosomes possess an exocytotic pool of glutamate. Nature. 321 (6072), 772-773 (1986).
- Dunkley, P. R., Jarvie, P. E., Robinson, P. J. A rapid Percoll gradient procedure for preparation of synaptosomes. Nature Protocols. 3 (11), 1718-1728 (2008).
- Cotman, C. W., Matthews, D. A. Synaptic plasma membranes from rat brain synaptosomes: Isolation and partial characterization. Biochimica et Biophysica Acta. 249 (2), 380-394 (1971).
- Booth, R. F., Clark, J. B. A rapid method for the preparation of relatively pure metabolically competent synaptosomes from rat brain. Biochemical Journal. 176 (2), 365-370 (1978).
- Takamori, S., Riedel, D., Jahn, R. Immunoisolation of GABA-specific synaptic vesicles defines a functionally distinct subset of synaptic vesicles. Journal of Neuroscience. 20 (3), 4904-4911 (2000).
- Burger, P. M., et al. Synaptic vesicles immunoisolated from rat cerebral cortex contain high levels of glutamate. Neuron. 3 (6), 715-720 (1989).
- Blondeau, F., et al. Tandem MS analysis of brain clathrin-coated vesicles reveals their critical involvement in synaptic vesicle recycling. Proceedings of the National Academy of Sciences of the United States of America. 101 (11), 3833-3838 (2004).
- Maycox, P. R., Link, E., Reetz, A., Morris, S. A., Jahn, R. Clathrin-coated vesicles in nervous tissue are involved primarily in synaptic vesicle recycling. Journal of Cell Biology. 118 (6), 1379-1388 (1992).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved