Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Biology
Karakterisering af epitelsårheling in vivo ved hjælp af Cnidarian Model Organism Clytia hemisphaerica
Dette papir beskriver en metode til at skabe sår i epitelet af en levende Clytia hemisphaerica medusa og billedsårheling ved en høj opløsning in vivo. Derudover præsenteres en teknik til at introducere farvestoffer og lægemidler til forstyrrelsessignalprocesser i epitelcellerne og ekstracellulær matrix under sårheling.
Alle dyreorganer, fra hud til øjne til tarm, er dækket af plader af epitelceller, der giver dem mulighed for at opretholde homeostase og samtidig beskytte dem mod infektion. Derfor er det ikke overraskende, at evnen til at reparere epitelsår er kritisk for alle metazoer. Epitelsårheling hos hvirveldyr involverer overlappende processer, herunder inflammatoriske reaktioner, vaskularisering og re-epithelialisering. Regulering af disse processer involverer komplekse interaktioner mellem epitelceller, naboceller og den ekstracellulære matrix (ECM); ECM indeholder strukturelle proteiner, regulatoriske proteiner og aktive små molekyler. Denne kompleksitet sammen med det faktum, at de fleste dyr har uigennemsigtigt væv og utilgængelige ECM'er, gør sårheling vanskelig at studere i levende dyr. Meget arbejde med epitelsårheling udføres derfor i vævskultursystemer med en enkelt epitelcelletype belagt som et monolag på en kunstig matrix. Clytia hemisphaerica (Clytia) giver et unikt og spændende supplement til disse undersøgelser, der gør det muligt at studere epitelsårheling i et intakt dyr med en autentisk ECM. Det ektodermale epitel af Clytia er et enkelt lag af store pladeepitelceller, der tillader billeddannelse med høj opløsning ved hjælp af differentiel interfererende kontrast (DIC) mikroskopi hos levende dyr. Fraværet af migrerende fibroblaster, vaskulatur eller inflammatoriske reaktioner gør det muligt at dissekere de kritiske hændelser i re-epithelialisering in vivo. Helingen af forskellige typer sår kan analyseres, herunder enkeltcellede mikrosår, små og store epitelsår og sår, der beskadiger kældermembranen. Lamellipodia dannelse, pung streng sammentrækning, cellestrækning, og kollektiv cellemigration kan alle observeres i dette system. Desuden kan farmakologiske midler introduceres via ECM for at ændre celle: ECM-interaktioner og cellulære processer in vivo. Dette arbejde viser metoder til at skabe sår i levende Clytia, fange film af helbredelse og sondere helingsmekanismer ved mikroinjektion af reagenser i ECM.
Ark af epitelceller dækker den ydre overflade af alle metazoer, linje indre organer og opdele dyrekroppen i diskrete rum. Epitelet adskiller også den indre krop fra det ydre miljø og beskytter det mod skader og infektion. Derfor var fremkomsten af epitellag en væsentlig del af udviklingen af flercellede dyr, og epitellag ses hos alle dyr fra hvirveldyr til de mest basale metazoer1. Epitelet af nogle organer er et enkelt monolag, såsom i lungeluftsække, blodkar og tarm2 såvel som i epidermis hos hvirvelløse dyr som planaria og cnidarians3. I andre væv, såsom hud4 og hornhinde5 hos hvirveldyr, er epitelet stratificeret, hvilket betyder, at der er flere epitelcellelag2. I alle tilfælde er det mest basale epitellag fastgjort til kældermembranen, et proteinark, der danner et specialiseret område af den ekstracellulære matrix (ECM)6,7,8.
Brud i epitelet skal hurtigt repareres for at genskabe et kontinuerligt epitelark. Skader på epitelet opstår under naturlige processer, såsom afgivelse af epitelceller i tarmen,9,10 og som følge af betændelse eller fysisk traume. Når en enkelt epitelcelle er beskadiget, skal den enten reparere sig selv eller fjernes, så de omgivende celler kan binde sig til hinanden og lukke hullet11,12. I sår, der er større end størrelsen på en enkelt celle, skal epitelceller bevæge sig for at nå hinanden og reparere arket13. Dette kan opnås ved cellespredning, hvis hullerne er små eller kan kræve migration af epitelceller fra kanten af et sår for at lukke sårgabet; Denne sidstnævnte proces kaldes re-epithelialisering14,15. I embryonale væv spredes epitelceller og migrerer for at lukke sår eller trækkes over kløften ved sammentrækning af actomyosinkabler, der dannes mellem cellerne ved sårmargenen i en mekanisme, der ligner en pungstreng16. I mange voksne væv involverer re-epithelialisering migration af sammenhængende celleark, hvor celler opretholder deres kryds med naboceller14,17,18. I andre væv demonteres celle: celleforbindelser, og epitelceller opfører sig mere som mesenkymale celler og bevæger sig på en koordineret, men uafhængig måde ind i sårområdet under re-epithelialisering 14,19,20,21.
Epitelcellebevægelser reguleres af komplekse interaktioner mellem de migrerende celler og mellem cellerne og ECM. Mens der er en enorm mængde eksperimentel litteratur, der behandler mekanismer til såraktivering af epitelceller og efterfølgende migration, er der stadig meget at opdage. For eksempel er det oprindelige signal, der aktiverer epitelceller til at migrere som reaktion på et sår, ikke blevet endeligt identificeret 22, og det er heller ikke helt forstået, hvordan actin omfordeles for at skabe lamellipodia på siden af epitelceller tættest på såret 22,23,24,25,26,27. Kollektiv cellemigration kræver, at information fra celler ved såret deles med celler, der er distale til såret, og kommunikationsvejen er stadig uklar28. Celle:celle-kryds og celle:ECM-vedhæftede filer skal adskilles og reformeres, efterhånden som cellerne i arket omarrangerer sig selv, men regulering af denne proces forstås dårligt14,29. Fremskridt på disse og andre relaterede spørgsmål er ikke kun vigtigt som et grundlæggende biologisk problem, men også på grund af den kliniske betydning af korrekt sårheling. Sygdomme, der kompromitterer epitelcellernes evne til at migrere korrekt, resulterer i kroniske sår; et eksempel er den genetiske sygdom epidermolysis bullosa, hvor gener, der er involveret i fastgørelsen af epitelcellerne til ECM, muteres, hvilket resulterer i skrøbelig hud, der skræller og blærer. Re-epithelialisering er også kompromitteret i naturligt aldrende væv30,31. En bedre forståelse er derfor afgørende for at udvikle interventioner til forbedring af sårhelingsresultater.
Epitelcellemigration i sårheling er blevet undersøgt ved hjælp af både in vitro-tilgange og modelorganismer. De fleste undersøgelser af sårheling og mekanismer for cellemigration er udført i vævskultur, hvor monolag af en enkelt epitelcelletype dyrkes på et substrat, der erstatter ECM. Cellemonolag er enten ridset eller dyrket med stencils for at skabe huller i bestemte former og størrelser og observeres derefter32,33,34. In vitro-modellen muliggør en ideel visualisering af celleadfærd samt muligheden for at ændre substratets kvaliteter, udsætte celler for lægemidler og abiotiske og biotiske faktorer og transfektere celler med konstruktioner, der udtrykker eller undertrykker forskellige gener af interesse. Imidlertid kan denne reduktionistiske tilgang muligvis ikke fange nogle af de vigtige parametre, der er involveret i epitelcelleadfærd i en in vivo-sammenhæng, herunder kommunikation mellem forskellige celletyper og signalhændelser, der forekommer i ECM11. In vivo-modeller giver den autentiske kontekst af et sår med flere celletyper, overlappende signalveje og en kompleks ECM35. En sådan model for sårhelingsundersøgelser er musen19, hvor nylige fremskridt har gjort det muligt for forskere at observere epidermale celler under heling af sår i fuld tykkelse hos levende dyr36. Musen og andre in vivo-systemer giver dog udfordringer med at studere re-epithelialisering. For det første opvejes den store fordel ved at observere celleadfærd i en naturlig sammenhæng af kompleksiteten af de tidsmæssigt overlappende begivenheder, der opstår under sårheling af hvirveldyr, herunder blodkoagulation, rekruttering af immunceller og betændelse, rekruttering af fibroblaster og celledifferentiering, revaskularisering og ombygning af ECM. Endvidere gør uigennemsigtige væv billeddannelse vanskelig. Drosophila larven og zebrafisk epidermis systemerne 37,38 har overvundet nogle af disse vanskeligheder på grund af deres relative enkelhed39.
Vores laboratorium introducerede for nylig en ny model til undersøgelse af epitelsårheling: medusa (vandmænd) form af hydrozoan cnidarian Clytia hemisphaerica (Clytia)40. Clytia er en ny modelorganisme med et fuldt sekventeret og kommenteret genom 41, enkeltcelle RNAseq-transkriptom42 og protokoller på plads til genommodifikation (mutagenese og transgenese)43,44,45. Cnidarians er en af de ældste eksisterende slægter, der har epitellag, så forståelse af cnidarian sårheling giver indsigt i de forfædres veje, der sikrede epitelintegritet. For de veje, der er bevaret i hele livets træ, tilbyder Clytia et spændende nyt system til at studere epitelcelledynamik og den funktionelle regulering af sårheling in vivo.
Epitelet, der dækker den øvre overflade af Clytia medusa (exumbrella), er et monolag af gennemsigtige, pladeepitelceller, der er ca. 50 μm brede og 1-2 μm tykke (figur 1). De er knyttet til en ECM kaldet mesoglea - vandmændenes "gelé". Mesoglea er sammensætningsmæssigt ligner ECM, der findes hos andre dyr 46,47,48 inklusive hvirveldyr, har en kældermembran 40 og er fuldstændig gennemsigtig. Epitellaget i Clytia medusa kan let ridses eller såres (se nedenfor). Epithelets og ECM's enkelhed og gennemsigtighed muliggør billeddannelse i høj opløsning af cellerne og deres bevægelser under heling. For nylig karakteriserede Kamran et al. helingen af små sår i Clytia epitelet i detaljer40. Det blev påvist, at heling i Clytia sker gennem lamellipodia-baseret cellecrawling, cellespredning og kollektiv cellemigration samt lukning af pungstreng, der er mere typisk for embryonale systemer (selvom det tidligere er set i voksne dyrestrukturer som hornhinden49). Clytia sårheling er ekstremt hurtig, som det er set i andre systemer, der mangler en inflammatorisk respons40,50. Heling i Clytia exumbrella er helt afhængig af bevægelser af de eksisterende epitelceller - ingen celler formerer sig eller migrerer gennem ECM til sårstedet (supplerende film 1). Alle disse resultater tyder på, at Clytia er et nyttigt modelsystem til at studere epitelsårheling. Faktisk førte den lette billeddannelse af epitelceller i Clytia under sårheling til opdagelsen af, at epitelcellelamellipodier strækker sig og spredes over områder med udsat ECM, så længe der er en intakt kældermembran; Hvis kældermembranen er beskadiget, skifter epitelheling til en pungstrengmekanisme40. Dette var den første demonstration af en mekanisme, der ligger til grund for beslutningen om at lukke ved lamellipodia-baseret crawling versus lukning af pungstreng, hvilket fremhæver vigtigheden af specifikke celle: ECM-interaktioner i heling og observation af celler i deres naturlige kontekst.
Nedenfor beskrives protokoller til oprettelse og billeddannelse af enkeltcellede mikrosår, små sår, der primært lukker ved cellespredning, og store sår, der kræver kollektiv cellemigration for at lukke. Desuden beskrives en protokol for introduktion af små molekyler i ECM og epitelceller, hvilket tillader eksperimentelle forstyrrelser af formodede regulatoriske veje for sårheling.
1. Dyrekultur
- Vedligehold Clytia polypkolonier på mikroskopglas og medusae i kunstigt havvand (ASW) ved 18 °C i et zebrafiskesystem med 2 L zebrafisketanke til polypkolonier og specialfremstillede 5 L pseudokreiseltanke til medusae (supplerende figur 1)51. ASW består af 4% Instant Ocean i deioniseret (DI)H2O.
- Dyrene fodres dagligt med 2-3 dage gammel artemia som beskrevet51.
BEMÆRK: Sårhelingsbilleddannelse er lettere, hvis dyrene ikke for nylig er blevet fodret, da der er mindre snavs frigivet fra tarmen i synsfeltet. - Saml babymedusae fra de etablerede polypkolonier efter behov ved at placere kolonier i et 2 L bægerglas fyldt med 1 L ASW natten over. Brug 2-3 uger gammel kvindelig medusae til alle sårhelingsforsøg. Formering af Clytia er beskrevet detaljeret andetsteds51.
2. Såring
- Oprettelse af mikrosår i og mellem celler (20-500 μm2)
- Opret en modificeret overførselspipette ved at skære spidsen med en saks for at lave en større åbning (0,5-0,7 cm diameter).
BEMÆRK: Åbningen i pipetten skal være bred nok til at undgå skade på dyret. - Brug den modificerede overførselspipette til at placere medusa på et fordybningsglas med medusa-paraplyen opad med lige nok ASW til at dække dyret.
- Placer straks en dækseddel over dyret og billedet (se nedenfor for beskrivelse af billeddannelsen). Dæksedlen komprimerer mesoglea, og rebound af det komprimerede væv skaber en kraft, der skubber cellerne lidt fra hinanden52. Dette vises straks som mellemrum mellem hver celle og skader i nogle celler (figur 1B, B ', figur 2 og figur 3A-C).
- Opret en modificeret overførselspipette ved at skære spidsen med en saks for at lave en større åbning (0,5-0,7 cm diameter).
- Oprettelse af små epitelsår (0,02-0,125 mm2)
- Brug en modificeret overførselspipette (som ovenfor) til at placere medusa på et fordybningsglas med medusa-paraplyen opad.
- Brug en 200 μL pipettespids til forsigtigt at ridse overfladen af medusa. Blid ridser kan også skabe revner i kældermembranen, som er let synlige22. Dæk dyret med et dæksel til billeddannelse. Alternativt er placering af dæksedlen undertiden tilstrækkelig til at skabe små epitelsår, selv uden ridser (figur 1C, C ', figur 2 og figur 3A-C).
BEMÆRK: Tryk ikke ned, når du ridser overfladen af medusa, da dette beskadiger ECM og skaber en uregelmæssig overflade - epitelceller, der migrerer på en uregelmæssig overflade, er sværere at holde fokus.
- Oprettelse af store epitelsår (0,5-0,9 mm2)
- Lav en mikroinjektionsnål ved hjælp af en mikropipettetrækker og glaskapillarrør (trin 5.2). Anbring den tomme mikroinjektionsnål i en mikroinjektorholder, der er fastgjort til en mikromanipulator. Skær spidsen af nålen, så åbningen er ca. 20-40 μm.
BEMÆRK: Afskårne nåle til store epitelsår kan opbevares og genbruges for at øge konsistensen mellem eksperimenter. - Indstil holdtrykket på mikroinjektoren til nul, og indstil udskubningstrykket til ca. 20 PSI. Indstil mikroinjektoren til at levere en 2 s luftpuls.
BEMÆRK: Udskubningstrykket skal muligvis justeres baseret på nåleåbningens diameter (dvs. mindre spidser bruger højere tryk, mens større spidser bruger lavere tryk). - Placer medusa med eksparaplyen opad på et fordybningsglas på scenen i et dissekeringsomfang med lige nok ASW til at dække dyret. Brug mikromanipulatoren til at justere mikroinjektionsnålespidsen, så den er lige over vandet. For at gøre dette skal du forsigtigt dyppe spidsen i vand (vand kan komme ind i pipettespidsen) og derefter trække den tilbage, så den er tæt på medusas epiteloverflade.
BEMÆRK: Spidsen skal placeres over en kvadrant af medusa. Medusas radiale kanaler deler medusaklokken i fire forskellige kvadranter. Målretning mod en kvadrant vil resultere i renere billeddannelse, da gonaderne og de radiale kanaler er udelukket fra sårområdet. - Pulsluft ved at trykke på start på injektoren. Gentag pulsen på samme sted to til fire gange, afhængigt af spidsens bredde. Større spidser kræver færre impulser.
BEMÆRK: En fordybning i vandet/medusa forårsaget af luftpulsen skal være synlig. - Det sårede dyr dækkes med en dækseddel til billeddannelse af store sår (figur 1D, D').
- Følg nedenstående trin (afsnit 3) for billeddannelse af epitelsårheling.
- Lav en mikroinjektionsnål ved hjælp af en mikropipettetrækker og glaskapillarrør (trin 5.2). Anbring den tomme mikroinjektionsnål i en mikroinjektorholder, der er fastgjort til en mikromanipulator. Skær spidsen af nålen, så åbningen er ca. 20-40 μm.
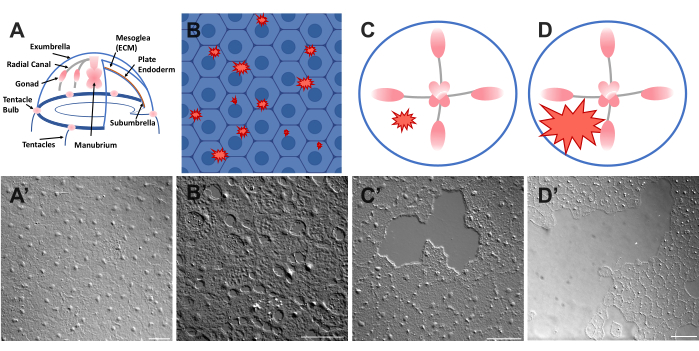
Figur 1: Intakt og såret exumbrella epitellag i Clytia medusa. (A) Tegneseriegrafik af Clytia medusa-kroppen. (A') Intakt medusa exumbrella epitel set ovenfra. (B) Tegneserie af encellede mikrosår (røde takkede former) med epitelceller i blåt. (B') Enkeltcellede mikrosår. (C) Tegneserie af et lille epitelsår (rød takket form). (C') Lille epitelsår. (D) Tegneserie af et stort epitelsår (rød takket form). (D') Stort epitelsår. Billeder blev alle opnået ved hjælp af DIC-mikroskopi. Skalastænger i (A'-C'): 50 μm. Skalabjælke i (D'): 100 μm. Klik her for at se en større version af denne figur.
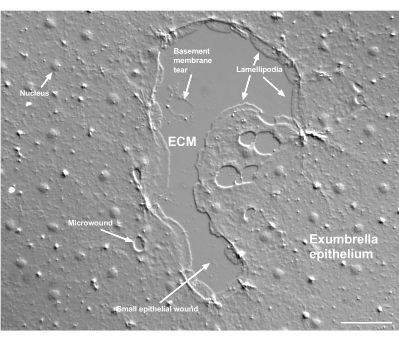
Figur 2: Sår i flere størrelser og en beskadiget kældermembran. Et typisk lille exumbrella epitelsår er vist, med etiketter, der angiver lamellipodier, der dannes fra marginale celler. Derudover ses mikrosår i og mellem epitelceller. Bemærk den lille kældermembranrivning i den øverste del af såret. Film 4 viser heling af dette sår. Skalabjælke: 50 μm. Klik her for at se en større version af dette tal.
3. Billeddannelse af epitelsårheling
- Sørg for, at mikroskopet er justeret til Köhler-belysning53, og at det er korrekt indstillet til differentialinterfererende kontrast (DIC) mikroskopi54. Epitelceller er næsten usynlige med standardoptik (figur 3D, E).
- Juster fokus til exumbrella. Selvom dette er et tyndt lag, skal sekskantede celler være klare.
BEMÆRK: Exumbrella og subumbrella er adskilt af en tyk mesogela, der understøttes af lodrette fibre. Subumbrellarcellerne er i samme brændplan som de radiale kanaler. Hvis du oprindeligt fokuserer på subumbrellar-laget, skal du justere fokus langsomt gennem mesoglea og lodrette fibre, indtil du finder exumbrella. - Identificer manuelt et sår til billedet. For store sår skal du bruge et 10x mål. For mindre sår og enkeltcellesår skal du bruge et 20x mål.
- Start et program, der indsamler billeder som en film i realtid, eller som indsamler en række billeder med jævne mellemrum. Overvåg fremskridtene for at sikre, at sårområdet ikke glider ud af synsfeltet, og at cellerne af interesse forbliver i fokus.
- Enkeltcellesår lukker inden for et minut; Forestil dig derfor deres lukning med en film.
- For at fange detaljer om celledynamik for små sår skal du indsamle billeder ca. hver 10. s. Lukning af små sår tager 20-50 min afhængig af størrelse.
- Tag ikke billeder af de uforseglede dias i mere end 45 minutter, da fordampning af vand fra objektglasset over tid fører til dyredød og brud på cellerne.
- For længere observation forsegles omkring dækslet med vaselin for at reducere fordampningen.
BEMÆRK: Nogle medusa kan pulsere på diaset, hvilket forstyrrer billeddannelsen. I dette tilfælde tjener montering af dyr i en 1:10 fortynding af 1% ethyl-3-aminobenzoatmethansulfonat (Tricaine), justeret til pH 7,5, i ASW som et effektivt bedøvelsesmiddel og har ingen tilsyneladende virkning på heling i en tidsramme på 1 time. Dyrene vil dog dø, hvis de efterlades i flere timer i Tricaine.

Figur 3: Oprettelse af et lille sår i exumbrellar epitelet. (A) Skånsom ridser af eksparaplyen med en 200 μL pipettespids for at skabe et lille epitelsår. (B) Placering af dæksedlen er undertiden tilstrækkelig til at skabe små epitelsår. (C) Medusa monteret på et fordybningsobjektglas. (D ) Lille epitelsårbillede uden DIC-optik og (E) med DIC-optik. Vægtstænger: 50 μm Klik her for at se en større version af denne figur.
4. Bedømmelse
- Forberedelse af billedfiler
BEMÆRK: For at behandle billedfilerne skal du bruge FIJI / ImageJ med opdaterede BioFormat-plugins.- Indstil skalaen til det korrekte pixel pr. mikron-forhold, før du registrerer billedstakken; Analyser > indstil skala. Dette er nødvendigt for at udtrække faktiske størrelsesmålinger i downstream-analyser.
- Ofte driver dyret lidt på mikroskopets dias; derfor, for at eliminere drift i film, skal du registrere billederne ved hjælp af FIJI-pluginets lineære stakjustering med SIFT. Plugins > registrering > lineær stakjustering med SIFT.
- Gem den registrerede stak som en .avi fil. Fil > Gem som > AVI ... I pop op-vinduet skal du indstille billedhastigheden (animerede figurer heri er indstillet til 10 fps) og klikke på OK. Brug dette output til at udføre sårhelingsanalyse.
- Analyse af sårområde
- Brug lassoværktøjet i FIJI/ImageJ til at skitsere såret ved at spore cellekanterne. Mål sårområdet, der lige er skitseret, med Kommando+M eller CTRL+M.
- Gentag måling af sårareal hver 10. ramme. Målingerne fra FIJI/ImageJ kan derefter plottes ved hjælp af Prisme 9 (figur 4).
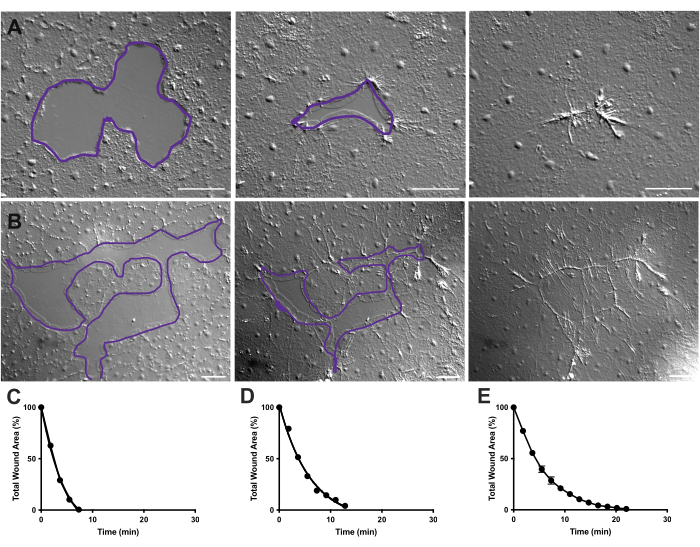
Figur 4: Analyse af sårområdet i små epitelsår. (A ) Eksempel på en lille epitelsårheling over 10 min. (B) Eksempel på en anden epitelsårheling over 21 min. De lilla konturer i A,B er sammenlignelige med målingerne af sårområder ved hjælp af lassoværktøjet i FIJI/ImageJ. (C) Normaliseret reduktion af sårområdet over tid i A. (D) Normaliseret reduktion af sårområdet over tid i B. (E) Gennemsnitlig reduktion af sårområdet over tid for 14 små sår. n = 14. Fejlbjælker centreret omkring gennemsnitlig ± SEM. Skalabjælker: 50 μm Klik her for at se en større version af denne figur.
5. Mesogleal injektioner
- Oprettelse af injektionsskål
- Polydimethylsiloxan (PDMS) fremstilles ved at kombinere en PDMS-base og et hærdningsmiddel i et forhold på 10 dele base til 1 del hærdningsmiddel efter vægt. Rør kraftigt for at blande basen og hærdningsmidlet helt.
- For at fjerne bobler sættes blandingen i et vakuumkammer i 15 minutter. Hæld blandingen i en 60 mm petriskål med mikrocentrifugerørhætter for at holde formen på plads. Placer straks formen på rørhætter i en 45 ° skråning og tape på plads. Formen er tre stablede, forskudte glasskinner limet sammen for at skabe kamme i den endelige injektionsskål.
- Anbring hele fadet, formen og blandingen i en ovn ved 60 °C i 2 timer for at hærde elastomeren. Fjern formen til en færdig injektionsskål.
- Træk i mikropipetter
- Brug en mikroelektrodetrækker til at designe et trækprogram. Brug et et-trins program med høj hastighed. Varmen er omtrent glasrampetestresultatet55,56. Kontroller resulterende mikropipetter for lange konsistente tilspidsninger.
BEMÆRK: Brug tyndvæggede borosilikatkapillærer af glas med en ydre diameter på 1,0 mm, en indvendig diameter på 0,75 mm og en længde på 10 cm.
- Brug en mikroelektrodetrækker til at designe et trækprogram. Brug et et-trins program med høj hastighed. Varmen er omtrent glasrampetestresultatet55,56. Kontroller resulterende mikropipetter for lange konsistente tilspidsninger.
- Injektion af farvestoffer og lægemidler
- Lav en mikroinjektionsnål (som ovenfor).
- Fyld mikroinjektionsnålen tilbage med en lang pipettespids med en overskydende mængde farvestof eller lægemiddel til injektion i medusa.
BEMÆRK: For Clytia bør dimethylsulfoxid (DMSO) holdes ved en <1:100 fortynding med ASW, da højere DMSO-koncentrationer hæmmer sårheling. Ved injektion af en klar opløsning kan Fast Green FCF-opløsning (1:100 fortynding af 0,1% Fast Green FCF i ASW) tilsættes for at visualisere den injicerede væske. - Brug en modificeret overførselspipette som ovenfor til at placere en medusa med underparaplyen opad i en PDMS-injektionsskål med lige nok ASW til at dække dyret (figur 5C). Placer skålen på scenen med et dissekeringsomfang.
BEMÆRK: Begrænsning af overskydende ASW forhindrer medusa i at svømme i skålen og tillader mere vellykkede injektioner. - Fokuser på mikroinjektionsnålens spids og før den i vandet nær medusa. Med mikromanipulatoren skal du trykke nålen ind i skålen, indtil den bøjes og går i stykker. Denne spidsåbning er ca. 10-20 μm.
BEMÆRK: Denne nål kan bruges gentagne gange til de samme farvestof-/lægemiddelinjektioner den dag. Det anbefales at bruge et nyt tip hver dag og til separate farvestoffer / lægemidler. - Brug mikromanipulatoren til at indsætte spidsen af nålen gennem underparaplyen i mesoglea uden at punktere exumbrella.
BEMÆRK: En foldning / foldning af epitelet vil være mærkbar. Når nålen er indsat i medusa, ophører foldningen/foldningen. - På mikroinjektoren skal du indstille holdtrykket til nul og udstødningstrykket til ≤20 PSI. Injicer i en eller to kvadranter, fyld hver med en plet farvestof eller lægemiddel ca. 1/4 af arealet af den kvadrant.
BEMÆRK: Afhængigt af medusas størrelse er større eller mindre volumener passende på enkelte injektionssteder. Overfyldning af medusa resulterer i ekstrem skade på epitelet og endda dyrets død. - Afhængigt af hvilket farvestof eller lægemiddel der injiceres, placeres dyrene i et bægerglas frisk ASW for at muliggøre farvestof eller lægemiddeldiffusion og inkubation.
- Til billeddannelse monteres medusaen på et fordybningsglas ved hjælp af en modificeret overførselspipette, og dyret placeres, så paraplyen vender opad (figur 5). Dyr kan blive såret på dette stadium for at teste effekten af et injiceret reagens.
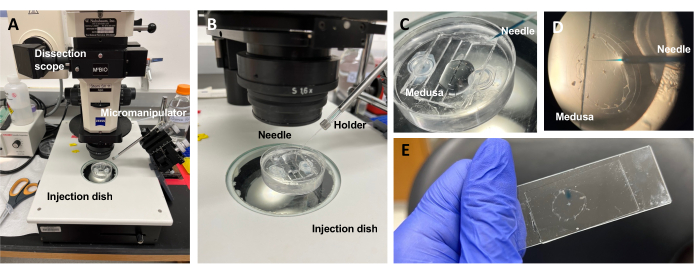
Figur 5: Injektionsopsætning til introduktion af farvestoffer eller lægemidler til ECM. (A) Opsætning af injektion. (B) Nærbillede af injektionsopstillingen, der viser mikroinjektionskanylens retning (ca. 45° vinkel i forhold til dyret i skålen). (C) Nærbillede af silikoneinjektionsskålen med medusa i en lille mængde ASW til injektion. (D) En mikroinjektionsnål fyldt med Fast Green FCF, der kommer ind i medusas mesoglea gennem underparaplyen. E) Efter injektion af Fast Green FCF i monteret medusa. Klik her for at se en større version af denne figur.
Efter protokollerne ovenfor blev enkeltcellede mikrosår, små sår og store sår afbildet. Registrerede stakke af billedfiler blev gemt som .avi filer.
I film 1 kan mikrosår ses at lukke mellem og inden i celler (figur 1 og figur 2). Små lamellipodier observeres under lukning efterfulgt af sammentrækning og heling. Affald er udelukket og frigivet i vandet. Healing er afsluttet på et minut eller mindre.
I film 2 og 3 heler små sår af forskellig form gennem dannelse af lamellipodia, forlængelse af lamellipodielle kontakter og spredning af celler ved sårmargenen, som tidligere beskrevet40 (figur 1 og figur 2). Celler i niveauer bag de marginale celler deltager ikke i heling af sår af denne størrelse, og der er heller ikke kollektiv cellemigration. Hurtig og progressiv lukning af epitelhuller efterfølges af vævskontraktion langs den nydannede sårsøm40. Den normaliserede helingshastighed for disse to sår, udtrykt som en procentdel af det oprindelige område over tid, er vist (figur 4C, D). Mens der er en vis variation i dynamikken i sårlukning, giver gennemsnittet af den procentvise områdelukning over tid for 14 sår i forskellige former fra 0,02-0,125 mm2 mulighed for at etablere en gennemsnitskurve for sårheling hos ubehandlede dyr (figur 4E).
Skader på kældermembranen kan tydeligt ses, når de opstår (figur 2). I film 4 spredes celler i margenen af et lille sår, hvor der er kældermembranskader, rundt om det beskadigede område, og mellemrumslukning afsluttes med en sammentrækning af pungstrengen.
Hvis vævet er dehydreret eller for beskadiget til at reparere, kan cellebevægelser stoppe, eller hele cellearket kan briste (film 5 og film 6). Dette sker normalt efter lange perioder med billeddannelse (45 minutter eller længere). Hvis cellesprængning sker tidligt i billeddannelsen, kasseres prøven.
Som vist i film 7 heler store sår i flere faser. For det første bliver kanten af såret glat og regelmæssigt på grund af sammentrækninger i margenen, som tidligere rapporteret57. Derefter ses lamellipodia at dannes fra cellerne ved sårmargenen, hvor lamellipodia bevæger sig fremad for at maksimere kontakten med tilstødende lamellipodia. Sporing af kernerne i celler ved sårmargenen og flere niveauer bag marginalcellerne viser, at store huller tæt ved kollektiv cellemigration40. Celler løsner sig aldrig, men bevæger sig sammen som et ark.
Indførelsen af farvestoffer og farmakologiske midler kan være et kraftfuldt værktøj til dissekering af biologiske mekanismer. Mange stoffer er udelukket fra Clytia (ikke vist), sandsynligvis på grund af slimlaget, der dækker dyrets overflade. Imidlertid kan mikroinjektion bruges til direkte at introducere molekyler i ECM, forstyrre ECM-strukturen eller forstyrre regulerende aktiviteter i ECM. Derudover er farvestoffer og andre molekyler i stand til at komme ind i epitelceller fra basalsiden. Figur 6 viser f.eks. nuklear farvning med Hoechst, membranfarvning med FM1-43 og hæmning af dannelsen af lamellipodia ved cytochalasin B, efter at disse reagenser er mikroinjiceret i ECM. Indførelsen af disse molekyler til ECM og epitelceller før sår tillader eksperimenter, der tester effekten af farmakologiske værktøjer på helingsprocessen.
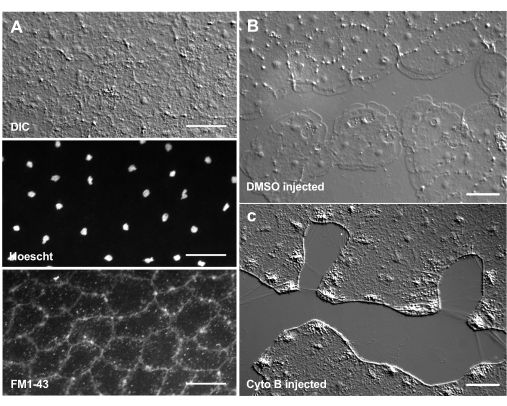
Figur 6: Medusaens epitelceller efter mikroinjektion af farvestoffer eller farmakologiske midler. (A) Epitelceller vist i toppanel 5 min efter injektion med 20 μM Hoechst (kerner) og 50 μM FM1-43 (membraner). (B,C) Sårheling efter injektion med 1:1.000 DMSO kontrol (B) eller 100 μM cytochalasin B (C). Sår blev lavet 15 minutter efter injektion. Billeder blev taget 5 minutter efter såret. Dannelsen af lamellipodia hæmmes af cytochalasin B. De tilsyneladende "fibre", der ofte ses mellem celler i sårområdet, menes at være resultatet af spændinger, der strækker kældermembranen - de pletter ikke med phalloidin (ikke vist). Skalabjælker: 50 μm. Klik her for at se en større version af denne figur.
Film 1: Time-lapse film af enkeltcelle mikrosårheling. Forløbet tid: 20 sek. Billedhastighed: 10 fps. Skalabjælke: 50 μm. Klik her for at downloade denne film.
Film 2: Time-lapse film om en lille epitelsårheling. Forløbet tid: 9 min 54 s. Billedhastighed: 10 fps. Skalabjælke: 50 μm. Klik her for at downloade denne film.
Film 3: Time-lapse film af en lille epitelsårheling. Dette sår er større og mere uregelmæssigt formet end såret i film 2. Forløbet tid: 20 min 54 s. Billedhastighed: 10 fps. Skalabjælke: 50 μm. Klik her for at downloade denne film.
Film 4: Time-lapse film om et lille sår og et mikrosår, der heler med en kældermembranrivning. Lamellipodia spredes rundt om kældermembranrivningen, selvom de kan gå videre over resten af ECM. Når sårets område med kældermembranskaden er omgivet, trækker en pungstrengkontraktion celler over regionen. Forløbet tid: 19 min 4 sek. Billedhastighed: 10 fps. Skalabjælke: 50 μm. Klik her for at downloade denne film.
Film 5: Celler, der dør i et lille epitelsår. Celledød skyldes sandsynligvis dehydrering af dyret. Forløbet tid: 4 min 24 s. Billedhastighed: 10 fps. Skalabjælke: 100 μm. Klik her for at downloade denne film.
Film 6: Et lille epitelsår heler ikke helt. Forløbet tid: 42 min 32 s. Billedhastighed: 10 fps. Skalabjælke: 50 μm. Klik her for at downloade denne film.
Film 7: Stor epitelsårheling. Forløbet tid: 25 min 29 s. Billedhastighed: 10 fps. Skalabjælke: 100 μm. Klik her for at downloade denne film.
Supplerende figur 1: Skemaer for Clytia-tankdimensioner. 3D visualisering af de specialfremstillede Clytia tanke. (A) Set forfra og bagfra. (B) Set fra siden. Udskæringen i stykket vist i grønt er dækket af nylonnet. Vand kommer ind i tanken direkte over masken, fejer over masken og skaber en cirkulær strøm. Vand kommer ud af systemet gennem hullet i endestykket vist med blåt. Klik her for at downloade denne fil.
Supplerende film 1: Acellulær ekstracellulær matrix i Clytia. Z-stak af Clytia taget ved hjælp af konfokal mikroskopi. Stakken fokuserer oprindeligt på exumbrella og scanner derefter hver 10 μm gennem ECM til pladeendoderm og underparaply. Billeder med DIC (venstre) og Hoechsts kernefarvning (højre) viser manglen på celler i ECM. Vægtstang: 100 μm. Klik her for at downloade denne fil.
Her præsenteres metoden til billeddannelse af sår in vivo i Clytia, en relativt ny invertebratmodelorganisme40,43,58. Der er flere faktorer, der gør dette system til et unikt og kraftfuldt forskningsværktøj, der adskiller sig fra andre modeller, der bruges til at studere sårheling og re-epithelialisering. For det første er monolagepitelet bundet til en gennemsigtig ECM og ligner således in vitro-vævskulturassays (figur 1, figur 2, figur 3, figur 4). Som i in vitro-assays kan celler afbildes i høj opløsning. Men i modsætning til i vævskultur er der et autentisk cellulært miljø og ECM, så sårheling kan ses i sammenhæng med de komplekse signalhændelser, der forekommer hos et levende skadet dyr. For det andet mangler Clytia inflammatoriske reaktioner, migrerende fibroblaster, vaskulatur og blod. Dette gør det muligt at undersøge re-epithelialiseringsprocessen in vivo i fravær af de overlappende hændelser, der forekommer hos mere komplekse voksne dyr under sårheling59. For det tredje er ECM acellulær (supplerende film 1) og stor, hvilket giver nem adgang med en mikroinjektionsnål (figur 5 og figur 6). Ved hjælp af denne tilgang kan forskere teste effekten af farmakologiske reagenser, der forstyrrer ECM-struktur eller signalering på sårheling in vivo. Reagenser kan også indføres i epitelceller, og deres virkninger på in vivo sårheling kan vurderes. For det fjerde er der protokoller, der findes til oprettelse af mutanter og transgene dyr i Clytia-systemet42,43,44,45. In vivo sårheling kan derfor observeres hos dyr med øget/nedsat ekspression af gener af interesse.
Der er flere kritiske trin i denne teknik. For det første, som vist i figur 3, er det nødvendigt at bruge et mikroskop, der er korrekt konfigureret til DIC-mikroskopi, da de flade, gennemsigtige epitelceller er næsten usynlige med standard lysmikroskopi. Det er også vigtigt at udvikle evnen til at såre dyr forsigtigt, så epitelet er beskadiget uden at skære ECM. En tilsvarende blid berøring er nødvendig for mikroinjektion af materialer i ECM, da omfattende skader på dyret under injektion kan kompromittere en efterfølgende analyse af sårheling. Mens der er en indlæringskurve til disse teknikker, har selv begynderstuderende mestret dem hurtigt i Malami-laboratoriet. Faktisk er disse protokoller blevet brugt til at demonstrere cellemigration i bachelorlaboratoriekurser ved University of Chicago.
For optimal billeddannelse er det vigtigt, at dyret ikke bevæger sig, og det valgte sårområde ikke driver ud af synsfeltet. Hvis dyr pulserer, er behandling med Tricaine som beskrevet meget effektiv. Til drifting er det ofte nødvendigt at flytte prøven manuelt. Disse bevægelser kan elimineres fra den endelige film ved hjælp af registreringsfunktionen i FIJI/ImageJ.
En begrænsning ved dette system er, at det ikke er muligt at skabe identiske sår, da sårene varierer i både form og størrelse ved hjælp af de her beskrevne metoder. Derfor kan det være svært at kvantificere den nøjagtige hastighed af sårlukning eller cellemigration. Positionsmarkører såsom kulstofkorn klæber til den udsatte ECM i et såret dyr og kan bruges til at måle hastigheden af kollektiv cellemigration i store sår (ikke vist). For analyse af små sårlukninger, selv med variabel sårstørrelse og -form, er der et begrænset interval af lukningshastigheder blandt sår af denne størrelse (figur 4). Det er derfor muligt kvantitativt at påvise virkningerne af promotoriske eller repressive farmakologiske reagenser.
Mens dette arbejde beskriver karakteriseringen af sårheling ved kun at bruge DIC-mikroskopi, kan de samme tilgange bruges til billedheling ved hjælp af fluorescens eller konfokal mikroskopi. For at hjælpe med dette er protokoller på plads til at generere transgene dyr, hvor forskellige cellulære og ekstracellulære proteiner er fluorescerende mærket. Samtidig billeddannelse med DIC og fluorescens kombineret med forstyrrelse af sårheling ved hjælp af farmakologiske midler eller mutante linjer vil være en stærk tilgang til forståelse af mekanismer, der ligger til grund for sårhelingsprocessen i epitelet.
Intet at afsløre.
E.E.L.L. er støttet af en bevilling fra National Science Foundation PRFB 2011010. Vi vil gerne takke Tsuyoshi Momose og Evelyn Houliston for at hjælpe os med at etablere vores Clytia kolonier, Jean-Baptiste Reynier for indsamling af mikrosårhelingsbilleder, Harry Kyriazes for konstruktion af pseudo-kreisel tanke og Elizabeth Baldo for at opretholde Clytia habitat. Figur 1B blev oprettet med BioRender.com.
| Name | Company | Catalog Number | Comments |
| 20500 ACE EKE Microscope Fiber Optic Light Source | Kramer Scientific Corporation | ||
| AxioCam 506 mono | ZEISS | 426557-0000-000-MA285 | |
| Capillary tubes | World Precision Instruments | TW1004 | |
| Cytochalasin B | Abcam | ab143482 | |
| Depression slides | Amscope | BS-C12 | |
| DMR with DIC options and fluorescence halogen lamp | Leica | ||
| Ethyl 3-aminobenzoate methanesulfonate | Sigma Aldrich | E10521-10G | |
| Fast Green FCF | Thermo Scientific | A16520-06 | |
| FM1-43 | Biotium | 70022 | Excitation/Emission: 480/598 nm |
| Hoechst 33342 | Thermo Scientific | 62249 | Excitation/Emission: 361/497 nm |
| imageJ | NIH | ||
| Microloader tips (0.5-10 μL /2-20 μL) | Eppendorf | 930001007 | |
| Micromanipulator | World Precision Instruments | 3301R / M3301L | |
| Microscope Cover Glass (22X40-1.5) | Fisherbrand | 12-544-BP | |
| Petri Dish (60 mm x 15 mm) | Fisherbrand | FB085713A | |
| PicoNozzle v2 | World Precision Instruments | 5430-ALL | |
| Pipette puller | Sutter Instrument Co | P-97 | |
| Pneumatic PicoPump | World Precision Instruments | PV820 | |
| Polycarbonate vacuum, desiccator | Bel-art | F42025-0000 | |
| Prism 9 | GraphPad | ||
| STEMI Sv11 Dissection scope | ZEISS | STEMI SV11 | |
| SYLGARD 184 | Dow Silicones | 1024001 | |
| Transfer pipettes | Fisherbrand | 13-711-7M | |
| Z-Hab mini system | Pentair | ||
| ZEN Microscopy software | Zeiss |
- Tyler, S. Epithelium-the primary building block for metazoan complexity. Integrative and Comparative Biology. 43 (1), 55-63 (2003).
- Kurn, H., Daly, D. T. Histology, Epithelial Cell. StatPearls. , (2022).
- Schempp, C., Emde, M., Wölfle, U. Dermatology in the Darwin anniversary. Part 1: Evolution of the integument. Journal of the German Society of Dermatology. 7 (9), 750-757 (2009).
- Lopez-Ojeda, W., Pandey, A., Alhajj, M., Oakley, A. M. Anatomy, Skin (Integument). StatPearls. , (2022).
- Bukowiecki, A., Hos, D., Cursiefen, C., Eming, S. A. Wound-healing studies in cornea and skin: parallels, differences and opportunities. International Journal of Molecular Sciences. 18 (6), 1257 (2017).
- Frantz, C., Stewart, K. M., Weaver, V. M. The extracellular matrix at a glance. Journal of Cell Science. 123 (24), 4195-4200 (2010).
- Hynes, R. O. The evolution of metazoan extracellular matrix. The Journal of Cell Biology. 196 (6), 671-679 (2012).
- Fidler, A. L., et al. Collagen IV and basement membrane at the evolutionary dawn of metazoan tissues. eLife. 6, 24176 (2017).
- Bullen, T. F., et al. Characterization of epithelial cell shedding from human small intestine. Laboratory Investigation; a Journal of Technical Methods and Pathology. 86 (10), 1052-1063 (2006).
- Watson, A. J. M., et al. Epithelial barrier function in vivo is sustained despite gaps in epithelial layers. Gastroenterology. 129 (3), 902-912 (2005).
- Sonnemann, K. J., Bement, W. M. Wound repair: toward understanding and integration of single-cell and multicellular wound responses. Annual Review of Cell and Developmental Biology. 27, 237-263 (2011).
- Abreu-Blanco, M. T., Verboon, J. M., Parkhurst, S. M. Single cell wound repair. BioArchitecture. 1 (3), 114-121 (2011).
- Fenteany, G., Janmey, P. A., Stossel, T. P. Signaling pathways and cell mechanics involved in wound closure by epithelial cell sheets. Current Biology. 10 (14), 831-838 (2000).
- Pastar, I., et al. Epithelialization in wound healing: a comprehensive review. Advances in Wound Care. 3 (7), 445-464 (2014).
- Rousselle, P., Braye, F., Dayan, G. Re-epithelialization of adult skin wounds: Cellular mechanisms and therapeutic strategies. Advanced Drug Delivery Reviews. 146, 344-365 (2019).
- Bement, W. M., Forscher, P., Mooseker, M. S. A novel cytoskeletal structure involved in purse string wound closure and cell polarity maintenance. The Journal of Cell Biology. 121 (3), 565-578 (1993).
- Vedula, S. R. K., Ravasio, A., Lim, C. T., Ladoux, B. Collective Cell migration: a mechanistic perspective. Physiology. 28 (6), 370-379 (2013).
- Li, L., He, Y., Zhao, M., Jiang, J. Collective cell migration: Implications for wound healing and cancer invasion. Burns & Trauma. 1 (1), 21-26 (2015).
- Bornes, L., Windoffer, R., Leube, R. E., Morgner, J., van Rheenen, J. Scratch-induced partial skin wounds re-epithelialize by sheets of independently migrating keratinocytes. Life Science Alliance. 4 (1), 202000765 (2021).
- Theveneau, E., Mayor, R. Collective cell migration of epithelial and mesenchymal cells. Cellular and Molecular Life Sciences. 70 (19), 3481-3492 (2013).
- Haensel, D., Dai, X. Epithelial-to-mesenchymal transition in cutaneous wound healing: where we are and where we are heading. Developmental Dynamics. 247 (3), 473-480 (2018).
- Cordeiro, J. V., Jacinto, A. The role of transcription-independent damage signals in the initiation of epithelial wound healing. Nature Reviews. Molecular Cell Biology. 14 (4), 249-262 (2013).
- Abreu-Blanco, M. T., Watts, J. J., Verboon, J. M., Parkhurst, S. M. Cytoskeleton responses in wound repair. Cellular and Molecular Life Sciences. 69 (15), 2469-2483 (2012).
- Klarlund, J. K., Block, E. R. Free edges in epithelia as cues for motility. Cell Adhesion & Migration. 5 (2), 106-110 (2011).
- Enyedi, B., Niethammer, P. Mechanisms of epithelial wound detection. Trends in Cell Biology. 25 (7), 398-407 (2015).
- Niethammer, P. The early wound signals. Current Opinion in Genetics & Development. 40, 17-22 (2016).
- Jacinto, A., Martinez-Arias, A., Martin, P. Mechanisms of epithelial fusion and repair. Nature Cell Biology. 3 (5), 117-123 (2001).
- Mayor, R., Etienne-Manneville, S. The front and rear of collective cell migration. Nature reviews. Molecular Cell Biology. 17 (2), 97-109 (2016).
- Gupta, S., Yap, A. S. How adherens junctions move cells during collective migration. Faculty Reviews. 10, 56 (2021).
- Blair, M. J., Jones, J. D., Woessner, A. E., Quinn, K. P. Skin structure-function relationships and the wound healing response to intrinsic aging. Advances in Wound Care. 9 (3), 127-143 (2020).
- Falanga, V., et al. Chronic wounds. Nature Reviews. Disease Primers. 8 (1), 50 (2022).
- Liang, C. -. C., Park, A. Y., Guan, J. -. L. In vitro scratch assay: a convenient and inexpensive method for analysis of cell migration in vitro. Nature Protocols. 2 (2), 329-333 (2007).
- Jonkman, J. E. N., et al. An introduction to the wound healing assay using live-cell microscopy. Cell Adhesion & Migration. 8 (5), 440-451 (2014).
- Poujade, M., et al. Collective migration of an epithelial monolayer in response to a model wound. Proceedings of the National Academy of Sciences. 104 (41), 15988-15993 (2007).
- Masson-Meyers, D. S., et al. Experimental models and methods for cutaneous wound healing assessment. International Journal of Experimental Pathology. 101 (1-2), 21-37 (2020).
- Park, S., et al. Tissue-scale coordination of cellular behaviour promotes epidermal wound repair in live mice. Nature Cell Biology. 19 (2), 155-163 (2017).
- Tsai, C. -. R., Wang, Y., Galko, M. J. Crawling wounded: molecular genetic insights into wound healing from Drosophila larvae. The International Journal of Developmental Biology. 62 (6-7-8), 479-489 (2018).
- Richardson, R., et al. Adult zebrafish as a model system for cutaneous wound-healing research. The Journal of Investigative Dermatology. 133 (6), 1655-1665 (2013).
- Erickson, J. R., Echeverri, K. Learning from regeneration research organisms: The circuitous road to scar free wound healing. Developmental Biology. 433 (2), 144-154 (2018).
- Kamran, Z., et al. In vivo imaging of epithelial wound healing in the cnidarian Clytia hemisphaerica demonstrates early evolution of purse string and cell crawling closure mechanisms. BMC Developmental Biology. 17 (1), 17 (2017).
- Chari, T., et al. Whole-animal multiplexed single-cell RNA-seq reveals transcriptional shifts across Clytia medusa cell types. Science Advances. 7 (48), (2021).
- Weissbourd, B., et al. A genetically tractable jellyfish model for systems and evolutionary neuroscience. Cell. 184 (24), 5854-5868 (2021).
- Momose, T., et al. High doses of CRISPR/Cas9 ribonucleoprotein efficiently induce gene knockout with low mosaicism in the hydrozoan Clytia hemisphaerica through microhomology-mediated deletion. Scientific Reports. 8 (1), 11734 (2018).
- Houliston, E., Leclère, L., Munro, C., Copley, R. R., Momose, T. Past, present and future of Clytia hemisphaerica as a laboratory jellyfish. Current Topics in Developmental Biology. 147, 121-151 (2022).
- Schmid, V., et al. The extracellular matrix (mesoglea) of hydrozoan jellyfish and its ability to support cell adhesion and spreading. Hydrobiologia. 216 (1), 3-10 (1991).
- Day, R. M., Lenhoff, H. M. Hydra mesoglea: a model for investigating epithelial cell-basement membrane interactions. Science. 211 (4479), 291-294 (1981).
- Zhang, X., et al. The collagens of hydra provide insight into the evolution of metazoan extracellular matrices. The Journal of Biological Chemistry. 282 (9), 6792-6802 (2007).
- Danjo, Y., Gipson, I. K. Actin 'purse string' filaments are anchored by E-cadherin-mediated adherens junctions at the leading edge of the epithelial wound, providing coordinated cell movement. Journal of Cell Science. 111 (22), 3323-3332 (1998).
- Arenas Gómez, C. M., Sabin, K. Z., Echeverri, K. Wound healing across the animal kingdom: Crosstalk between the immune system and the extracellular matrix. Developmental Dynamics. 249 (7), 834-846 (2020).
- Lechable, M., et al. An improved whole life cycle culture protocol for the hydrozoan genetic model Clytia hemisphaerica. Biology Open. 9 (11), (2020).
- Casares, L., et al. Hydraulic fracture during epithelial stretching. Nature Materials. 14 (3), 343-351 (2015).
- Wayne, R. Chapter 4 - Bright-Field Microscopy. Light and Video Microscopy (Third Edition). , 95-116 (2019).
- Murphy, D. B., Davidson, M. W. . Fundamentals of Light Microscopy and Electronic Imaging: Second Edition. , (2012).
- . Micropipette Techniques for Electrophysiology Available from: https://www.sutter.com/micropipette/cookbook.html (2022)
- Brown, A. L., Johnson, B. E., Goodman, M. B. Making patch-pipettes and sharp electrodes with a programmable puller). Journal of Visualized Experiments. (20), e939 (2008).
- Klarlund, J. K. Dual modes of motility at the leading edge of migrating epithelial cell sheets. Proceedings of the National Academy of Sciences. 109 (39), 15799-15804 (2012).
- Houliston, E., Momose, T., Manuel, M. Clytia hemisphaerica: a jellyfish cousin joins the laboratory. Trends in Genetics. 26 (4), 159-167 (2010).
- Rodrigues, M., Kosaric, N., Bonham, C. A., Gurtner, G. C. Wound healing: a cellular perspective. Physiological Reviews. 99 (1), 665-706 (2019).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved