Summary
Abstract
Introduction
Protocol
Representative Results
Discussion
Acknowledgements
Materials
References
Biology
Karakterisering av epitelial sårheling in vivo ved bruk av Cnidarian Model Organism Clytia hemisphaerica
Denne artikkelen beskriver en metode for å lage sår i epitelet til en levende Clytia hemisphaerica medusa og avbilde sårheling med høy oppløsning in vivo. I tillegg presenteres en teknikk for å introdusere fargestoffer og stoffer for å forstyrre signalprosesser i epitelceller og ekstracellulær matriks under sårheling.
Alle dyreorganer, fra huden til øynene til tarmene, er dekket med ark av epitelceller som gjør at de kan opprettholde homeostase samtidig som de beskytter dem mot infeksjon. Derfor er det ikke overraskende at evnen til å reparere epitelsår er kritisk for alle metazoans. Epitelial sårheling hos vertebrater innebærer overlappende prosesser, inkludert inflammatoriske responser, vaskularisering og reepitelisering. Regulering av disse prosessene involverer komplekse interaksjoner mellom epitelceller, naboceller og den ekstracellulære matrisen (ECM); ECM inneholder strukturelle proteiner, regulatoriske proteiner og aktive små molekyler. Denne kompleksiteten, sammen med det faktum at de fleste dyr har ugjennomsiktig vev og utilgjengelige ECM, gjør sårheling vanskelig å studere hos levende dyr. Mye arbeid med sårheling av epitel utføres derfor i vevskultursystemer, med en enkelt epitelcelletype belagt som et monolag på en kunstig matriks. Clytia hemisphaerica (Clytia) gir et unikt og spennende supplement til disse studiene, slik at sårheling av epitel kan studeres i et intakt dyr med en autentisk ECM. Det ektodermale epitelet av Clytia er et enkelt lag av store plateepitelceller, som tillater høyoppløselig avbildning ved bruk av differensiell forstyrrende kontrast (DIC) mikroskopi hos levende dyr. Fraværet av migrerende fibroblaster, vaskulatur eller inflammatoriske responser gjør det mulig å dissekere de kritiske hendelsene i reepitelialisering in vivo. Helbredelsen av ulike typer sår kan analyseres, inkludert enkeltcellede mikrosår, små og store epitelsår og sår som skader kjellermembranen. Lamellipodia dannelse, vesken streng sammentrekning, celle strekking, og kollektiv celle migrasjon kan alle observeres i dette systemet. Videre kan farmakologiske midler innføres via ECM for å modifisere celle:ECM-interaksjoner og cellulære prosesser in vivo. Dette arbeidet viser metoder for å lage sår i levende Clytia, fange filmer av helbredelse og undersøke helbredelsesmekanismer ved å mikroinjisere reagenser i ECM.
Ark av epitelceller dekker den ytre overflaten av alle metazoans, linje indre organer og deler dyrekroppen i diskrete rom. Epitelet skiller også den indre kroppen fra det ytre miljø og beskytter den mot skade og infeksjon. Derfor var fremkomsten av epitellag en viktig del av utviklingen av flercellede dyr, og epitellag ses hos alle dyr fra virveldyr til de mest basale metazoanene1. Epitelet til noen organer er et enkelt monolag, som i lungeluftsekkene, blodkarene og tarmen2, så vel som i epidermis av hvirvelløse dyr som planaria og cnidarians3. I andre vev, som hud4 oghornhinnen 5 av vertebrater, er epitelet stratifisert, noe som betyr at det er flere epitelcellelag2. I alle tilfeller er det mest basale epitellaget festet til kjellermembranen, et proteinark som danner en spesialisert region av den ekstracellulære matrisen (ECM) 6,7,8.
Brudd i epitelet må repareres raskt for å gjenskape et kontinuerlig epitelark. Skader på epitelet oppstår under naturlige prosesser, for eksempel utskillelse av epitelceller i tarmen,9,10 og som følge av betennelse eller fysisk traume. Når en enkelt epitelcelle er skadet, må den enten reparere seg selv eller elimineres slik at de omkringliggende cellene kan feste seg til hverandre og lukke hullet11,12. I sår som er større enn størrelsen på en enkelt celle, må epitelceller bevege seg for å nå hverandre og reparere arket13. Dette kan oppnås ved cellespredning hvis hullene er små eller kan kreve migrasjon av epitelceller fra sårkantene for å lukke sårgapet; Denne siste prosessen kalles re-epithelialization14,15. I embryonale vev sprer epitelceller seg og migrerer for å lukke sår eller trekkes over gapet ved sammentrekning av actomyosinkabler som dannes mellom cellene ved sårmarginen, i en mekanisme som ligner en veskestreng16. I mange voksne vev innebærer reepitelialisering migrasjon av sammenhengende celleark, hvor celler opprettholder sine kryss med naboceller14,17,18. I andre vev demonteres celle-celleforbindelser og epitelceller oppfører seg mer som mesenkymale celler, og beveger seg på en koordinert, men uavhengig måte inn i sårområdet under reepitelialisering 14,19,20,21.
Epitelcellebevegelser reguleres av komplekse interaksjoner mellom de migrerende cellene og mellom cellene og ECM. Selv om det finnes en enorm mengde eksperimentell litteratur som omhandler mekanismer for såraktivering av epitelceller og påfølgende migrasjon, gjenstår det fortsatt mye å oppdage. For eksempel er det første signalet som aktiverer epitelceller for å migrere som respons på et sår, ikke definitivt identifisert 22, og det er heller ikke helt forstått hvordan aktin omdisponeres for å skape lamellipodi på siden av epitelceller nærmest såret 22,23,24,25,26,27. Kollektiv cellemigrasjon krever at informasjon fra cellene i såret deles med celler distalt for såret, og kommunikasjonsveien er fortsatt uklar28. Celle:cellekryss og celle:ECM-vedlegg må demonteres og reformeres ettersom cellene i arket omorganiserer seg selv, men regulering av denne prosessen er dårlig forstått14,29. Å gjøre fremskritt på disse og andre relaterte spørsmål er ikke bare viktig som et grunnleggende biologisk problem, men også på grunn av den kliniske betydningen av korrekt sårheling. Sykdommer som kompromitterer epitelcellers evne til å migrere riktig, resulterer i kroniske sår; Et eksempel er den genetiske sykdommen epidermolysis bullosa, hvor gener involvert i vedlegget av epitelceller til ECM er mutert, noe som resulterer i skjør hud som skreller og blemmer. Reepitelisering er også kompromittert i naturlig aldrende vev30,31. En bedre forståelse er derfor viktig for å utvikle intervensjoner for å forbedre sårhelingsresultatene.
Epitelcellemigrasjon i sårtilheling har blitt studert ved bruk av både in vitro-tilnærminger og modellorganismer. De fleste studier av sårheling og mekanismer for cellemigrasjon har blitt utført i vevskultur, hvor monolayers av en enkelt epitelcelletype dyrkes på et substrat som erstatter ECM. Cellemonolag er enten riper eller vokst med sjablonger for å skape hull i bestemte former og størrelser og observeres deretter32,33,34. In vitro-modellen tillater en ideell visualisering av celleadferd, samt muligheten til å endre substratets kvaliteter, å eksponere celler for stoffer og abiotiske og biotiske faktorer, og å transfektere celler med konstruksjoner som uttrykker eller undertrykker forskjellige gener av interesse. Imidlertid kan denne reduksjonistiske tilnærmingen mislykkes i å fange opp noen av de viktige parametrene som er involvert i epitelcelleadferd i en in vivo-kontekst, inkludert kommunikasjon mellom forskjellige celletyper og signalhendelser som forekommer i ECM11. In vivo-modeller gir den autentiske konteksten til et sår, med flere celletyper, overlappende signalveier og en kompleks ECM35. En slik modell for sårhelingsstudier er musen19, der nyere fremskritt har gjort det mulig for forskere å observere epidermale celler under helbredelse av sår i full tykkelse hos levende dyr36. Musen og andre in vivo-systemer gir imidlertid utfordringer for å studere reepitelisering. For det første balanseres den store fordelen ved å observere celleadferd i en naturlig sammenheng av kompleksiteten til de tidsmessig overlappende hendelsene som oppstår under virveldyr sårheling, inkludert blodpropp, rekruttering av immunceller og betennelse, rekruttering av fibroblaster og cellededifferensiering, revaskularisering og remodellering av ECM. Videre gjør ugjennomsiktig vev avbildning vanskelig. Drosophila-larven og Zebrafish epidermis systems 37,38 har overvunnet noen av disse vanskelighetene på grunn av deres relative enkelhet39.
Vårt laboratorium introduserte nylig en ny modell for å studere sårheling av epitel: medusa-formen (maneter) av hydrozoan cnidarian Clytia hemisphaerica (Clytia)40. Clytia er en fremvoksende modellorganisme med et fullstendig sekvensert og kommentert genom41, enkeltcelle RNAseq-transkriptom 42, og protokoller på plass for genommodifisering (mutagenese og transgenese)43,44,45. Cnidarians er en av de eldste bevarte linjene som har epitellag, så forståelse av cnidarian sårheling gir innsikt i forfedrenes veier som sikret epitelintegritet. For de veiene som har blitt bevart gjennom livets tre, tilbyr Clytia et spennende nytt system for å studere epitelcelledynamikk og funksjonell regulering av sårheling in vivo.
Epitelet som dekker den øvre overflaten av Clytia medusa (exumbrella) er et monolag av gjennomsiktige, plateepitelceller som er ca. 50 μm brede og 1-2 μm tykke (figur 1). De er festet til en ECM kalt mesoglea - manetens "gelé". Mesoglea er komposisjonelt lik ECM funnet i andre dyr 46,47,48 inkludert vertebrater, har en kjellermembran 40, og er helt gjennomsiktig. Epitellaget i Clytia medusa kan lett ripes eller såres (se nedenfor). Enkelheten og gjennomsiktigheten til epitelet og ECM tillater høyoppløselig avbildning av cellene og deres bevegelser under helbredelse. Nylig karakteriserte Kamran et al. helbredelsen av små sår i Clytia-epitelet i detalj40. Det ble demonstrert at helbredelse i Clytia skjer gjennom lamellipodibasert cellekryping, cellespredning og kollektiv cellemigrasjon, samt veskestrenglukking som er mer typisk for embryonale systemer (selv om det tidligere er sett i voksne dyrestrukturer som hornhinnen49). Clytia sårheling er ekstremt rask, som det har blitt sett i andre systemer som mangler en inflammatorisk respons40,50. Helbredelse i Clytia-eksparaplyen er helt avhengig av bevegelser av de eksisterende epitelcellene - ingen celler sprer seg eller migrerer gjennom ECM til sårstedet (Supplemental Movie 1). Alle disse funnene tyder på at Clytia er et nyttig modellsystem for å studere epitelial sårheling. Faktisk førte den enkle avbildningen av epitelceller i Clytia under sårheling til oppdagelsen av at epitelcellelamellipodi strekker seg og sprer seg over områder med eksponert ECM så lenge det er en intakt kjellermembran; Hvis kjellermembranen er skadet, bytter epitelheling til en veskestrengmekanisme40. Dette var den første demonstrasjonen av en mekanisme som lå til grunn for beslutningen om å lukke ved lamellipodibasert gjennomgang versus lukking av veskestreng, og fremhevet viktigheten av spesifikke celle:ECM-interaksjoner i helbredelse og å observere celler i deres naturlige kontekst.
Nedenfor er protokoller beskrevet for å lage og avbilde encellede mikrosår, små sår som lukkes primært ved cellespredning, og store sår som krever kollektiv cellemigrasjon for å lukke. Videre er det beskrevet en protokoll for innføring av små molekyler i ECM og epitelceller, noe som tillater eksperimentelle forstyrrelser av antatte regulatoriske veier for sårheling.
1. Dyrekultur
- Opprettholde Clytia polyppkolonier på mikroskopglass og medusae i kunstig sjøvann (ASW) ved 18 °C i et sebrafisksystem, med 2 L sebrafisktanker for polyppkolonier og skreddersydde 5 L pseudo-kreiseltanker for medusae (tilleggsfigur 1)51. ASW består av 4% Instant Ocean i avionisert (DI) H2O.
- Fôr dyrene daglig med 2-3 dager gammel artemia som beskrevet51.
MERK: Sårhelingsavbildning er lettere hvis dyrene ikke nylig har blitt matet, da det er mindre rusk som slippes ut fra tarmen til synsfeltet. - Samle baby medusae fra de etablerte polypkoloniene etter behov ved å plassere kolonier i et 2 L beger fylt med 1 L ASW over natten. Bruk 2-3 uker gamle kvinnelige medusae for alle sårhelingseksperimenter. Forplantning av Klytia har blitt beskrevet i detalj andre steder51.
2. Sår
- Lage mikrosår i og mellom celler (20-500 μm2)
- Lag en modifisert overføringspipett ved å klippe spissen med en saks for å lage en større åpning (0,5-0,7 cm diameter).
MERK: Åpningen i pipetten skal være bred nok til å unngå skade på dyret. - Bruk den modifiserte overføringspipetten til å plassere medusa på et forsenkningslysbilde med medusa-paraplyen vendt oppover, med akkurat nok ASW til å dekke dyret.
- Legg en dekkseddel over dyret og bildet umiddelbart (se nedenfor for beskrivelse av bildebehandling). Dekselet komprimerer mesoglea, og rebound av det komprimerte vevet skaper en kraft som skyver cellene litt fra hverandre52. Dette vises umiddelbart som mellomrom mellom hver celle og skade i noen celler (figur 1B,B', figur 2 og figur 3A-C).
- Lag en modifisert overføringspipett ved å klippe spissen med en saks for å lage en større åpning (0,5-0,7 cm diameter).
- Opprette små epitelsår (0,02-0,125 mm2)
- Bruk en modifisert overføringspipette (som ovenfor) til å plassere medusa på en forsenkningsslide med medusa-paraplyen vendt oppover.
- Bruk en 200 μL pipettespiss til å skrape overflaten av medusa forsiktig. Skånsom skraping kan også skape riper i kjellermembranen, som er lett synlig22. Dekk dyret med en coverslip for avbildning. Alternativt er plassering av dekkslippet noen ganger tilstrekkelig til å skape små epitelsår selv uten riper (figur 1C,C', figur 2 og figur 3A-C).
MERK: Ikke trykk ned når du skraper overflaten av medusa, da dette skader ECM og skaper en uregelmessig overflate - epitelceller som migrerer på en uregelmessig overflate er vanskeligere å holde i fokus.
- Opprette store epitelsår (0,5-0,9 mm2)
- Lag en mikroinjeksjonskanyle ved hjelp av en mikropipettetrekker og kapillærrør av glass (trinn 5.2). Plasser den tomme mikroinjeksjonskanylen i en mikroinjektorholder festet til en mikromanipulator. Klipp nålens spiss slik at åpningen er ca. 20-40 μm.
MERK: Kuttnåler for store epitelsår kan lagres og gjenbrukes for å øke konsistensen mellom eksperimenter. - Sett holdetrykket på mikroinjektoren til null, og sett utkasttrykket til ca. 20 PSI. Sett mikroinjektoren til å levere en 2 s luftpuls.
MERK: Det kan være nødvendig å justere utkasttrykket basert på diameteren på nåleåpningen (dvs. mindre spisser vil bruke høyere trykk, mens større spisser vil bruke lavere trykk). - Plasser medusa med eksparaplyen vendt opp på en depresjonssklie på scenen av et dissekeringsomfang, med akkurat nok ASW til å dekke dyret. Bruk mikromanipulatoren til å justere nålespissen på mikroinjeksjonen slik at den er like over vannet. For å gjøre dette, dypp forsiktig spissen i vann (vann kan komme inn i pipettespissen), og trekk den deretter inn slik at den er nær medusas epiteloverflate.
MERK: Spissen skal plasseres over en kvadrant av medusa. Medusas radiale kanaler deler medusaklokken i fire forskjellige kvadranter. Målretting av en kvadrant vil resultere i renere avbildning, da gonadene og radialkanalene er ekskludert fra sårområdet. - Pulsluft ved å trykke på start på injektoren. Gjenta pulsen på samme sted to til fire ganger, avhengig av bredden på spissen. Større spisser krever færre pulser.
MERK: Et innrykk i vannet/medusa forårsaket av luftpulsen skal være synlig. - Dekk det sårede dyret med en dekkseddel for avbildning av store sår (figur 1D,D').
- Følg trinnene nedenfor (avsnitt 3) for avbildning av tilheling av epitel.
- Lag en mikroinjeksjonskanyle ved hjelp av en mikropipettetrekker og kapillærrør av glass (trinn 5.2). Plasser den tomme mikroinjeksjonskanylen i en mikroinjektorholder festet til en mikromanipulator. Klipp nålens spiss slik at åpningen er ca. 20-40 μm.
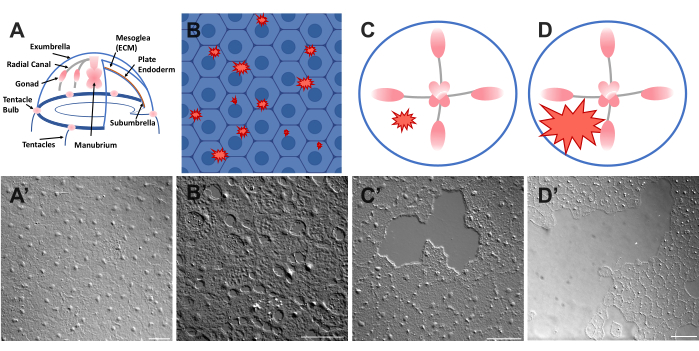
Figur 1 Intakt og såret eksumplyepitellag i Clytia medusa. (A) Tegneseriegrafikk av Clytia medusa-kroppen. (A') Intakt medusa exumbrella epitel sett ovenfra. (B) Tegneserie av encellede mikrosår (røde, taggete former) med epitelceller i blått. (B') Enkeltcelle mikrosår. (C) Tegneserie av et lite epitelsår (rød, taggete form). (C') Lite epitelial sår. (D) Tegneserie av et stort epitelsår (rød, taggete form). (D') Stort epitelsår. Alle bildene ble tatt ved hjelp av DIC-mikroskopi. Vektstenger i (A'-C'): 50 μm. Skala bar i (D'): 100 μm. Klikk her for å se en større versjon av denne figuren.
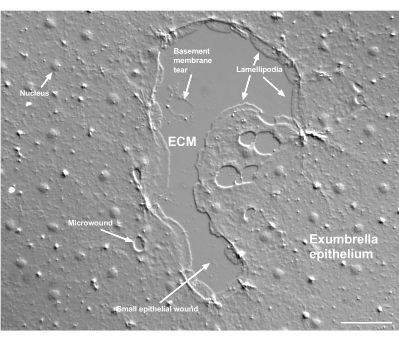
Figur 2 Sår i flere størrelser og en skadet kjellermembran. Et typisk lite eksumplyepitelial sår er vist, med etiketter som indikerer lamellipodi som dannes fra marginale celler. I tillegg ses mikrosår i og mellom epitelceller. Legg merke til den lille kjellermembranriften i den øvre delen av såret. Film 4 viser helbredelse av dette såret. Skala bar: 50 μm. Klikk her for å se en større versjon av denne figuren.
3. Imaging epitelial sårheling
- Kontroller at mikroskopet er justert for Köhler-belysning53, og at det er riktig konfigurert for DIC-mikroskopi (differensiell forstyrrende kontrast)54. Epitelceller er nesten usynlige med standard optikk (figur 3D,E).
- Juster fokus til paraplyen. Selv om dette er et tynt lag, bør sekskantede celler være klare.
MERK: Paraplyen og subparaplyen er adskilt av en tykk mesoglea som støttes av vertikale fibre. De subumbrallære cellene er i samme fokalplan som radialkanalene. Hvis du først fokuserer på det subumbrelære laget, justerer du fokuset sakte gjennom mesoglea og vertikale fibre til du finner eksparaplyen. - Identifiser et sår manuelt til bilde. For store sår, bruk et 10x mål. For mindre sår og encellede sår, bruk et 20x mål.
- Start et program som samler bilder som en film i sanntid, eller som samler en serie bilder med jevne mellomrom. Overvåk fremdriften for å sikre at sårområdet ikke driver ut av synsfeltet og at cellene av interesse forblir i fokus.
- Enkeltcellede sår lukkes innen et minutt; Se derfor for deg avslutningen med en film.
- For å fange detaljer om celledynamikk for små sår, samle bilder omtrent hver 10. Lukking av små sår tar 20-50 min avhengig av størrelse.
- Ikke se for deg de uforseglede lysbildene i mer enn 45 minutter, da fordampning av vann fra raset over tid fører til dyredød og brudd på cellene.
- For lengre observasjon, tett rundt dekselet med vaselin for å redusere fordampning.
MERK: Noen medusa kan pulsere på lysbildet, noe som forstyrrer bildebehandling. I dette tilfellet fungerer montering av dyr i en 1:10 fortynning av 1% etyl-3-aminobenzoatmetansulfonat (Tricaine), justert til pH 7,5, i ASW som et effektivt bedøvelsesmiddel og har ingen tilsynelatende effekt på helbredelse i en 1 timers tidsramme. Imidlertid vil dyrene dø hvis de blir liggende i flere timer i Tricaine.

Figur 3: Lage et lite sår i eksumbrelærepitelet. (A) Forsiktig skraping av eksparaplyen med en 200 μL pipettespiss for å skape et lite epitelsår. (B) Plassering av dekselet er noen ganger tilstrekkelig til å skape små epitelsår. (C) Medusa montert på et forsenkningslysbilde. (D ) Lite epitelsårbilde uten DIC-optikk og (E) med DIC-optikk. Skala barer: 50 μm Klikk her for å se en større versjon av denne figuren.
4. Analyse
- Klargjøre bildefiler
MERK: For å behandle bildefilene, bruk FIJI/ImageJ med oppdaterte BioFormat-plugins.- Sett skalaen til riktig piksel per mikron-forhold før du registrerer bildestakken; Analyser > angi skala. Dette er nødvendig for å trekke ut faktiske størrelsesmålinger i nedstrømsanalyser.
- Ofte driver dyret litt på mikroskoplysbildet; Derfor, for å eliminere drift i filmer, registrer bildene ved hjelp av FIJI plugin lineær stabeljustering med SIFT. Plugins > registrering > lineær stakkjustering med SIFT.
- Lagre den registrerte stakken som en .avi-fil. Fil > Lagre som > AVI ... I popup-vinduet angir du bildefrekvensen (animerte figurer her er satt til 10 fps) og klikker OK. Bruk denne utdataene til å utføre sårhelingsanalyse.
- Analyse av sårområde
- Bruk lassoverktøyet i FIJI/ImageJ til å skissere såret ved å spore cellekantene. Mål sårområdet som nettopp ble skissert med Kommando+M eller CTRL+M.
- Gjenta sårområdemåling hver 10. Målingene fra FIJI/ImageJ kan deretter plottes inn ved hjelp av prisme 9 (figur 4).
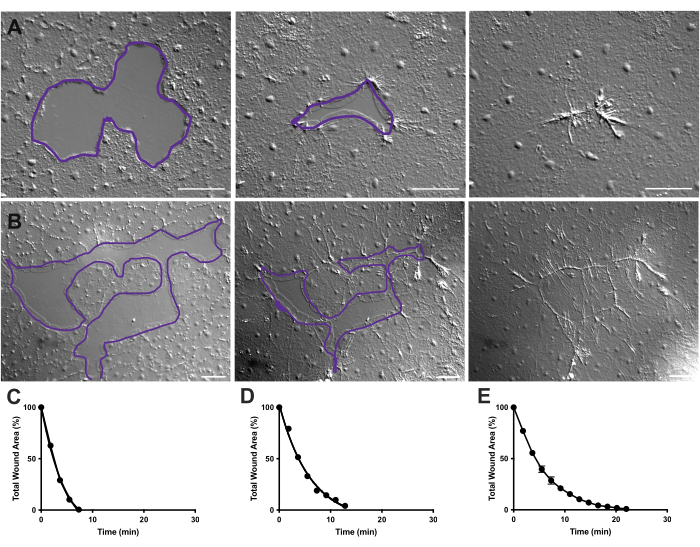
Figur 4 Analyse av sårområde ved små epitelsår. (A) Eksempel på et lite sårheling i epitel over 10 min. (B) Eksempel på en annen sårheling av epitel over 21 min. De lilla konturene i A,B er sammenlignbare med målingene av sårområder ved hjelp av lassoverktøyet i FIJI/ImageJ. (C) Normalisert reduksjon av sårområdet over tid i A. (D) Normalisert reduksjon av sårområdet over tid hos B. (E) Gjennomsnittlig reduksjon av sårområdet over tid for 14 små sår. n = 14. Feilfelt sentrert rundt gjennomsnittlig ± SEM. Skala barer: 50 μm Klikk her for å se en større versjon av denne figuren.
5. Mesogleal injeksjoner
- Opprette injeksjonsskål
- Forbered polydimetylsiloksan (PDMS) ved å kombinere en PDMS-base og herdemiddel, i et forhold på 10 deler base til 1 del herdemiddel etter vekt. Rør kraftig for å blande basen og herdemiddelet helt.
- For å fjerne bobler, sett blandingen i et vakuumkammer i 15 minutter. Hell blandingen i en 60 mm petriskål med mikrosentrifugerørhetter for å holde formen på plass. Legg formen umiddelbart på rørhetter i en 45 ° skråstilling og tape på plass. Formen er tre stablede, offsetglassglass limt sammen for å lage rygger i den endelige injeksjonsfatet.
- Sett hele fatet, formen og blandingen inn i en ovn ved 60 °C i 2 timer for å herde elastomeren. Fjern formen for en fullført injeksjonsfat.
- Trekking av mikropipette
- Bruk en mikroelektrodeavtrekker til å designe et trekkprogram. Bruk et ett-trinns program med høy hastighet. Varmen er omtrent glasset RAMP testresultat55,56. Kontroller resulterende mikropipetter for lange, konsistente avsmalninger.
MERK: Bruk tynnveggsglass borosilikatkapillærer med en 1,0 mm ytre diameter, 0,75 mm indre diameter og 10 cm lengde.
- Bruk en mikroelektrodeavtrekker til å designe et trekkprogram. Bruk et ett-trinns program med høy hastighet. Varmen er omtrent glasset RAMP testresultat55,56. Kontroller resulterende mikropipetter for lange, konsistente avsmalninger.
- Injeksjon av fargestoffer og rusmidler
- Lag en mikroinjeksjonsnål (som ovenfor).
- Fyll på mikroinjeksjonsnålen med en lang pipettespiss med et overflødig volum fargestoff eller legemiddel til injeksjon i medusa.
MERK: For Clytia bør dimetylsulfoksid (DMSO) holdes på en <1:100 fortynning med ASW, da høyere DMSO-konsentrasjoner hindrer sårheling. Hvis du injiserer en klar oppløsning, kan Fast Green FCF oppløsning (1:100 fortynning av 0,1% Fast Green FCF i ASW) tilsettes for å visualisere den injiserte væsken. - Bruk en modifisert overføringspipette som ovenfor, plasser en medusa med subparaplyen vendt opp i en PDMS-injeksjonsskål med akkurat nok ASW til å dekke dyret (figur 5C). Legg fatet på scenen av et dissekeringsomfang.
MERK: Begrensning av overflødig ASW forhindrer medusa i å svømme i parabolen og tillater mer vellykkede injeksjoner. - Fokuser på nålespissen og før den i vannet nær medusa. Trykk nålen inn i fatet med mikromanipulatoren til den bøyer seg og går i stykker. Denne spissåpningen er omtrent 10-20 μm.
MERK: Denne nålen kan brukes gjentatte ganger for samme fargestoff / legemiddelinjeksjoner den dagen. Det anbefales å bruke et nytt tips hver dag og for separate fargestoffer / legemidler. - Bruk mikromanipulatoren til å stikke nålens spiss gjennom subparaplyen inn i mesoglea uten å punktere eksparaplyen.
MERK: En krølling / folding av epitelet vil bli merkbar. Når nålen er satt inn i medusa, opphører krøllingen/foldingen. - Sett holdetrykket på mikroinjektoren til null og utkastingstrykket til ≤20 PSI. Injiser i en eller to kvadranter, fyll hver med et sted av fargestoff eller stoff omtrent 1/4 av arealet av den kvadranten.
MERK: Avhengig av størrelsen på medusa, er større eller mindre volumer egnet i enkeltinjeksjonssteder. Overfylling av medusa resulterer i ekstrem skade på epitelet og til og med døden til dyret. - Avhengig av hvilket fargestoff eller stoff som injiseres, plasseres dyr i et beger med fersk ASW for å tillate fargestoff eller medikamentdiffusjon og inkubasjon.
- For avbildning, monter medusa på et forsenkningslysbilde ved hjelp av en modifisert overføringspipette, og plasser dyret slik at eksparaplyen vender opp (figur 5). Dyr kan bli såret på dette stadiet for å teste effekten av et injisert reagens.
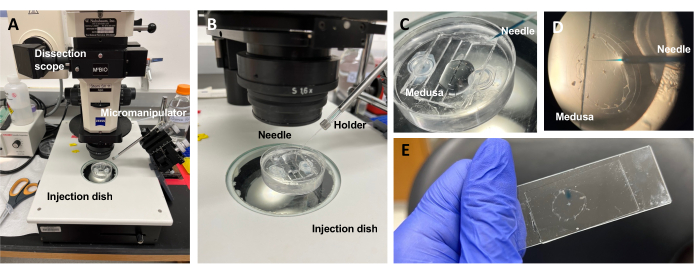
Figur 5: Injeksjonsoppsett for innføring av fargestoffer eller legemidler til ECM. (A) Oppsett av injeksjon. (B) Nærbilde av injeksjonsoppsettet som viser kanyleretning for mikroinjeksjon (ca. 45° vinkel i forhold til dyret i skålen). (C) Nærbilde av silikoninjeksjonsfatet med medusa i en liten mengde ASW til injeksjon. (D) En mikroinjeksjonsnål lastet med Fast Green FCF som kommer inn i medusas mesoglea gjennom subparaplyen. (E) Etter injeksjon av Fast Green FCF i en montert medusa. Klikk her for å se en større versjon av denne figuren.
Etter protokollene ovenfor ble encellede mikrosår, små sår og store sår avbildet. Registrerte stabler med bildefiler ble lagret som .avi filer.
I film 1 ser man mikrosår som lukker seg mellom og inne i cellene (figur 1 og figur 2). Små lamellipodier observeres under lukking, etterfulgt av sammentrekning og tilheling. Rusk er utelukket og sluppet ut i vannet. Healing er fullført om et minutt eller mindre.
I film 2 og 3 leges små sår av ulik form gjennom dannelse av lamellipodi, forlengelse av lamellipodialkontakter og spredning av celler i sårmargen, som tidligere beskrevet40 (figur 1 og figur 2). Celler i tier bak marginalcellene deltar ikke i helbredelse av sår av denne størrelsen, og det er heller ikke kollektiv cellemigrasjon. Rask og progressiv lukking av epitelgap etterfølges av vevskontraksjon langs den nydannede sårsøm40. Den normaliserte tilhelingshastigheten for disse to sårene, uttrykt som en prosentandel av det opprinnelige arealet over tid, er vist (figur 4C,D). Selv om det er en viss variasjon i dynamikken i sårlukking, gjør gjennomsnitt av prosentvis areallukking over tid for 14 sår av forskjellige former fra 0,02-0,125 mm2 det mulig å etablere en gjennomsnittlig kurve for sårheling hos ubehandlede dyr (figur 4E).
Skader på kjellermembranen kan tydelig ses når den oppstår (figur 2). I film 4 spres celler i margen av et lite sår der det er kjellermembranskader rundt det skadede området, og gaplukking fullføres med en veskestrengkontraksjon.
Hvis vevet er dehydrert eller for skadet til å repareres, kan cellebevegelsene stoppe, eller hele cellearket kan sprekke (film 5 og film 6). Dette skjer vanligvis etter lange perioder med bildebehandling (45 minutter eller lenger). Hvis cellesprengning skjer tidlig i avbildningen, kasseres prøven.
Som vist i film 7, leges store sår i flere stadier. For det første blir sårkanten glatt og regelmessig på grunn av sammentrekninger på marginen, som tidligere rapportert57. Deretter ser man at lamellipodi dannes fra cellene i sårmarginen, med lamellipodi som beveger seg fremover for å maksimere kontakten med tilstøtende lamellipodi. Sporing av kjernene i celler ved sårmarginen og flere lag bak marginalcellene viser at store hull lukkes ved kollektiv cellemigrasjon40. Celler løsner aldri, men beveger seg sammen som et ark.
Innføringen av fargestoffer og farmakologiske midler kan være et kraftig verktøy for å dissekere biologiske mekanismer. Mange stoffer er ekskludert fra Clytia (ikke vist), sannsynligvis på grunn av slimlaget som belegger overflaten av dyret. Imidlertid kan mikroinjeksjon brukes til å direkte introdusere molekyler i ECM, forstyrre ECM-strukturen eller forstyrre regulatoriske aktiviteter i ECM. I tillegg er fargestoffer og andre molekyler i stand til å komme inn i epitelceller fra basalsiden. For eksempel viser figur 6 nukleær farging med Hoechst, membranfarging med FM1-43 og hemming av lamellipodidannelse av cytochalasin B etter at disse reagensene er mikroinjisert i ECM. Innføringen av disse molekylene til ECM og epitelceller før sår tillater eksperimenter som tester effekten av farmakologiske verktøy på helingsprosessen.
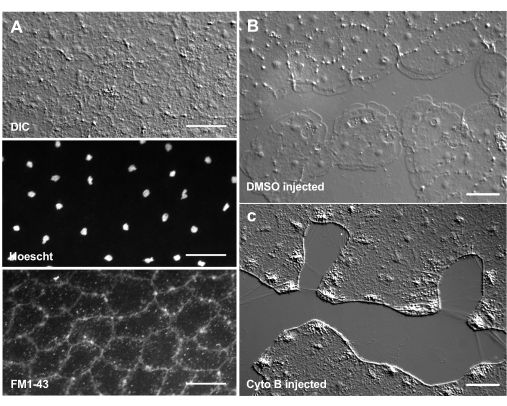
Figur 6 Epitelceller i medusa etter mikroinjeksjon av fargestoffer eller farmakologiske midler. (A) Epitelceller vist i topppanelet 5 minutter etter injeksjon med 20 μM Hoechst (kjerner) og 50 μM FM1-43 (membraner). (B,C) Sårtilheling etter injeksjon med 1:1000 DMSO kontroll (B) eller 100 μM cytochalasin B (C). Sår ble laget 15 min etter injeksjon. Bildene ble tatt 5 min etter såret. Dannelsen av lamellipodi hemmes av cytochalasin B. De tilsynelatende "fibrene" som ofte ses mellom celler i sårområdet, antas å være et resultat av spenning som strekker kjellermembranen - de flekker ikke med falloidin (ikke vist). Skala barer: 50 μm. Klikk her for å se en større versjon av denne figuren.
Film 1: Time-lapse-film av mikrosårheling med én celle . Tid gått: 20 s. Bildefrekvens: 10 bilder per sekund. Skala bar: 50 μm. Klikk her for å laste ned denne filmen.
Film 2: Time-lapse-film av en liten sårheling i epitel. Tid gått: 9 min 54 s. Bildefrekvens: 10 bilder per sekund. Skala bar: 50 μm. Klikk her for å laste ned denne filmen.
Film 3: Time-lapse-film av en liten sårheling i epitel. Dette såret er større og mer uregelmessig formet enn såret i film 2. Tid gått: 20 min 54 s. Bildefrekvens: 10 bilder per sekund. Skala bar: 50 μm. Klikk her for å laste ned denne filmen.
Film 4: Time-lapse-film av et lite sår og en mikrosårheling med en rift i kjellermembranen. Lamellipodia sprer seg rundt kjellermembranen, selv om de kan gå videre over resten av ECM. Når sårområdet med kjellermembranskaden er omringet, trekker en veskestrengkontraksjon celler over regionen. Tid gått: 19 min 4 s. Bildefrekvens: 10 bilder per sekund. Skala bar: 50 μm. Klikk her for å laste ned denne filmen.
Film 5: Celler som dør i et lite sår i epitel. Celledød skyldes sannsynligvis dehydrering av dyret. Tid gått: 4 min 24 s. Bildefrekvens: 10 bilder per sekund. Skala bar: 100 μm. Klikk her for å laste ned denne filmen.
Film 6: Et lite sår i epitel klarer ikke å fullføre helbredelsen. Tid gått: 42 min 32 s. Bildefrekvens: 10 bilder per sekund. Skala bar: 50 μm. Klikk her for å laste ned denne filmen.
Film 7: Stor tilheling av epitel. Tid gått: 25 min 29 s. Bildefrekvens: 10 bilder per sekund. Skala bar: 100 μm. Klikk her for å laste ned denne filmen.
Tilleggsfigur 1: Clytia tankdimensjonsskjemaer. 3D-visualisering av de skreddersydde Clytia-tankene. (A) Sett forfra og bakfra. (B) Sett fra siden. Utskjæringen i stykket vist i grønt er dekket med nylonnett. Vann kommer inn i tanken direkte over nettet, feier over nettet og skaper en sirkulær strøm. Vann kommer ut av systemet gjennom hullet i endestykket vist i blått. Klikk her for å laste ned denne filen.
Tilleggsfilm 1: Acellulær ekstracellulær matrise i Clytia. Z-stack av Clytia tatt ved hjelp av konfokal mikroskopi. Stakken fokuserer først på eksparaplyen og skanner deretter hver 10 μm gjennom ECM til plateendoderm og subumply. Bilder ved hjelp av DIC (venstre) og Hoechst kjernefysisk farging (høyre) demonstrerer mangelen på celler i ECM. Skala bar: 100 μm. Klikk her for å laste ned denne filen.
Her presenteres metodikken for avbildning av sår in vivo i Clytia, en relativt ny virvelløse modellorganisme40,43,58. Det er flere faktorer som gjør dette systemet til et unikt og kraftig forskningsverktøy, forskjellig fra andre modeller som brukes til å studere sårheling og reepitelisering. Først er monolagsepitelet festet til en gjennomsiktig ECM, og ligner dermed in vitro vevskulturanalyser (figur 1, figur 2, figur 3, figur 4). Som in vitro-analyser kan celler avbildes med høy oppløsning. Imidlertid, i motsetning til i vevskultur, er det et autentisk cellulært miljø og ECM, slik at sårheling kan ses i sammenheng med de komplekse signalhendelsene som oppstår i et levende skadet dyr. For det andre mangler Clytia inflammatoriske responser, migrerende fibroblaster, vaskulatur og blod. Dette gjør at reepitelialiseringsprosessen kan studeres in vivo i fravær av overlappende hendelser som forekommer hos mer komplekse voksne dyr under sårheling59. For det tredje er ECM acellulær (tilleggsfilm 1) og stor, noe som gir enkel tilgang med en mikroinjeksjonsnål (figur 5 og figur 6). Ved hjelp av denne tilnærmingen kan forskere teste effekten av farmakologiske reagenser som forstyrrer ECM-struktur eller signalering på sårheling in vivo. Reagenser kan også innføres i epitelceller, og deres effekter på in vivo sårheling kan vurderes. For det fjerde er det protokoller som eksisterer for å skape mutanter og transgene dyr i Clytia-systemet42,43,44,45. In vivo sårtilheling kan derfor observeres hos dyr med økt/redusert uttrykk av gener av interesse.
Det er flere kritiske trinn i denne teknikken. For det første, som vist i figur 3, er det nødvendig å bruke et mikroskop som er riktig konfigurert for DIC-mikroskopi, da de flate, gjennomsiktige epitelcellene er nesten usynlige med standard lysmikroskopi. Det er også viktig å utvikle ferdigheten til å såre dyr forsiktig slik at epitelet blir skadet uten å ødelegge ECM. En tilsvarende skånsom berøring er nødvendig for mikroinjeksjon av materialer i ECM, da omfattende skade på dyret under injeksjon kan kompromittere en påfølgende analyse av sårheling. Selv om det er en læringskurve for disse teknikkene, har selv nybegynnerstudenter mestret dem raskt i Malamy-laboratoriet. Faktisk har disse protokollene blitt brukt til å demonstrere cellemigrasjon i laboratoriekurs ved University of Chicago.
For optimal avbildning er det viktig at dyret ikke beveger seg og det valgte sårområdet ikke driver ut av synsfeltet. Hvis dyr pulserer, er behandling med Tricaine som beskrevet svært effektiv. For drifting er det ofte nødvendig å flytte prøven manuelt. Disse bevegelsene kan elimineres fra den endelige filmen ved hjelp av registreringsfunksjonen i FIJI/ImageJ.
En begrensning med dette systemet er at det ikke er mulig å lage identiske sår, da sårene varierer i både form og størrelse ved hjelp av metodene beskrevet her. Derfor kan det være vanskelig å kvantifisere den eksakte frekvensen av sårlukking eller cellemigrasjon. Posisjonsmarkører som karbonkorn fester seg til den eksponerte ECM i et såret dyr og kan brukes til å måle hastigheten på kollektiv cellemigrasjon i store sår (ikke vist). For små sårlukkingsanalyser, selv med variabel sårstørrelse og -form, er det begrenset lukkefrekvens blant sår av denne størrelsen (figur 4). Det er derfor mulig å kvantitativt oppdage effekten av promotive eller repressive farmakologiske reagenser.
Mens dette arbeidet beskriver karakterisering av sårheling ved hjelp av bare DIC-mikroskopi, kan de samme tilnærmingene brukes til bildeheling ved hjelp av fluorescens eller konfokal mikroskopi. For å hjelpe til med dette er protokoller på plass for å generere transgene dyr der forskjellige cellulære og ekstracellulære proteiner er fluorescerende merket. Samtidig avbildning med DIC og fluorescens, kombinert med forstyrrelse av sårheling ved bruk av farmakologiske midler eller mutantlinjer, vil være en kraftig tilnærming til å forstå mekanismer som ligger til grunn for sårhelingsprosessen i epitelet.
Ingenting å avsløre.
E.E.L.L. støttes av et stipend fra National Science Foundation PRFB 2011010. Vi vil gjerne takke Tsuyoshi Momose og Evelyn Houliston for å hjelpe oss med å etablere våre Clytia-kolonier, Jean-Baptiste Reynier for innsamling av mikrosårhelingsbilder, Harry Kyriazes for bygging av pseudo-kreisel-tankene, og Elizabeth Baldo for å opprettholde Clytia-habitatet. Figur 1B ble laget med BioRender.com.
| Name | Company | Catalog Number | Comments |
| 20500 ACE EKE Microscope Fiber Optic Light Source | Kramer Scientific Corporation | ||
| AxioCam 506 mono | ZEISS | 426557-0000-000-MA285 | |
| Capillary tubes | World Precision Instruments | TW1004 | |
| Cytochalasin B | Abcam | ab143482 | |
| Depression slides | Amscope | BS-C12 | |
| DMR with DIC options and fluorescence halogen lamp | Leica | ||
| Ethyl 3-aminobenzoate methanesulfonate | Sigma Aldrich | E10521-10G | |
| Fast Green FCF | Thermo Scientific | A16520-06 | |
| FM1-43 | Biotium | 70022 | Excitation/Emission: 480/598 nm |
| Hoechst 33342 | Thermo Scientific | 62249 | Excitation/Emission: 361/497 nm |
| imageJ | NIH | ||
| Microloader tips (0.5-10 μL /2-20 μL) | Eppendorf | 930001007 | |
| Micromanipulator | World Precision Instruments | 3301R / M3301L | |
| Microscope Cover Glass (22X40-1.5) | Fisherbrand | 12-544-BP | |
| Petri Dish (60 mm x 15 mm) | Fisherbrand | FB085713A | |
| PicoNozzle v2 | World Precision Instruments | 5430-ALL | |
| Pipette puller | Sutter Instrument Co | P-97 | |
| Pneumatic PicoPump | World Precision Instruments | PV820 | |
| Polycarbonate vacuum, desiccator | Bel-art | F42025-0000 | |
| Prism 9 | GraphPad | ||
| STEMI Sv11 Dissection scope | ZEISS | STEMI SV11 | |
| SYLGARD 184 | Dow Silicones | 1024001 | |
| Transfer pipettes | Fisherbrand | 13-711-7M | |
| Z-Hab mini system | Pentair | ||
| ZEN Microscopy software | Zeiss |
- Tyler, S. Epithelium-the primary building block for metazoan complexity. Integrative and Comparative Biology. 43 (1), 55-63 (2003).
- Kurn, H., Daly, D. T. Histology, Epithelial Cell. StatPearls. , (2022).
- Schempp, C., Emde, M., Wölfle, U. Dermatology in the Darwin anniversary. Part 1: Evolution of the integument. Journal of the German Society of Dermatology. 7 (9), 750-757 (2009).
- Lopez-Ojeda, W., Pandey, A., Alhajj, M., Oakley, A. M. Anatomy, Skin (Integument). StatPearls. , (2022).
- Bukowiecki, A., Hos, D., Cursiefen, C., Eming, S. A. Wound-healing studies in cornea and skin: parallels, differences and opportunities. International Journal of Molecular Sciences. 18 (6), 1257 (2017).
- Frantz, C., Stewart, K. M., Weaver, V. M. The extracellular matrix at a glance. Journal of Cell Science. 123 (24), 4195-4200 (2010).
- Hynes, R. O. The evolution of metazoan extracellular matrix. The Journal of Cell Biology. 196 (6), 671-679 (2012).
- Fidler, A. L., et al. Collagen IV and basement membrane at the evolutionary dawn of metazoan tissues. eLife. 6, 24176 (2017).
- Bullen, T. F., et al. Characterization of epithelial cell shedding from human small intestine. Laboratory Investigation; a Journal of Technical Methods and Pathology. 86 (10), 1052-1063 (2006).
- Watson, A. J. M., et al. Epithelial barrier function in vivo is sustained despite gaps in epithelial layers. Gastroenterology. 129 (3), 902-912 (2005).
- Sonnemann, K. J., Bement, W. M. Wound repair: toward understanding and integration of single-cell and multicellular wound responses. Annual Review of Cell and Developmental Biology. 27, 237-263 (2011).
- Abreu-Blanco, M. T., Verboon, J. M., Parkhurst, S. M. Single cell wound repair. BioArchitecture. 1 (3), 114-121 (2011).
- Fenteany, G., Janmey, P. A., Stossel, T. P. Signaling pathways and cell mechanics involved in wound closure by epithelial cell sheets. Current Biology. 10 (14), 831-838 (2000).
- Pastar, I., et al. Epithelialization in wound healing: a comprehensive review. Advances in Wound Care. 3 (7), 445-464 (2014).
- Rousselle, P., Braye, F., Dayan, G. Re-epithelialization of adult skin wounds: Cellular mechanisms and therapeutic strategies. Advanced Drug Delivery Reviews. 146, 344-365 (2019).
- Bement, W. M., Forscher, P., Mooseker, M. S. A novel cytoskeletal structure involved in purse string wound closure and cell polarity maintenance. The Journal of Cell Biology. 121 (3), 565-578 (1993).
- Vedula, S. R. K., Ravasio, A., Lim, C. T., Ladoux, B. Collective Cell migration: a mechanistic perspective. Physiology. 28 (6), 370-379 (2013).
- Li, L., He, Y., Zhao, M., Jiang, J. Collective cell migration: Implications for wound healing and cancer invasion. Burns & Trauma. 1 (1), 21-26 (2015).
- Bornes, L., Windoffer, R., Leube, R. E., Morgner, J., van Rheenen, J. Scratch-induced partial skin wounds re-epithelialize by sheets of independently migrating keratinocytes. Life Science Alliance. 4 (1), 202000765 (2021).
- Theveneau, E., Mayor, R. Collective cell migration of epithelial and mesenchymal cells. Cellular and Molecular Life Sciences. 70 (19), 3481-3492 (2013).
- Haensel, D., Dai, X. Epithelial-to-mesenchymal transition in cutaneous wound healing: where we are and where we are heading. Developmental Dynamics. 247 (3), 473-480 (2018).
- Cordeiro, J. V., Jacinto, A. The role of transcription-independent damage signals in the initiation of epithelial wound healing. Nature Reviews. Molecular Cell Biology. 14 (4), 249-262 (2013).
- Abreu-Blanco, M. T., Watts, J. J., Verboon, J. M., Parkhurst, S. M. Cytoskeleton responses in wound repair. Cellular and Molecular Life Sciences. 69 (15), 2469-2483 (2012).
- Klarlund, J. K., Block, E. R. Free edges in epithelia as cues for motility. Cell Adhesion & Migration. 5 (2), 106-110 (2011).
- Enyedi, B., Niethammer, P. Mechanisms of epithelial wound detection. Trends in Cell Biology. 25 (7), 398-407 (2015).
- Niethammer, P. The early wound signals. Current Opinion in Genetics & Development. 40, 17-22 (2016).
- Jacinto, A., Martinez-Arias, A., Martin, P. Mechanisms of epithelial fusion and repair. Nature Cell Biology. 3 (5), 117-123 (2001).
- Mayor, R., Etienne-Manneville, S. The front and rear of collective cell migration. Nature reviews. Molecular Cell Biology. 17 (2), 97-109 (2016).
- Gupta, S., Yap, A. S. How adherens junctions move cells during collective migration. Faculty Reviews. 10, 56 (2021).
- Blair, M. J., Jones, J. D., Woessner, A. E., Quinn, K. P. Skin structure-function relationships and the wound healing response to intrinsic aging. Advances in Wound Care. 9 (3), 127-143 (2020).
- Falanga, V., et al. Chronic wounds. Nature Reviews. Disease Primers. 8 (1), 50 (2022).
- Liang, C. -. C., Park, A. Y., Guan, J. -. L. In vitro scratch assay: a convenient and inexpensive method for analysis of cell migration in vitro. Nature Protocols. 2 (2), 329-333 (2007).
- Jonkman, J. E. N., et al. An introduction to the wound healing assay using live-cell microscopy. Cell Adhesion & Migration. 8 (5), 440-451 (2014).
- Poujade, M., et al. Collective migration of an epithelial monolayer in response to a model wound. Proceedings of the National Academy of Sciences. 104 (41), 15988-15993 (2007).
- Masson-Meyers, D. S., et al. Experimental models and methods for cutaneous wound healing assessment. International Journal of Experimental Pathology. 101 (1-2), 21-37 (2020).
- Park, S., et al. Tissue-scale coordination of cellular behaviour promotes epidermal wound repair in live mice. Nature Cell Biology. 19 (2), 155-163 (2017).
- Tsai, C. -. R., Wang, Y., Galko, M. J. Crawling wounded: molecular genetic insights into wound healing from Drosophila larvae. The International Journal of Developmental Biology. 62 (6-7-8), 479-489 (2018).
- Richardson, R., et al. Adult zebrafish as a model system for cutaneous wound-healing research. The Journal of Investigative Dermatology. 133 (6), 1655-1665 (2013).
- Erickson, J. R., Echeverri, K. Learning from regeneration research organisms: The circuitous road to scar free wound healing. Developmental Biology. 433 (2), 144-154 (2018).
- Kamran, Z., et al. In vivo imaging of epithelial wound healing in the cnidarian Clytia hemisphaerica demonstrates early evolution of purse string and cell crawling closure mechanisms. BMC Developmental Biology. 17 (1), 17 (2017).
- Chari, T., et al. Whole-animal multiplexed single-cell RNA-seq reveals transcriptional shifts across Clytia medusa cell types. Science Advances. 7 (48), (2021).
- Weissbourd, B., et al. A genetically tractable jellyfish model for systems and evolutionary neuroscience. Cell. 184 (24), 5854-5868 (2021).
- Momose, T., et al. High doses of CRISPR/Cas9 ribonucleoprotein efficiently induce gene knockout with low mosaicism in the hydrozoan Clytia hemisphaerica through microhomology-mediated deletion. Scientific Reports. 8 (1), 11734 (2018).
- Houliston, E., Leclère, L., Munro, C., Copley, R. R., Momose, T. Past, present and future of Clytia hemisphaerica as a laboratory jellyfish. Current Topics in Developmental Biology. 147, 121-151 (2022).
- Schmid, V., et al. The extracellular matrix (mesoglea) of hydrozoan jellyfish and its ability to support cell adhesion and spreading. Hydrobiologia. 216 (1), 3-10 (1991).
- Day, R. M., Lenhoff, H. M. Hydra mesoglea: a model for investigating epithelial cell-basement membrane interactions. Science. 211 (4479), 291-294 (1981).
- Zhang, X., et al. The collagens of hydra provide insight into the evolution of metazoan extracellular matrices. The Journal of Biological Chemistry. 282 (9), 6792-6802 (2007).
- Danjo, Y., Gipson, I. K. Actin 'purse string' filaments are anchored by E-cadherin-mediated adherens junctions at the leading edge of the epithelial wound, providing coordinated cell movement. Journal of Cell Science. 111 (22), 3323-3332 (1998).
- Arenas Gómez, C. M., Sabin, K. Z., Echeverri, K. Wound healing across the animal kingdom: Crosstalk between the immune system and the extracellular matrix. Developmental Dynamics. 249 (7), 834-846 (2020).
- Lechable, M., et al. An improved whole life cycle culture protocol for the hydrozoan genetic model Clytia hemisphaerica. Biology Open. 9 (11), (2020).
- Casares, L., et al. Hydraulic fracture during epithelial stretching. Nature Materials. 14 (3), 343-351 (2015).
- Wayne, R. Chapter 4 - Bright-Field Microscopy. Light and Video Microscopy (Third Edition). , 95-116 (2019).
- Murphy, D. B., Davidson, M. W. . Fundamentals of Light Microscopy and Electronic Imaging: Second Edition. , (2012).
- . Micropipette Techniques for Electrophysiology Available from: https://www.sutter.com/micropipette/cookbook.html (2022)
- Brown, A. L., Johnson, B. E., Goodman, M. B. Making patch-pipettes and sharp electrodes with a programmable puller). Journal of Visualized Experiments. (20), e939 (2008).
- Klarlund, J. K. Dual modes of motility at the leading edge of migrating epithelial cell sheets. Proceedings of the National Academy of Sciences. 109 (39), 15799-15804 (2012).
- Houliston, E., Momose, T., Manuel, M. Clytia hemisphaerica: a jellyfish cousin joins the laboratory. Trends in Genetics. 26 (4), 159-167 (2010).
- Rodrigues, M., Kosaric, N., Bonham, C. A., Gurtner, G. C. Wound healing: a cellular perspective. Physiological Reviews. 99 (1), 665-706 (2019).
ABOUT JoVE
Copyright © 2024 MyJoVE Corporation. All rights reserved