Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Оптимизированный автоматизированный анализ модуляции гомеостаза митохондрий живых нейронов изоформ-специфическими рецепторами ретиноевой кислоты
В этой статье
Резюме
Митохондриальная сеть чрезвычайно сложна, что делает ее очень сложной для анализа. Новый инструмент MATLAB анализирует митохондрии с конфокальными изображениями в реальном времени на таймлапс-изображениях, но приводит к большому объему вывода, требующему индивидуального ручного вмешательства. Для решения этой проблемы была разработана рутинная оптимизация, позволяющая быстро анализировать файлы.
Аннотация
Сложная митохондриальная сеть делает очень сложной сегментацию, отслеживание и анализ живых клеток. Инструменты MATLAB позволяют анализировать митохондрии в таймлапс-файлах, значительно упрощая и ускоряя процесс обработки изображений. Тем не менее, существующие инструменты выдают большой объем выходных данных, требующий индивидуального ручного вмешательства, а базовые экспериментальные установки позволяют выводить тысячи файлов, каждый из которых требует длительной и трудоемкой обработки.
Для решения этих проблем была разработана рутинная оптимизация, как в коде MATLAB, так и в формах live-script, что позволило ускорить анализ файлов и значительно сократить чтение документов и обработку данных. Со скоростью 100 файлов/мин оптимизация позволяет проводить общий быстрый анализ. Оптимизация позволяет получить результаты путем усреднения данных, специфичных для отдельных митохондрий, за все периоды времени, анализируя данные определенным образом, в соответствии с результатами, полученными существующими инструментами. Конфокальную визуализацию в реальном времени проводили с использованием метилового эфира красителя тетраметилродамина, а рутинная оптимизация была подтверждена путем обработки нейрональных клеток агонистами рецепторов ретиноевой кислоты (RAR), влияние которых на митохондрии нейронов установлено в литературе. Полученные результаты согласовывались с литературными данными и позволили в дальнейшем охарактеризовать поведение митохондриальной сети в ответ на изоформ-специфическую модуляцию RAR.
Эта новая методология позволила быстро и достоверно охарактеризовать сеть митохондрий целых нейронов, а также дифференцировать митохондрии аксонов и митохондрий клеточного тела, что является важной функцией для применения в области нейробиологии. Более того, этот протокол может быть применен к экспериментам с использованием быстродействующих методов лечения, позволяя визуализировать одни и те же клетки до и после лечения, выходя за рамки области неврологии.
Введение
Клеточные митохондрии находятся в центре всех физиологических состояний, и глубокое понимание их гомеостаза (митостаза) и поведения имеет первостепенное значение для помощи в определении фармакологического лечения широкого спектра заболеваний, включая раки болезнь Альцгеймера.
Митохондрии играют важнейшую клеточную роль в энергетическом гомеостазе, выработке АТФ, буферизации кальция и регуляции АФК, а митостаз необходим для поддержания белкового гомеостаза, поскольку молекулярные шапероныэнергетически зависимы. Они требуют постоянной и динамической модуляции и адаптации сети для эффективного удовлетворения клеточных потребностей, а транспорт митохондрий регулируется различными сигнальными путями; В предыдущей работе был описан один из таких путей — рецепторы ретиноевой кислоты (RARs)4,5. Ретиноевая кислота (РА) способствует росту аксонов и нейритов путем активации RAR. В первичных корковых нейронах мыши активация RAR-β стимулирует рост, скорость и подвижность митохондрий в нейрите6.
Учитывая адаптивность и динамику митохондриальной сети, возможность оценки митостаза в «реальном времени» имеет важное значение не только для исследования энергетического гомеостаза, но и для протеостаза, клеточного здоровья, пролиферации или передачи сигналов. Широко используемый метод оценки митостаза основан на конфокальной микроскопии после выделения митохондрий с помощью флуоресцентного красителя или маркера, а также на специальной микроскопической установке, позволяющей регулировать температуру и/илиCO2 7. Этот тип экспериментальной установки подразумевает, что за один раз выполняется одна экспериментальная репликация. В дополнение к экспериментальному повторению различных методов лечения, следует учитывать, что большинство экспериментов должны иметь свои технические повторы (когда на пластину изображается более одного положения), с серией фокальных плоскостей (z-стеков), записываемых в ряд временных точек. Таким образом, экспериментальный дизайн с тремя повторениями одного контрольного и двух сеансов обработки, с пятью позициями визуализации на пластину и 15 временными точками, приводит к 225 стопкам для обработки. Как правило, видеозаписи живых митохондрий анализировались путем построения кимографов, которые анализировались индивидуально8, в трудоемком процессе, требующем большого количества ручного ввода, даже при использовании компьютерных инструментов.
Недавнобыл описан алгоритм, который позволяет автоматически сегментировать и отслеживать митохондрии в 2-D и 3-D таймлапс-файлах живых клеток. Существуют и другие методы количественной оценки, и все они имеют свои ограничения10. Mitometer, автоматизированное приложение с открытым исходным кодом, особенно подходит для анализа интервальной съемки и динамики митохондрий, требующего минимального участия пользователя. Это приложение имеет ряд преимуществ по сравнению с другими существующими инструментами на основе MATLAB, а именно, позволяет автоматически обрабатывать отдельные стеки TIF, используя до 13 различных параметров, что особенно интересно для нейронаук, поскольку оно различает пери- и телеядерные митохондрии.
Однако для эксперимента, подобного описанному выше, эти 13 параметров, примененных к 225 стекам, приводят к 2925 отдельным выходным файлам. Для этого требуется четыре отдельных компьютерных входа, что в сумме составляет более 10 000 ручных входов, необходимых для загрузки всех выходных файлов. Для крупных экспериментальных проектов это приводит к неоправданно трудоемкому анализу каждого файла и интеграции данных. Здесь мы представляем рутинную оптимизацию, которая позволяет быстро анализировать файлы, значительно сокращая чтение документов и обработку данных, анализируя данные определенным образом, в соответствии с результатами существующих инструментов.
протокол
ПРИМЕЧАНИЕ: Этот протокол состоит из двух основных этапов: этап мокрой лаборатории, включающий культуру клеток и живую конфокальную микроскопию для получения изображений живых митохондрий (рис. 1), и этап in silico для анализа полученных изображений (рис. 2). Для автоматизированного анализа данных митохондрий с 3D-изображениями в реальном времени использовалось приложение MATLAB Mitometer, предоставленное Lefebvre et al.9. Рутинная оптимизация написана на MATLAB. Программное обеспечение, обновленные версии и обработка макросов ImageJ находятся в свободном доступе онлайн на GitHub по адресу https://github.com/JoseJoaoMV/Routine_Optimization_Mitometer_APP_MATLAB.
1. Живая микроскопия
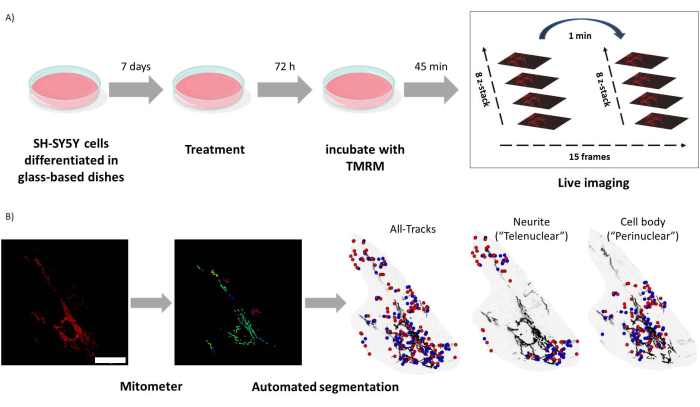
Рисунок 1: Протокол эксперимента. Клетки SH-SY5Y дифференцировали и лечили ретиноидами. (A) TMRM использовали для живого изображения здоровых митохондрий в обработанных клетках с помощью конфокального микроскопа, захватив интервальную съемку z-стека из пяти полей зрения. (B) Приложение для митометра MATLAB автоматически сегментирует и анализирует изображения митохондрий. В дополнение к анализу, это программное обеспечение автоматически различает митохондрии в соответствии с ядерной близостью. Синие точки – начальные позиции митохондрий; Красными точками обозначены конечные позиции. Масштабная линейка = 30 мкм. Аббревиатура: TMRM = тетраметилродамин, метиловый эфир. Пожалуйста, нажмите здесь, чтобы увидеть увеличенную версию этого рисунка.
- Клеточная культура
- Инкубируют клетки SH-SY5Y при 37 °C во влажной атмосфере с содержанием 5%CO2 и 95% воздуха, культивируют в равных частях среды MEM (минимальная эссенциальная среда) и F12 (питательная смесь F12 для ветчины), дополненные 10% фетальной бычьей сывороткой (FBS).
- Пластинчатые клетки SH-SY5Y в чашках со стеклянным дном при плотности 15 × 104 клетки/мл.
- Дифференциация клеток в течение 5 дней проводилась с помощью 10 мкМ полностью транс-ретиноевой кислоты в 1% FBS-содержащей питательной среде, а затем 2 дня лечения 10 ƞg/мл нейротрофического фактора головного мозга (BDNF).
- Лечение клеток
- Промывают клетки стерильным фосфатно-солевым буфером (PBS) и обрабатывают в течение 72 ч 10-7 М агонистами изоформ RAR, равными частями среды MEM (минимальная эссенциальная среда) и F12 (питательная смесь F12 Ham's F12) с добавлением 1% FBS.
ПРИМЕЧАНИЕ: В качестве агониста RARα использовался AM580; В качестве агониста RARβ использовался CD2314; Ch55 использовали в качестве агониста в качестве RARα и β коагониста; уВ качестве положительного контроля использовали РА; BMS493 использовался в качестве пан-антагониста RAR.
- Промывают клетки стерильным фосфатно-солевым буфером (PBS) и обрабатывают в течение 72 ч 10-7 М агонистами изоформ RAR, равными частями среды MEM (минимальная эссенциальная среда) и F12 (питательная смесь F12 Ham's F12) с добавлением 1% FBS.
- Конфокальная визуализация в реальном времени
- Питательную среду заменяют свежей 1%-ной питательной средой, содержащей FBS, с 20 нМ тетраметилродамином, метиловым эфиром (TMRM) в течение 45 мин.
ПРИМЕЧАНИЕ: TMRM представляет собой флуоресцентный краситель, проникающий в клетку, секвестрированный активными митохондриями, и этот инкубационный период позволяет TMRM достичь равновесия и быть поглощенным поляризованными митохондриями11. Визуализацию следует начинать до того, как будет установлено равновесие, так как интенсивность сигнала TMRM может искусственно увеличиваться во время визуализации. - Поместите клетки в инкубатор, подключенный к лазерному сканирующему конфокальному микроскопу, при температуре 37 °C.
- Захват изображений с помощью 63-кратного апохроматного объектива с масляным погружением с размером изображения 512 x 512 пикселей, полученным с апертурой точечного отверстия в 1 единицу Эйри, захват временного ряда из 15 кадров из пяти различных полей зрения в каждой ячейке и z-стека из 8 равноудаленных z-плоскостей. Результирующий LSM-файл представляет собой стек времени, позиции и z.
ПРИМЕЧАНИЕ: Настройки усиления, контрастности и яркости должны быть изначально оптимизированы с использованием минимальной мощности лазера, необходимой для использования всего динамического диапазона детектора, и поддерживаться постоянными на протяжении всего исследования, гарантируя, что все изображения выполняются в одинаковых условиях. В этой аппаратно-программной комбинации можно регистрировать до девяти различных положений, и микроскоп автоматически переключается между положениями изображения.
- Питательную среду заменяют свежей 1%-ной питательной средой, содержащей FBS, с 20 нМ тетраметилродамином, метиловым эфиром (TMRM) в течение 45 мин.
2. Анализ изображений
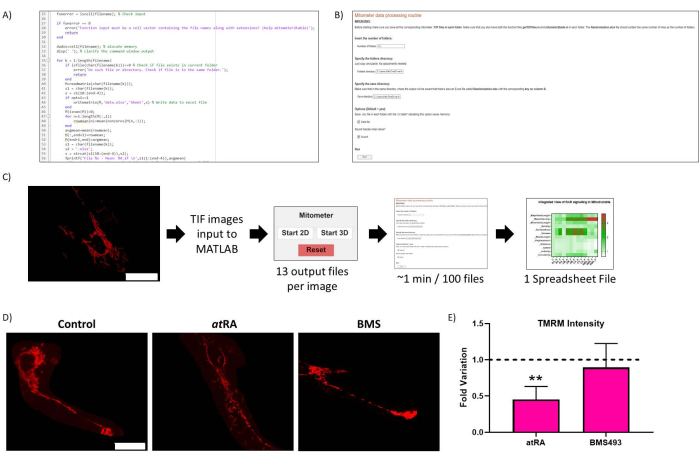
Рисунок 2: Рутинная оптимизация. (A) Репрезентативный код рутинной оптимизации. (B) Рутинная оптимизация Live-Script. (C) Рутинный рабочий процесс оптимизации. (D) Валидация результатов рутинной оптимизации: репрезентативное изображение митохондрий в необработанных клетках (левая панель), обработанных РА(10-7 М, 72 ч, средняя панель) и обработанных антагонистом RAR BMS493 (10-7 М, 72 ч, правая панель), визуализированное после инкубации с TMRM (20 нМ, 45 мин инкубации). Масштабная линейка = 30 мкм. (E) Интенсивность TMRM в митохондриях клеточного тела. Достоверного снижения при лечении полностью транс-ретиноевой кислотой (приРА 10-7 М, 72 ч) по сравнению с контролем (р=0,0062) не наблюдалось при лечении антагонистом РАР (BMS493, 10-7 М, 72 ч). Пять клеток были количественно определены из каждого из трех повторений для каждого условия. Пожалуйста, нажмите здесь, чтобы увидеть увеличенную версию этого рисунка.
- Обработка изображений
- Открывайте файлы в ImageJ 2.1.0 и разделяйте стеки позиций по визуальным полям: Откройте ImageJ и нажмите Строка меню | Изображение | Дубликат | Входные срезы/номер кадра | ОК.
ПРИМЕЧАНИЕ: Чтобы уменьшить количество повторяющихся входных данных в программное обеспечение, был разработан макрос ImageJ для облегчения дублирования и сохранения изображений визуального поля.
- Открывайте файлы в ImageJ 2.1.0 и разделяйте стеки позиций по визуальным полям: Откройте ImageJ и нажмите Строка меню | Изображение | Дубликат | Входные срезы/номер кадра | ОК.
- Макропротокол
- Нарисуйте область интереса (ROI) вокруг ячейки с помощью свободного инструмента выделения.
- Запустите макрос, открыв ImageJ и перейдя в строку меню | Плагины | Макросы | Запустите макрос Очистить фон и сохранить изображения.
ПРИМЕЧАНИЕ: В этом процессе изображения могут быть рандомизированы, сохраняя ключ решения в соответствии с требованиями оптимизации. - Определите размер пикселя и глубину воксела: Откройте ImageJ | Изображение и перейдите в Строка меню | Изображение | Свойства.
- Альтернативный прямой протокол
ПРИМЕЧАНИЕ: Эта альтернатива не использует макрос для обработки изображений- Найдите размер пикселя и глубину воксела: Откройте ImageJ | Откройте Изображение и перейдите в Строка меню | Изображение | Свойства.
- Нарисуйте ROI вокруг ячейки с помощью инструмента свободного выделения, убедившись, что она охватывает всю ячейку на протяжении 15 кадров.
- Перейдите в строку меню | Редактировать | Снаружи чисто.
- Перейдите в строку меню | Файл | Сохранить как | Выберите Tiff.
- Выберите «Папка сохранения» и нажмите «Сохранить».
ПРИМЕЧАНИЕ: На этом этапе изображения могут быть ослеплены/рандомизированы вручную, прежде чем продолжить анализ.
- Автоматизированный анализ изображений
- Подготовьте папки для файлов анализа.
- Создайте три основные папки, озаглавленные «Все треки», «Перинуклеарные треки» и «Теленуклеарные треки».
ПРИМЕЧАНИЕ: Они соответствуют основным параметрам автоматической трассы. - В каждой главной папке создайте вложенную папку для каждого изображения для обработки, определяемую числами от 1 и выше.
- Добавьте копию двух дополнительных файлов оптимизации (mitometer2table.m и getTXTfiles.m) в каждую папку изображений.
ПРИМЕЧАНИЕ: Эти файлы помогают в анализе данных и окончательном упорядочивании формата. Количество папок должно совпадать с количеством элементов в рандомизированной электронной таблице (.xlsx). После создания всех пронумерованных вложенных папок с дополнительными файлами для одного набора данных их можно скопировать и вставить в остальные наборы данных.
- Создайте три основные папки, озаглавленные «Все треки», «Перинуклеарные треки» и «Теленуклеарные треки».
- Подготовьте папки для файлов анализа.
- Используйте приложение MATLAB Mitometer для анализа изображений.
ПРИМЕЧАНИЕ: Этот протокол был запущен на митометре, установленном на MATLAB R2022a. Загружайте изображения партиями по 30 штук для оптимального распределения времени и выходных данных. Максимальный размер MAT-файла устанавливается родной файловой системой: по умолчанию операции «сохранения» могут создать файл < 231 байта (~2 ГБ); Вместо него можно использовать формат сохранения MAT-Files версии 7.3, так как он допускает максимальные размеры переменных, превышающие 2 ГБ.- Определите/измените версию MAT-файла по умолчанию: На вкладке « Главная » в разделе «Среда » нажмите «Настройки » и выберите «MATLAB | Общие сведения | MAT-файлы.
- Используйте инструмент MATLAB Митометр для анализа: Откройте MATLAB и перейдите в строку меню | ПРИЛОЖЕНИЯ | Открытый Митометр | Выберите Запустить 3D | Входные данные (Размер пикселя (мкм): 0.1395089/Время между кадрами (с): 2/Количество z-плоскостей: 8/Осевое расстояние между z-плоскостями (мкм): 0.418809 | Выберите изображения для ввода.
- Перейдите в боковое меню митометра, выберите «Изображение», нажмите «Выбрать выделенное», перейдите в строку меню митометра | Выбор треков | Просмотры треков | выберите All-Tracks, Telenuclear или Perinuclear | Строка меню митометра | Выберите Анализ | Выбор элемента (например, Длина) | выберите Сохранить в ".txt".
ПРИМЕЧАНИЕ: Можно загрузить несколько параметров одновременно, если они выбраны одновременно. - Распакуйте результирующие файлы в созданные папки (2.2.1).
- Рутинная оптимизация и анализ данных
- Подготовьте/адаптируйте файл "Randomization.xlsx", содержащий ключ для кодирования изображения.
- Вставьте список последовательных целых чисел от 1 и выше в столбец A.
ПРИМЕЧАНИЕ: Желательно хранить дубликат папки с изображениями с оригинальными названиями. - Поместите аналитические переменные в столбец B, состоящий из буквенно-цифровых символов.
ПРИМЕЧАНИЕ: Количество строк в документе должно соответствовать количеству папок, присутствующих в основном наборе данных. Скопируйте и вставьте этот файл "Randomization.xlsx" в два других основных набора данных.
- Вставьте список последовательных целых чисел от 1 и выше в столбец A.
- Оптимизированный анализ данных
- Дважды щелкните "executable.mlx", введите количество папок, укажите каталог папок (скопируйте каталог из верхней части папки) | каталог сохранения (скопируйте каталог сверху папки) | имя электронной таблицы в выходном файле и нажмите кнопку "Выполнить".
- При необходимости выполняйте статистический анализ.
ПРИМЕЧАНИЕ: По желанию можно выбрать создание .xlsx файла в каждой папке с .txt данными и звуковым оповещением об окончании анализа. Live Script выводит один файл электронной таблицы в табличном формате. В этих выходных данных столбцы представляют анализируемые параметры (например, "Длина большой оси"; «Интенсивность»), а линии представляют собой поля зрения аналитических переменных (например, «Контроль»).
- Подготовьте/адаптируйте файл "Randomization.xlsx", содержащий ключ для кодирования изображения.
Результаты
Чтобы улучшить и ускорить анализ выходных файлов в .txt формате, была закодирована рутинная оптимизация, которая считывает данные в соответствии с выходными файлами Mitometer .txt, со столбцами, представляющими рамку, и линиями, представляющими идентифицированные митохондрии. Рутинная оптими...
Обсуждение
Визуализация живых клеток позволяет создавать большие файлы, которые требуют серьезной вычислительной обработки, но даже самые современные инструменты требуют большого количества ручного ввода для обработки. Эта рутинная оптимизация направлена на упрощение процесса анализа митохо?...
Раскрытие информации
У авторов нет конфликта интересов, о котором можно было бы заявлять.
Благодарности
Получение изображений было выполнено на объекте LiM iBiMED, узле PPBI (Португальская платформа биовизуализации): POCI-01-0145-FEDER-022122. Эта работа была поддержана FCT (EXPL/BTM-SAL/0902/2021) LCF (CI21-00276), грантом DT от Fundação para a Ciência e Tecnologia Ministério da Educação e Ciência (2020.02006.CEECIND), грантом ATG-The Gabba Alumni Association для вице-президента и Институтом биомедицины iBiMED, Университет Авейру.
Материалы
| Name | Company | Catalog Number | Comments |
| AM580 | Sigma-Aldrich | A8843 | |
| BDNF | Thermo-Fisher | RP8642 | |
| BMS493 | Tocris Bioscience | 3409 | |
| CD2314 | Tocris Bioscience | 3824 | |
| Ch55 | Tocris Bioscience | 2020 | |
| Foetal Bovine Serum | Thermo-Fisher | 10270106 | |
| GraphPad Prism v4.0 | GraphPad Software, La Jolla | n/a | |
| Ham’s F12 Nutrient Mix | Thermo-Fisher | 21765029 | |
| MATLAB R2022a | MathWorks | n/a | |
| Minimal Essential Medium | Thermo-Fisher | 31095 | |
| Nunc Glass Bottom Dishes | Thermo-Fisher | 150680 | |
| Phosphate Buffer Saline Solution | Thermo-Fisher | 28372 | |
| Retinoic acid | Sigma-Aldrich | R2625 | |
| TMRM | Thermo-Fisher | T668 | |
| Zeiss LSM 510 | Carl Zeiss | n/a | Equiped with live-cell imaging culture chamber and 63x oil immersion objective |
Ссылки
- Trigo, D., Avelar, C., Fernandes, M., Sa, J., da Cruz, E. S. O. Mitochondria, energy, and metabolism in neuronal health and disease. FEBS Letters. 596 (9), 1095-1110 (2022).
- Zong, W. X., Rabinowitz, J. D., White, E. Mitochondria and cancer. Molecular Cell. 61 (5), 667-676 (2016).
- Clare, D. K., Saibil, H. R. ATP-driven molecular chaperone machines. Biopolymers. 99 (11), 846-859 (2013).
- Tourniaire, F., et al. All-trans retinoic acid induces oxidative phosphorylation and mitochondria biogenesis in adipocytes. Journal of Lipid Research. 56 (6), 1100-1109 (2015).
- Psarra, A. M., Sekeris, C. E. Nuclear receptors and other nuclear transcription factors in mitochondria: regulatory molecules in a new environment. Biochimica et Biophysica Acta. 1783 (1), 1-11 (2008).
- Trigo, D., Goncalves, M. B., Corcoran, J. P. T. The regulation of mitochondrial dynamics in neurite outgrowth by retinoic acid receptor beta signaling. FASEB Journal. 33 (6), 7225-7235 (2019).
- Mitra, K., Lippincott-Schwartz, J. Analysis of mitochondrial dynamics and functions using imaging approaches. Current Protocols in Cell Biology. Chapter 4 (Unit 4), 1-21 (2010).
- Sajic, M., et al. Impulse conduction increases mitochondrial transport in adult mammalian peripheral nerves in vivo. PLoS Biology. 11 (12), e1001754 (2013).
- Lefebvre, A., Ma, D., Kessenbrock, K., Lawson, D. A., Digman, M. A. Automated segmentation and tracking of mitochondria in live-cell time-lapse images. Nature Methods. 18 (9), 1091-1102 (2021).
- Chu, C. -. H., Tseng, W. -. W., Hsu, C. -. M., Wei, A. -. C. Image analysis of the mitochondrial network morphology with applications in cancer research. Frontiers in Physics. 10, 855775 (2022).
- Creed, S., McKenzie, M. Measurement of mitochondrial membrane potential with the fluorescent dye tetramethylrhodamine methyl ester (TMRM). Methods in Molecular Biology. 1928, 69-76 (2019).
- Kovalevich, J., Langford, D. Considerations for the use of SH-SY5Y neuroblastoma cells in neurobiology. Methods in Molecular Biology. 1078, 9-21 (2013).
- Sahin, M., Oncu, G., Yilmaz, M. A., Ozkan, D., Saybasili, H. Transformation of SH-SY5Y cell line into neuron-like cells: Investigation of electrophysiological and biomechanical changes. Neuroscience Letters. 745, 135628 (2021).
- Trigo, D., et al. Mitochondria dysfunction and impaired response to oxidative stress promotes proteostasis disruption in aged human cells. Mitochondrion. 69, 1-9 (2022).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
ISSN 1940-087X
Авторские права © 2025 MyJoVE Corporation. Все права защищены
Мы используем файлы cookie для улучшения качества работы на нашем веб-сайте.
Продолжая пользоваться нашим веб-сайтом или нажимая кнопку «Продолжить», вы соглашаетесь принять наши файлы cookie.