Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Bioimpresión 3D de hidrogeles fotoajustables para estudiar la activación de fibroblastos
En este artículo
Resumen
Este artículo describe cómo bioimprimir hidrogeles fotoajustables en 3D para estudiar el endurecimiento de la matriz extracelular y la activación de fibroblastos.
Resumen
Los hidrogeles fotosintonizables pueden transformarse espacial y temporalmente en respuesta a la exposición a la luz. La incorporación de este tipo de biomateriales en plataformas de cultivo celular y el desencadenamiento dinámico de cambios, como el aumento de la rigidez microambiental, permite a los investigadores modelar los cambios en la matriz extracelular (MEC) que se producen durante la progresión de la enfermedad fibrótica. En este trabajo se presenta un método para la bioimpresión 3D de un biomaterial de hidrogel fotosintonizable capaz de dos reacciones secuenciales de polimerización dentro de un baño de soporte de gelatina. La técnica de bioimpresión de Incrustación Reversible de Hidrogeles Suspendidos (FRESH) de forma libre se adaptó ajustando el pH del baño de soporte para facilitar una reacción de adición de Michael. En primer lugar, la biotinta que contenía poli(etilenglicol)-alfa metacrilato (PEGαMA) se hizo reaccionar fuera de la estequiometría con un reticulante degradable por células para formar hidrogeles blandos. Estos hidrogeles blandos se expusieron posteriormente al fotoinitador y a la luz para inducir la homopolimerización de los grupos no reaccionados y endurecer el hidrogel. Este protocolo cubre la síntesis de hidrogeles, la bioimpresión 3D, el fotoendurecimiento y las caracterizaciones de puntos finales para evaluar la activación de fibroblastos dentro de estructuras 3D. El método presentado aquí permite a los investigadores bioimprimir en 3D una variedad de materiales que se someten a reacciones de polimerización catalizadas por pH y podrían implementarse para diseñar varios modelos de homeostasis, enfermedad y reparación de tejidos.
Introducción
La bioimpresión 3D es una tecnología transformadora que permite a los investigadores depositar con precisión células y biomateriales dentro de volúmenes 3D y recrear la compleja estructura jerárquica de los tejidos biológicos. Durante la última década, los avances en la bioimpresión 3D han creado tejidos cardíacos humanos1, modelos funcionales de tejidos renales2, modelos de intercambio de gases dentro del pulmón3 y modelos tumorales para la investigación del cáncer4. La invención de las técnicas de bioimpresión 3D integradas, como la bioimpresión de forma libre y reversible de hidrogel suspendido (FRESH), ha hecho posible reproducir estructuras complejas de tejidos blandos como los vasos sanguíneos pulmonares5 e incluso el corazón humano6 en 3D. La bioimpresión 3D FRESH facilita la impresión capa por capa de biotintas blandas y de baja viscosidad a través de la extrusión en un baño de soporte de adelgazamiento por cizallamiento. El baño de soporte consiste en un material, como micropartículas de gelatina compactas, que actúa como un plástico Bingham y mantiene la forma y estructura previstas de la biotinta después de la impresión. Una vez que la construcción impresa se ha solidificado, el baño de soporte se puede disolver aumentando la temperatura a 37 °C7.
Un reciente artículo de revisión resumió los materiales que han sido bioimpresos en 3D en diversas publicaciones utilizando la técnica FRESH. Estos materiales de origen natural van desde el colágeno tipo I hasta el ácido hialurónico metacrilato y representan varios mecanismos de gelificación diferentes7. La mayoría de los estudios de investigación realizados con esta técnica de bioimpresión 3D emplean biomateriales estáticos que no cambian en respuesta a estímulos externos. Los biomateriales dinámicos de hidrogel fotosintonizable han sido utilizados por nuestro laboratorio y otros 8,9,10,11,12 para modelar una variedad de enfermedades fibróticas. A diferencia de los biomateriales estáticos, las biotintas fotosintonizables permiten crear un modelo suavizado con un valor de módulo elástico más bajo y luego endurecerlo para explorar las respuestas celulares a los aumentos en el endurecimiento microambiental.
Las enfermedades fibróticas se caracterizan por un aumento en la producción de la matriz extracelular que puede causar cicatrices y endurecimiento13. El endurecimiento del tejido puede iniciar más lesiones y destrucción del tejido impactado, causando daño permanente a los órganos e incluso la muerte; Los trastornos fibróticos son responsables de un tercio de la mortalidad en todo el mundo. Los fibroblastos producen exceso y aberración de matriz extracelular en este estado de enfermedad14,15. El aumento de la proliferación de fibroblastos y el depósito de matriz extracelular endurecen aún más el tejido y activan un bucle de retroalimentación positiva profibrótica16,17,18,19. El estudio de la activación de los fibroblastos es vital para comprender las enfermedades fibróticas. Aquí presentamos la hipertensión arterial pulmonar humana (HAP) como ejemplo de un trastorno fibrótico en el que es importante imitar la geometría 3D del vaso sanguíneo mediante bioimpresión 3D e introducir las capacidades de refuerzo dinámico de los hidrogeles fotosintonizables. La HAP es una afección en la que la presión en las arterias pulmonares principales supera los niveles normales y ejerce presión sobre el corazón, lo que aumenta la activación de los fibroblastos adventiciales de la arteria pulmonar humana (HPAAF) y endurece los tejidos de los vasos sanguíneos16,17,18,19. Una formulación de biotinta de poli(etilenglicol)-alfa metacrilato (PEGαMA) fotoajustable permite la rigidez temporal en las construcciones y ayuda a modelar tanto el tejido sano como la progresión de la enfermedad 5,8,9,10. La explotación de esta característica única permite cuantificar la activación y proliferación de HPAAF en respuesta al endurecimiento microambiental en 3D y puede proporcionar información valiosa sobre los mecanismos celulares implicados en esta enfermedad. El protocolo descrito aquí permitirá a los investigadores crear modelos 3D que recapitulen los cambios en el microambiente extracelular durante la progresión de la enfermedad o la reparación de tejidos y estudien la activación de fibroblastos.
Protocolo
1. Síntesis y caracterización de PEGαMA
NOTA: La síntesis de poli(etilenglicol)-alfa metacrilato (PEGαMA) se adaptó de Hewawasam et al . y se realizó en condiciones libres de humedad9.
- Pesa los reactivos.
NOTA: Por ejemplo, pese 5 g 10 kg/mol de PEG-hidroxilo de 8 brazos (PEG-OH) y 0,38 g de hidruro de sodio (NaH) (consulte la Tabla de materiales). - Agregue una barra de agitación al matraz Schlenk de 250 ml y purgue con argón.
- Disolver el PEG-OH en el volumen más bajo de tetrahidrofurano anhidro (THF) requerido para la disolución dentro del matraz Schlenk.
NOTA: Aproximadamente 80 ml de THF disolverán 5 g de PEG-OH. Agregue la cantidad mínima de THF necesaria para disolver el PEG-OH. - Agregue 3 veces el exceso molar de NaH a la mezcla de reacción y revuelva a temperatura ambiente (RT) durante 30 min.
- Agregue 6 veces el exceso molar de 2-(bromometil)acrilato (EBrMA, consulte la tabla de materiales) gota a gota al matraz Schlenk y cubra el recipiente de reacción con papel de aluminio para protegerlo de la luz. Agitar la reacción a temperatura ambiente durante aproximadamente 48 h.
NOTA: Para 5 g de PEG-OH y 0,38 g de NaH, use 3,68 ml de EBrMA para esta reacción. - Agregue unas gotas de ácido acético 1 N para apagar la reacción. Filtre al vacío la solución a través de un coadyuvante de filtración.
NOTA: La adición de ácido acético producirá burbujas de gas. Deje de agregar gotas de ácido acético cuando las burbujas dejen de formarse, ya que esto indica que la mezcla se ha enfriado con éxito. - Concentrar el filtrado en un evaporador rotativo y precipitar en éter dietílico a 4 °C. Dejar el precipitado protegido de la luz a 4 °C durante 12-18 h.
- Añade un papel de filtro Whatman a un embudo Buchner. Vierta lentamente la mezcla de reacción sobre el papel de filtro y use la succión al vacío para separar el precipitado del éter dietílico. Recoja el precipitado en un matraz de filtración seco y limpio.
- Secar el producto al vacío durante al menos 5 h o toda la noche a temperatura ambiente y disolver en el volumen mínimo de agua desionizada necesaria. Transfiera el producto disuelto a un tubo de diálisis (consulte la Tabla de materiales) y diálice con 3,5 L de agua desionizada durante al menos cuatro días. Cambiar el agua de diálisis cada 12 h.
NOTA: El producto aparecerá como polvo sólido blanco puro completamente seco después del secado al vacío. - Congelar rápidamente el producto y liofilizarlo durante aproximadamente 72 h o hasta que esté completamente seco.
- Disolver el producto en cloroformo D (CDCl3). Ejecute la muestra utilizando RMN de 1H con un protocolo que realiza 248 exploraciones con un tiempo de relajación de 2,5 s.
- Verifique la funcionalización y pureza del producto calibrando el pico de solvente CDCl3 a 7.26 PPM. Integre el pico para los protones de la red troncal PEG (d3.71) y calibre la integración a 114.
- Integre los picos restantes: RMN PEGαMA 1 H (300 MHz, CDCl 3): d (ppm) 1,36(t, 3H, CH 3-),3,71 (s, 114H, PEG CH 2-CH 2), 4,29 (t, s, 4H, -CH 2-C(O)-O-O, -O-CH 2-C(=CH 2)-), 5,93 (q, 1H, -C=CH 2), 6,34 (q, 1H, -C=CH 2) y compare la integración de los picos del grupo terminal de alquenos αMA con el valor esperado (1H) basado en la calibración de la red troncal PEG (Figura 1).
NOTA: Promedie los dos picos etiquetados como "a" (Figura 1) y multiplíquelos por 100 para obtener el porcentaje promedio de funcionalización de PEGαMA.
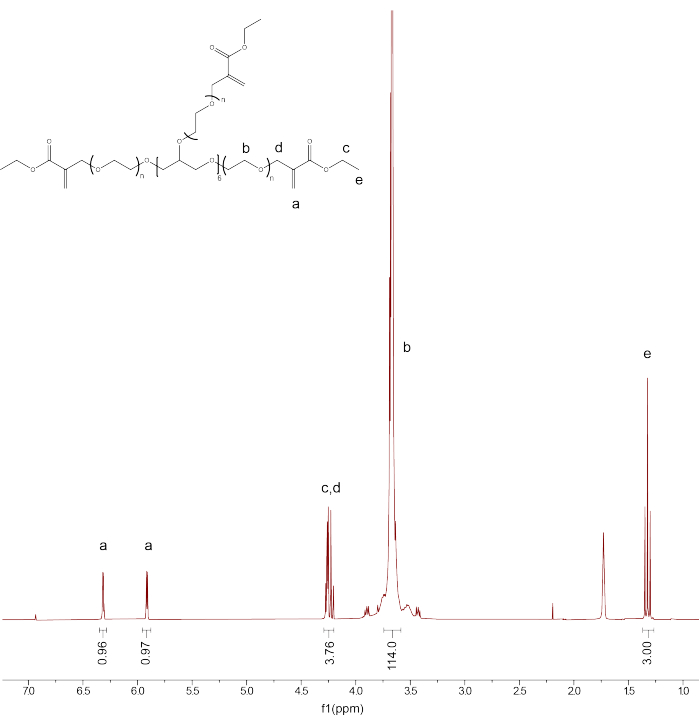
Figura 1: La RMN de protones confirmó la funcionalización exitosa de PEGαMA. El análisis de RMN se realizó en cloroformo-D (CDCl3) y mostró una funcionalización del 96,5%. RMN PEGαMA 1 H (300 MHz, CDCl3): d (ppm) 1,36(t, 3H, CH 3-),3,71 (s, 114H, PEG CH 2-CH 2), 4,29 (t, s, 4H, -CH 2-C(O)-O-O, -O-CH2-C(=CH 2)-), 5,93 (q, 1H, -C=CH 2), 6,34 (q, 1H, -C=CH 2). Haga clic aquí para ver una versión más grande de esta figura.
2. Diseño del modelo y configuración de la bioimpresora 3D
NOTA: Se modificó una impresora 3D disponible comercialmente (ver Tabla de Materiales) reemplazando la extrusora termoplástica con una extrusora de bomba de jeringa hecha a medida y adaptada de Hinton et al.20. Los diseños de código abierto están disponibles en línea: https://3d.nih.gov/users/awfeinberg.
- Abra el software Fusion 360 (consulte la tabla de materiales) y realice un diseño de cilindro hueco asistido por ordenador en 3D.
NOTA: En el Archivo Suplementario 1 se puede encontrar un archivo descargable que se puede utilizar para este paso e imita la geometría de los vasos sanguíneos. - Guarde el archivo y ábralo en el software Slic3r (consulte la tabla de materiales). Verifique que todos los parámetros sean los deseados y luego presione el botón de exportación del código G. Guarde el código G en la computadora.
- Abra el software Pronterface (consulte la Tabla de materiales) y cargue el archivo de código G.
NOTA: El software Pronterface interactúa con la bioimpresora y proporciona suficiente control de entrada de hardware. Se puede encontrar un archivo de código G utilizable en el Archivo Suplementario 2. - Transfiera la bioimpresora y todas las piezas asociadas a una cabina de bioseguridad (BSC) utilizando técnicas asépticas.
- Ensamble una punta de aguja roma de 30 G y 0,5" de largo (consulte la Tabla de materiales) en la jeringa de vidrio de impresión y déjela a un lado.
- Enchufe el cable de alimentación de la bioimpresora en una toma de corriente. Presione el botón rojo de encendido en la parte frontal de la bioimpresora para encenderla. Conecte el cable de bus serie universal (USB) entre la computadora y la bioimpresora y asegúrese de que todas las conexiones de cables estén establecidas y enchufadas.
3. Preparación del baño de apoyo y de los reactivos
NOTA: Realice todos los pasos en una cabina de bioseguridad utilizando técnicas asépticas.
- Prepare el medio de cultivo celular que consiste en medio basal SmBM (CC-3181) y suplementos SmGM-2 SingleQuots (CC-4149), excluyendo el suero fetal bovino (FBS), de acuerdo con las instrucciones del fabricante. Conservar a 4 °C hasta su uso.
- Alícuota 50 mL del medio de cultivo celular y añadir 1% v/v de FBS (CC-4149) (ver Tabla de Materiales) para hacer un medio con bajo contenido sérico. Conservar a 4 °C hasta su uso.
- Vuelva a suspender la suspensión de gelatina en polvo de acuerdo con las instrucciones del fabricante utilizando medios de cultivo celular estériles sin FBS como disolvente (consulte la Tabla de materiales). Inmediatamente antes de su uso, ajuste el pH final de la suspensión de gelatina a pH 9 utilizando hidróxido de potasio (KOH) 2 M y/o ácido clorhídrico 2 M (HCl) para ajustar el pH de la solución según sea necesario utilizando un medidor de pH.
- Llene el número deseado de pocillos de una placa de 24 pocillos, cada uno aproximadamente hasta la mitad, usando 1 ml de lechada de gelatina por pocillo, usando una jeringa sin la aguja.
NOTA: Llene uniformemente el centro de los pocillos y confirme que no existan bolsas de aire. Golpee la placa para ayudar a distribuir uniformemente la suspensión de micropartículas. Ajuste la altura y el volumen de la lechada por pocillo según sea necesario para adaptarse a cada tamaño y forma de bioimpresión. Los usuarios pueden crear una jeringa casera para transferir la mezcla de gelatina a cada pocillo. Esto se puede hacer agregando un émbolo de jeringa del tamaño correcto en un tubo de ensayo de 50 ml que ya contiene la suspensión de gelatina compactada en la parte inferior. Mientras inserta el émbolo, inserte un pequeño alambre guía a lo largo del tubo de ensayo para ayudar a que escape el aire y luego retírelo cuando el émbolo esté en contacto con la suspensión de gelatina. Inmediatamente antes de usar, corte la punta del tubo de ensayo con una cuchilla de afeitar para crear un orificio para que salga la suspensión de gelatina y presione el émbolo. - Coloque la placa llena de 24 pocillos en el centro de la platina de la bioimpresora y asegúrela a la platina.
NOTA: La Figura 2 muestra una configuración genérica de bioimpresora. Coloque una banda elástica alrededor de la platina de impresión para asegurar una placa de 24 pocillos a la plataforma y evitar el movimiento.

Figura 2: Configuración básica de la bioimpresión 3D. La bioimpresora se instaló en un entorno estéril, como un armario de bioseguridad, y el cabezal de impresión se montó de modo que la jeringa de vidrio y la aguja se bajaran verticalmente a la zona de impresión del baño de soporte que se encontraba debajo. Haga clic aquí para ver una versión más grande de esta figura.
4. Cultivo celular
NOTA: Realice todos los pasos en una cabina de bioseguridad utilizando técnicas asépticas.
- Descongele las células HPAAF (obtenidas comercialmente, consulte la Tabla de materiales) y amplíelas en matraces de plástico tratados con cultivo de tejidos T-75 que contengan medio basal SmBM (CC-3181) y todos los suplementos SmGM-2 SingleQuots (CC-4149) de acuerdo con las instrucciones del fabricante (consulte la Tabla de materiales).
NOTA: Se deben utilizar protocolos estándar de cultivo celular para células adherentes, manteniendo las células a 37 °C y 5% de CO2 y reponiendo el medio cada pocos días. - Una vez que los HPAAF hayan alcanzado ~80-90% de confluencia, aspire el medio y enjuague las células una vez con solución salina tamponada con fosfato (PBS).
- Agregue aproximadamente 4 ml de tripsina-EDTA precalentada al 0,05% a cada matraz T-75. Incline el matraz para asegurarse de que toda la superficie del cultivo celular esté cubierta con una solución de tripsina-EDTA al 0,05%. Incubar los matraces durante 3-5 minutos a 37 °C y comprobar si hay desprendimiento de células.
- Una vez que las células estén flotando, agregue al menos 6 ml de medio Eagle modificado (DMEM) de Dulbecco a cada matraz y transfiera las células a un tubo cónico de 50 ml.
- Centrifugar la suspensión celular a 300 x g durante 5 min a temperatura ambiente para granular las celdas. Aspire el sobrenadante del gránulo celular y vuelva a suspender las células en medios de 1-3 ml con FBS utilizando una pipeta de 1000 μl, asegurando una suspensión de una sola célula.
- Transfiera 10 μL de la suspensión celular a un tubo de microcentrífuga. Agregue 10 μL de solución de Azul de Tripano y mezcle bien. Use 10 μL de esta mezcla para contar células dentro de un hemocitómetro usando un microscopio óptico invertido.
NOTA: Para lograr una concentración final de biotinta de 4 x 106 células/mL, se reservaron 800.000 fibroblastos por cada 200 μL de biotinta.
5. Preparación de la biotinta de hidrogel
NOTA: La preparación de la biotinta fue adaptada de Davis-Hall et al.5. Los pasos 5.1-5.2 se pueden completar en paralelo con los pasos 4.1-4.3 para minimizar el tiempo entre la recolección de células y la resuspensión en la biotinta. Realizar los pasos en una cabina de bioseguridad utilizando una técnica aséptica.
- Prepare una solución de 20 mM de tris(2-carboxietil) fosfina (TCEP, ver Tabla de materiales) pH 7 y un filtro estéril utilizando un filtro de jeringa de 0,2 μm. Inmediatamente antes de usar, agregue 2 M KOH y/o 2 M HCl para ajustar el pH de la solución según sea necesario. Mida con un medidor de pH y ajuste en consecuencia.
NOTA: El TCEP reduce los enlaces disulfuro. - Preparar una solución madre de 0,25 mg/ml de PEGαMA resuspendida en medios de cultivo celular estériles sin FBS, soluciones madre de 250 mM de 1,4-ditiotreitol (DTT), reticulante degradable MMP2 y péptido CGRGDS (RGD) (consulte la Tabla de materiales), resuspendiendo todo en TCEP estéril de 20 mM y una solución madre de poli(óxido de etileno) (PEO) al 15% en peso en agua destilada (DI) utilizando pipetas según sea necesario.
- Siguiendo la Tabla 1 como guía, combine las cantidades respectivas necesarias de PEGαMA, DTT, reticulante degradable MMP2, PEO, CGRGDS y medios de cultivo celular de bajo contenido sérico junto con los fibroblastos en un tubo cónico de 50 mL.
NOTA: Se recomienda verificar el pH con tiras de pH después de agregar todos los medios de cultivo excepto el celular, ya que esta combinación debería dar como resultado que el pH esté muy cerca de 6.2. Si se requieren más ajustes de pH, lleve un registro de cuánto volumen adicional se necesita para ajustar el pH de la solución precursora. Aumente el volumen total a 200 μL añadiendo el volumen restante del medio de cultivo celular menos cualquier volumen añadido durante el ajuste final del pH. - Mezcle la biotinta con una pipeta de desplazamiento positivo para asegurarse de que las células son células individuales y confirme que la solución precursora final tiene un pH de 6,2 para evitar la polimerización catalizada por bases durante la bioimpresión 3D.
- Cargue la biotinta en la jeringa de vidrio quitando el émbolo y usando una jeringa separada con una punta de aguja roma de calibre 15 de 1.5" de largo (consulte la Tabla de materiales) adjunta para transferir la biotinta del tubo de centrífuga a la jeringa, teniendo cuidado de evitar la formación de burbujas de aire dentro de la solución.
- Coloque la jeringa de vidrio dentro del cabezal de impresión y coloque los componentes del cabezal de impresión para que todo esté firmemente ensamblado y listo para imprimir.
NOTA: En este punto, la jeringa de vidrio dentro del cabezal de impresión debe tener una punta de aguja roma de calibre 30 de 0.5" de largo unida a ella para imprimir.
| Componente | Concentración de la solución madre | Cantidad a añadir |
| PEGαMA | 0,25 mg/ml | 140 μL |
| TDT | 250 mM | 12,24 μL |
| Reticulante degradable MMP2 | 250 mM | 5,25 μL |
| RGD | 250 mM | 1,6 μL |
| PEO | 15 % en peso | 33,33 μL |
| Medios de activación y/o reactivos de ajuste de pH | - | 7,58 μL |
| Fibroblastos | - | 800000 celdas |
Tabla 1: Ejemplos de volúmenes necesarios para preparar 200 μL de biotinta (solución precursora de hidrogel y células de fibroblastos).
6. Bioimpresión .3D
NOTA: Realice todos los pasos en una cabina de bioseguridad utilizando técnicas asépticas.
- Usando las flechas direccionales dentro del software Pronterface, ajuste manualmente la posición de la aguja de extrusión en el centro de un pozo y dentro de la lechada del baño de soporte. Deje al menos 1 mm de lodo de baño de soporte debajo de la punta de la aguja.
NOTA: El software no tiene la capacidad de saber dónde está la aguja dentro del espacio. Depende completamente del usuario mover la aguja haciendo clic manualmente en las flechas dentro del software (por ejemplo, al hacer clic en la flecha hacia arriba se moverá la aguja hacia arriba o lejos de la plataforma de impresión, etc.). Maniobre la aguja con cuidado para asegurarse de que no golpee ningún límite del pozo. - Una vez que la punta de la aguja esté situada en el centro de la lechada dentro del pozo, presione el botón de inicio dentro de la superficie y espere a que se complete la impresión para lograr construcciones, como se muestra en la Figura 3A.
NOTA: Para bioimprimir una construcción utilizando el archivo provisto (Archivo Suplementario 1), tomará aproximadamente 3 min. Se tarda aproximadamente 5 minutos en orientar y mover la aguja y luego imprimir una construcción por completo de principio a fin. - Repita los pasos 6.1-6.2 hasta que se alcance el número deseado de construcciones bioimpresas.
NOTA: Se recomienda hacer más construcciones de las necesarias para tener en cuenta cualquier impresión fallida. Si se produce un error, pase al siguiente pozo, reinicie todo y repita los pasos 6.1 y 6.2 nuevamente. - Deje la placa de pocillos a temperatura ambiente y cúbrala en el BSC durante 1 h después de que haya finalizado la impresión para permitir la polimerización catalizada por bases del hidrogel fotosintonizable.
- Coloque la placa de pocillos que contiene las construcciones bioimpresas en 3D en una incubadora estéril a 37 °C y déjelas durante 12-18 h para que derritan la lechada del baño de soporte.
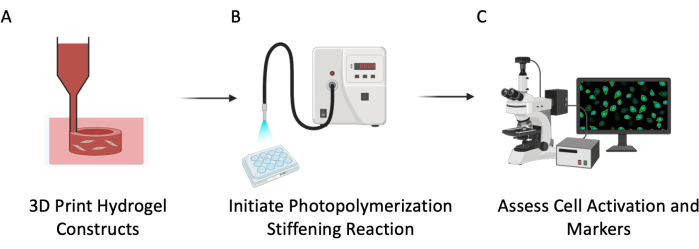
Figura 3: Esquema experimental. Este protocolo se describió en tres pasos principales: (A) Bioimpresión 3D de tubos huecos PEGαMA con células incrustadas para imitar la vasculatura pulmonar. (B) Fotoiniciación de la reacción de homopolimerización para endurecer el microambiente celular. (C) Evaluación de marcadores celulares para la proliferación y activación. Haga clic aquí para ver una versión más grande de esta figura.
7. Cultivo de construcción bioimpresa .3D y fotorigidez
NOTA: Todos los pasos deben realizarse en una cabina de bioseguridad utilizando técnicas asépticas.
- Preparar 2,2 mM de fenil-2,4,6-trimetilbenzoilfosfinato (LAP) de litio (ver Tabla de Materiales) solución madre en PBS y filtro estéril utilizando un filtro de jeringa de 0,2 μm. Mantenga la solución LAP protegida de la luz.
- Después de 12-18 h, cambie el soporte que rodea las construcciones bioimpresas. Retire manualmente el medio y el baño de soporte de gelatina derretida dentro de los pocillos y tenga cuidado de no alterar las construcciones bioimpresas.
NOTA: Es útil retirar lentamente el medio mientras sostiene la placa en un ángulo de 45° para que las construcciones emerjan dentro del pozo y se puedan ver. Un cilindro de hidrogel transparente debe ser identificable en cada pocillo con una impresión exitosa (Figura 4A). - Agregue un volumen apropiado de medios con bajo contenido de suero a cada pocillo.
NOTA: Para una placa de 24 pocillos, 700 μL de medio por pocillo deben cubrir completamente las construcciones bioimpresas. Ajústelo según sea necesario. - Regrese la placa a la incubadora y cambie el medio de las muestras cada 3 días o de acuerdo con el diseño experimental.
- Veinticuatro horas antes del punto de tiempo de endurecimiento deseado, retire los medios de las muestras y reemplácelos con medios con bajo contenido de suero suplementados con 2,2 mM de LAU estéril.
NOTA: Para etiquetar fluorescentemente la estructura, hinche las construcciones bioimpresas en 3D en PBS suplementadas con 10 μM de metacriloxiletiltiocarbamoil rodamina B (verT able de materiales) durante la noche, luego endurezca como se describe en el paso 7.6 para etiquetar fluorescentemente la estructura. Transfiera a PBS durante 2 días a 4 °C para eliminar el exceso de rodamina y obtenga imágenes con un filtro TRITC (Figura 4B, C). - En el punto de tiempo de endurecimiento deseado, retire la mitad del medio de los pocillos que se van a endurecer y coloque la placa sin la tapa bajo la luz ultravioleta. Encienda la luz UV y refuerce estas construcciones aplicando luz de 10 mW/cm2 365 nm durante 5 min usando Omnicure (ver Tabla de materiales) y un filtro de paso de banda de 365 nm (Figura 3B).
NOTA: Utilice el radiómetro/fotómetro para confirmar que la intensidad de la luz es correcta antes de exponer las células a la luz ultravioleta. - Retire el medio restante de estos pocillos y agregue medios nuevos con bajo contenido de suero a cada pocillo. Regrese la placa a la incubadora.
- Saque la placa de la incubadora y realice el estudio de activación de fibroblastos en el momento deseado siguiendo el paso 9.
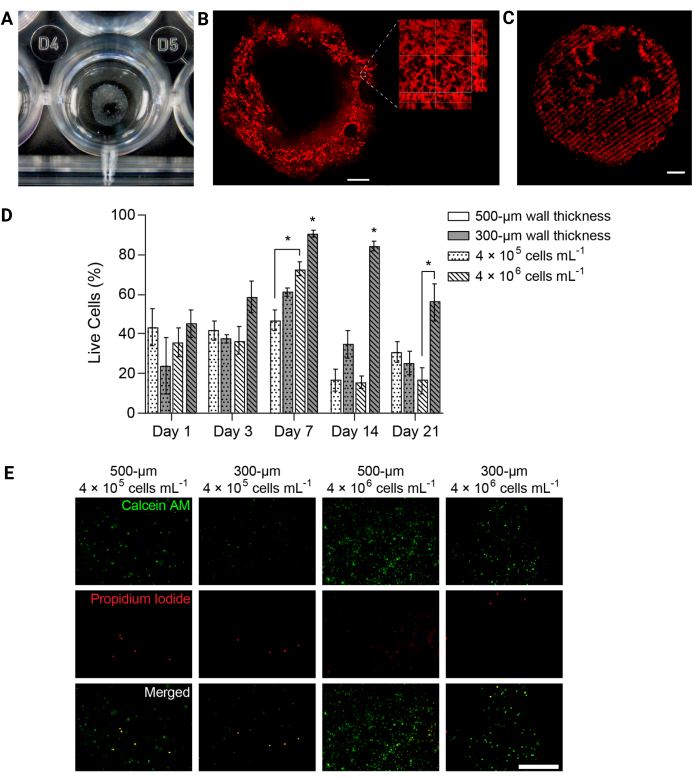
Figura 4: Las estructuras de hidrogel bioimpresas en 3D apoyaron la viabilidad celular a lo largo del tiempo. (A) Fotografía de la estructura de hidrogel impresa en 3D en una placa de 24 pocillos. (B) Proyección de intensidad máxima de hidrogel impreso en 3D PEGαMA marcado con fluorescencia. Barra de escala = 1 mm. La microscopía de mayor aumento mostró poros dentro de la estructura del hidrogel inducidos por micropartículas de gelatina en el baño de soporte de bioimpresión FRESH. (C) El tubo PEGαMA impreso en 3D con regiones rígidas marcadas con fluorescencia obrificadas en un microscopio confocal (pila z de 100 μm mostrada como una proyección de intensidad máxima) mostró control espacial sobre la rigidez en 3D. Barra de escala = 500 μm. (D) Viabilidad de HPAAF en construcciones bioimpresas en 3D medida mediante ensayos Live/Dead. Los constructos con un espesor de 300 μm y 4 × 106 células/ml superaron a todas las demás condiciones en todos los puntos de tiempo. La viabilidad alcanzó su punto máximo el día 7. Esta condición y punto de tiempo fueron seleccionados para futuros experimentos. Las columnas muestran la media ± SEM, n = 3. *, p < 0,05, ANOVA, Tukey HSD. (E) Imágenes confocales representativas de células en construcciones 3D teñidas con reactivo vivo/muerto en el día 7, el punto de tiempo con mayor viabilidad general. La calceína AM marcó las células vivas en verde y el yoduro de propidio marcó las células muertas en rojo. La columna de la derecha muestra que la condición de mejor rendimiento tenía una distribución celular uniforme y un alto porcentaje de células vivas. Barra de escala = 500 μm. Reproducido con permiso de Davis-Hall et al.5. Haga clic aquí para ver una versión más grande de esta figura.
8. La evaluación de la viabilidad de los fibroblastos
- En los puntos de tiempo de viabilidad deseados, teñir con calceína AM y yoduro de propidio (ver Tabla de Materiales).
NOTA: En resumen, se deben retirar los medios de cada pocillo y las construcciones deben enjuagarse con PBS estéril. Incubar las construcciones en una solución de tinción viva/muerta durante 40 min a 37 °C en un balancín. La solución de tinción debe contener calceína AM (dilución 1:1000) y yoduro de propidio (dilución 1:1000) para identificar células vivas o muertas en la toma de imágenes. - Transfiera las construcciones a PBS estéril e inmediatamente obtenga imágenes en un microscopio de fluorescencia confocal. Adquiera tres imágenes diferentes de pila z de 100 μm por muestra por punto de tiempo y exprese la viabilidad como el porcentaje promedio de células vivas (Figura 4D, E).
9. La evaluación de la activación de los fibroblastos
- Preparar 3% p/v albúmina sérica bovina (BSA) y 0,1% v/v Tween 20 en PBS. Esta solución se denominará solución de inmunofluorescencia (IF).
- En los puntos de tiempo deseados, retire los medios de los pocillos de muestra y enjuague las construcciones con PBS. Sustituya el PBS por paraformaldehído (PFA) al 4% y mantenga estas muestras a 37 °C durante 30 minutos en un balancín. Luego, reemplace el PFA al 4% con 100 mM de glicina en PBS y deje estas muestras en un balancín a temperatura ambiente (RT) durante otros 15 minutos.
- A continuación, transfiera estas muestras a los criomoldes Tissue-Tek, cubra la muestra completamente con una solución de temperatura óptima de corte (OCT) (consulte la Tabla de materiales) y deje que la OCT se difunda en las muestras durante 12-18 h a 4 °C.
- Congele rápidamente las muestras empapadas en OCT en 2-metilbutano utilizando nitrógeno líquido. Llene una caja de espuma de poliestireno u otro recipiente apropiado con nitrógeno líquido y luego coloque un segundo recipiente lleno de 2-metilbutano dentro del nitrógeno líquido para que quede al menos sumergido hasta la mitad. Use fórceps para sostener cada criomold que contenga una muestra cubierta con OCT en 2-metilbutano refrigerado por nitrógeno líquido hasta que se congele visiblemente. Estas muestras pueden almacenarse a -80 °C hasta que estén listas para la criosección.
PRECAUCIÓN: Se debe usar equipo de protección personal (EPP) como guantes protectores contra el frío, un delantal protector contra el frío y un protector facial provistos en el kit de seguridad criogénica (consulte la Tabla de materiales) mientras se manipula nitrógeno líquido. - Crioseccionar las muestras de OCT congeladas a -22 °C y fijar rodajas de 10 μm de grosor a portaobjetos de microscopio de vidrio cargados positivamente. Prepare tres portaobjetos de microscopio con al menos 3-5 criosecciones por portaobjetos para cada muestra de hidrogel 3D.
NOTA: Los portaobjetos del microscopio pueden almacenarse en este punto a -80 °C si es necesario como punto de parada. - Fije las criosecciones en acetona helada durante 15 minutos para ayudar a que las criosecciones se adhieran a los portaobjetos. Enjuague suavemente las criosecciones con agua RT para eliminar cualquier resto de OCT. Deje que estas muestras se sequen y delinee las criosecciones con un bolígrafo hidrofóbico (consulte la Tabla de materiales).
- Permeabilizar las muestras a temperatura ambiente con Triton X-100 al 0,2 % v/v en PBS durante 10 min y, a continuación, bloquear las secciones con BSA al 5 % p/v en PBS durante 1 h a RT.
- Añadir el anticuerpo primario de actina del músculo liso alfa humano (αSMA) de ratón (dilución 1:250) (ver Tabla de materiales) a la solución de FI. Almacene estas muestras seccionadas con el anticuerpo primario durante la noche a 4 °C. Enjuague las muestras 3 veces con solución de FI.
- Incubar las secciones en una solución de FI que contenga el anticuerpo secundario Alexa Fluor 555 anti-ratón de cabra (dilución 1:250) y dos gotas de ActinGreen 488 ReadyProbe (ver Tabla de Materiales) por mililitro de solución de FI. Cubra las muestras para todos los pasos posteriores con papel de aluminio para protegerlas de la luz y deje que la solución de anticuerpos secundarios permanezca en las muestras durante 1 h en RT.
- Enjuague las secciones 3 veces con solución de FI. Incubarlas en 300 nM 4',6-diamidino-2-filindol (DAPI) en agua desionizada durante 15 min a RT. Realizar un enjuague final de las secciones 3 veces con agua desionizada.
- Utilizando 10 μL de un reactivo antidecoloración disponible en el mercado (véase la Tabla de materiales), cubra las secciones utilizando métodos estándar.
NOTA: Los portaobjetos montados se pueden almacenar protegidos de la luz en un congelador a -80 °C hasta que se necesiten para la obtención de imágenes. - Tome imágenes de las criosecciones con un microscopio de fluorescencia (Figura 3C y Figura 5B). Imagina tres secciones aleatorias por diapositiva usando un objetivo 10x.
NOTA: Las imágenes deben tomarse en los canales DAPI, FITC y TRITC. - Cargue las imágenes en ImageJ (NIH). Cuantifique el porcentaje de células αSMA positivas como medida de la activación de fibroblastos (Figura 5A) dividiendo el número total de células αSMA positivas por el número total de núcleos celulares para cada campo de visión.
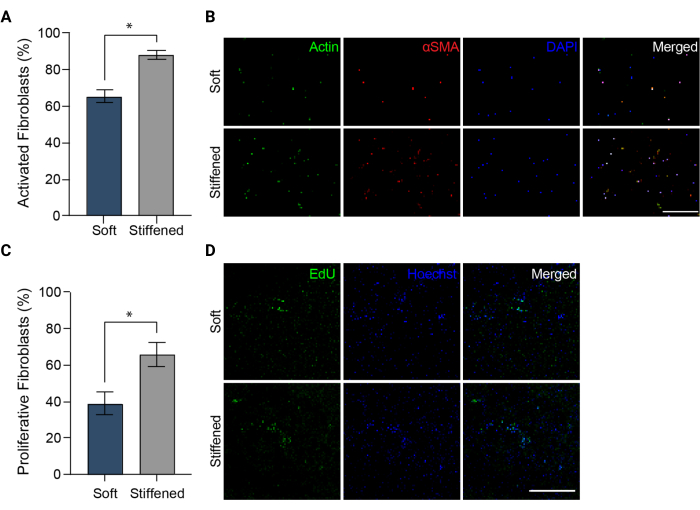
Figura 5: Activación de fibroblastos en modelos bioimpresos en 3D de adventicia arterial pulmonar. (A) Activación fibrótica en hidrogeles 3D blandos y endurecidos medida por la expresión de αSMA. Los HPAAF en las construcciones rígidas fueron significativamente más positivos para la αSMA que las células en las construcciones blandas. Las columnas representan la media ± SEM, n = 3. *, p < 0,05, prueba U de Mann-Whitney. (B) Imágenes confocales representativas de inmunotinción para αSMA, actina y DAPI en hidrogeles 3D blandos y rígidos. Los HPAAF en construcciones rígidas mostraron una inmunofluorescencia αSMA más prevalente que las células en construcciones blandas. Barra de escala = 250 μm. (C) Proliferación de fibroblastos en construcciones bioimpresas 3D blandas y rígidas medida por positividad de EdU. Los HPAAF en las construcciones rígidas fueron significativamente más positivos para la EdU que las células en las construcciones blandas. Las columnas representan la media ± SEM, n = 3. *, p < 0,05, prueba U de Mann-Whitney. (D) Imágenes confocales representativas de inmunotinción para colorantes EdU y Hoechst en hidrogeles 3D blandos y endurecidos. Las HPAAF en las construcciones rígidas mostraron una inmunofluorescencia de EdU más prevalente que las células en las construcciones blandas. Barra de escala = 300 μm. Reproducido con permiso de Davis-Hall et al.5. Haga clic aquí para ver una versión más grande de esta figura.
10. La evaluación de la proliferación de fibroblastos
- Veinticuatro horas antes del momento de proliferación deseado, retire los medios de cultivo celular de cada pocillo y reemplácelos con medios con bajo contenido de suero suplementados con una solución de 10 μM de EdU del kit de proliferación celular disponible comercialmente (consulte la Tabla de materiales). Regrese las muestras a la incubadora para que se incuben durante la noche.
- En el momento de proliferación deseado, fijar las muestras incubadas con EdU utilizando PFA al 4% a 37 °C durante 30 min en un balancín. Sustituir la solución de PFA al 4% por 100 mM de glicina en PBS e incubar las muestras a 37 °C durante al menos 15 minutos. Agregue el Hoechst a una concentración adecuada durante 30 minutos y luego enjuague las construcciones 2 veces con PBS.
NOTA: Las muestras pueden almacenarse protegidas de la luz a 4 °C hasta la obtención de imágenes. - Tome imágenes de todas las muestras de EdU fijadas y almacenadas utilizando un microscopio de fluorescencia y los ajustes y filtros sugeridos por el fabricante del kit de proliferación celular (Figura 3C y Figura 5D). Adquiera tres imágenes diferentes de pila z de 100 μm por muestra y cree proyecciones máximas a partir de cada una de estas pilas z. Mida la proliferación de HPAAF contando el número de células positivas para EdU y dividiéndolas por el número total de células identificadas por la contratinción de Hoechst dentro de las imágenes de proyección máxima (Figura 5C).
Resultados
Este protocolo describe cómo bioimprimir en 3D hidrogeles fotosintonizables dentro de un baño de soporte para crear construcciones capaces de endurecerse dinámica y temporalmente para estudiar la activación de fibroblastos en geometrías que imitan tejidos humanos. En primer lugar, el protocolo explicaba cómo sintetizar PEGαMA, la columna vertebral de este sistema de polímeros fotosintonizables. Las mediciones de espectroscopia de resonancia magnética nuclear (RMN) mostraron una funcionalización exitosa de PEGα...
Discusión
Las reacciones de polimerización de doble etapa en respuesta a la exposición controlada a la luz pueden endurecer los biomateriales con control espacial y temporal. Varios estudios han aprovechado esta técnica para evaluar las interacciones célula-matriz en diversas plataformas 5,8,9,10,11,21,22,23.
Divulgaciones
Los autores no tienen ningún conflicto de intereses que revelar. Partes de este manuscrito se reproducen con permiso de © IOP Publishing https://doi.org/10.1088/1758-5090/aca8cf. 5 Todos los derechos reservados.
Agradecimientos
Los autores desean agradecer al Dr. Adam Feinberg (Universidad Carnegie Mellon) y a quienes organizaron el Taller de código abierto de bioimpresión 3D. Estas personas permitieron aprender las técnicas de bioimpresión FRESH y construir la bioimpresora 3D utilizada para estos estudios. Además, los autores desean agradecer Biorender.com, que se utilizó para producir las figuras de este manuscrito. Este trabajo fue apoyado por múltiples grupos o fuentes de financiamiento, incluida la Fundación Comunitaria Rose (DDH y CMM), un Premio de Investigación de Enfermedades Vasculares Pulmonares de Colorado (DDH y CMM), la Fundación Nacional de Ciencias bajo el Premio 1941401 (CMM), el Departamento del Ejército bajo el Premio W81XWH-20-1-0037 (CMM), el Instituto Nacional del Cáncer de los NIH bajo el Premio R21 CA252172 (CMM), el Centro de la Familia Ludeman para la Investigación de la Salud de la Mujer en el Campus Médico Anschutz de la Universidad de Colorado (DDH y CMM), el Instituto Nacional del Corazón, los Pulmones y la Sangre de los Institutos Nacionales de Salud bajo los premios R01 HL080396 (CMM), R01 HL153096 (CMM), F31 HL151122 (DDH) y T32 HL072738 (DDH y AT).
Materiales
| Name | Company | Catalog Number | Comments |
| AccuMax Radiometer/Photometer Kit | Spectronics Corporation | XPR-3000 | To measure light intensity, used for photostiffening |
| Acetic Acid | Fisher Scientific | BP2401-500 | Used during PEGaMA synthesis |
| Acetone | Fisher Scientific | A184 | Used with the cryosections |
| ActinGreen 488 ReadyProbes | Fisher Scientific | R37110 | Used for staining |
| Aluminum Foil | Reynolds | F28028 | |
| Anhydrous Tetrahydrofuran (THF) | Sigma-Aldrich | 401757-1L | Used during PEGaMA synthesis |
| Argon Compressed Gas | Airgas | AR R300 | Used during PEGaMA synthesis |
| 8 Arm Poly(ethylene glycol)-hydroxyl (PEG-OH) | JenKem Technology | 8ARM-PEG-10K | Used during PEGaMA synthesis |
| 365 nm Bandpass Filter | Edmund Optics | 65-191 | Used for photostiffening |
| Bovine Serum Albumin (BSA) | Fisher Scientific | BP9700-100 | Used during staining process |
| Buchner Funnel | Quark Glass | QFN-8-14 | Used during PEGaMA synthesis |
| Calcein AM | Invitrogen | 65-0853-39 | Used during staining process |
| Celite 545 (Filtration Aid) | EMD Millipore | CX0574-1 | Used during PEGaMA synthesis |
| Charged Microscope Slides | Globe Scientific | 1358W | |
| Chloroform-d | Sigma-Aldrich | 151823-10X0.75ML | Used to characterize PEGaMA |
| Click-iT Plus EdU Cell Proliferation Kit | Invitrogen | C10637 | Used for staining |
| 50 mL Conical Tubes | CELLTREAT | 667050B | |
| Cryogenic Safety Kit | Cole-Parmer | EW-25000-85 | |
| Cryostat | Leica | CM 1850-3-1 | |
| Dialysis Tubing | Repligen | 132105 | |
| 4’,6-Diamidino-2-Phylindole (DAPI) | Sigma-Aldrich | D9542-1MG | Used for staining |
| Diethyl Ether | Fisher Scientific | E1384 | Used during PEGaMA synthesis |
| 1,4-Dithiothreitol (DTT) | Sigma-Aldrich | 10197777001 | Bioink component |
| Dulbecco's Modified Eagle's Medium (DMEM) | Cytiva | SH30271.FS | |
| Ethyl 2-(Bromomethyl)Acrylate (EBrMA) | Ambeed Inc. | A918087-25g | Used during PEGaMA synthesis |
| Filter Paper | Whatman | 1001-090 | Used during PEGaMA synthesis |
| Freezone 2.5L Freeze Dry System | Labconco | LA-2.5LR | Lyophilizer |
| Fusion 360 | Autodesk | N/A | Software download |
| 2.5 mL Gastight Syringe | Hamilton | 81420 | Used for bioprinting |
| 15 Gauge 1.5" IT Series Tip | Jensen Global | JG15-1.5X | Used for bioprinting |
| 30 Gauge 0.5" HP Series Tip | Jensen Global | JG30-0.5HPX | Used for bioprinting |
| Goat Anti-Mouse Alexa Fluor 555 Antibody | Fisher Scientific | A21422 | Used for staining |
| Glycine | Fisher Scientific | C2H5NO2 | Used during staining process |
| Hemocytometer | Fisher Scientific | 1461 | |
| Hoechst | Thermo Scientific | 62249 | Used during staining process |
| Human Pulmonary Artery Adventitial Fibroblasts (HPAAFs) | AcceGen | ABC-TC3773 | From a 2-year-old male patient |
| Hydrochloric Acid (HCl) | Fisher Scientific | A144-500 | Used to pH adjust solutions |
| ImageJ | National Institutes of Health (NIH) | N/A | Free software download |
| ImmEdge® Pen | Vector Laboratories | H-4000 | Used during staining process |
| Incubator | VWR | VWR51014991 | |
| LifeSupport Gelatin Microparticle Slurry (Gelatin Slurry) | Advanced Biomatrix | 5244-10GM | Used for bioprinting |
| Light Microscope | Olympus | CKX53 | Inverted light microscope |
| Lithium Phenyl-2,4,6-Trimethylbenzoylphosphinate (LAP) | Sigma-Aldrich | 900889-5G | Photoinitiator used for photostiffening |
| Liquid Nitrogen | N/A | N/A | |
| LulzBot Mini 2 | LulzBot | N/A | Bioprinter adapted |
| Methacryloxyethyl Thiocarbamoyl Rhodamine B | Polysciences Inc. | 669775-30-8 | |
| 2-Methylbutane | Sigma-Aldrich | M32631-4L | |
| Microman Capillary Pistons CP1000 | VWR | 76178-166 | Positive displacement pipette tips |
| MMP2 Degradable Crosslinker (KCGGPQGIWGQGCK) | GL Biochem | N/A | Bioink component |
| Mouse Anti-Human αSMA Monoclonal Antibody | Fisher Scientific | MA5-11547 | Used for staining |
| OmniCure Series 2000 | Lumen Dynamics | S2000-XLA | UV light source used for photostiffening |
| Paraformaldehyde (PFA) | Electron Microscopy Sciences | 15710 | Used to fix samples |
| pH Meter | Mettler Toledo | FP20 | |
| pH Strips | Cytiva | 10362010 | |
| Phosphate Buffered Saline (PBS) | Hyclone Laboratories, Inc. | Cytiva SH30256.FS | |
| Pipette Set | Fisher Scientific | 14-388-100 | |
| 10 µL Pipette Tips | USA Scientific | 1120-3710 | |
| 20 µL Pipette Tips | USA Scientific | 1183-1510 | |
| 200 µL Pipette Tips | USA Scientific | 1111-0700 | |
| 1000 µL Pipette Tips | USA Scientific | 1111-2721 | |
| Poly(Ethylene Glycol)-Alpha Methacrylate (PEGαMA) | N/A | N/A | Refer to manuscript for synthesis steps |
| Poly(Ethylene Oxide) (PEO) | Sigma-Aldrich | 372773-250G | Bioink component |
| Positive Displacement Pipette | Fisher Scientific | FD10004G | 100-1000 µL |
| Potassium Hydroxide (KOH) | Sigma-Aldrich | 221473-500G | Used to pH adjust solutions |
| ProLong Gold Antifade Reagent | Invitrogen | P36930 | Used during staining process |
| Pronterface | All3DP | N/A | Software download |
| Propidium Iodide | Sigma-Aldrich | P4864-10ML | Used for staining |
| RGD Peptide (CGRGDS) | GL Biochem | N/A | Bioink component |
| Rocker | VWR | 10127-876 | |
| Rotary Evaporator | Thomas Scientific | 11100V2022 | Used during PEGaMA synthesis |
| Rubber Band | Staples | 808659 | |
| Schlenk Flask | Kemtech America | F902450 | Used during PEGaMA synthesis |
| Slic3r | Slic3r | N/A | Software download |
| Smooth Muscle Cell Growth Medium-2 (SmGM-2) BulletKit | Lonza | CC-3182 | Kit contains CC-3181 and CC-4149 components |
| Sodium Hydride | Sigma-Aldrich | 223441-50G | Used during PEGaMA synthesis |
| Sorvall ST 40R Centrifuge | Fisher Scientific | 75-004-525 | |
| Stir Bar | VWR | 58948-091 | |
| Syringe Filter | VWR | 28145-483 | Used to sterile filter solutions |
| T-75 Tissue-Cultured Treated Flask | VWR | 82050-856 | Used for cell culture work |
| Tissue-Tek Cyromold | Sakura | 4557 | |
| Tissue-Tek O.C.T Compound (OCT) | Sakura | 4583 | |
| Tris(2-Carboxyethyl) Phosphine (TCEP) | Sigma-Aldrich | C4706-2G | |
| Triton X-100 | Fisher Bioreagents | C34H622O11 | Used during staining process |
| Trypan Blue | Sigma-Aldrich | T8154-20ML | Used for cell culture work |
| 0.05% Trypsin-EDTA | Gibco | 25-300-062 | Used for cell culture work |
| Tween 20 | Fisher Bioreagents | C58H114O26 | Used during staining process |
| Upright Microscope | Olympus | BX63F | Fluorescent microscope capabilities |
| Water Bath | PolyScience | WBE20A11B | |
| 24-Well Tissue Culture Plates | Corning | 3527 |
Referencias
- Ahrens, J. H., et al. Programming cellular alignment in engineered cardiac tissue via bioprinting anisotropic organ building blocks. Advanced Materials. 34 (26), e2200217 (2022).
- Lin, N. Y. C., et al. Renal reabsorption in 3D vascularized proximal tubule models. Proceedings of the National Academy of Sciences of the United States of America. 116 (12), 5399-5404 (2019).
- Grigoryan, B., et al. Multivascular networks and functional intravascular topologies within biocompatible hydrogels. Science. 364 (6439), 458-464 (2019).
- Kang, Y., Datta, P., Shanmughapriya, S., Ozbolat, I. T. 3D bioprinting of tumor models for cancer research. ACS Applied Biomaterials. 3 (9), 5552-5573 (2020).
- Davis-Hall, D., Thomas, E., Pena, B., Magin, C. M. 3D-bioprinted, phototunable hydrogel models for studying adventitial fibroblast activation in pulmonary arterial hypertension. Biofabrication. 15 (1), (2022).
- Mirdamadi, E., Tashman, J. W., Shiwarski, D. J., Palchesko, R. N., Feinberg, A. W. FRESH 3D bioprinting of a full-size model of the human heart. ACS Biomaterials Science & Engineering. 6 (11), 6453-6459 (2020).
- Shiwarski, D. J., Hudson, A. R., Tashman, J. W., Feinberg, A. W. Emergence of FRESH 3D printing as a platform for advanced tissue biofabrication. APL Bioengineering. 5 (1), 010904 (2021).
- Petrou, C. L., et al. Clickable decellularized extracellular matrix as a new tool for building hybrid hydrogels to model chronic fibrotic diseases in vitro. Journal of Materials Chemistry B. 8 (31), 6814-6826 (2020).
- Hewawasam, R. S., Blomberg, R., Serbedzija, P., Magin, C. M. Chemical modification of human decellularized extracellular matrix for incorporation into phototunable hybrid hydrogel models of tissue fibrosis. ACS Applied Materials & Interfaces. 15 (12), 15071-15083 (2023).
- Saleh, K. S., et al. Engineering hybrid hydrogels comprised healthy or diseased decellularized extracellular matrix to study pulmonary fibrosis. Cellular and Molecular Bioengineering. 15 (5), 505-519 (2022).
- Guvendiren, M., Burdick, J. A. Stiffening hydrogels to probe short- and long-term cellular responses to dynamic mechanics. Nature Communications. 3, 792 (2012).
- Rosales, A. M., Vega, S. L., DelRio, F. W., Burdick, J. A., Anseth, K. S. Hydrogels with reversible mechanics to probe dynamic cell microenvironments. Angewandte Chemie International Edition English. 56 (40), 12132-12136 (2017).
- Wynn, T. A., Ramalingam, T. R. Mechanisms of fibrosis: therapeutic translation for fibrotic disease. Nature Medicine. 18 (7), 1028-1040 (2012).
- Huertas, A., Tu, L., Humbert, M., Guignabert, C. Chronic inflammation within the vascular wall in pulmonary arterial hypertension: more than a spectator. Cardiovascular Research. 116 (5), 885-893 (2020).
- Kendall, R. T., Feghali-Bostwick, C. A. Fibroblasts in fibrosis: novel roles and mediators. Frontiers in Pharmacology. 5, 123 (2014).
- Parker, M. W., et al. Fibrotic extracellular matrix activates a profibrotic positive feedback loop. The Journal of Clinical Investigation. 124 (4), 1622-1635 (2014).
- Habiel, D. M., Hogaboam, C. Heterogeneity in fibroblast proliferation and survival in idiopathic pulmonary fibrosis. Frontiers in Pharmacology. 5, 2 (2014).
- Hu, C. J., Zhang, H., Laux, A., Pullamsetti, S. S., Stenmark, K. R. Mechanisms contributing to persistently activated cell phenotypes in pulmonary hypertension. The Journal of Physiology. 597 (4), 1103-1119 (2019).
- Li, M., et al. Emergence of fibroblasts with a proinflammatory epigenetically altered phenotype in severe hypoxic pulmonary hypertension. The Journal of Immunology. 187 (5), 2711-2722 (2011).
- Hinton, T. J., et al. Three-dimensional printing of complex biological structures by freeform-reversible embedding of suspended hydrogels. Science Advances. 1 (9), e1500758 (2015).
- Brown, T. E., et al. Secondary photocrosslinking of click hydrogels to probe myoblast mechanotransduction in three dimensions. Journal of the American Chemical Society. 140 (37), 11585-11588 (2018).
- Ondeck, M. G., et al. Dynamically stiffened matrix promotes malignant transformation of mammary epithelial cells via collective mechanical signaling. Proceedings of the National Academy of Sciences of the United States of America. 116 (9), 3502-3507 (2019).
- Caliari, S. R., et al. Stiffening hydrogels for investigating the dynamics of hepatic stellate cell mechanotransduction during myofibroblast activation. Scientific Reports. 6, 21387 (2016).
- Liu, F., et al. Feedback amplification of fibrosis through matrix stiffening and COX-2 suppression. Journal of Cell Biology. 190 (4), 693-706 (2010).
- Tschumperlin, D. J., Ligresti, G., Hilscher, M. B., Shah, V. H. Mechanosensing and fibrosis. The Journal of Clinical Investigation. 128 (1), 74-84 (2018).
- Chelladurai, P., Seeger, W., Pullamsetti, S. S. Matrix metalloproteinases and their inhibitors in pulmonary hypertension. European Respiratory Journal. 40 (3), 766-782 (2012).
- Caracena, T., et al. Alveolar epithelial cells and microenvironmental stiffness synergistically drive fibroblast activation in three-dimensional hydrogel lung models. Biomaterials Science. 10 (24), 7133-7148 (2022).
- Ruskowitz, E. R., DeForest, C. A. Proteome-wide analysis of cellular response to ultraviolet light for biomaterial synthesis and modification. ACS Biomaterials Science & Engineering. 5 (5), 2111-2116 (2019).
- Kruse, C. R., et al. The effect of pH on cell viability, cell migration, cell proliferation, wound closure, and wound reepithelialization: In vitro and in vivo study. Wound Repair and Regeneration. 25 (2), 260-269 (2017).
- Filippi, M., et al. Perfusable biohybrid designs for bioprinted skeletal muscle tissue. Advanced Healthcare Materials. , e1500758 (2023).
- Matthiesen, I., et al. Astrocyte 3D culture and bioprinting using peptide-functionalized hyaluronan hydrogels. Science and Technology of Advanced Materials. 24 (1), 2165871 (2023).
- Xu, L., et al. Bioprinting a skin patch with dual-crosslinked gelatin (GelMA) and silk fibroin (SilMA): An approach to accelerating cutaneous wound healing. Materials Today Bio. 18, 100550 (2023).
- Bliley, J. M., Shiwarski, D. J., Feinberg, A. W. 3D-bioprinted human tissue and the path toward clinical translation. Science Translational Medicine. 14 (666), eabo7047 (2022).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados