このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
ヒト幹細胞維持と腸管オルガノイド生成のための基底膜マトリックスの比較研究
要約
オルガノイドは、疾患モデリングのための貴重なツールとなっています。細胞外マトリックス(ECM)は、オルガノイド生成中の細胞運命を導き、天然組織に似たシステムを使用することで、モデルの精度を向上させることができます。この研究では、動物由来のECMとゼノフリーのハイドロゲルにおける人工多能性幹細胞由来ヒト腸オルガノイドの生成を比較しています。
要約
細胞外マトリックス(ECM)は、細胞の挙動と発生において重要な役割を果たします。ヒト人工多能性幹細胞(hiPSC)から作製したオルガノイドは、多くの研究分野で注目されています。しかし、従来の細胞培養材料には生理的な手がかりがないため、効率的なiPS細胞の分化が妨げられています。市販のECMを幹細胞培養に組み込むと、細胞の維持に有益な物理的および化学的手がかりが得られます。動物由来の市販基底膜製品は、ECMタンパク質と細胞の維持をサポートする成長因子で構成されています。ECMは細胞の運命を調節できる組織特異的な特性を保持しているため、ゼノフリーマトリックスを使用して翻訳を臨床研究に流します。市販のマトリックスは、hiPSCやオルガノイドの研究に広く使用されていますが、これらのマトリックスの同等性はまだ評価されていません。本研究では、マトリゲル(Matrix 1-AB)、Geltrex(マトリックス2-AB)、Cultrex(マトリックス3-AB)、VitroGel(マトリックス4-XF)の4つの異なるマトリックスにおけるヒトヒト腸管オルガノイド(hIO)の産生について比較研究を行いました。コロニーは完全な円形を欠いていましたが、自発的な分化は最小限であり、細胞の85%以上が幹細胞マーカーSSEA-4を発現していました。マトリックス4-XFは、3Dの丸い塊の形成につながりました。また、Matrix 4-XFハイドロゲル溶液の調製に用いる培地中のサプリメントおよび成長因子の濃度を上げると、SSEA-4のhiPSC発現が1.3倍改善しました。マトリックス2-AB維持型ヒトPSCの分化により、他の動物由来の基底膜と比較して、中腸/後腸期のスフェロイド放出が少なくなりました。他のものと比較して、ゼノフリーオルガノイドマトリックス(Matrix 4-O3)は、より大きく、より成熟したhIOをもたらし、ゼノフリーハイドロゲルの物理的特性を利用してオルガノイド生成を最適化できることを示唆しています。全体として、この結果は、異なるマトリックスの組成の変動がIO分化の段階に影響を与えることを示唆しています。この研究は、市販の行列の違いについての認識を高め、iPSCおよびIO作業中の行列最適化のガイドを提供します。
概要
細胞外マトリックス(ECM)は、細胞の挙動と発生の調節に中心的な役割を果たす組織の動的で多機能な構成要素です。複雑なネットワークとして、構造的な支持体、細胞接着性リガンド1、細胞シグナル伝達を調節する成長因子やサイトカインの貯蔵を提供します。例えば、創傷治癒中、ECMは移動する細胞の足場として、また組織修復に関与する成長因子の貯蔵庫として機能します2。同様に、ECMの調節不全は、線維症や癌などのさまざまな疾患の重症度の増加につながる可能性があります3,4。胚発生中、ECMは組織の形態形成を導きます。例えば、心臓の発達において、ECMコンポーネントは、心臓組織の正しい構造および機能を作り出す役割を果たす5。10年以上にわたる研究により、微小環境の硬さだけでも6,7が幹細胞の系統の仕様を制御できることが示されています。したがって、in vitroでの細胞分化中に、ECMが分化のシグナルを提供することで幹細胞の運命に影響を与えることは驚くべきことではありません。
オルガノイドは、人工多能性幹細胞(iPSC)から作製できます。オルガノイドを成功裏に作製するためには、適切に特性評価されたiPS細胞株から始める必要があります。しかし、従来の細胞培養材料には生理学的な手がかりがないため、効率的なiPS細胞の分化やオルガノイドの生成が妨げられています。さらに、最近の研究では、細胞外マトリックス(ECM)の組成、細胞とECMとの間の相互作用8、オルガノイドの拡大と分化12の文脈における機械的および幾何学的な手がかり9,10,11の重要性が強調されている。再現性を向上させてオルガノイド技術を進歩させるには、組織特異的な物理的および化学的手がかりを組み込む必要があります。
オルガノイドは、生理学的に類似した微小環境内で天然組織を再現することを目的としています。天然組織ECMを厳密に模倣したECMシステムを選択することは、細胞の挙動、機能、および刺激に対する応答に関する生理学的関連性を達成するために重要である13。ECMコンポーネントの選択は、オルガノイド内の幹細胞の特定の細胞タイプへの分化に影響を与える可能性があります。さまざまなECMタンパク質とその組み合わせは、細胞の運命を導く手がかりを提供することができます14。例えば、特定のECM成分を使用すると、腸幹細胞の成熟した腸細胞型への分化が促進され、生理学的に関連性のある腸オルガノイドが得られることが研究で示されています15。オルガノイドは疾患モデリングや薬物試験において貴重なツールですが、適切なECMシステムを選択することは、このアプリケーションにとって極めて重要です。適切なECMシステムは、罹患組織16に似た微小環境を作り出すことにより、疾患モデリングの精度を向上させることができる。さらに、組織特異的ECMは、疾患に関連する表現型や薬物反応をよりよく再現するオルガノイドの生成に役立つ可能性があります17。オルガノイドの分化に使用されるECMシステムの最適化は、望ましい分化結果を達成するために重要です。
動物のECM源(Matrigel、Cultrexなど)および異種フリーのハイドロゲル(VitroGelなど)に由来する市販の基底膜システムは、iPS細胞およびオルガノイドの研究に広く使用されています。それらを商品化する企業とそれらを使用する研究者は、長年にわたって特定の製品とアプリケーションについて多くの指示を示してきました。これらの指示の多くは、このプロトコルを生成するためのガイドとして機能しました。さらに、それらの本質的な特性に関連する利点と挫折は、多くの18,19,20,21によって個別に注目されています。しかし、iPSCおよびオルガノイドの作業に最適なシステムを選択するための体系的なワークフローはありません。ここでは、iPSCおよびオルガノイド研究のために、さまざまなソースからのECMシステムの同等性を体系的に評価するワークフローを提供します。これは、マトリゲル(マトリックス1-AB)、ゲルトレックス(マトリックス2-AB)、カルトレックス(マトリックス3-AB)、およびVitroGel(マトリックス4-XF)の4つの異なるマトリックスにおける2つの異なるヒトiPS細胞株(hiPSC)とヒト腸オルガノイド(hIO)の生成の維持に関する比較研究です。オルガノイド培養には、オルガノイド1(マトリックス4-O1)、オルガノイド2(マトリックス4-O2)、オルガノイド3(マトリックス4-O3)、オルガノイド4(マトリックス4-O4)の4つのバージョンの異種フリーマトリックスVitroGelを使用しました。また、オルガノイドに最適化された動物由来のマトリックスであるMatrigel High Concentration(Matrix 1-ABO)とCultrex Type 2(Matrix 3-ABO)を使用しました。市販の幹細胞培養培地(mTeSR Plus)とオルガノイド分化キット(STEMdiff腸管オルガノイドキット)を使用しました。このプロトコルは、製品メーカーからの個々の指示とラボでの経験を組み合わせて、読者が特定のiPS細胞およびオルガノイド研究のためのECMの最適化を成功させるように導きます。全体として、このプロトコルと代表的な結果は、幹細胞の働きとオルガノイドの分化に最適な微小環境を選択することの重要性を強調しています。
プロトコル
1. hiPSCのメンテナンス
注意:すべての作業は、標準的な無菌技術に従ってバイオセーフティキャビネット(BSC)で行われます。白衣、手袋、ゴーグルなどの個人用保護具の適切な使用を含む、研究所のOSHA安全基準に従う必要があります。
- マトリックス、アリコート、細胞培養培地の調製
- 市販の動物由来基底膜(BM;Matrix 1-AB, Matrix 2-AB, Matrix 3-AB)は、 表1 に要約されたメーカーの推奨に従って作業量のアリコートを調製し、-20°Cまたは-80°Cで長期保存します。気泡の形成を避けてください。気泡が形成された場合は、保存する前に、サンプルを4°C、<200 x gで1~2分間遠心分離して 、 気泡を表面に浮かべます。
注:シングルユースアリコートを作成すると、ECMアーキテクチャを混乱させる凍結融解サイクルの繰り返しを回避できます。BM濃度はロット番号によって異なるため、メーカーの推奨に従ってシングルユースアリコートを準備し、コーティング溶液を調製してください。高濃度のBMは粘性があり、ピペッティングが困難です。以前に-20°Cで保存したコールドチップを使用してください。 - 幹細胞培養液は、メーカーの推奨に従って調製してください。このプロトコルで使用される特定の市販の完全培地を調製するには、100 mLの5倍サプリメントカクテルを400 mLの基礎培地に加えます。次に、この培地を完全に混合し、20°Cで保存する40 mLの容量に分注します。 使用するには、完全培地の各アリコートを解凍するか、分注した完全培地をすぐに使用するか、2〜8°Cで最大2週間保存してください。再凍結しないでください。
- サプリメントカクテルの3倍の濃度を含む幹細胞完全培地のアリコートを調製して、マトリックス4-XEハイドロゲルを調製します、すなわち、5倍サプリメントを3倍に希釈します。
- 市販の動物由来基底膜(BM;Matrix 1-AB, Matrix 2-AB, Matrix 3-AB)は、 表1 に要約されたメーカーの推奨に従って作業量のアリコートを調製し、-20°Cまたは-80°Cで長期保存します。気泡の形成を避けてください。気泡が形成された場合は、保存する前に、サンプルを4°C、<200 x gで1~2分間遠心分離して 、 気泡を表面に浮かべます。
- 組織培養プラスチックに動物由来のBMsをコーティング(Matrix 1-3AB)
- 始める前に、次のものを準備してください:解凍して取り扱うときは、マトリックスがゲル化するのを防ぐために、常にマトリックスを氷の中に置いてください。冷媒体を使用して、希釈したマトリックスを調製します。開始前およびhiPSC分化プロセスおよびhIOオルガノイド生成のすべての段階で細胞をアッセイするために、条件ごとに十分な複製ウェルを準備します。
注:ここでは、この研究に24ウェルプレートを使用しました。他のプレートサイズの推奨コーティング量については、 表2 を参照してください。 - マトリックスの種類ごとに、15 mM HEPES を含む 25 mL のコールドアドバンス DMEM/F-12 を 50 mL のコニカルチューブに調製します。これらを氷の上に置いてください。
- 解凍したマトリックスをそれぞれのコールドアドバンスDMEM/F-12に加え、よく混ぜます。混合プロセス中は、メディアを冷たく保ちます。塊がないことを確認することにより、均質な混合を視覚的に確認します。
- 希釈したマトリックス溶液を直ちに使用して、使用するために選択した各ウェルをコーティングします(24ウェルプレートを使用する場合は250 μL/ウェル)。
- 培養器をゆっくりと傾けて、コーティング溶液を表面全体に均一に広げます。使用前に室温(15〜25°C)で少なくとも1時間インキュベートしてください。
注:すぐに使用しない場合は、プレートをコーティング後最大1週間2〜8°Cで保存できますが、蒸発を防ぐために透明フィルムで密封する必要があります。保管されたプレートを使用する場合は、次のステップに進む前に、室温(15〜25°C)に30分間到達させてください。 - 血清学的ピペットまたは吸引により、余分な溶液を静かに除去します。コーティングされた表面に傷が付いていないことを確認してください。
- 温かい完全幹細胞培地をすぐに追加します(特定のウェルに必要な全容量の50%、たとえば、24ウェルプレートを使用する場合は250 μL/ウェル)。
- 始める前に、次のものを準備してください:解凍して取り扱うときは、マトリックスがゲル化するのを防ぐために、常にマトリックスを氷の中に置いてください。冷媒体を使用して、希釈したマトリックスを調製します。開始前およびhiPSC分化プロセスおよびhIOオルガノイド生成のすべての段階で細胞をアッセイするために、条件ごとに十分な複製ウェルを準備します。
- 組織培養プラスチックをMatrix 4-XEハイドロゲルでコーティング
- 開始する前に、次のものを準備します:Matrix 4-XEハイドロゲルを冷蔵庫から取り出し、室温(25°C)まで温めます。開始前およびhiPSC分化プロセスおよびhIOオルガノイド生成のすべての段階で細胞をアッセイするために、条件ごとに十分な複製ウェルを準備します。
注:ここでは、この研究に24ウェルプレートを使用しました。他のプレートサイズの推奨コーティング量については、 表3 を参照してください。 - 幹細胞培養用の標準製剤(3x Stem Cell Medium)と比較して、3倍の成長因子濃度を含む完全な幹細胞培養培地を調製します。
- マトリックス4-XEハイドロゲルと3倍幹細胞培地を2:1 v / vの混合比で混合し、5倍から10倍まで静かにピペットで上下させて完全に混合します。
- ヒドロゲル混合物をウェルプレートに移し、培養器を慎重に傾けて、混合物を表面全体に均一に広げます。24ウェルプレートを使用する場合は、250 μL/ウェルを使用してください。推奨されるボリュームについては、 表 3 を参照してください。
- 柔らかいゲルが形成されるまで室温で10〜15分待ちます。ハイドロゲル形成プロセス中は、プレートを傾けたり振ったりしてハイドロゲルを破壊しないでください。
- 開始する前に、次のものを準備します:Matrix 4-XEハイドロゲルを冷蔵庫から取り出し、室温(25°C)まで温めます。開始前およびhiPSC分化プロセスおよびhIOオルガノイド生成のすべての段階で細胞をアッセイするために、条件ごとに十分な複製ウェルを準備します。
- hiPSC酵素フリーの塊の継代と播種
- 始める前に、次のものを準備します:継代の少なくとも1時間前に、目的のプラスチック製品をマトリックスでコーティングします。十分な完全幹細胞培地を分量し、室温(15〜25°C)まで温めます。メディア全体に対して複数の加熱サイクルを避けることができます。
注:以下のステップでは、すでに確立されている>90%のコンフルエント培養物であるiPS細胞を6ウェルプレート上で通過させ、腸オルガノイドの分化のために24ウェルプレートに播種する手順を説明しています。 - 1mLのD-PBS(Ca++およびMg++を含まない)で細胞をすすぎ、吸引します。酵素を含まないヒト多能性幹細胞選択試薬1 mLを加え、均一に広がるように慎重に渦巻き、1分以内に吸引します。コロニーは、液体の薄い膜にさらすだけで済みます。
- コロニーが圧縮されなくなるまで37°Cでインキュベートします(これには3~8分かかります)。
注:最適なインキュベーション時間は、使用する細胞株によって異なる場合があります。最適なインキュベーション時間は、酵素を含まないヒト多能性幹細胞選択試薬で各細胞株を初めて継代する際に決定する必要があります。 - 1 mLの完全幹細胞培地を添加します。プレートの側面を慎重に軽くたたいて、コロニーを取り外してください。プレートは必ずもう一方の手で持ってください。
- 1 mL以上のピペットを使用して、細胞凝集懸濁液を15 mLコニカルチューブに移します。明視野顕微鏡を使用して凝集体のサイズを評価し、細胞凝集体のサイズが50〜200μmであることを確認します。大きい場合は、円錐形のチューブをそっと振って分解します。
- 塊のカウントに使用する平底96ウェルプレートの各ウェルの底にx-yグリッドを描き、各ウェルに50μLのD-PBSを追加します。3つのウェルからカウントされた塊を平均化することをお勧めします。
- チューブを静かに振って細胞の凝集液が均一に分布していることを確認してから、5 μLの凝集懸濁液を平底96ウェルプレートの各ウェルに移します。
注:自動セルカウンターを使用して凝集をカウントすることはお勧めしません。手動カウントをお勧めします。 - 各ウェル内の直径50〜200μmの塊の総数を数えます。ほとんどの細胞塊の直径が200μm>場合( 図1を参照)、手順1.4.5〜1.4.7を繰り返します。
- 6,000個の凝集液を播種するために必要な凝集懸濁液の量(μL)を次のように計算します。
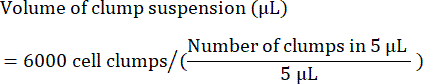
注:最適な播種密度は、すべての細胞株で最適化する必要があります。最適な播種密度を決定するには、さまざまな凝集密度(たとえば、ウェルあたり4,000、5,000、および6,000凝集)で初期播種を行い、播種後24〜48時間で85%〜90%のコンフルエントに達したかどうかを確認することをお勧めします。 - 品質管理として、幹細胞マーカーのフローサイトメトリー検査のために細胞のサンプルを分離します。一般的なマーカーのリストについては、 表4 を参照してください。
- 異なるECMでコーティングしたウェル上のシードに必要な量のiPSC凝集懸濁液を別々の15 mLチューブに分離します。
- iPSC塊溶液の入ったチューブを200 x g で5分間遠心分離し、酵素フリーのヒト多能性幹細胞選択試薬を含む培地を除去します。遠心分離を待っている間に、まだ行われていない場合は、各ウェルあたり必要な容量の50%を各ウェルに加えます。
- 始める前に、次のものを準備します:継代の少なくとも1時間前に、目的のプラスチック製品をマトリックスでコーティングします。十分な完全幹細胞培地を分量し、室温(15〜25°C)まで温めます。メディア全体に対して複数の加熱サイクルを避けることができます。
- 動物由来マトリックスを含むプレートでのiPS細胞培養
- 計算容量の50%の完全幹細胞培地にiPS細胞の凝集体を穏やかに再懸濁して目的の密度にし、計算された完全幹細胞培地の50%を含むコーティングウェルに細胞凝集体混合物をプレート化します。
注:一部の細胞株や凝集体が50 μm以下の場合は、ROCK-1阻害剤の添加が必要になる場合があります。早期原腸陥入を避けるために、<10μmを追加することをお勧めします。 - マトリックスの上に細胞を載せた培地を慎重に加えます(24ウェルプレートを使用する場合は250 μL/ウェル)。他のサイズのウェルプレートの細胞培地の推奨容量については、 表2を確認してください。
- プレートを前後および左右に数回の短い動きで傾けて、細胞の凝集体を均等に分散させます。
注意:凝集体の分布が不均一になると、ヒトiPS細胞の自然分化が増加します。塊の懸濁液が円形に広がると、塊がウェルの境界に凝集し、中心の密度が低下します。 - プレートを37°Cでインキュベートし、毎日または隔日で完全な幹細胞培地を使用して培地交換を行います。培地交換を行う場合は、培養物を視覚的に評価して増殖をモニタリングし、細胞が継代時間が必要か、分化の準備ができているかを判断します。2日間連続して給餌をスキップするには、1日に必要な培地の2倍の量を追加します。
- 計算容量の50%の完全幹細胞培地にiPS細胞の凝集体を穏やかに再懸濁して目的の密度にし、計算された完全幹細胞培地の50%を含むコーティングウェルに細胞凝集体混合物をプレート化します。
- Matrix 4-XEを含むプレートでのiPS細胞培養
- iPSCの凝集体を計算された3倍完全幹細胞培地の総量に穏やかに再懸濁し、目的の密度を得ます。
- 24ウェルプレートを使用する場合は、ハイドロゲル250 μL/ウェルの上に細胞を載せた培地を慎重に加えます。他のサイズのウェルプレートの細胞培地の推奨容量については、 表3を確認してください。
注意:ヒドロゲルは膨潤し、作りたてのものよりも大きな体積を占めます。iPSCコロニーはプレートの底部のハイドロゲルに部分的に埋め込まれるため、ハイドロゲルを乱さずに上部培地の50%〜80%を交換することをお勧めします。 - プレートを数回、すばやく、短く、前後に、および左右に動かして、細胞の凝集を均等に分散させます。
- プレートを5%のCO2 と湿度95%の37°Cのインキュベーターに置きます。完全な幹細胞培地を使用して細胞培地を交換します。毎日または隔日で媒体の変更を行います。後者の場合は、媒体の2倍のボリュームを追加します。
- 文化を視覚的に検査して、分化に適した段階に到達するまでの成長を追跡します。
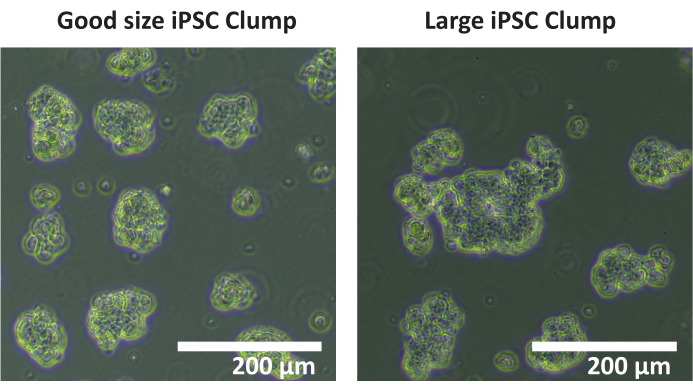
図1:最適な塊のサイズ。 最適な凝集体サイズの一例を示すiPS細胞株SCTi003Aの凝集体の画像。スケールバー = 200 μm. この図の拡大版を表示するには、ここをクリックしてください。
2. ヒトiPS細胞の分化と腸管オルガノイドの作製
注意:すべての作業は、標準的な無菌技術に従ってバイオセーフティキャビネット(BSC)で行われます。白衣、手袋、ゴーグルなどの個人用保護具の適切な使用を含む、研究所のOSHA安全基準に従う必要があります。
- 始める前に、各ステージに必要な分化培地のアリコートを準備します。アリコートを解凍した後は、すぐに使用してください。再凍結しないでください。 表5 に従って、各ステージの培地タイプと24ウェルプレートに必要な容量の一般的なガイドを示します。
注:各分化段階での最適時間は、細胞株ごとに異なる場合があります。各ステージの細胞マーカーの発現を確認することは、分化効果を向上させるために推奨されます。iPSCS培養物での遺伝子発現の定期的な評価は、低継代でベンダー適格なバッチを活用したため、この研究には含まれていませんでしたが、その後の分化ステップで新規またはまだ適格化されていないiPS細胞株の品質管理ステップとして推奨されます。 - ステージ1:確定型内胚葉(DE)
- 差別化を開始する準備状況を評価するには、次の条件を確認します。
- 顕微鏡を使用して、幹細胞コロニーのコンフルエンシーと培養物中の自然分化の量を評価します。形態学的評価だけに頼ってはいけません。最適なコンフルエンシーは85%〜90%(~105 細胞/cm2以上)で、観察される最小の自然分化は<5%の分化であるべきです。
- 次のステップに進む前に、hiPSCマーカーのフローサイトメトリー特性評価のために犠牲ウェルから細胞を採取します。フォワードスキャッターおよびサイドスキャッターゲーティング戦略を、代表的なフローサイトメトリーの特性評価に使用しました。細胞が最適な基準を満たしている場合は、分化を開始します。細胞の合格基準は、理想的には3つのマーカーの>85%の発現であり(表4)、特にラボで新規またはまだ適格化されていないiPS細胞株の場合です。
注:異なるマトリックス上で増殖したiPS細胞培養物は、マトリックス4-XE上でのiPS細胞増殖のみで同じ全体的なプロセスを経るため、半包埋細胞を乱さないように、より穏やかな培地交換が必要です。この段階では細胞が特に敏感であるため、決定的内胚葉の誘導中にかなりの細胞死が予想されます。培地交換中は注意を払い、細胞が37°Cのインキュベーション環境外にさらされる時間をできるだけ最小限に抑えることを目指します。
- 以下に述べるように細胞コロニーの分化を開始します。
- 0日目:DEミディアムのアリコートを37°Cに温めます。 加温-冷却サイクルによる培地の変性を防ぐため、0日目に必要な量(0.7 mL/ウェル)のみを温めるようにしてください。
- hiPSCからメディアを吸引します。ウェルの側面にウェルあたり0.7 mLのDE培地を慎重に加えます。コロニーを剥離または損傷する可能性のある過酷なピペッティングは避けてください。プレートを37°C、5%のCO2 、95%の湿度で24時間インキュベートします。
- 1日目:1日目に必要な量(0.5mL/ウェル)のみを含むDE培地のアリコートを37°Cまで温めます。 細胞からDE培地を吸引し、ウェルの側面にウェルごとに0.5 mLのDE培地を慎重に加えます。37°C、5%CO2 、湿度95%で24時間インキュベートします。
- 3日目:細胞は、決定的な内胚葉形成のためにアッセイする準備ができています。推奨されるマーカーについては、 表4 を参照してください。次のフェーズに進む前に、ウェルを犠牲にして、DEに関連する特定のマーカーのフローサイトメトリー特性評価を行います。フォワードスキャッターおよびサイドスキャッターゲーティング戦略を、代表的なフローサイトメトリーの特性評価に使用しました。1つ以上のマーカーの発現を確認することが推奨されます(特に、ラボ内の新規またはまだ適格化されていないiPSCラインの場合)。
- 差別化を開始する準備状況を評価するには、次の条件を確認します。
- ステージ2:中腸/後腸(MH)
- 3日目:3日目に必要な量のMH培地(0.5mL/ウェル)のみを15〜25°Cに温めます。 細胞からDE培地を吸引し、0.5 mLのMH培地と交換します。37°C、5%CO2 、湿度95%で24時間インキュベートします。
- 4日目〜9日目:毎日の培地を交換する前に、顕微鏡を2倍または4倍の倍率で使用して、目に見える3D構造を確認することによりスフェロイドの形成を評価します(4日目から発生する可能性があります)。浮遊スフェロイド(5日目から発生する場合があります)。
- スフェロイドが剥離し始めたら、1 mLピペッターを使用して培地を細胞から無菌の15 mLコニカルチューブに穏やかに移し、細胞から剥離したスフェロイドの数を評価します。
注:単層から3D構造を切り離す可能性のあるせん断力は避けてください。準備が整うと、回転楕円体は自然に分離します。 - 剥離したスフェロイドが50個未満の場合は、200 x g で5分間遠心分離し、古い培地を取り出し、スフェロイドを0.5 mL/ウェルの培地に再懸濁し、十分なスフェロイドが成熟するまでそれぞれのウェルに移します。
注:中腸/後腸培地への曝露時間は、十二指腸(短時間露露)や回腸(長期露)などの小腸オルガノイドの発達の地域的アイデンティティを決定する上で重要な役割を果たします。同じアイデンティティでより均一な培養を達成するためには、中腸/後腸培地に同時に曝露されたスフェロイドを採取することを目指します。 - 十分な数のスフェロイドが分離してヒト腸オルガノイド(hIO)培養を埋め込み開始するまで、ステップ2.3.3を繰り返します。
- 次のフェーズに進む前に、スフェロイドのサンプルを分離し、ミッドガット/ヒンドガット(MH)に関連する特定のマーカーのフローサイトメトリー特性評価を実施します。フォワードスキャッターおよびサイドスキャッターゲーティング戦略を、代表的なフローサイトメトリーの特性評価に使用しました。一般的に使用されるマーカーのリストについては、 表4 を参照してください。1つ以上のマーカーの発現を確認することが推奨されます(特に、ラボ内の新規またはまだ適格化されていないiPSCラインの場合)。
- ステージ3:回転楕円体の埋め込み
- 手続きを開始する前に、以下のものをご用意ください。
- Matrix 1-ABOとMatrix 3-ABOのアリコートを氷上で解凍します。ドームあたり30〜40μLのマトリックスが必要な場合、必要なマトリックスの総量を決定するために収集されたスフェロイドの数を考慮してください。
- 15 mM HEPESを含む25 mLのコールドAdvance DMEM/F-12を調製します。高濃度ECMは粘性があり、ピペッティングが困難です。滅菌済みの100 μLピペットチップの箱を-20°Cに置き、プロセスに役立つコールドチップを調製します。腸管オルガノイド増殖培地(OGM)のアリコートを調製しますが、これには4回のフィードが必要です(1フィードあたり0.5 mL/ウェル)。準備については 、表5 を参照してください。
- OGMサプリメントのアリコートを氷の上で解凍します。アリコートを解凍した後は、すぐに使用してください。再凍結しないでください。完全なOGMは2〜8°Cで最大2週間保存してください。
- (3x OGM)の標準製剤と比較して、3xのサプリメントを含むOGMを調製します。Matrix 4-XFO1 thought Matrix 4-XFO4を冷蔵庫から取り出し、室温(25°C)まで温めます。
- 動物由来のシステムの場合は、以下で説明する手順を実行します。
- 滅菌済みの24ウェル組織培養プレートをインキュベーターに置き、スフェロイドとマトリックスを調製しながら37°Cに温めます。採取したスフェロイドを15mLの円錐形チューブの底に沈殿させます。上清を慎重に吸引して捨てます。
注:マトリックスの影響をより正確に比較するには、hiPSCから採取したスフェロイドを各マトリックスで区別して別々のチューブに入れてください。 - 1 mLのDMEM/F-12と15 mM HEPESをスフェロイドに加えます。300 x g で5分間、室温(15〜25°C)で遠心分離します。
- 上澄みをできるだけ慎重に取り除きます。1mLピペッターで除去を開始し、100μL、さらには10μLのピペットに切り替えて、スフェロイドのペレットを乱さずにできるだけ除去することをお勧めします。
注:残りのメディア容量が大きいほど、マトリックスは希釈されます。マトリックスを希釈すると、ゲル化の問題やドームの軟化につながる可能性があります。ドームが柔らかいほど、最小限の妨害で崩壊する可能性が高くなります。 - 冷たい100 μLピペットチップ付きのピペッターを使用して、冷たい(2 - 8 °C)マトリックス1-ABOまたはマトリックス3-ABOの40 μL/50回転楕円体をそれぞれのチューブに加えます。スフェロイドをマトリックスに穏やかに分配するために、ピペッティングで~5回行います。ピペットチップを完全に空にしないでください、気泡が発生する可能性があります。
- プレートをインキュベーターから取り出し、コールドピペットチップを使用して、 図2の手順に従って、埋め込まれたスフェロイドをプレートの中央にゆっくりと移します。マトリックス1-ABOとマトリックス3-ABOを培養皿に急いで分注すると、ドームが平らになるので避けてください。
- プレートを慎重に37°Cのインキュベーターに移し、30分間インキュベートしてドームゲル化を確保します。輸送中やインキュベーター内での揺れや激しい動きには特に注意してください。
- ゲル化のためにドームをインキュベートしながら、使用するウェル数に対して十分な量の腸内OGM(0.5 mL/ウェル)を37°Cで温めます。
注意: 必要な量だけ温めてください。温暖化と冷却のサイクルは避けてください。メディアをドームに追加する前に、メディアが温まっていることを確認してください。冷たい媒体はドームの崩壊につながる可能性があります。 - 30分後、ドームを乱さないように、ウェルの側面に0.5mLの腸OGMを慎重に追加します。37°C、5%CO2 、湿度95%でインキュベートします。3〜4日ごとに培地を取り外してから新しい培地を追加して、フル培地の交換を行います。
- 滅菌済みの24ウェル組織培養プレートをインキュベーターに置き、スフェロイドとマトリックスを調製しながら37°Cに温めます。採取したスフェロイドを15mLの円錐形チューブの底に沈殿させます。上清を慎重に吸引して捨てます。
- Matrix 4-XFオルガノイドシステムの場合、記載されている手順に従ってください。
注:マトリックス4-XFオルガノイドシステムには、4つの異なるオプション(O1-O4)が含まれています。各タイプの配合は、生体機能リガンド、剛性、および分解性が異なります。したがって、特定のアプリケーションに最適なタイプを決定するために初期実験を行うことが推奨されます。このプロトコールでは、4つのオプションを使用して、hiPSC由来の腸管オルガノイドの最適な製剤を見つける方法について説明します。さらに、使用可能な培養プロトコルは複数ありますが(例:3Dカプセル化、ドームカプセル化)、このプロトコルでは、動物由来の基底膜システムを使用する際に使用される一般的な方法と直接比較できるように、ドーム法を使用します。- 16 mM HEPESを含む1 mL/ウェルのコールドアドバンスDMEM/F-12を、Matrix 4-XFO4システムで生成されたスフェロイドに加えます。300 x g で5分間、室温(15〜25°C)で遠心分離します。
注:アプリケーションに最適な処方を見つけるには、遠心分離の前にスフェロイドを4つの別々のチューブに分配してください。動物由来のマトリックス上で生成されたスフェロイドは、このシステムを使用して腸内オルガノイドに成熟させることもできます。 - 1 mLのピペッターを使用して、スフェロイドを乱さずに上清を取り除きます。50 μL の 3x OGM をスフェロイドペレット (~100 スフェロイド) に加えます。選択したMatrix 4-XFOの100 μLを50 μLのスフェロイド懸濁液に加え、5回から10回穏やかに混合します。Matrix 4-XFOと3x OGMを2:1 v/vの混合比に保ち、最終濃度を1倍にします。
- 40 μLのハイドロゲル-スフェロイド混合物を24ウェル組織培養プレートの中央に加えます。プレートを慎重に37°Cのインキュベーターに移し、30分間インキュベートします。
注:Matrix 4-XFOは、ゲル化のために37°Cのインキュベーションを必要としません。ただし、ドームのゲル化を改善するために37°Cを必要とするMatrix 1-ABOおよびMatrix 3-ABOシステムと比較した場合、オルガノイドを同様の条件にさらしておくことをお勧めします。 - 30分後、ドームを乱さないように、ウェルの側面に腸内OGMを0.5mL慎重に加えます。37°C、5%CO2 、湿度95%でインキュベートします。3〜4日ごとにフルミディアムの交換を行い、メディウムを取り外してから新しいメディウムを追加します。
- 16 mM HEPESを含む1 mL/ウェルのコールドアドバンスDMEM/F-12を、Matrix 4-XFO4システムで生成されたスフェロイドに加えます。300 x g で5分間、室温(15〜25°C)で遠心分離します。
- 手続きを開始する前に、以下のものをご用意ください。
- hIO継代と成熟
- ステップ2.4.1で行ったのと同じ化学薬品、溶液、試薬を調製します。
- 15mLのコニカルチューブ(1条件につき1本)に1〜2mLの付着防止リンス液を加え、渦巻き状にしてチューブをコーティングします。
- 付着防止液を取り出し、5mLのD-PBS(Ca++およびMg++なし)でチューブをすすぎます。すべてのコーティングされたチューブにキャップをし、必要になるまで室温(15〜25°C)に保ちます。
- ドームからメディウムを吸引します。1 mLピペットを使用して、1 mLの冷たいDMEM/F-12をドームに直接加えます。目標は、ドームをプレートから取り外すことです。
- さらに1 mLの冷たいDMEM/F-12をウェルに加え、ピペットで上下させて残りのオルガノイドを回収します。コーティングされた15mLコニカルチューブに移します。
注:顕微鏡でウェルを視覚的に調べることにより、オルガノイドの収穫が成功したことを確認します。残存オルガノイドが観察された場合は、手順2.5.5を繰り返します。 - 1 mLピペッターを使用して、懸濁液を上下にピペッティングし、オルガノイドを崩壊させ、目的のオルガノイドサイズ(100 - 500 μmなど)で均一なフラグメント懸濁液が得られます。
注:200 μLのピペッターを使用して、オルガノイドが推奨サイズに適合していることを確認してください。200 μLピペッターを使用すると、必要に応じて追加のフラグメンテーションが容易になり、フラグメントが200 μLのピペットチップをスムーズに通過できるようになります。
注意:過酷または長時間のピペッティングによってフラグメントを単一細胞に分裂させないでください。 - フラグメントをカウントするか、分割比を使用して、目的のオルガノイド密度を確立します。アリコートを分離し、ステップ 1.4.6-1.4.9 の塊カウントと同じ手順を使用してカウントを実行します。
注:最適なオルガノイド密度は、ラインごとに最適化する必要があります。一般的には、ドームあたり40〜80個の腸オルガノイドの密度が推奨されます。 - オルガノイドのカウントプロセス中にチューブが氷上に置かれていることを確認してください。約5分後、オルガノイドの破片は重力によりチューブの底に沈殿します。
注:オルガノイド溶液の体積が大きいほど、底に沈殿するまでに時間がかかります。 - オルガノイドの上に形成された上清と濁った層をできるだけ多く静かに取り除きます。オルガノイドが成熟する初期の継代では、この曇った相はマトリックスと個々の細胞を包み込みます。
- ペレットに直接ピペッティングして、2 mLの冷たいDMEM/F-12を加えます。200 x g で5分間、室温(15〜25°C)で遠心分離します。
- 動物由来のシステムの場合は、手順2.4.2.4-2.4.2.9で説明されているのと同じ手順に従って、上清を慎重に除去して廃棄します。
- Matrix 4-XFO システムの場合は、ステップ 2.4.3.2-2.4.3.4 で説明したのと同じ手順に従って、上清を慎重に取り除いて廃棄します。
注:Matrix 4-XFOシステムを使用する場合は、残留ヒドロゲルを最適に除去するために、ゼノフリーのヒドロゲルオルガノイド回収ソリューションを使用することをお勧めします。この回収ソリューションは、動物由来のハイドロゲルシステムからゼノフリーのハイドロゲルシステムに切り替える場合に特に推奨され、異種物質を確実に排除します。
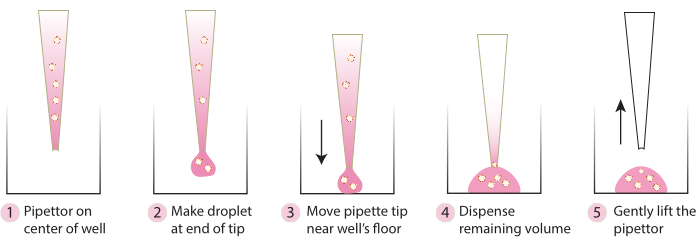
図 2.ドーム形成に推奨される技術の概略図です。 この回路図は、すべてのシステムでドーム形成を成功させるために推奨されるステップバイステップのプロセスを説明しています。 この図の拡大版を表示するには、ここをクリックしてください。
3. IOサイズ特性評価
注:オルガノイドのサイズは、4倍と10倍で撮影された明視野画像によって特徴付けられました。画像処理解析はMATLABを使用して自動化されました。プロセスの全体的な手順を以下に説明し、コードのサンプルは 補足ファイル 1 に含まれています。
- イメージを含むディレクトリを定義し、ディレクトリ内のすべてのイメージ ファイルを一覧表示します。テーブルを初期化して結果を格納します。ファイル内の明視野画像を読み取ります。
- ピクセルからμmへの変換を定義し、スケールを設定します。画像にスケールバーが含まれていない場合は、ピクセルからμmへの変換係数をユーザーに要求します。
- 画像をグレースケールに変換します。ガウスフィルターを適用して、画像内のノイズを減らします。フィルタリングされた画像をしきい値にして、オルガノイドを背景から分離します。
- 小さな穴を埋め、小さなオブジェクトを削除して、バイナリイメージをクリーンアップします。連結成分分析を実行して、個々のオルガノイドを特定し、面積、重心、長軸の長さ、短軸の長さなどの特性を計算します。
- 長軸と短軸の長さに基づいてオルガノイドサイズを計算します。セグメント化されたオルガノイドを元の画像に表示し、そのサイズでラベルを付けます。オルガノイドサイズを印刷し、結果を.cvsファイルに保存します。
注:最初のいくつかの画像は、ガウスフィルタの標準偏差としきい値までの領域の最適なパラメータを決定するために手動で分析されました。 補足ファイル1 のコードは、明視野画像からのオルガノイドサイズ分析の基本的なフレームワークの例を示しています。ただし、各画像タイプと品質の特定の要件に合わせて、さらに改良する必要があります。同じプロセスは、ImageJのFIJIなどのオープンソースソフトウェアを使用して実行できます。 - 以下の手順に従って、FIJIソフトウェアを使用してください。
- ピクセルからμmへの変換を定義し、スケールを設定します。画像にスケールバーが含まれていない場合は、[ 分析] > [スケールの設定] をクリックして、ピクセルから μm への変換係数をユーザーに要求します。
- [ Image (画像)] > Type > 8 bit(8ビットタイプ)をクリックして、画像をグレースケールに変換します。ガウス フィルターを適用して画像のノイズを減らすには 、[処理] > [フィルター] >をクリックし、[ガウスの宣伝文句] > [使用するシグマ (半径)] : 2 をクリックします。
- オルガノイドを背景から分離するためにフィルタリングされた画像をしきい値にするには 、「Image > Threshold」>「MaxEntropy」>「Apply」をクリックします。
- 小さな穴を埋め、小さなオブジェクトを削除してバイナリ画像をクリーンアップするには、[ 処理] > [ノイズ] > [外れ値の削除] を 20 ピクセル>クリックします。
- 接続された成分分析を実行して個々のオルガノイドを特定し、面積、重心、長軸の長さ、短軸の長さなどのプロパティを計算するには、[ 分析] > [測定を設定] >をクリックし、[面積]、[周囲長]、[直径] >が含まれていることを確認します [分析] > [粒子の分析] > [アウトラインを表示] をクリックします。
- 統計分析
- JMP(SAS)ソフトウェアを使用したSaphiro-Wilk検定によるデータ分布の正規性を評価します。グループ間の統計的差を調べるには、二元配置分散分析を実行し、JMP(SAS)ソフトウェアのノンパラメトリックWilcoxon法を使用して事後検定を実行します。有意性は、p ≤ 0.05 のアルファ レベルで確立されました。
結果
このプロトコールに従って、市販の基底膜とゼノフリーのハイドロゲルシステムを利用して、hiPSC細胞を培養し、それらをhIOに分化させることに成功しました。これらの実験の主な目的は、hiPSCおよびhIO研究のためのさまざまなソースからのマトリックスの同等性を体系的に評価することでした。このプロトコールの最初のセクションでは、効率的な腸内オルガノイド生成をもたらす健康なiPS...
ディスカッション
幹細胞およびオルガノイドの作業に最適な微小環境を選択することは、これらのプラットフォームを幅広いアプリケーションに使用する際の極めて重要な初期ステップです。私たちの代表的な結果は、マトリックス4-XFO3が高濃度の成長因子と組み合わさってより大きなオルガノイドにつながることを示しており、ゼノフリーハイドロゲルの物理的特性を利用して、これらのシステムを使用し?...
開示事項
ジョン・フアン博士は、TheWell Bioscienceの創設者兼CEOです。
謝辞
著者らは、Christina Pacak博士、Silveli Susuki-Hatano博士、Russell D'Souza博士によるhiPSCおよびオルガノイド研究の開始に関する以前のトレーニングと一般的な推奨事項を認めています。彼らは、 in vitro 細胞培養作業にハイドロゲルシステムを使用するための指導を提供してくれたChelsey Simmons博士に感謝しています。また、著者らは、hiPSC培養に関する指導をいただいたSTEMCELL TechnologiesのChristine Rodriguez博士とThomas Allison博士に感謝します。また、著者は、出版費用を負担してくれたTheWell Bioscienceにも感謝しています。
資料
| Name | Company | Catalog Number | Comments |
| 24-Well Plate (Culture treated, sterile) | Falcon | 353504 | |
| 37 °C water bath | VWR | ||
| 96-well plate | Fisher Scientific | FB012931 | |
| Advanced DMEM/F12 | Life Technologies | 12634 | |
| Anti-adherence Rinsing Solutio | STEMCELL Technologies | 7010 | |
| Biological safety cabinet (BSC) | Labconco | Logic | |
| Brightfield Microscope | Echo Rebel | REB-01-E2 | |
| BXS0116 | ATCC | ACS-1030 | |
| Centrifuge with temperature control (4 °C capabilities) | ThermoScientific | 75002441 | |
| Conical tubes, 15 mL, sterile | Thermo Fisher Scientific | 339650 | |
| Conical tubes, 50 mL, sterile | Thermo Fisher Scientific | 339652 | |
| Cultrex RGF BME, Type 2 | Bio-techne | 3533-005-02 | |
| Cultrex Stem Cell Qualified RGF BME | Bio-techne | 3434-010-02 | |
| D-PBS (Without Ca++ and Mg++) | Thermo Fisher Scientific | 14190144 | |
| GeltrexLDEV-Free, hESC-Qualified Reduce Growth Factor | Gibco | A14133-02 | |
| GlutaMAX Supplement | Thermo Fischer Scientific | 35050-061 | |
| Guava Muse Cell Analyzer or another flow cytometry equipment (optional) | Luminex | 0500-3115 | |
| HEPES buffer solution | Thermo Fischer Scientific | 15630-056 | |
| Heralcell Vios Cell culture incubator (37 °C, 5% CO2) | Thermo Scientific | 51033775 | |
| JMP Software | SAS Institute | JMP 16 | |
| MATLAB | MathWorks, Inc | R2022b | |
| Matrigel Growth Factor Reduced (GFR) Basement Membrane Matrix LDEV free | Corning | 356231 | |
| Matrigel Matrix High Concentration (HC), Growth Factor Reduced (GFR) LDEV-free | Corning | 354263 | |
| mTeSR Plus Medium | STEMCELL Technologies | 100-0276 | |
| Nunclon Delta surface treated 24-well plate | Thermo Scientific | 144530 | |
| PE Mouse Anti-human CD326 (EpCAM) | BD Pharmingen | 566841 | |
| PE Mouse Anti-human CDX2 | BD Pharmingen | 563428 | |
| PE Mouse Anti-human FOXA2 | BD Pharmingen | 561589 | |
| PerCP-Cy 5.5 Mouse Anti-human SSEA4 | BD Pharmingen | 561565 | |
| ReLeSR | STEMCELL | 5872 | |
| SCTi003-A | STEMCELL Technologies | 200-0510 | |
| Serological pipettes (10 mL) | Fisher Scientific | 13-678-11E | |
| Serological pipettes (5 mL) | Fisher Scientific | 13-678-11D | |
| STEMdiff Intestinal Organoid Growth Medium | STEMCELL Technologies | 5145 | |
| STEMdiff Intestinal Organoid Kit | STEMCELL Technologies | 5140 | |
| Vitrogel Hydrogel Matrix | TheWell Bioscience | VHM01 | |
| VitroGel ORGANOID Discovery Kit | TheWell Bioscience | VHM04-K |
参考文献
- Hynes, R. O. Integrins: Bidirectional, allosteric signaling machines. Cell. 110 (6), 673-687 (2002).
- Frantz, C., Stewart, K. M., Weaver, V. M. The extracellular matrix at a glance. J Cell Sci. 123, 4195-4200 (2010).
- Hinz, B., Gabbiani, G. Fibrosis: Recent advances in myofibroblast biology and new therapeutic perspectives. F1000 Biol Rep. 2, 78 (2010).
- Pickup, M. W., Mouw, J. K., Weaver, V. M. The extracellular matrix modulates the hallmarks of cancer. EMBO Rep. 15 (12), 1243-1253 (2014).
- Rozario, T., DeSimone, D. W. The extracellular matrix in development and morphogenesis: A dynamic view. Dev Biol. 341 (1), 126-140 (2010).
- Even-Ram, S., Artym, V., Yamada, K. M. Matrix control of stem cell fate. Cell. 126 (4), 645-647 (2006).
- Engler, A. J., Sen, S., Sweeney, H. L., Discher, D. E. Matrix elasticity directs stem cell lineage specification. Cell. 126 (4), 677-689 (2006).
- Tran, O. N., et al. Organ-specific extracellular matrix directs trans-differentiation of mesenchymal stem cells and formation of salivary gland-like organoids in vivo. Stem Cell Res Ther. 13 (1), 306 (2022).
- Nikolaev, M., et al. Homeostatic mini-intestines through scaffold-guided organoid morphogenesis. Nature. 585 (7826), 574-578 (2020).
- Gjorevski, N., et al. Designer matrices for intestinal stem cell and organoid culture. Nature. 539 (7630), 560-564 (2016).
- Gjorevski, N., et al. Tissue geometry drives deterministic organoid patterning. Science. 375 (6576), (2022).
- Heo, J. H., Kang, D., Seo, S. J., Jin, Y. Engineering the extracellular matrix for organoid culture. Int J Stem Cells. 15 (1), 60-69 (2022).
- Shamir, E. R., Ewald, A. J. Three-dimensional organotypic culture: experimental models of mammalian biology and disease. Nat Rev Mol Cell Biol. 15 (10), 647-664 (2014).
- Clevers, H. Modeling development and disease with organoids. Cell. 165 (7), 1586-1597 (2016).
- Jung, P., et al. Isolation and in vitro expansion of human colonic stem cells. Nat Med. 17 (10), 1225-1227 (2011).
- Lancaster, M. A., Knoblich, J. A. Organogenesis in a dish: Modeling development and disease using organoid technologies. Science. 345 (6194), 1247125 (2014).
- Huch, M., et al. In vitro expansion of single Lgr5+ liver stem cells induced by Wnt-driven regeneration. Nature. 494 (7436), 247-250 (2013).
- Greenlee, A. R., Kronenwetter-Koepel, T. A., Kaiser, S. J., Liu, K. Comparison of Matrigel and gelatin substrata for feeder-free culture of undifferentiated mouse embryonic stem cells for toxicity testing. Toxicol In Vitro. 19 (3), 389-397 (2005).
- Geltrex LDEV-Free, HESC-Qualified, Reduced Growth Factor Basement Membrane Matrix User Guide (Pub.No. MAN0007336 3.0. Fisher Scientific Available from: https://www.thermofisher.com/document-connect/document-connect.html?url=https://assets.thermofisher.cn/TFS-Assets%2FLSG%2Fmanuals%2FGeltrex_LDEV_Free_hESC_qualified_PI.pdf (2024)
- biotechne R&D Systems. Cultrex Stem Cell Qualified Reduced Growth Factor. biotechne R&D Systems. , (2024).
- VitroGel Organoid Protocol. TheWell Bioscience Available from: https://www.thewellbio.com/video-protocols (2024)
- Spence, J. R., et al. Directed differentiation of human pluripotent stem cells into intestinal tissue in vitro. Nature. 470 (7332), 105-110 (2011).
- Henderson, J. K., et al. Preimplantation human embryos and embryonic stem cells show comparable expression of stage-specific embryonic antigens. Stem Cells. 20 (4), 329-337 (2002).
- Haruna, N. F., Huang, J. Investigating the dynamic biophysical properties of a tunable hydrogel for 3D cell culture. J Cytol Tissue Biol. 7, 30 (2020).
- Cherne, M. D., et al. A synthetic hydrogel, VitroGel ORGANOID-3, improves immune cell-epithelial interactions in a tissue chip co-culture model of human gastric organoids and dendritic cells. Front Pharmacol. 12, 707891 (2021).
- Stewart, D. C., et al. Quantitative assessment of intestinal stiffness and associations with fibrosis in human inflammatory bowel disease. PLoS One. 13, e0200377 (2018).
- Hernandez-Gordillo, V., et al. Fully synthetic matrices for in vitro culture of primary human intestinal enteroids and endometrial organoids. Biomaterials. 254, 120125 (2020).
- Broguiere, N., et al. Growth of epithelial organoids in a defined hydrogel. Adv Mater. 30, 1801621 (2018).
- Barthes, J., et al. Cell microenvironment engineering and monitoring for tissue engineering and regenerative medicine: The recent advances. BioMed Res Int. 2014, 921905 (2014).
- Engler, A. J., Sen, S., Sweeney, H. L., Discher, D. E. Matrix elasticity directs stem cell lineage specification. Cell. 126 (4), 677-689 (2006).
- Aisenbrey, E. A., Murphy, W. L. Synthetic alternatives to Matrigel. Nat Rev Mater. 5 (7), 539-551 (2020).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved