Method Article
Syngeneic fare B hücreli lenfoma manken CD19 araba T hücrelerinin önceden klinik değerlendirme için
Bu Makalede
Özet
Burada, üretim ve retroviral iletim ve kullanımı karşı kurulan syngeneic A20 B hücreli lenfoma veya lymphodepleting olmadan BALB/c farelerde tedavi olarak fare CD19 araba T hücrelerinin önceden klinik test için bir iletişim kuralı mevcut önceden Klima.
Özet
CD19 chimeric antijen reseptör (araba) T-hücre tedavisi şaşırtıcı klinik başarı iki ikinci nesil chimeric antijen reseptör (CARs) onayı ile akut lenfoblastik lösemi (ALL) andnon-Hodgkin Lenfoma (NHL) açmıştır. Alanın odak şimdi nerede daha az etkileyici tam yanıt oranları gözlenmektedir diğer hematolojik maligniteler bu başarılar taklit olduğunu. Daha fazla araba T hücreleri veya diğer tedavi şekilleri, iş yönetimi mühendislik başarıyla diğer kanser ayarları başarılı tedavi için engelleri aşmak.
Bu yüzden hangi-ebilmek davranış diğerleri CD19 araba T hücrelerinin önceden klinik test modeli mevcut. Bu iyi test B hücreli lenfoma model sonuçlarında bilgilendirici araba T-hücre tedavisi genel olarak etkilenebilir.
Bu iletişim kuralı kalsiyum fosfat transfection Plat-E yapımcı hücre MP71 retroviral yapıları ve pCL-Eco ambalaj plazmid salgılanan retroviral parçacıklar topluluğu tarafından takip ile araba T hücreleri fare tekrarlanabilir üretimi sağlar ve Rekombinant insan fibronektin parçası ve Santrifüjü kullanarak hedefidirler. Retroviral hedefidirler geçerliliğini ve hedef lenfoma hücreleri ex vivo, akış sitometresi, luminometry ve enzim bağlı immunosorbent kullanılarak öldürmek için yetenek araba T hücrelerinin onay assay (ELISA), ayrıca tanımlanmaktadır.
Araba T testleri için protokolleri hücreleri vivo içinde lymphoreplete ve lymphodepleted syngeneic fareler, kurulan, sistemik lenfoma taşıyan açıklanmıştır. Anti-kanser faaliyet içinde vivo bioluminescence ve hastalık ilerleme tarafından izlenir. Biz tipik sonuçları giderme kurulan B hücreli lenfoma 1st veya 2nd üretimi arabalar lymphodepleting öncesi klima ve araba T kullanan zaman uzun süreli remisyon elde fareler bir azınlık ile birlikte kullanan göstermek IL-12 lymphoreplete farelerde ifade hücreleri.
Bu protokoller CD19 araba T hücreleri farklı ek değişiklik, araba T hücrelerinin kombinasyonları ve diğer terapötik ajanlar ile değerlendirmek için kullanılan ya da farklı hedef antijenlere karşı araba T hücreleri kullanımı için uyarlanmış.
Giriş
Chimeric antijen reseptör (araba) T-hücre tedavisi CD19 tedavisinde şaşırtıcı klinik başarı göstermiştir+ tisagenlecleucel Relaps Akut lenfoblastik lösemi1 ve axicabtagene için onaylanması için önde gelen maligniteler ciloleucel ilerici büyük B hücreli non-Hodgkin Lenfoma için2 2017.
Kanser ve bağışıklık sistemi hastalığı ilerleme ve tedavi mekanizmaları arasındaki etkileşimler önemi giderek tanınan3,4,hale geliyor5. Örneğin, iyi tümör microenvironment (TME) suda yüzen bağışıklık hücreleri6,7,8efektör fonksiyonları önleyebilirsiniz faktörleriyle olduğu belgelenmiştir. Alternatif olarak astar endojen bağışıklık hücreleri ve epitope yayılan tümör ortadan kaldırılması ve uzun vadeli direnci tümör meydan9,10anahtar olabilir. Bu olayların her ikisi de bir bağışıklık sistemi eksikliği xenogeneic modellerinde değerlendirilemez. Aynı şekilde, transgenik proteinler kullanan sistemleri11,12yayılan epitope için gerekli olan bağışıklık toleransı kırma meydan doğru bir şekilde yansıtmıyor. Syngeneic manken tamamen işlevsel bir bağışıklık sistemi, bu nedenle, kanser hastalığı ilerleme ve bağışıklık tedavi bu önemli yönleri modelleme için her şeyden önemlidir.
Araba T-hücre tedavisinin önemli bir uyarı lymphodepleting öncesi Klima tedavi başarı13,14için gerekli olmasıdır. Bu genellikle hastalarda infüzyon araba T hücreleri15,16önce kemoterapi yönetmek olarak elde edilir. Standart bir yöntem, hasta ayarlarında kullanılan lymphodepletion taklit etmek için bizi 5 Gy tüm vücuda radyasyon vermeliyiz (TBY) lymphodepletion sistemik A20 B hücreli lenfoma taşıyan fareler için tedavi edici araba T hücrelerinin yönetim önce ulaşmak için yönetmek.
Lymphodepleting öncesi Klima hastaların çoğu için bir sorun olmasa da, kemoterapötik ajanlar ile gelir toksisitesi düşük performans durumu hastaların araba T-hücre tedavisi için uygun değildir anlamına gelir. Lymphodepletion için uygun olmayan hastalar temsil eden bir test sistemi oluşturmak için hangi biz araba T-hücre tedavisi lenfoma model bir lymphoreplete syngeneic fare modeli kurduk. Bu modelde, biz IL-12 den salgı araba T hücreleri içinde kurulan lenfoma eradikasyonu ile başarı oranı neden olabilir gösterdi ~ % 2517. Ayrıca, endojen bağışıklık hücreleri kanser eradikasyonu dahil gösterdi.
Burada biz ayrıntılı olarak fare araba T hücrelerinin üretimi için protokol syngeneic fareler ve araba T hücreleri ile veya lymphodepleting öncesi Klima kullanımı olmadan lenfoma tedavisinde lenfoma kurulması tarif. Bu araba T hücreleri ile diğer transgenes test diğer ajanlar ile araba T hücrelerinin kombinasyonu etütler veya diğer evlat edinen hücre terapisi ya da immünoterapi stratejileri lenfoma karşı kullanımı için kullanılabilir.
Protokol
Tüm hayvan deneyleri hayvanlar (bilimsel yordamlar) Yasası 1986'da ve İngiltere'de Koordinasyon Komitesi altında kanser araştırma yönergeleri için yapılmıştır. Tüm hayvan çalışmaları CRUK-Manchester Enstitüde yürütülen ve yerel hayvan refah tarafından onaylanmış ve etik vücut (CRUK-MI AWERB) gözden geçirin.
1. hazırlıkları
- Maxiprep pMP71 retroviral inşa plazmid ve pCL-Eco retrovirüsü ambalaj plazmid18.
Not: pMP71 mCherry ve FMDV2A dizisi tarafından ayrılmış araba kodlar. Bu diğer retroviral yapıları ile değiştirilebilir. pCL-Eco gag, pol ve ecotropic zarf protein kodlar. - Tam T hücre Orta (TCM) RPMI 1640 orta, % 10 FCS, %1 100 x penisilin-streptomisin-glutamin (PSG) kullanarak fare T hücre kültürü çalışmalarının için hazırlayın.
Not: Çözüm içeren 100 IU/mL penisilin, 100 µg/mL streptomisin ve 2 mM L-glutamin), 50 mikron β-mercaptoethanol ve 25 mM 4-(2-hydroxyethyl)-1-piperazineethanesulfonic asit (HEPES). - RPMI 1640, % 10 FCS ve 0.05 mM β-mercaptoethanol 37 ° c, % 5 CO2A20 hücre kültür.
- Tam Dulbecco'nın değiştirilmiş kartal Orta (DMEM) (DMEM ile % 10 fetal buzağı serum (FCS), 2 mM L-glutamin, 1 μg/mL puromisindir ve 10 μg/mL blasticidin) 37 ° C'de platin-E (Plat-E) hücrelerdeki %5 kültür CO2.
Not: Plat-E hücreleri 293T hücrelerden türetilir ve gag, pol ve ecotropic zarf retroviral proteinler ifade eder. - Transfection medya çözümleri 1 ve 2 transfection hemen önce hazırlayın. Çözüm 1 (pH 7,9) DMEM + % 10 FCS + 25 mM HEPES, çözüm DMEM + 25 mM HEPES içerecek şekilde 2 (pH 7.1) içerecek şekilde hazırlayın.
- Steril fosfat tamponlu tuz ile (PBS) sulandrarak 10 μg/mL rekombinant insan fibronektin parçası solüsyon hazırlamak ve -20 ° C'de kullanmak kadar saklamak.
- Steril tüm medya kullanım (hariç rekombinant insan fibronektin parçası) önce 0,2 mikron filtrelerden filtre.
2. retroviral iletim T hücreleri
- 1. gün: Hazırlık transfection için
- Tohum 7.5 x 106 platin-E (Plat-E) 15 cm2 doku kültürü yemekleri 18 ml tam DMEM hücreleri ve gecede kuluçkaya 37 ° C, % 5 CO2.
- 2. gün: Transfection Plat-E retroviral ambalaj hücre hattı
- Pcl-Eco ambalaj vektörünün DNA, transfected retroviral araba yapý ve 1 M CaCl2 3 mL transfection çözüm 2 15 cm2 çanak başına son hacmi 150 μL kodlama plazmid DNA 39,6 μg 20.4 μg hazırlayın. 10 s ve 5 dk boyunca için girdap
- DMEM medya gelen 15 cm2 yemekler kaldırın ve 12 mL transfection çözeltisi 1 ile değiştirin.
Dikkat Medya değiştirirken, 15 cm2 yemekleri merkezinde kuru olabilir. Bu transfected Plat-E hücrelerinin önemli ölüme neden olabilir. Hızla iş ve medya sadece 1-2 tabak bir zaman kaldırabilirsiniz. - 3 mL transfection solüsyon içeren DNA ve CaCl2 her 15 cm2 yemek için drop-wise, eşit olarak her plaka arasında 2 ekleyin. Yavaşça 37 ° c, % 5 CO2 gecede 10 s. Incubate için bir yan yana hareket ile taş plakalar.
- 3. gün: Hazırlık virüs içeren süpernatant iletim için
- 18 mL transfected plaka-E hücrelerle medya TCM tamamlamak ve kuluçka için dönmek eski yerine koymak.
Dikkat Ne zaman medya 15 cm2 yemekleri değiştirme merkezinde kuru olabilir. Bu transfected Plat-E hücrelerinin önemli ölüme neden olabilir. Hızla iş ve medya sadece 1-2 tabak bir zaman kaldırabilirsiniz.
- 18 mL transfected plaka-E hücrelerle medya TCM tamamlamak ve kuluçka için dönmek eski yerine koymak.
- 3. gün: İzolasyon ve vitro fare dalak T Hücre aktivasyonu
- 6-8-hafta-yaşlı BALB/c fareler daha önce Parkinson vd tarafından açıklandığı gibi dalağı kaldırmak 19 ve onları içinde steril, buz gibi PBS 50 mL konik tüp içinde.
- Bir dalak 1.5 mL microcentrifuge tüp aktarıp bir havaneli ile en az güç kullanarak homojenize cımbız kullanın.
- 1000 μL pipet kullanın ve ~ 5 mL bir tek hücre süspansiyon ulaşmak için PBS içeren bir 50 mL tüp yapıştırılmış bir 100 mikron gözenek hücre süzgeç homogenate aktarmak için 800 μL PBS. 2.4.2 ek dalağı için yineleyin. Tüp başına 3 dalağı fazla olamaz.
Dikkat Filtreden geçirilen Splenocytes kümeleri ayakta bırakılırsa oluşabilir. El ile tüpler zaman zaman girdap topaklanma Hücre önlemek için birkaç dalağı işleme. Hücre süzgeç parçaları kalan daha fazla bir dalgıç dan en az güç kullanarak bir 5 mL şırınga kullanarak püre. - 20 mL PBS ile top. 20 mL hücre süspansiyon yavaşça 20 mL yoğunluğu degrade medya (Tablo reçetesi) 50 mL tüp üzerine katman. Uygulanan hiçbir fren ile 800 x g-20 dk için de sonuç yer paylaşımlı süspansiyon santrifüj kapasitesi.
- Hücreleri bir steril Pasteur pipet ve 50 mL tüp transferi kullanarak arabirim katmanı, hasat. 50 mL yıkamak için PBS ve vasıl 800 x g 10 dk santrifüj ile top. Süpernatant atın ve tam TCM hücrelerde yeniden askıya alma.
- Bir hemasitometre kullanarak hücreleri saydırmak.
- Kültür hücreleri, 5 x 106 hücre/mL 30 ng/mL anti-CD3ε antikor ile tam TCM yoğunluğu (145-2 C 11 Clone), 30 ng/mL anti-CD28 antikor (klon 37.51), 100 U/mL rekombinant insan IL-2 ve 2 ng/mL rekombinant fare IL-7. Bir uygun ölçekli doku kültürü şişesi hasat hücreleri cilt için kullanın.
Not: -Antijen sunan hücreler arıtılmış T hücreleri ile işe antikorlar ile kat plakalar için gerekli ise T Hücre aktivasyonu için CD3 ve CD28 antikorlar tarafından gerekli olan veya manyetik boncuklar (Tablo reçetesi) kullanın - Fare splenocytes 37 ° c, % 5 CO2 gecede kuluçkaya.
- 3. gün: Hazırlanması işi tabak iletim
- Kat doku kültürü 6-şey tabak 2 mL 10 μg/mL rekombinant insan fibronektin ile parçalara ayırması ve gecede 4 ° C'de kuluçkaya
- 4. gün: İletim fare T hücrelerinin
- Rekombinant insan fibronektin parçası boyalı tabak taze doku kültürü 6-şey tabakaları bana aktarın. Bu tabakları gecede 4 ° C'de 2. round iletim için kuluçkaya.
- TCM 2 mL orijinal rekombinant insan fibronektin parçası kaplı levhalar her şey için eklenir ve non-spesifik bağlama engellemek için oda sıcaklığında 30 dakika bırakılır.
- Retrovirüs içeren süpernatant 15 cm doku kültürü yemekleri ve eski yerine koymak ile tam TCM 18 mL transfected Plat-E hücrelerden hasat.
Dikkat Hızla Plat-E hücrelerinin kurutma önlemek için çalışır.
Not: Transfection başarısı bu aşamada bir floresan marker gen mCherry (Şekil 1) gibi kullanarak Eğer floresans mikroskobu tarafından denetlenebilir. - Retrovirüs içeren süpernatant 0,45 mikron hücre artıkları kaldırmak için filtre filtre. TCM rekombinant insan fibronektin parçası kaplı 6-şey plakalar kaldırın ve filtre uygulanmış süpernatant retrovirüsü içeren veya her şey için 2.5 mL ekleyin (kullanım yüzdesi TCM sahte transfection için). Her şey retrovirüsü veya sahte medya eklenmesi olarak etiketleyin.
- Plakayı vasıl 1200 x g için oda sıcaklığında 30 dk santrifüj kapasitesi.
- Tabak iplik aktive T hücreleri toplamak ve bir hemasitometre kullanarak saymak.
- İletim 5 x 10 aktif6 splenocytes 5 mL/iyi toplam ile gerçekleştirilir. Santrifüjü 500 x g 5 min için de tarafından splenocytes sahte/iletim ayrı tüpler için gerekli sayıda cips.
- Filtre uygulanmış retrovirüsü içeren süpernatant adım 2.6.4 2.5 mL başına 5 x 106 hücre yoğunluğu, splenocytes veya TCM bir negatif kontrol yeniden askıya alma. Rekombinant insan IL-2 (hIL-2) ve rekombinant fare (MIL-7) 7 Il-200 IU/mL ve 4 ng/mL nihai bir konsantrasyon sırasıyla ekleyin.
- 6-iyi plakaları adım 2.6.5 bitiminde santrifüj toplamak ve iyi/5 mL son hacmi yapmak için uygun wells ve 100 U/mL hIL-2 ve 2 ng/mL MIL-7 son bir konsantrasyon 2.5 mL/iyi yeniden askıya alınmış splenocytes ekleyin.
- Plakaları, 1200 x g için oda sıcaklığında 90 dk santrifüj kapasitesi. Santrifüjü sonra plakaları 37 ° c, % 5 CO2 gecede kuluçkaya.
- 5. gün: 2. Round iletim
- Bu yeniden kullanılabilir olarak rekombinant insan fibronektin parçası plakalar toplamak. Adımları yineleyin 2.6.2 - 2.6.5.
- Tabak iplik iken, hücreleri 1st bir Pasteur pipet kullanarak iletim, toplamak. Her şey 2 mL PBS ile durulayın, girdap ve her şey içinde kalan hücreleri toplamak.
Not: Pipet yukarı ve aşağı posalı hücreleri yeniden askıya almak. Ayrı tüpler her denetim/iletim grupta toplamak. - Santrifüj tüpleri 500 x g 5 dk. yeniden askıya hücrelerde iletim 200 IU/mL IL-2 ve 4 ng/mL 7 Il-kuyu başına 2.5 mL için de. Adımları yineleyin 2.6.7 - 2.6.8.
- Santrifüj hücre kaldırma ve 37 ° c, % 5 CO2 4 h toplamak transduced hücreler olduğu gibi adımları 2.7.2-2.7.3 için kuluçkaya.
- Hücreleri saymak, santrifüj kapasitesi 500 x g 5 min için de ve 1 x 106 hücre/mL 100 U/mL hIL-2 ve 2ng/mL yoğunluğu, tam TCM yeniden askıya MIL-7. Bir uygun ölçekli kültür şişesi aktarmak ve 37 ° C, % 5 CO2kuluçkaya.
- Taze TCM medya 100U/mL hIL-2 ve 2ng/mL içeren eklemek MIL-7 her 2 günde 1 x 106 hücre/mL hücre yoğunluğu korumak.
Not: Hasat splenocytes hücre türü içerir. Bu kültür koşullar altında olmayan T hücreleri 2-3 gün boyunca uzakta ölmek. Sonra ~ 4 gün içinde hücre kültürü, T hücre sayısı 0 gün hasat splenocytes toplam sayısı genellikle eş değerdir.
3. iletim verimlilik ölçümü
- 4. gün mesaj iletim üzerinde transduced veya transduced T hücreleri (yaklaşık 3 x 105 hücreleri) örnek toplamak. 500 x g 5 min için de hücre süspansiyon santrifüj kapasitesi, süpernatant atmak, PBS pelleted hücrelerle bir kez yıkama ve tekrar santrifüj kapasitesi.
- Süpernatant atmak ve bir uygun Amin reaktif boya (Örneğin, canlı/ölü leke, 1 100 seyreltme) iyi ücret içeren PBS 100 μL ekleyin. 15 dakika içinde belgili tanımlık karanlık oda sıcaklığında kuluçkaya.
- İki kez PBS ile yıkama ve 5 dk. atma süpernatant 500 x g, santrifüj kapasitesi ve Fc reseptör (1 100 seyreltme) engelleme için anti-fare CD16/CD32 antikorlar içeren FACS arabelleği 50 μL ile kuluçkaya. 4 ° C'de 10 dakika için kuluçkaya
- Doğrudan Anti-fare BV786 CD4 ve CD8-BV711 antikorlar (1 μL/kuyuda FACS arabellek son konsantrasyonu) içeren ana mix boyama antikor 50 μL ekleyin. Karanlıkta 4 ° C'de 30 dk için kuluçkaya. 3.3 yıkama adımı yineleyin. % 1 İngiltere'de yılın arabellek hücrelerde yeniden askıya alma ve tutmak göre Akış Sitometresi Analizi kadar 4 ° C'de karanlıkta.
- Hücreleri CD4 ve CD8 alt ve sırasıyla (Şekil 2) geçişi araba ifade işaretleyici olarak BV711, BV785 ve mCherry floresan kullanarak eşdeğer uygun sitometresi ile analiz.
4. vitro doğrulama araba T hücre etkinliği
- Tohum syngeneic hedef CD19+ tümör hücreleri içeren veya içermeyen bir yoğunluk luciferase ifade 1 x 104 hücrelerinin 100 μL TCM/iyi bir 96-şey U-alt doku kültürü plaka.
- 1 x 104 CD19 araba T hücreleri/iyi 100 μL/hedef (E:T) oranı 1:1 bir efektör ulaşmak için iyi bir ses ekleyin.
Not: E:T oranları kurulan her araç için inşa ve hedef hücre satırı. - Kullanım T hücreleri yalnız ve tümör hücreleri negatif kontrolleri yalnız ve T hücrelerinin phorbol-myristate-asetat tarafından (PMA) uyarılmış (50 ng/mL) ve ionomycin (1 μg/mL) Interferon Gama (IFNγ) serbest bırakılması için pozitif kontrol olarak. Ortak kültür hücreleri 37 ° c, % 5 CO2 16-24 h için.
- Ortak kültür, 500 x g 5 min için de tabak santrifüj kapasitesi ve daha fazla IFNγ ve IL - 12p 70 ELISA analiz süpernatant toplamak.
Not: Bu-ebilmek var olmak stok-80 ° C'de - Hücre granül biyoluminesans (son konsantrasyon 1.5 mg/mL) içeren PBS 100 μL içinde yeniden askıya alma. Plakayı 37 ° C'de 10 dakika için kuluçkaya Sonra uygun bir luminometer ile her kuyudan ışıldama ölçmek.
Not: Pozlama süreleri hücre satırları ve yoğunluğu için optimize edilmiş olması gerekir. Temsilcisi sonuçları Şekil 3aiçinde gösterilir. Ex vivo sitotoksisite araba T hücrelerinin hızlı biyoluminesans için hedef antijen ifade hücre hatları ile ortak kültür tarafından değiştirilebilir. Araba T hücreleri hedef hücreleri öldürmek gibi biyoluminesans serbest bırakmak, bu nedenle luminometry sinyal bir azalma hücre öldürme ile ilişkilidir. Sigara transduced hücreleri kez özellikle uzun bir kuluçka dönemi hedef hücre canlılığı üzerinde bir etkisi olabilir. Konsantrasyon fare IFNγ ve IL - 12 p 70 süpernatant üreticinin ELISA protokolleri göre ölçmek. Temsilcisi sonuçları (Şekil 3b ve 3 c) gösterilir. Araba T hücreleri hedef antijen ifade hücre hatları ile ortak kültür tarafından aktivasyonu ex vivo süpernatant içeriğini ELISA kullanarak analiz ederek denetlesinler. Ortak kültür süresinin uzunluğu ve araba T hücre hedef hücrelere oranı her araba inşa etmek, hedef hücre kültürünü ve analit için optimize edilmiş olması gerekir. PMA ve ionomycin tedavi olumlu bir denetim olarak T hücreleri ve tepki yeteneğini kendi kalitesini doğrulamak için kullanılabilir.
5. anti-kanser faaliyet farelerde değerlendirmek
-
Protokol 1
- 100 mg/kg intravenöz (IV) teslimini siklofosfamid 6-8 haftalık BALB/c fareler içine gerçekleştirin. Bu tümör engraftment önemli lymphodepletion17 (Şekil 4) olmadan sağlar.
Not: A20 kurulması lenfoma suboptimal almak oranıyla üzerinden 2 ay sürebilir. Bu tarafından 1 gün önce teslim lenfoma hücrelerinin siklofosfamid kullanımı geliştirilebilir. Lymphoreplete fareler çalışma için bir doz lymphodepletion neden olmadan lenfoma verimliliğini artırabilir siklofosfamid tespit edilmiştir. - Ertesi gün, 5 x 105 syngeneic A20 B hücreli lenfoma hücre luciferase ve yeşil flüoresan protein (GFP) hızlı şekilde modifiye 100 µL intravenöz (IV) enjeksiyonu ile fareler enjekte.
- Fareler için sistemik lenfoma geliştirmek izin ~ 17 gün.
- Sistemik lenfoma varlığı 30 mg/mL biyoluminesans ve bir vivo bioluminescence görüntüleme sistemi kullanarak görüntüleme 100 μL mayi (IP) enjeksiyonu ile onaylayın.
- Sinyal yayılma bitişik fareler önlemek için ayırıcı kullanın. Fare ile bir sabit boyutlu bölge ventral tarafta 1dk ilgi için maruz.
- Fotonlar / saniye (p/s) olarak göreli ışık birimleri (RLU) görüntüleyin. Ayarları her tümör modeli için optimize edilmiş olması gerekir; tümör erken tespiti seçebilirsiniz, ancak tümör bitiş noktaları ulaştığı ile doygunluğu yol değil Riziko kullanın.
- Her fare ile bir sabit için kayıt toplam RLU bölge ilgi ölçekli. (Şekil 5a ve b).
- 1 x 106 araba T hücreleri taşıyan lymphoreplete fareler içine IV enjeksiyon tarafından kurulan tek doz lenfoma enjekte.
Not: (önemli) Düzeyleri dozaj her için araba inşa araba T hücrelerden kaynaklanan herhangi bir olası toksisitesine ile karakterizedir ve ele alınabileceği emin olmak için bir doz yükseltme zamanlama kullanarak oluşturulmuş olmalıdır. Anti-fare CD19 araba T hücreleri toksisitesine görüntüleme rağmen araba T hücreleri için beklenmeyen toksisitesine çıkmasına neden olabilir. Birden çok araba yapıları ve iletim verimliliği aynı değildir nerede, T hücre yönetilen toplam sayısı hücre hazırlıkları içine Sigara transduced T hücrelerinin eklenmesiyle eşit tutulmalıdır. - Hastalık haftalık 100 μL IP enjeksiyon yoluyla 30 mg/mL biyoluminesans ve ilerlemesini görüntüleme sistemi (Şekil 5 c) bir vivo içinde bioluminescence kullanarak görüntüleme izlemek.
- Yakından fareler toksisite belirtileri için izlemek ve herhangi bir acı ortaya çıkmadan önce hind felç (HLP) veya patolojik tümör yükü erken belirtileri gösteren herhangi bir fare ötenazi.
Not: Toksisite A20 lenfoma üzerinden hind felç tümör işgali meninkslerde aracılığıyla ekleyebilirsiniz. Düzenli olarak değiştirilmiş yürüyüş erken belirtileri kontrol. Aynı şekilde, büyük IP tümörleri olan değiştirilmiş davranışı tarafından gösterilen rahatsızlık neden olabilir ortaya çıkabilir. - Fareler yaşam için 60-100 gün (Şekil 5 d) izlemek. Ötenazi programı-1 yöntemi üzerine deneme sonuç yerine getirilir.
- 100 mg/kg intravenöz (IV) teslimini siklofosfamid 6-8 haftalık BALB/c fareler içine gerçekleştirin. Bu tümör engraftment önemli lymphodepletion17 (Şekil 4) olmadan sağlar.
-
Protokolü 2
- 200 mg/kg siklofosfamid 6-8 - hafta eski BALB/c fare kuyruğu ven enjeksiyon içinde 100 μL PBS fare başına tarafından teslim.
- Ertesi gün, 5 x 105 syngeneic A20 B hücreli lenfoma hücre luciferase ve GFP 100 μL PBS üzerinden kuyruk ven yerleştirmeye ifade enjekte et.
- Fareler için sistemik lenfomalarin bazilarinin geliştirmek izin ~ 7-14 gün
- Sistemik lenfoma 30 mg/mL biyoluminesans ve bir vivo bioluminescence görüntüleme sistemi kullanarak görüntüleme 100 μL IP enjeksiyonu ile onaylayın.
- 5 Gy tüm vücuda radyasyon vermeliyiz (TBY) 0,02 Gy/dk lymphodepletion için gerçekleştirin.
Not: Araba T-hücre tedavisi gören hastalar rejimleri artıran önemli ölçüde engraftment, adoptively araba T hücrelerinin yönetim araba T hücreleri transfer önce lymphodepletion elde etmek için bir dizi tabi. Bu farelerde tüm vücuda radyasyon vermeliyiz (TBY) (Şekil 6) ile çoğaltılabilir. - Ertesi gün, 100 μL tümörlerin PBS üzerinden kuyruk ven taşıyan fareler içine enjeksiyon kurulan 1 x 106 araba T hücreleri enjekte.
- Kan örnekleri ile kuyruk ven kanamaları 7 gün sonra toplamak.
- Kırmızı hücre lizis arabellek her kan örneği ekleyin, sonra akış sitometresi için madde 3 te açıklandığı şekilde hazırlayın. Araba T hücre sebat dolaşımda akış sitometresi (Şekil 2) tarafından analiz.
Not: Sitometresi hemen önce sayım boncuk eklenmesi kan mililitre başına araba T hücre sayısı tayini sağlar. - Hastalığın ilerlemesini adımlarda 5.1.5 - 5.1.8 (Şekil 7) açıklandığı gibi izlemek.
Sonuçlar
İçin yüksek verimlilik iletim T hücrelerinin taze retroviral parçacıklar elde etmek gereklidir. PCL-Eco yapımcı plazmid ve pMP71 retrovirüsü plazmid Plat-E hücre satırıyla transfection retroviral parçacıklar salgı süpernatant hücresine artış sağlar. MCherry gibi bir floresan marker gen retrovirüsü kodlandığında, başarılı transfection floresans mikroskobu (Şekil 1) tarafından onaylanabilir. Virüs içeren süpernatant transfected Plat-E hücrelerden T hücreleri ile 2 spin-fection fibronektin parçası kaplı tabaklarda yuvarlar transduce için kullanılır. İletim verimliliği iletim yolu ile akış sitometresi 4 gün sonrası belirlenebilir. Başarılı bir şekilde transduced hücreleri retrovirüsü (Şekil 2) kodlanmış marker gen ifade. İletim verimliliği aralığı ~ % 50-90 verimlilik ilk nesil reseptörleri ile ~ 10-%40 araba ile yakın retroviral paketleme kapasitesi oluşturur. Marker gen ekspresyonu başarılı retroviral iletim gösterirken, hücrelerle o hızlı hedef antijen onların yüzey üzerinde ilgi çekici üzerine araba T hücrelerinin işlevselliği göstermek için her şeyden önemlidir. Hedef hücre hatları için hızlı luciferase modifiye luciferase deneyleri içinde hücre-kill araba T hücreleri doğrudan (Şekil 3A) tarafından derecesini test etmek için kullanılabilir. Ortak kültür üzerine araba T hücreleri tarafından ELISA, belirlenen hedef hücrelerle efektör sitokinler sürümünden de araba T hücre sitotoksisite (Şekil 3B ve 3 C) dolaylı bir ölçüt olarak kullanılabilir.
Bu protokol için üretilen araba T hücreleri lymphoreplete farelerde siklofosfamid (intravenöz enjekte), 5 x 105 A20 hücre (Şekil 4) IV enjeksiyonu öncesinde 1 gün 100 mg/kg doz sistemik A20 lenfoma kurarak değerlendirilebilir. IP enjeksiyon vivo içinde bioluminescence Imager kullanarak biyoluminesans ve görüntü yakalama ile tümör yükü (Şekil 5A-C) boyunca sabit bir yatırım getirisi ve pozlama zaman kullanarak izlemek için kullanılabilir. Hızlı IL-12 modifiye araba T hücreleri hastalıksız sağkalım fareler (Şekil 5 d) yaklaşık % 25 veren önceden Merkezi Klima lymphodepleting ile sistemik lenfoma ortadan kaldırılması yeteneğine sahiptirler. Lymphodepleting, Önkoşullanma 5 tarafından elde Gy TBY 1 gün önceden IV yönetim araba T hücrelerinin önemli ölçüde artırır engraftment (Şekil 6). Bu modelde, ilk nesil araba T hücreleri genellikle hastalıksız sağkalım % 100 fare (Şekil 7) inducing sistemik A20 lenfoma ortadan kaldırılması yeteneğine sahiptirler.
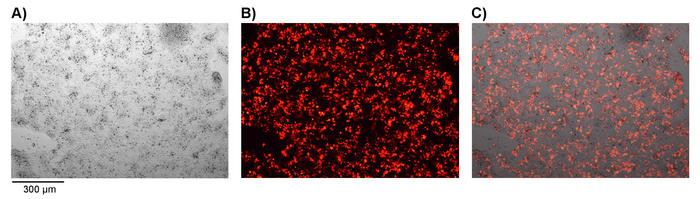
Şekil 1. Plat E hücre başarılı transfection onayı. Plat-E hücreleri retroviral araba inşa etmek ve pMP71 ve pcl-Eco ambalaj vektör plazmid DNA ile transfected. Başarılı transfection mCherry floresan marker gen ifade tarafından gösterilir. A) parlak alan mikroskobu, B) floresan mikroskopi ve C) birleştirilmiş resimler gösterilir. Büyütme = 50 X. Bu rakam daha büyük bir versiyonunu görüntülemek için buraya tıklayınız.

Şekil 2. İletim verimliliği akış sitometresi tarafından belirlenmesi. Akış Sitometresi gün 4 mesaj iletim, zombi UV canlı/ölü, mCherry, BV711 kullanarak fare T hücreleri iletim verimliliğini belirlemek için kullanılır ve BV785 canlı tespiti için aracı, CD4 ve CD8 hücreleri, sırasıyla oluşturur. Temsilcisi sonuçlarını A) Non-transduced, B) mCherry.αmCD19.mCD3z ve C) mCherry.αmCD19.mCD3z.mIL12 1 / geçişi ile gösterilir) tekli 2) canlı hücreleri 3) CD4 ve CD8 4) ve 5) mCherry pozitif hücrelerinin araba ifade değerlendirilmesi. Bu rakam daha büyük bir versiyonunu görüntülemek için buraya tıklayınız.
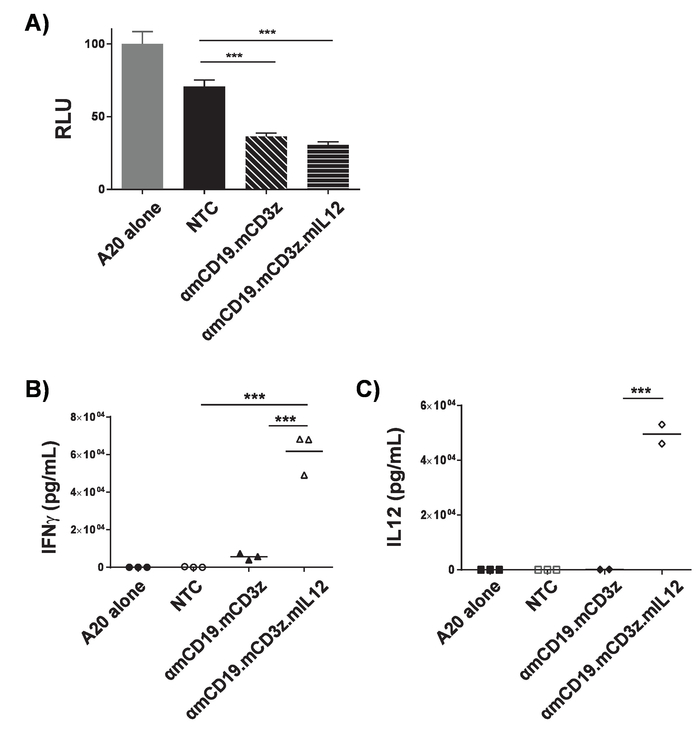
Şekil 3. Doğrulama araba T-hücre faaliyetinin. ΑmCD19 araba T hücreleri ortak kültürlü A20 lenfoma hücrelerini hızlı luciferase için modifiye (1 x 104: 1 x 104) bir U-alt 96-şey plaka 16 h için. Ortak kültür sonra hücreleri pelleted, ve süpernatant denizden çıkarıldı. A) hücreleri PBS içinde yeniden askıya alınmış ve luminometry hedef hücre canlılığı değerlendirmek için kullanıldı. Ortak kültür süpernatant IL-12 (C) ve IFNγ (B) varlığı için değerlendirildi. Ortak kültür süresinin uzunluğu ve araba T hücre hedef hücrelere oranı gerekir, optimize edilebilir her araç için inşa ve hedef hücre satırı. PMA ve ionomycin tedavi olumlu bir denetim olarak yanıt vermek için onların yetenek hücreleri ve T hücreleri kalitesini doğrulamak için kullanılabilir. Hata çubukları SD istatistiksel analiz tek yönlü ANOVA kullanarak gerçekleştirilen gösterir. p < 0.001). Bu rakam17değiştirildi. Bu rakam daha büyük bir versiyonunu görüntülemek için buraya tıklayınız.
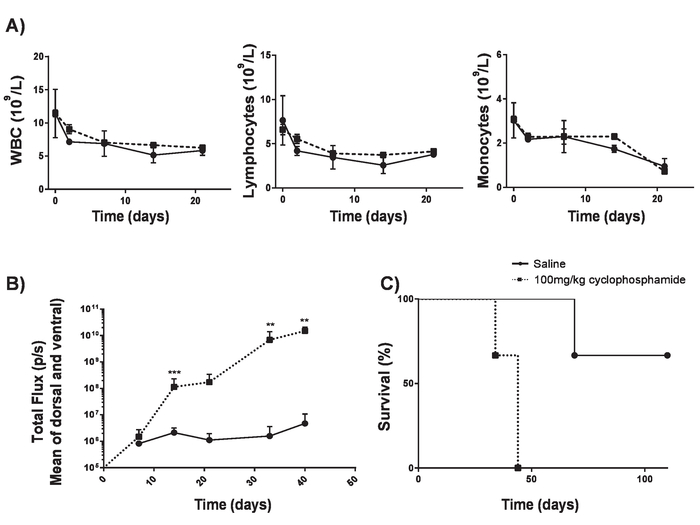
Şekil 4. A20 lenfoma lymphodepletion olmadan kuran. Siklofosfamid lymphodepletion neden olmadan lenfoma indüksiyon verimliliğini artırabilirsiniz. A) 6-8-hafta-yaşlı BALB/c fare siklofosfamid 100 mg/kg IV teslim sonra kan sayımı. Hata çubuklarını göster SD B) 6-8-hafta-yaşlı BALB/c fare sonra 100 mg/kg siklofosfamid veya serum gün -1 IV teslimi ve IV teslim gün bir luminometer kullanarak ölçülen 0 5 x 105 A20 hücre Lenfomasi yükünü. C) farelerde yaşama B). Hata çubukları SD istatistiksel analiz 2 yönlü ANOVA kullanarak gerçekleştirilen gösterir. ** p < 0,01, *** p < 0.001). Bu rakam Kueberuwa ve ark. değiştirildi 17. Bu rakam daha büyük bir versiyonunu görüntülemek için buraya tıklayınız.
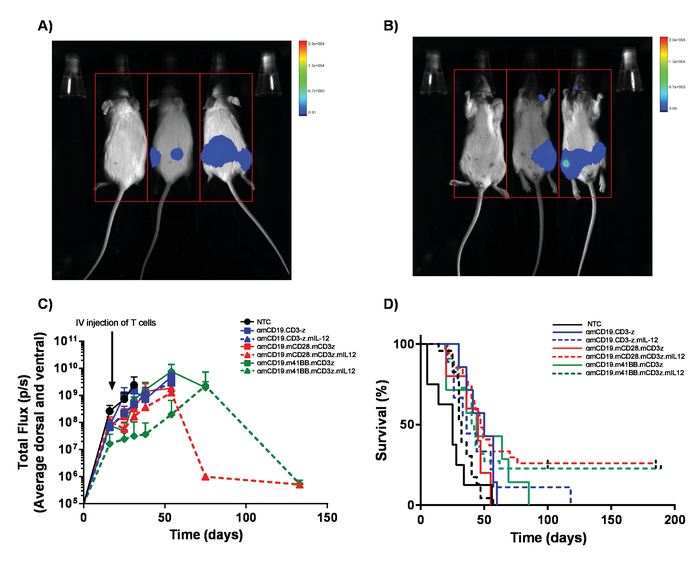
Şekil 5. Lenfoma yük ve hayatta kalma izleme. Luciferase ifade A20 lenfoma taşıyan fareler 100 µL mayi (IP) enjeksiyonu 30 mg/mL biyoluminesans almak ve görüntüleme sistemi bir vivo içinde bioluminescence kullanarak görüntüsü. A) fareler ventral tarafta 1 dk. için maruz kalan ve hemen görüntüye tümör kitleleri organları (B)her iki tarafında almak için dorsal devrildiğinde. C) değişen αmCD19 araba T hücreleri lymphodepletion olmadan alma BALB/c fare lenfoma yükünün temsilcisi sonuçları. Hata çubuklarını göster SEM D) aynı farelerin sağkalım oranı. Bu rakam Kueberuwa ve ark. değiştirildi 17. Bu rakam daha büyük bir versiyonunu görüntülemek için buraya tıklayınız.
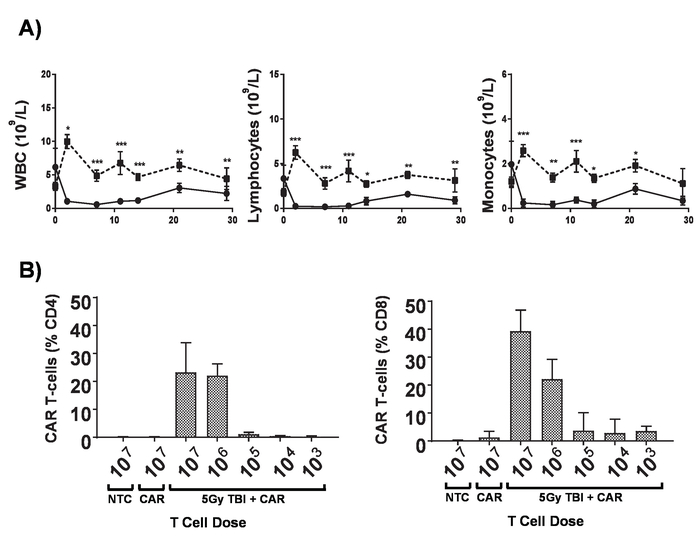
Şekil 6. Lymphodepletion etkileri. A) 5 Gy TBY 0,02 Gy/dak; doz oranında aldıktan sonra 6-8-hafta-yaşlı BALB/c farelerin kan sayımı hata çubukları iki yönlü ANOVA göre SD istatistiksel analiz gösterir. p < 0,05, ** p < 0,01, *** p < 0,001. B) izleme, CD4+ ve CD8+ araba T mCherry marker gen 7 gün sonrası yönetim için akış sitometresi tarafından fareler periferik kan hücreleri. SD hata çubuklarını göster Bu rakam Kueberuwa ve ark. değiştirildi 17. Bu rakam daha büyük bir versiyonunu görüntülemek için buraya tıklayınız.
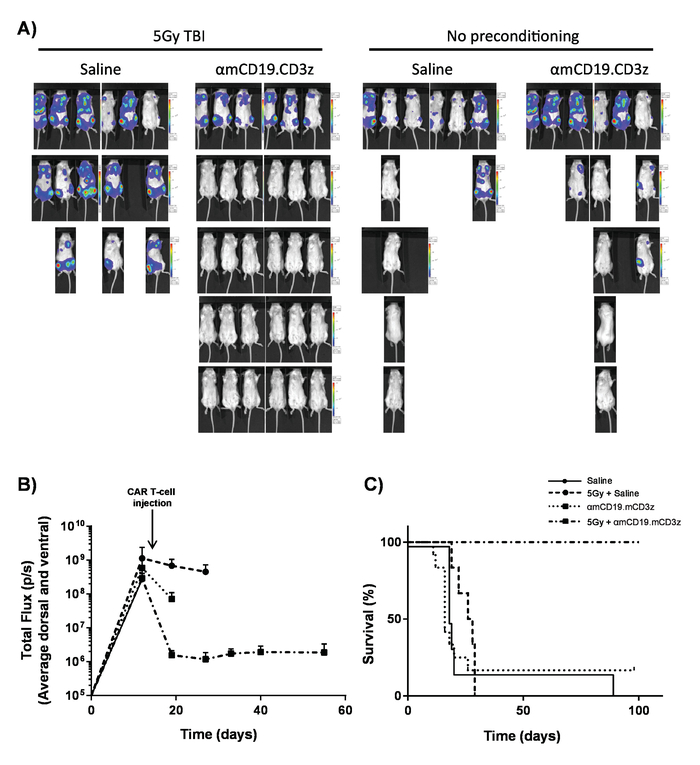
Şekil 7. Araba T hücre lymphodepleting öncesi Klima aktivitesiyle. Gün önce araba T hücreli yönetim 5 Gy TBY etkisini gösteren tipik sonuçları. A) 100 µL mayi (IP) enjeksiyonu görüntüleme sistemi bir vivo içinde bioluminescence kullanarak 30 mg/mL biyoluminesans sonra farelerin görüntüleme görüntüleme ve (B) grafik görüntüler. Hata çubuklarını göster SEM C) aynı farelerin yaşam. Bu rakam değiştirilmiş fromKueberuwa vd oldu 17. Bu rakam daha büyük bir versiyonunu görüntülemek için buraya tıklayınız.
Tartışmalar
Syngeneic fare modelleri hastalık ilerleme ve terapi test sağlam bir bağışıklık sistemi koruyarak sağlar. Bağışıklık sistemi ve özellikle immunotherapeutic maddeleri için etkileşim tedaviler gelince bu her şeyden önemlidir.
Burada açıklanan protokol iki kritik iş akışı var., ilkini genetik olarak fare T hücre arabalar hızlı değiştirme. Bu başlangıç itibaren 7 gün iletim doğrulama gerektirir. Farelerde sistemik lenfoma araba T hücrelerinin üretimi ile eşlik eden bir tesistir. Araba T hücre üretim başarısız veya kalite varlık genellikle fareler önce yedek hücreleri üretmek için yeterince zaman kalmadı yetersiz Lenfoma için ölmek gerekir. Bu nedenle araştırmacılar bu modeller doğru bir şekilde kullanarak başarılı bir şekilde tedavi yönetimi için araba T hücrelerinin üretimini zaman için tümör dozaj ve hastalık ilerleme çalışmaları gerçekleştirmek çok önemlidir.
Düşük T-hücre iletim verimliliği için tipik nedenleri yapımcı hücreleri, genellikle yoksul plazmid saflık ya da yanlış transfection ortam pH tayini neden zavallı transfection verimliliğini içerir. Bu zavallı transfection T hücre iletim verimliliği sınırlar gibi tam protokolü ile devam etmeden önce yapımcı hücre transfection verimliliğini kontrol etmek için tavsiye edilir. Rekombinant insan fibronektin parçaları toplanabilir ve -20 ° c yeniden kullanmak, ancak, birden çok donma-thaws sonucunda düşük iletim verimliliği depolanan. Koleksiyonu da yüksek almak için önemlidir sonra fare dalağı hızlı işleme uygun T hücrelerinin verir.
Burada açıklanan protokol A20 hücre luciferase ifade kullanır belirtmek gerekir. Sistemik tümör yükünü bioluminescence görüntüleme tarafından ölçmek için yeteneği sağlar bu tercih edilir. Ancak, işlevsel bir bağışıklık sistemi huzurunda luciferase yanıt sonuçları çarpık. Fare işaretçisi transgenes17hayatta kalma bağışıklık tepkileri daha önce test ettik. Bunu doğrulamak için A20 hücre transgenes ücretsiz kullanarak anahtar deneyler çoğaltmak için o bunlar bağışıklık hücreleri tarafından tümör imha içinde önemli bir rol oynamak yok anahtarıdır.
Klinik ajanlar-ebilmek biricik var olmak kullanılmış içinde vivo bağışıklık eksikliği farelerde iken fare araba T hücreleri fare kanser hücrelerine karşı kullanımı tedavi edici etkinliği veya hastalık ilerlemesi için bağışıklık sisteminin katkıları değerlendirmek için bize izin verir. Bu iletişim kuralı B hücreli lenfoma veya diğer arabalar salgı IL-12 burada açıklandığı gibi ek değişiklikler ile hedefleme arabalar önceden klinik değerlendirilmesi için yararlanılabilir. Bu bağışıklık hücreleri arasındaki etkileşimi syngeneic fare modellerinde değerlendirilebilir olmasına rağmen onlar doğru insanlar içinde vivoetkileşiminde özetlemek değil olduğunu belirtmek gerekir. Özellikle dikkat, insan ve fare araba hangi aşağı akım sonuçlara yol açabilir yapısında değişiklik gösterir; T hücrelerinin büyüme için uygun harekete geçirmek ve hücre kültür koşulları farklı20, doku dağıtım hedef antijen ifade insanlar ve fareler arasında değişiklik gösterebilir ve deneyimli toksisitesine kökten farklı olabilir. Bu nedenle ex vivo ve sonuçları teyit için xenogeneic modelleri kullanmak esastır.
Özet olarak, syngeneic lymphodepleted ve lymphoreplete modeli lenfoma hastaları ve önceki kemoterapi/radyoterapi olmadan özetlemek. Bu hangi ile yeni bağışıklık terapisi ajanların dalga önümüzdeki önemli olacaktır tedavi stratejileri bir dizi test izin vermek için klinik ayarları taklit etmek bir model sistemi sağlar.
Ön Klima kullanımı ile tüm fareler genellikle lenf kanserini temizleyin belirtilecektir. Kadar % 90 tam yanıt oranları, insanlarda bu temsilcisi etmektir. Ancak, sorunlar CD19 araba T-hücre tedavisi için çabaladıkça gözlenen yüksek frekans önlenmesi üzerinde menteşe çoğu zaman CD19 vardır. Çabaladıkça bu modelde en fazla ve genellikle 100 günden fazla gözlenmiştir değil. Değişiklik klinikte görülen çabaladıkça taklit CD19 araba T-hücre tedavisi gelecekteki sorunları ile yardımcı olabilir.
Açıklamalar
David Gilham araba T hücrelerinin üretiminde yer Celyad için çalışır. Yazarlar kalan ifşa etmek hiçbir şey yok.
Teşekkürler
Bu araştırma (grant 13031) ve bu eser desteklemek için CRUK Manchester biyolojik kaynak birimi, görüntüleme ve Sitometresi ve moleküler biyoloji core imkanları finansman için Bloodwise teşekkür etmek istiyorum.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 0.2 µm syringe filter | Appleton Woods | FC121 | |
| 0.45 µm syringe filter | Appleton Woods | FC122 | |
| 1.5ml pestle and microtube | VWR | 431-0098 | |
| 100X penicillin-streptomycin-glutamine (PSG) | Gibco | 10378016 | |
| 2-Mercaptoethanol (50 mM) | Gibco | 31350-010 | |
| Blasticidine S hydrochloride | Sigma- Aldrich | 15205 | |
| Bottle Top Filter (0.2 µm) | Scientific Laboratory Supplies | FIL8192 | |
| Brilliant Violet 711 anti-mouse CD8a Antibody | BioLegend | 100759 | 1 in 100 staining dilution. Clone 53-6.7 |
| Brilliant Violet 785 anti-mouse CD4 Antibody | BioLegend | 100552 | 1 in 100 staining dilution. Clone RM4-5 |
| Calcium chloride dihydrate | Sigma- Aldrich | C7902 | |
| Cell counting beads – CountBright absolute counting beads | Molecular Probes | C36950 | |
| Cell Strainer 100μm | VWR | 734-0004 | |
| Cyclophosphamide Monohydrate | Merck | 239785-1GM | |
| Dulbecco’s Modified Eagle medium (DMEM) - High Glucose | Sigma Aldrich | D6546 | |
| Dynabeads | Gibco | 11131D | |
| Ficoll Paque Plus | GE Healthcare | GE17-1440-03 | Sold by Sigma- Aldrich |
| Flow cytometer - LSR Fortessa x20 | BD Biosciences | 658222R1 | |
| Foetal Bovine Serum | Gibco | 10270 | |
| Haemacytometer | Appleton Woods | HC001 | |
| HEPES solution | Sigma- Aldrich | H0887 | |
| IL-12 p70 Mouse Uncoated ELISA Kit | Invitrogen | 88-7121-76 | |
| IL2, Proleukin | Novartis | PL 00101/0936 | |
| in vivo bioluminescence imaging system – in vivo xtreme II imaging system | Bruker | T149094 | |
| Ionomycin Calcium Salt | Sigma- Aldrich | I0634 | |
| Live/dead stain - Zombie Violet Fixable Viability Kit | BioLegend | 423114 | 1 in 100 staining dilution |
| Luminometer - Lumistart Omega | BMG Labtech | 415-301 | |
| Murine IFN-γ ELISA kit | Diaclone | 861.050.010 | |
| Paraformaldehyde | Sigma- Aldrich | 16005 | |
| pCL-Eco | Novus Biologicals | NBP229540 | |
| Phorbol 12-myristate 13-acetate (PMA) | Sigma- Aldrich | P8139 | |
| Platinum E cell line | Cell Biolabs | RV-101 | (RRID:CVCL_B488) |
| Purified NA/LE Hamster Anti-Mouse CD28 | BD Biosciences | 553294 | Clone 37.51 |
| Purified NA/LE Hamster Anti-Mouse CD3ε | BD Biosciences | 553057 | Clone 145-2C11 |
| Purified Rat Anti-Mouse CD16/CD32 (Mouse BD Fc Block) | BD Biosciences | 553142 | 1 in 100 staining dilution. Clone 2.4G2 |
| Puromycin Dihydrochloride | Sigma- Aldrich | P8833 | |
| Recombinant human fibronectin fragment - RetroNectin Reagent | TaKaRa | T100B | |
| Recombinant Mouse IL-7 (carrier-free) | BioLegend | 577806 | |
| Red cell lysis buffer | eBioscience | 004-4333-57 | |
| RPMI 1640 Medium | Lonza | BE12-167F | |
| Trypsin - EDTA solution | Sigma- Aldrich | T3924 | |
| XenoLight D-Luciferin | Perkin Elmer | 122799 |
Referanslar
- . Food and Drugs Administration Biologics Licence Application Approval letter Available from: https://www.fda.gov/downloads/BiologicsBloodVaccines/CellularGeneTherapyProducts/ApprovedProducts/UCM574106.pdf (2017)
- . Food and Drugs Administration Biologics Licence Application Approval letter Available from: https://www.fda.gov/downloads/biologicsbloodvaccines/cellulargenetherapyproducts/approvedproducts/ucm581259.pdf (2017)
- Liu, Y., Zeng, G. Cancer and Innate Immune System Interactions: Translational Potentials for Cancer Immunotherapy. Journal of Immunotherapy. 35 (4), 299-308 (2012).
- Janssen, L. M. E., Ramsay, E. E., Logsdon, C. D., Overwijk, W. W. The immune system in cancer metastasis: friend or foe. Journal for ImmunoTherapy of Cancer. 5 (1), 79 (2017).
- Pandya, P. H., Murray, M. E., Pollok, K. E., Renbarger, J. L. The Immune System in Cancer Pathogenesis: Potential Therapeutic Approaches. Journal of Immunology Research. 2016, 13 (2016).
- Vinay, D. S., et al. Immune evasion in cancer: Mechanistic basis and therapeutic strategies. Seminars in Cancer Biology. 35, S185-S198 (2015).
- Gajewski, T. F., Meng, Y., Harlin, H. Immune Suppression in the Tumor Microenvironment. Journal of Immunotherapy. 29 (3), 233-240 (2006).
- Munn, D. H., Bronte, V. Immune suppressive mechanisms in the tumor microenvironment. Current opinion in immunology. 39, 1-6 (2016).
- Vanderlugt, C. L., Miller, S. D. Epitope spreading in immune-mediated diseases: implications for immunotherapy. Nature Reviews Immunology. 2, 85 (2002).
- Hardwick, N., Chain, B. Epitope spreading contributes to effective immunotherapy in metastatic melanoma patients. Immunotherapy. 3 (6), 731-733 (2011).
- Makkouk, A., Weiner, G. Cancer Immunotherapy and Breaking Immune Tolerance-New Approaches to an Old Challenge. Cancer research. 75 (1), 5-10 (2015).
- Jackson, S. R., Yuan, J., Teague, R. M. Targeting CD8(+) T-cell tolerance for cancer immunotherapy. Immunotherapy. 6 (7), 833-852 (2014).
- Brentjens, R. J., et al. Lymphodepletion and tumor burden govern clinical responses in patients with B-cell malignancies treated with autologous, CD19-targeted T cells. Journal of Clinical Oncology. 29 (15_suppl), 2534 (2011).
- Brentjens, R. J., et al. Safety and persistence of adoptively transferred autologous CD19-targeted T cells in patients with relapsed or chemotherapy refractory B-cell leukemias. Blood. 118 (18), 4817 (2011).
- Hay, K. A., et al. Kinetics and Biomarkers of Severe Cytokine Release Syndrome after CD19 Chimeric Antigen Receptor-modified T Cell Therapy. Blood. 130, 2295-2306 (2017).
- Zhang, T., et al. Efficiency of CD19 chimeric antigen receptor-modified T cells for treatment of B cell malignancies in phase I clinical trials: a meta-analysis. Oncotarget. 6 (32), 33961-33971 (2015).
- Kueberuwa, G., Kalaitsidou, M., Cheadle, E., Hawkins, R. E., Gilham, D. E. CD19 CAR T Cells Expressing IL-12 Eradicate Lymphoma in Fully Lymphoreplete Mice through Induction of Host Immunity. Molecular Therapy - Oncolytics. 8, 41-51 (2018).
- Engels, B., et al. Retroviral vectors for high-level transgene expression in T lymphocytes. Human Gene Therapy. 14 (12), 1155-1168 (2003).
- Parkinson, C. M., et al. Diagnostic Necropsy and Selected Tissue and Sample Collection in Rats and Mice. Journal of Visualized Experiments: JoVE. (54), e2966 (2011).
- Kueberuwa, G., et al. CCR7(+) selected gene-modified T cells maintain a central memory phenotype and display enhanced persistence in peripheral blood in vivo. Journal for Immunotherapy of Cancer. 5, 14 (2017).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır