Method Article
Büyük Ölçekli Nükleer Etkileşimom Profilleme için Etiketsiz İmmünoprekütle Spektrometresi İş Akışı
Bu Makalede
Özet
Açıklanan ilgi ve etiket-free kütle spektrometresi belirli bir protein in immünafinite zenginleştirme kullanarak bir nükleer hücre altı fraksiyonu protein etkileşim ortakları tanımlamak için bir proteomik iş akışıdır. İş akışı hücre altı fraksiyonu, immünoprepitasyon, filtre destekli numune hazırlama, çevrimdışı temizleme, kütle spektrometresi ve aşağı akım biyoinformatik boru hattını içerir.
Özet
İmmünafinitasyon kütle spektrometresi (IP-MS) protein-protein etkileşimlerini tanımlamak için sağlam bir kantitatif yöntem olarak ortaya çıkmıştır. Bu yayın, diğer hücre altı bölmelere de uygulanabilen çekirdekten düşük miktarda protein-protein etkileşimlerini belirlemek için tasarlanmış tam bir etkileşim proteomik iş akışı sunmaktadır. Bu iş akışı hücre altı fraksiyonları, immünopreksiyon, numune hazırlama, çevrimdışı temizleme, tek çekim etiketsiz kütle spektrometresi ve downstream hesaplamalı analiz ve veri görselleştirmeiçerir. Protokolümüz, endojen proteinlerin immünopresiyonu ile tüm hücre lisatlarından (örn. transkripsiyon faktörü etkileşimleri) saptanması zor olan kompartıraklaştırılmış, düşük bolluk etkileşimlerini tespit etmek için optimize edilmiştir. fraksiyona alilmiş hücre altı bölmeleri. Burada özetlenen örnek hazırlama boru hattı HeLa hücre nükleer ekstresi hazırlanması için ayrıntılı talimatlar sağlar, endojen yem proteinimmünaffinity arıtma, ve kantitatif kütle spektrometresi analizi. Ayrıca kütle spektrometresi tabanlı etkileşim profilleme deneylerinde büyük ölçekli immünoprepitasyon yapmak için metodolojik hususları tartışıyorve gerçek pozitif proteini ayırt etmek için veri kalitesinin değerlendirilmesi için kılavuzlar sağlıyoruz. nonspesifik etkileşimlerden etkileşimler. Bu yaklaşım burada CMGC kinaz, DYRK1A, çekirdek içinde kötü tanımlanmış etkileşimleri ile düşük bir bolluk protein kiaz ın nükleer etkileşimaraştırerek gösterilmiştir.
Giriş
İnsan proteomu, kararlı çok alt birim kompleksleri ve geçici protein-protein etkileşimleri ile geniş yapısal ve biyokimyasal çeşitlilik sergiler. Buna göre, bir ilgi proteini için etkileşim ortaklarının belirlenmesi, moleküler mekanizmayı çözmek için yapılan araştırmalarda yaygın olarak gereklidir. Yakınlık arınma protokollerinde son gelişmeler ve yüksek çözünürlüklü hızlı tarama kütle spektrometresi enstrümantasyonunun ortaya çıkması, tek bir tarafsız deneyde protein etkileşimi manzaralarının kolay haritalanmasına olanak sağlamıştır.
Protein etkileşim protokolleri genellikle ilgi bir protein tanıma yüksek kaliteli antikorlar gerek kalmadan protein etkileşimlerini belirlemek için yakınlık etiketli füzyon yapıları ile ektopik ifade sistemleri istihdam1,2. Ancak, epitop etiket tabanlı yöntemlerin çeşitli dezavantajları vardır. Epitop ile fiziksel etkileşimler nonspesifik kopurifying proteinlerin tespitine yol açabilir3. Ayrıca, bir proteinin N- veya C-terminaline bu epitop etiketlerin füzyonu yerli protein-protein etkileşimlerini engelleyebilir veya fizyolojik olmayan konformasyonları teşvik etmek için protein katını bozabilir4. Ayrıca, ektopik ekspresyon sistemleri genellikle suprafizyolojik konsantrasyonlarda yem proteini aşırı ekspres, hangi artifactual protein etkileşimlerinin belirlenmesi ile neden olabilir, özellikle dozaj duyarlı genler için5. Bu sorunları aşmak için, endojen yem proteini ilişkili etkileşimli av proteinleri ile birlikte immünopprepititated olabilir, yerli protein tanıyan yüksek kaliteli bir antikor durumu varsayarak.
Burada bir örnek olarak CMGC protein kiaz DYRK1A kullanarak endojen bir proteinin nükleer etkileşimi tespit etmek için bir etkileşim proteomik iş akışı sağlanmaktadır. DYRK1A kopya numarası, aktivite düzeyi veya ifade bozulması insanlarda ciddi zihinsel özürlülük neden olabilir, ve farelerde embriyoniköldürücülük 6,7,8,9. DYRK1A, farklı hücre altı bölmelerine özgü düşük bolluk etkileşim ilerleçlerini tespit edebilen yaklaşımlar gerektiren dinamik spatiotemporal regülasyon10ve bölümlü protein etkileşimleri11,12,sergiler.
Bu protokol, insan HeLa hücrelerinin sitosol ve nükleoplazm fraksiyonlarına hücresel fraksiyonunu, immünopresidasyon, kütle spektrometresi için numune hazırlama ve veri kalitesini niçin değerlendirmek ve sonuçları görselleştirmek için biyoinformatik bir boru hattının genel görünümünü, analiz ve görselleştirme için sağlanan R komut dosyaları ile kullanır (Şekil 1). Bu iş akışında kullanılan Proteomics yazılım paketlerinin tümü ücretsiz olarak indirilebilir veya bir web arabirimi üzerinden erişilebilir. Yazılım ve hesaplama yöntemleri hakkında daha fazla bilgi için, ayrıntılı öğreticiler ve talimatlar sağlanan bağlantılarda mevcuttur.
Protokol
NOT: Tüm tampon kompozisyonları ve proteaz karışımları Tablo 1'deözetlenmiştir.
1. Hücrelerin hazırlanması
NOT: Bu immünopreplit kütle spektrometresi (IP-MS) yaklaşımı için çoğaltma başına 1−10 mg nükleer lysate başlangıç malzemesi istenir. Hücre miktarları trilikat artı trilikat kontrolleri nükleer immünopresians 1 mg verilecektir.
- Bir yapışık hücre hattı kullanıyorsanız, hasat tan önce çoğaltma başına 3 x 15 cm tabaklarda hücreleri %90'lık bir araya kadar büyütün.
NOT: Yem ve kontrol koşulları için en az üç çoğaltma immünopresipits yapmak için tavsiye edilir. Bu protokol, bölüm 4'ten başlayarak boncuklarla bol miktarda spesifik olmayan etkileşimleri kontrol eden 'yalnızca boncuk' denetimlerinin kullanımını varsayacaktır. Diğer denetim türleri yararlı olabilir. Bunlar tartışma bölümünde derinlemesine açıklanmıştır.- 15 cm plaka başına %0,25 tripsin 3 mL kullanarak fosfat tamponlu salin (PBS) ve trypsin hücreleri ile yıkama plakaları 2 kat. Hücreleri 5 dk için 1.200 x g'de aşağı doğru çevirin ve tripsini dekant.
- Süspansiyon hücreleri için, toplam protein 70−80 mg elde etmek için benzer bir ölçek / yoğunluk büyümek.
- Pelet hücreleri 1.200 x g ve 4 °C'de 5 dk. Ortama dikkatlice decant.
NOT: Peletler bölüm 2'de özetlenen büyük ölçekli hücre altı fraksiyonu kullanılarak verimli bir şekilde işlenmesini sağlamak için bu adımda birleştirilebilir.
- Pelet hücreleri 1.200 x g ve 4 °C'de 5 dk. Ortama dikkatlice decant.
- Hücre peletini 2x PBS + 5 mM MgCl2 proteaz inhibitörleri (PIs) ve fosfataz inhibitörleri (PhIs) ile birlikte yıkayın (Bkz. Tablo 1).
NOT: Hücre peletleri sıvı nitrojen içinde dondurulup -80 °C'de fraksiyona hazır olana kadar saklanabilir.
2. Nükleer ekstre hazırlanması
NOT: Proteaz ve fosfataz inhibitörleri kullanımdan 30 dakika içinde fraksiyon tamponlarına eklenmelidir.
- Eğer dondurulursa, hücre peletlerini 15 dakika boyunca 1x pelet hacminde soğuk Tampon A + PIs/ PhIs'te eritin. Hücre peletini 4 °C'de bir besleyicinin üzerine yerleştirin ve çözülürken yeniden süspansiyona yardımcı okurun. Aksi takdirde, hücre peletini adım 1.3'ten 1x pelet hacmine geri uzaklaştırın Arabellek A + /PhIs.
- Pelet 2.000 x g ve 4 °C 10 dk. Tampon decant için.
- 5x Buffer A ile paketlenmiş hücre hacmi ile hücreleri askıya ve 20 dakika boyunca buz üzerinde kuluçka.
- Pelet 2.000 x g ve 4 °C 10 dk. Tampon decant ve 2x orijinal paketlenmiş hücre hacmi Tampon A + / PhIs ile resuspend ve A / gevşek pestisit ile ~ 7x bırakın.
- 2000 x g ve 4 °C'de 10 dk için lysate santrifüj.
- Dikkatle supernatant kapalı pipet ve sıvı nitrojen ile flaş dondurma. Lysate'yi -80 °C'de saklayın. Bu adımdaki süpernatant sitosolik hücre altı fraksiyonudur.
NOT: Nükleer pelet bu adımda sıvı nitrojenle flaş dondurularak ve -80 °C'de depolayarak kaydedilebilir. - Tampon B + PIs/ PhIs 0.9x pelet hacmine sahip peleti yeniden askıya alın ve 4 °C'de 5 dakika boyunca bir nutator üzerinde karıştırın.
- Çekirdekleri lyse için, daha sıkı bir havaneli ile 20x damlatın "B".
- 4 °C'de 30 dakika boyunca bir nutator üzerinde nükleer lysate karıştırın böylece homojen.
- 4 °C'de 21.000 x g'de 30 dk boyunca nükleer lysate santrifüj. Pipet supernatant kapalı ve çözünür bir nükleer protein özü olarak kaydedin.
NOT: Ortaya çıkan nükleer peletin nükleaz tedavisi kromatin ilişkili protein fraksiyonunun geri kazanılmasına olanak sağlar. - 4 °C'de 3 saat için Buffer C + PIs'e karşı çözünür nükleer ekstresi diyalize sok.
- 24 mm genişliğinde diyaliz borusu uygun bir uzunlukta 8 kDa moleküler ağırlık kesilmiş ile kesin. Tüpün bir tarafını kenetle ve nükleoplazmayı tüpe yükleyin. Lysate yüklendikten sonra, diğer ucunu kelepçeleyin ve Tampon C + içeren temiz bir cam kap içine batırın.
- 30 dk. Aliquot 3x 20 μL nükleer ekstresin batı leketarafından fraksiyondoğrulama için 4 °C'de 21.000 x g'de diyalize konan nükleer özü/nükleoplazmı santrifüj edin. IP-MS analizi için kullanılan nükleer ekstre, sıvı nitrojen içinde dondurularak -80 °C'de saklanabilir.
3. Hücre altı fraksiyonunun doğrulanması
- Nükleer lysate protein konsantrasyonu belirlemek için bir protein tonu tamamlayın. Bir bicinchoninic asit protein tsay downstream uygulaması için yeterli hassasiyet sağlar.
- Yük 20 μg hem sitosolik ve nükleer fraksiyonları bir SDS-PAGE jel daha önce açıklandığı gibi batı leke analizi için13. Bir örneğin yanlış karakterizasyonunu önlemek için yüklerken şeritleri atlayın.
- Nükleer bir belirteç olarak p84 (THOC1) için batı lekesini ve sitosolik belirteç olarak GAPDH'yi inceleyin. Kesirlerin kapsamını nükleer fraksiyondaki sitosolik belirteç oranına göre belirleyin ve tam tersi.
NOT: Diğer nükleer ve sitosolik belirteçler için antikorlar kullanılabilir.
4. Endojen nükleer yem proteininin immünopresidiresi
NOT: Bu noktadan itibaren düşük tutma tüpleri kullanılması tavsiye edilir. Bu, numune işleme sırasında tüplere nonspesifik bağlanmayı azaltacak ve gereksiz numune kaybını önleyecektir. Ayrıca, LCMS grade H2O'nun kalan adımlar için arabellek hazırlamak için kullanıldığından emin olun.
- Mikrosantrifüj tüplerinde hem protein-A hem de protein-G için 12,5 μL boncuk hacmini birleştirerek her çoğaltma için bir protein A/G boncuk karışımı hazırlayın. Boncuk stoklarını %20 etanol içeren bir bulamaç olarak saklayın. Bulamaç %(v/v) içindeki boncuk konsantrasyonu ve pipet, boncukların uca girebilmesini sağlamak için ucunda kesilmiş bir pipet ucu kullanarak gerekli hacmi belirleyin.
- Protein A/G boncuk karışımını 2x 300 μL IP Tampon 1 ile yıkayın. Boncukları 1 dk ve decant tamponu için 4 °C'de 1.500 x g'da döndürün.
- Antikor-protein A/G boncuklarını hazırlayın: Antikorları boncuklara bağlamak için, istenilen antikordan 300 μL IP Tampon 1 ve 10 μg ekleyin. Boncuk/antikor karışımının bir gecede 4 °C'de bir besleyicinin üzerine sallanmaya izin verin. Sadece boncuk kontrolleri için herhangi bir antikor eklemeyin.
NOT: Çoğaltma başına toplam 10 μg antikor başlangıç noktası olarak kullanılabilir, ancak deneyde kullanılan lysate'nin her bir antikor ve ölçeği için tam miktarın optimize edilmesi gerekir. - Bir su banyosunda 2.10.
- 30 dk için 16.000 x g lysate spin ve yeni bir tüp için supernatant aktarın.
- 1 mg'lık benzonaz (250 birim/μL) ekleyin ve 4 °C'de 10−15 dakika boyunca bir besleyiciye kaya ekleyin.
- Lysate preclearing için boncuk hazırlayın. Adım 4.1'deki gibi 1,5 mL düşük tutma tüplerine her protein A ve protein G boncuklarından 12,5°L ekleyin. IP Yıkama Tampon1 + ile 2x yıkayın ve tampon decant.
- Adım 4.5 gelen boncuklar için nükleer lysate 1 mg ekleyin. 4 °C'de 1 saat boyunca bir nutator üzerinde sallarken kuluçka.
- Santrifüj 1 dk için 1.500 x g ve 4 °C'de önceden temizlenir.
- Nükleer lysates adım 4.5.1 boncuk ile kuluçka iken, IP Tampon 1 + ile antikor-protein A / G boncuk 2x yıkayın. 1 dk için 1.500 x g ve 4 °C'de santrifüj ve tampon decant.
- Önceden temizlenmiş nükleer lysate'yi 4.6.1 adımdan antikor-protein A/G boncuklarına aktarın. Kuluçka sırasında 4 °C'de bir nutator üzerinde 4 saat boyunca 1.500 x g ve 4 °C'de 1 dk.
- Supernatant'ı her çoğaltma için akış olarak etiketlenmiş tüplere aktarın.
- Antikor-protein A/G boncuklarını 1 mL IP Tampon 2 + ile yıkayın. 1 dk için 1.500 x g ve 4 °C'de santrifüj, decant tampon, ve 3x toplam tekrarlayın.
- Boncukları 2x ip Tampon 1+ santrifüjü ile bir önceki adımda olduğu gibi yıkayın. Son yıkamadan sonra tüm arabellek kaldırıldığından emin olun.
- Her biri 30 dakika boyunca 0,1 M glisin (pH 2,75) 20 μL ile 2x. Tüplere elüsyon tamponu ile kuluçka sırasında sallanan olduğundan emin olun. Her 30 dk kuluçkadan sonra supernatant kapalı 1 dakika ve pipet için 750 x g ve 4 °C spin.
NOT: Burada açıklanan düşük pH glisin yöntemi çoğu yem proteinini eutes iken, bazı antikor-antijen etkileşimleri daha sıkı tampon koşulları gerektirir. - Flaş donma sıvı azot içinde eluates ve -80 °C'de saklanır.
5. Örnek hazırlama
NOT: İnsülin immünopreplasyon elüsyonu örnekleri içine çivili düşük bolluk endojen yem proteinleri için önemli olan trikloroasetik asit (TCA) yağış ve örnek işleme sırasında proteinlerin kurtarma yardımcı olur.
- Eğer dondurulursa oda sıcaklığında eluates çözülür.
- Örnekleri buza yerleştirin ve her 100 μL eluat için 10 μL 1.0 mg/mL insülin ekleyin. Girdap ve sonra hemen% 1 sodyum deoksikolat 10 μL ekleyin. Girdap örnek tekrar ve 30 μL ekleyin 20% TCA son bir girdap izledi.
- Örnekleri 20 dk buz üzerinde kuluçkaya yatırın, ardından 21.000 x g'de 4 °C'de 30 dakika boyunca santrifüj edin.
- Supernatant aspire ve -20 °C önceden soğutulmuş olan aseton 0,5 mL ekleyin. Girdap ve sonra 21.000 x g ve 4 ° C 30 dk. Bu adımı tekrarlayın spin.
- Supernatant aspire ve hava tüp altında kalan pelet kuru.
- Örneklem,aşağıda belirtildiğigibi örnek işlemeyi azaltmak için optimize edilmiş değiştirilmiş Filtre Destekli Numune Hazırlama (FASP) yöntemini kullanarak kütle spektrometresi için numuneyi hazırlayın.
- Protein peletini adım 5.1.4'ten 30 μL SDS Alkylation Tamponu ile yeniden askıya alın (Bkz. Tablo 1). Numuneyi 95 °C'lik bir ısı bloğuna 5 dakika kuluçkaya yatırın. Bir sonraki adımdan önce 15 dakika oda sıcaklığında soğumaya bırakın.
- Her numuneye 300 μL UA çözeltisi ve 30 00 mM TCEP ekleyin. Bu çözeltiyi 30k santrifüj filtresine yükleyin. Santrifüj filtreyi oda sıcaklığında 21.000 x g'da 10 dk çevirin.
NOT: Yem proteini ve putatif interaktörler bu noktada filtreye bağlanmalıdır. Ancak, filtreyle ilgili bir sorun olması durumunda akış tutulabilir. - Filtreyi 250 μL UA ve santrifüj ile 21.000 x g'de 10 dk. Akış'ı dekant ve toplam 3x boyunca tekrarlayın.
- Filtreyi 100 μL 100 mM Tris pH 8,5 ve santrifüj 21.000 x g'de 10 dk. akıştan geçirin ve toplam 3x tekrarlayın.
- 0,1 M Tris pH 8,5'te 3 μL 1 μg/μL Lys C yeniden asılı ekleyin. Filtreleri 100 μL işaretine kadar doldurun ve bir nutator üzerinde sallarken 37 °C'de 1 saat sindirimine izin verin.
- 1 μL 1 μg/ μL MS dereceli tripsin ekleyin. Hafifçe karıştırın ve bir nutator üzerinde sallanan ise 37 ° C'de bir gecede numune ile inküp izin tripsin için izin verin.
- Filtreden peptit iyelik 20 dk için 21.000 x g santrifüj.
NOT: Tüm eluate kurtarmak için birden fazla santrifüj tur gerekli olabilir. Bu yapılmazsa, ciddi numune kaybı potansiyeli vardır.
- C18 spin sütunları kullanarak peptidleri tuzdan arındırın. Üretici tarafından sağlanan protokolü izleyin.
- Lyophilized peptid in 7 μL 0.1% TFA% 5 asetonitril resuspend. Peptidlerin askıya alınmasından emin olmak için numuneyi 3 dakika sonicate edin. 10 dakika boyunca 14.000 x g aşağı çevirin.
- Sıvı kromatografi-kütle spektrometresi (LC/MS) sistemine yüklenmesi için resuspended peptidin uygun bir numune şişesine aktarın.
6. LC/MS sistemine uygunluk
NOT: Afinite saflaştırılmış numunelerden alınan proteinin küçük ölçek ve genellikle daha düşük olması nedeniyle, LC/MS platformunun maksimum hassasiyet ve sağlamlıkta faaliyet etmesi çok önemlidir.
- Add 1 mL of LC/MS grade formic acid to 1 L of LC/MS grade water for mobile phase A, and add 1 mL of LC/MS grade formic acid to 1 L of LC/MS grade acetonitrile for mobile phase B.
- ≥250 mm uzunluğunda <2 μm ters fazlı C18 reçine ile paketlenmiş 75 μm erimiş-silika kılcal kolon hazırlayın veya kurun. En iyi sonuçlar sütuna doğrudan numune enjeksiyonu ile elde edilecektir.
- Ultra Performans sıvı kromatografisi (UPLC) sistemini taze mobil aşamalarla temizle. C18 kolon takılı ile, uygun bir yayıcı ile istikrarlı bir akış hızı ve elektrosprey kurmak (yani, 20 μm id x 360 μm od 10 μm ucu çekti). Kolon40−60 °C'de saklayın.
- HeLa tam hücre lisat triptik sindiriminin 100−200ng'si gibi karmaşık bir kalite kontrol standardı enjekte ederek genel LC/MS sistem performansını test edin. Karmaşık bir örnek için uygun bir degrade (yani, 2−3 saat degrade elüsyon süresi) ile elute. Peptit ve protein tanımlamalarının temel sistem performansını belirleyin.
NOT: En iyi sonuçlar için, 20.000−35.000 benzersiz peptidden 3.000−5.000 veya daha fazla protein tanımlaması deneysel numuneler için en iyi performansı sağlayacaktır. - Rutin LC/MS sistemine uygunluk için, Bovine Serum Albumin (BSA) gibi tek bir protein sindirimi standardından 100−200 fmol veya daha az enjekte edin. Kısa bir degrade (yani, 20−30 dk) ile elute.
NOT: Bir protein digest birden fazla enjeksiyon temel LC / MS sistem performansı kurulmasına yardımcı olacak ve her IP-MS örnek deneme boyunca sistem performansının bir ölçüsü sağlar ve etiketsiz deneyler önyargı olabilir enstrüman sürüklenme, tespiti için izin sonra tekrar enjeksiyon. Seçili tek tek tepe yoğunluklarının ve tepe şekillerinin temeli MS, LC ve sütun performansı hakkında bilgi verecektir. - Analitik sütunun aşırı yüklenmesini önlemek için, deneysel bir numunenin küçük bir kısmını (toplamın %15−30'u) kolona yükleyin ve karmaşık numuneler için uygun bir degrade (yani 2−3 saat) kullanarak ayırın. Protein tanımlama larının sayısı yetersizse, numunenin tamamını sütuna yükleyin.
- LC/MS sistem performansını ve numune taşımasını izlemek için numuneler arasında tek bir protein sindirimi standardı uygulayın. Numunelerinize bağlı olarak numune taşımayı azaltmak için birden fazla standart gerekebilir.
7. Veri İşleme
- MaxQuant'ın https://www.maxquant.org/'da bulduğu proteomik yazılım paketini indirin.
NOT: Bu işlem, RAW MS veri dosyasını adım 6.6'dan protein kimliklerinin, gen adlarının ve bunların alt akış analizi için tanımlanmasıyla ilişkili nicel değerlerin veri tablolarına işlemek için kullanılacaktır.- Ham Veri sekmesinin Giriş Veri alt başlığıiçinde Yükle'yi seçin. MS ham dosyalarının depolandığı dosya konumunu açın ve her MS/MS çalışması için ham dosyaları seçin.
- Gruba Özel sekmesine tıklayın ve Sindirim'iseçin. Enzim listesinde LysC'yi seçin ve bu enzimi aramada kullanılacak listeye eklemek için sağ oka tıklayın. Ardından, Instrument'ı seçin ve ekranın üst kısmındaki açılır listede doğru enstrüman türünün göründüğünden emin olun. Diğer gruba özgü arama parametrelerini standart ayarlarda bırakın.
- Genel Parametreler sekmesine tıklayın ve Dizileriseçin. Bu aramada kullanılacak taksonomi için uygun FASTA dosyasını ekleyin. Bu yapılmazsa peptidler düzgün atanmayacak. İnsan proteom için, https://www.uniprot.org/help/human_proteome adresinden UniProt'tan FASTA dosyasını indirin.
- Küresel Parametreler sekmesinde Protein Niceliği'netıklayın. Quantification açılır menü için Peptidler içinde, Benzersiz + Razorseçin.
NOT: MaxQuant, yoğunluk bazlı mutlak niceleme (iBAQ) ve etiketsiz niceleme (LFQ) yoluyla proteinlerin alternatif nicelleştirmesini sunar. Ancak, peptit sayısı bilgileri bu protokol15'tekidownstream analizi için yeterlidir. - MaxQuant arabiriminin sol alt kısmında, arama için kullanılacak işlemci sayısını seçin. Bu, çalışma için gereken süreyi doğrudan etkiler, bu nedenle bunun için mümkün olduğunca çok sayıda seçim yapacağız). Çalıştırmayı başlatmak için ekranın sol alt kısmındabaşlat'ı tıklatın. Aramanın ilerlemesini görüntülemek için ekranın üst kısmındaki Performans sekmesini seçin.
- Çalışma tamamlandığında, perseus, bir proteomics hesaplama platformu veya diğer elektronik tablolama programı veri16görüntülemek için proteingroups.txt dosyasını açın.
- Perseus'u kullanarak ortak kirleticimaddeleri ve darbeleri ters protein dizilerine giderin. http://www.coxdocs.org/doku.php?id=perseus:user:use_cases:interactions detaylı Perseus belgelerini takip edin.
NOT: Analiz yazılımında proteingroups.txt dosyasının açılması (örneğin, Excel) belirli gen ve protein adlarını otomatik olarak bozar.
- Perseus'u kullanarak ortak kirleticimaddeleri ve darbeleri ters protein dizilerine giderin. http://www.coxdocs.org/doku.php?id=perseus:user:use_cases:interactions detaylı Perseus belgelerini takip edin.
- Affinity Purification (CRAPome) için Kirletici Deposu'nu kullanarak deneysel verileri analiz edin. Bu depoda bir hesap http://crapome.org/ kaydedin ve gerektiğinde öğretici izleyin17,18.
- CRAPome ana sayfasında bulunan Verilerinizi Çözümle iş akışını kullanın. Bu etkileşim deneyinde kullanılan yakınlık arınma sistemine karşılık gelen dış denetimleri seçin.
NOT: Bu denetimler, ortak kirleticimaddeleri algılamak için yararlı olan ikinci kat değişim zenginleştirmesini hesaplamak için kullanılabilir. - Perseus veya uygun bir elektronik tablo uygulaması kullanarak MaxQuant'tan proteingroups.txt çıkışından bir giriş dosyası oluşturun. El ile biçimlendirme ayrıntıları http://crapome.org/?q=fileformatting bulunabilir. Alternatif olarak, SAINT/CRAPome giriş dosyasını oluşturmak için sağlanan R komut dosyası "export_CRAPomeSAINT_Input_File.R" kullanın. Ek Kodlama DosyalarındaREADME.txt'ye bakın.
- İmmünoena ndaki her yem proteini için kat değişimi zenginleştirme ve SAINT (INTeractome'nin Önemi Analizi) olasılığını belirlemek için bir analiz yapın. FC-A altındaki açılan menüde 'Kullanıcı Denetimleri'seçildiğinden, FC-B açılır menüsünde 'CRAPome denetimleri' veya 'Tüm Denetimler' seçildiğinden ve SAINT olasılıkları oluşturmak için Olasılık Puanı'nın seçildiğinden emin olun. Çalışma sona erdiğinde, 'Analiz Sonuçları' altında bulunan çıktıyı bir iş kimliğiyle birlikte görüntüleyin. Gelecekteki çizim ve veri görselleştirmesi için veri matrisini 'Analiz Sonuçları'ndan indirin.
- CRAPome ana sayfasında bulunan Verilerinizi Çözümle iş akışını kullanın. Bu etkileşim deneyinde kullanılan yakınlık arınma sistemine karşılık gelen dış denetimleri seçin.
- Ek Kodlama Dosyaları'ndasağlanan R-Scriptleri izleyerek proteinleri FC-A (IP'lere karşı kullanıcı denetimleri) ve SAINT olasılığının bir fonksiyonu olarak çizin.
NOT: FC-A vs. SAINT olasılık ve iBAQ vs. log2 (protein bolluğu) çizimlerinin üretimi için, etiketsiz yoğunlukların ampirik Bayes analizinden ayarlanmış p değer aralığıile renklendirilen bir dizi R komut dosyası sağlanır. Diferansiyel istatistiksel analiz ve çizimin ayrıntıları README.txt ve R komut dosyası "main_differential_analysis. Ek Kodlama DosyalarındaR" bulunmaktadır. - Yem proteininin bilinen etkileşen proteinlerinin FC-A ve SAINT tarafından sıralandığı yeri değerlendirin. Başlangıç noktası olarak triplicate tek yem deneyleri için FC-A > 3.00 ve SAINT > 0.7'yi kesin.
NOT: "Yüksek güven" etkileşimcisi ve "düşük güven" etkileşimcisi için kesit seçimi biyolojik bilgilerle bilgilendirilmelidir.
8. Veri görselleştirme
NOT: Proteomik verileri etkili bir şekilde görselleştirebilen birçok program vardır (örneğin, R, Perseus, Cytoscape, STRING-DB). Yüksek güven isabetleri arasındaki bağlantıyı analiz etmek ve bu etkileşimlerin işlevsel zenginleştirilmesi, daha fazla doğrulama ve işlevsel karakterizasyon için isabetleri önceliklendirmek için yararlı bir strateji olabilir.
- Indirin Cytoscape, https://cytoscape.org/download.html19bir açık kaynak ağ görselleştirme aracı .
- Üç sütunla biçimlendirilmiş bir sekme olarak etkileşim verileri için bir giriş dosyası hazırlayın: yem (kaynak düğümü), av (hedef düğüm), etkileşim türü (kenar türü). Bu Perseus veya seçtiğiniz herhangi bir elektronik tablo programı yapılabilir.
- Dosya simgesinden programın sol üst kısmındaki Tabloyu (simgede aşağı doğru ok ve matris tarafından belirlenmiş) seçin. Cytoscape, etkileşim verilerini özel biçimlendirme ve tasarıma hazır bir ağa otomatik olarak dolduracaktır.
- Cytoscape için denetim panelindeki Stil sekmesini seçin ve tüm ağın özniteliğini ayarlamak için Def sütunundaki karelere tıklayın. Ağdaki belirli düğümleri veya kenarları seçin ve ardından varsayılan ayarları atlamak ve yalnızca seçili nesneleri ayarlamak için stil menüsünün Byp. sütunundaki kareyi seçin. Alternatif olarak, önceden ayarlanmış ağ biçimlerini görüntülemek için stil menüsünün üst kısmındaki açılır menüye tıklayın.
NOT: STRING-db protein-protein etkileşim verileri bu ağ içine şu anda ya giriş dosyası üzerinden elle ya da Cytoscape eklentileri olarak mevcut çeşitli zenginleştirme araçları aracılığıyla entegre edilebilir, http://apps.cytoscape.org/20. Zenginleştirme analizi için önerilen sitoscape eklentisi21 http://apps.cytoscape.org/apps/cluegobulunur. - Bu iş akışında oluşturulan veri kümesine olan güveni artırmak için, yem olarak av proteinlerini hedefleyen karşılıklı IP-MS veya IP-western deneyleri gerçekleştirin.
Sonuçlar
BIR IP-MS deneyinde tanımlanan protein kütlesinin büyük bir kısmı nonspesifik proteinlerden oluşur. Bu nedenle, bir IP-MS deneyinin en önemli zorluklarından biri proteinlerin yüksek güven interaktörleri ile nonspesifik interaktörler arasında yorumlanmasıdır. Veri kalitesinin değerlendirilmesinde kullanılan önemli parametreleri göstermek için çalışma, boncuk sadece kontrol kullanılarak 5 mg HeLa nükleer ekstresinden triplicate immünopreplitleri analiz etti. Bir IP-MS deneyinin güvenilir olduğundan emin olmak için ilk iç kontrol, yem proteininin hem kontrol hem de SAINT olasılığı üzerinde kat değişimi ile tanımlanan en yüksek zenginleştirilmiş proteinlerden biri olup olmadığıdır. Bu durumda, yem DYRK1A kontrol üzerinde ilk üç zenginleştirilmiş proteinler arasında yer aldı (Şekil 2A,B). DYRK1A bir nükleer etkileşimom çalışmada dört bağımsız antikorlar kullanarak, bir FC-A kesme >3.00 ve SAINT olasılık kesme >0.7 hem roman ve daha önce doğrulanmış interactors22belirlenmesi için sıkı bir kesme sağladı . Bu deneye uygulandığında, yüksek güven interaktörleri ile nonspesifik olarak tanımlanan saflaştırılmış proteinlerin %195'i arasında net bir ayrım görülebilir(Şekil 2A,B). Hem kat değişim zenginleştirme hem de olasılık eşiğinin uygulanması, biyolojik kopyalar arasında protein yetersizliklerinin sürekli olarak yüksek bir zenginleştirme gerektirmesi ile sıkılığı artırır.
Istatistiksel puanlama ek olarak, CRAPome analizi iş akışı da daha önce yem-av veri23üzerine bildirilen etkileşimleri haritalar . Bu haritalama yüksek ve düşük güven etkileşimleri eşik için yararlı olabilir, daha önce bildirilen etkileşimler FC-A ve SAINT olasılıkları tarafından kötü puan olabilir, potansiyel olarak belirli bir yem birçok bilinen etkileşimleri sadece belirli hücre türleri, bağlamlar veya organeller var olabileceğini gösteren. Örneğin DYRK1A veri seti, iREF etkileşimci FC-A değerleri 0,45 gibi düşük, kontrol üzerinde çok düşük bir zenginleştirme temsil eden(Şekil 2C). Yanlış pozitiflerin enflasyonunu önlemek için, istatistiksel eşik, yanlış negatiflerin azaltılmasına göre sıkılığa öncelik veren bir şekilde yapılmalıdır. Bu etkileşimlerin saptanması protein bolluğundan bağımsızdır (Şekil 2C). HeLa hücreleri içindeki her iREF etkileşiminin hesaplanan mutlak kopya sayısı, IP-MS24ile etkileşim ortağının algılama düzeyleriyle bir korelasyon göstermedi.
Cytoscape etkileşim verilerinin birden fazla katmanını görselleştirmek için etkili bir araç olarak hizmet vermektedir19. Burada açıklanan DYRK1A immünopresipite deneyinde, FC-A > 3.0 ve SAINT > 0.9'un kombine kullanımı yüksek güven interaktörlerin listesini altı proteine indirgedi(Şekil 2D). Ancak, > 3.0'ın FC-A kesimi izolasyonhalinde uygulandığında ağa sekiz protein daha eklendi. Bu ek protein interaktörler ağ zaten interaktörler ile yüksek bağlantı var, onlar benzer kompleksleri veya fonksiyonel rolleri ilişkili olduğunu düşündürmektedir. Bu amaçla, protein-protein etkileşimlerinin STRING-DB'sinden elde edilen kanıtlar bu ağa mavi kesik çizgiler20olarak entegre edilmiştir. Bu tek yem, triplicate deney tam DYRK1A etkileşim ağının sınırlı bir örnek sağlarken, ek yemler, çoğaltmalar ve büyük genel veri kümelerinin entegrasyonu yüksek güven etkileşimleri ağını genişletmek için kullanılabilir. Bu nedenle istatistiksel kesintiler her deneye özgü olacak ve iyice değerlendirilmesi gerekecektir.
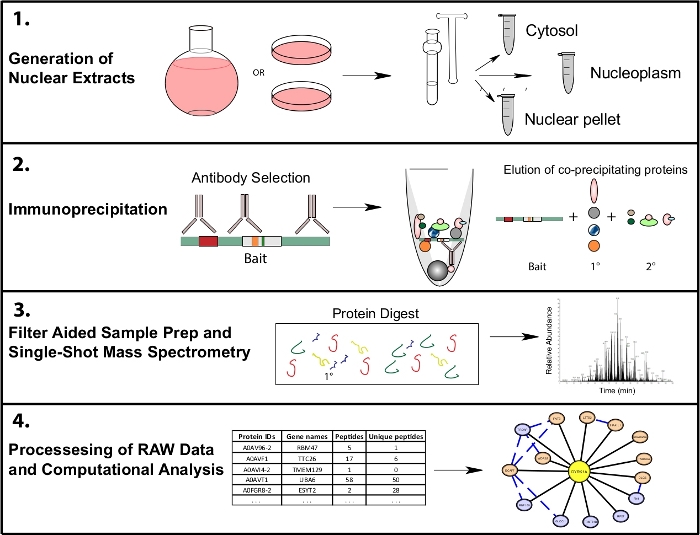
Şekil 1: Hücre altı IP-MS için temsili proteomik iş akışı. Hücreler ya 4 L yuvarlak alt şişelerde veya 15 cm doku kültürü tabaklarında yetiştirilir ve hücre altı fraksiyonu için aynı anda hasat edilir. Hücreler sitosolik, nükleer ve nükleer pelet içine fraksiyona alınır ve immünopreside 1−10 mg nükleer lysate ile aynı yemi tanıyan bir veya birden fazla antikor kullanılarak yapılır. Filtre destekli numune hazırlığı (FASP) ve çevrimdışı numune temizliği tek çekim kütle spektrometresi öncesinde gerçekleştirilir. Verileri yorumlanabilir etkileşim verilerine işlemek için bir akış aşağı hesaplama ardışık işlem akışı kullanılır. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
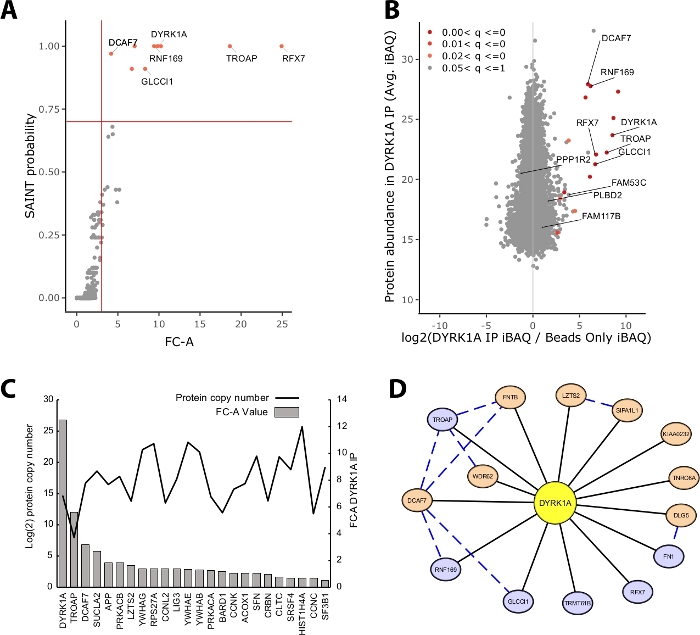
Şekil 2: Tek yemlik tek antikorLU IP-MS deneyi için temsili veriler. (A) FC-A ve SAINT olasılık çıktısı CRAPome analizi iş akışı ndan en iyi deney için kinaz DYRK1A için tek bir antikor kullanarak (n = 3). Karşılaştırma için yalnızca boncuk denetimleri kullanılmıştır. Kırmızı düz çizgiler FC-A > 3.00 ve SAINT > 0.7'de ayarlanan kesintileri temsil eder. (B) MaxQuant protein bolluğu tahminleri (iBAQ) çıkış ve dyrk1A IP protein bolluğu log2 oranı kontrol etmek için, etiket içermeyen yoğunlukları ampirik Bayes analizi nden ayarlanmış p değer aralığı ile renkli. (C) FC-A ve iRef veritabanında etkileşen proteinler olarak listelenen proteinlerin tahmini kopya sayısı23,24. (D) DYRK1A interaktörlerin Cytoscape ağ görselleştirme. Mavi düğümler = FC-A > 3.00, SAINT > 0.7. Turuncu düğümler = FC-A > 3.00. Siyah kenarlar = IPMS deneyinde interaktörler olarak tanımlanan proteinler. Mavi kesik kenar = av proteini arasındaki SAINT etkileşimi (güven > 0,150). Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
| Proteaz inhibitörü (PI) karışımı | |
| Reaktif | Son Konsantrasyon |
| Sodyum Metabisülfit | 1 mM |
| Benzamidin | 1 mM |
| Dithiothreitol (DTT) | 1 mM |
| Fenilmetansülfonil florür (PMSF) | 0,25 mM |
| Fosfataz Inhibitörü (PhI) karışımı | |
| Reaktif | Son Konsantrasyon |
| Mikrosistin LR | 1 μM |
| Sodyum Orthovanadate | 0,1 mM |
| Sodyum florür | 5 mM |
| Hücre altı fraksiyonaraleri: | |
| Tampon A pH 7.9 | |
| Reaktif | Son Konsantrasyon |
| HEPES | 10 mM |
| MgCl2 | 1,5 mM |
| Kartal | 10 mM |
| Tampon B pH 7.9 | |
| Reaktif | Son Konsantrasyon |
| HEPES | 20 mM |
| MgCl2 | 1,5 mM |
| Nacl | 420 mM |
| Etilendimintetraasetik asit (EDTA) | 0,4 mM |
| Gliserol | %25 (v/v) |
| Tampon C pH 7.9 | |
| Reaktif | Son Konsantrasyon |
| HEPES | 20 mM |
| MgCl2 | 2 mM |
| Kartal | 100mm |
| Etilendimintetraasetik asit (EDTA) | 0,4 mM |
| Gliserol | %20 (v/v) |
| İmmünopreprezan tamponlar: | |
| IP Arabellek 1 | |
| Reaktif | Son Konsantrasyon |
| HEPES | 20 mM |
| Kartal | 150 mM |
| Edta | 0,1 mM |
| NP-40 | %0,1 (v/v) |
| Gliserol | %10 (v/v) |
| IP Arabellek 2 | |
| Reaktif | Son Konsantrasyon |
| HEPES | 20 mM |
| Kartal | 500 mM |
| Edta | 0,1 mM |
| NP-40 | %0,1 (v/v) |
| Gliserol | %10 (v/v) |
| SDS Alkylation Tampon pH 8.5 | |
| Reaktif | Son Konsantrasyon |
| SDS | %4 (v/v) |
| Kloroasetamid | 40 mM |
| TCEP | 10 mM |
| Tris | 100mm |
| UA pH 8.5 | |
| Reaktif | Son Konsantrasyon |
| Üre | 8 M |
| Tris | 0,1 M |
| * HPLC sınıfı H2O kullanın | |
Tablo 1: Arabellek kompozisyonları
Ek Kodlama Dosyaları. Bu dosyayı indirmek için lütfen buraya tıklayınız.
Tartışmalar
Burada özetlenen proteomik iş akışı ilgi bir protein için yüksek güven protein interaktörleri tanımlamak için etkili bir yöntem sağlar. Bu yaklaşım, hücre altı fraksiyonu ile örnek karmaşıklığını azaltır ve sağlam numune hazırlama, çevrimdışı numune temizleme ve LC-MS sisteminin sıkı kalite kontrolü yoluyla tanımlama etkileşim ilerleçiş ortaklarını artırmaya odaklanır. Burada açıklanan aşağı akım veri analizi yem ile copurifying olarak tanımlanan proteinlerin basit bir istatistiksel değerlendirme sağlar. Ancak, deneysel değişkenlerin (ölçek, hücre hattı, antikor seçimi) yüksek sayıda nedeniyle, her deney farklı cutoffs ve veri görselleştirme ve zenginleştirme ile ilgili hususlar gerektirir.
Bir IP-MS deneyinde ilk tasarım konusu, etkileşen ortakları ile birlikte ilgi proteininin saflaştırılmasında kullanılacak antikorların seçimidir. Ticari antikorların kullanılabilirliği son birkaç on yıl içinde insan proteom büyük bölümlerini kapsayacak şekilde genişletilmiş olsa da, reaktifler sınırlı olduğu için hala birçok protein vardır. Ayrıca, batı leke tespiti gibi uygulamalar için doğrulanmış antikorlar immünopredibat deneyinde hedef proteinin selektif zenginleştirme yeteneğine sahip olmayabilir. Büyük ölçekli bir etkileşim proteomik deneyi gerçekleştirmeden önce, bir IP'nin %90'lık bir 10 cm'lik çanak tan veya eşdeğer hücre numarasından tamamlanması ve batı lekeleme ile ilgi çekici hedef protein için sonda lanması önerilmektedir. İmmünenyağış için birden fazla antikor mevcutsa, proteinin farklı kısımlarında epitopsları tanıyan birden fazla antikor seçilmesi önerilmektedir. Bir antikorbir yem proteinine bağlanması putatif etkileşimli ortaklar için gerekli bağlayıcı arabirimi tıkayabilir. Yem proteini için ikincil bir epitop seçimi, kütle spektrometresi tabanlı bir deneyle tanımlanan etkileşim profilinin kapsamını artıracaktır.
İkinci önemli husus, yüksek güven etkileşimlerini yemle işbirliği olarak tanımlananlardan düşük güven veya nonspesifik etkileşimlerden ayırmak için uygun kontrolün seçiminde yatsıdır. Bir IP-MS deneyi için en sıkı kontrol, bayem bir CRISPR KO hücre hattından immünoprepitasyon tamamlamaktır. Böyle bir kontrol, yem proteini yerine doğrudan antikora bağlanan spesifik olmayan proteinlerin tanımlanmasını ve filtrelanmasını sağlar. Her yem proteininin CRISPR KO hücre hattı nın üretilmesinin mümkün olmadığı durumlarda, yem antikorunun aynı izotipinin IgG-boncuk kontrolü kullanılabilir. Birden fazla türü temsil eden antikorlardan oluşan bir panel kullanan deneylerde, boncukların sadece kontrolü uygun olabilir, ancak yüksek güven interaktörler olarak tanımlanan yanlış pozitif lerin oranını artıracaktır.
BIR IP-MS denemesinde kullanılan hücre hattının seçimi birkaç önemli etkene bağlıdır. Protein ekspresyonu ve lokalizasyonu büyük ölçüde hücre tipine bağlıdır. RNA ekspresyonu tahminleri birçok yaygın olarak kullanılan hücre hatlarında çoğu gen için bulunabilir iken, protein ekspresyonu rna ekspresyonu ile kötü ilişkilidir ve deneysel olarak belirlenmelidir25. Bir yem proteininin çok düşük kopya numarasıyla ifade edildiği hücre çizgileri, gerekli olabilecek hücre kültürü ölçeğindeki ciddi artışlarla ilişkili sorunları atlatmak için kaçınılmalıdır. Ancak, örnek hazırlama çok düşük bolluk proteinlerinin tespiti için optimize edilebilir unutulmamalıdır. Filtre destekli numune hazırlama (FASP) yöntemi, sağlam olmakla birlikte, bir numunede %50'den fazla peptid kaybına neden olabilir. Tek Pot Katı Fazlı Gelişmiş Numune Hazırlama (SP3), numune kaybını en aza indiren kütle spektrometresi analizi için numune oluşturmanın etkili bir yöntemidir26. Numune hazırlama nın SP3 yöntemi yle etkin hale gelen artan geri kazanım, algılama sınırına yakın olan proteinlerin nicelleştirilmesi için bu iş akışında yararlı bir alternatif olabilir.
Bu proteomik iş akışı kinazlar, E3 ubiquitin ligases ve multisubunit komplekslerinin iskele üyeleri de dahil olmak üzere birçok nükleer yemler arasında uygulanmıştır. Antikor reaktiflerinin doğru doğruluğunu varsayarsak, bu iş akışının başarılı bir şekilde yürütülmesi, yüksek güven emüldomu proteini nükleer etkileşim ortaklarının ilgi çekici bir protein için saptanmasına neden olacaktır.
Açıklamalar
Yazarların açıklayacak bir şeyi yok.
Teşekkürler
Bu çalışma, Linda Crnic Down sendromu Enstitüsü'nden W.M.O.'ya verilen Grand Challenge bursu ve DARPA işbirliği anlaşması 13-34-RTA-FP-007 ile desteklenmiştir. Jesse Kurland ve Kira Cozzolino'ya el yazmasının okunması ve yorumlanmasındaki katkılarından dolayı teşekkür ederiz.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 0.25% Trypsin, 0.1% EDTA | Thermo Fisher Scientific | 25200056 | |
| 1.5 ml low-rention microcentrifuge tubes | Fisher Scientific | 02-681-320 | |
| 4-20% Mini PROTEAN TGX Precast Protein Gels | Bio-Rad | 4561096 | |
| acetone (HPLC) | Thermo Fisher Scientific | A949SK-4 | |
| Amicon Ultra 0.5 ml 30k filter column | Millipore Sigma | UFC503096 | |
| Benzamidine | Sigma-Aldrich | 12072 | |
| benzonase | Sigma-Aldrich | E1014 | |
| Chloroacetamide | Sigma-Aldrich | C0267 | |
| Dialysis tubing closure | Caroline Biological Supply Company | 684239 | |
| DTT | Sigma-Aldrich | 10197777001 | |
| EDTA | Sigma-Aldrich | EDS | |
| GAPDH antibody | Santa Cruz Biotechnology | Sc-47724 | |
| Glycerol | Fisher Scientific | 887845 | |
| Glycine | Sigma-Aldrich | G8898 | |
| HeLa QC tryptic digest | Pierce | 88329 | |
| HEPES | Fisher Scientific | AAJ1692630 | |
| insulin | Thermo Fisher Scientific | 12585014 | |
| iodoacetamide | Sigma-Aldrich | I1149 | |
| KONTES Dounce homogenizer 7 ml | VWR | KT885300-0007 | |
| Large Clearance pestle 7ml | VWR | KT885301-0007 | |
| Lysyl endopeptidase C | VWR | 125-05061 | |
| Magnesium Chloride | Sigma-Aldrich | 208337 | |
| Microcystin | enzo life sciences | ALX-350-012-C100 | |
| Nonidet P 40 Substitute solution | Sigma-Aldrich | 98379 | |
| p84 antibody | GeneTex | GTX70220 | |
| Phosphate Buffered Saline | |||
| Pierce BCA Protein Assay Kit | Thermo Fisher Scientific | 23227 | |
| Pierce BSA Protein Digest, MS grade | Thermo Fisher Scientific | 88341 | LCMS QC |
| Pierce C18 spin columns | Thermo Fisher Scientific | PI-89873 | |
| Pierce Trypsin Protease, MS Grade | Thermo Fisher Scientific | 90057 | For mass spectrometry sample prep |
| PMSF | Sigma-Aldrich | P7626 | |
| Potassium Chloride | Sigma-Aldrich | P9541 | |
| Protein A Sepharose CL-4B | GE Healthcare Bio-Sciences | 17-0780-01 | |
| Protein G Sepharose 4 Fast Flow | GE Healthcare Bio-Sciences | 17-0618-01 | |
| SDS | Sigma-Aldrich | L3771 | |
| Silica emitter tip | Pico TIP | FS360-20-10 | |
| Small Clearance pestle 7ml | VWR | KT885302-0007 | |
| Sodium Chloride | Sigma-Aldrich | S3014 | |
| Sodium Fluoride | Sigma-Aldrich | 201154 | |
| Sodium metabisulfite | Sigma-Aldrich | 31448 | |
| Sodium orthovanadate | Sigma-Aldrich | S6508 | |
| Spectra/ Por 8 kDa 24 mm dialysis tubing | Thomas Scientific | 3787K17 | |
| TC Dish 150, Standard | Sarstedt | 83.3903 | Tissue culture dish for adherent cells |
| TCA | Sigma-Aldrich | T9159 | |
| TCEP | Thermo Scientific | PG82080 | |
| TFA | Thermo Fisher Scientific | 28904 | |
| Thermo Scientific Orbitrap Fusion MS | Thermo Fisher Scientific | ||
| Trizma Base | Sigma-Aldrich | T6066 | |
| Urea | Thermo Fisher Scientific | 29700 | |
| Waters ACQUITY M-Class UPLC | Waters | ||
| Waters ACQUITY UPLC M-Class Column Reversed-Phase 1.7µm Spherical Hybrid (1.7 µm, 75 µm x 250 mm) | Waters | 186007484 | nanoflow C18 column |
Referanslar
- Varjosalo, M., et al. The protein interaction landscape of the human CMGC kinase group. Cell Reports. 3, 1306-1320 (2013).
- Kimple, M. E., Brill, A. L., Pasker, R. L. Overview of Affinity Tags for Protein Purification. Current Protocols in Protein Science. 73, (2013).
- Mahmood, N., Xie, J. An endogenous 'nonspecific' protein detected by a His-tag antibody is human transcription regulator YY1. Data in Brief. 2, 52 (2015).
- Zordan, R. E., Beliveau, B. J., Trow, J. A., Craig, N. L., Cormack, B. P. Avoiding the ends: internal epitope tagging of proteins using transposon Tn7. Genetics. 200, 47-59 (2015).
- Gibson, T. J., Seiler, M., Veitia, R. A. The transience of transient overexpression. Nature Methods. 10, 715-721 (2013).
- Bronicki, L. M., et al. Ten new cases further delineate the syndromic intellectual disability phenotype caused by mutations in DYRK1A. European Journal of Human Genetics. 23, 1482-1487 (2015).
- Antonarakis, S. E. Down syndrome and the complexity of genome dosage imbalance. Nature Reviews Genetics. , (2016).
- Dowjat, W. K., et al. Trisomy-driven overexpression of DYRK1A kinase in the brain of subjects with Down syndrome. Neuroscience Letters. 413, 77-81 (2007).
- Fotaki, V., et al. Dyrk1A haploinsufficiency affects viability and causes developmental delay and abnormal brain morphology in mice. Molecular and Cellular Biology. 22, 6636-6647 (2002).
- Hämmerle, B., Elizalde, C., Tejedor, F. J. The spatio-temporal and subcellular expression of the candidate Down syndrome gene Mnb/Dyrk1A in the developing mouse brain suggests distinct sequential roles in neuronal development. European Journal of Neuroscience. 27, 1061-1074 (2008).
- Funakoshi, E., et al. Overexpression of the human MNB/DYRK1A gene induces formation of multinucleate cells through overduplication of the centrosome. BMC Molecular and Cell Biology. 4, 12 (2003).
- Yu, D., Cattoglio, C., Xue, Y., Zhou, Q. A complex between DYRK1A and DCAF7 phosphorylates the C-terminal domain of RNA polymerase II to promote myogenesis. Nucleic Acids Research. , 1-14 (2019).
- Towbin, H., Staehelin, T., Gordon, J. Electrophoretic transfer of proteins from polyacrylamide gels to nitrocellulose sheets: procedure and some applications. Proceedings of the National Academy of Sciences of the United States of America. 76, 4350-4354 (1979).
- Wiśniewski, J. R., Zougman, A., Nagaraj, N., Mann, M. Universal sample preparation method for proteome analysis. Nature Methods. 6, 359-362 (2009).
- Tyanova, S., Temu, T., Cox, J. The MaxQuant computational platform for mass spectrometry-based shotgun proteomics. Nature Protocols. 11, 2301-2319 (2016).
- Tyanova, S., et al. The Perseus computational platform for comprehensive analysis of (prote)omics data. Nature Methods. 13, 731-740 (2016).
- Mellacheruvu, D., et al. The CRAPome: A contaminant repository for affinity purification-mass spectrometry data. Nature Methods. 10, 730-736 (2013).
- Choi, H., et al. SAINT: Probabilistic scoring of affinity purificationg-mass spectrometry data. Nature Methods. 8, 70-73 (2011).
- Shannon, P., et al. Cytoscape: a software environment for integrated models of biomolecular interaction networks. Genome Research. 13, 2498-2504 (2003).
- Szklarczyk, D., et al. The STRING database in 2017: quality-controlled protein-protein association networks, made broadly accessible. Nucleic Acids Research. 45, 362-368 (2017).
- Bindea, G., et al. ClueGO: a Cytoscape plug-in to decipher functionally grouped gene ontology and pathway annotation networks. Bioinformatics. 25, 1091-1093 (2009).
- Guard, S. E., et al. The nuclear interactome of DYRK1A reveals a functional role in DNA damage repair. Scientific Reports. 9, 6539 (2019).
- Razick, S., Magklaras, G., Donaldson, I. M. iRefIndex: A consolidated protein interaction database with provenance. BMC Bioinformatics. 9, 405 (2008).
- Kulak, N. A., Pichler, G., Paron, I., Nagaraj, N., Mann, M. Minimal, encapsulated proteomic-sample processing applied to copy-number estimation in eukaryotic cells. Nature Methods. 11, 319-324 (2014).
- Liu, Y., Beyer, A., Aebersold, R. On the Dependency of Cellular Protein Levels on mRNA Abundance. Cell. 165, 535-550 (2016).
- Hughes, C. S., et al. Ultrasensitive proteome analysis using paramagnetic bead technology. Molecular Systems Biology. 10, 757 (2014).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır