Method Article
İnsan Trombositlerinde Amotrofik Lateral Sklerozun Potansiyel Biyobelirteçlerini Aramak İçin Kapiller Elektroforez İmmünoassay Kullanımı
Bu Makalede
Özet
Nörodejeneratif hastalıklar için kan bazlı biyobelirteçler büyük ölçekli klinik çalışmaların uygulanması için gereklidir. Güvenilir ve doğrulanmış bir kan testi küçük bir örnek hacmi yanı sıra daha az invaziv örnekleme yöntemi, uygun fiyatlı ve tekrarlanabilir olmalıdır. Bu makale, yüksek iş itimatlı kapiller elektroforez immünoassay'In potansiyel biyomarker gelişimi için kriterleri karşıladığını göstermektedir.
Özet
Kapiller elektroforez immünoassay (CEI), ayrıca kapiller batı teknolojisi olarak bilinen, klinik çalışmalarda hastalık ile ilgili protein ve ilaçların taranması için tercih edilen bir yöntem haline gelmektedir. Tekrarlanabilirlik, duyarlılık, küçük numune hacmi gereksinimi, aynı numunede birden fazla protein etiketlemesi için çokluk antikorları, 24 ayrı numuneyi analiz etmek için otomatik yüksek iş hacmi yeteneği ve kısa süreli gereksinim CEI klasik batı leke immünoassay üzerinde avantajlı. Bu yöntemin bazı sınırlamaları vardır, örneğin bir degrade jel kullanamama gibi (%4-20). matris, rafine edilmemiş biyolojik numuneler ile yüksek arka plan ve bireysel reaktiflerin ticari kullanılamaması. Bu makalede, CEI'yi birden çok tahkikat ayarında çalıştırmak, protein konsantrasyonu ve birincil antikor titrasyonu tek bir tahkikat plakasında optimize etmek ve numune hazırlama için kullanıcı dostu şablonlar sağlamak için etkili bir yöntem açıklanmaktadır. Nörodejeneratif hastalıklariçin kan bazlı biyomarker geliştirme girişiminin bir parçası olarak pan TDP-43 ve trombosit lysate sitosolda fosforlu TDP-43 türevi ölçüm yöntemleri de açıklanmıştır.
Giriş
Burada açıklandığı gibi CEI genel amacı insan trombosithedef proteinlerin analizi için güncelleştirilmiş bir adım adım protokolü sağlamaktır. Kan bazlı imza molekülünün atanması, Alzheimer hastalığı (AD), amiyotrofik lateral skleroz (ALS), frontotemporal lobar gibi insan nörodejeneratif hastalıklarında biyomarker gelişimi alanındaki en önemli görevlerden biridir. dejenerasyon (FTLD), Parkinson hastalığı (PH), inklüet vücut miyoziti (IBM) ve diğer protein agregasyonu ile ilgili patolojik durumlar. Birçok müdahale edici ajanlar ile kan büyük hacimlerde bu tür imza proteinlerin dakika miktarlarının tespiti bir meydan okumadır. Bu nedenle, çok sayıda örneği işleme yeteneği ve seçilen yöntemin tekrarlanabilirliği çok önemlidir.
İnsan trombositleri nörodejeneratif hastalık için potansiyel biyomarker proteinlerini tanımlamak ve atamak için bir ortam görevi görebilir. Trombositler nöronal hücrelerin bazı özelliklerini yansıtan bir vekil birincil hücre modeli olarak hizmet etmek için fırsat sağlamak1,2,3. Trombositleri biyomarker adayı proteinleri ve kimyasal türevlerini analiz etmek için tercih edilen araçlardan biri haline getiren bazı özellikler vardır. İlk olarak, trombositler kolayca donörler kan toplayarak daha az invaziv bir yaklaşım kullanılarak elde edilebilir (yani, venipuncture) veya toplum kan bankalarından büyük miktarlarda. İkincisi, trombositkolayca minimal donanımlı laboratuvarlarda minimal hazırlık çalışmaları ile tam kan izole edilebilir4,5. Üçüncü olarak, trombositlerin çekirdekleri yoktur; bu nedenle, transkripsiyonel düzenleme olmadan metabolizma değişiklikleri incelemek için iyi bir model hücre vardır. Dördüncü olarak, trombositlerin biyomolekül içeriği kapsüllenir; bu nedenle trombosit mikroortamı içeriğini seruma müdahale eden maddelerden (örn. proteazlar) korur. Beşinci olarak, trombositle zenginleştirilmiş plazma, metabolik aktiviteyi kaybetmeden 7-8 gün oda sıcaklığında saklanabilir. Bu nedenle trombositler dış etkenlerin en aza indirildiği ve kontrol edildiği bir çalışma modeli sağlar.
İmmünoblotlama (örneğin, batı lekeleme) ve enzime bağlı immünosorbent tahlil (ELISA) gibi geleneksel immünoassay teknikleri spesifik protein analizinde daha yaygın olarak kullanılmaktadır. Ancak, bu iki yöntem, birden fazla deneme adımları, tehlikeli kimyasallar ve reaktifler gereksinimi, büyük numune boyutu, test tekrarlanabilirliği ile ilgili sorunlar ve birlikte çalıştırılan veri çeşitleri dahil olmak üzere çeşitli dezavantajları vardır. Bunlar, daha az adımla daha basit ve nispeten kısa bir süre içinde ulaşılabilir bir yöntemin geliştirilmesini istesin. Klasik batı leke tekniği popüler bir laboratuvar yöntemi olmaya devam edecek olsa da, çok aşamalı prosedürü, sarf malzemeleri, toksik atıklar (akrilamid, metanol, vb.) ve test süresi yüksek iş yapma kantitatif gerçekleştirirken daha az arzu edilir hale gelmektedir protein analizi.
Otomatik cei yaklaşımı yavaş yavaş yüksek iş letimatif proteintahlilleri6 yapan laboratuvarlar için tercih bir yöntem haline gelmektedir. CEI jeller, jel elektroforez cihazları, membranlar, elektroforez ve elektro-transfer cihazları ve daha fazla fiziksel taşıma tutulumu ihtiyacını ortadan kaldırır. Eğer iyi tasarlanmışsa, nicel veri analizi, yayın kalitesi elektrofegramı ve istatistiksel analizli grafikler de dahil olmak üzere yaklaşık 3,5 saat içinde bir CEI tahlilleri tamamlanmalıdır. CEI sisteminin bir diğer üstünlüğü 10x-20x daha az protein konsantrasyonu gereksinimi, klinik çalışmalarda kullanılan insan örneklerinde kullanım için ideal hale7,8.
CEI'nin en kritik parçası, farklı satıcılardan satın alınan her antikor, antikor tipi (monoklonal vs. poliklonal), optimum protein konsantrasyonları, numune hazırlama, numune denatürasyon sıcaklığı ve kılcal damarlara uygulanan elektroforez gerilimi için test koşullarını optimize etmektir. CEI için zaman ve kaynak tasarrufu sağlayacak yeni tahlillerden önce uygulanması gereken tek bir tahlil formatı optimizasyon yöntemi geliştirdik. Bu optimizasyon adımını, transaktivasyon yanıtı DNA/RNA bağlayıcı proteinin (TARDP) hem toplam hem de fosforilize türevinin otomatik kantitatif değerlendirmesi takip eder. Boyutu (43 kDa) nedeniyle, tdp-43 kısaltması bu yazı boyunca kullanılacaktır. Burada ALS hastalarından elde edilen insan trombosit lisatındaki TDP-43 proteini, potansiyel prognostik biyobelirteç olarak tahmine dayalı fosforilasyon değerinin (PPV) geliştirilmesine yardımcı olmak için değerlendirilmektedir.
TDP-43 ALS için yeni bir potansiyel hastalık biyomarker adayıdır. TDP-43 tüm çekirdekli hücrelerde her yerde bulunan bir proteindir; bu nedenle, çeşitli normal hücresel olaylar sırasında ve nörodejeneratif hastalık ta TDP-43 fonksiyonları araştırılmıştır9,10,11,12,13,14. TDP-43 bir nükleer protein olmasına rağmen15, nükleer lokalizasyon ve nükleer ihracat dizileri16varlığı nedeniyle çekirdek ve sitoplazma arasında mekik ve dışarı mekik yeteneğine sahiptir 16,17,18,19. Sitoplazmik TDP-43, mRNA stabilitesi ve taşınması, stres tepkisi, mitokondriyal fonksiyon, otofazom20gibi çeşitli hücresel olaylarda yer almaktadır. Ancak, Nörodejeneratif hastalık21patogenezinde rollerinin dışında TDP-43'ün fosforitürevlerinin rolü hakkında çok fazla bilgi yoktur.
Bu protokol, CEI yaklaşımını kullanarak Trombositlerde TDP-43 ve fosforilasyonlu türevinin içeriğini analiz etmek için test koşullarının nasıl optimize edilebildiğini göstermektedir. Fosforlu TDP-43 ticari olarak mevcut olmadığından ALS hastalarında TDP-43 profillerini değerlendirmek için tahmine dayalı fosforilasyon değeri (PPV) kullanılması önerilmektedir. Bu CEI sistemi küçük bir hacimde örnek karışım kullanır (kılcal damar başına 2.5-3.0 μL). Toplam test hacmi kurulumu, üreticiprotokolüne göre kılcal damar başına 8,0 μL'dir; bu nedenle, araştırmacılar iki ayrı çalışır için bir örnek karışım hazırlama kullanabilirsiniz. Üretici, tamamen ortadan kaldırılmazsa, herhangi bir pipetleme hatası en aza indirilmesi için test protokolünü tasarlatılmıştır. 24 ayrı insan trombositli numune karışımları yarım hacimlere (örn. örnek başına 2,5-3,0 μL) bölünür ve ~7 saat içinde iki farklı antikor tarafından ardışık olarak analiz edilir. Burada açıklanan CEI sistemi arzu edilen yüksek iş itimat lı bir hesaplama yöntemi sağlar. Kullanıcıların büyük ölçekli tarama yapmadan önce farklı satıcılardan antikorları ve hedef protein için numune hazırlama yöntemlerini test etmesi gerekir.
Protokol
İnsan trombositlerinin işlenmesiyle ilgili tüm protokoller Hem Kansas Üniversitesi Tıp Merkezi hem de Kansas City Tıp Üniversitesi ve Biyobilim IRB komitelerinin yönergelerini izler.
1. Tampon ve reaktiflerin hazırlanması
NOT: Tüm numuneleri üreticinin yönergelerine göre hazırlayın. Bu işlem sırasında kişisel koruma ekipmanları (laboratuvar önlükleri, eldivenler ve gözlükler) takın.
- 0,941 g sakaroz (11 mM son konsantrasyon), 6,4 mL 5 M NaCl (128 mM final), 5,4 mL 0,2 M NaH2PO4 (4,3) birleştirerek sitrat yıkama tamponhazırlayın mM final), 9.4 mL 0.2 M Na2PHO4 (7.5 mM final), 0.352 g sodyum sitrat (4.8 mM final) ve 0.115 g sitrik asit (2.4 mM final). DdH2O. Filtre 0,45 μm filtre diski ile toplam hacmi 250 mL'ye ayarlayın ve pH'ı 6,5'e ayarlayın. 4 °C'de 1 yıla kadar saklayın. 22 kullanmadan önce çözelti oda sıcaklığını (RT)getirin.
- 100 mL son hacimde 250 mM sakaroz, 1 mM EDTA ve 10 mM Tris-Cl (pH 7.4) birleştirerek kopma tamponunu hazırlayın. 4 °C'de 1 yıla kadar saklayın. 2 mL kopma tamponuna 2 μL fosfataz inhibitörleri kokteyli (1:1000 son) ve 1 μL proteaz inhibitörleri kokteyli (1:2000 final) ekleyin. Kullanıma kadar buzda tutun. Kullanılmayan kopma arabelleği atın.
2. Trombosit izolasyonu
- Asit-sitrat-dekstroz (ACD) çözeltisi (75 mM trisodyum sitrat, 124 mM dekstroz ve 38 mM sitrik asit, pH = 7,4 içeren sarı kapaklı kan toplama tüpünde 8-10 mL insan kanı toplamak; ACD:kan = 1:9). Tüp içeriğini elle 5x-6x ters çevirerek hafifçe karıştırın.
- Tüpleri 200 x g'de, rt'de 20 dk boyunca sallanan bir kova rotorunda santrifüj edin.
- 15 mL konik alt tüp içine trombosit açısından zengin plazma (PRP) (~3-4 mL) toplayın ve kontaminasyonu önlemek için buffy coat'dan (puslu görünümlü fraksiyon) yaklaşık 0,5 mL PRP bırakın. Herhangi bir kırmızı kan hücresi kontaminasyonu oluşursa, bu adımı tekrarlayın.
- PRP numunelerini 1.200 x g'de 15 dk RT'de santrifüj edin.
- Trombosit peletlerini (P1) 1 mL'lik sitrat yıkama tamponu ve peletini 1.200 x g'de 15 dakika boyunca sentrasyonla hafif çetreyle yıkayın.
- Saf trombosit pelet kaydedin. Supernatant atın.
- Inhibitör kokteyller içeren kopma tamponunun 600 μL'lik trombosit peletlerini yeniden askıya alın.
- Bir sonicator kullanarak trombosit süspansiyon sonicate. Örneği mini bir buz kovası içine yerleştirin. Sonicator'u sürekli modda 20 s'ye 3 ayarla'da ayarlayın.
NOT: Sondayı %10 çamaşır suyu ve ardından distile su ile temizlediğinden emin olun. - Membranöz fraksiyonları çıkarmak için sonicated örnekleri 20.000 x g 30 dakika 4 °C'de santrifüj. Aliquot 60 μL'de süpernatantlar ve -80 °C'de saklayın. Trombosit sitosolik fraksiyonları için tekrarlanan erime/donma döngülerinden kaçının.
3. CEI için hazırlık
NOT: ALS hastalarından (n = 8-10) 100 μL insan trombositlyatbirlildi ve sağlıklı denekler (n = 8-10) ayrı ayrı biraraya getirilmiş ve tahsin optimizasyonu için kullanılmıştır.
- CEI düzeni (Tablo 1) ve örnek hazırlama(Tablo 2)için şirket içi oluşturulan şablonları doldurun. Numune karışımı hazırlama tablosu dinamiktir ve kaynaktan ne kadar hacim alınması gerektiğini otomatik olarak hesaplar.
NOT: Dinamik Tablo-2'ye gerekli kaynak hacmi girildiğinde, 0,1 X örnek arabellek hacmi otomatik olarak hesaplanır. - Ön etiketli 25 0.2 mL PCR tüpler, kılcal damarları #1-#25 ve PCR rafa yerleştirin. Buza ayarla.
- Ön etiketli 0,6 mL mikrosantrifüj tüpler: her birincil antikor ve seyreltme için bir tane (gerekirse) kullanılacak, biri 0,1x numune tamponu için, diğeri luminol-S/peroksit için ve her numune nin seyreltilmesi için bir tane (gerekirse). Tüp rafbuz üzerine yerleştirin.
- ÖRNEK tampon, yıkama tamponu, bir plaka ve CEI ayırma 12-230 kDa ana kiti ayırma modülünde sağlanan bir kartuş alın.
- 4 °C'lik buzdolabından antikor seyreltme tamponu, primer antikorlar, sekonder antikorlar, luminol, hidrojen peroksit ve standart paketi çıkarın. RT'de kalan standart paket hariç tüm reaktifleri buza yerleştirin.
NOT: Standart paketlerdeki reaktifler lyophilized ve folyo kapak ile mühürlü. Bu ürün kaybını azaltmak için açmadan önce bir mini santrifüj kullanılarak kısa bir süre aşağı bükülmüş olmalıdır. Açmak için, reaktif tüpleri ya bir pipet ucu ile delinmiş veya köşeden geri çekilebilir. - 400 mM DTT'yi hazırlamak için, DTT içeren berrak tüpe 40 μL deiyonize su ekleyin.
- 40 μL floresan 5x ana karışım hazırlamak için, 10x numune tamponunun 20 μL'sini ve hazırlanan 400 mM DTT çözeltisinin 20 μL'sini kitte sağlanan pembe tüpe ekleyin.
- Biyotinylated merdivenhazırlamak için, kit sağlanan beyaz tüp için hazırlanan 400 mM DTT çözeltisi 16 μL deiyonize su, 2 μL 10x numune tampon ve 2 μL ekleyin. Hafifçe karıştırın ve denatüre için 0,2 mL PCR tüp içine aktarın.
- 0,6 mL mikro-santrifüj tüpüne 10x numune tamponu ve 148,5 μL deiyonize su ekleyerek 0,1x numune tamponu hazırlayın. Girdap karıştırmak ve buz üzerine yerleştirmek için.
- İstediğiniz antikor seyreltmelerini hazırlayın. Her önceden etiketlenmiş mikro santrifüj tüp için belirlenen hacimlerde antikor dilüent ekleyin. Hacimler aynıysa, ters pipetleme tekniği23kullanın; değilse, dağıtmadan önce pipet ucunu önceden durula.
NOT: Bu tsözde a-TDP-43 pan antikor ve a-p(S409/410-2) TDP-43 antikor kullanılmıştır. Anti-ERK antikor, bir iç kontrol için, elektbileşenlerinin çalıştığından emin olmak için kullanılmıştır. - Aşağıda açıklandığı gibi antikor seyreltme için ters pipetleme gerçekleştirin. Alternatif olarak, ek bilgi literatürde bulunabilir24.
NOT: Küçük sıralı çözelti hacimleri dağıtılırken ters pipetleme tekniği tercih edilir23. Bu teknik bazı avantajlar sunar: (i) hassas bir hacim sağlamak, (ii) uç delikten köpüren reaktifi ortadan kaldırmak ve (iii) küçük hacimli (<5 μL) reaktifler, viskoz çözeltiler, yüzey aktif solüsyonlar ve yüksek buhar basıncına sahip çözeltiler için idealdir.- Bir pipete uygun bir ipucu koyun ve ikinci durağı (Adım-2) aşağı piston basın. Pipet ucunu çözeltiye birkaç milimetre batırın. İpucu çözeltiye batırılırken pipet ucunu çözeltiyle doldurmak için yavaşça pistonu bırakın. Ucu çözeltiden çıkarın ve ucun dışında kalan fazla sıvının çıkarılabilsin diye reaktif haznesi kenarına hafifçe dokunun.
- Solüsyonu ilk durdurmaya (Adım-1) bastırarak çözeltiyi dağıtın. Kalan çözeltiyi uçta dağıtmayın.
- Geri kalan çözeltiyi ikinci durdurmaya (Step-2) basarak reaktif haznesine boşaltın. Bir sonraki pipetleme adımı için pistonu hazır konuma bırakın.
- Önceden etiketlenmiş her mikrosantrifüj tüpüne belirlenen hacimlerde gerekli antikorekleyin (Tablo 1) Pipet ucunu önceden durulamayın: doğrudan dilüent'e ekleyin ve antikoru çıkarmak için ucu birden fazla kez yıkayın. Tüpleri buza yerleştirin.
- CEI örnek karışımını hazırlamak için, kap#2 ile kap#2 etiketli PCR tüpleri için aşağıda listelenen adımları gerçekleştirin: Bu tablo 1'degöründüğü gibi aynı sıradadır.
- Tüm tüpleri açın, ters pipetleme tekniği kullanarak her tüpe 1,6 μL floresan 5x numune tamponu ekleyin, ardından numune kaybını en aza indirmek için 5x tampon un eklenmesi üzerine her PCR tüpünü kapatın.
- Tüm tüpleri açın, tablo 2'de belirtilen hacimlerde her tüpe 0,1x örnek arabellek ekleyin ve hemen ardından kapatın. Hacimler aynıysa, ters pipetleme tekniği kullanın. Değilse, 0,1x numune arabelleği dağıtmadan önce pipet ucunu önceden durula.
- Tüm tüpleri açın, her tüpe Tablo 2'de belirtilen hacimlerde protein örneği ekleyin ve hemen ardından kapatın. Hacimler aynıysa, ters pipetleme tekniğini kullanın. Değilse, 0,1x numune arabelleği dağıtmadan önce pipet ucunu önceden durula.
- Kısaca bir tezgah üstü santrifüj (30 s için 13.000 x g), flick / girdap PCR tüpler karıştırmak için tüm PCR tüpleri santrifüj, sonra santrifüj tekrarlayın.
- Tüm PCR tüplerini ısıtmalı kapaklı termocycler'a aktarın. Tanımlı sıcaklık ve sürede denature numuneleri (yani 5 dk için 95 °C; 10 dk için 70 °C).
NOT: Denatürasyon sıcaklığı ve süresi hedef protein için optimize edilmelidir. - Adımı 3.12.4'e tekrarlayın.
- Tüm PCR tüplerini tüp rafa geri döndürün ve buza yerleştirin.
- Denaturing adımı sırasında, geliştirme çözeltisini (1:1 luminol-S:peroksit çözeltisi) hazırlayın, ardından 200 μL luminol-S ve 200 μL peroksit ekleyin. Buzun üzerine yerleştirin.
- CeI önceden doldurulmuş bir plakayı yukarıda hazırlanan örnekle birlikte yüklemek için, reaktifleri ve numuneleri, test düzeninde gösterilen test plakasına dağıtın (Şekil 1). Hava kabarcıkları tanıtmaktan kaçının.
NOT: Hacimler ve çözüm aynıysa, ters pipetleme tekniği kullanın. Değilse, dağıtımdan önce pipet ucunu önceden durulayın ve pipetteki ikinci sekme durağını kullanarak geri kalanını tabağa atmayın. 12-230 kDa ayırma modülü renk kodlu plaka yükleme kılavuzu içerebilir. Kuyuya reaktifler ve numuneler eklerken bu kılavuzu plakanın altına yerleştirin, bu da numune yüklemesi sırasında görsel olarak yardımcı olur. Plaka yükleme kılavuzu şirket web sitesinden de indirilebilir.- E satırında, her kuyuya 15 μL luminol:peroksit karışımı ekleyin.
NOT: İdeal olarak, kullanmadan hemen önce bu reaktifi hazırlayın ve her kuyuya ekleyin. Bu uygun değilse, bu karışım plaka yüklemesinden en fazla 30 dakika önce hazırlanabilir. - Satır D, iyi D1 için, streptavidin-HRP 10 μL ekleyin.
- D-D25 kuyularına 10 μL'lik ikincil antikor ekleyin.
- B satırında, her kuyuya 10 μL antikor dilüent ekleyin.
- C satırında, iyi C1 için, antikor dilüent 10 μL ekleyin.
- C-C25 kuyularına C2-C25 satırında, 10 μL belirlenmiş birincil antikor ekleyin.
- A satırında, iyi A1 için, PCR tüp #1 5 μL biyotinylated merdiven ekleyin.
- A satırında, A2-A25 kuyularına, numunenin 3 μL'sini ekleyin, PCR tüpleri #2-#25 ilgili kuyulara #2-#25.
- Belirlenen her yıkama tamponuna 500 μL yıkama tamponu ekleyin.
- Plakayı RT'de 1.000 x g'da 5 dk santrifüj edin.
- E satırında, her kuyuya 15 μL luminol:peroksit karışımı ekleyin.
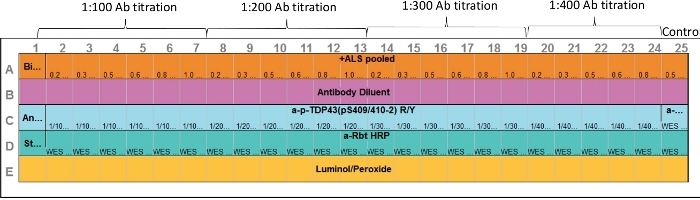
Şekil 1: Tspün düzeni. Hem primer antikor hem de hedef protein örneği optimizasyonu tek bir tahminde yapılabilir. Kılcal damarlar 2-7, 8–13, 14-19 ve 20-24 çeşitli protein konsantrasyonu ve primer antikor aralığını temsil eder. Kılcal damar 25 pozitif kontrolü temsil eder. Anti-ERK antikor kullanılmıştır; ancak, herhangi bir uygun pozitif kontrol dahil edilebilir. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
4. CEI'nin 1.
- Önce CEI(Malzeme Tablosu)çözümleyicisini açın, ardından bilgisayarı açın. Yazılımı açın (Malzeme Tablosu)
- Analizciyi çevrimiçi sisteme bağlayın(Malzeme Tablosu). Bu, sorun giderme amaçları ve veri kurtarma için çalıştırılabilmek için çalıştırılabilmek için gerekli bir adımdır.
- Sol üst menüden Enstrüman'a tıklayın ve ardından Bağlan'ıtıklatın. Açılır menü olarak görünen enstrüman seri numarasını seçin. Bağlan'ı tıklatın.
- "Tsay" sekmesini seçin ve Yeni Tsay'ı seçin veya kaydedilmiş bir şablon seçin.
- Giriş giriş hesaplama parametreleri(Tablo 1) veya şu anda şablonu değiştirin. Dosya adını ve konumunu kaydedin.
- Çözümleyicideki yanıp sönen mavi renk göstergesinin düz mavi kaldığından emin olun.
- Açmak için turuncu kapının üstündeki gümüş metal düğmeye dokunun.
- Kılcal kartuşun ambalajından dikkatlice çıkarın. Üretici protokolünde açıklandığı şekilde kılcal kartuş ekleyin. Doğru yüklenirse, iç ışık "mavi"ye döner.
- Koruyucu mührü temizleme plakasından çıkarın. Hava kabarcıkları için önceden doldurulmuş kuyuları görsel olarak gözlemleyin. Gözlenirse, küçük bir pipet ucu ile pop (Uzun şaft P10 pipet ucu iyi çalışır).
- Plakayı titreterek plakayı yükleyin ve kapıyı kapatın. Bilgisayarda Başlat düğmesine tıklayın.
- Isıya duyarlı reaktifler ve numuneler içeren buz tepsisini, önceden doldurulmuş ikinci plakahazır olana kadar 4 °C'de karanlıkta yerleştirin.
- Reaktifleri/malzemeleri ikinci plaka için oda sıcaklığında bırakın.
5. CEI'nin 2.
NOT: Bu plaka fosforlu TDP-43 seviyelerini analiz etmek için ayarlanmıştır.
- 4 °C'de saklanan buz tepsisini çıkarın ve ilk plakanın tahmini tamamlanma süresinden 1 saat önce tezgahın üzerine yerleştirin. İkinci bir plaka ve kartuş alın.
- İkinci koşu için gerekli antikor seyreltmelerini hazırlayın ve buzda saklayın. Taze hazırlayın 1:1 luminol-S:peroksit çözeltisi (adım 3.12.8 yukarıda).
- Remix ve kısaca önceden doldurulmuş plaka yükleme için gerekli örnek karışımı ve reaktifler yeniden santrifüj. İkinci plakayı Şekil 1'egöre yükleyin. A-p(S409-410-2) TDP-43 antikor solüsyonu c kuyularında yükleyin.
- İlk çalıştırma tamamlandığında, ilk plakayı ve kartuşunu atın. Kartuşu çıkarın ve imha için bir keskin kapta yerleştirin. Çıkartmaları referans amacıyla plaka ve kartuştan saklayın.
- Yazılım dosyasını kapatın ve aynı şablonu yeniden seçin. Yazılım önceki çalıştırmadaki ayarları hatırlayacaktır. Gerektiğinde ek açıklamada herhangi bir değişiklik yapın (örn. birincil antikor değiştirin).
- Adımları 4.8-4.10'u yineleyin. Tüm 12-230 kDa master kiti ayırma modülü reaktifleri ve sarf malzemeleri koyun
- Üniversite yönetmeliklerine uygun olarak CEI örnek karışımı, antikor seyreltmeleri, 0,1 x numune tamponu ve luminol-S:peroksit karışımları üzerine sol akıtın.
6. Veri analizi
- Çalıştırma tamamlandıktan sonra, aşağıdaki kalite denetimlerinin gerçekleştirildiğinden emin olun.
- Yazılımda, Standartları Göster simgesini ve Grafik Görünümü sekmesini seçin. İç floresan işaretçi boyutlarına en yüksek hizalamalar için tüm 25 kılcal damarı kontrol edin. Kuvvet Standardı'nı seçerek veya yanlış tepeye sağ tıklayarak yanlış hizalamaları düzeltin, ardından Standart Değil'iseçin. Her yeni kılcal damar için bu denetimi gerçekleştirin.
- Örnekler ve Tek Görünüm simgesine tıklayın. Deney sekmesinde kılcal #1 (biyotinylated merdiven) seçin. Moleküler ağırlık belirteçleri için tepe hizalamagözden. Grafik Görünümü'ndeki tepeye tıklayın ve tepenin yanlış seçimi yazılım tarafından yapılıyorsa, Tepeyi Kaldır'ıseçin.
NOT: Örnek olarak, 12-230 KDa biyotinylated merdiven 12 kDa, 40 kDa, 66 kDa, 116 kDa, 180 kDa ve 230 kDa boyutlandırma zirveleri gösterecektir. Bu adım gerçekleştirilmezse örnek tepelerinin boyutlandırılması yanlış olur ve yanlış sonuçlar oluşturur. - Elektroforetik filmi görüntüleyin ve çalışma sırasında herhangi bir anormal göç olup olmadığını not edin.
- Daha fazla hesaplama için gerekli olan verileri (örn. moleküler ağırlık, tepe alanı, tepe yükseklik ve sinyal-gürültü [S/N]) dahil olmak üzere tepe tablosu elde edin. Grafik hakkında daha fazla bilgi sağlamak için Grafik penceresinin sağ üst köşesinde bulunan grafik ek açıklama araçları vardır.
Sonuçlar
Trombosit sitosolik protein konsantrasyonu ve primer antikor titrasyonuoptimizasyonu
Sinyaldeki değişiklikler trombosit sitosolundaki protein değişiklikleriyle doğru orantılı olduğundan, tsözde doğrusal bir dinamik trombosit sitosolik protein aralığı nın oluşturulması önemlidir. Tüm trombosit lysate karışımının tizinde kullanılması hedef proteinlerin (TDP-43 ve P(S409-412) TDP-43) sinyal yoğunluğunu azaltabilir ve yüksek arka plan sinyaline katkıda bulunabilir. Bu nedenle, bu tozta trombositlerin yırtılmasından sonra berrak süpernatant (sitosolik fraksiyon) kullanılmıştır (Şekil 2).
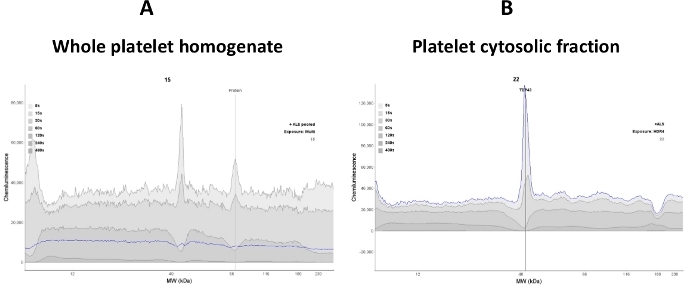
Şekil 2: Sinyal netliği numune kalitesine bağlıdır. (A) Tüm trombosit lisate homojen anti-TDP-43 antikor bağlanması ile müdahale; bu nedenle gürültülü bir elektrofefotogram gözlendi. (B) Trombosit sitosolik fraksiyonu, tüm lysat'ı santrifüje (30 dk için 16.000 x g) tmaruz bırakarak elde edilmiştir. Membranöz proteinlerin çoğu çıkarıldı; bu nedenle TDP-43 proteinine bağlanan anti-TDP-43 antikor gelişmiştir (mavi çizgi izi). Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
Trombosit sitosol protein konsantrasyonu için doğrusal dinamik aralık 0.2-0.8 mg/mL olarak belirlendi. Hem protein konsantrasyonu hem de primer antikor titrasyonunun tek bir tahkikte yapılabildiği bir tahsin şablonu benimsenmiştir(Şekil 3).
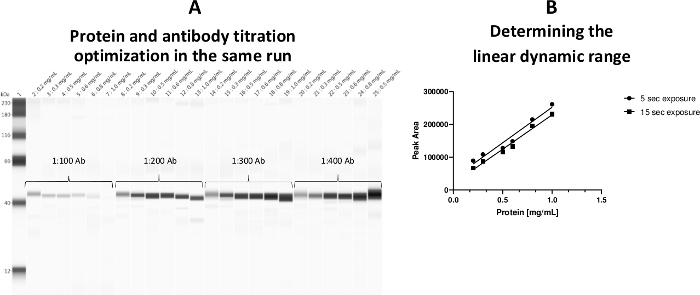
Şekil 3: Trombosit sitosol protein konsantrasyonu için lineer dinamik aralık. (A) Aynı çalışma sırasında hem protein konsantrasyonları hem de antikor titrasyonları tek bir tabakta optimize edildi. (B) Protein için lineer çalışma aralığı (0.2-0.8 mg/mL) oluşturuldu. 0.5 mg/mL protein yükü a-ERK antikoru ile pozitif kontrol olarak etiketlendi (kılcal damar 25). Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
Bu örnek hazırlama tüpügliserol içeriği daha az olması gerektiği unutulmamalıdır 20% (nihai), aksi takdirde yüksek gliserol konsantrasyonu olumsuz primer antikor bağlanmasını etkileyecektir.
Optimum pozlama süresinin belirlenmesi
Yazılımın eski sürümünde, optimum maruz kalma süresi protein konsantrasyonuna (mg/mL) karşı pik alan çizilerek belirlenmelidir. Yeni sürüm, yüksek dinamik aralık (HDR) algılama profili(Şekil 4)adlı yeni bir araç sağlar. Görüntü panelinin kullanılması, tüm pozlama sürelerini (örn. 5 s, 15 s, 30 s, 60 s, 120 s, 240 s, 480 s) birlikte görüntüleme seçeneği ni sağladı. Bilgisayar yazılımı tüm pozlama sürelerini analiz etti ve otomatik olarak en iyi pozlama süresini (HDR) belirledi. HDR algılama profili, CEI'nin daha fazla hassasiyeti nedeniyle önemli ölçüde daha geniş bir dinamik aralık sağladı, bu da daha geniş bir numune konsantrasyon aralığında daha iyi algılama ve nicellik anlamına geliyor. Ancak, kullanıcılar hala deneysel hedefi tatmin eden herhangi bir pozlama zamanı seçme seçeneğine sahiptir. Bu özellik kullanılarak TDP-43 proteini için optimum pozlama süresi saptadı. Tepe optimum pozlama süresini temsil eder (Şekil 4A). 1-512 s(Şekil 4B)arasında değişen dokuz pozlama süresi gözden geçirildikten sonra bu antikor için tek bir maruz kalma süresi (4 s) tanımlanmıştır.

Şekil 4: Hedef protein için yüksek dinamik aralık (HDR) algılama profili. (A) TDP-43 protein tepe hedef protein için optimum maruz kalma süresini temsil eder. a-TDP-43 Ab titrasyonu 1:300, trombosit sitosol protein konsantrasyonu 0.5 mg/mL idi. Yazılım tanımlı mavi çizgi optimum pozlama süresini gösterir. (B) Bu şekil, 1-512 s. arasında değişen dokuz pozlama süresini inceledikten sonra kullanıcı tanımlı tek pozlama süresini (4 s) temsil eder.
ALS hastalarının insan trombosit sitosollarında TDP-43 düzeyleri
Kan tabanı biyomarker gelişimi yapıldı. Als hastalarından elde edilen trombosit litosolik fraksiyonları kullanılarak iki dizi antikor (yani, Anti-TDP-43 [Pan] antikor, TDP-43 proteininin fosforlu türevlerini tanıyan bir antikor; burada a-P [S409/410-2] TDP-43 kullanılmıştır). Bu gösteride hastalığa özgü TDP-43 ve fosforilted türevi sunulmuştur (Şekil 5).
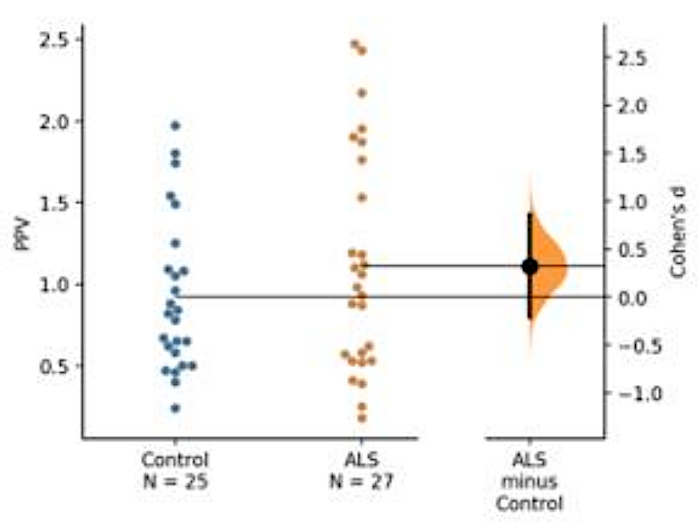
Şekil 5: TDP-43'ün tahmine dayalı fosforilasyon değerinin (PPV) temsili. Mutlak fosforilasyon miktarı TDP-43 ve pan TDP-43 tek başına ALS ve kontrol grupları arasında çok fazla fark göstermedi. Ancak PPV, iki grup arasında yeterli sayıda denek (ALS = 25, control = 27) nedeniyle istatistiksel bir fark olmamasına rağmen ALS kohortunda hafif bir artış olduğunu belirtmiştir. ALS ve kontrol grubu arasındaki düşük Cohen d değeri, küçük örneklem büyüklüğü nedeniyle iki grup arasında düşük etki boyutu göstermiştir (kontrol = 25, ALS = 27). Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
Toplam TDP-43 kalibrasyon eğrisi kullanılarak ölçüldü (Şekil 6)

Şekil 6: Standart kalibrasyon eğrisi. Standart bir eğri oluşturmak için ticari olarak satın alınan rekombinant TDP-43 protein konsantrasyonları kullanılmıştır. Her veri üç aylık ortalamayı temsil eder. Protein bandı yoğunlukları konsantrasyona bağlıydı (Inset). Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
Fosforilasyonlu TDP-43 proteininin sayısallaştırılması, bu proteinin ticari olarak kullanılamaması nedeniyle mümkün değildi. Bunun yerine, TDP-43'ün fosforilasyon türlerinin yüzdesini tanımlayan bir öngörülen fosforilasyon değeri (PPV) oluşturulmuştur. PPV, aynı örnek için aşağıdaki denklem kullanılarak iki sıralı CEI tahlillerinden belirlendi.

Havuzlu insan ALS trombosit sitosolik fraksiyonlarında intra-ve inter-run test değişkenliği test edilmiştir (Şekil 7)
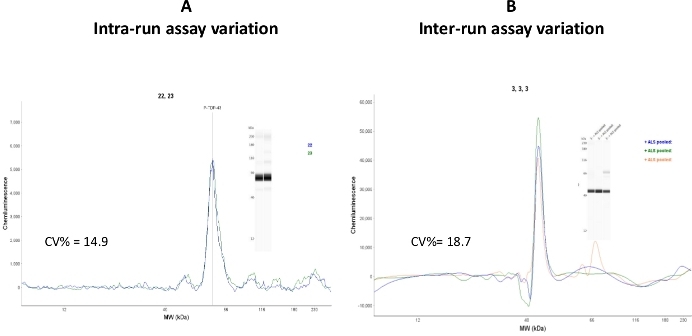
Şekil 7: Tsay varyasyonları. (A) Aynı örnekle yüklenen iki kılcal damar CEI tarafından analiz edildi ve intra-run test varyasyonu CV% = 14.9 olarak hesaplandı. (B) Aynı örnek üç farklı test gününde ve üç farklı test koşusunda analiz edildi. Inter-run tsay varyasyonu CV% = 18,7 olarak hesaplanmıştır. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
Intra-run (kapiller-kapiller varyasyon) katsayısı değişim değerleri kabul edilebilir aralıkta (CV% = 14,9) düşse de, inter-run değerlendirme değeri nispeten yüksekti (CV% = 18,7). Bu varyasyonun farklı kuralardan kılcal kartuşlar ve numune plakaları kullanılmasından kaynaklandığı yorumlanır. Aynı lot numarasına sahip CEI bileşenlerinde tekrarlanabilirlik çalışmalarının yapılması önerilir.
Tablo 1: CEI titreşme plakası yükleme şablonu. Bu tabloyu indirmek için lütfen buraya tıklayınız.
Tablo 2: İnteraktif numune hazırlama şablonu. Bilinmeyen örneklerden stok protein konsantrasyonu girdikten sonra, interaktif hücreler örnek karışımıhazırlamak için ne kadar hacim kullanılması gerektiğini otomatik olarak hesaplar. Bu tabloyu indirmek için lütfen buraya tıklayınız.
Tartışmalar
Kapiller elektroforetik tabanlı immünoassay şimdi yüksek iş artışı örnek analizi ve ilaç taramaları için tercih edilenyöntemdir 25. Küçük numune hacimleri, iyi optimize edilmiş deneme bileşenleri, kullanıcı dostu deneme platformu ve enstrümantasyon, reaktif harcamaları ve düşük CV yüzdesi birincil avantajları26,27. Proteinleri farklı tahnit yöntemleriyle ayırmak için çeşitli yöntemler bulunmasına rağmen, burada açıklanan antikor bazlı CEI, kan bazlı biyomarker gelişimi ile uğraşan küçük laboratuvarlar tarafından uyarlanabilir. Burada kullanılan CEI ispon teknolojisi, TDP-4328 ve fosforlu türevi5için güvenilir, tekrarlanabilir ve hassas ölçümler sağlar.
CEI sistemi aynı anda TDP-43 ve fosforilted türevlerini analiz etme ve saflaştırılmış veya rekombinant hedef protein varsa hedef proteinin doğrudan niceliklendirilmesini sağlayan bir çoklama seçeneği de sunmaktadır. Tam uzunlukta rekombinant TDP-43 proteini ticari olarak mevcuttur; ancak rekombinant fosforilasyonlu TDP-43 türevi değildir. Fosforlu TDP-43 ticari olarak mevcut olmadığından ALS hastalarında TDP-43 profilini değerlendirmek için bir tahmine dayalı fosforilasyon değeri (PPV) uygulanmıştır. Pan TDP-43 ve fosforlu TDP-43 miktarları kalıcı olarak florofor ile etiketlendi; bu nedenle, TDP-43 profili nicel bir birim (yani ng/mL, pg/mL, vb.) ile veya olmadan aynı kalır. TDP-43'ün ve fosforile türevlerinin (yani P [S409-410-12] TDP-43) mutlak miktarının belirlenmesi daha nicel bir ölçüm sağlasa da, PPV hesaplanması, ticari olarak mevcut olmadığı için rekombinant fosforlu TDP-43'ün standardizasyon ihtiyacını ortadan kaldırır.
CEI, bir tizin başarısız olması durumunda sorunu doğru bir şekilde tanımlamak için, denetim platformunda çeşitli denetim noktaları sağlar. Bu engelleri ortadan kaldırır ve daha iyi deneysel tasarım sağlar. Numune plakasının doldurulması dışında tam otomatik olarak test işlemi yapılır. Bu standart batı lekeleme analizi ile karşılaştırıldığında önemli bir özelliktir. Bu özellik, çalıştırıla-çalıştır'dan tutarlılık sağlar. Her laboratuvar benzersiz standart işletim prosedürleri olmasına rağmen, insan hatasını en aza indiren uygulamalara bağlı kalmak önemlidir. Örneğin, luminol içine peroksit ekleyerek enzimatik reaksiyon başlar ve luminol substrat tüketir, plaka yükleme hemen önce luminol-S / peroksit karışımı hazırlamak için önemlidir. Numunelerin ve birincil/ikincil antikorların hava kabarcığı olmayan plaka kuyularına yüklenmesi de kritik öneme karşı önemli adımlardır.
Ayrıca, plaka kuyularının hacmi küçük olduğundan ve kuyular arasında boşluk olmadığından, kullanıcılar pipetleme sırasında dikkatli olmalıdır, bu da her şey otomatik olduğundan en önemli adımdır. Örneklerin, antikorların ve diğer reaktiflerin yükleme sırası, testin tutarlılığı için önemlidir (Şekil 1). Plaka hazırlama işlemi yaklaşık 40-45 dakika sürer. Bu nedenle, ilk gerekli tsay bileşenleri ile plaka yüklemek ve pipetleme hemen önce luminol-S / peroksit karışımı hazırlamak tavsiye edilir. Bu şekilde, tutarlı bir reaktif ekleme dizisi vardır ve tutarlı parlaklık sinyali gücüne ulaşılacaktır. Öncelikle peroksit gücünü etkiler gibi, süresi dolmuş bir luminol-S / peroksit reaktif kullanılması tavsiye edilmez. Bölünmüş tampon sisteminin tanıtılmasında ve kimyasal ve deterjan uyumluluk aralığının da dahil olmak üzere son zamanlarda ki ilerlemesi taht kalitesini artırmış ve daha çoğaltılabilir ve öngörülebilir sonuçlar üretmiştir. Şimdi, aynı üreticiden yeni bir açılan analizör, aynı çalışmada kemilüminesans ve floresan konjuge antikorlarla etiketlenmiş örnekleri analiz etme özelliğine sahiptir. Bu yeni özellik, iki ayrı plakayı art arda çalıştırma gereksinimini ortadan kaldırır ve çalıştırılaç varyasyonunu ortadan kaldırır.
Tonist plakalar ortam sıcaklığında saklanmalıdır. Eğer 4 °C'lik bir buzdolabında ki titretplakaları muhafaza etmek için seçilirse, plakalar bir gece önce çıkarılmalı ve ortam sıcaklığına getirilmelidir. Yanlış yüklenen numune kuyularının, doğru numuneyi eklemeden önce kitte sağlanan tamponla kapsamlı (4-5 kez) yıkanması gerekir. Her birincil antikor ve biyolojik örnekler benzersizdir; bu nedenle, biyolojik sıvılarda hedef proteinler için numuneler analiz edilmeden önce antikor/protein optimizasyonu yapılmalıdır.
Burada, birincil antikor kuluçka süresi varsayılan olarak 30 dakika olarak belirlenmiştir. Sinyal zayıfsa, kullanıcılar floresan sinyali tükenmeden istenilen sinyal gücüne ulaşana kadar birincil antikor kuluçka süresini artırmayı düşünmelidir. İnsan trombositleri için hastalardan birleştirilmiş numuneler hazırlandı ve optimizasyon tahdidi olarak kullanıldı. Örnek birleştirme daha iyi hedef biyomoleküller arasındaki varyasyontemsil eder. CEI için toplam lysate veya total homojenate yerine net süpernatantların kullanılması önerilir.
Tüm trombosit lysate karışımında proteinin yüksek konsantrasyonu sinyal-gürültü oranını azaltabilir(Şekil 2). Bu, primer antikor bağlanmasını olumsuz etkilediği için, numunelerin tekrarlanan donma-çözülme döngülerinden kaçınılmalıdır. Bazı reaktifler CEI29ile uyumlu olmadığı için lysate tamponun içeriği önemlidir. Numune hazırlamadan önce üreticinin web sitesinde sağlanan uyumlu reaktiflerin listesini çapraz kontrol etmek tavsiye edilir. Bu, numune hazırlama için yüksek sıkılık koşullarını tolere etmeyen sistemin bir sınırlamasıdır. Daha sonra bireysel örnekleri analiz etmek için havuzlu numuneler kullanılarak test çalıştırma parametrelerinin (örn. birincil antikor seyreltme, protein konsantrasyonu, primer antikor kuluçka süresi, vb.) optimize edilmesi önerilir.
Açıklamalar
Yazarlar ProteinSimple, Inc dışında hiçbir rakip mali faiz beyan bu makalenin yayın maliyeti kapalı.
Teşekkürler
Bu araştırma, A.A. için verilen intramural bir hibe ile desteklenmiştir. Bu çalışma, NCATS'in Kansas Üniversitesi Frontiers Tıp Merkezi: Heartland Klinik ve Çevirisel Araştırma Enstitüsü'ne (#UL1TR606381) verdiği CTSA bursuyla desteklenmiştir. İçeriği sadece yazarların sorumluluğundadır ve NIH veya NCATS'in resmi görüşlerini temsil etmek zorunda değildir. Biz Kansas Üniversitesi Tıp Merkezi ALS kliniği için sağlıklı gönüllü ve ALS hastalardan kan örneği toplama için IRB onayı almak için kişisel müteşekkiriz. Yazarlar, emre Ağabaş'a müsveddeleri doğrulattığı için teşekkür eder.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 12-230 kDa Separation kit | ProteinSimple | SM-W004 | Contains pre-filled assay plate and 25-channel capillary cartridge |
| 3000G Thermocycler | Techne | FTC3G/02 | We used this thermocylcer for heating the sample mix |
| Anti-Mouse detection kit | ProteinSimple | 042-205 | Includes HRP-conjugated secondary antibody, buffer, luminol reagent, molecular weight marker |
| Anti-P(S409-410) TDP-43 antibody | ProteinTech | 22309-1-AP | Primary antibody that recognizes phosphorylated TDP-43 |
| Anti-P(S409-412) TDP-43 antibody | CosmoBio-USA | TIP-PTD-P02 | Primary antibody that recognizes phosphorylated TDP-43 |
| Anti-Rabbit detection kit | ProteinSimple | DM-001 | Includes HRP-conjugated secondary antibody, buffer, luminol reagent, molecular weight marker |
| Anti-TDP-43 (pan) antibody | ProteinTech | 10782-2-AP | Primary antibody that recognizes whole TDP-43 protein |
| Compass for SimpleWestern (SW) | ProteinSimple | Ver.4.0.0. | Compass for SW is the control and data analysis application for SimpleWestern instruments |
| Sonic Dismembrator; Model100 | Fisher Scientific | Sonicator. Used to rupture the cell membrane. This model is discontinued (Model XL2000-350) | |
| Table top centrifuge | Eppendorf | 22625004 | Model# 5810 with swinging plate bucket |
| Wes analyzer | ProteinSimple | 55892-WS-2203 | Performs the capillary gel electrophoresis |
Referanslar
- Blair, P., Flaumenhaft, R. Platelet alpha-granules: basic biology and clinical correlates. Blood Reviews. 23 (4), 177-189 (2009).
- Mercado, C. P., Kilic, F. Molecular mechanisms of SERT in platelets: regulation of plasma serotonin levels. Molecular Interventions. 10 (4), 231-241 (2010).
- Goubau, C., et al. Regulated granule trafficking in platelets and neurons: a common molecular machinery. European Journal of Paediatric Neurology. 17 (2), 117-125 (2013).
- Basu, S. S., et al. Human platelets as a platform to monitor metabolic biomarkers using stable isotopes and LC-MS. Bioanalysis. 5 (24), 3009-3021 (2013).
- Wilhite, R., et al. Platelet phosphorylated TDP-43: an exploratory study for a peripheral surrogate biomarker development for Alzheimer's disease. Future Science OA. 3 (4), 238 (2017).
- Worth, A. J., et al. LC-MS Analysis of Human Platelets as a Platform for Studying Mitochondrial Metabolism. Journal of Visualized Experiments. (110), e53941 (2016).
- Statland, J. M., et al. Rasagiline for amyotrophic lateral sclerosis: A randomized, controlled trial. Muscle and Nerve. 59 (2), 201-207 (2019).
- Charytan, D. M., et al. Safety and cardiovascular efficacy of spironolactone in dialysis-dependent ESRD (SPin-D): a randomized, placebo-controlled, multiple dosage trial. Kidney International. 95 (4), 973-982 (2019).
- Ugras, S. E., Shorter, J. RNA-Binding Proteins in Amyotrophic Lateral Sclerosis and Neurodegeneration. Neurology Research International. , 432780 (2012).
- Amador-Ortiz, C., et al. TDP-43 immunoreactivity in hippocampal sclerosis and Alzheimer's disease. Annal of Neurology. 61 (5), 435-445 (2007).
- Baloh, R. H. TDP-43: the relationship between protein aggregation and neurodegeneration in amyotrophic lateral sclerosis and frontotemporal lobar degeneration. FEBS Journal. 278 (19), 3539-3549 (2011).
- Buratti, E., Baralle, F. E. The molecular links between TDP-43 dysfunction and neurodegeneration. Advances in Genetics. 66, 1-34 (2009).
- Guo, W., et al. An ALS-associated mutation affecting TDP-43 enhances protein aggregation, fibril formation and neurotoxicity. Nature Structural Molecular Biology. 18 (7), 822-830 (2011).
- Geser, F., et al. Motor neuron disease clinically limited to the lower motor neuron is a diffuse TDP-43 proteinopathy. Acta Neuropathologica. 121 (4), 509-517 (2011).
- Neumann, M., et al. Ubiquitinated TDP-43 in frontotemporal lobar degeneration and amyotrophic lateral sclerosis. Science. 314 (5796), 130-133 (2006).
- Buratti, E., Baralle, F. E. TDP-43: gumming up neurons through protein-protein and protein-RNA interactions. Trends in Biochemical Sciences. 37 (6), 237-247 (2012).
- Fallini, C., Bassell, G. J., Rossoll, W. The ALS disease protein TDP-43 is actively transported in motor neuron axons and regulates axon outgrowth. Human Molecular Genetics. 21 (16), 3703-3718 (2012).
- Ayala, Y. M., et al. Structural determinants of the cellular localization and shuttling of TDP-43. Journal of Cell Sciences. 121, 3778-3785 (2008).
- Fiesel, F. C., Kahle, P. J. TDP-43 and FUS/TLS: cellular functions and implications for neurodegeneration. FEBS Journal. 278 (19), 3550-3568 (2011).
- Birsa, N., Bentham, M. P., Fratta, P. Cytoplasmic functions of TDP-43 and FUS and their role in ALS. Seminars in Cell and Development Biology. , (2019).
- Liachko, N. F., et al. CDC7 inhibition blocks pathological TDP-43 phosphorylation and neurodegeneration. Annals of Neurology. 74 (1), 39-52 (2013).
- Qureshi, A. H., et al. Proteomic and phospho-proteomic profile of human platelets in basal, resting state: insights into integrin signaling. PLoS One. 4 (10), 7627 (2009).
- Suominen, I., Koivisto, S. Increasing Precision When Pipetting Protein Samples: Assessing Reliability of the Reverse Pipetting Technique. American Laboratory. , (2011).
- . Pipetting tool box for life sciences Available from: https://www.mt.com/us/en/home/library/guides/laboratory-division/life-science/pipetting-toolbox-for-life-sciences.html (2019)
- Hale, L. J., et al. 3D organoid-derived human glomeruli for personalised podocyte disease modelling and drug screening. Nature Communication. 9 (1), 5167 (2018).
- Chen, J. Q., Wakefield, L. M., Goldstein, D. J. Capillary nano-immunoassays: advancing quantitative proteomics analysis, biomarker assessment, and molecular diagnostics. Journal of Translational Medicine. 13, 182 (2015).
- Moser, A. C., Hage, D. S. Capillary electrophoresis-based immunoassays: principles and quantitative applications. Electrophoresis. 29 (16), 3279-3295 (2008).
- Fourier, A., et al. Development of an automated capillary nano-immunoassay-Simple Western assay-to quantify total TDP43 protein in human platelet samples. Analytical and Bioanalytical Chemistry. 411 (1), 267-275 (2019).
- . Compatibility, S.W.S.A.B Available from: https://www.proteinsimple.com/technical_library.html (2017)
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır