Purificación de compuestos por recristalización
Fuente: Laboratorio del Dr. Jimmy Franco - Merrimack College
La recristalización es una técnica utilizada para purificar compuestos sólidos. 1 sólidos tienden a ser más soluble en líquidos calientes que en líquidos fríos. Durante la recristalización, un compuesto sólido impuro se disuelve en un líquido caliente hasta que la solución está saturada, y entonces el líquido se deja enfriar. 2 el compuesto entonces debe formar cristales relativamente puros. Idealmente, las impurezas que están presentes se mantendrá en la solución y no se incorporarán a los cristales crecientes (figura 1). Los cristales pueden eliminarse luego de la solución por filtración. No todo el compuesto es recuperable, algunos permanecerán en la solución y se perderán.
La recristalización no es considerada como una técnica de separación; por el contrario, es una técnica de purificación en el que se elimina una pequeña cantidad de una impureza de un compuesto. Sin embargo, si las propiedades de solubilidad de dos compuestos son lo suficientemente diferentes, la recristalización puede utilizarse para separarlas, aunque están presentes en cantidades casi iguales. Recristalización funciona mejor cuando la mayoría de las impurezas ya se han quitado por otro método, como extracción o columna cromatografía.
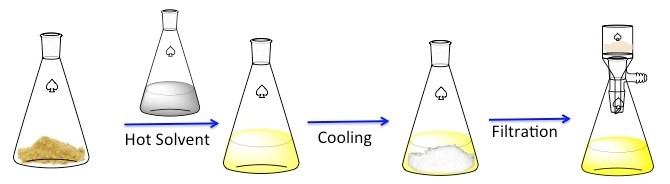
Figura 1. El esquema general para recristalización.
Una recristalización acertada depende de la elección adecuada del disolvente. El compuesto debe ser soluble en el solvente caliente e insoluble en el solvente mismo cuando hace frío. A los efectos de la recristalización, tener en cuenta 3% w/v la línea divisoria entre soluble e insoluble: Si 3 g de un compuesto se disuelve en 100 mL de un solvente, se considera soluble. En la elección de un disolvente, mayor será la diferencia entre solubilidad en caliente y frío solubilidad, el producto más recuperable de recristalización.
La tasa de enfriamiento determina el tamaño y la calidad de los cristales: enfriamiento rápido favorece pequeños cristales, y enfriamiento lento favorece el crecimiento de cristales grandes y generalmente más puros. La velocidad de recristalización es generalmente mayor a unos 50 ° C por debajo del punto de fusión de la sustancia; la máxima formación de cristales se produce a unos 100 ° C por debajo del punto de fusión.
Aunque los términos "cristalización" y "recristalización" a veces se usan indistintamente, técnicamente se refieren a diferentes procesos. Cristalización se refiere a la formación de un nuevo producto insoluble de una reacción química; Este producto entonces se precipita de la solución de reacción como un sólido amorfo que contiene muchas impurezas atrapadas. La recristalización no implica una reacción química; el producto crudo simplemente se disuelve en solución, y luego se cambian las condiciones para permitir que los cristales se vuelven a formar. Recristalización produce un producto final más puro. Por esta razón, los procedimientos experimentales que producen un producto sólido por cristalización normalmente incluyen un paso final de recristalización para dar el compuesto puro.
Realizar todos los pasos en una campana de humos para evitar la exposición a los vapores de disolvente.
1. selección de un solvente
- Coloque 50 mg de la muestra (N-bromosuccinimide) en un matraz Erlenmeyer.
- Agregar 0,5 mL de solvente (agua) que hierve. Si la muestra se disuelva por completo, la solubilidad en el solvente frío es demasiado alta para ser un solvente de recristalización buena.
- Si la muestra no se disuelve en el solvente frío, calentar el tubo de ensayo hasta que el solvente se reduce.
- Si la muestra no se disuelve completamente en este punto, añadir más solvente punto de ebullición mediante goteo, hasta que todo el sólido se disuelva. Si toma más de 3 mL para disolver la muestra en el solvente caliente, la solubilidad en este solvente es probablemente demasiado baja para que sea un disolvente de recristalización buena.
- Si la primera opción del disolvente no es un solvente de recristalización buena, probar con otros. Si no encuentra un disolvente único que funciona, probar con un sistema solvente dos.
- Si no puede encontrar un solo sistema solvente adecuado, un par de solvente puede ser necesario. Hora de identificar una pareja solvente, hay varias consideraciones claves 1) el primer solvente fácilmente debe disolver el sólido. 2) el segundo solvente debe ser miscible con el disolvente dest 1, pero tiene una solubilidad mucho más baja para el soluto.
- Como regla general "como disolver le gusta" lo que significa que los compuestos polares tienden a ser solubles en solventes polares y no polares compuestos suelen ser más solubles compuestos no polares.
- Pares de disolvente común (tabla 1)
- Asegúrese de que el disolvente tiene un punto de ebullición de al menos 40 ° C, por lo que hay una diferencia de temperatura razonable entre solvente y disolvente de la temperatura de ebullición.
- Asegúrese de que el solvente tiene un punto de ebullición por debajo de 120 ° C, por lo que es más fácil eliminar los últimos restos de solvente de los cristales.
- También asegúrese de que el punto de ebullición del solvente es menor que el punto de fusión del compuesto, por lo que el compuesto forma cristales sólidos en lugar de un aceite insoluble.
- Confirmar que las impurezas sean insolubles en el solvente caliente (para que puedan ser filtradas hacia fuera, una vez que se disuelve el compuesto) o soluble en el solvente frío (por lo que permanecen disueltos durante todo el proceso).
2. disolver la muestra en el solvente caliente
- Coloque el compuesto a ser recristalizado en un matraz Erlenmeyer. Se trata de una opción mejor que un vaso de precipitados, ya que los lados inclinados ayudar a vapores de solventes de trampa y retardar la velocidad de evaporación.
- Coloque el solvente (agua) en un matraz de Erlenmeyer aparte y agregar chips hirviendo o una barra de agitación para mantenerlo hirviendo suavemente. Calentar a ebullición sobre una placa.
- Añadir solvente caliente a un matraz a temperatura ambiente que contiene el compuesto en pequeñas porciones, se arremolinan después de cada adición, hasta que el compuesto se disuelva completamente.
- Durante el proceso de disolución, mantener la solución caliente en todo momento descansando sobre la placa, también. No agregue más caliente solvente del necesario - lo suficiente para disolver la muestra.
- Si una porción del sólido parece no disolverse, incluso después de añadir más solvente caliente, es probable debido a la presencia de impurezas muy insolubles. Si esto sucede, dejar de agregar solvente y hacer una filtración caliente antes de proceder.
- Para realizar una filtración caliente, doblar un trozo de papel de filtro en forma de cono acanalado y lo coloca en un embudo sin tallo de cristal.
- Añadir un exceso de 10-20% de disolvente caliente a la solución caliente para permitir la evaporación en el procedimiento.
- Verter la solución a través del papel. Si los cristales se empiezan a formar en cualquier momento durante el proceso, agregar una pequeña porción del solvente caliente para disolverlas.
3. enfriamiento de la solución
- Coloque el frasco que contiene el compuesto disuelto en una superficie que no conducen el calor lejos demasiado rápido, tal como una toalla de papel en un banco.
- Cubra ligeramente el matraz como se enfría para evitar la evaporación y evitar que el polvo caiga en la solución.
- Deje reposar el frasco hasta que se enfríe a temperatura ambiente.
- Una vez que los cristales se han formado, colocar la solución en un baño de hielo para asegurar que se obtiene la máxima cantidad de cristales. Las soluciones deben dejarse imperturbadas en el baño de hielo durante 30 min a 1 h, o hasta que el compuesto parece haber totalmente cristalizada de la solución.
- Si no hay formación de cristales es evidente, puede ser inducida por rayar el interior las paredes del matraz con una varilla de vidrio o mediante la adición de un cristal de la pequeña semilla del mismo compuesto.
- Si esto todavía no funciona, entonces demasiado solvente fue utilizada probablemente. Recaliente la solución, permitir que algunos del solvente a hervir apagado, luego enfriarlo.
4. aislar y secar los cristales
- Coloque el matraz frío que contiene el recién formados cristales en un banco.
- Cubra ligeramente el frasco para evitar la evaporación y evitar que el polvo caiga en la solución.
- Aislar los cristales por filtración de vacío, utilizando embudo de Hirsch o Büchner (abrazadera el matraz a un anillo de soporte de primera).
- Lave los cristales en el embudo Büchner con una pequeña cantidad de disolvente fresco, frío (el mismo disolvente utilizado para recristalización) para eliminar las impurezas que pueden pegarse a los cristales.
- Para secar los cristales, deja en el embudo de filtro y jalar aire a través de ellos durante varios minutos. Cristales pueden también ser secadas al aire por lo que les permite reposar destapado varias horas o días. Más eficientes métodos incluyen secado al vacío o colocar en un desecador.
| Solvente polar | Menos solvente Polar |
| Acetato de etilo | Hexano |
| Metanol | Cloruro de metileno |
| Agua | Etanol |
| Tolueno | Hexano |
Tabla 1. Pares de disolventes comunes.
En la figura 2se muestra un ejemplo de los resultados de la recristalización. Se han eliminado las impurezas amarillo presentes en el compuesto crudo, y el producto puro queda como un sólido blanco. La pureza del compuesto recristalizada ahora puede ser verificada por la espectroscopia de resonancia magnética nuclear (RMN) o, si se trata de un compuesto con un punto de fusión publicado, por lo parecido su punto de fusión es el punto de fusión de la literatura. Si es necesario, pueden realizarse múltiples recristalizaciones hasta que la pureza es aceptablemente alta.

Figura 2. 2a) un 2b (izquierda), compuesto crudo) recristalizado producto antes de filtración (medio) y 2 c) el mismo compuesto después de la recristalización (derecha).
La recristalización es un método de purificación de un compuesto mediante la eliminación de las impurezas que podrían mezclarse con él. Funciona mejor cuando el compuesto es muy soluble en un disolvente caliente, pero muy insolubles en la versión fría del mismo disolvente. El compuesto debe ser un sólido a temperatura ambiente. Recristalización se utiliza a menudo como un paso final de limpieza, después de otros métodos (tales como cromatografía extracción o columna) que son eficaces en la eliminación de grandes cantidades de impurezas, pero que no suba la pureza del compuesto final a un nivel suficientemente alto.
La recristalización es la única técnica que puede producir monocristales absolutamente puros y perfectos de un compuesto. Estos cristales pueden utilizarse para análisis de rayos x, que es la máxima autoridad en la determinación de la estructura y la forma tridimensional de una molécula. En estos casos, la recristalización puede proceder muy lentamente, a lo largo de semanas o meses, para permitir que el enrejado cristalino para formar sin la inclusión de impurezas. Vidrio especial es necesario para permitir que el solvente se evapora tan lentamente como sea posible durante este tiempo, o dejar que el disolvente se mezcla con otro disolvente en el que el compuesto es insoluble (llamado adición antisolvent) muy lentamente.
La industria farmacéutica también hace uso pesado de recristalización, ya que es un medio de purificación más fácilmente escalar de cromatografía en columna. 3 la importancia de la recristalización en aplicaciones industriales ha desencadenado educadores para enfatizar la recristalización en el plan de estudios de laboratorio. 4 por ejemplo, el medicamento Stavudine, que se utiliza para reducir los efectos del VIH, se aísla normalmente por cristalización. 5 a menudo, las moléculas tienen estructuras múltiples de cristal diferentes disponibles, por lo que es necesario para la investigación evaluar y entender que forma cristalina se aísla en qué condiciones, tales como el enfriamiento tipo, composición solvente y así sucesivamente. Estas formas diferentes de cristal podrían tener propiedades biológicas diferentes o sean absorbidas por el cuerpo a diferentes velocidades.
Un uso más común de recristalización es en la fabricación del caramelo de la roca. Caramelo de la roca se hace disolviendo azúcar en agua caliente hasta el punto de saturación. Palillos de madera se colocan en la solución y la solución se permite refrescar y se evaporan lentamente. Después de varios días, cristales grandes de azúcar han crecido en todo los palillos de madera.
- Mayo, D. W.; Pike, R. M.; Forbes, D. C., Microscale organic laboratory : with multistep and multiscale syntheses. 5th ed.; J. Wiley & Sons: Hoboken, NJ, p xxi, 681 p (2011).
- Armarego, W. L. F.; Chai, C. L. L., Purification of laboratory chemicals. 5th ed.; Butterworth-Heinemann: Amsterdam ; Boston; p xv, 609 p (2003).
- Ray, P. C.; Tummanapalli, J. M. C.; Gorantla, S. R., Process for the large scale production of Stavudine. Google Patents: (2011).
- Hightower, T. R.; Heeren, J. D., Using a Simulated Industrial Setting for the Development of an Improved Solvent System for the Recrystallization of Benzoic Acid: A Student-Centered Project. Journal of Chemical Education 83 (11), 1663 (2006).
- Rohani, S.; Horne, S.; Murthy, K., Control of Product Quality in Batch Crystallization of Pharmaceuticals and Fine Chemicals. Part 1: Design of the Crystallization Process and the Effect of Solvent. Organic Process Research & Development 9 (6), 858-872 (2005).
- Mayo, D. W.; Pike, R. M.; Forbes, D. C., Microscale organic laboratory : with multistep and multiscale syntheses. 5th ed.; J. Wiley & Sons: Hoboken, NJ, p xxi, 681 p (2011).
- Armarego, W. L. F.; Chai, C. L. L., Purification of laboratory chemicals. 5th ed.; Butterworth-Heinemann: Amsterdam ; Boston; p xv, 609 p (2003).
- Ray, P. C.; Tummanapalli, J. M. C.; Gorantla, S. R., Process for the large scale production of Stavudine. Google Patents: (2011).
- Hightower, T. R.; Heeren, J. D., Using a Simulated Industrial Setting for the Development of an Improved Solvent System for the Recrystallization of Benzoic Acid: A Student-Centered Project. Journal of Chemical Education 83 (11), 1663 (2006).
- Rohani, S.; Horne, S.; Murthy, K., Control of Product Quality in Batch Crystallization of Pharmaceuticals and Fine Chemicals. Part 1: Design of the Crystallization Process and the Effect of Solvent. Organic Process Research & Development 9 (6), 858-872 (2005).
Skip to...
Videos from this collection:

Now Playing
Purificación de compuestos por recristalización
Organic Chemistry
692.2K Views

Introducción a la catálisis
Organic Chemistry
33.7K Views

Montaje de un sistema de reflujo para reacciones químicas calientes
Organic Chemistry
159.3K Views

Realizar reacciones por debajo de la temperatura ambiente
Organic Chemistry
69.3K Views

Líneas de Schlenk para transferencia de disolventes
Organic Chemistry
41.1K Views

Desgasificación de líquidos con ciclos de congelación-bomba-descongelación
Organic Chemistry
55.0K Views

Preparación de equipos y reactivos anhidros
Organic Chemistry
78.1K Views

Separación de mezclas por precipitación
Organic Chemistry
154.3K Views

Extracción sólido-líquida
Organic Chemistry
234.0K Views

Evaporación rotatoria para eliminar solventes
Organic Chemistry
209.2K Views

Destilación fraccionada
Organic Chemistry
326.8K Views

Crecimiento de cristales para el análisis de difracción de rayos x
Organic Chemistry
32.1K Views

Performing 1D Thin Layer Chromatography
Organic Chemistry
284.8K Views

Cromatografía en columna
Organic Chemistry
352.9K Views

Espectroscopia de resonancia magnética nuclear (RMN)
Organic Chemistry
242.8K Views
ABOUT JoVE
Copyright © 2025 MyJoVE Corporation. All rights reserved