Method Article
测量电导率以研究火星条件下盐水的形成
* 这些作者具有相同的贡献
摘要
该方案的目的是监测盐的水合和盐水形成过程。电导率用作测量技术。实验是在温度、相对湿度和二氧化碳大气的模拟火星环境中进行的。
摘要
本文描述了一种方案,用于设计实验以研究火星条件下盐水的形成,并通过电导率测量监测该过程。我们使用宜居性的工程鉴定模型 (EQM):盐水、辐照和温度 (HABIT)/ExoMars 2022 仪器进行实验设置,但我们简要介绍了如何构建一个简单且廉价的电导率测量设置。该协议用于在模拟火星环境中校准盐潮解到盐水中的电导率测量值。在瑞典吕勒奥理工大学的 SpaceQ 火星模拟室中,模拟了火星温度(-70 °C 至 20 °C)、相对湿度(0% 至 100%)和压力(7 - 8 mbar)以及二氧化碳大气的条件。一对电极之间容纳的已知盐量的水合物形式以及测得的电导率主要取决于其含水量以及系统的温度和相对湿度。电导率测量以 1 Hz 进行,同时将盐暴露在不同火星温度下不断增加的相对湿度(以迫使盐通过各种水合物过渡)。为了进行演示,在火星 Oxia Planum(ExoMars 2022 任务的着陆点)重建了昼夜循环。
引言
行星探测的主要研究课题之一是水循环,但很难设计一个通用的、稳健的和可扩展的程序来监测大气与地面的相互作用。实验室模拟可以重建行星大气、表面和内部的相互作用。然而,从采购必要的设备到培训人员,这都带来了挑战。本文描述了一种方案,用于设计实验以研究在火星温度、相对湿度和二氧化碳气氛条件下盐水的形成,并通过电导率测量来监测该过程。我们还简要介绍了如何构建一种简单且廉价的电导率测量装置。该协议可能适用于在真空或其他行星大气中设计类似的实验。
盐水形成研究的重要性
吸湿性盐可以吸收大气中的水蒸气,形成液体溶液,这个过程称为潮解。这个过程在地球和火星表面的有利条件下产生盐水,这些盐水可能存在于某些时间和地点。当盐水在不利条件下脱水时,也称为风化的相反过程也是可能的。盐水在火星表面或地下可能存在,这对当前的地球和火星研究有几点影响。此外,盐可以水合、保持和释放水分子,这也会影响水循环和风化层的特性。
对于地球和火星,确定由于盐和盐混合物的潮解而有利于形成盐水的温度、相对湿度和压力条件,国际上的兴趣越来越大。对唐胡安池塘 (DJP) 流域附近黑暗陡坡水道的实地观察以及南极洲麦克默多干谷潮湿斑块的形成归因于富含氯化钙的沉积物中的盐水形成1。
这些结果也已通过模拟 -30 °C 至 15 °C 之间的低温和 20% 至 40% 之间的相对湿度的实验室实验得到验证2。智利阿塔卡马沙漠极度干旱核心的 Yungay 地区的含氯蒸发物可以吸收水分并滋生微生物生命 3。在 DJP 和地球上最干燥的地方(如阿塔卡马沙漠)发生的过程可能类似于火星的几项研究表明,类似的过程可能发生在今天的火星1、2、4、5、6、7、8、9、10、11、12、13,14,15,16。最近对乌尤尼盐沼(玻利维亚高原)的遥感观测描述了与从火星 17 号轨道观察到的过程类似的过程。尽管条件恶劣,但潮解驱动的盐水形成过程可以维持足够多的液态水,使细菌菌落在盐结核深处茁壮成长3。这是天体生物学家和行星科学家感兴趣的。
据报道,火星风化层中的潮解盐昼夜吸收和解吸大气中的水分 4,5。已经研究了火星上存在的高氯酸盐的盐水形成过程,观察了单个盐颗粒的相或水合状态的变化 1,9,18。在火星相关条件下,还进行了不同的盐水相关研究,以确定火星相关盐和盐混合物发生潮解和风化的相对湿度值 19,20,21。其他人使用这些实验条件来研究盐水在火星温度、相对湿度和二氧化碳大气中的蒸发速率22。
盐水形成检测和监测方法
有几种方法可以监测盐水形成过程。可见光波长的目视观察和图像是最简单的。称量盐以监测质量增加23.通常监测温度、相对湿度和压力等环境参数以正确解释观测结果。一些研究使用了湿度计。盐的吸湿性也可以用差分迁移率分析仪或电动天平来测量,但在相对湿度为 90%24 的情况下,它们的作不够准确。在最近的研究中,透射和扫描电子显微镜(TEM 和 SEM)得到了广泛的应用。这两种显微镜都具有环境池,可以研究水与单个盐颗粒的相互作用24。单个盐颗粒中的相变和转变通常使用实验装置中加入的光学、红外 (IR) 或拉曼光谱来检测 8,13,19,20,25。现有的光谱方法提供了良好的观察限和对相变的清晰检测,但它们不兼容于监测散装盐样品以及通过相变的中间阶段连续监测盐水形成过程。此外,基于激光的显微设备(如“拉曼显微镜”)价格昂贵,并且可能需要复杂的实验设置。
我们使用电导率作为测量技术。使用电导率进行测量以确定盐发生潮解时的相对湿度,其中得出的值与使用标准湿度计26 测定的值非常一致。Heinz 等人早些时候已经使用电导率研究了潮解盐水形成过程的时间序列27。在这里,他们使用了 JSC Mars-1a 模拟物和高氯酸盐或氯化物的混合物。导电技术还用于检测土壤中的液态或冰冻水28,29。这种方法的优点是,它既可以应用于中小型样品,只要它们包含在两个电极之间的空间中即可。
该协议可用于设计类似的实验,这些实验涉及控制真空中的温度和相对湿度或模拟外星大气,例如火星等。

图 1:实验装置的构建。 框图显示了一个简单的电导率测量装置,由电极、测量电路和 Arduino 等主要组件组成。请单击此处查看此图的较大版本。
盐水的电导率可以通过简单、廉价的设置来测量,如图 1 所示。材料 表中给出了构建设置的特定产品。该装置主要由一对相同尺寸的金属电极组成,这些电极之间相隔着已知距离,在该距离内容纳用于研究的盐或盐混合物。PT1000 电阻温度检测器可用于测量盐的温度。电极的一个平端可以焊接到屏蔽同轴电缆的每个端子上。同样,传感器的两个端子可以焊接到另一根屏蔽同轴电缆上。这些同轴电缆的另一端可以连接到电路上,分别测量电导率和温度。Arduino 板和简单的串行数据监视器可用于检索和存储数据。
在这个实验的背景下,我们使用了 HABIT/ExoMars 2022 仪器的工程鉴定模型 (EQM),这是将于 2022 年飞往火星的飞行模型 (FM) 的最接近复制品。HABIT 代表 HabitAbility:盐水、辐照和温度。它是 ExoMars 2022 表面平台 Kazachok 中的两个欧洲有效载荷之一,旨在研究火星着陆点 Oxia planum 的宜居条件。盐水观测过渡到液体实验 (BOTTLE) 是 HABIT 仪器的组成部分之一,旨在展示火星31 上的液态水稳定性。此处描述的协议用于校准电导率测量值,作为火星温度、相对湿度和二氧化碳大气条件下盐水形成的函数31。这用于检索 BOTTLE 的校准电导率测量值,这有助于检测火星上的液体盐水形成过程,这是其主要任务目标之一18。这里所说的校准是指实验级校准。通过确定每个电极对的几何电极常数和已知电导率31 的校准标准来执行仪器级校准。
研究方案
1. 测量电导率的实验装置的构建
- 选择电极的尺寸和电极对之间的距离。电极的尺寸取决于样品容器的尺寸,从而取决于盐的用量。下面提到的 HABIT BOTTLE 容器尺寸的尺寸可以作为样品容器的参考,盐的量可以从步骤 2.1 中参考。几何电极常数可以从公式 (1) 中导出。
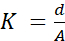 (1)
(1)
其中,d - 电极对之间的距离,以及
A - 电极面积(= 长度 x 宽度)。
几何单元常数 K 决定了测量设置敏感的电导率范围。例如,K = 1 cm-1 可以在 5 - 200, 000 μScm-1 范围内测量,而 K = 10 cm-1 可以在 10 μScm-1 - 1 Scm-1 范围内测量。电极对可能有多种级别。材料可以选择铜、铂、金等。在瑞典 Omnisys Instrument AB 工厂使用金和铂电极在盐水介质中通过直流电 (DC) 的几项长期实验表明,金电极在此作中具有更好的耐腐蚀性。
注意:HABIT 共有 16 个电极对,可以在尺寸为 25 mm x 15 mm x 15 mm(长 x 宽 x 高)的容器中研究三个水平的六种不同盐(两个角池仅用低电极对和中电极对测量)。BOTTLE 使用三级尺寸的电极对:低:1.6 x 0.4,中:1.6 x 0.2,高:1.6 x 0.2,在 2.5 cm 处分离,产生 3,9062 cm-1 和 7.8125 cm-1 的电极常数。使用光学测量系统(例如 Mitutoyo MF 176)进行测量。 - 准备一个具有平坦表面的容器来盛放盐进行研究,如图 1 所示。容器尺寸可以根据电极的几何尺寸和容纳盐的电极对之间的距离来选择。可以适应多个容器配置。容器可以用 PLA 进行 3D 打印,或者最好用铝或其他金属铣削,应防止因蒸汽或液体通过壁泄漏而损失水分。
- 准备环氧树脂 2216 树脂涂层并将其涂在容器壁上。放置 1 小时,使其凝固并在 66 °C 下固化涂层容器 2 小时。
注意:环氧树脂涂层可以溶解在溶剂中并喷涂以获得最佳效果。 - 将电极对放在容器的相对壁上,并用已经涂布的环氧树脂 2216 将它们粘合在一起。
- 使用长屏蔽同轴电缆,将一侧的末端焊接成对每个电极的接触点。
- 将屏蔽同轴电缆的另一端连接到电导率测量电路的两个端子。
注意:可以构建一个简单的电导率测量电路,其中一个端子连接到交流电压源,以产生指定频率的电脉冲,另一个端子连接到分压器电路,以读取电极对上的电压降。Arduino 的数字输出引脚可用于脉宽调制 (PWM) 模式,以产生所需的交流电压。交流电压用于防止电极腐蚀。电极对上的电压降也可以使用 Arduino 的模拟输入引脚及其内置的 10 位模数转换器 (ADC) 来测量。其他商业电路也可用。 - 同样,使用导热膏将 PT1000 电阻温度检测器 (RTD) 粘在容器的一壁上。
- 使用另一根长屏蔽同轴电缆将一侧连接到 PT1000 传感器的两个端子,另一侧连接到温度测量电路。
注意: 可以构建一个简单的温度测量电路,其中一个端子连接到直流电压源,另一个端子连接到分压器电路,以读取 PT1000 传感器上的电压降,这可以通过 Arduino 的模拟输入引脚及其内置的 10 位模数转换器 (ADC) 进行测量。其他商业电路也可用。- 要为实验设置准备 HABIT 仪器,请将 BOTTLE 组件和电子单元 (EU) 之间的电缆连接分开。然后,拧下 BOTTLE 的 8 个 M3 螺栓,取下顶盖和 HEPA 过滤器支架,以露出六个打开的细胞。在加入盐进行研究之前,清洁 BOTTLE 的细胞和电极,最好使用电极清洁溶液和无菌棉签去除任何颗粒或液体。
- 在加入盐之前,使用一组具有已知电导率值的校准标准品对装置的电导率测量进行校准,以确定每个电极对的校准函数系数。当 BOTTLE 在热真空室中承受真空条件并保持在 25 °C 时,使用 0.0364 μScm-1(作为零点或干点)的电导率测量值作为系统的绝对零电导率。此外,使用两个校准标准品:84 μScm-1 和 1413 μScm-1 来得出两点校准函数,如公式 (2) 所示。
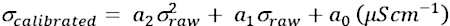 (2)
(2)
其中,σcalibrated - 校准的实际电导率,
测量σ - 原始测量的电导率,以及
a2,a 1,a 0 - 多项式常数 - 将设置测量的原始电导率拟合到衍生的校准函数中,以实现真正的电导率测量。
注意:在将系统温度保持在 25 °C 的同时实现初始校准。 然而,随着实验过程中温度的变化,电导率值也会发生变化。由于推导出不同温度下的温度与电导率函数变得复杂,因此我们只使用温度数据来确定盐水的相态。Nazarious 等人 31 详细讨论了这方面。
2. 处理潮解盐样品
- 称量特定量的盐或考虑用于研究的样品。我们在单独的容器中称取四种不同盐的各 1.5 克:氯化钙 CaCl2、硫酸铁 Fe2(SO4)3、高氯酸镁 Mg(ClO4)2 和高氯酸钠 NaClO4。
注意:一些盐类,尤其是高氯酸盐,具有腐蚀性,因此必须避免与皮肤或眼睛接触。- 处理盐时,请使用适当的化学服装、护目镜和丁腈手套。如果接触到皮肤或眼睛,请立即用大量清水冲洗并就医。
注:除盐外,我们还在四个容器中分别添加了 0.75 g 海藻酸钠盐(高吸收性聚合物,SAP)并充分混合,以获得均匀的盐-SAP 混合物。我们使用 SAP 作为固化剂作为安全措施,以避免盐水通过毛细作用上升并从飞行模型仪器中流出。盐从大气环境中吸收气态水,而 SAP 则从液态吸收水,即与盐的液态盐水接触后吸收水。添加 SAP 纯粹是由于在地球条件下储存盐的工程限制(在 2022 年 ExoMars 发射之前),并且对实验本身的意义不大。因此,电导率测量是盐 + SAP + 水混合的结果,这是预期的。由于本实验的目标是监测整个系统中水的吸收情况,因此从盐+SAP 的干燥状态到水合状态的电导率变化被认为与解释有关。还对相同的盐 + SAP 组合进行了校准程序。 - 使用与 HABIT/ExoMars 仪器的 BOTTLE 组件飞行模型相同的盐和 SAP 混合物和砝码。
- 处理盐时,请使用适当的化学服装、护目镜和丁腈手套。如果接触到皮肤或眼睛,请立即用大量清水冲洗并就医。
3. 在实验装置中加入盐样品
- 小心地将步骤 2 中先前称量的全部盐转移到实验容器中。
注意:将先前称量的盐-SAP 混合物按以下顺序小心地转移到 BOTTLE 的四个单元中:细胞 2:氯化钙 CaCl2,细胞 3:硫酸铁 Fe2(SO4)3,细胞 4:高氯酸镁 Mg(ClO4)4,细胞 5:高氯酸钠 NaClO4。Cell-1 和 Cell-6 留空。- 在 BOTTLE 的飞行模型中遵循相同的顺序,因此此配置和实验旨在校准和解释其在火星上的作。
- 调平盐的顶面,使其覆盖电极。选择盐的量以达到此标准。
注意:BOTTLE 的每个盐-SAP 混合物总重 2.25 克,并覆盖每个电池中的低电极。选择这个量是为了使形成的盐水不会溢出。 - 使用 HEPA 过滤器覆盖容器顶部。这将允许盐与模拟环境的环境相对湿度相互作用。
注意:使用带有支架框架的尼龙基 HEPA 过滤器覆盖 BOTTLE 中的盐-SAP 混合物,并使用 8x M3 螺栓固定 BOTTLE 的顶盖。
4. 在模拟室中安装实验装置
- 将实验容器放入模拟室32 中。确保腔室的工作台和容器之间有良好的热接触。
- 将电导率和温度测量电路放在腔室外。这将避免电路中任何可能影响测量的温度感应噪声。
- 通过模拟室的中间连接器在测量电路和容器之间建立电源和数据连接。
注意:BOTTLE 使用专用的分体电缆将其 EU 的 2x DB-9 连接器连接到腔室的内部 DB-25 连接器。分体式电缆是专门用于此目的的定制电源和数据连接电缆。从腔室的 DB-25 连接器的外部,另一根带有电源连接的分体电缆插入直流电源,并将 2 个 USB 数据连接到安装了 HABIT EQM LabView 软件的笔记本电脑。
5. 模拟室的控制

图 2:模拟室的控制装置32. 火星模拟室及其用于控制温度、相对湿度和二氧化碳压力的各种系统。此外,还会显示电源和数据连接插座。请单击此处查看此图的较大版本。
- 将工作台的温度保持在 20 °C 和 -30 °C 之间
注意:工作台的温度根据图 2 所示的协议使用液氮 (LN2) 馈入系统进行调节。最初,腔室保持在实验室环境温度下。- 打开 LN2 流量的阀门。温度将开始降低。
- 在反馈控制器上设置所需的温度。安装在工作台上的 PT100 温度传感器充当反馈回路。
- 达到所需温度后,关闭阀门以关闭 LN2 的流量。
- 保持二氧化碳压力
- 打开真空泵,直到腔室内的压力变为真空。
- 一旦真空室处于真空状态,关闭真空泵,并向真空室注入 CO2 气体,直到其压力达到 7-8 mbar。
- 保持相对湿度
- 使用安装在腔室上的不锈钢世伟洛克注射器以 0.5 mL 的增量注入水。这将逐渐增加相对湿度。
注意: 注射器反过来连接到球阀,因此注射器可用于多次注射水。 - 确保压力在限制范围内。否则,通过调节阀门来释放压力。
- 使用安装在腔室上的不锈钢世伟洛克注射器以 0.5 mL 的增量注入水。这将逐渐增加相对湿度。
6. 电导率与相对湿度实验

图 3:电导率与相对湿度实验。 实验方案中用于执行校准实验的步骤,以推导出电导率与相对湿度的关系。请单击此处查看此图的较大版本。
- 打开旋转真空泵以冲洗出腔室内的所有空气。腔室内的压力将降低到 10-3 mbar 的数量级。
注意: 相对湿度将接近零。腔室工作台的环境温度约为 20 °C。 随着压力的降低,电导率和 BOTTLE 温度可能会升高(潮解是一种放热反应)。 - 小心地从气瓶中注入二氧化碳气氛,以保持 7 到 8 mbar 之间的压力。
- 将工作台温度设置为某个值,以便测量容器温度的 PT1000 将记录 20 °C。
- 在 20 °C 下等待约 5 分钟以达到平衡,然后按照步骤 7 开始数据采集。
- 使用注射器系统将水缓慢注入腔室内,并保持相对湿度为 10%,等待 5 分钟以达到平衡。如果在增加相对湿度时压力升高,请调整旋转真空泵阀以去除多余的气氛。
- 减慢将相对湿度增加到 20%、30%、40%、50%、60%、70%、80%、90% 和 100%。在每个相对湿度值下,保持约 5 分钟以达到平衡,然后按照步骤 7 开始数据采集。
注意:根据 图 3 所示的协议,一组校准实验到此结束。 - 盐样现在可能已经形成了盐水。丢弃容器中的盐样品。
- 更新盐样品,用于步骤 8 之后的下一个实验。
- 同样,降低工作台温度,将容器温度保持在 15 °C、10 °C、5 °C、0°C、-5 °C、-10 °C、-15 °C、-20 °C、-25 °C 和 -30 °C。 在每个停止点,重复步骤 6.5 到 6.8 以测量盐样品的电导率。
注意:作为一项安全功能,低于 -33 °C 时,BOTTLE 加热器将启动以将温度保持在 -30 °C 和 -33 °C 之间。 因此,我们将实验运行到 -30 °C。 但人们可能会选择较低的温度。 - 通过关闭实验,释放真空并打开腔室前门,让实验室环境空气混合并自然提高容器温度,可以实现从最冷的温度 -30 °C 上升到环境温度。对于其他数据,可以选择让腔室内的温度自然升高。不过,这将是一个非常缓慢的过程,可能需要 7-10 个小时。
7. 记录和保存数据
- 使用 Arduino 的内置串行监视器或第三方串行监视器软件(例如 Teraterm、Realterm 等)。
- 将 Arduino 配置为以 1 Hz 的频率连续读取 1 小时,然后是每小时的前 5 分钟。这可能适用于步骤 9 中描述的 Marian 昼夜模拟。
- 根据测量电路的规定设置直流电源电压。
注意:HABIT 的电源线连接到 28 V 的直流电源,并将 2 个 USB 数据连接到安装了 HABIT EQM LabView 软件的笔记本电脑。该软件仅支持 Windows 10。 - 输入串行 COM 端口用于数据连接并执行 Arduino 程序。
注意: 请参阅 设备管理器 以识别正确的 COM 端口。 - 在前 100 秒内采集数据,然后通过关闭串行监视器停止数据采集。请记住从 Arduino 串行监视器窗口复制数据。
- 打开文本编辑器并粘贴复制的数据,以另存为 .txt 或 .csv 数据文件格式,以便更轻松地使用 MATLAB 或 Python 进行后处理。
注意:第三方软件可能具有自动保存功能。 - 为数据文件命名以匹配实验描述。
- 对于下一组数据采集,首先通过关闭和打开直流电源来重启实验设置,然后重复步骤 7.3 到 7.7。
- 对于 HABIT EQM LabView 软件:在 “主要 ”选项卡中,输入两个 COM 端口 COM 端口 1 和 COM 端口 2,每个端口对应于一个 USB 数据连接。单击 Connect(连接 ),然后单击 Start(开始 ),以 1 Hz 的频率采集数据。记录前 100 秒的数据。
- 通过单击 Debug 选项卡和 Open on Real-time data view 来查看获取的数据。这将打开一个新窗口,其中包含多个选项卡,每个选项卡对应于 HABIT 仪器的不同测量值。对于此实验,我们关注选项卡:“Cell 2”、“Cell 3”、“Cell 4”、“Cell 5”、“EU Temperature”和“CU Temperature”。数据将以十六进制格式的“Log.txt”保存在笔记本电脑的“C:\LABVIEW\Data”文件夹中。重新运行软件将替换 “Log.txt” 文件中的现有数据。
8. 更新盐样品
注意:遵循此步骤为每个新实验引入干盐样品。
- 停止实验并小心地断开电缆,然后从模拟室中卸下实验容器。
- 小心地从容器中取出 HEPA 过滤器和盐样品,并将它们放入单独的生物危害密封袋中。
注意:高氯酸盐和其他盐类不安全,不能用流水处理在水槽中或一般废物处理。必须小心将它们包装在生物危害密封袋中,并按照化学废物处理规范进行处理。如果研究了其他样品,例如风化层样品或聚合物等,则可以按照这些产品的安全数据表 (SDS) 的建议处理废品。 - 轻轻清洁并重置容器以进行下一次实验。
- 按照步骤 2 到 4 将盐样品填充到容器中,然后将其放回模拟室内。
9. 模拟火星上的昼夜循环

图 4:火星上昼夜循环的模拟。 执行火星溶胶模拟的实验方案的步骤。请注意,步骤 6 和 7 是从图 3 切换而来的,因为对于火星昼夜模拟,相对湿度在温度降低(昼夜转换)之前最初设置在 80% 以上。请单击此处查看此图的较大版本。
- 按照步骤 2 到 4 设置演示实验。
- 按照步骤 7 设置实验的数据记录,并以 1 Hz 的频率每小时采集第一个小时和前 5 分钟的数据连续数据。
注意:HABIT 使用这种时间表以良好的频率进行监测,并防止电极过度暴露于交流电中。 - 在室内模拟 Oxia Planum, Mars 的环境条件
注意:我们使用瑞典吕勒奥理工大学的 SpaceQ 火星模拟室进行演示,如图 4 所示。
注意:Oxia Planum 是 ExoMars 2022 在火星的计划着陆点。- 打开旋转真空泵以冲洗出腔室内的所有空气。内部压力将降低到 10-3 mbar 的数量级。
注意: 相对湿度将接近零。腔室工作台的环境温度约为 20 °C。 随着压力的降低,电导率和容器温度可能会升高(潮解是一种放热反应)。 - 小心地从气瓶中注入二氧化碳气氛,以保持 7 到 8 mbar 之间的压力。
- 使用世伟洛克注射器在腔室内缓慢注入水,以逐渐增加相对湿度。如果压力增加超过所需限值,请小心调整旋转真空泵阀以去除多余的气氛。
- 在大约 7% 的相对湿度下,将二氧化碳大气压保持在约 8-8 mbar。
- 缓慢打开 LN2 馈入系统值以降低工作台温度,以模拟火星昼夜转换。观察工作台温度和容器温度的可能差异。
注意: 可以通过调整 LN2 流速来控制温度下降的速度。 - 让温度下降,直到容器温度读数为 -30 °C(工作台温度为 -70 °C),然后关闭 LN2 液流。
注意:作为一项安全功能,低于 -33 °C 时,BOTTLE 加热器将启动以将温度保持在 -30°C 和 -33 °C 之间。 因此,我们将实验运行到 -30 °C。 但人们可能会选择较低的温度。 - 工作台和容器将缓慢升温至实验室环境温度(昼夜转换)。相对湿度也可能增加,压力也会增加。请记住作旋转真空泵阀以去除多余的压力。
注:这里,相对湿度是指将空气中的水蒸气量相关联。由于相对湿度传感器测量的是空气,因此可以合理地说,水分含量越高,相对湿度越高。最初,当工作台冻结到 -30 °C 时,水蒸气在工作台上冷凝并冻结,当温度升高时,这些冷凝水在火星压力下蒸发,并被相对湿度传感器感应为空气中的水分。因此,环境空气相对湿度的变化是由于水态的变化,以及当温度升高时,霜以蒸汽的形式从工作台释放到空气中。 - 当容器温度达到 20 °C(类似于工作台温度)时,关闭实验,释放真空并打开腔室前门以移除实验装置。
- 打开旋转真空泵以冲洗出腔室内的所有空气。内部压力将降低到 10-3 mbar 的数量级。
结果
以 HABIT 获取的数据为 HEX 格式,并在分析前转换为 ASCII 格式。校准实验建立了在不同火星温度和相对湿度条件下对应于四种不同盐-SAP 混合物的水合物形式的电导率值之间的关系。图 5A 显示了空气在 25 °C 时的关系,四种不同的盐-SAP 混合物、氯化钙 CaCl2-SAP、硫酸铁 Fe2(SO4)3 - SAP、高氯酸镁 Mg(ClO4)2 - SAP 和高氯酸钠 NaClO4 的关系- SAP 的我们观察并编目了:i) 电导率测量随温度的变化,以及 ii) 空气和盐-SAP 混合物的电导率范围随相对湿度的函数。考虑到检索到的电导率、温度和相对湿度条件,这些信息对于解释火星上 BOTTLE作中盐-SAP 混合物的水化水平至关重要。
在图 5A 中,我们观察到空气的电导率和相对湿度之间存在直接相关性。由于以 0.5 mL 的增量注入水增加了腔室内的相对湿度,因此空气增加了其相对湿度,就像在火星条件下发生的那样。电导率显着增加。由于靠近冷藏台,下电极可能更冷,这反过来又导致更高的 RH 和更高的 EC。对于本实验中火星压力下温度和相对湿度的给定组合,我们还记录了相对湿度为 59% 时空气的最大电导率(非温度补偿)。图 5B-5 E 显示,所有四种盐-SAP 混合物都在不同程度上捕获了水。对于氯化钙和高氯酸钠,观察到电导率从 RH=0% 逐渐增加,在硫酸铁和高氯酸镁的情况下,RH=50% 左右增加。所有盐-SAP 混合物的最大值为 85%,这是我们在腔室内达到的最大值。
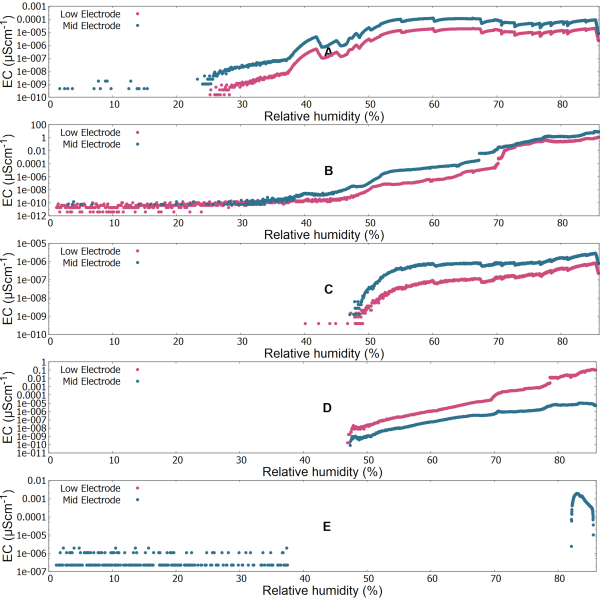
图 5:25 °C 时电导率与相对湿度 (1% - 85%) 的函数关系。(A) 空气、(B) 氯化钙、(C) 硫酸铁、(D) 高氯酸镁、(E) 高氯酸钠的电导率以 10 为基数的对数刻度表示。电子装置 (EU) 记录的平均温度为 25.27 °C(最低:24.12 °C,最高:25.95 °C),集装箱装置 (CU) 记录的温度由于水捕获的放热性而从 19.6 °C 上升到 32.91 °C。工作台平均温度为 19.11 °C,平均空气温度为 19.16 °C。请点击此处查看此图的较大版本。
盐的电导率取决于多种因素。在实验结束时,我们注意到硫酸铁的水合度最低(见 图 7),显示电导率值低于空气。电极之间的电导率对与 salt+SAP 混合物的接触区域也很敏感。一些颗粒材料(包括 SAP)可能比潮湿空气更好的隔离器。空容器中的空气具有足够的水分含量,可以自由移动,导致比硫酸铁更高的导电性(见 图 5A),硫酸铁在吸收足够的水方面没有贡献,无法显示显着的导电信号(见 图 5C)。我们还在实验结束时观察到空容器中的水滴,表明电极之间的空气在某个时候是饱和的,可以形成雾,其中一些雾在侧面凝结,如图 5A 所示。没有低电极电导率可能意味着与下电极接触的盐颗粒完全冻结(由于它与腔室的工作台直接接触,仪器底部最冷),没有显示出导电性。
作为 2021 年初成功着陆后在火星上运行 HABIT 的示范实践,我们在 ExoMars 2022 任务的计划着陆点 Oxia Planum 模拟了一个 Sol 的环境条件。获得的结果模拟了 BOTTLE 在火星上的昼夜循环,并提供了相关条件下的第一手数据。图 6 显示,在模拟火星昼夜循环期间,在所有盐-SAP 混合物中都观察到潮解。图 6C-6 F 显示了四种不同盐-SAP 混合物的电导率值,分别是氯化钙 CaCl2-SAP、硫酸铁 Fe2(SO4)3-SAP、高氯酸镁 Mg(ClO4)2 - SAP 和高氯酸钠 NaClO4-SAP。
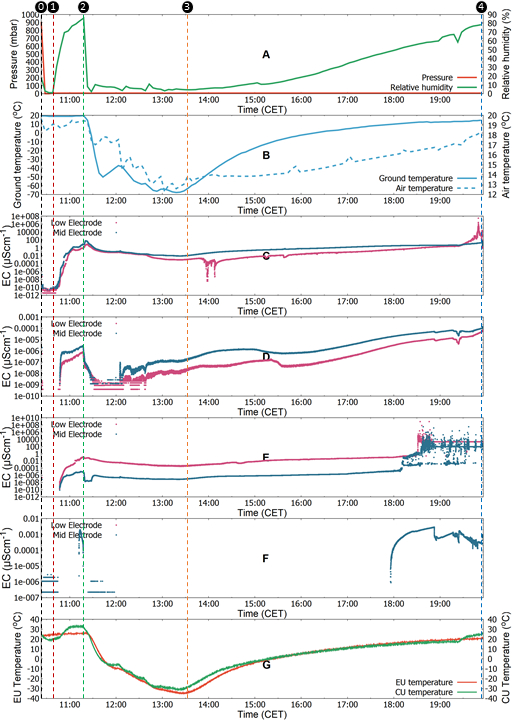
图 6:火星溶胶模拟的校准电导率测量值。(A) 压力和相对湿度,(B) 地面和空气温度,(C) 氯化钙,(D) 硫酸铁,(E) 高氯酸镁,(F) 高氯酸钠电导率(以 10 为基数的对数刻度),以及 (G) 电子单位 (EU) 和容器单位 (CU) 或 BOTTLE 温度。带有圆圈数字的垂直线表示模拟的各个阶段。0-1:抽出空气以获得真空和二氧化碳注入,以在恒温下保持 7-8 mbar 的压力,1-2:注水以增加恒温下的相对湿度,2-3:工作台冷却开启以降低温度(昼夜转换),伴随着相对湿度降低,以及 3-4:工作台冷却关闭以提高温度(昼夜转换), 伴随着相对湿度的增加。请单击此处查看此图的较大版本。
电导率的初始上升可能归因于相对湿度保持较高的压力快速下降,加速了水捕获过程,然后混合物中剩余的水脱气。这也与盐捕获水过程的放热性一致。电子单元 (EU) 和 BOTTLE 中的温度升高可能是快速减压(在恒定体积下)和盐水相互作用放热行为的组合。在 13:00 左右观察到的压力下降可能与达到工作台中的最低温度有关,这也与 RH 的小幅上升相吻合。在较冷的温度下,工作台的行为就像一个水槽,冻结了水滴,因此空气的相对湿度很低。在火星昼夜转换的这一阶段,电导率曲线中的迹象不太明显。但是,在昼夜转换期间,当温度升高,相对湿度升高时,盐-SAP 混合物开始稳定地捕获水分,实验后期导电性的增加也反映了 BOTTLE 温度的突然升高。最终的电导率值表示四种盐-SAP 混合物中每一种的水分捕获程度,如图 7 所示。所有的盐-SAP 混合物都捕获了水,特别是氯化钙盐-SAP 混合物产生了液体盐水。CaCl2 盐水的最大电导率值为 ̴100 μScm-1,与文献31 一致。

图 7:盐-SAP 混合物的图像。 (A) 在火星太阳模拟之前和 (B) 之后。从左到右:初始条件:氯化钙、硫酸铁、高氯酸镁、高氯酸钠各 1.5 g,每种盐中含 0.75 g SAP。左上角的氯化钙产生液态盐水,也显示出 ̴100 μScm-1 的相关电导率值。所有其他盐-SAP 混合物也捕获了大量的水,在图像中看起来是湿的。请单击此处查看此图的较大版本。
讨论
这是在真空或火星压力条件下表征盐水形成过程的电导率的首次尝试。该实验的关键要素是用火星模拟室模拟火星昼夜循环,以研究盐分。盐潮解的结果显示为代表性结果,而重点更多地放在实现模拟火星环境所需的条件上。通过第一个实验,我们现在了解了手稿讨论部分提到的腔室的过程和局限性。在未来的实验中,我们将遵循此协议进行与火星过程相关的各种科学实验。早期的研究已经在环境实验室压力 27,28,29 中进行了电导率测量。在较低压力下进行测量是一项挑战,因此需要修改用于地球压力条件的协议。在之前的环境压力下在气候室中进行校准活动期间,在每组实验之前,通过添加规定量的盐和水来制备不同的水合物,以得出不同火星温度下电导率和盐水合物形式之间的关系31。但是,在火星压力下,用于形成水合物的添加水最终会在降低压力时脱气,因此我们从干盐-SAP 混合物开始每个实验,并调节相对湿度以通过各种水合物形式过渡。
过去使用拉曼光谱方法监测盐水形成过程的研究,通常是在环境池中使用盐颗粒的单个颗粒进行,并观察拉曼光谱O-H 拉伸区域的相变 1,9,18。盐水形成过程的电导率表征被认为比现有的拉曼光谱对中间相变更敏感,并提供了盐水形成过程的连续时间序列27。从我们的实验中,我们还证明了电导率是散装盐样品的可行测量选项,具有良好的精度。
在为 HABIT 仪器设计电导率测量系统期间,我们遇到了需要解决的挑战。电极材料的选择基于其耐腐蚀性和表面光滑度,以避免电导率测量中出现零星的毛刺。吸湿性盐有时会通过毛细作用沿着容器壁向上攀升,因此必须选择疏水涂层。我们使用了基于环氧树脂组合物的涂层,以防止盐水毛细管上升。此外,电脉冲电压、频率和电流感应参考电阻器等电气特性对设计也至关重要。BOTTLE 使用 ±2.048 V 偏置电压,电脉冲为 ±70 mV,低电导和高电导模式为 ±700 V。1 kHz 的电脉冲通过金电极和盐样品进行研究,并在另一侧的金电极上用 10 k-ohm 和 100-ohm 参考电阻器分别用于低电导和高电导模式读出。
由于将电导率描述为相对湿度的函数的每项实验都需要恒定且稳定的温度,因此该协议旨在适应火星模拟室的温度稳定性限制。由于热隔离,工作台温度(由腔室的 LN2 馈入系统调节)和 BOTTLE 温度存在明显差异。这意味着工作台温度并不总是与 BOTTLE 温度相同,必须考虑差异以获得最佳实验条件。
未来在火星模拟室中的实验将包括推导出不同温度下的空气电导率和相对湿度之间的关系。在火星太阳模拟期间,我们观察到空气的相对湿度与其电导率之间可能存在相关性。这可能与校准 BOTTLE 两端的两个空细胞相关,并将其与盐-SAP 混合物的校准相结合,以更精确地解释其水合作用水平。为了进行此实验,可以按照相同的实验方案调整空实验容器,无需任何盐样品。
所描述的实验方案提供了一种更简单、易于适应的替代方法来监测盐水形成过程,该方法也适用于可能与大气水分相互作用的其他样品。对于了解海盐混合物形成的盐水的物理和化学性质的研究,它可以作为补充,这将适用于定义盐水可能与通常用于储存核燃料和核废料的罐表面反应的条件33,34。通过调整方案,可以研究不同环境条件下盐水对不同材料的腐蚀性能。我们应用该协议来研究我们通过 HABIT 仪器携带到火星的四种盐和 SAP 混合物的潮解特性。然而,盐或任何形式的盐混合物(例如烟雾颗粒)的吸湿特性都可以分析其云成核电位24。该实验方案还可用于模拟火星和实验室内其他地方的各种大气表面相关现象。
披露声明
作者没有什么可披露的。
致谢
用于实验的 HABIT 工程鉴定模型 (EQM) 由瑞典 Omnisys 制造,作为 HABIT 项目开发的一部分,在 MPZ 和 JMT 的监督下,由瑞典国家航天局 (SNSA) 资助。HABIT 和 BOTTLE 是 MPZ 和 JMT 的原创想法。SpaceQ 火星模拟室是位于瑞典吕勒奥的吕勒奥理工大学设施。Kempe 基金会资助了 SpaceQ 舱的设计和制造。SpaceQ 腔室由英国 Kurt J. Lesker 公司在 MPZ 的监督下制造。MPZ 由西班牙国家研究局 (AEI) 项目编号MDM-2017-0737 Unidad de Excelencia “María de Maeztu” - 天体生物学中心 (INTA-CSIC) 和西班牙科学与创新部 (PID2019-104205GB-C21)。AVR 和 JMT 感谢瓦伦堡基金会的支持。
材料
| Name | Company | Catalog Number | Comments |
| 84 µS/cm and 1413 µS/cm conductivity calibration standard | Atlas Scienific | CHEM-EC-0.1 | |
| Arduino Uno | Arduino | 8058333490090 | |
| Calcium Chloride | Sigma Aldrich | CAS Number: 10043-52-4 | Anhydrous, free-flowing, ≥96% |
| Carbon Dioxide gas cylinder | AGA Gas | ||
| Experiment container | 3D printed in PLA or milled in aluminum/other metal | ||
| EZO Conductivity circuit | Atlas Scienific | EZO-EC | |
| EZO RTD circuit | Atlas Scienific | EZO-RTD | |
| Ferric Sulphate | Sigma Aldrich | CAS Number: 15244-10-7 | 97% |
| Gold electrodes | Custom designed | ||
| HEPA filter | Nitto | NTF9317-H02 | |
| Liquid Nitrogen tank | AGA Gas | ||
| Magnesium Perchlorate | Sigma Aldrich | CAS Number: 10034-81-8 | Free-flowing, ≥99.0% |
| Pressure gauge | Pirani | CCPG−H2−1 | 1x10-9 to 1000 mbar |
| PT100 sensor | |||
| PT1000 sensor | |||
| Scotch-Weld Epoxy Adhesive | 3M | EC-2216 B/A | |
| Sodium Perchlorate | Sigma Aldrich | CAS Number: 7601-89-0 | Free-flowing, ≥98.0% |
| Sodium salt of alginic acid (SAP) | Sigma Aldrich | CAS Number: 9005-38-3 | Powder |
| Sterile water | VWR Chemicals BDH | CAS Number: 7732-18-5 VWR: 75881-014 | Water ASTM Type II, Reagent Grade |
| Swagelok syringe | Fischer scientific | KD Scientific 780812 | |
| T/RH probe | Vaisala | HMT 334 | (-70 to + 180C) and (0 to 100 % RH) |
| Teraterm | |||
| Whitebox Labs Tentacle Shield | Atlas Scienific | TEN-SH |
参考文献
- Gough, R. V., et al. Brine formation via deliquescence by salts found near Don Juan Pond, Antarctica: laboratory experiments and field observational results. Earth and Planetary Science Letters. 476, 189-198 (2017).
- Gough, R. V., Chevrier, V. F., Tolbert, M. A. Formation of liquid water at low temperatures via the deliquescence of calcium chloride: implications for Antarctica and Mars. Planetary and Space Science. 131, 79-87 (2016).
- Farris, H. N., Davila, A. Deliquescence-driven brine formation in the Atacama Desert, Chile: Implications for liquid water at the Martian surface. 47th Lunar and Planetary Science Conference. , (2016).
- Martín-Torres, J., Zorzano, M. -P. Should We Invest in Martian Brine Research to Reduce Mars Exploration Costs. Astrobiology. 17 (1), 3-7 (2017).
- Martín-Torres, J., et al. Transient liquid water and water activity at Gale crater on Mars. Nature Geoscience. 8, 357-361 (2015).
- Zorzano, M. -P., Mateo-Martí, E., Prieto-Ballesteros, O., Osuna, S., Renno, N. Stability of liquid saline water on present day Mars. Geophysical Research Letters. 36, 20201(2009).
- Chevrier, V. F., Hanley, J., Altheide, T. Stability of perchlorate hydrates and their liquid solutions at the Phoenix landing site, Mars. Geophysical Research Letters. 36, 10202(2009).
- Gough, R. V., Chevrier, V. F., Baustian, K. J., Wise, M. E., Tolbert, M. A. Laboratory studies of perchlorate phase transitions: support for metastable aqueous perchlorate solutions on Mars. Earth and Planetary Science Letters. 312 (3-4), 371-377 (2011).
- Gough, R. V., Chevrier, V. F., Tolbert, M. A. Formation of aqueous solutions on Mars via deliquescence of chloride-perchlorate binary mixtures. Earth and Planetary Science Letters. 393, 73-82 (2014).
- Fischer, E., Martínez, G. M., Elliott, H. M., Rennó, N. O. Experimental evidence for the formation of liquid saline water on Mars. Geophysical Research Letters. 41, 4456-4462 (2014).
- Nuding, D. L., Rivera-Valentin, E. G., Davis, R. D., Gough, R. V., Chevrier, V. F., Tolbert, M. A. Deliquescence and efflorescence of calcium perchlorate: an investigation of stable aqueous solutions relevant to Mars. Icarus. 243, 420-428 (2014).
- Nuding, D. L., Davis, R. D., Gough, R. V., Tolbert, M. A. The aqueous stability of a Mars salt analog: instant Mars. Journal of Geophysical Research: Planets. 120, 588-598 (2015).
- Nikolakakos, G., Whiteway, J. A. Laboratory investigation of perchlorate deliquescence at the surface of Mars with a Raman scattering lidar. Geophysical Research Letters. 42, 7899-7906 (2015).
- Chojnacki, M., McEwen, A., Dundas, C., Ojha, L., Urso, A., Sutton, S. Geologic context of recurring slope lineae in melas and coprates chasmata, Mars. Journal of Geophysical Research: Planets. 121, 1204-1231 (2016).
- Pál, B., Kereszturi, Á Possibility of microscopic liquid water formation at landing sites on Mars and their observational potential. Icarus. 282, 84-92 (2017).
- Rivera-Valentín, E. G., et al. Constraining the potential liquid water environment at Gale Crater, Mars. Journal of Geophysical Research: Planets. 123 (5), 1156-1167 (2018).
- Bhardwaj, A., et al. UAV Imaging of a Martian Brine Analogue Environment in a Fluvio-Aeolian Setting. Remote Sensing. 11 (18), 2104(2019).
- Martin, S. T. Phase transitions of aqueous atmospheric particles. Chemical Reviews. 100 (9), 3403-3454 (2000).
- Primm, K. M. Freezing of perchlorate and chloride brines under Mars-relevant conditions. Geochimica et Cosmochimica Acta. 212, 211-220 (2017).
- Primm, K. M. The effect of mars-relevant soil analogs on the water uptake of magnesium perchlorate and implications for the near-surface of Mars. Journal of Geophysical Research: Planets. 123 (8), 2076-2088 (2018).
- Toner, J. D. The formation of supercooled brines, viscous liquids, and low-temperature perchlorate glasses in aqueous solutions relevant to Mars. Icarus. 233, 36-47 (2014).
- Altheide, T., et al. Experimental investigation of the stability and evaporation of sulfate and chloride brines on Mars. Earth and Planetary Science Letters. 282 (1-4), 69-78 (2009).
- Slank, R. A., Chevrier, V. F. Experimental simulation of deliquescence and implications for brine formation at the Martian surface. Mars Workshop on Amazonian Climate. , (2018).
- Freney, E. J., Martin, S. T., Buseck, P. R. Deliquescence Measurements of Potassium Salts. American Geophysical Union, Fall Meeting. , (2007).
- Baustian, J., Wise, M. E., Tolbert, M. A. Depositional ice nucleation on solid ammonium sulfate and glutaric acid particles. Atmospheric Chemistry and Physics. 10 (5), 2307-2317 (2010).
- Yang, L., Pabalan, R. T., Juckett, M. R. Deliquescence Relative Humidity Measurements Using an Electrical Conductivity Method. Journal of Solution Chemistry. 35 (4), 583-604 (2006).
- Heinz, J., Schulze-Makuch, D., Kounaves, S. P. Deliquescence induced wetting and RSL-like darkening of a Mars analogue soil containing various perchlorate and chloride salts. Geophysical Research Letters. 43, 4880-4884 (2016).
- McKay, C. P., Friedmann, E. I., Gómez-Silva, B., Cáceres-Villanueva, L., Andersen, D. T., Landheim, R. Temperature and moisture conditions for life in the extreme arid region of the Atacama desert: Four years of observations including the El Niño of 1997-1998. Astrobiology. 3 (2), 393-406 (2003).
- Davis, W. L., de Pater, I., McKay, C. P. Rain infiltration and crust formation in the extreme arid zone of the Atacama Desert, Chile. Planetary and Space Science. 58 (4), 616-622 (2010).
- Martín-Torres, J., et al. The HABIT (HabitAbility: Brine Irradiation and Temperature) environmental instrument for the ExoMars 2022 Surface Platform. Planetary and Space Science. 190, (2020).
- Nazarious, M. I., Vakkada Ramachandran, A., Zorzano, M. -P., Martin-Torres, J. Calibration and preliminary tests of the Brine Observation Transition To Liquid Experiment on HABIT/ExoMars 2020 for demonstration of liquid water stability on Mars. Acta Astronautica. 162, 497-510 (2019).
- Vakkada Ramachandran, A., Nazarious, M. I., Mathanlal, T., Zorzano, M. P., Martín-Torres, J. Space Environmental Chamber for Planetary Studies. Sensors. 20 (14), 3996(2020).
- Carroll, S., Rard, J., Alai, M., Staggs, K. Technical Report: Brines formed by multi-salt deliquescence. Lawrence Livermore National Lab. (LLNL). , Livermore, CA (United States. (2005).
- Bryan, C. R., Schindelholz, E. J. Properties of Brines formed by Deliquescence of Sea-Salt Aerosols. Sandia National Laboratories. , Albuquerque., NM 87185 U.S.A. (2017).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。