Method Article
Technik der Schweineleber Beschaffung und orthotopen Transplantation mit einem Active Porto-Kava-Shunt
In diesem Artikel
Zusammenfassung
Experimental animal research plays a pivotal role in the development of clinical transplantation practice. The porcine orthotopic liver transplantation model (OLTx) closely resembles human conditions and is frequently used in clinically oriented research. The following protocol contains all information for a reliable porcine OLTx model using an active porto-caval-jugular shunt.
Zusammenfassung
The success of liver transplantation has resulted in a dramatic organ shortage. Each year, a considerable number of patients on the liver transplantation waiting list die without receiving an organ transplant or are delisted due to disease progression. Even after a successful transplantation, rejection and side effects of immunosuppression remain major concerns for graft survival and patient morbidity.
Experimental animal research has been essential to the success of liver transplantation and still plays a pivotal role in the development of clinical transplantation practice. In particular, the porcine orthotopic liver transplantation model (OLTx) is optimal for clinically oriented research for its close resemblance to human size, anatomy, and physiology.
Decompression of intestinal congestion during the anhepatic phase of porcine OLTx is important to guarantee reliable animal survival. The use of an active porto-caval-jugular shunt achieves excellent intestinal decompression. The system can be used for short-term as well as long-term survival experiments. The following protocol contains all technical information for a stable and reproducible liver transplantation model in pigs including post-operative animal care.
Einleitung
Lebertransplantation (OLTx) ist die einzige Behandlungsoption für Patienten im Endstadium einer Lebererkrankung oder fortgeschrittenem Leberzellkarzinom. In den letzten 25 Jahren hat sich die Zahl der Kandidaten auf der Warteliste nach und nach erhöht und jetzt weit die Anzahl der verfügbaren Transplantate überschreitet. In den meisten Regionen der Transplantation, 20 bis 30% der Patienten auf der Warteliste für eine Lebertransplantation sterben, ohne eine Organtransplantation oder durch Fortschreiten der Krankheit ausgelistet. Strategien, um die Spenderpool zu erhöhen und damit die Anzahl der verfügbaren Transplantate, werden dringend benötigt. Erweiterte Kriterien Organzuteilung, verlängerte Transplantaterhaltung, und die Induktion von Immuntoleranz noch stellen eine große klinische Herausforderung 1-3. Daher ist experimentelle OLTx Forschung entscheidende, um klinische OLTx Praxis zu optimieren.
Porcine OLTx ist ein gut etabliertes experimentellen Modell, das menschliche OLTx in vielerlei Hinsicht einschließlich l ähneltiver Größe, Anatomie und Physiologie 4-6. So hat es sich zu einem Standard experimentelle Methode in Forschungsbereichen wie Operationstechniken, Physiologie, Immunologie, Erhaltung und Ischämie-Reperfusionsschaden. Zahlreiche Techniken der Transplantat Beschaffung Empfänger Hepatektomie, und insbesondere eine Gefäßrekonstruktion, wurden in der Literatur 5 beschrieben. Die Wahl der geeigneten Technik variiert je nach Präferenz des Forschers und technische Leistungsfähigkeit.
Im Gegensatz zum menschlichen Szenario splanchnic Staus während des anhepatischen Phase repräsentiert ein wichtiges Problem in porcine OLTx. Nachfolgende Darmischämie und kongestive Gefäßschäden kann schwere hämodynamische Instabilität verursachen, zu gefährden das Schwein Überleben und damit den Erfolg des Experiments 7-9. Daher ist eine ausreichende Darm Dekompression verpflichtend, vor allem in weniger technisch verfeinert experimentellen Einstellungen.
Unsing eine aktive porto-Kava-Halsschlag Shunt für die Dauer des anhepatischen Phase ist eine zuverlässige Möglichkeit, Darm-Staus zu vermeiden. Das System kann für frühen Reperfusion Experimenten als auch langfristige Überleben Szenarien verwendet werden. Das folgende Protokoll enthält alle Informationen für eine stabile und reproduzierbare Lebertransplantationsmodell in Schweinen, einschließlich Spenderleber Beschaffung, Empfängerbetrieb einschließlich Hepatektomie und End-to-End-Schiff Rekonstruktionstechniken und postoperative Pflege.
Protokoll
Alle Tiere erhielten humane Pflege im Einklang mit den '' Principles of Laboratory Animal Care '' von der Nationalen Gesellschaft für Medizinische Forschung und dem "Leitfaden für die Pflege von Labortieren" formuliert "von den National Institutes of Health, Ontario, Canada veröffentlicht . Die Animal Care Committee der Toronto General Research Institute stimmten allen Studien.
1. Organ Retrieval
- Haus männlichen Yorkshire Schweine zwischen 30 und 35 kg in der Forschungsanlage für 1 Woche vor der Transplantation, eine spannungsinduzierte körperliche Reaktion (der die Durchblutung des Ergebnisses 10,11 verändern können) und um die Tiere, um die Wohnverhältnisse zu akklimatisieren zu verhindern. Schnell das Schwein für mindestens 6 Stunden vor der Einleitung der Narkose.
- Betäuben das Spenderschwein durch eine intramuskuläre (im) Injektion einer Mischung aus Ketamin (25 mg / kg), Atropin (0,04 mg / kg) und Midazolam (0,15 mg / kg).
- Vor Intubation, sicherzustellen, das Schwein spontan atmet 2 L von Sauerstoff mit 5% Isofluran dosiert. In Rückenlage, sprühen die Stimmbänder mit 2% Lidocain 2 min vor der Intubation zu Stimmbandkrämpfe zu vermeiden. Für einen 35 kg Schwein, verwenden Sie ein 6,5 Fr Trachealtubus. Sperrung der Trachealtubus mit 3-5 ml Raumluft.
- Nach der Intubation, benutzen Kapnometrie korrekte Intubation zu bestätigen. Überwachen Sie die Herzfrequenz und Sauerstoffsättigung durch Pulsoximetrie bei der Schweineschwanz. Senken Sie die Isofluran-Verdampfer bis 2%.
- Stellen Sie die Tiefe der Anästhesie durch Werte minimal alveolare Konzentration (MAC); Ziel für 2-2,5 MAC. Stellen Sie das Beatmungsgerät 14 bis 16 Atemzüge / min und einem Atemvolumen von 10 bis 15 ml / kg Körpergewicht.
- Ein 18G intravenöse (iv) Katheter nach einem der Ohrvenen der Infusion von Ringer-Laktat-Lösung (200 ml / h) zu ermöglichen. Scrub die Schweine- und decken Sie es mit sterilen Tüchern.
- Nachdem er sich vergewissert sterilen Bedingungen, machen Sie eine Mittellinie Laparotomie Follodurch eine linke seitliche Erweiterung heiraten. Verwenden Sie ein Handtuch auf großen und kleinen Darm, bevor sie auf die linke Seite zu decken.
- Teilen Sie das Ligamentum falciforme und den dreieckigen Ligament mit einem Brenneisen.
- Lassen Sie die Leber vor der Membran auf der rechten Seite unter Verwendung eines elektro cautery; mit einer Schere für den oberen Teil zwischen dem Cava und Zwerchfell. Sezieren die infrahepatische cava auf dem Zweig des Nebennierenvene auf der rechten Seite und der Nierenvene auf der linken Seite.
- Trennen Sie die infrahepatische Cava und Aorta distal voneinander; ligieren Aortenäste an der Wirbelsäule; isolieren und kostenlos Nierenarterien von anhaftendem Gewebe. Umgeben Sie jedes Nierenarterie mit einem 2-0 Unentschieden.
- Kranial der linken Nierenvene, sezieren die Aorta und A. mesenterica. Umgeben die A. mesenterica mit einem 2-0 Unentschieden.
- Nach dem Öffnen des Bauchfells kranial der A. mesenterica, befolgen Sie die Aorta in Richtung des Truncus coeliacus. Präparieren Sie die Truncus coeliacus kaudal zum Portal vein; umgeben die Milz und linken Magen-Arterien, die Niederlassung nach hinten aus dem Truncus coeliacus. Präparieren Sie die Zöliakie-Stamm aus der Pfortader.
- Lassen Sie die Pfortader durch eine Peritonealdialyse Einschnitt zwischen der Bauchspeicheldrüse und der Pfortader. Abbinden Venen aus der Bauchspeicheldrüse in die Pfortader.
- Trennen Sie den Gallengang aus dem Ligamentum hepatoduodenale und teilen sie distal nach der Ligation.
- Ligieren die Lymphgefäße im Ligamentum hepatoduodenale zu lymphatischen Auslaufen zu verhindern. Teilen Sie die gastroduodenalen Arterie und rechts Magen Arterien zwischen Krawatten. Ligieren kleineren Adern.
- Präparieren Sie die Aorta hinter der Membran zwischen dem Herzen und Truncus coeliacus. Legen Sie eine 2-0 Krawatte um die Aorta kranial des Truncus coeliacus.
- Entfernen Sie die Gallenblase und kauterisieren Blutung aus der Gallenblase Bett.
- Öffnen Sie die Blende. Verwalten 1.000 IE / kg Spendergewicht von Heparin intrakardial oder iv Set Isofluran bis 5% (> 2,5 MAC), um zu erreichenein tieferer Narkoseniveau. Auf ein Spender nach Kreislauf Tod (DCD) Modell, induzieren Herzstillstand durch intrakardiale Injektion von 40 mval KCl 3 min nach Heparingabe. Stellen Herzstillstand als Startpunkt der warmen Ischämie.
- Binden Sie die zuvor eingestellte Krawatten um den Nieren, Milz, mesenterialen und linken Magen-Arterien. Binden Sie die Aorta distal zwischen Nieren- und Beckenarterien und kanülieren die Aorta mit einer Orgel Spülleitung.
- Binden Sie die Pfortader als proximal wie möglich und kanülieren es mit einem anderen Organ Spülleitung.
- Nach dem Schließen der voreingestellten Krawatte um den proximalen Aorta, spülen Sie die Leber mit 2 l kaltem University of Wisconsin (UW) Lösung mit Dual-Perfusion via Aorta (Drucksack) und Pfortader (schwerkraftgetriebenen).
- Auszuschneiden die Leber, lange verlassen alle verbleibenden Schiffe. Lassen Sie eine großzügige Zwerchfell Rand um die suprahepatischen cava. Legen Sie die Leber in eine sterile Orgel Tasche auf Eis.
- Während der Rück Tisch Vorbereitung, clamp die suprahepatischen Cava mit einem Satinsky Klemme und spülen Sie die Leber ein zweites Mal mit etwa 0,5 l UW-Lösung retrograd über die untere untere Hohlvene bis die Pfortader Abfluss ist klar.
- Binden Sie alle Arterienäste der Aorta und Truncus coeliacus. Führen Sie eine arterielle zurück-Tabelle Druck Perfusion mit dem restlichen 0,5 l UW-Lösung 12.
- Spülen Sie den Gallengang mit UW-Lösung.
- Schneiden Sie die Zwerchfell-Patch, um eine anständige Größe. Schließen Sie alle Zwerchfellvenen - in der Regel 3, 1 jeweils links und rechts, und 1 posterior - mit 4-0-Monofilament Polypropylen Stiche.
- Schließen Sie die Orgel Beutel und lagern Sie die Leber auf Eis.
2. Empfänger Hepatektomie
- Betäuben den Empfänger Schwein durch eine im Injektion eines Gemisches von Ketamin (25 mg / kg), Atropin (0,04 mg / kg) und Midazolam (0,15 mg / kg).
- Legen Sie das Schwein in Rückenlage auf einen Operationstisch auf einem Heizmatte. Decken Sie die Schweine with eine wärme zirkulierenden Decke.
- Vor Intubation, sicherzustellen, das Schwein spontan atmet 2 L von Sauerstoff mit 5% Isofluran dosiert. Sprühen Sie die Stimmbänder mit 2% Lidocain 2 min vor der Intubation zu Stimmbandkrämpfe zu vermeiden. Für einen 35 kg Schwein, verwenden Sie ein 6,5 Fr Trachealtubus. Sperrung der Trachealtubus mit 3-5 ml Raumluft.
- Nach der Intubation, benutzen Kapnometrie korrekte Intubation zu bestätigen. Überwachen Sie die Herzfrequenz und Sauerstoffsättigung durch Pulsoximetrie bei der Schweineschwanz. Platzieren und befestigen eine Temperatursonde in das Schwein Schnauze. Senken Sie die Isofluran-Verdampfer bis 2% (Ziel für 2-2,5 MAC). Stellen Sie das Beatmungsgerät 14 bis 16 Atemzüge / min und einem Atemvolumen von 10 bis 15 ml / kg Körpergewicht.
- Verwenden Salbe auf die Augen bis zur Trockenheit während der Narkose zu verhindern.
- Verwenden Seldinger-Technik 13, einen Mantel Induktor (8,5 Fr) in die linke Vena jugularis externa einfügen. Verwenden Sie diese Katheter später für ein aktives Portal-Kava-Halsschlag Bypass.
- Verwenden Seldinger technique, um eine totale parenterale Ernährung (TPN) Katheter (9,5 Fr) in die rechte äußere Jugularvene einzufügen.
- Unter sterilen Bedingungen, sezieren die rechte Halsschlagader und legen Sie eine Polypropylen-Katheter (18 G) zur invasiven arteriellen Drucküberwachung. Umgeben die Arterie mit einem 2-0 Seidenkrawatte Notfallligation zu ermöglichen.
- Drehen Sie die Isofluran-Verdampfer bis 1% (1,5-2 MAC) und fügen Propofol (5-8 mg / kg / h iv), um die Narkosetiefe zu erhalten. Zur Analgesie, benutzen kontinuierlichen iv-Infusion von Fentanyl-Citrat (am meisten bevorzugt 2 & mgr; g / kg / h) oder Remifentanil (zweite Wahl, 15 ug / kg / h).
- Vor der Hautschnitt, geben 1000 mg Cefuroxim und 500 mg Metronidazol iv. Up eine Infusionspumpe mit Ringer-Laktat mit 5% Glucose bei 150 ml / h eingestellt.
- Setzen Sie den Kühlumlauf Decke auf den Kopf und Nackenbereich. Scrub die Schweine- und decken Sie es mit sterilen Tüchern.
- Unter sterilen Bedingungen, machen Sie eine Mittellinie Laparotomie. Legen Sie eine Bauch retractor ausreichenden Zugang zu der rechten oberen Quadranten zu bekommen.
- Teilen Sie die falciforme Band und den dreieckigen Ligament mit Brenneisen.
- In mehreren Schritten, teilen Sie die Ligamentum hepatoduodenale Nähe der Leber zwischen Krawatten. Zu identifizieren, zu teilen, und markieren Sie die Zweige der Leberarterie und Gallengang.
- Präparieren Sie die Leberarterie retrograde, bis die Teilung der gastroduodenalen Arterie. Stellen Sie sicher, dass ein Bulldog Klemme passt um die gemeinsame Leberarterie proximal der gastroduodenalen Arterie für die spätere Spannen.
- Befreien Sie die Pfortader von anhaftendem Gewebe.
- Zu mobilisieren, die Vena cava von Retroperitoneums auf der rechten Seite unter Verwendung eines elektro Kauterisation. Mit einer Schere für den oberen Teil zwischen dem Cava und Zwerchfell. Sezieren die infrahepatische cava auf dem Zweig des Nebennierenvene auf der rechten Seite und der Nierenvene auf der linken Seite.
- Setzen Sie den Hilus der Milz. Etwa auf halbem Weg entlang der Milz Länge, sorgfältig weg vonf der Milz Arterie und Vene aus halten Bauchfellschichten. Umgeben Sie beide Milz Arterie und Vene mit 4 2-0 Seidenkrawatten.
- Legen Sie eine 8,5 Fr Hülle Induktor mit 2 zusätzlichen Löcher in die Katheterspitze in die Milzvene und deutete distal in Richtung der Pfortader. Befestigen Sie den Katheter distal um seine Einführung mit einer der Bindungen 2-0 und schließen Sie die Vene proximal der Insertion mit einem anderen 2-0 Krawatte. Lassen Sie die anderen 2 Bindungen geöffnet.
- Zeichnen Sie Blut aus dem Katheter, spülen Sie es mit 10 ml Kochsalzlösung, und schließen Sie die Klemme des Katheters.
- Füllen Kochsalzlösung in einem Bypass, bestehend aus einer Kreiselpumpe Kopf, einer Halsschlagrohr (3/16 "), und der Mittelzufluss aus sowohl einem Portal Zweig (3/16") und einer Kava-Zweig (1/4 ", Luer-Lock-Anschluss am proximalen Öffnung). Setzen Sie ein Schlauchklemme auf das proximale Ende des Kava-Schläuche.
- Schließen Sie das Portal und die Halsschlag Öffnung des Umgehungs sowohl Mantelintubator Katheter (Abbildung 1) und dichten die connection mit einem Metallschlauch Klemmring. Legen Sie die Zentrifugalpumpenkopf in seine Pumpenposition.
- Geben Sie 1000 mg Tranexamsäure und 10.000 IE Heparin 3 min iv vor Querspann. Reduzieren Sie die Propofol-Infusionsrate bis 2 mg / kg / h für die Zeit des anhepatischen Phase. Stellen Sie die Isofluran-Konzentration auf den arteriellen Druck und das Schwein Reaktivität.
- Öffnen Sie die Klemmen beider Mantelintubator Katheter und Kreuzklemme der Pfortader. Stellen Sie sicher, dass das Blut durch den Bypass läuft passiv.
- Starten Sie die Kreiselpumpe bei etwa 1.500 U / min. Weiterhin Kreuzklemm wenn a) das Schwein kardiovaskulären stabil und b) der Bypass bei etwa 500 ml / min ausgeführt wird. Wenn das Schwein nicht die Querspann, Ersatzvolumen (Kristalloide oder Kolloide) und inotrope Mittel (Noradrenalin in kleinen Boli) nicht tolerieren.
- Quer klemmen die infrahepatische Hohlvene nur kranial der Nierenvenen mit einer De Bakey-Beck Klemme. Festem Druck auf die Leber tissue den Squeeze-out ein Teil des Restblut. Quer klemmen die suprahepatischen Hohlvene mit einer Zwerchfell Felge mit einem Satinsky Klemme, während das Zurückziehen der Leber kaudal.
- Schneiden Sie die suprahepatischen Hohlvene direkt an der Grenze zu dem Lebergewebe. Als nächstes schneiden die Pfortader in der Nähe der Leberpforte.
- Ca. 4 cm kranial des infrahepatische cava Klemme, schnitt ein Loch in die vordere Wand der Vena Cava. In dieses Loch, positionieren Sie den Stecker des Bypass 'Kava-Öffnung mit der Luer-Lock mit Blick nach vorn.
- Sichern Sie den Stecker in der infrahepatische cava mit 1-0 Seidenkrawatten. Öffnen Sie dann die Schlauchklemme des Kava-Zweig der Bypass.
- Schließlich öffnen Sie die infrahepatische cava Klemme, eine Kava-Halsschlag Bypass zusätzlich zu der bestehenden porto-Halsschlag Bypass zu ermöglichen. Erhöhen Sie die Pumpendrehzahl auf über 2500 U / min, so dass der Bypass-Abfluss an der Halsschlagseite ist zwischen 900 - 1.100 ml / min.
- Auszuschneiden die Leber an seinem verbleibenden cnschluss kranial der infrahepatische Bypass-Anschluss, um sicherzustellen, dass die Bande Sicherung der Bypass-Anschluss werden nicht abgeschnitten. Positionieren Sie den Bypass-Schlauch vorsichtig um Knicken zu vermeiden. Geben Sie 500 mg Methylprednisolon Immunsuppression zu initialisieren.
3. Vessel Wiederaufbau
- Verwendung 4-0 Monofilament Polypropylen Nähte, schließen Sie alle 3 phrenic Venenmündungen auf der Empfängerseite an der suprahepatischen cava der Blende. Stich-Doppel bewaffnet 4-0 Monofilament Polypropylen Nähte von innen nach außen in beiden Ecken des suprahepatischen cava auf der Empfängerseite.
- Entfernen Sie das Spenderorgan Tasche aus dem Eisschrank. Öffnen Sie die Orgel Tasche, nehmen Sie die Spenderleber, und legen Sie sie in die Bauchhöhle.
- Für eine End-to-End-Anastomose des suprahepatischen cava, schneiden Sie die Geber suprahepatischen Hohlvene, um die Empfängerseite passen. Mit Hilfe der im Inneren Nadeln der Empfängerseite Ecke Stiche, tun ein Innen-Außen Ecke Masche auf jeder der Seiten des suprahepatic Spender cava.
- Erschossen die beiden Enden des rechten Naht zusammen. Nähern sowohl Ostien von Empfänger und Spender cava, dann binden Sie die beiden Enden des linken Naht.
- Schoss das kürzere Ende und machen einen Außen-Innen-Stich des Empfängers cava Rückwand neben der Krawatte. Führen Sie über die Rückwand, ideal Umstülpen des Cava Wänden.
- In 2-3 Vorderwand Stiche mit der gleichen Naht einmal die rechte Seite erreicht worden ist, dann schoss dieses Naht Ende. Führen Sie über die Vorderwand mit der restlichen Naht von der linken Ecke. Verknüpfen Sie die beiden Fäden für die hinteren und vorderen Wände verwendet. Binden Sie die beiden anderen Nahtenden in der rechten Ecke.
- Nach dem Trimmen den Spender Pfortader auf eine geeignete Länge, führen Sie eine End-to-End-Anastomose Pfortader auf die gleiche Weise, mit 6-0 Monofilament Polypropylen Nähte. Kurz vor dem Abschluss mit der Vorderwand, intubieren das Lumen des infrahepatische Cava mit einem anderen Spülleitung und spülen, die UW-Lösung mit 1 l Kochsalzlösungbei RT über die infrahepatische cavaportal Vene.
- Füllen Sie das Anastomose und binden Sie die Fäden, so dass ca. 0,5 cm von Wachstumsfaktor. Anders De Bakey- Beck Klammer auf die Spender infrahepatische cava.
- Öffnen Sie die suprahepatischen cava Klemme und prüfen Blutungen. Dann reperfuse der Leber durch das Öffnen der Klemm Portal.
- Verwenden Sie 6-0 Monofilament Polypropylen Nähte für blutstillende Stiche. Verringern Sie die Drehzahl der Bypasspumpe bis etwa 1500 U / min, und schließen Sie die Klemme des Portals Mantelintubator Katheter.
- Umspannen der Empfängerseite des infrahepatische Hohlvene und legte eine Schlauchklemme auf der Kava-Teil des Bypass. Stoppen Sie die Kreiselpumpe.
- Schneiden Sie die Bindungen des Kava-Stecker und entfernen. Schicken Sie das restliche Blut vom Bypass zum Schwein durch die Jugularkatheter.
- Schließen Sie die Klemme des Jugularkatheter und ziehen Sie den Bypass. Gib 100 mg Protaminsulfat, um die Heparin antagonisieren. Besondere Vorsicht der pig die Hämodynamik während dieser Schritte; benutzen Katecholamin für Druckunterstützung und Ersatz Natriumbicarbonat für metabolische Azidose.
- Durchführen eines End-zu-End-Anastomose des infrahepatische cava wieder in der oben beschriebenen Weise, mit 5-0 Monofilament-Polypropylen-Nähte. Reperfuse die infrahepatische unteren cava durch die Freigabe beide Klemmen.
- Schneiden Sie einen Aorta Patch um Truncus des Spenders. Binden Sie den Empfänger A. gastroduodenalis in der Nähe der gemeinsamen Leberarterie. Legen Sie eine Bulldogge Klammer auf die gemeinsame Leberarterie proximal zu der Kreuzung der gastroduodenalen Arterie. Schneiden Sie einen kleinen arteriellen Patch mit einem Potts Schere, mit der Gefäßgewebe rund um die Kreuzung.
- Spülen Sie die Spenderleberarterie mit 10 ml heparinisierter Kochsalzlösung und legte eine andere Bulldog Klemme weiter distal zu vermeiden, wieder zu bluten. Anastomosieren den arteriellen Ostien Ende-zu-Ende in einer Lauffallschirm-Technik unter Verwendung eines 6-0-Monofilament Polypropylen Naht. Indem zunächst ope Reperfusening die distale und die proximale Bulldogklemmen.
- Anastomosieren den Gallengang Ende-zu-Ende mit 2 6-0 Monofilament-Nahtmaterial aus Polypropylen mit der oben beschriebenen Technik ausgeführt. Stellen Sie sicher, dass große Teile der peribiliären Gewebe sind enthalten, weil die Schweine-Gallengang ist sehr zerbrechlich und leicht reißt.
- Nach Überprüfung zur Blutstillung, entfernen Sie die Hülle Einführkatheter aus der Milzvene. Schließen der proximalen und distalen Enden mit den verbleibenden 2 Krawatten.
- Schließen Sie die Bauchwand mit einer Größe 1 Monofilament resorbierbares Nahtmaterial. Schließen Sie die Haut entweder mit einem Hautklammergerät oder einem Lauf 2-0 Nahtmaterial.
4. postoperativen Phase
- Verwenden Sie das Heizkissen und Wärmezirkulation Decke, das Schwein warm zu halten.
- Probe Blutgasen stündlich. Passen Austrocknung durch die Erhöhung der Infusionsrate.
- Wean die Anästhesie. Lüften Sie das Schwein für weitere 2 Std.
- Entfernen Sie die Hülle Einführkatheter von der linken Halsschlag vein. Drücken Sie fest für ein paar Minuten, um Blutungen zu verhindern.
- Tunnel der TPN Katheter subkutan an der Seite des Halses des Schweins. Sichern Sie sie mit 2-0 Nähten.
- Entfernen Sie die arterielle Leitung nach 2 Stunden, wenn das Schwein ist ohne Katecholamin Unterstützung hämodynamisch stabil. Stellen Sie sicher, dass die Punktionsseite nicht bluten. Ansonsten machen einen 6-0 Tabaksbeutelstich um den arteriellen Loch ohne Schließen der Arterie. Schließen Sie die Einschnittstelle.
- Stoppen Sie die Lüftungs einmal das Schwein ist in der Lage, selbständig zu atmen. Trennen Sie das Lüftungsschlauch vom Trachealtubus. Immer wieder zu überprüfen, ob das Schwein ausreichend atmen.
- Legen Sie das Schwein in Bauchlage in einem einzigen Tiergehege mit einer Wärmelampe zur Verfügung gestellt. Extubieren einmal das Schwein ist in der Lage, unabhängig zu halten den Kopf. Haben ein Tier nicht unbeaufsichtigt lassen, bis er wieder zu sich kam, um ausreichende Brustlage zu halten. Haus das Schwein gesondert für die gesamte postoperativen Phase.
- Lieferniv ausreichend Schmerzmittel nach der Operation (zB Buprenorphin 0,01 bis 0,05 mg / kg alle 6 Stunden).
- Wenn das Schwein nicht unabhängig zu trinken, zu ersetzen genügend Volumen iv
- Weiter Methylprednisolon als Immunsuppression (250 mg postoperativen Tag (POD) 1 Morgen und dann 125 mg jeden Morgen). Beginnen Cephalosporin 2 mg / kg zweimal täglich po aus POD2 auf.
- Verabreichen 500 mg Metronidazol und 1,000 mg Cefazolin zweimal täglich sowie 20 mg Pantoprazol einmal täglich bis Pod3.
- Überwachen Sie die Schweine eng. Zögern Sie nicht, es zu opfern, wenn es Anzeichen von Leiden (zB Lethargie, refusion zu trinken, persistent Azidose oder Hypoglykämie, oder Anzeichen von Blutungen oder Bauchfellentzündung). Um Sterbehilfe, exsanguinate das Schwein unter tief Isofluran-Narkose (5%,> 2,5 MAC) durch Schneiden des suprahepatischen cava.
Ergebnisse
In einem ersten Transplantationsstudie einer Heart-Beating-Donor-Modell (HBD, n = 5) wurde mit einem DCD Modell (n = 10) bis 45 min warmer Ischämie in situ ausgesetzt verglichen. In beiden Gruppen wurden Transplantate auf Eis für 10 Stunden nach der Auftragsvergabe aufbewahrt.
In der HBD-Gruppe 100% der Empfänger Schweine überlebten bis zum Ende des Follow-up am Tag 5 nach der Transplantation. In der DCD-Gruppe, nur 50% der Empfänger überlebte Schweine für 5 Tage durch Gerinnungsprobleme oder Stoffwechselentgleisung, als Folge der verminderten postoperativen Leberfunktion.
Alle Blutproben wurden aus dem zentralen Venenkatheter gesammelt. Nach der Zentrifugation wurden Serumproben gewonnen und auf hepatozellulären Verletzung (Aspartataminotransferase, AST), Gallenfunktion (Gesamt-Bilirubin und alkalische Phosphatase), und die Leberfunktion (INR) analysiert. 5 - der zeitliche Verlauf eines jeden Markers in den 2 gezeigt ist.
AST-Werte erreichte ihren Höhepunkt nach 24 Stunden (1414 ± 538 U / L in der HBD-Gruppe und 2296 ± 1313 U / L in der DCD-Gruppe, p = 0,13) und nach 5 Tagen wieder auf fast normale Werte. In ähnlicher Weise wurden die alkalische Phosphatase-Werte deutlich nach 36 Stunden in der DCD-Gruppe (224 ± 111 U / l) im Vergleich zu der HBD Gruppe (162 ± 54 U / l, p = 0,27) erhöht. Während Gesamt-Bilirubin war in der HBD-Gruppe stabil (≤ 10 & mgr; mol / L in), sie nach und nach in der DCD-Gruppe bis zum Tag 5 (23 ± 31 & mgr; mol / l, p = 0,43) erhöht. Das große Standardabweichung in der Bilirubin-Werte im DCD-Gruppe zeigt eine eigentümliche Heterogenität Gallen Verletzungen in dieser Gruppe. INR als Marker der Leberfunktion zeigte einen Trend ähnlich dem AST-Werte. Werte erreichte 24 Stunden und wurden auf fast normale Werte nach 5 Tagen wieder hergestellt. Die HBD Gruppe hatten niedrigere Werte mit einem Peak bei 1,47 ± 0,34 im Vergleich zur Gruppe DCD (Peak 1,70 ± 0,36, p = 0,32).
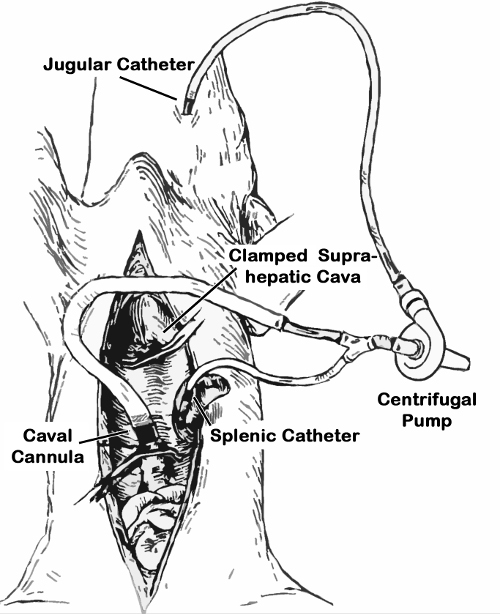
Abbildung 1. Schema der porto-Kava-Shunt jugular. Der Bypass ist mit Ringer-Lactat-Lösung gefüllt. Dann wird der Kava-Teil mit einer Schlauchklemme festgeklemmt ist, werden die Halsschlagader und der Milz Teile zu den voreingestellten Katheter angeschlossen ist, wird der Bypass geöffnet und die Kreiselpumpe nach Pfortader Klemm gestartet. Nach Leberresektion ist die Kava-Teil der Bypass eingelegt und in der infrahepatische Hohlvene Stumpf auf die Nierenvenen gesichert, Schädel. Die Schlauchklemme gelöst wird, um caval Dekompression zu ermöglichen, zusätzlich zu dem Portal Dekompression.
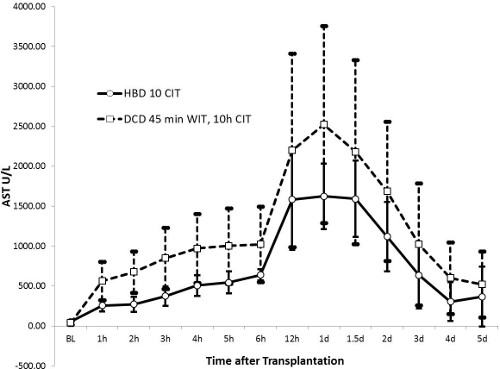
Abbildung 2. Aspartat-Aminotransferase (AST) (HBD n = 5, DCD n = 10). AST ist ein empfindlicher Marker der Leberzellschädigung. Der Peak Achterner 24 Stunden in der HBD niedriger als in der DCD-Gruppe, was auf weniger Leber Reperfusionsschaden; die kleinere Standardabweichung zeigt homogenere Ergebnisse in der HBD-Gruppe.
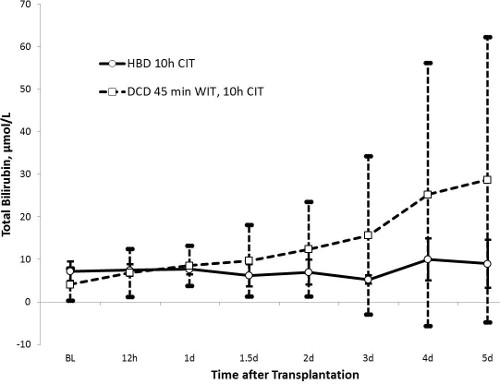
Abbildung 3. Gesamtbilirubin (HBD n = 5, DCD n = 10). Gesamtbilirubin, als Marker der biliäre Clearance und Gallen Integrität, eine stabile und homogene Trend mit Werten unter 10 & mgr; mol / l in der HBD-Gruppe. Das Bilirubin Kurve im DCD Gruppe graduell über die Zeit und zeigt eine hohe Standardabweichung, was darauf hindeutet, Gallenschäden nur in einem Teil der Versuchsgruppe.
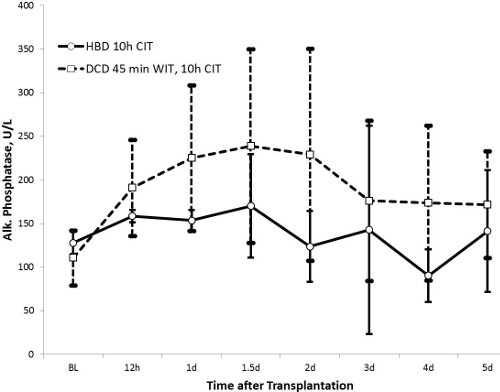
Abbildung 4. Die alkalische Phosphatase (HBD n = 5, DCD n = 10). Die alkalische Phosphatase is einen Indikator für Gallen Verletzungen. Die Werte für die HBD-Gruppe sind niedriger als die der DCD-Gruppe, die weniger Gallen Verletzung impliziert.
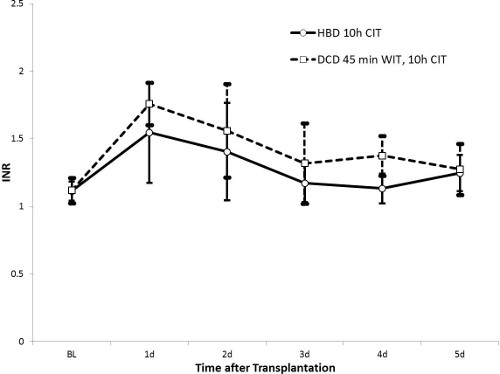
Abbildung 5. INR (HBD n = 5, DCD n = 10). Ein hoher Wert zeigt INR verminderten Leberfunktion aufgrund der verringerten Freisetzung von Gerinnungsfaktoren. In beiden HBD und DCD Gruppen, kehren die INR-Werte auf normale Werte von 5 Tagen nach der Transplantation, was darauf hindeutet Erholung der Leberfunktion. Die Werte für die HBD-Gruppe erscheinen niedriger.
Diskussion
Experimental Schweine OLTx ist ein anspruchsvolles Verfahren für ein Forschungs Einstellung ohne die Intensiv Ressourcen eines klinischen Szenario. Mögliche Komplikationen sind hämodynamische Instabilität, Blutungen, Organ Ischämie, Hypothermie, und Stoffwechsel sowie der Atemwege, Dekompensation. Für jede Arbeitsgruppe, genügt Verfahrens Ausbildung der Operationstechnik 5 als auch das Schwein Anästhesie 14,15 um repräsentative und reproduzierbare Ergebnisse zu erhalten obligatorisch.
Vielen technischen Feinheiten sind in der Literatur beschrieben worden, insbesondere in Bezug auf die Gefäßrekonstruktion Phase 5. Die oben beschriebene OLTx Protokoll bietet die erforderlichen Informationen für einen Sekt-Austausch-Modell ähnelt menschlichen OLTx. Die zur Verfügung gestellten Ergebnisse zeigen zuverlässig das Überleben der Tiere und Graft Erholung in beiden HBD und DCD-Modelle. Das Protokoll ist in kurzfristige Überleben Szenarien in Graft Reperfusion expe gebraucht wird,riments zum Beispiel als auch in Langzeitüberleben Modelle wie Toleranzstudien.
Ein großes Hindernis von Schweine OLTx ist die relativ schlechte Toleranz Cava und Pfortader Querspann. Splanchnischen Staus während der anhepatischen Phase verursacht venösen Bluthochdruck und Kapillare Schäden, die zu den wichtigsten Darmischämie und hämodynamische Instabilität auf den Punkt eines irreversiblen Schock auch nach Organ Reperfusion 7 führen kann. Da die Hohlvene vollständig in Leberparenchym eingebettet, ist ein Cava erhaltHuckepackVerfahren nicht durchführbar. Die Gesamt Okklusion der Vena Cava im Cava Wiederaufbauphase beeinträchtigt die hämodynamische Stabilität des Schweins. Obwohl einige Berichte zeigen, dass Schweine OLTx während insgesamt Cava und Pfortader Okklusion von weniger als 25 min 16,17 erreicht werden, ist eine porto-cava-Halsschlag Bypass Technik zum Zeitpunkt der Gefäßrekonstruktion der sicherer und praktischer Option 7- 9,18. In thErfahrung e Autoren, ist eine passive porto-Halsschlag Bypass nicht optimal, das Schwein hämodynamisch während der anhepatischen Phase stabil zu halten. Die Bypass-Modell, einschließlich der aktiven Druckverlust beider infrahepatische Cava und Pfortader, ermöglicht ein ruhiges Wiederaufbauphase der suprahepatischen caval und Portal Anastomosen sogar mit erweiterten Klemmzeit aufgrund unvorhergesehener Komplikationen. Im Gegensatz zu früheren Berichten 7 eine Splenektomie nicht zwingend erforderlich, wenn das Portal Bypasskatheter wird entfernt. Sowohl Milz Arterie und Vene sind etwa auf halbem Weg entlang der Länge der Milz Verlassen der proximalen Hälfte ausreichend durchblutet geschlossen. Komplikationen wie Blutungen oder Luftembolie durch Bypass-Abschaltung sind vermeidbar, indem sichergestellt wird, dass der Bypass wird sorgfältig platziert und ordnungsgemäß gesichert.
In langfristige Überleben OLTx Experimenten wird die Gallenganganastomose aufgrund seiner hohen Komplikationsrate 19 als eine Schwachstelle. Die Gallengewebe ist sehr zerbrechlich und needs besondere Sorgfalt bei der Handhabung. Viele verschiedene Anastomose Techniken wurden beschrieben 5,19. Eine End-zu-End-Anastomose ist technisch einfach und mit minimalem Komplikationen 19 verbunden. Eine fortlaufende Naht mit einer nicht-schneidenden Nadel darunter große Abschnitte peribiliären Bindegewebe erscheint überlegen einer unterbrochenen Naht. Der Gallengang wird unter unnötige Spannung gesetzt, wenn die einzelnen Maschen der Knopfnaht verknotet werden. Dies kann in Gewebe Tränen und in Folge Galle Lecks führen. Das Nahtmaterial - resorbierbar oder nicht resorbierbar - ist in der Regel nicht von Bedeutung, da ihre begrenzte Lebensdauer, bis das Schwein wird beendet. Für langfristige Überleben Modelle über mehrere Monate, resorbierbares Nahtmaterial - bevorzugt - wie in der menschlichen OLTx.
Besondere Sorgfalt muss mit der postoperativen Follow-up genommen werden. Ausreichende Ernährung und Flüssigkeitszufuhr, eine zuverlässige Schmerzlinderung Protokoll und eine richtige ImmunsuppressionRegime sind obligatorisch. Für Langzeitversuche, erscheint Immunsuppression besonders wichtig. Im Vergleich zu anderen Säugetieren, Schweine zeigen eine überraschend geringe immunologische Abstoßung Rate nach OLTx 20,21. Knopfzelle Infiltrationen sind in der zweiten Woche nach der Transplantation maximale und verringern spontan auch ohne Immunsuppression. Die Ablehnung ist nur selten die Todesursache nach Schweine OLTx 22. Aber auch bei der Immunsuppression Protokoll mit der Verwaltung hier genannten Steroide iv und po Calcineurin-Inhibitoren, Transplantatabstoßung wird durch eine leichte Erhöhung der Transaminasen ab etwa 4 Tage nach OLTx angegeben und durch scheinbare Portal Feldrundzellinfiltration bestätigt. Calcineurin-Inhibitoren gegeben entweder po oder iv 23,24 25,26 werden; Beide Methoden haben Nachteile. Auch bei oraler Applikationshilfen, bleibt die tatsächliche Menge Erreichen des Gastrointestinaltraktes schwer fassbar. Auf der anderen Seite, kontinuierlichen iv-Infusion inein Schweinestall mit einer aktiven Tier ist schwierig. Daher muß der iv Applikation in Form eines Bolus, der in hohen Wirkstoffkonzentrationsspitzen zusammen mit potentiellen toxischen Wirkungen führt geführt werden. Dennoch beide Anwendungsverfahren anscheinend langfristige Überleben zu ermöglichen.
Ähnlich wie bei einer klinischen Umgebung, wird postoperativen Stress-Ulkus-Prophylaxe empfohlen. Postoperative Blutungen aus Magengeschwüren ist ein häufiges Problem und kann zu einer Leberfunktions 27 bezogen werden. Nach ein paar Fälle von Magen-Darm-Blutungen in beiden OLTx Gruppen begannen die Autoren regelmäßige Prophylaxe mit Pantoprazol und keine gastrointestinalen Blutungen seitdem erleben.
Strikte Aufrechterhaltung steriler Bedingungen, intraoperativ, vergleichbar mit den Verhältnissen in einer klinischen Operationsraum und folglich Antibiotikaprophylaxe, verringert das Risiko von infektiösen Komplikationen.
Zusammenfassend diesem Artikel provides praktische Informationen für den Aufbau einer Schweine OLTx Programm in einem Forschungs Einstellung. Ausreichend Engagement, Praxis und Teamarbeit ist, um die Lernphase zu verringern, um zuverlässige Ergebnisse zu erzeugen, und um die Kosten und die Anzahl der Versuchstiere zu reduzieren wichtig.
Offenlegungen
The authors have nothing to disclose.
Danksagungen
The study was supported by research grants from the Roche Organ Transplant Research Foundation (ROTRF) and Astellas. Markus Selzner was supported by an ASTS Career Development Award. Matthias Knaak was supported by the Astellas Research Scholarship. We thank Uwe Mummenhoff and the Birmingham family for their generous support.
Materialien
| Name | Company | Catalog Number | Comments |
| Atropine Sulphate 15 mg/30ml | Rafter 8 Products | 238481 | |
| Buprenorphine 0.3 mg/ml | RB Pharmaceuticals LDT | N/A | |
| Cefazolin 1 g | Pharmaceutical Partners of Canada Inc. | 2237138 | |
| Cyclosporin Oral Solution 5,000 mg/50 ml | Novartis Pharmaceuticals Canada Inc. | 2150697 | |
| Fentanyl Citrate 0.25 mg/5 ml | Sandoz Canada Inc. | 2240434 | |
| Heparin 10,000 iU/10 ml | Leo Pharma A/S | 453811 | |
| Isoflurane 99.9%, 250 ml | Pharmaceutical Partners of Canada Inc. | 2231929 | |
| Ketamine Hydrochloride 5000 mg/50 ml | Bimeda-MTC Animal Health Inc. | 612316 | |
| Lactated Ringer’s + 5% Dextrose, 0.5 L | Baxter Corporation | 61131 | |
| Lacteted Ringer’s, 1 L | Baxter Corporation | 61085 | |
| Metronidazole 500 mg/100 ml | Baxter Corporation | 870420 | |
| Midazolam 50 mg/10 ml | Pharmaceutical Partners of Canada Inc. | 2242905 | |
| Pantoprazole 40 mg | Sandoz Canada Inc. | 2306727 | |
| Potassium Chloride 40 mEq/20 ml | Hospira Healthcare Corporation | 37869 | |
| Propofol 1,000 mg/100 ml | Pharmascience Inc. | 2244379 | |
| Protamine Sulfate 50 mg/5 ml | Pharmaceutical Partners of Canada Inc. | 2139537 | |
| Saline 0.9%, 1 L | Baxter Corporation | 60208 | |
| Sodium Bicarbonate 50 mEq/50 ml | Hospira Healthcare Corporation | 261998 | |
| Solu-Medrol 500 mg | Pfizer Canada Inc. | 2367963 | |
| Tranexamic Acid 1,000 mg/10 ml | Pfizer Canada Inc. | 2064413 | |
| University of Wisconsin Solution, SPS-1 | Organ Recovery Systems | SPS-1 | |
| Xylocaine Endotracheal 10 mg/50 ml | AstraZeneca | 2003767 | |
| Appose ULC 35 W skin stapler | Covidien Canada | 803712 | |
| Maxon, 1 | Covidien Canada | 606173 | |
| Sofsilk, 0 | Covidien Canada | S606 | |
| Sofsilk, 2-0 | Covidien Canada | S405 | |
| Sofsilk, 3-0 | Covidien Canada | S404 | |
| Surgipro II, 4-0 | Covidien Canada | VP581X | |
| Surgipro II, 5-0 | Covidien Canada | VP725X | |
| Surgipro II, 6-0 | Covidien Canada | VP733X | |
| Catheter i.v, 18 G | BD Canada | 381147 | |
| Cook TPN catheter, 9.5 Fr | Cook Medical Company | C-TPNS-9.5-90 | |
| PSI Kit for sheath catheter, 8.5 Fr | Arrow International | ASK-09803-UHN | |
| Infusion Pump Line | Smith Medical ASD Inc. | 21-0442-25 | |
| Liver Admin Set (flush line) | CardioMed Supplies Inc | 17175 | |
| Mallinckrodt, Tracheal Tube, 6.5 mm | Covidien Canada | 86449 | |
| Med-Rx Suction Connecting Tube | Benlan Inc. | 70-8120 | |
| Organ Bag | CardioMed Supplies Inc | 2990 | |
| Suction Tip | Tyco Healthcare Group LP | 8888501023 | |
| Valleylab, Cautery Pencil | Covidien Canada | E2515H | |
| Valleylab, Patient Return Electrode | Covidien Canada | E7507 | |
| Bypass Connector 3/8” x 1/4“ | Raumedic AG | 955083-001 | |
| Bypass Connector 3/8” x 3/8” Luer Lock | Raumedic AG | 955163-001 | |
| Bypass Connector Y 3/8” x 3/8” x 1/4” | Raumedic AG | 961360-002 | |
| Bypass Tubing 1/4” x 1/16” | Raumedic AG | 039505-010 | |
| Bypass Tubing 3/8” x 3/32” | Raumedic AG | 039535-005 | |
| Rotaflow Centrifugal Pump | Maquet-Dynamed | HC 2821 | |
| Stainless Steel Hose Clamp Ring, 5mm | Oetiker | 16700007 | |
| Abdominal Retractor | Medite GmbH | N/A | |
| De Bakey – Beck, Infrahepatic Cava Clamp | Aesculap Inc. | FB519R | |
| Deithrich, Atraumatic Clamp (Portal Vein) | Aesculap Inc. | FB525R | |
| Gregory Bulldog Clamp, curved | Aesculap Inc. | FB382R | |
| Gregory Bulldog Clamp, straight | Aesculap Inc. | FB381R | |
| Potts – De Martel, Scissors | Aesculap Inc. | BC648R | |
| Satinsky, Suprahepatic Cava Clamp | Aesculap Inc. | FB605R | |
| Symetrical Tubing Clamp | Codman Instruments | 198010 | |
| Anesthesia Machine, Optimax | Moduflex Anesthesia Equipment | SN5180 | |
| Bypass Flow meter, HT 110 | Transonic Systems Inc. | HT110B11106 | |
| Flow meter probe, H6XL | Transonic Systems Inc. | H6Xl689 | |
| Heat Therapy Pump, T/Pump | Gaymar Industries Inc | TP500-G89D19 | |
| Infusion Pump 3,000 | SIMS Graseby LTD. | SN300050447 | |
| Isoflurane Vapor 19.1 | Draeger Medical Canada Inc. | N/A | |
| Monitor, Datex AS 3 | Instrumentarium Corp./ Hitachi | D-VHC14-23-02 | |
| Rotaflow Centrifugal Drive Unit | Maquet-Dynamed | 952301 | |
| Rotaflow Console | Maquet-Dynamed | 706035 | |
| Temperature Therapy Pad | Gaymar Industries Inc | TP26E | |
| Valleylab Force Tx | Valleylab Inc. | 216151480 | |
| Ventilator, AV 800 | DRE Medical Equipment | 40800AVV | |
| Warm Touch, Patient Warming System | Nellcor/ Covidien Canada | 5015300A |
Referenzen
- Mehrabi, A., Fonouni, H., Muller, S. A., Schmidt, J. Current concepts in transplant surgery: liver transplantation today. Langenbecks Arch. Surg. 393 (3), 245-260 (2008).
- Qiu, J., Ozawa, M., Terasaki, P. I. Liver transplantation in the United States. Clin. Transpl. , 17-28 (2005).
- Chalstrey, L. J. Technique of orthotopic liver transplantation in the pig. Br. J. Surg. 58 (3), 585-588 (1971).
- Esmaeilzadeh, M. Technical guidelines for porcine liver allo-transplantation: a review of literature. Ann. Transplant. 17 (2), 101-110 (2012).
- Calne, R. Y. Observations of orthotopic liver transplantation in the pig. Br. Med. J. 2 (5550), 478-480 (1967).
- Memsic, L., Quinones-Baldrich, W., Kaufman, R., Rasool, I., Busuttil, R. W. A comparison of porcine orthotopic liver transplantation using a venous-venous bypass with and without a nonpulsatile perfusion pump. J. Surg. Res. 41, 33-40 (1986).
- Torres, O. J. Hemodynamic alterations during orthotopic liver experimental transplantation in pigs. Acta. Cir. Bras. 23 (2), 135-139 (2008).
- Battersby, C., Hickman, R., Saunders, S. J., Terblanche, J. Liver function in the pig. 1. The effects of 30 minutes' normothermic ischaemia. Br. J. Surg. 61 (1), 27-32 (1974).
- Smith, A. C., Swindle, M. M. Preparation of swine for the laboratory. Ilar. J. 47 (4), 358-363 (2006).
- Swindle, M. M., Smith, A. C. Best practices for performing experimental surgery in swine. J. Invest. Surg. 26 (2), 63-71 (2013).
- Moench, C., Moench, K., Lohse, A. W., Thies, J., Otto, G. Prevention of ischemic-type biliary lesions by arterial back-table pressure perfusion. Liver Transpl. 9 (3), 285-289 (2003).
- Koski, E. M., Suhonen, M., Mattila, M. A. Ultrasound-facilitated central venous cannulation. Crit. Care Med. 20 (3), 424-426 (1992).
- Lange, J. J., Hoitsma, H. F., Meijer, S. Anaesthetic management in experimental orthotopic liver transplantation in the pig. Eur. Surg. Res. 16 (6), 360-365 (1984).
- Kaiser, G. M., Heuer, M. M., Fruhauf, N. R., Kuhne, C. A., Broelsch, C. E. General handling and anesthesia for experimental surgery in pigs. J. Surg. Res. 130 (1), 73-79 (2006).
- Heuer, M. Liver transplantation in swine without venovenous bypass. Eur. Surg. Res. 45 (1), 20-25 (2010).
- Gruttadauria, S. Porcine orthotopic liver autotransplantation: facilitated technique. J. Invest. Surg. 14 (2), 79-82 (2001).
- Falcini, F. Veno-venous bypass in experimental liver transplantation: portal-jugular versus caval-portal-jugular. G. Chir. 11 (4), 206-210 (1990).
- Filipponi, F., Benassai, C., Falcini, F., Martini, E., Cataliotti, L. Biliary tract complications in orthotopic liver transplantation: an experimental study in the pig. Ital. J. Surg. Sci. 19 (2), 131-136 (1989).
- Terblanche, J. Orthotopic liver homotransplantation: an experimental study in the unmodified pig. S. Afr. Med. J. 42 (20), 486-497 (1968).
- Calne, R. Y. Prolonged survival of liver transplants in the pig. Br. Med. J. 4 (5580), 645-648 (1967).
- Battersby, C., Egerton, W. S., Balderson, G., Kerr, J. F., Burnett, W. Another look at rejection in pig liver homografts. Surgery. 76 (4), 617-623 (1974).
- Net, M. The effect of normothermic recirculation is mediated by ischemic preconditioning in NHBD liver transplantation. Am. J. Transplant. 5 (10), 2385-2392 (2005).
- Guarrera, J. V. Hypothermic machine perfusion of liver grafts for transplantation: technical development in human discard and miniature swine models. Transplant Proc. 37 (1), 323-325 (2005).
- Minor, T. Hypothermic reconditioning by gaseous oxygen improves survival after liver transplantation in the pig. Am. J. Transplant. 11 (12), 2627-2634 (2011).
- Kelly, D. M. Porcine partial liver transplantation: a novel model of the 'small-for-size' liver graft. Liver Transpl. 10 (2), 253-263 (2004).
- Meijer, S., Hoitsma, H. F., Visser, J. J., de Lange, J. J. Long term survival following orthotopic liver transplantation in pigs; with special reference to gastric ulcer complications. Neth. J. Surg. 36 (6), 168-171 (1984).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten