Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Disección de Host-virus Interacción en la replicación lítica de un Herpesvirus Modelo
En este artículo
Resumen
Se describe un protocolo para identificar las principales funciones de las moléculas de señalización de acogida en la replicación lítica de un modelo herpesvirus, virus herpes gamma 68 (γHV68). La utilización de cepas de ratón modificados genéticamente y los fibroblastos embrionarios de γHV68 replicación lítica, el protocolo permite tanto la caracterización fenotípica y molecular de las interacciones interrogatorio virus-huésped durante la replicación viral lítico.
Resumen
En respuesta a la infección viral, un huésped desarrolla varias respuestas de defensa, tales como la activación de las vías inmunológicas innatas de señalización que conducen a la producción de citoquinas 1,2 antiviral. Con el fin de colonizar el huésped, los virus son obligado a evadir las respuestas del huésped antivirales y manipular las vías de señalización. Desentrañar la interacción huésped-virus arrojará luz sobre el desarrollo de nuevas estrategias terapéuticas contra la infección viral.
Murine γHV68 está estrechamente relacionado con el sarcoma de Kaposi asociado a humano oncogénico del virus del herpes y Epsten-Barr 3,4. γHV68 infección en ratones de laboratorio proporciona un modelo de animal pequeño manejable para examinar todo el curso de las respuestas del huésped y la infección viral in vivo, que no están disponibles para los herpesvirus humanos. En este protocolo, se presenta un grupo de métodos para la caracterización fenotípica y molecular disección de componentes de sistema principal de señalización en γHV68 replic líticoación tanto in vivo como ex vivo. La disponibilidad de las cepas de ratón modificados genéticamente permite la interrogación de los papeles de las rutas de señalización de acogida durante γHV68 infección aguda in vivo. Además, fibroblastos embrionarios de ratón (MEFs) aisladas a partir de estas cepas de ratón deficientes se puede utilizar para diseccionar las funciones de estas moléculas durante γHV68 vivo ex lítico de replicación.
El uso de ensayos de biología molecular y virológicos, podemos señalar el mecanismo molecular de la interacción virus-huésped y anfitrión identificar y genes virales esenciales para la replicación viral lítica. Finalmente, un cromosoma artificial bacteriano (BAC) sistema facilita la introducción de mutaciones en el factor viral (s) que específicamente interrumpir la interacción huésped-virus. Recombinante γHV68 llevar estas mutaciones se puede utilizar para recapitular los fenotipos de γHV68 replicación lítica en MEFs deficientes en la clave de host componentes de señalización.Este protocolo ofrece una excelente estrategia para interrogar interacción huésped-patógeno en múltiples niveles de intervención in vivo y ex vivo.
Recientemente, se ha descubierto que γHV68 usurpa una vía de señalización inmune innata para promover la replicación viral lítico 5. Específicamente, γHV68 de novo infección activa la quinasa IKKβ inmune y IKKβ activada fosforila el factor de transcripción viral maestro, la replicación y transactivador (RTA), para promover la activación transcripcional viral. Al hacerlo, γHV68 eficientemente su pareja de activación transcripcional de acoger la activación inmune innata, facilitando de ese modo la transcripción y la replicación viral lítica. Este estudio proporciona un excelente ejemplo de que se puede aplicar a otros virus para interrogar a la interacción huésped-virus.
Protocolo
1. Ratón infección con γHV68
- De seis a ocho semanas de edad, género de concordancia de ratones hermanos de camada (8 a 12 ratones / grupo) se utilizan para la infección viral. Permitir ratones para aclimatarse durante cuatro días completos (96 horas) después del envío.
- Protocolo de pasos utilizando virus debe llevarse a cabo en un gabinete de bioseguridad de nivel 2 (BSL2) usando BSL2 precauciones.
- Preparar una suspensión viral (40 a 1 x 10 5 unidades formadoras de placa [UFP]) de γHV68 en 30 l de PBS estéril por ratón justo antes del experimento. Mantenga suspensión viral en hielo.
- Preparar la solución de ketamina / xilazina (1,5 mg de ketamina y 0,15 mg xylazine/20 g de peso corporal, 100 l / ratón) para la sedación ratón. Asegúrese de que los ratones han sido sedados mediante la realización de un sujetador del pie.
- Sedate ratones con ketamina 1,5 mg y 0,15 mg por xilazina 20 mg de peso corporal (100 l / ratón) por inyección intra-peritoneal.
- Entregar suspensión viral (30 l / ratón) por vía intranasal, en un gota a gotamoda, a una ventana de la nariz de los ratones sedados.
- Lay ratones en un lado durante 5 - 10 min para facilitar la entrega de las vías respiratorias del virus en el pulmón.
- Ratones vuelva a colocarlo en ratones jaula y el monitor hasta que se hayan recuperado totalmente de la sedación.
- En varios días después de la infección, sacrificar los ratones por asfixia de CO 2 y la cosecha de los pulmones después de asegurar la muerte / pérdida del conocimiento profundo. Coloque los pulmones en estériles de 1,5 ml con tapón de rosca tubos que contienen 500 l de 1,0 mm de zirconia / sílice cuentas. Mantenga los tubos en hielo. Almacene las muestras a -80 ° C si no se continuar con el paso siguiente en el mismo día. El bazo o tejido del hígado podría ser recogidos en este momento para el análisis de la latencia viral en función de marco de tiempo del experimento.
- Añadir 1 ml de frío DMEM libre de suero en el tubo y homogeneizar los pulmones por bead-latidos 30 segundos. Enfriar los tubos en hielo durante al menos 1 min. Repita este proceso una vez.
- Pulmón centrífuga lisados a 16.000 RCF a 4 ° C durante 1 min y utilizar supernatant para determinar el título viral mediante un ensayo en placa utilizando una monocapa NIH3T3 o BHK21 (véase la Sección 5 para más detalles).
2. Determinar γHV68 varios pasos cinética de crecimiento de fibroblastos de embriones de ratón
- Grow tipo salvaje fibroblastos embrionarios de ratón (MEFs) y deficientes en un gen del huésped a sub-confluente (aproximadamente 80%) antes de la densidad de células en placas.
- Dividir en MEFs 24-así placa a 10.000 células / pocillo para un bajo multipilicity-de-infección (MOI) en el día antes de la infección. Los experimentos se llevan a cabo normalmente por triplicado y en un MOI entre 0,001 a 0,05 se utiliza generalmente.
- Preparar γHV68 suspensión que contiene la cantidad deseada de virus (0,5 ml por pocillo).
- Eliminar el medio y cubrir MEFs con 0,5 ml de γHV68 suspensión por pocillo.
- Se incuba la placa en la incubadora de cultivo de tejidos, roca cada 30 min, y permitir incubación proceder durante 2 h.
- Retire suspensión viral, y cubra las células con 0,5 ml fresco complete medio DMEM que contenía 8% de suero bovino fetal.
- En días diferentes después de la infección, se recoge el medio y las células en tubos de 1,5 ml estériles de centrífuga. Inmediatamente congelar tubos a -80 ° C.
- Release γHV68 de MEFs por congelación a -80 ° C, la descongelación en 37 ° C baño de agua y agitar. Tres ciclos de congelación y descongelación se aplica generalmente a las muestras.
- Determinar el título viral en un ensayo en placa utilizando una monocapa NIH3T3 o BHK21 (véase la Sección 5 para más detalles).
- Lea título viral y la trama γHV68 varios pasos curva de crecimiento en MEFs.
3. Disección molecular de la replicación lítica γHV68 en fibroblastos de embriones de ratón
- Realice una infección viral como se describe en los pasos 2.1 a 2.6 de la sección 2.
- En días diferentes después de la infección, descartar el sobrenadante. Enjuagar las células con PBS frío y células Tripsinizar. Pellet las células por centrifugación a 1.000 RCF a temperatura ambiente durante 1 min. Eliminar el sobrenadante yLas células se almacena a -80 ° C.
- Extraer el ADN total (anfitrión y el genoma viral) y el ARN total de acuerdo con métodos previamente publicados 5,6.
- Realizar PCR en tiempo real utilizando ADN total y cebadores específicos para transcripciones virales líticos, tales como RTA (ORF50), ORF57 y ORF60. Determinar la cantidad relativa de intracelular γHV68 genoma en referencia a un gen de mantenimiento de acogida (por ejemplo, β-actina).
- Para eliminar la contaminación de ADN genómico, el tratamiento con RNasa libre de DNasa es crítica para la preparación de ADNc con ARN total y oligo (dT) 11-19. Ver referencia 5 para más detalles sobre la extracción de ARN, incluyendo el tratamiento con RNasa libre de DNasa y RT-PCR. Realizar PCR en tiempo real utilizando cebadores y ADNc como anteriormente para determinar la cantidad relativa de transcritos virales en referencia a la del gen del huésped de limpieza.
4. Generación de recombinantes utilizando γHV68 cromosoma artificial bacteriano
La metod describe aquí se usa para introducir mutaciones en un gen γHV68 que está implicado en la interacción huésped-virus.
- Preparar un fragmento de ADN (aproximadamente 1,5 kb) de secuencia de tipo salvaje o la secuencia que llevan mutaciones deseadas en la región central por PCR.
- Preparar cromosoma artificial bacteriano (BAC) que contiene un transposón inserción 7 alrededor del sitio de la mutación, que específicamente se inactiva el gen gen de interés, por midi escala purificación (OriGene). Tienda BAC ADN a 4 º C (evitar la congelación / descongelación del ADN de BAC).
- Transfectar ADN de BAC y el producto de PCR que contenía las mutaciones deseadas del gen de interés en células (por ejemplo, NIH3T3 o BHK21), que son altamente permisiva para la replicación lítica γHV68, con Lipofectamine 2000 (Invitrogen).
- Mantenga dividir celdas hasta que el efecto citopático (CPE) se muestra en la monocapa. Recoger sobrenadante que contenía virus y, si es necesario, amplificar virus en células NIH3T3 o BHK21.
- Infect células NIH3T3 convirus recombinante por centrifugación a 1.800 rpm, 30 º C durante 30 min.
- Cosecha γHV68 infectadas NIH3T3 células y preparar genoma viral mediante el protocolo circularized Hirt 8,9.
- Electro-MAX transformar células DH10B competentes (Invitrogen) por electroporación y la pantalla de colonias que son la resistencia a cloranfenicol (Cm), pero sensibles a la kanamicina (Kan) (Cm gen resistente a la columna vertebral está en BAC, mientras que Kan gen resistente es en transposón inserción).
- Crecer colonias Cm R S Kan en chlorophenicol medio que contiene y preparar BAC ADN con la purificación o mini-midi escala-(OriGene).
- Verificar la mutación deseada en el gen diana mediante PCR, utilizando cebadores específicos para las regiones flanqueantes del sitio de la mutación, y la secuenciación.
- Confirmar no reordenamiento cromosómico en BAC por digestión con enzimas de restricción seleccionados y de campo de pulsos electroforesis en gel.
- Transfectar BAC recombinante en células NIH 3T3 o BHK21 con Lipofectamine2000 (Invitrogen) para preparar recombinante γHV68.
- Mantenga pases células hasta CPE se muestra en la monocapa. Recoger sobrenadante que contenía virus y amplificar recombinante γHV68 en NIH3T3 o células BHK21.
- Determinar el título del virus recombinante y caracterizar las propiedades de crecimiento viral ex vivo e in vivo como se describe en las secciones 1 y 2.
5. Determinar el título viral por un ensayo de placa
- Crecer las células NIH3T3 a sub-confluente (aproximadamente 80%) antes de densidad células en placas.
- Dividir NIH3T3 en 24 y placas a 20.000 células / pocillo en el día antes de la infección.
- Preparar 10-veces sobrenadantes de virus en serie diluidas con medio DMEM que contenía 8% de suero de ternero recién nacido (NCS).
- Eliminar el medio y cubrir las células NIH3T3 con 0,5 ml de suspensión γHV68.
- Incubar la placa de cultivo de tejidos incubadora, mueva cada 30 minutos, y permite la incubación de procederdurante 2 h.
- Eliminar suspensión viral y células cubren con 0,5 ml de medio DMEM que contiene 2% NCS y 0,75% de metilcelulosa (Sigma).
- Se incuba la placa en la incubadora de cultivo tisular. Contar las placas en el día 6 después de la infección. La tinción de la monocapa, por ejemplo, con violeta de cristal, puede facilitar el recuento de placa.
- Calcular el título viral en los lisados de tejidos sin diluir o lisados celulares usando la siguiente fórmula: Título (UFP / ml) = D x N x 1000 l / ml ÷ l V. N, la media de número de la placa a una dilución apropiada; D, diluciones (por ejemplo, 5, 10, 100 .....) V (l), el volumen de sobrenadante diluido en serie por pocillo.
6. Los resultados representativos:
Tres figuras representativas se muestran aquí, incluyendo γHV68 replicación lítica en el pulmón de tipo salvaje y los Mavs - / - ratón 10, γHV68 fenotipos de replicación líticas en fibroblastos de embriones de ratón (MEF), y recombinhormiga γHV68 que llevan mutaciones en los sitios de fosforilación que son moduladas por la IKKβ MAVS-dependiente. Estos tres experimentos que corroboran constituir un esquema para definir las funciones de defensa innata en γHV68 replicación lítica in vivo y ex vivo.

Figura 1 γHV68 cargas en los pulmones de los Mavs + / + y los Mavs -. / - Ratones. A) Dos vías de señalización innata principal aguas abajo de MAVS. Los Mavs relés adaptador de moléculas de señalización de citosólicas RIG-I-como los receptores para activar NF-kB y los factores reguladores del interferón (IRF) que, a su vez, hasta de regular la expresión génica de citocinas proinflamatorias y los interferones. B) Mavs + / + y - / - Mavs ratones fueron infectados con 40 PFU γHV68 intranasal y las cargas virales en el pulmón en los puntos de tiempo indicados se determinaron minado por un ensayo en placa usando NIH3T3 monocapa. Cada símbolo representa un ratón.
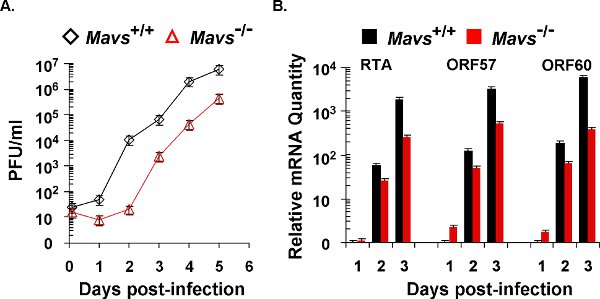
Figura 2. ΓHV68 cinética de replicación líticas en fibroblastos embrionarios de ratón (MEFs). La replicación lítica de γHV68 en Mavs + / + y Mavs - / - MEFs se evaluó por las curvas de crecimiento de varios pasos (A) y cuantitativa en tiempo real PCR (B). Para ambos experimentos, igual número de MEFs y la cantidad de γHV68 se utilizaron para la infección viral a una multiplicidad de infección (MOI) de 0,01. (A) Las células y los sobrenadantes se cosecharon a los puntos de tiempo indicados y sujeto a una placa de ensayo para determinar los títulos virales. (B) ARN total fue extraído a partir de γHV68-infectada MEFs y se analizaron por cuantitativa en tiempo real PCR con cebadores específicos para determinados transcripciones líticas (RTA, ORF57, ORF60 y).
ig3.jpg "/>
Figura 3. La cinética de replicación líticas de γHV68 recombinantes que llevan mutaciones en el dominio de transactivación RTA que suprimen la fosforilación por IKKγ. (A) de varios pasos curvas de crecimiento recombinante de virus de tipo salvaje (γHV68.wt) y el virus mutante (γHV68.mut) en Mavs + / + y Mavs - / - células MEFs (MOI = 0,01). MEFs fueron infectadas con γHV68 a una MOI de 0,01. Las células y los sobrenadantes se cosecharon a los puntos de tiempo indicados y los títulos virales se determinaron mediante un ensayo en placa usando monocapa NIH 3T3. (B) γHV68 RTA nivel de ARNm en γHV68 infectadas con células NIH3T3 (MOI = 0,01). En 30 h después de la infección, el ARN total fue extraído a partir de células infectadas con γHV68 NIH 3T3 y se analizaron por cuantitativa en tiempo real PCR.
Discusión
En respuesta a la infección viral, los MAVS dependientes de las vías inmunológicas innatas de señalización se activan para promover la producción de citoquinas inflamatorias antivirales 10-14. Uso de murino γHV68 como un virus modelo para asociado al sarcoma de Kaposi humano oncogénico del virus del herpes y virus de Epstein-Barr 3,4, descubrimos que γHV68 usurpa la vía MAVS-IKKβ para promover la replicación lítico viral a través de la activación transcripcional 5. Emplean...
Divulgaciones
No hay conflictos de interés declarado.
Agradecimientos
Los autores desean agradecer al Dr. James (Zhijian) Chen (UT Southwestern, Biología Molecular) para proporcionar reactivos esenciales, incluidos los Mavs - / - ratones, y el Dr. Ren Sol (Universidad de California-Los Angeles, Farmacología y Medicina Molecular ) para proporcionar el cromosoma bacteriano artificial de γHV68 para este estudio.
Materiales
| Name | Company | Catalog Number | Comments |
| Nombre del reactivo | Empresa | Número de catálogo | |
| Lipofectamine 2000 | Invitrogen | 11668-019 | |
| Electro-MAX DH10B células competentes | Invitrogen | 18290-015 | |
| Metilcelulosa | Sigma | M0512 | |
| POWERPREP HP plásmido Sistema Miniprep | OriGene | NP100004 | |
| POWERPREP HP plásmido Sistema Midiprep | OriGene | NP100006 |
Referencias
- Akira, S., Uematsu, S., Takeuchi, O. Pathogen recognition and innate immunity. Cell. 124, 783-801 (2006).
- Medzhitov, R. Recognition of microorganisms and activation of the immune response. Nature. 449, 819-826 (2007).
- Speck, S. H., Virgin, H. W. Host and viral genetics of chronic infection: a mouse model of gamma-herpesvirus pathogenesis. Curr. Opin. Microbiol. 2, 403-409 (1999).
- Speck, S. H., Ganem, D. Viral latency and its regulation: lessons from the gamma-herpesviruses. Cell Host Microbe. 8, 100-115 (2010).
- Dong, X. Murine gamma-herpesvirus 68 hijacks MAVS and IKKbeta to initiate lytic replication. PLoS Pathog. 6, e1001001-e1001001 (2010).
- Strauss, W. M., Ausubel, F. M. Preparation of genomic DNA from mammalian tissues. Current Protocols in Molecular Biology. , 2-2 (1998).
- Song, M. J. Identification of viral genes essential for replication of murine gamma-herpesvirus 68 using signature-tagged mutagenesis. Proc. Natl. Acad. Sci. U. S. A. 102, 3805-3810 (2005).
- Hirt, B. Selective extraction of polyoma DNA from infected mouse cell cultures. J. Mol. Biol. 26, 365-369 (1967).
- Eva-Maria Borst, E., Crnkovic-Mertens, I., Messerle, M., Zhao, S., Stodolsky, M. Cloning of β-herpesvirus genomes as bacterial artificial chromosomes. Methods in Molecular Biology. , 256-256 (2004).
- Sun, Q. The specific and essential role of MAVS in antiviral innate immune responses. Immunity. 24, 633-642 (2006).
- Seth, R. B., Sun, L., Ea, C. K., Chen, Z. J. Identification and characterization of MAVS, a mitochondrial antiviral signaling protein that activates NF-kappaB and IRF 3. Cell. 122, 669-682 (2005).
- Kawai, T. IPS-1, an adaptor triggering RIG-I- and Mda5-mediated type I interferon induction. Nat. Immunol. 6, 981-988 (2005).
- Meylan, E. Cardif is an adaptor protein in the RIG-I antiviral pathway and is targeted by hepatitis C virus. Nature. 437, 1167-1172 (2005).
- Xu, L. G. VISA is an adapter protein required for virus-triggered IFN-beta signaling. Mol. Cell. 19, 727-740 (2005).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados