Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Dissection hôte-virus interaction dans la réplication lytique d'un virus de l'herpès modèle
Dans cet article
Résumé
Nous décrivons un protocole pour identifier les rôles clés des molécules de l'hôte de signalisation dans la réplication lytique d'un virus de l'herpès modèle, gamma herpèsvirus 68 (γHV68). L'utilisation de lignées de souris génétiquement modifiées et des fibroblastes embryonnaires de γHV68 réplication lytique, le protocole permet à la fois la caractérisation phénotypique et moléculaire de l'interrogatoire interactions virus-hôte dans la réplication virale lytique.
Résumé
En réponse à une infection virale, une foule se développe diverses réactions défensives, telles que l'activation de l'immunité innée voies de signalisation qui conduisent à la production de cytokines 1,2 antiviral. Afin de coloniser l'hôte, les virus sont obligatoire pour échapper réponses de l'hôte antiviraux et de manipuler des voies de signalisation. Démêler l'interaction hôte-virus fera la lumière sur le développement de nouvelles stratégies thérapeutiques contre l'infection virale.
ΓHV68 murin est étroitement liée à oncogène humain sarcome de Kaposi associé au virus de l'herpès et Epsten-Barr 3,4. γHV68 infection chez les souris de laboratoire fournit un modèle animal docile petite pour examiner toute la durée de réponse de l'hôte et l'infection virale in vivo, qui ne sont pas disponibles pour les herpèsvirus humains. Dans ce protocole, nous vous présentons un panel de méthodes de caractérisation phénotypique et dissection moléculaire des composants de l'hôte de signalisation dans γHV68 replic lytiquetion à la fois in vivo et ex vivo. La disponibilité de souches de souris génétiquement modifiées permet l'interrogation des rôles des voies de signalisation hôtes pendant γHV68 infection aiguë in vivo. En outre, des fibroblastes embryonnaires de souris (MEF) isolés à partir de ces souches de souris déficientes peut en outre être utilisé pour décortiquer les rôles de ces molécules in vivo au cours de γHV68 réplication lytique ex.
En utilisant des tests de biologie moléculaire et virologiques, nous pouvons identifier le mécanisme moléculaire de interactions hôte-virus et d'identifier l'hôte et des gènes viraux essentiels à la réplication virale lytique. Enfin, un chromosome artificiel bactérien (BAC) système facilite l'introduction de mutations dans le facteur viral (s) spécifiquement interrompre l'interaction hôte-virus. ΓHV68 recombinant portant ces mutations peuvent être utilisés pour récapituler les phénotypes de γHV68 réplication lytique dans les MEF déficientes en clé d'hôte de signalisation composants.Ce protocole offre une excellente stratégie pour interroger interaction hôte-pathogène à de multiples niveaux d'intervention in vivo et ex vivo.
Récemment, nous avons découvert que γHV68 usurpe une voie de signalisation immunitaire inné pour promouvoir la réplication virale lytique 5. Plus précisément, γHV68 infection de novo active la kinase IKKβ immunitaire et IKKβ activée phosphoryle le facteur de transcription virale maître, de réplication et de transactivateur (RTA), afin de promouvoir virale activation de la transcription. Ce faisant, γHV68 efficacement son activation transcriptionnelle couples d'accueillir l'activation immunitaire innée, ce qui facilite la transcription virale et la réplication lytique. Cette étude fournit un excellent exemple de ce que peut être appliqué à d'autres virus d'interroger les interactions hôte-virus.
Protocole
1. L'infection de souris avec γHV68
- Souris même portée de six à huit semaines vieux, genre assortie (8 à 12 souris / groupe) sont utilisés pour l'infection virale. Permettez-souris pour s'acclimater pendant quatre jours complets (96 heures) après l'expédition.
- Étapes du protocole à l'aide de virus doit être effectué dans un cabinet de biosécurité de niveau 2 (BSL2) en utilisant des BSL2 précautions.
- Préparer une suspension virale (40 à 1 x 10 5 unités formant des plages [UFP]) de γHV68 dans 30 ul de PBS stérile par souris juste avant l'expérience. Gardez suspension virale sur la glace.
- Préparer la solution de kétamine / xylazine (1,5 mg de kétamine et de 0,15 mg xylazine/20 g de poids corporel, 100 ul / souris) pour la sédation de la souris. Assurez-vous que les souris ont été mis sous sédation en effectuant un pincement de l'orteil.
- Souris calmes avec 1,5 mg de kétamine et de 0,15 mg de xylazine par 20 mg de poids corporel (100 ul / souris) par injection intra-péritonéale.
- Livrer suspension virale (30 ul / souris) par voie intranasale, en goutte à gouttela mode, à une narine de la souris sous sédation.
- Lay souris sur un côté pendant 5 - 10 minutes pour faciliter la livraison du virus des voies respiratoires dans les poumons.
- Replacez les souris chez la souris et le moniteur cage jusqu'à ce qu'ils aient complètement remis de la sédation.
- À différents jours après l'infection, le sacrifice des souris par le CO 2 asphyxie et la récolte des poumons après avoir assuré la mort / perte de conscience profonde. Placez-les dans les poumons stériles de 1,5 ml tubes à bouchon vissé contenant 500 ul de 1,0 mm en zircone / silice perles. Garder les tubes sur la glace. Conserver les échantillons à -80 ° C, sinon passer à l'étape suivante, le même jour. La rate ou foie pourraient être recueillies à ce moment pour l'analyse de la latence virale en fonction de délai d'expérience.
- Ajouter 1 ml d'eau froide DMEM sans sérum dans le tube et homogénéiser les poumons en perles battant 30 secondes. Refroidir les tubes sur la glace pendant au moins 1 min. Répétez cette procédure qu'une seule fois.
- Centrifugeuse poumon lysats à 16.000 rcf à 4 ° C pendant 1 min et utiliser supernatant pour déterminer le titre viral par un dosage de la plaque à l'aide d'une monocouche NIH3T3 ou BHK21 (voir la section 5 pour plus de détails).
2. Déterminer γHV68 cinétique de croissance multi-étapes dans les fibroblastes embryonnaires de souris
- Développer des fibroblastes de souris de type sauvage embryonnaires (MEF) et les lacunes dans un gène de l'hôte à la sous-confluence (environ 80%) de densité avant étalement des cellules.
- Séparer les MEF en 24 et la plaque à 10.000 cellules / puits pour une faible multipilicity-de-infection (MOI) le jour avant l'infection. Des expériences sont normalement effectuées en triple et à une MOI entre 0,001 à 0,05 est généralement utilisé.
- Préparer γHV68 suspension contenant la quantité désirée de virus (0,5 ml par puits).
- Retirer moyen et couvrir MEF avec 0,5 ml de suspension γHV68 par puits.
- Incuber la plaque de culture de tissu incubateur, rock toutes les 30 minutes, et de permettre l'incubation poursuivie pendant 2 h.
- Levée de la suspension virale, et couvrir les cellules avec 0,5 ml fraîche cemplissez milieu DMEM contenant 8% de sérum bovin foetal.
- À différents jours après l'infection, la récolte du milieu et les cellules dans des tubes à centrifuger stérile de 1,5 ml. Geler immédiatement les tubes à -80 ° C.
- Communiqué de γHV68 MEF par congélation à -80 ° C, la décongélation à 37 ° C et bain d'eau vortex. Trois cycles de gel et de dégel est généralement appliquée aux échantillons.
- Déterminer le titre viral par un dosage de la plaque à l'aide d'une monocouche NIH3T3 ou BHK21 (voir la section 5 pour plus de détails).
- Lire titre viral et l'intrigue γHV68 courbe de croissance multi-étape sur la MEF.
3. Dissection moléculaire de la réplication lytique γHV68 dans les fibroblastes embryonnaires de souris
- Effectuer une infection virale comme décrit dans les étapes 2.1 à 2.6 de la section 2.
- À différents jours après l'infection, éliminer le surnageant. Rincer les cellules avec du PBS froid et les cellules Trypsiniser. Sédimenter les cellules par centrifugation à 1.000 rcf à température ambiante pendant 1 min. Jeter le surnageant etcellules conserver à -80 ° C.
- Extraire l'ADN total (hôte et le génome viral) et l'ARN total selon les méthodes précédemment publiées 5,6.
- Effectuer PCR en temps réel en utilisant l'ADN total et des amorces spécifiques de transcription viraux lytiques, tels que RTA (ORF50), ORF57 et ORF60. Déterminer la quantité relative de γHV68 intracellulaire du génome en référence à un gène de ménage hôte (par exemple, β-actine).
- À éliminer la contamination de l'ADN génomique, le traitement par la DNase sans RNase est essentielle pour la préparation d'ADNc de l'ARN total et d'oligo (dT) 11-19 amorce. Reportez-vous à la référence 5 pour plus de détails sur l'extraction de l'ARN, y compris le traitement à la RNase-Free DNase et RT-PCR. Effectuer PCR en temps réel en utilisant l'ADNc et des amorces comme ci-dessus pour déterminer la quantité relative des transcrits viraux en référence à celle du gène de ménage d'accueil.
4. Génération recombinant utilisant γHV68 chromosomes bactériens artificiels
La méthod décrit ici est utilisé pour introduire des mutations dans un gène γHV68 qui est impliqué dans l'interaction hôte-virus.
- Préparer un fragment d'ADN (environ 1,5 kb) de séquence de type sauvage ou une séquence portant des mutations désirées dans la zone centrale par PCR.
- Préparer chromosome artificiel bactérien (BAC) qui contient une insertion du transposon 7 autour du site de mutation qui inactive le gène spécifique du gène d'intérêt, par purification midi-échelle (OriGene). Magasin d'ADN de BAC à 4 ° C (éviter le gel / dégel ADN de BAC).
- Transfecter ADN de BAC et du produit de PCR contenant les mutations désirées du gène d'intérêt dans les cellules (par exemple, NIH3T3 ou BHK21), qui sont très permissives à la réplication lytique γHV68, avec Lipofectamine 2000 (Invitrogen).
- Gardez séparer les cellules jusqu'à ce que l'effet cytopathogène (ECP) apparaît dans la monocouche. Recueillir contenant le virus surnageant et, si nécessaire, d'amplifier le virus dans les cellules NIH3T3 ou BHK21.
- Infecter des cellules NIH3T3 avecle virus recombinant par centrifugation à 1.800 tours par minute, 30 ° C pendant 30 min.
- Récolte γHV68 infectés par des cellules NIH3T3 et préparer circularisé génome viral en utilisant le protocole Hirt 8,9.
- Transformez Electro-MAX cellules DH10B compétentes (Invitrogen) par électroporation et un écran pour les colonies qui sont résistants au chloramphénicol (Cm), mais sensible à la kanamycine (Kan) (Cm gène de résistance est en épine dorsale BAC, Kan-gène de résistance est en transposon d'insertion).
- Croître les colonies Cm R S Kan dans un milieu contenant chlorophenicol et préparer ADN de BAC à la purification des mini ou midi-échelle (OriGene).
- Vérifier la mutation désirée dans le gène cible par PCR, en utilisant des amorces spécifiques aux régions flanquantes de site de mutation, et le séquençage.
- Confirmer l'absence de réarrangement chromosomique en BAC par digestion avec des enzymes de restriction choisies et l'électrophorèse en champ pulsé.
- Transfecter BAC recombiné dans des cellules NIH 3T3 ou BHK21 avec Lipofectamine2000 (Invitrogen) pour préparer recombinant γHV68.
- Gardez passage de cellules jusqu'à CPE apparaît dans la monocouche. Recueillir le surnageant contenant le virus recombinant et amplifier γHV68 dans NIH3T3 ou BHK21 cellules.
- Déterminer le titre du virus recombinant et de caractériser les propriétés de croissance virale ex vivo et in vivo, comme décrit dans les sections 1 et 2.
5. Déterminer le titre viral par un dosage de la plaque
- Cultiver des cellules NIH3T3 à la sous-confluence (environ 80%) de densité avant étalement des cellules.
- Diviser NIH3T3 en 24 et plaque à 20.000 cellules / puits le jour avant l'infection.
- Préparer un facteur 10 surnageants de virus dilué en série avec un milieu DMEM contenant 8% de sérum de veau nouveau-né (NCS).
- Retirer moyen et couvrir les cellules NIH3T3 avec 0,5 ml de suspension γHV68.
- Incuber la plaque en incubateur de culture tissulaire, du rock toutes les 30 min, et permettent d'incubation de procéderpendant 2 h.
- Retirer suspension virale et des cellules de couverture avec 0,5 ml du milieu DMEM contenant 2% de NCS et la méthylcellulose à 0,75% (Sigma).
- Incuber la plaque en incubateur de culture tissulaire. Comptez plaques au jour 6 après l'infection. La coloration de la monocouche, par exemple avec du violet de cristal, peut faciliter le comptage plaque.
- Calculer le titre viral dans les lysats de tissus non dilués ou lysats cellulaires en utilisant la formule suivante: Titre (UFP / ml) = D x N x 1000 pl / ml ÷ V pi. N, le nombre moyen de plaque à une dilution appropriée, D, dilutions (comme le 5, 10, 100 .....) V (pi), volume de surnageant dilué en série par puits.
6. Les résultats représentatifs:
Trois figures représentatives sont présentées ici, y compris γHV68 réplication lytique dans le poumon de type sauvage et Mavs - / - souris 10, γHV68 phénotypes de réplication lytiques dans les fibroblastes embryonnaires de souris (MEF), et recombinant γHV68 portant des mutations dans les sites de phosphorylation qui sont modulés par l'IKKβ MAVS-dépendante. Ces trois expériences concordantes de créer un régime de définir les rôles des composantes immunitaires innées dans γHV68 réplication lytique in vivo et ex vivo.

Figure 1 γHV68 charges dans les poumons des Mavs + / + et - Mavs. / - Souris. A) Deux voies de signalisation principal innée en aval de MAVS. Les relais de signalisation Mavs molécule adaptatrice de cytosoliques RIG-I-like receptors pour activer NFkB et les facteurs réglementaires interféron (IRF) qui, à son tour, en hausse de réguler l'expression des gènes de cytokines pro-inflammatoires et les interférons. B) Mavs + / + et - / - Mavs souris ont été infectées avec 40 PFU γHV68 par voie intranasale et les charges virales dans les poumons à des points de temps indiqués ont été de dissuader minée par un dosage de la plaque à l'aide NIH3T3 monocouche. Chaque symbole représente une souris.
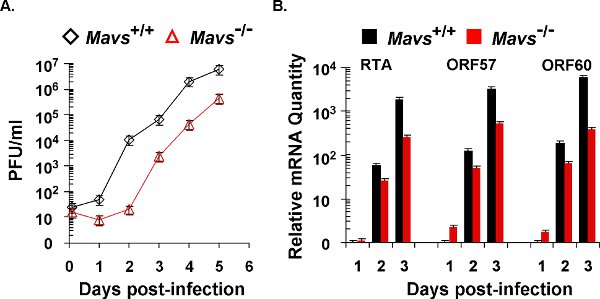
Figure 2. ΓHV68 cinétique de réplication lytiques dans les fibroblastes embryonnaires de souris (MEF). La réplication lytique de γHV68 sur Mavs + / + et Mavs - / - MEF a été évaluée par des courbes de croissance multi-étapes (A) et quantitative PCR en temps réel (B). Pour les deux expériences, le même nombre de MEF et la quantité de γHV68 ont été utilisés pour l'infection virale à une multiplicité de l'infection (MOI) de 0,01. (A) Les cellules et les surnageants ont été récoltés à des moments indiqués et soumis à un essai sur plaque pour déterminer les titres viraux. (B) L'ARN total a été extrait de γHV68 infecté par MEF et analysées par quantitative en temps réel PCR avec des amorces spécifiques pour certaines transcriptions lytiques (RTA, ORF57 et ORF60).
ig3.jpg "/>
Figure 3. La cinétique de réplication lytiques de recombinants portant des mutations γHV68 dans le domaine de transactivation RTA qui abolissent la phosphorylation par IKKγ. (A) courbes de croissance multi-étapes de recombinaison virus de type sauvage (γHV68.wt) et le virus mutant (γHV68.mut) dans Mavs + / + et Mavs - / - cellules FAE (MOI = 0,01). FAE ont été infectées par le γHV68 à une MOI de 0,01. Les cellules et les surnageants ont été récoltés à des moments indiqués et les titres viraux ont été déterminés par un dosage de la plaque à l'aide du NIH 3T3 monocouche. (B) le niveau d'ARNm γHV68 RTA dans γHV68 infectés par des cellules NIH3T3 (MOI = 0,01). À 30 h post-infection, l'ARN total a été extrait des cellules NIH 3T3 infectées par γHV68 et analysées par quantitative PCR en temps réel.
Discussion
En réponse à une infection virale, les Mavs dépendantes immunitaires innées des voies de signalisation sont activés pour promouvoir la production de cytokines inflammatoires antiviraux 10-14. Utilisation γHV68 murin comme un virus oncogène humain modèle pour le sarcome de Kaposi associé au virus de l'herpès et le virus d'Epstein-Barr 3,4, nous avons découvert que γHV68 usurpe la voie MAVS-IKKβ de promouvoir la réplication virale lytique via l'activation de la transcription...
Déclarations de divulgation
Aucun conflit d'intérêt déclaré.
Remerciements
Les auteurs tiennent à remercier le Dr James (Zhijian) Chen (UT Southwestern, biologie moléculaire) pour fournir des réactifs essentiels, y compris les Mavs - / - souris, et le Dr Ren Sun (Université de Californie-Los Angeles, pharmacologie et de médecine moléculaire ) pour fournir le chromosome bactérien artificiel de γHV68 pour cette étude.
matériels
| Name | Company | Catalog Number | Comments |
| Nom du réactif | Entreprise | Numéro de catalogue | |
| Lipofectamine 2000 | Invitrogen | 11668-019 | |
| Electro-MAX cellules DH10B compétentes | Invitrogen | 18290-015 | |
| Méthylcellulose | Sigma | M0512 | |
| POWERPREP HP plasmide système Miniprep | OriGene | NP100004 | |
| POWERPREP HP plasmide système Midiprep | OriGene | NP100006 |
Références
- Akira, S., Uematsu, S., Takeuchi, O. Pathogen recognition and innate immunity. Cell. 124, 783-801 (2006).
- Medzhitov, R. Recognition of microorganisms and activation of the immune response. Nature. 449, 819-826 (2007).
- Speck, S. H., Virgin, H. W. Host and viral genetics of chronic infection: a mouse model of gamma-herpesvirus pathogenesis. Curr. Opin. Microbiol. 2, 403-409 (1999).
- Speck, S. H., Ganem, D. Viral latency and its regulation: lessons from the gamma-herpesviruses. Cell Host Microbe. 8, 100-115 (2010).
- Dong, X. Murine gamma-herpesvirus 68 hijacks MAVS and IKKbeta to initiate lytic replication. PLoS Pathog. 6, e1001001-e1001001 (2010).
- Strauss, W. M., Ausubel, F. M. Preparation of genomic DNA from mammalian tissues. Current Protocols in Molecular Biology. , 2-2 (1998).
- Song, M. J. Identification of viral genes essential for replication of murine gamma-herpesvirus 68 using signature-tagged mutagenesis. Proc. Natl. Acad. Sci. U. S. A. 102, 3805-3810 (2005).
- Hirt, B. Selective extraction of polyoma DNA from infected mouse cell cultures. J. Mol. Biol. 26, 365-369 (1967).
- Eva-Maria Borst, E., Crnkovic-Mertens, I., Messerle, M., Zhao, S., Stodolsky, M. Cloning of β-herpesvirus genomes as bacterial artificial chromosomes. Methods in Molecular Biology. , 256-256 (2004).
- Sun, Q. The specific and essential role of MAVS in antiviral innate immune responses. Immunity. 24, 633-642 (2006).
- Seth, R. B., Sun, L., Ea, C. K., Chen, Z. J. Identification and characterization of MAVS, a mitochondrial antiviral signaling protein that activates NF-kappaB and IRF 3. Cell. 122, 669-682 (2005).
- Kawai, T. IPS-1, an adaptor triggering RIG-I- and Mda5-mediated type I interferon induction. Nat. Immunol. 6, 981-988 (2005).
- Meylan, E. Cardif is an adaptor protein in the RIG-I antiviral pathway and is targeted by hepatitis C virus. Nature. 437, 1167-1172 (2005).
- Xu, L. G. VISA is an adapter protein required for virus-triggered IFN-beta signaling. Mol. Cell. 19, 727-740 (2005).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon