Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Trichuris muris Infection: Un modèle de type 2 Immunité et inflammation de l'intestin
Dans cet article
Résumé
Trichuris muris infection est un modèle de l'immunité intestinale Th2 où les souris résistantes générer une réponse immunitaire protectrice Th2 et souris susceptibles de générer une réponse Th1 pathologique.
Résumé
Trichuris muris est un pathogène naturel des souris et est biologiquement et antigéniquement similaires aux espèces de Trichuris qui infectent les humains et le bétail 1. Œufs infectieux sont donnés par gavage oral, éclosent dans l'intestin grêle distal, envahissent les cellules épithéliales intestinales (CEI) qui bordent les cryptes du cæcum et du côlon proximal et sur la maturation des œufs des vers la libération dans l'environnement 1. Ce modèle est un outil puissant pour examiner les facteurs qui contrôle l'activation des cellules CD4 + T helper (Th), ainsi que des changements dans l'épithélium intestinal. La réponse immunitaire qui se produit dans les souches résistantes consanguines, telles que C57BL / 6 et BALB / c, est caractérisée par des cytokines Th2 polarisées (IL-4, IL-5 et IL-13) et l'expulsion des vers tout type Th1 associée de cytokines (IL -12, IL-18, IFN-γ) de promouvoir des infections chroniques chez AKR génétiquement sensibles / souris J 2-6. Cytokines Th2 promouvoir des changements physiologiques dans le microenvironnement intestinale, y compris le roulement rapide des CEI, la différenciation des cellules caliciformes, le recrutement et l'évolution de la perméabilité épithéliale et la contraction des muscles lisses, qui ont tous été impliqués dans l'expulsion 7-15 ver. Ici, nous détaillons un protocole pour la propagation de Trichuris muris oeufs qui peuvent être utilisées dans des expériences ultérieures. Nous fournissons également une récolte expérimentale de l'échantillon avec des suggestions pour l'analyse post-infection. Globalement, ce protocole permettra aux chercheurs les outils de base pour réaliser un modèle d'infection par Trichuris muris souris qui peut être utilisé pour traiter les questions relatives à la propension Th dans le tractus gastro-intestinal ainsi que des fonctions effectrices immunitaires des CEI.
Protocole
1. Propagation Trichuris muris oeufs
- Pour générer de nouveaux lots d'œufs de Trichuris muris, infecter 20 à 30 des souris immunodéficientes (ex-NOD.Cg Prkdc scid IL2RG tm1Wjl / SZJ (NSG) ou 129S6/SvEvTac-Rag2 tm1Fwa (RAG2 - / -)) ou des souris génétiquement sensibles ( par exemple. AKR / J) qui sont âgées de 6-8 semaines, avec environ 300 oeufs de Trichuris muris par gavage oral.
- Après 32-35 jours le sacrifice de la souris par le CO 2 asphyxie.
- Exposer la partie ventrale de la souris et humide de l'abdomen avec de l'éthanol à 70%.
- En utilisant des pinces saisir la peau de l'abdomen et de faire une petite incision à l'aide des ciseaux. Coupez la peau pour exposer le contenu abdominal.
- Identifier le caecum et l'intestin proximal grande, et les supprimer.
- Placez le caecum et le gros intestin proximal dans un plat de 10 cm de Pétri contenant Eagle modifié par Dulbecco (DMEM) avec 500 U / ml de pénicilline et 500 ug / ml de streptomycine (P / S). Couper le caecum ouverte pour exposer la lumière et les vers. En utilisant une pince cæcum lieu dans un bécher de tampon phosphate salin (PBS) et secouer délicatement pour enlever les excréments.
- Retour au cæcum boîte de Pétri et en utilisant des pinces lisses incurvées (Roboz RS-5047) tirez délicatement vers et les placer dans un puits d'une plaque de 6 puits contenant 5 ml de DMEM + P / S.
- Répétez ce processus pour toutes les souris.
- Mettez la plaque 6 puits dans un contenant Tupperware avec une serviette en papier humide pour maintenir l'humidité et incuber à 37 ° C pendant 4 heures.
- Après 4 heures supprimer un ver utilisant une pince incurvée lisse et les diviser en deux nouveaux puits de la plaque de 6 puits contenant 5 ml de DMEM + P / S. Récolte du contenu de la même origine et le placer dans un tube Falcon de 15 ml. Spin tubes à 3000 tpm et retirez et réservez surnageant comme antigène 4 h (peut être utilisé pour la restimulation des cellules après PBS dialyse, où les rendements en protéines typiques sont de 10-20 mg par 20 souris) et resuspendre œuf contenant le culot dans l'eau du robinet en autoclave.
- Mettez la plaque de 6 puits de retour à 37 ° C pendant la nuit. Retirez et jetez les vers. Récolte du contenu des puits dans un tube Falcon et tournent à 3000 rpm pendant 5 min. Retirer le surnageant et la réserve de l'antigène pendant la nuit (peut être utilisé pour Trichuris Ag ELISA spécifiques d'isotypes d'anticorps après la dialyse PBS, où les rendements en protéines typiques sont de 10-20 mg par 20 souris) et contenant des oeufs Resuspendre le culot dans l'eau du robinet en autoclave.
- Combinez 4 heures et les oeufs une nuit et filtrer les œufs à travers le tamis 70μm de supprimer tout les vers restants, puis transférer dans un flacon de 75 cm2. Gardez ballon dans un endroit sombre et couvert de feuilles pendant 6 semaines à température ambiante (RT).
- Lavez les oeufs dans de l'eau du robinet à l'autoclave et resuspendre à 50 œufs viables dans 50 pi. Pour ce faire, centrifugeuse oeufs à 3000 rpm pendant 5 min et remettre en suspension dans l'eau du robinet ~ 50ml stérile. Retirer 50 oeufs ul et le placer sur une lame de verre. Utiliser le grossissement 40x compter le nombre de viabilité des oeufs embryonnés dans l'ul 50. Diluer les œufs pour donner 50 œufs viables dans 50 pi. Pour les images d'œufs viables s'il vous plaît voir l'étude de Kopper et Mansfield 16.
2. L'infection aiguë des souris expérimentales avec Trichuris muris œufs (200 œufs / souris)
- Bien resuspendre oeufs et enlever un volume suffisant pour traiter le nombre de souris X 2 (par exemple pour 10 souris prendre 200 x 10 souris ul x 2 = 4 ml d'oeufs) et les placer dans un tube de 14 ml pression bouchon.
- Inverser le tube de 14 ml bouchon pression pour mélanger. Amener 200 pi d'œufs dans une seringue ml sur une aiguille de taille appropriée d'alimentation (pour les souris pesant 25 grammes, nous avons utilisé de calibre 18 1 1 / 2 "d'aiguilles). Dans un Scruff la main de la souris et en utilisant la main d'autres administrent des œufs par gavage oral .
- Attendre 21 jours.
3. De pêche expérimentale
- Le 21ème jour du sacrifice des souris en utilisant du CO 2.
- Recueillir le sang de souris par ponction cardiaque, dans une seringue non hépariné, et conserver à 4 ° C. Le jour suivant, d'isoler le sérum et le congeler à -20 ° C. Le sérum peut être utilisé pour la détection de Trichuris spécifiques IgG et IgE par ELISA.
- Exposer la partie ventrale de la souris et humide de l'abdomen avec de l'éthanol à 70%.
- En utilisant des pinces saisir la peau de l'abdomen et de faire une petite incision à l'aide des ciseaux. Coupez la peau et la membrane sous-jacente pour exposer le contenu abdominal.
- Identifier l'intestin grêle, le caecum et le colon. Prenez le caecum avec une pince et tirez hors de la cavité abdominale. Avec une autre paire de pinces poussez intestin grêle vers la droite exposer les ganglions mésentériques (mLNs). Retirez le mLNs en faisant attention de ne pas couper dans les intestins et les placer dans un faucon de 15 ml contenant 2 ml de médias. Si désiré, ces peuvent être traitées et restimulées in vitro (4x10 6 / ml dans 1 ml de plaques de 24 puits avec 1 ug / ml αCD3/CD28 ou avec 50μg/ml 4h Ag Trichuris) pendant 72 heures pour l'analyse des cytokines par ELISA et f intracellulairecytométrie en bas.
- Découpez le caecum et le colon.
- En utilisant une pince, sortez pelotes fécales du côlon distal et le placer dans un tube de 2 ml Axygen. Congeler à -20 ° C. Pelotes fécales peuvent être analysés par western blot pour l'expression de la résistine-like molecule-β (β-RELM).
- Enlevez l'extrémité du cæcum (~ 0,5 cm). Pour enlever les excréments maintenir la pointe du cæcum avec une pince et rincer avec du PBS en utilisant une seringue de 3 ml et de calibre 22 aiguille dans une boîte de Pétri. Placer dans du paraformaldéhyde 4% frais dans un tube de 5 ml Falcon bouchon clin d'oeil. Conserver à 4 ° C. Elles peuvent être inclus en paraffine, coupés et montés sur des lames pour l'analyse histologique.
- Supprimer un morceau de côlon proximal (~ 1 cm) pour l'ARN. Mettez l'échantillon dans 2 ml Axygen tube avec 500 ul RNAlater. Conserver à 4 ° C. Ces échantillons peuvent être analysés pour l'expression des ARNm par qPCR.
- Placez le reste du cæcum dans une boîte de Pétri étiquetés et congeler à -20 ° C.
4. Énumération des Trichuris muris ver dans le caecum
- Retirer du congélateur et le caecum place dans une boîte de Pétri contenant de l'eau ~ 5 ml.
- Avec des ciseaux, couper le caecum ouverte pour exposer la lumière.
- Tenez le caecum avec des pinces et agiter vigoureusement le caecum pour enlever la majorité des matières fécales.
- Transfert cæcum à l'autre boîte de Pétri contenant de l'eau douce et en utilisant une pince incurvée gratter délicatement l'IECS le tissu sous-jacent.
- Transfert cæcum d'un nouveau plat de Pétri contenant de l'eau et vigoureusement grattez tissus restants avec une pince, déchirant le tissu en petits morceaux.
- Utiliser un microscope à dissection pour compter tous les vers dans tous les 3 des boîtes de Pétri. Comme vous trouvez un ver retirez le plat pour assurer le même ver n'est pas comptée deux fois. Si les vers sont endommagé (cassé dans la moitié) ne comptent que se termine fin ou épais pour obtenir un décompte précis.
5. Les résultats représentatifs
Le modèle d'infection par Trichuris muris permet aux chercheurs de quantifier la charge parasitaire et des réponses immunitaires systémiques, ainsi que d'examiner histologiquement la réponse inflammatoire dans le cæcum distale. Lorsque la lumière du cæcum récolté est exposé, vers Trichuris peuvent être énumérés en utilisant un microscope à dissection (figure 1A-B). Les paramètres de l'immunité à Trichuris également isotype d'anticorps IgG1 commutation d'(associé à l'immunité de type Th2) chez les animaux résistants, et IgG2a (associé à l'immunité de type Th1) chez les animaux sensibles (figure 1C). Expression de la coupe spécifique des cellules de protéines résistine-like molecule-β (β-RELM) est associée à la clairance de Trichuris et est détectable par Western blot (figure 2). La partie distale du caecum peut être coloré avec l'acide périodique-Schiff (PAS) pour évaluer les réponses des cellules caliciformes et l'étendue de l'inflammation intestinale en réponse à l'infection (figure 3).
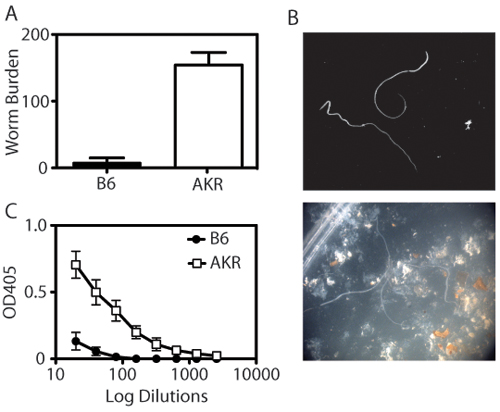
Figure 1. Quantification de l'immunité à Trichuris muris. (A) Résistant (B6) des souris expulser muris Trichuris par jour 21 post-infection. En revanche, sensibles (AKR / J) les souris deviennent chroniquement infectés par Trichuris, résultant en l'établissement du parasite. Chaque barre représente la moyenne ± SEM de 4-8 animaux par groupe. (B) vers sont comptés en utilisant un microscope à dissection. Panneau supérieur montre des vers dans l'isolement, le panneau du bas montre les vers, en présence de l'IECS et les fèces. (C) Trichuris spécifique des titres IgG2a sont déterminés par ELISA de sérum dilué (1:2 dilution, à partir de 01h20 et se terminant à la dilution 1:2560) sur des plaques recouvertes d'antigène Trichuris excréteurs (O / N Ag, 5 ug / ml). Sensible AKR / J souris ont des niveaux considérablement plus élevés de Trichuris spécifiques IgG2a sérum que résistants souris B6.

Figure 2. Apurement des Trichuris muris est associée à l'expression de la coupe spécifique des cellules β des protéines RELM-7. RELM-β production peut être détectée à partir des pelotes fécales de Trichuris infectés résistants (B6), mais pas sensibles (AKR / J) chez la souris par une analyse Western blot. Chaque voie est représentatif d'un seul animal, (N) = Naive, (Tm) = 21 jours Trichuris souris infectées.
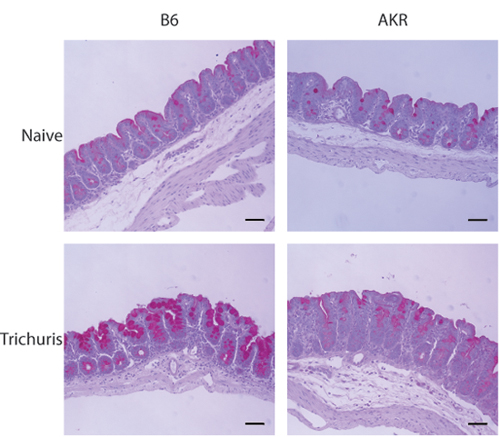
Figure 3. L'examen histologique de l'infection à Trichuris cæcum distale suivantes. Sections um 5-7 de la distale cæcum colorés avec le PAS. Hyperplasie des cellules caliciformes et de la production de mucus sont évidents dans résistants (B6), mais pas sensibles (AKR / J) des souris suite à une infection par Trichuris.
Discussion
Ce protocole détaille une dose standard de haute aiguë Trichuris muris infection qui peut être modifiée au besoin par l'investigateur. Par exemple, les souris peuvent être sacrifiés et les tissus récoltés à des jours différents. Afin de déterminer que les souris ont réussi à établir la charge parasitaire complète qu'ils peuvent être sacrifiés au jour 14, date à laquelle toutes les souris doivent porter un fardeau de quelque 200 vers. Les souris peuvent également être infectés pendan...
Déclarations de divulgation
Remerciements
Ce travail a été soutenu par les Instituts canadiens de recherche en santé (MSH-95368, 89773 et MOP-MOP-106623 à CZ) et la Fondation canadienne pour l'innovation. SMC est le récipiendaire d'une Association des IRSC / canadienne de gastroentérologie de bourses postdoctorales. CZ est un chercheur des IRSC Nouveau.
matériels
| Name | Company | Catalog Number | Comments |
| Nom du réactif | Société | Numéro de catalogue | Commentaires |
|---|---|---|---|
| Aiguilles alimentation animale (18 x 1 ½ ") | Popper | 7912 | |
| Pince courbée lisse | Roboz | RS-5047 | |
| DMEM | Gibco | 11965 | |
| NOD.Cg-Prkdc scid IL2R gtm1Wjl / SZJ (NSG) | Jackson Laboratories | 005557 | Ce sont les souris, nous avons utilisé, cependant, aucune des souris immunodéficientes ou souche sensible devrait fonctionner. |
| RNAlater | Qiagen | 76104 | |
| Tubes de 2 ml | Axygen | MCT-200-C | |
| Tubes de 15 ml | Falcon | 352096 | |
| 6 assiettes bien | Falcon | 353046 | |
| Paraformaldéhyde | Sciences Electron Microscopy | 15710 | |
| α-RELMβ d'anticorps | PeproTech Inc | 0694270Rb |
Références
- Cliffe, L. J., Grencis, R. K. The Trichuris muris system: a paradigm of resistance and susceptibility to intestinal nematode infection. Adv. Parasitol. 57, 255-307 (2004).
- Else, K. J., Finkelman, F. D., Maliszewski, C. R., Grencis, R. K. Cytokine-mediated regulation of chronic intestinal helminth infection. J. Exp. Med. 179, 347-351 (1994).
- Bancroft, A. J., Grencis, R. K. Th1 and Th2 cells and immunity to intestinal helminths. Chem. Immunol. 71, 192-208 (1998).
- Bancroft, A. J., McKenzie, A. N., Grencis, R. K. A critical role for IL-13 in resistance to intestinal nematode infection. J. Immunol. 160, 3453-3461 (1998).
- Helmby, H., Takeda, K., Akira, S., Grencis, R. K. Interleukin (IL)-18 promotes the development of chronic gastrointestinal helminth infection by downregulating IL-13. J. Exp. Med. 194, 355-364 (2001).
- Owyang, A. M. Interleukin 25 regulates type 2 cytokine-dependent immunity and limits chronic inflammation in the gastrointestinal tract. J. Exp. Med. 203, 843-849 (2006).
- Artis, D. RELMβ/FIZZ2 is a goblet cell-specific immune-effector molecule in the gastrointestinal tract. Proc. Natl. Acad. Sci. U. S. A. 101, 13596-13600 (2004).
- Datta, R. Identification of novel genes in intestinal tissue that are regulated after infection with an intestinal nematode parasite. Infect. Immun. 73, 4025-4033 (2005).
- Cliffe, L. J. Accelerated intestinal epithelial cell turnover: a new mechanism of parasite expulsion. Science. 308, 1463-1465 (2005).
- Artis, D. New weapons in the war on worms: identification of putative mechanisms of immune-mediated expulsion of gastrointestinal nematodes. Int. J. Parasitol. 36, 723-733 (2006).
- Finkelman, F. D. Cytokine regulation of host defense against parasitic gastrointestinal nematodes: lessons from studies with rodent models. Annu. Rev. Immunol. 15, 505-533 (1997).
- Grencis, R. K. Enteric helminth infection: immunopathology and resistance during intestinal nematode infection. Chem. Immunol. 66, 41-61 (1997).
- Khan, W. I. Modulation of intestinal muscle contraction by interleukin-9 (IL-9) or IL-9 neutralization: correlation with worm expulsion in murine nematode infections. Infect. Immun. 71, 2430-2438 (2003).
- Khan, W. I., Blennerhasset, P., Ma, C., Matthaei, K. I., Collins, S. M. Stat6 dependent goblet cell hyperplasia during intestinal nematode infection. Parasite Immunol. 23, 39-42 (2001).
- Akiho, H., Blennerhassett, P., Deng, Y., Collins, S. M. Role of IL-4, IL-13, and STAT6 in inflammation-induced hypercontractility of murine smooth muscle cells. Am. J. Physiol. Gastrointest. Liver Physiol. 282, 226-2232 (2002).
- Kopper, J. J., Mansfield, L. S. Development of improved methods for delivery of Trichuris muris to the laboratory mouse. Parasitol. Res. 107, 1103-1113 (2010).
- Bancroft, A. J., Else, K. J., Grencis, R. K. Low-level infection with Trichuris muris significantly affects the polarization of the CD4 response. Eur. J. Immunol. 24, 3113-3118 (1994).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon