Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Séparation spatiale des conformateurs moléculaires et des amas
Dans cet article
Résumé
Nous présentons une technique qui permet la séparation spatiale de différents conformères ou amas présents dans un faisceau moléculaire. Un déflecteur électrostatique est utilisé pour séparer les espèces par leur rapport masse/moment dipolaire, conduisant à la production d’ensembles en phase gazeuse d’un seul conformateur ou d’une stœchiométrie en grappes.
Résumé
Les expériences de physique moléculaire et de chimie physique en phase gazeuse utilisent couramment des expansions supersoniques à travers des vannes pulsées pour la production de faisceaux moléculaires froids. Cependant, ces poutres contiennent souvent plusieurs conformères et grappes, même à de basses températures de rotation. Nous présentons une méthodologie expérimentale qui permet la séparation spatiale de ces parties constitutives d’une expansion de faisceau moléculaire. À l’aide d’un déflecteur électrique, le faisceau est séparé par son rapport de moment masse/dipôle, analogue à un spectromètre de masse à bender ou à secteur électrique dispersant spatialement des molécules chargées sur la base de leur rapport masse/charge. Ce déflecteur exploite l’effet Stark dans un champ électrique inhomogène et permet la séparation d’espèces individuelles de molécules et d’amas neutres polaires. Il permet en outre la sélection de la partie la plus froide d’un faisceau moléculaire, car les états quantiques de rotation de basse énergie connaissent généralement la plus grande déviation. Différents isomères structurels (conformères) d’une espèce peuvent être séparés en raison de la disposition différente des groupes fonctionnels, ce qui conduit à des moments dipolaires distincts. Ceux-ci sont exploités par le déflecteur électrostatique pour la production d’un échantillon conformationnellement pur à partir d’un faisceau moléculaire. De même, des stœchiomères de cluster spécifiques peuvent être sélectionnées, car la masse et le moment dipolaire d’un cluster donné dépendent du degré de solvaation autour de la molécule parente. Cela permet des expériences sur des tailles et des structures de grappes spécifiques, permettant l’étude systématique de la solvaation de molécules neutres.
Introduction
Les expériences modernes de physique moléculaire et de chimie physique en phase gazeuse utilisent souvent des expansions supersoniques de molécules cibles pour produire des échantillons moléculaires froids en rotation dans un faisceau moléculaire. Cependant, même à de basses températures de rotation de 1 K, ce qui peut être systématiquement réalisé en utilisant des expansions supersoniques, les grandes molécules peuvent encore rester dans de multiples conformations au sein du faisceau1. De même, la production de grappes moléculaires dans une source de faisceau n’entraîne pas une seule espèce, mais plutôt la formation d’une « soupe de grappes », contenant de nombreuses stœchiomères de grappes différentes, ainsi que des molécules parentales pures restantes. Cela rend difficile l’étude de ces systèmes avec de nouvelles techniques telles que l’imagerie des orbitales moléculaires2,des distributions angulaires photoélectroniques à cadre moléculaire3-5 ou de l’électron6-10 et de la diffraction des rayons X11-13, car celles-ci nécessitent des échantillons purs, cohérents et homogènes en phase gazeuse.
Bien que plusieurs méthodologies soient maintenant disponibles pour séparer les différents conformateurs des espèces chargées en phase gazeuse(par exemple, les tubes dérivants de mobilité ionique14,15)et que les grappes chargées soient facilement séparées par leur rapport masse/charge, ces techniques ne sont pas applicables aux espèces neutres. Nous avons récemment démontré que ces problèmes peuvent être surmontés avec l’utilisation d’un dispositif de déviation électrostatique16,17,permettant la séparation des conformères moléculaires ainsi que des grappes et la production de faisceaux moléculaires froids en rotation.
L’utilisation de la déviation électrostatique est une technique classique de faisceau moléculaire, dont les origines remontent loin18,19. Les premières idées d’utilisation de la déviation électrostatique pour la séparation des états quantiques ont été introduites par Stern en 192620. Alors que les premières expériences ont été menées sur de petites molécules à haute température, nous démontrons l’application de cette technique à de grandes molécules polaires et à des amas à basse température16,21.
Les molécules polaires subissent une force à l’intérieur d’un champ électrique inhomogène(E)en raison des différences spatiales d’énergie potentielle. Cette force 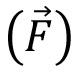 dépend du moment dipolaire effectif, μeff, de la molécule et peut être évaluée comme
dépend du moment dipolaire effectif, μeff, de la molécule et peut être évaluée comme
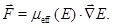 (1)
(1)
Comme différents conformateurs moléculaires possèdent généralement différents moments dipolaires et que des nombres différents de molécules de solvant au sein d’un cluster conduisent à des masses d’amas et des moments dipolaires différents, ces espèces connaîtront une accélération différente en présence d’un fort champ électrique inhomogène. La force de l’effet Stark résultant d’un champ électrique non homogène peut donc être utilisée pour la séparation des conformateurs et des états quantiques22. Ceci est indiqué à la figure 1,montrant les courbes de Stark calculées pour les états de rotation J = 0,1,2 des cis et des trans-conformères du 3-fluorophénol, respectivement. Cela conduit à de grandes différences dans μeff, comme le montrent les figures 1c et 1d, et donc une accélération différente est subie par les deux conformères dans les champs électriques non homogènes. Par conséquent, un dispositif de déviation électrostatique peut être utilisé comme séparateur de rapport de moment masse/dipôle(m/μeff),par analogie à un spectromètre de masse agissant comme filtre de rapport masse/charge(m/z)23.
De plus, ces techniques permettent la séparation des états quantiques rotationnels24,25. Comme les états de rotation du sol (courbes bleues dans les figures 1a et 1b)présentent le plus grand décalage de Stark, ceux-ci seront les plus déviés et peuvent être séparés spatialement des molécules dans les états J supérieurs17. La partie la plus froide d’un faisceau moléculaire peut donc être sélectionnée, aidant de manière significative dans de nombreuses applications, telles que l’alignement et l’orientation des molécules cibles17, 26-28.
Dans cette contribution, nous montrons comment un dispositif de déviation électrostatique peut être utilisé pour séparer spatialement différentes espèces de grandes molécules polaires et d’amas. Des exemples de données sont présentés pour la production d’un faisceau pur d’un conformateur individuel et d’un amas soluté-solvant de taille et de rapport bien définis. Plus précisément, nous présentons des données sur le 3-fluorophénol, où un faisceau pur contenant uniquement le trans conformateur est produit, et sur les amas d’indole-eau, où l’amas d’indole(H2O)1 peut être spatialement séparé de l’eau, indole, indole(H2O)2, etc.
Protocole
1. Description de l’installation expérimentale
Un schéma de la configuration du faisceau moléculaire en phase gazeuse et du déflecteur est représenté sur la figure 221. Il se compose de
- Une vanne Even-Laviepulsée 29 contenant l’échantillon moléculaire. D’autres vannes à faisceau moléculaire pulsé peuvent être utilisées aussi bien qu’un faisceau moléculaire froid (O (1 K)) est formé. Les paramètres suivants sont spécifiques à la vanne Even-Lavie utilisée. Dans les expériences présentées ici, la vanne fonctionne à un taux de répétition de 20 Hz avec des pressions de support élevées (hélium à ~ 50 bars) et élargie dans une chambre à vide évacuée à <10-6 mbar.
- Un écumeur à faisceau moléculaire (diamètre de 2 mm) est placé à 22 cm en aval de la vanne, collimant le faisceau moléculaire et conduisant à des conditions de pompage différentielles entre la vanne pulsée et le reste du système de vide.
- Immédiatement après l’écumoire, les molécules pénètrent dans le dispositif de déviation électrostatique. Il s’agit d’une tige (rayon de 3,0 mm) et d’une auge (rayon de courbure de 3,2 mm), chacune de 24 cm de long. L’écart vertical entre les électrodes au centre de l’appareil est de 2,3 mm. Une différence de potentiel entre 0-26 kV est appliquée entre la tige et l’auge, produisant un fort champ électrique inhomogène avec un gradient de champ presque constant30,comme indiqué dans l’encart de la figure 2.
- Directement après que les molécules déflecteurs entrent dans la région d’interaction par un deuxième écumeur, fournissant un autre étage de pompage différentiel.
- La région d’interaction (évacuée à des pressions <10à 9 mbar) contient une configuration standard du temps de vol (TOF) Wiley-McLaren. Les molécules sont ionisées par des impulsions laser focalisées au centre de la région d’extraction, entre les électrodes du répulsif et de l’extracteur. Les ions produits sont accélérés vers un détecteur à plaques multicanaux (MCP), où un spectre de masse est enregistré.
- Les impulsions laser sont dérivées d’un laser à colorant pompé Nd:YAG, fournissant des longueurs d’onde de sortie typiques autour de 283 nm (expériences indole) ou 272 nm (expériences 3-fluorophénols) et des énergies d’impulsion de quelques mJ. Les durées d’impulsion sont de l’ordre de 10 nsec et les impulsions sont focalisées avec une lentille f = 750 mm à une taille de spot d’environ 100 μm dans la région d’interaction.
- La séquence de synchronisation est contrôlée par un générateur de retard numérique fournissant l’horloge principale. Cela déclenche le laser Nd:YAG (lampes flash et interrupteur Q), la vanne pulsée et la carte numériseur utilisée pour enregistrer les spectres de masse.
- Les spectres de masse sont enregistrés sur une carte numériseur, déclenchée en même temps que le Q-switch laser. Les densités de faisceau moléculaire sont extraites des portes de masse appropriées dans les spectres de temps de vol enregistrés.
2. Production et caractérisation d’un faisceau moléculaire sélectionné de conformateur
- Un faisceau moléculaire froid des molécules cibles est créé par expansion supersonique et caractérisé à l’aide du profilage spatial (directions x, y) et temporel (direction z).
- Charger le réservoir d’échantillon de la vanne pulsée avec l’échantillon chimique. Dissoudre les échantillons solides dans un solvant approprié et placer quelques gouttes sur un petit morceau de papier filtre qui est inséré dans la cartouche d’échantillon. Placez les échantillons liquides directement sur le papier filtre.
- Produire l’expansion supersonique, en utilisant un gaz de support haute pression de haute pureté. Régler la température du réservoir de prélèvement à l’intérieur de la vanne de manière à ce que la pression partielle de l’échantillon soit d’environ 10 mbar.
Remarque: Pour les échantillons liquides, aucun chauffage n’est généralement nécessaire. Le temps d’ouverture de la vanne dépend du modèle exact de vanne pulsée utilisé, pour les expériences présentées ici, la vanne Even-Lavie fonctionne avec une durée d’impulsion électrique de 10 μsec. - Caractériser le faisceau moléculaire produit avec le déflecteur électrostatique éteint. Réglez le laser à ionisation sur une longueur d’onde connue pour l’ionisation multiphotonique améliorée par résonance (REMPI) d’un conformateur particulier de l’échantillon. Enregistrer un profil temporel de l’impulsion du faisceau moléculaire en surveillant le rendement total en ions parents sur le détecteur MCP en fonction du retard valve-laser.
- Fixer le retard valve-laser à la position d’intensité maximale pour toutes les mesures ultérieures.
- Enregistrez un profil spatial transversal du faisceau moléculaire en surveillant le rendement total en ions parents en fonction de la position y du foyer laser. Pour ce faire, déplacez la lentille de mise au point perpendiculairement à la direction de propagation du laser, de sorte que la mise au point se déplace dans la direction y par rapport au faisceau moléculaire.
- Répétez le profilage temporel et spatial pour tous les conformères d’intérêt dans le faisceau.
Remarque: Ceux-ci ont typiquement des résonances REMPI distinctes, telles que chaque conformateur puisse être sondé séparément. En l’absence de champ de déviation cependant, les profils temporel et spatial sont identiques pour tous les conformères. - Caractérisation de la poutre déviée. Allumez l’alimentation haute tension du déflecteur et enregistrez les profils spatiaux pour tous les isomères. Ceux-ci doivent maintenant être déviés en fonction du rapport de moment masse/dipôle.
Note: Pour les espèces subissant de grandes déviations, il peut être nécessaire de déplacer l’écumoire immédiatement après le déflecteur pour assurer une bonne transmission du faisceau dévié dans la région de détection. - Mener des expériences sur la partie conformiste ou de taille sélectionnée du faisceau moléculaire en veillant à ce quel’interaction (par exemple, un faisceau laser croisé) ait lieu dans la partie du faisceau moléculaire contenant uniquement les espèces d’intérêt.
Résultats
La technique de déviation électrostatique a été appliquée avec succès à la séparation des isomèresstructuraux 16 et des grappes neutres21,ainsi qu’à la production d’échantillons moléculaires sélectionnés à l’état quantique de rotation31. Nous démontrons ceci avec des résultats représentatifs pour la séparation du cis et des trans conformères du fluorophénol 3, et de la taille a sélectionné des faisceauxd’indole (H2O) ...
Discussion
Tout au long de ce manuscrit, on suppose qu’il est familier avec les composants à ultra-vide, les vannes à faisceau moléculaire pulsé et les sources laser et que les procédures de sécurité associées doivent toujours être respectées. Un soin particulier doit être pris lors de la manipulation des électrodes haute tension pour le déflecteur. Leurs surfaces doivent être polies à un niveau élevé et doivent être absolument propres pour éviter les arcs à l’intérieur de la chambre à vide. Avant la première utilisation, les...
Déclarations de divulgation
Les auteurs n’ont rien à divulguer.
Remerciements
Ce travail a été soutenu par le pôle d’excellence « The Hamburg Center for Ultrafast Imaging – Structure, Dynamics and Control of Matter at the Atomic Scale » de la Deutsche Forschungsgemeinschaft et par l’Institut virtuel Helmholtz « Dynamic Pathways in Multidimensional Landscapes ».
matériels
| Name | Company | Catalog Number | Comments |
| Vacuum system | various, e.g. Pfeiffer Vacuum, Varian, Edwards, Leybold | ||
| Dye laser system | various, e.g. Coherent, Spectra Physics, Syrah, LIOP-TEC, Radiant Dyes… | ||
| Pulsed valve | Even-Lavie | ||
| High voltage power supply | eg. FUG | HCP 14-20000 | |
| Deflector | Custom made | ||
| Time-of-flight spectrometer | Jordan TOF | C-677 | |
| TOF power supply | Jordan TOF | D-603 | |
| Focusing lens | Thorlabs | LA4745 | |
| Translation stage | e.g. Vision Lasertechnik | 8MT167-25 | |
| Digitizer | e.g. Agilent | Acquiris DC440 | |
| Digital delay generator | Stanford Systems | SRS DG645 | |
| Molecular beam skimmer | Beam Dynamics Inc. | http://www.beamdynamicsinc.com/ |
Références
- Rizzo, T. R., Park, Y. D., Peteanu, L., Levy, D. H. Electronic spectrum of the amino acid tryptophan cooled in a supersonic molecular beam. J. Chem. Phys. 83, 4819-4820 (1985).
- Itatani, J., et al. Tomographic imaging of molecular orbitals. Nature. 432, 867-871 (2004).
- Kumarappan, V., et al. Multiphoton electron angular distributions from laser-aligned CS2 molecules. Phys. Rev. Lett. 100 (9), 093006-0910 (2008).
- Bisgaard, C. Z., et al. Time-resolved molecular frame dynamics of fixed-in-space CS2 molecules. Science. 323 (5920), 1464-1468 (2009).
- Holmegaard, L., et al. Photoelectron angular distributions from strong-field ionization of oriented molecules. Nat. Phys. 6, 428-4210 (2010).
- Ihee, H., et al. Direct imaging of transient molecular structures with ultrafast diffraction. Science. 291 (5503), 458-462 (2001).
- Chergui, M., Zewail, A. H. Electron and x-ray methods of ultrafast structural dynamics: Advances and applications. Chem. Phys. Chem. 10 (1), 28-43 (2009).
- Siwick, B. J., Dwyer, J. R., Jordan, R. E., Miller, R. J. D. An atomic-level view of melting using femtosecond electron diffraction. Science. 302 (5649), 1382-1385 (2003).
- Sciaini, G., Miller, R. J. D. Femtosecond electron diffraction: heralding the era of atomically resolved dynamics. Rep. Prog. Phys. 74 (9), 096101-0910 (2011).
- Hedberg, K., et al. Bond lengths in free molecules of buckminsterfullerene, C60, from gas-phase electron diffraction. Science. 254 (5030), 410-412 (1991).
- Filsinger, F., Meijer, G., Stapelfeldt, H., Chapman, H., Küpper, J. S. t. a. t. e. -. and conformerselected beams of aligned and oriented molecules for ultrafast diffraction studies. Phys. Chem. Chem. Phys. 13 (6), 2076-2087 (2011).
- Seibert, M. M., et al. Single mimivirus particles intercepted and imaged with an x-ray laser. Nature. 470 (7332), (2011).
- Chapman, H. N., et al. Femtosecond x-ray protein nanocrystallography. Nature. 470 (7332), (2011).
- von Helden, G., Wyttenbach, T., Bowers, M. T. Conformation of macromolecules in the gasphase – use of matrix-assisted laser-desorption methods in ion chromatography. Science. 267, 1483-1485 (1995).
- Jarrold, M. Helices and sheets in vacuo. Phys. Chem. Chem. Phys. 9, 1659-1671 (2007).
- Filsinger, F., et al. Pure samples of individual conformers: the separation of stereo-isomers of complex molecules using electric fields. Angew. Chem. Int. Ed. 48, (2009).
- Filsinger, F., et al. Quantum-state selection, alignment, and orientation of large molecules using static electric and laser fields. J. Chem. Phys. 131, 10-1063 (2009).
- Kallmann, H., Reiche, F. Über den Durchgang bewegter Moleküle durch inhomogene Kraftfelder. Z. Phys. 6, 352-375 (1921).
- Wrede, E. Über die Ablenkung von Molekularstrahlen elektrischer Dipolmoleküle im inhomogenen elektrischen Feld. Z. Phys. 44 (4-5), 4-5 (1927).
- Gerlach, W., Der Stern, O. experimentelle Nachweis der Richtungsquantelung im Magnetfeld. Z. Phys. 9, 349-352 (1922).
- Trippel, S., Chang, Y. -. P., Stern, S., Mullins, T., Holmegaard, L., Küpper, J. Spatial separation of state- and size-selected neutral clusters. Phys. Rev. A. 86, 10-1103 (2012).
- Filsinger, F., Erlekam, U., von Helden, G., Küpper, J., Meijer, G. Selector for structural isomers of neutral molecules. Phys. Rev. Lett. 100, 10-1103 (2008).
- Filsinger, F., Putzke, S., Haak, H., Meijer, G., Küpper, J. Tuning the resolution of the m=_- selector. Phys. Rev. A. 82, 052513-0510 (2010).
- Putzke, S., Filsinger, F., Haak, H., Küpper, J., Meijer, G. Rotational-state-specific guiding of large molecules. Phys. Chem. Chem. Phys. 13, (2011).
- Nielsen, J. H., et al. Stark-selected beam of ground-state OCS molecules characterized by revivals of impulsive alignment. Phys. Chem. Chem. Phys. 13, 18971-18975 (2011).
- Stapelfeldt, H., Seideman, T. Colloquium: Aligning molecules with strong laser pulses. Rev. Mod. Phys. 75 (2), 543-557 (2003).
- Holmegaard, L., et al. Laser-induced alignment and orientation of quantum-state-selected large molecules. Phys. Rev. Lett. 102, 10-1103 (2009).
- Ghafur, O., Rouzee, A., Gijsbertsen, A., Siu, W. K., Stolte, S., Vrakking, M. J. J. Impulsive orientation and alignment of quantum-state-selected NO molecules. Nat. Phys. 5, 289-293 (2009).
- Hillenkamp, M., Keinan, S., Even, U. Condensation limited cooling in supersonic expansions. J. Chem. Phys. 118 (19), 8699-8705 (2003).
- Ramsey, N. F. . Molecular Beams. The International Series of Monographs on Physics. , (1956).
- Nielsen, J. H., Stapelfeldt, H., Küpper, J., Friedrich, B., Omiste, J. J., González-Férez, R. Making the best of mixed-field orientation of polar molecules: A recipe for achieving adiabatic dynamics in an electrostatic field combined with laser pulses. Phys. Rev. Lett. 108 (19), 10-1103 (2012).
- Fujimaki, E., Fujii, A., Ebata, T., Mikami, N. Autoionization-detected infrared spectroscopy of intramolecular hydrogen bonds in aromatic cations. I. principle and application to fluorophenol and methoxyphenol. J. Chem. Phys. 110, 4238-4247 (1999).
- Kang, C., Korter, T. M., Pratt, D. W. Experimental measurement of the induced dipole moment of an isolated molecule in its ground and electronically excited states: Indole and indole–H2O. J. Chem. Phys. 122 (17), 174301-17 (2005).
- Korter, T. M., Pratt, D. W., Küpper, J. Indole-H2O in the gas phase. structures, barriers to internal motion, and S1 S0 transition moment orientation. solvent reorganization in the electronically excited state. J. Phys. Chem. A. 102 (37), 7211-7216 (1998).
- Küpper, J., Pratt, D. W., Meerts, L., Brand, C., Tatchen, J., Schmitt, M. Vibronic coupling in indole: II. experimental investigation of the 1La–1Lb interaction using rotationally resolved electronic spectroscopy. Phys. Chem. Chem. Phys. 12, 4980-4988 (2010).
- Suenram, R. D., Lovas, F. J. Millimeter wave spectrum of glycine - a new conformer. J. Am. Chem. Soc. 102, 7180-7184 (1980).
- Nir, E., Kleinermanns, K., de Vries, M. S. Pairing of isolated nucleic-acid bases in the absence of the DNA backbone. Nature. 408, 949-951 (2000).
- Bethlem, H. L., van Roij, A. J. A., Jongma, R. T., Meijer, G. Alternate gradient focusing and deceleration of a molecular beam. Phys. Rev. Lett. 88 (13), 10-1103 (2002).
- Wohlfart, K., Grätz, F., Filsinger, F., Haak, H., Meijer, G., Küpper, J. Alternating-gradient focusing and deceleration of large molecules. Phys. Rev. A. 77, 10-1103 (2008).
- Putzke, S., Filsinger, F., Küpper, J., Meijer, G. Alternating-gradient focusing of the benzonitrile-argon van der waals complex. J. Chem. Phys. 137 (10), 10-1063 (2012).
- Knight, W. D., Clemenger, K., de Heer, W. A., Saunders, W. A. Polarizability of alkali clusters. Phys. Rev. B. 31 (4), 2539-2540 (1985).
- Tarnovsky, V., Bunimovicz, M., Vuškovic, L., Stumpf, B., Bederson, B. Measurements of the DC electric-dipole polarizabilities of the alkali dimer molecules, homonuclear and heteronuclear. J. Chem. Phys. 98 (5), 3894-3904 (1993).
- Schäfer, R., Schlecht, S., Woenckhaus, J., Becker, J. . Polarizabilities of Isolated Semiconductor Clusters. Phys. Rev. Lett. 76 (3), 471-474 (1996).
- Antoine, R., et al. Electric dipole moments and conformations of isolated peptides. Eur. Phys. J. D. 20, 583-587 (2002).
- Cosby, P. C., Smith, G. P., Moseley, J. T. Photodissociation and photodetachment of molecular negative ions. IV. Hydrates of O. J. Chem. Phys. 69, 2779-2781 (1978).
- Hunton, D. E., Hofmann, M., Lindeman, T. G., Albertoni, C. R., Castleman Jr, ., W, A. Photodissociation spectroscopy and dynamics of negative ion clusters. II. CO. (H2O)1;2;3. J. Chem. Phys. 82, 2884-2895 (1985).
- Castleman, A. W., Bowen J, K. H., J, Clusters: Structure, energetics, and dynamics of intermediate states of matter. J. Phys. Chem. 100, 12911-12944 (1996).
- Verlet, J. R. R. Femtosecond spectroscopy of cluster anions: insights into condensed-phase phenomena from the gas-phase. Chem. Soc. Rev. 37, 505-517 (2008).
- Nevo, I., et al. Laser-induced 3D alignment and orientation of quantum state-selected molecules. Phys. Chem. Chem. Phys. 11, 9912-9918 (2009).
- Reckenthaeler, P., Centurion, M., Fuss, W., Trushin, S. A., Krausz, F., Fill, E. E. Time-resolved electron diffraction from selectively aligned molecules. Phys. Rev. Lett. 102 (21), 213001-2110 (2009).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon